文档内容
专项训练 氮族元素及其化合物(解析版)
1.利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:
下列操作错误的是
A.红磷使用前洗涤以除去表面杂质
B.将红磷转入装置,抽真空后加热外管以去除水和氧气
C.从a口通入冷凝水,升温使红磷转化
D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集
【答案】C
【详解】A.红磷表面有被氧化生成的五氧化二磷,五氧化二磷可以溶于水,因此红
磷在使用前应洗涤,A正确;
B.真空环境可以降低物质的熔沸点,有利于将红磷转化为白磷,但是由于抽真空时不
能将水气和氧气完全除去,还需要对装置外管进行加热,这时可以保证反应环境无水
无氧,B正确;
C.若从a口通入冷凝水,则冷凝水无法充满整个冷凝管,冷凝效果不好,需要用b口
通入,此时可以将冷凝水充满冷凝管,C错误;
D.白磷易被空气中的氧气氧化,因此在收集白磷时应将反应装置冷却,再在氮气氛
的条件下收集白磷,D正确;
故答案选C。
2.下列实验方案设计正确的是
编
目的 方案设计
号
检验固体试
在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿
A 样中有
润红色石蕊试纸变蓝的气体,该固体试样中不可能存在
资料收集整理【淘宝店铺:向阳百分百】探究S与Cl 向NaHS溶液中滴入稀盐酸,观察是否有生成臭鸡蛋气味气体(
B 的金属性强
)。
弱
向两支试管分别加入 和 溶液,向盛有
探究浓度对
C 化学反应速 溶液试管中加入 蒸馏水,再同时向两支试管中加
率的影响
,收集生成的 气体,比较生成气体的快慢
探究 的 在试管中加入少量酸性 溶液,然后向试管中逐滴加入
D
还原性 溶液,观察溶液颜色变化
A.A B.B C.C D.D
【答案】D
【详解】A.在某固体试样加水后的溶液中,滴加NaOH溶液,生成的氨气极易溶于
水,需进行加热,观察是否产生使湿润红色石蕊试纸变蓝的气体,故A错误;
B.向NaHS溶液中滴入稀盐酸,观察是否有生成臭鸡蛋气味气体( ),说明盐酸酸
性强于 ,非金属性的判断依据是比较最高价氧化物对应水化物的酸性强弱,故B
错误;
C.向两支试管分别加入 和 溶液,向盛有 溶液
试管中加入 蒸馏水,再同时向两支试管中加 ,收集生成的
气体,无法比较生成气体的快慢,应比较收集生成相同体积 气体所需的时间
快慢或比较相同时间收集 的体积多少,故C错误;
D.在试管中加入少量酸性 溶液,然后向试管中逐滴加入 溶液,
溶液褪色或变浅,则证明 的还原性,故D正确。
答案为:D。
3.实验室常利用难挥发性酸制备易挥发性酸的原理,用浓硫酸与硝石(NaNO )反应制
3
备HNO 反应装置如图,下列说法不正确的是
3
资料收集整理【淘宝店铺:向阳百分百】A.可从实验室中选无色透明洁净的试剂瓶盛装制得的硝酸
B.反应方程式为:
C.反应温度如果过高,制得HNO 可能会呈现黄色
3
D.曲颈甑不适宜制备沸点过低的物质
【答案】A
【详解】A.浓硝酸见光易分解,应用棕色玻璃细口瓶盛装浓硝酸,A错误;
B.该反应利用高沸点的浓硫酸制取低沸点的硝酸,反应方程式为:
,B正确;
C.硝酸在温度过高时能分解生成二氧化氮、氧气和水,NO 溶于水呈黄色,C正确;
2
D.曲颈是一种原始的蒸馏烧瓶,冷凝效果较差,不适宜制备沸点过低的物质,D正确;
故选A。
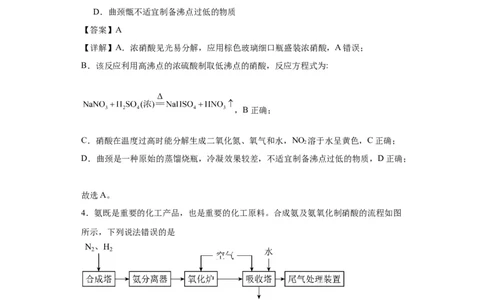
4.氨既是重要的化工产品,也是重要的化工原料。合成氨及氨氧化制硝酸的流程如图
所示,下列说法错误的是
A.酸 雨和光化学烟雾的形成均与氮氧化物有关
B.吸收塔中若转移 个电子,则反应的NO物质的量为0.1mol
C.氧化炉中发生反应的化学方程式为
D.从氨分离器中分离出氨,主要利用了其易液化的性质
【答案】B
资料收集整理【淘宝店铺:向阳百分百】【详解】A.酸雨和光化学烟雾的形成均与氮氧化物有关,A正确;
B.4NO+3O +2H O=4HNO ,反应中氮元素化合价由+2变为+5,电子转移关系为
2 2 3
4NO:12e-,若转移0.6N 个电子,则参与反应的NO为0.2mol,B错误;
A
C.氧化炉中发生反应的化学方程式为 ,C正确;
D.从氨分离器中分离出氨,主要利用了其易液化的性质,D正确;
故选B。
5. 的KOH溶液称为奈斯勒(Nessler)试剂,其制备流程及特色反应如图所示。
下列说法错误的是
A.反应①的离子方程式为:
B.由反应②可知用KI溶液可除去 中的
C.反应③中消耗的 和 的物质的量之比为1:4
D.可用奈斯勒试剂检验 中微量的
【答案】B
【详解】汞和过量的稀硝酸反应生成硝酸汞,再和过量的碘化钾溶液反应生成,再加
入氢氧化钾和微量的铵根离子反应生成奈斯勒试剂。
A.汞和硝酸反应生成硝酸汞和一氧化氮和水,反应的离子方程式为
,A正确;
B.反应②用碘化钾反应除去硝酸银,B错误;
C.反应③离子方程式为: = +3I-+3H O,其中消
2
耗的 和 的物质的量之比为1:4,C正确;
资料收集整理【淘宝店铺:向阳百分百】D.奈斯勒试剂遇到铵根离子反应生成红色沉淀,故能检验 中微量的
,D正确;
故选B。
6.利用NH 吸收液和ClO 可实现煤炭燃烧烟气高效脱硫(SO )脱硝(NO),吸收处理后
3 2 2
得到废液,其成分主要为(NH )SO 、NH NO 、NH Cl。已知ClO 在碱性条件下会产生
4 2 4 4 3 4 2
,下列说法错误的是
A.脱除NO的总反应为
B.标准状况下,脱除含SO 、NO各0.1mol的烟气,至少共需要8.96LNH
2 3
C.每生成1molNH Cl至少需要1molClO
4 2
D.碱性越强,脱除效率越高
【答案】D
【详解】A.脱除NO过程NO被氧化,总反应为
,故A正确;
B.结合得失电子守恒,标准状况下,脱除含SO 、NO各0.1mol的烟气,需要ClO 为
2 2
0.1mol,根据元素守恒,至少共需要0.4molNH ,为8.96LNH ,故B正确;
3 3
C.结合氯元素守恒,每生成1molNH Cl至少需要1molClO,故C正确;
4 2
D.ClO 在碱性条件下会产生 ,根据得电子数量判断,碱性越强,脱除效率越低,
2
故D错误;
故选D。
7.为探究木炭与浓硝酸的反应原理,某同学设计如下四组实验,发现所有实验过程均
有红棕色气体产生,不考虑空气对反应的影响,下列说法错误的是
① ② ③ ④
A.所有实验产生的气体均为混合物
B.③和④中生成的气体成分可能相同
资料收集整理【淘宝店铺:向阳百分百】C.②中红棕色气体全部为木炭与浓硝酸反应产生
D.①说明浓硝酸不稳定受热易分解
【答案】C
【分析】浓硝酸分解产生NO 和O 和HO,而浓硝酸和C反应产生CO、NO 、HO。
2 2 2 2 2 2
【详解】A.有上分析,所有实验中的气体均为混合物,A项正确;
B.③中可能浓硝酸受热分解,但可能与木炭接触发生反应;而④浓硝酸受热可能分解,
挥发的硝酸与木炭接触也可能发生反应,所有两个实验气体成分可能相同,B项正确;
C.木炭需要在加热条件下才能与浓硝酸发生反应产生NO ,该条件下木炭不和浓硝酸
2
反应,C项错误;
D.浓硝酸遇灼热的碎瓷片分解产生NO ,说明其不稳定易分解,D项正确;
2
故选C。
8.在密闭容器中,外接电路放电,研究压强与氧气的变化。实验操作如下:①外接电
路放电一段时间;②停止放电一段时间;③注入石蕊试液。得到压强、氧气浓度在以
上时间段的变化图像如下(忽略温度变化)。下列基于图像的推理或判断错误的是
A.Ⅰ~Ⅱ: 与 反应生成NO
B.Ⅱ~Ⅲ:NO与 反应生成
C.Ⅳ~Ⅴ: 与 生成 ,同时也存在NO与 生成 的反应
D.Ⅰ~Ⅴ:均明显存在 的反应
【答案】D
【详解】由题意可知,放电、停止放电条件下,会先有 ,然后有
,而且这两个反应都能使压强减小。
资料收集整理【淘宝店铺:向阳百分百】A.在Ⅰ~Ⅱ段图像中,放电情况下, ,氧气浓度下降,压强没有变化,
A正确;
B.在Ⅱ~Ⅲ段中,停止放电发生 ,氧气浓度下降,压强减小,B正
确;
C.在Ⅳ~Ⅴ段中,注入石蕊溶液发生 , ,
氧气浓度略有下降,压强减小,C正确;
D.从Ⅰ~Ⅱ段图像来看,压强不变,无 反应,D错误;
故选D。
9.一定条件下,含氮元素的物质可发生如图所示的循环转化。下列说法正确的是
A.循环转化中属于“固氮”过程的是“反应c”和“反应b”
B.转化过程中发生非氧化还原反应的过程只有“反应I”
C.若“反应h”是在NO 与HO的作用下实现的,则该反应中氧化产物与还原产物
2 2
的物质的量之比为1:2
D.工业上可以用氢氧化钠溶液消除NO
2
【答案】D
【详解】A.氮的固定指由游离态的氮转化为化合态,图中属于氮的固定的是“反应
c”和“反应k”,A错误;
B.没有元素化合价变化的反应属于非氧化还原反应,则过程中非氧化还原反应为a和
l,B错误;
C.过程h发生反应为: ,该反应中氧化剂与还原剂的物质的
量之比为: ,氧化产物与还原产物的物质的量之比为 ,C错误;
资料收集整理【淘宝店铺:向阳百分百】D. 能与 发生反应: ,所以工业上可
以用氢氧化钠溶液消除 ,D正确;
故选D。
10.根据下列实验操作和现象,所得出的结论或解释正确的是
选
实验操作和现象 结论或解释
项
淀粉-KI溶液中通入 ,再通入 ,溶液先出
A 还原性:
现蓝色,后蓝色褪去
盐酸具有强氧化性,将
B 向 溶液中滴加盐酸,溶液变为浅黄色
转为
用蘸有浓氨水的玻璃棒靠近某有色气体X,出现白
C 该气体一定是HCl
烟
用大理石和盐酸反应制取 气体,立即通入一定
D 酸性:
浓度的 溶液中,出现白色沉淀
A.A B.B C.C D.D
【答案】A
【详解】A.由现象可知氯气氧化碘离子生成碘单质,后碘与SO 发生氧化还原反应生
2
成硫酸、HI,则还原性为SO >I->Cl-,故A正确;
2
B.向 溶液中滴加盐酸,相当于溶液中存在硝酸,硝酸可以氧化亚铁离子为
铁离子,溶液变为浅黄色,并不是盐酸氧化了亚铁离子,故B错误;
C.用蘸有浓氨水的玻璃棒靠近某有色气体X,出现白烟,该气体为Cl,HCl没有颜
2
色,故C错误;
D.盐酸为挥发性酸,盐酸能与硅酸钠溶液反应,则该实验不能比较碳酸、硅酸的酸
性,故D错误;
故选A。
11.废旧CPU中的金(Au)、Ag和Cu回收的部分流程如下:
资料收集整理【淘宝店铺:向阳百分百】已知: 。下列说法正确的是
A.“酸溶”时用浓硝酸产生 的量比用稀硝酸的少
B.“操作a”需用到分液漏斗
C.用浓盐酸和 也可以溶解金
D.用过量Zn粉将1mol 完全还原为Au,参加反应的Zn为1.5mol
【答案】C
【分析】硝酸与金不反应,与银和铜反应,酸溶后操作a过滤得到金,滤液中含金属
离子为铜离子和银离子,经过溶金分离后得到氯金酸溶液,用锌粉还原得到金。
【详解】A.浓硝酸被还原产生NO ,产生1molNO 得1mol电子,稀硝酸被还原产生
2 2
NO,产生1molNO得3mol电子,金属的量相同,“酸溶”时用浓硝酸产生NO 的量
x
比稀硝酸的多,A错误;
B.“操作a”为过滤,需要用到烧杯、玻璃棒、普通漏斗,B错误;
C.浓盐酸和 在溶液中电离产生氢离子和硝酸根离子,相当于有硝酸,也可以溶
解金,C正确;
D. ,氢离子也会与锌反应, 参加反应时转移的电子
物质的量为4mol,消耗锌的物质的量为2mol,D错误;
故选C。
12.硝酸工业生产中常用纯碱溶液吸收排出的氮氧化物废气,废气中只含有NO、
两种气体。将一定量废气通入到足量的 溶液中被完全吸收,溶液中生成
的 、 两种离子的物质的量与废气中 的物质的量分数
变化关系可用如图所示。已知溶液中可发生以下两个反应:
①
②
资料收集整理【淘宝店铺:向阳百分百】下列说法正确的是
A.图中线段a表示 离子
B.随x值增大,溶液中 变大
C.若测得所得溶液中 为0.5 mol,则x值为0.8
D. 时,反应中可收集到标准状况下22.4 L
【答案】D
【详解】A.线段a上当x=0.5,发生反应① ,只
生成 ,其物质的量为2mol,而x=1.0,发生反应②
,溶液中生成的 、 均为1mol,随x
增大, 的物质的量减小,而 的物质的量增大,故线段a表示 、线段b表
示 ,故A错误;
B.由反应方程式可知 ≤1时,即x≥0.5,混合气体可以被完全吸收,由氮原子
守恒可知 = ,NO、NO 总物质的量一定,则
2
为定值,故B错误;
C.由A中分析可知,线段a表示 、线段b表示 ,溶液中 为0.4mol,
资料收集整理【淘宝店铺:向阳百分百】根据氮原子守恒可知 =2mol-0.4mol-1.6mol,作如图所示辅助线:
,可知AB为0.4mol,利用相似三角形有
,解得BC=0.2,故C点对应的x=0.5+0.2=0.7,故C错误;
D.x=0.6时,NO、NO 被完全吸收,由反应方程式可知n(CO)=
2 2
=0.5×2mol=1mol,标准状况下可以收集CO 体积为1mol×22.4L/mol=22.4L,故D正确;
2
故选D。
13.无色气体甲可能含 、 、 、 、 中的几种,将 气体甲经
过如图所示实验的处理,结果得到酸性溶液,而几乎无气体剩余,下列说法正确的是
A.气体甲中一定含有
B.经过 处理后剩余气体体积大于
C.气体甲的组成可能为 、 、
D.经过浓硫酸处理后余气中 、 体积比为
资料收集整理【淘宝店铺:向阳百分百】【答案】D
【分析】无色气体,不可能含有 ,将混合气体通过浓硫酸,气体体积减少
20mL,证明混合气体中含有 ,通过足量的 ,气体显红棕色,原混合
气体中含有 和 ,混合气体通入水中,几乎无气体剩余,所以很合气体中没有
,且 与 反应产生的 与 刚好完全反应: 。
【详解】A.根据以上分析,混合气体为无色,所以不可能含有 ,A错误;
B.将混合气体通过浓硫酸,气体体积减少20mL,剩余气体为 ,通过足量的
,气体变成红棕色,发生反应: ,和反应
,都是气体体积减小的反应,所以经过 处理后剩余气体体积小
于 ,B错误;
C.根据以上分析,混合气体中一定含有 和 ,一定没有 ,C错误;
D.根据反应: 和 ,
,所以 ,D正确;
故选D。
14.将 铜镁合金完全溶解于某浓度的硝酸中,得到 和 的混合气体
(标准状况),当向反应后的溶液中加入一定浓度 溶液时,金属离子全部转化为沉
淀,测得沉淀的质量为 。 和 的混合气体中, 的体积分数是
A. B. C. D.
【答案】A
【详解】金属阳离子沉淀后生成氢氧化物,因此
资料收集整理【淘宝店铺:向阳百分百】, , 根据得失电子数目守恒,
3n(NO)+n(NO )=1mol,n(NO)+n(NO )= ,联立解得n(NO)=0.3mol,
2 2
n(NO )=0.1mol,相同条件下,体积分数等于物质的量分数,因此二氧化氮的体积分数
2
为 =25%,故选A。
15.探究铜与硝酸反应的生成 时的硝酸浓度。如图所示,先通 一段时间后关闭
活塞K,将铜丝伸入溶液中,当A中气体变为无色时,上提铜丝,再将B中溶液稀释
至 ,取 ,用 的 溶液滴定至终点时消耗 (忽
略硝酸的挥发、分解及溶液体积变化)。下列说法正确的是
A.可用盛有 溶液的洗气瓶进行尾气吸收
B.铜与硝酸反应主要生成 时的硝酸浓度不大于
C.若不通 ,可能导致所得实验结果偏高
D.若通过直接滴定A中剩余酸的量(掩蔽掉 的干扰)进行求算,所得实验结果
偏低
【答案】D
【分析】A瓶中的反应为4HNO(浓)+Cu=2NO ↑+2H O+Cu(NO )。B中发生的反应为
3 2 2 3 2
3NO +H O=2HNO +NO。用0.20molL−1的NaOH溶液滴定至终点时消耗15.00mL,即
2 2 3
n(NaOH)=0.20×15.00×10-3mol=3×10-3⋅mol,有关系式为NaOH~HNO 则B瓶中产生的
3
n(HNO)= 3×10-3mol×10=3×10-2mol,又3NO ~2HNO 则A瓶中产生的NO 为3×10-
3 2 3 2
2mol× =4.5×10-2mol。由关系式得4HNO(浓)~2NO 则消耗的浓硝酸为4.5×10-
3 2
资料收集整理【淘宝店铺:向阳百分百】2×2=9×10-2mol。
【详解】A.NaOH溶液不能直接与NO反应,所以它不能吸收尾气,A项错误;
B.溶液中剩余的硝酸浓度为 。但当反
应产生无色NO气体时停止反应,即硝酸浓度大于8molL−1也产生了NO,B项错误;
C.若不同如N
2
,B瓶中NO也转变为HNO
3
,从而导致⋅消耗的HNO
3
偏大,A中剩余
HNO 偏低,结果偏低,C项错误;
3
D.当A中气体变为无色时停止反应,产生NO的浓度应该比A瓶的大。所以直接测
定A瓶中的酸可能导致结果偏低,D项正确;
故选D。
16.现用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。下列说法正确
的是
A.制取氨气时烧瓶中的固体常用
B.将湿润的蓝色石蕊试纸置于三颈烧瓶瓶口,试纸变红,说明 已经充满
C.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验,
电脑绘制三颈瓶内压强变化曲线如图2,则B点时喷泉最剧烈
D.若实验是在0℃、常压条件下完成,则在E点烧瓶中溶液溶质的物质的量浓度
为
【答案】D
【详解】A.CaO能与水反应,使c(OH-)增大,同时放出大量的热,有利于氨气的逸
出,氢氧化钠也可以抑制NH ·H O的电离,从而促进氨气的生成,固体常用氧化钙或
3 2
氢氧化钠,故A错误;
B.氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而导致氨水呈碱性,红色
资料收集整理【淘宝店铺:向阳百分百】石蕊试液遇碱变蓝色,所以检验三颈瓶集满NH 的方法是将湿润的红色石蕊试纸靠近
3
瓶口c,试纸变蓝色,证明NH 已收集满,故B错误;
3
C.三颈瓶内气体与外界大气压压强之差越大,其反应速率越快,C点压强最小、大气
压不变,所以大气压和C点压强差最大,则喷泉最剧烈,故C错误;
D.0℃、常压条件下气体摩尔体积是22.4L/mol,则在E点烧瓶中溶液溶质的物质的量
浓度为 ,故D正确;
故选:D。
17.铁与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系如图,下列说
法不正确的是
A.一般来说,不同密度硝酸与铁反应的还原产物不是单一的
B.一定量铁粉与足量密度为1.36g/mL的 反应,若在标准状况下得到2.24L
气体,则有0.3mol硝酸参加反应
C.足量铁与一定量密度为1.36g/mL的硝酸反应,反应的化学方程式始终是
D.硝酸的密度越大,其还原产物中高价态的成分所占比例越多
【答案】C
【详解】A.根据图像可知,随硝酸密度被还原产物不同,在浓硝酸密度为1.4g/mL中,
主要产物NO ,随着硝酸密度逐渐降低,产物NO 逐渐减少而NO的相对含量逐渐增
2 2
多,当密度为1.36g/mL时,主要产物是NO 和NO,当 的密度降到1.1g/mL时,
2
离子成为主要产物,故A正确;
资料收集整理【淘宝店铺:向阳百分百】B.一定量铁粉与足量密度为1.36g/mL的 反应,标准状况下得到气体2.24L,物
质的量为0.1mol,由图可知,此时生成0.05molNO、0.05molNO ,铁变化为硝酸铁,
2
~NO~3e-, ~NO~e-,Fe~Fe3+~3e-,反应生成的铁离子为
2
= mol,显酸性的硝酸为 mol=0.2mol,氧化剂的硝酸为
0.1mol,所以参加反应的硝酸为0.2mol+0.1mol=0.3mol,故B正确;
C.足量铁与一定量密度为1.36g/mL的硝酸反应过程中,硝酸不断被稀释,当硝酸浓
度较低时,只生成NO,故C错误;
D.还原产物中 的物质的量分数随硝酸密度减少而增大,铵根离子中氮元素化合
价最低是-3价,在浓硝酸浓度为1.4mol/L中,主要产物NO ,硝酸的密度越大、浓度
2
越大,其还原产物中高价态的成分所占比例越多,故D正确;
故选C。
18.某小组同学发现Cu与浓 反应所得混合溶液为绿色,Cu与稀 反应所得
混合溶液为蓝色,针对绿色产生的原因展开探究。
实验猜想:猜想a: 浓度大,猜想b: 溶解在 溶液中
实验方案
方案
配制饱和 溶液,观察溶液颜色
1
方案 取适量Cu与浓 反应后的绿色混合溶液,置于如图所示装置中,鼓入空
2 气后,溶液上方可观察到_______,5 min后,溶液完全变为蓝色
方案
加热该绿色溶液,观察溶液颜色
3
资料卡片:① 能与水反应生成 ,进而发生下述反应:
(绿色) ②亚硝酸受热易分解,产生NO和
③亚硝酸能被空气氧化
资料收集整理【淘宝店铺:向阳百分百】下列说法不正确的是
A.Cu与浓 反应中硝酸体现强氧化性和酸性
B.方案1中若配得溶液呈蓝色,则证明猜想a不成立
C.方案2中溶液上方看到生成红棕色气体,则证明猜想b一定成立
D.方案3观察到溶液上方生成红棕色气体,溶液完全变为蓝色
【答案】C
【详解】A.Cu与浓 反应中生成硫酸铜、二氧化氮和水,硝酸体现强氧化性和
酸性,故A正确;
B.猜想a认为 溶液浓度大时呈绿色,浓度小时呈蓝色,故若配制饱和
溶液,溶液呈蓝色,证明猜想a不成立,故B正确;
C.由于 与水反应能够生成 , 与 能够发生可逆反应
(绿色) ,|随着空气的通入, 被氧化为
,使得上述可逆反应平衡逆向移动,溶液由绿色变为蓝色,但溶液上方呈红棕
色气体说明 溶液中的确溶有 ,因此猜想b不严谨,不能说明溶液呈绿
色的原因一定是 溶解在 溶液,故C错误;
D.加热该绿色溶液,可以降低气体的溶解度,使溶解在其中的 逸出,且加热亚
硝酸分解产生NO和 ,溶液上方产生红棕色气体,溶液由绿色变为蓝色,故D正
确。
综上所述,答案为C。
19.无色的混合气体甲中可能含有 、 、 、 、 中的几种,将
气体甲经过图实验处理,结果得到酸性溶液,而无气体剩余,则下列说法不正
确的是
资料收集整理【淘宝店铺:向阳百分百】A. ;
B.气体甲的组成是 、 、
C.气体显红棕色的原因:
D.集气瓶中溶液的主要溶质是
【答案】A
【分析】开始时混合气体为无色,故混合气体中无NO ;通过浓HSO 后气体体积减
2 2 4
小,说明含有NH 且为20mL;通过足量过氧化钠后气体显红棕色,说明混合气体中含
3
有CO 和NO,相关的化学方程式为2NaO+2CO =2Na CO+O ,2NO+O =2NO;而最
2 2 2 2 2 3 2 2 2
后将剩余气体通入水中得到酸性溶液且几乎无剩余气体,说明原混合气体中无N,根
2
据反应方程式4NO+3O +2H O=4HNO 、2NaO+2CO =2Na CO+O ,故NO与CO 的
2 2 3 2 2 2 2 3 2 2
物质的量之比为4:6,则80mL气体中有32mL NO和48mL CO 。
2
【详解】A.根据分析可知 ; ,A错误;
B.根据分析可知气体甲的组成是 、 、 ,B正确;
C.根据分析可知气体显红棕色的原因: ,C正确;
D.根据分析可知集气瓶中溶液的主要溶质是 ,D正确;
故选A。
20.如图所示,实验室中利用洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体
生成,Y型管左侧得到Cu S和白色固体a,倾斜Y型管使左侧的物质全部转移到右侧
2
稀硝酸中,反应生成固体单质b、a的溶液和NO。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.白色固体为CuSO
4
B.NO为还原产物,b为氧化产物
C.NO与b的物质的量之和可能为0.2 mol
D.参加反应的浓硫酸中,表现氧化性的占25%
【答案】C
【分析】洁净的铜片(0.3 mol)和浓硫酸反应为5Cu+4H SO (浓)
2 4
=Cu S↓+3CuSO+4H O,则生成0.06molCu S,Cu S和硝酸、硫酸反应为
2 4 2 2 2
3Cu S+4HNO +6H SO =6CuSO+3S+4NO↑+8H O,则生成NO、S为0.14mol。
2 3 2 4 4 2
【详解】A.洁净的铜片(0.3 mol)和浓硫酸进行反应,实验中无气体生成,得到Cu S
2
和白色固体a,根据分析,a为CuSO ,A正确;
4
B.NO由HNO 被还原得到,为还原产物,b为Cu S和硝酸反应生成的S,Cu S被氧
3 2 2
化,为氧化产物,B正确;
C.根据分析,NO与b的物质的量之和为0.14mol,C错误;
D.根据5Cu+4H SO =Cu S↓+3CuSO+4H O,参加反应的浓硫酸中,表现氧化性的占
2 4 2 4 2
25%,D正确;
故选C。
资料收集整理【淘宝店铺:向阳百分百】