文档内容
专项训练 活化能的判断及计算(解析版)
一、单选题
1.某科研小组研究臭氧脱除 和NO工艺,反应原理如下:
反应I:
反应II:
已知:臭氧本身不稳定,适当的温度可以加速其分解反应: 。向容
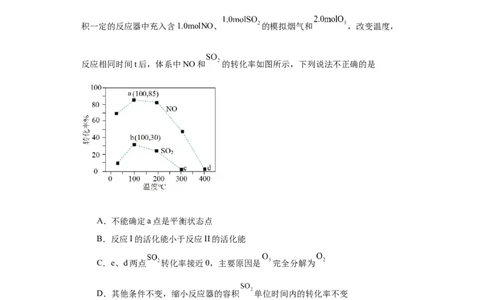
积一定的反应器中充入含1.0molNO、 的模拟烟气和 ,改变温度,
反应相同时间t后,体系中NO和 的转化率如图所示,下列说法不正确的是
A.不能确定a点是平衡状态点
B.反应I的活化能小于反应II的活化能
C.e、d两点 转化率接近0,主要原因是 完全分解为
D.其他条件不变,缩小反应器的容积 单位时间内的转化率不变
【答案】D
【详解】A.由图可知,温度高于100℃,NO的转化率减小,原因可能是平衡逆向移
动,也可能是 分解,使反应I的反应速率减慢,相同时间内NO转化率减小,故A
正确;
B.单位时间内转化率高,反应越快,活化能越小,由图可知相同时间内NO的转化率
高于 ,则反应I的活化能小于反应II,故B正确;
资料收集整理【淘宝店铺:向阳百分百】C.只有 完全分解了,NO、 才会接近不反应,故C正确;
D.其他条件不变,缩小反应器的容积,反应速率增大, 单位时间内的转化率会变
大,故D错误;
故选:D。
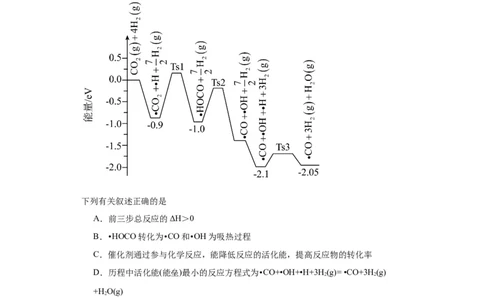
2.科学工作者结合实验与计算机模拟结果,研究了在Pt/SiO 催化剂表面上CO 与H
2 2 2
的反应历程,前三步历程如图所示,其中吸附在Pt/SiO 催化剂表面上的物种用“•”
2
标注,Ts表示过渡态。
下列有关叙述正确的是
A.前三步总反应的ΔH>0
B.•HOCO转化为•CO和•OH为吸热过程
C.催化剂通过参与化学反应,能降低反应的活化能,提高反应物的转化率
D.历程中活化能(能垒)最小的反应方程式为•CO+•OH+•H+3H (g)= •CO+3H (g)
2 2
+H O(g)
2
【答案】D
【详解】A.由图像分析可知,前三步总反应,反应物能量高,生成物能量低,故反
应放热,△H<0,A错误;
B.根据图像,•HOCO 转化为•CO和•OH是图中的第三步反应,是放热过程,B错误;
C.催化剂只能增大反应速率,不会影响平衡,对转化率无影响,C错误;
D.根据图像分析可知, Ts3活化能最小,历程中活化能(能垒)最小的反应方程式
为•CO+•OH+•H+3H (g)= •CO+3H (g)+HO(g),D正确;
2 2 2
故答案选D。
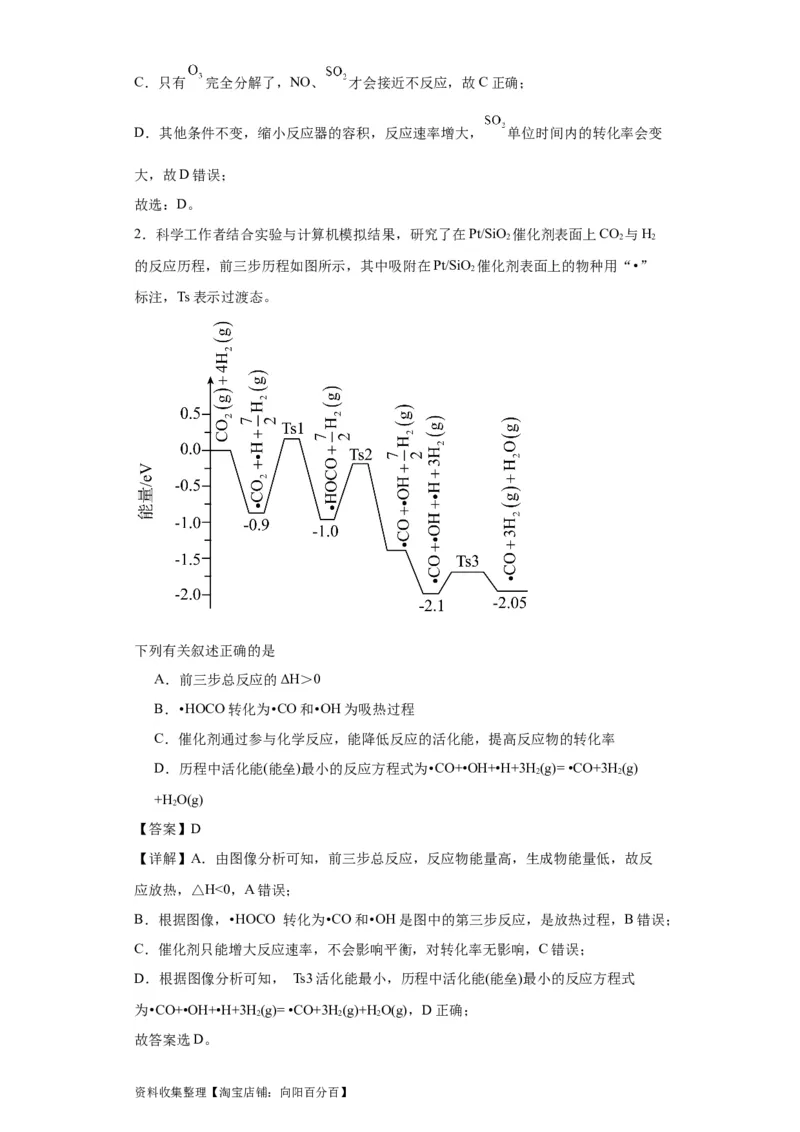
资料收集整理【淘宝店铺:向阳百分百】3.一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),
下列说法不正确的是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】C
【详解】A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于
反应Ⅱ放出的热量,反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应
Ⅱ,故A正确;
B.短时间里反应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的
速率快,速率越快,其活化能越小,则反应活化能:反应I<反应Ⅱ,故B正确;
C.增加 浓度,平衡正向移动,但平衡时产物Ⅱ和产物I的比例可能降低,故C错
误;
D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,故D
正确。
综上所述,答案为C。
4.已知阿仑尼乌斯公式是反应速率常数随温度变化关系的经验公式,可写作
(k为反应速率常数, 为反应活化能,R和C为大于0的常数),为探究
m、n两种催化剂对某反应的催化效能,进行了实验探究,依据实验数据获得曲线如图
所示。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.在m催化剂作用下,该反应的活化能 J⋅mol-1
B.对该反应催化效能较高的催化剂是m
C.不改变其他条件,只升高温度,反应的活化能不变
D.无法根据该图像判断升高温度时平衡移动的方向
【答案】B
【详解】A.将坐标 和 代入 中,计算可知
J⋅mol,A正确;
B.对比图中直线m和n的斜率绝对值的大小可知,使用催化剂n时对应的 较小,
则对该反应催化效能较高的催化剂是n,B错误;
C.图中m、n均为直线,斜率不发生变化,因此不改变其他条件,只升高温度,反应
的活化能不变,C正确;
D.阿仑尼乌斯公式表示反应速率常数随温度的变化关系,无法根据该图像判断升高
温度时平衡移动的方向,D正确;
故选B。
5.NO是一种温室气体,且易形成颗粒性污染物,研究NO的分解对环境保护有重要
2 2
意义。
途径I:
途径II:向盛有NO的容器中通入少量碘蒸气
2
① (快反应)
② (慢反应)
③ (快反应)
下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.途经I为吸热反应 B.反应②的活化能比反应③的小
C.IO为反应的中间产物 D.途径II中I 为催化剂
2
【答案】B
【详解】A.途经I为化学键断裂的过程是吸热反应,A正确;
B.途径Ⅱ中反应②的速率比反应③慢,则途径Ⅱ中反应②的活化能比反应③大,B错
误;
C.根据途径II的反应历程可知,IO在中间生成又消耗,所以为反应的中间产物,C
正确;
D.途径II中I 参与反应最终又生成I,所以I 为催化剂,D正确;
2 2 2
故选B。
6.2SO (g)+O(g) 2SO (g) ∆H=-198kJ•mol-1。在VO 存在时该反应机理为:
2 2 3 2 5
①VO+SO→2VO +SO(快);②4VO +O →2VO(慢)。下列说法不正确的是
2 5 2 2 3 2 2 2 5
A.该反应速率主要由第②步基元反应决定
B.由反应机理可知,VO 和VO 都是该反应的催化剂
2 5 2
C.VO 的存在提高了该反应活化分子百分数,使单位时间内有效碰撞次数增加,
2 5
反应速率加快
D.逆反应的活化能比正反应的活化能大198kJ•mol-1
【答案】B
【详解】A.反应①为快反应,反应②为慢反应,总反应速率由最慢的一步决定,该
反应速率主要取决于慢反应,即第②步反应,故A正确;
B.根据反应机理可知,VO 是反应的催化剂,而VO 是中间产物,故B错误;
2 5 2
C.根据反应机理可知,VO 是反应的催化剂,所以提高了该反应活化分子百分数,
2 5
使有效碰撞次数增加,反应速率加快,故C正确;
D.∆H=正反应的活化能﹣逆反应的活化能=-198kJ/mol,所以逆反应的活化能大于
198kJ/mol,故D正确;
故选B。
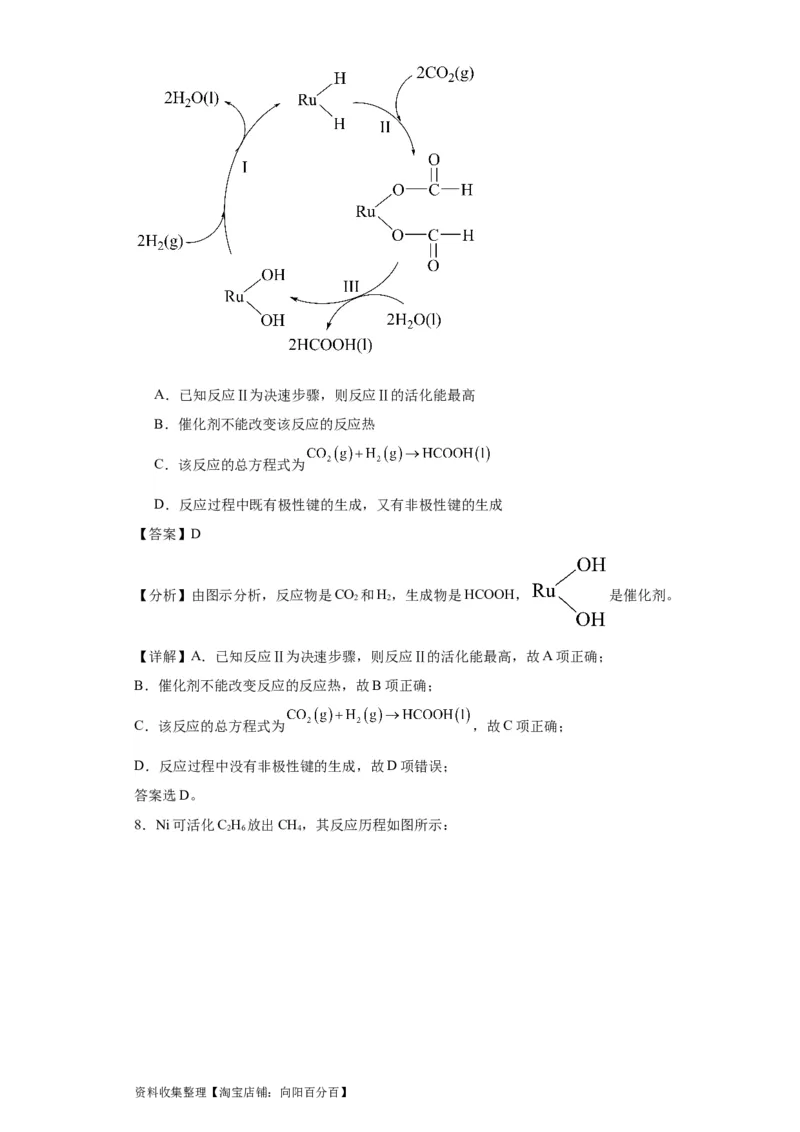
7. 的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂将 转化为有
机原料甲酸的反应机理如图所示。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.已知反应Ⅱ为决速步骤,则反应Ⅱ的活化能最高
B.催化剂不能改变该反应的反应热
C.该反应的总方程式为
D.反应过程中既有极性键的生成,又有非极性键的生成
【答案】D
【分析】由图示分析,反应物是CO 和H,生成物是HCOOH, 是催化剂。
2 2
【详解】A.已知反应Ⅱ为决速步骤,则反应Ⅱ的活化能最高,故A项正确;
B.催化剂不能改变反应的反应热,故B项正确;
C.该反应的总方程式为 ,故C项正确;
D.反应过程中没有非极性键的生成,故D项错误;
答案选D。
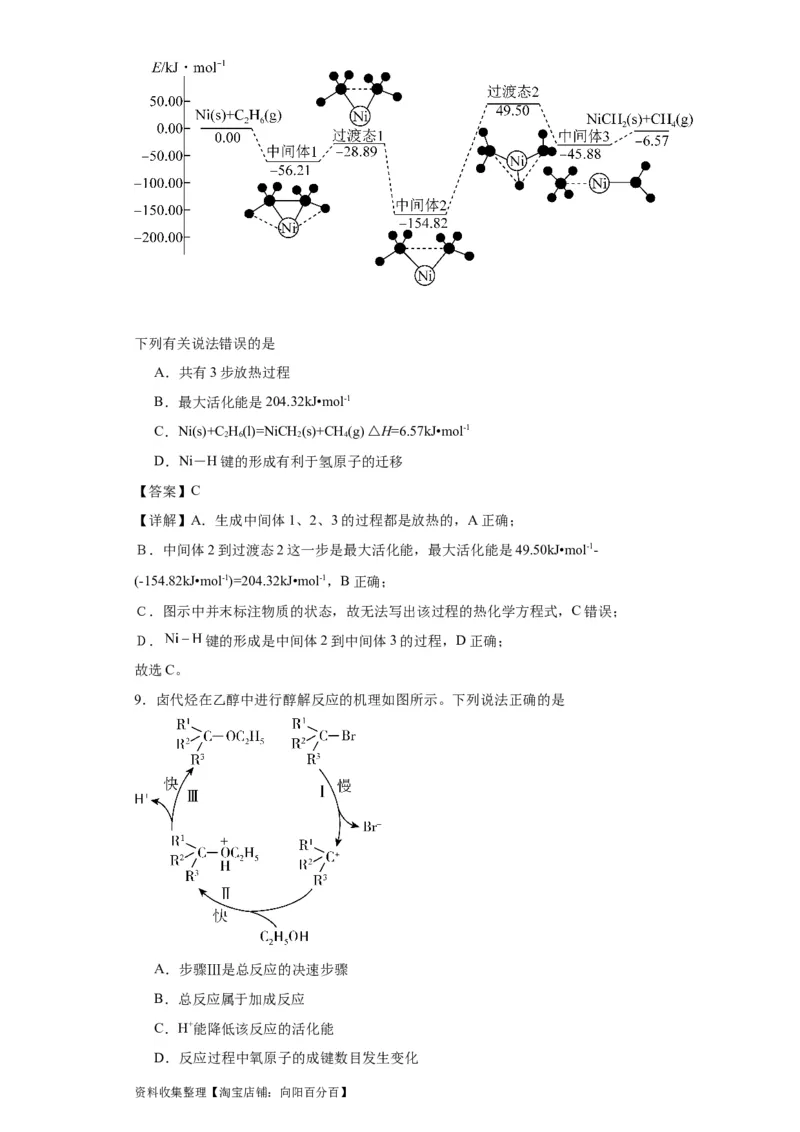
8.Ni可活化C H 放出CH,其反应历程如图所示:
2 6 4
资料收集整理【淘宝店铺:向阳百分百】下列有关说法错误的是
A.共有3步放热过程
B.最大活化能是204.32kJ•mol-1
C.Ni(s)+C H(l)=NiCH (s)+CH(g) △H=6.57kJ•mol-1
2 6 2 4
D.Ni-H键的形成有利于氢原子的迁移
【答案】C
【详解】A.生成中间体1、2、3的过程都是放热的,A正确;
B.中间体2到过渡态2这一步是最大活化能,最大活化能是49.50kJ•mol-1-
(-154.82kJ•mol-1)=204.32kJ•mol-1,B正确;
C.图示中并末标注物质的状态,故无法写出该过程的热化学方程式,C错误;
D. 键的形成是中间体2到中间体3的过程,D正确;
故选C。
9.卤代烃在乙醇中进行醇解反应的机理如图所示。下列说法正确的是
A.步骤Ⅲ是总反应的决速步骤
B.总反应属于加成反应
C.H+能降低该反应的活化能
D.反应过程中氧原子的成键数目发生变化
资料收集整理【淘宝店铺:向阳百分百】【答案】D
【详解】A.慢反应为总反应的决速步骤,因此步骤Ⅰ是总反应的决速步骤,选项A
错误;
B.总反应为卤代烃与醇生成醚的取代反应,选项B错误;
C. 是生成物,不是催化剂,选项C错误;
D.由图知,反应过程中,氧原子成两个键和三个键,选项D正确;
答案选D。
10.以乙烯制备环氧乙烷有两种方法,其中经典方法是氯代乙醇法,化学反应如下:
i.
ii.
现代石油化工采用银作催化剂,实现一步反应,原理如下:
设 为阿佛伽德罗常数的值,下列说法错误的是
A.标准状况下,11.2L乙烯中含极性键的数目
B.现代方法是理想的绿色化学工艺
C. 的电子式为
D.现代方法中Ag提高了反应的活化能
【答案】D
【详解】A.乙烯分子中四个碳氢键为极性键,故0.5mol乙烯含有极性键 ,A正
确;
B.现代方法是理想的绿色化学工艺,原子利用率100%,B正确;
C. 为离子化合物,电子式为 ,C正确;
D.Ag做催化剂,改变反应历程,降低活化能,D错误。
故选D。
资料收集整理【淘宝店铺:向阳百分百】11.等物质的量的 与HBr加成生成两种主要产物X、Y的能量与反
应过程如图所示下列说法正确的是
A.产物Y比产物X更稳定
B. 的过程放出能量
C.W→X正反应的活化能比W→Y正反应的活化能大
D. 的速率比W→X(或Y)的快
【答案】A
【详解】A.物质的能量越低物质越稳定,由图可知Y的能量更低,因此Y更稳定,
故A正确;
B.由图可知 与HBr的总能量低于W的总能量,该过程是吸收能
量,不是释放能量,故B错误;
C.由图可知W→X正反应的活化能比W→Y正反应的活化能小,故C错误;
D. 正反应活化能比W到X(Y)正反应活化能大,活
化能越大反应速率越慢,故D错误;
答案选A。
12.某反应加入催化剂后,反应历程变成两个基元反应,相关能量变化如图所示为(E
为正值,单位:kJ/mol)。下列有关说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.此条件下,第一个基元反应的反应速率小于第二个
B.总反应的活化能
C.对于Ea(活化能)>0的反应,必须加热才能进行
D.总反应的焓变
【答案】D
【详解】A.第一个基元反应活化能较小,反应速率较快,A错误;
B.该反应总反应的活化能为反应物的能量和过渡态Ⅱ的能量之差,即
,B错误;
C.反应是否需要加热与活化能没有必然联系,C错误;
D.反应物与生成物能量之差为 ,所以
,D正确;
故选:D。
13. 选择性催化还原 的反应为 ,其反应历程如图
所示。一定温度下,向恒容密闭容器中充入一定量的 、 和 ,发生反应。下
列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.使用催化剂, 、 的活化分子数增多,还原 的速率加快
B.①的反应速率快,说明反应①的活化能大,是整个反应的决速步
C. 与催化剂发生强的化学吸附,而 在此过程中几乎不被催化剂吸附
D.其他条件不变时,增大 的浓度,能使更多的 转化为
【答案】B
【详解】A.使用催化剂能降低反应的活化能,活化分子数增多,反应速率加快,A正
确;
B.反应①的反应速率快,说明反应①的活化能小,反应的决速步是反应速率最慢的反
应②,B错误;
C.由反应历程图可知,在反应过程中, 与催化剂发生强的化学吸附,而 与
NH 结合, 几乎不被催化剂吸附,C正确;
3
D.其他条件不变时,增大 的浓度,平衡正向移动,能使更多的 转化为 ,
D正确;
故选B。
14.在恒容密闭容器中,等物质的量的 和 混合气体发生反应:
,其反应机理分为三步进行:①
(快速平衡);② (慢反应);③
资料收集整理【淘宝店铺:向阳百分百】(快反应)。下列有关说法正确的是
A.反应②的活化能小于反应③的活化能
B.反应的中间产物是 ,而 是催化剂
C.v(第一步的逆反应)>v(第二步的正反应)
D.反应③中 与 的碰撞均为有效碰撞
【答案】C
【详解】A.反应②最慢,说明活化能最大,A错误;
B.反应过程中 和 均是中间产物,不是催化剂,B错误;
C.反应①快速平衡,说明第一步反应的正、逆反应速率都较大,则第一步反应的逆反
应速率大于第二步慢反应的正反应速率,C正确;
D.反应③为快反应,说明反应的活化能小,微粒之间的许多碰撞能发生化学反应,
但碰撞也是仅部分有效,D错误;
故选C。
15.阿伦尼乌斯经验公式为lnk=lnA (E 为活化能,k为速率常数,R和A为常数),
a
已知反应 (l) (l),其lnk 和lnk 随温度变化的曲线如图所
正 逆
示。下列有关该反应的说法不正确的是
A.正反应的活化能大于逆反应的活化能
B.完全燃烧等质量的M(l)、N(l),N(l)放出的热量多
C.选用合适的催化剂能提高 的平衡转化率
D.温度变化对速率常数的影响程度:lnk >lnk
正 逆
资料收集整理【淘宝店铺:向阳百分百】【答案】C
【详解】A.根据阿伦尼乌斯经验公式lnk=lnA-EaRT(Ea为活化能)可知,题图中曲线
的斜率代表活化能大小,lnk 的斜率大,活化能大,A正确;
正
B.正反应的活化能大于逆反应的活化能,则该反应为吸热反应,生成物N的能量更
高,完全燃烧等质量的M(l)、N(l),N(l)放出的热量更多,B正确;
C.催化剂只影响化学反应速率,不影响化学平衡,不能改变平衡转化率,C错误;
D.lnk 的斜率大,正反应的活化能大,温度变化对k 的影响程度大于对k 的影响
正 正 逆
程度,D正确;
故选:C。
16.已知反应SO (aq)+2I-(aq) 2SO (aq)+I (aq),若起始向反应体系中加入含
2 2
Fe3+的溶液,反应机理如图所示。下列说法正确的是
A.SO 中硫元素显+7价
2
B.反应速率与Fe3+浓度无关
C.由图可知氧化性:Fe3+>SO
2
D.若不加Fe3+,正反应的活化能比逆反应的小
【答案】D
【详解】A.硫最外层只有6个电子,不会显+7;SO 中含有过氧键存在-1价氧,使
2
得硫元素显+6价,A项错误;
B.反应中铁离子参与反应生成亚铁离子,亚铁离子又转化为铁离子,则铁离子为催化
剂,改变反应速率,故反应速率与Fe3+浓度有关,B项错误;
C.氧化剂氧化性大于氧化产物,由图示第二步反应可知,氧化性:Fe3+