文档内容
专项训练 键能、键长、键角及其应用
一、单选题
1.下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
A. 键的键能小于 键的键能
B.三氟乙酸的 大于三氯乙酸的
C.氟化氢分子的极性强于氯化氢分子的极性
D.气态氟化氢中存在 ,而气态氯化氢中是 分子
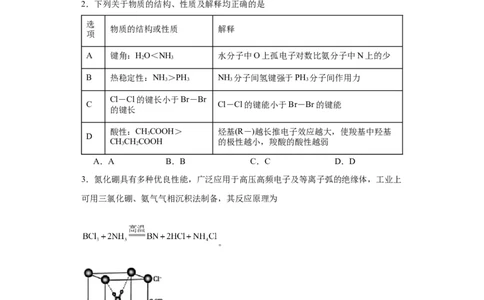
2.下列关于物质的结构、性质及解释均正确的是
选
物质的结构或性质 解释
项
A 键角:HO<NH 水分子中O上孤电子对数比氨分子中N上的少
2 3
B 热稳定性:NH >PH NH 分子间氢键强于PH 分子间作用力
3 3 3 3
Cl-Cl的键长小于Br-Br
C Cl-Cl的键能小于Br-Br的键能
的键长
酸性:CHCOOH> 烃基(R-)越长推电子效应越大,使羧基中羟基
D 3
CHCHCOOH 的极性越小,羧酸的酸性越弱
3 2
A.A B.B C.C D.D
3.氮化硼具有多种优良性能,广泛应用于高压高频电子及等离子弧的绝缘体,工业上
可用三氯化硼、氨气气相沉积法制备,其反应原理为
。
下列说法正确的是
A.电负性:
B.H-Cl键的键能大于H-F键的键能
C. 与 都是由极性键构成的极性分子
资料收集整理【淘宝店铺:向阳百分百】D.氯化铵的立方晶胞结构如图所示,氯化铵晶体的摩尔体积为
4.一定条件下,氨气与氟气发生反应: ,其中NF 分子构型
3
与NH 相似。下列有关说法错误的是
3
A.NF 的分子构型是三角锥型 B.NF 的键角大于NH 中的键角
3 3 3
C.第一电离能:F>N>H D.键能:N-HAsH
3 3
8.X、Y 、Z、W 、Q是原子序数依次增大的短周期主族元素。基态X原子核外有两
个未成对电子,Y是地壳中含量最高的元素 ,其中Z与X同族,W 与Y同族。下列
资料收集整理【淘宝店铺:向阳百分百】说法正确的是
A.原子半径:Z>Y>X
B.XY 和ZY 中的键角:Y-X-Y>Y- Z- Y
2 2
C.气态氢化物的沸点:Z>X
D.氧化物对应水化物的酸性:Q> W
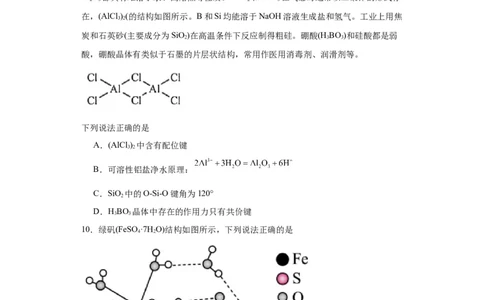
9.在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的。
Be(OH) 和Al(OH) 均为两性氢氧化物,Be(OH) 溶于强碱形成 。BeO和
2 3 2
Al O 都具有难溶于水、高熔点等性质。BeCl 和AlCl 在气态时通常以二聚体的形式存
2 3 2 3
在,(AlCl )(的结构如图所示。B和Si均能溶于NaOH溶液生成盐和氢气。工业上用焦
3 2
炭和石英砂(主要成分为SiO)在高温条件下反应制得粗硅。硼酸(H BO)和硅酸都是弱
2 3 3
酸,硼酸晶体有类似于石墨的片层状结构,常用作医用消毒剂、润滑剂等。
下列说法正确的是
A.(AlCl ) 中含有配位键
3 2
B.可溶性铝盐净水原理:
C.SiO 中的O-Si-O键角为120°
2
D.HBO 晶体中存在的作用力只有共价键
3 3
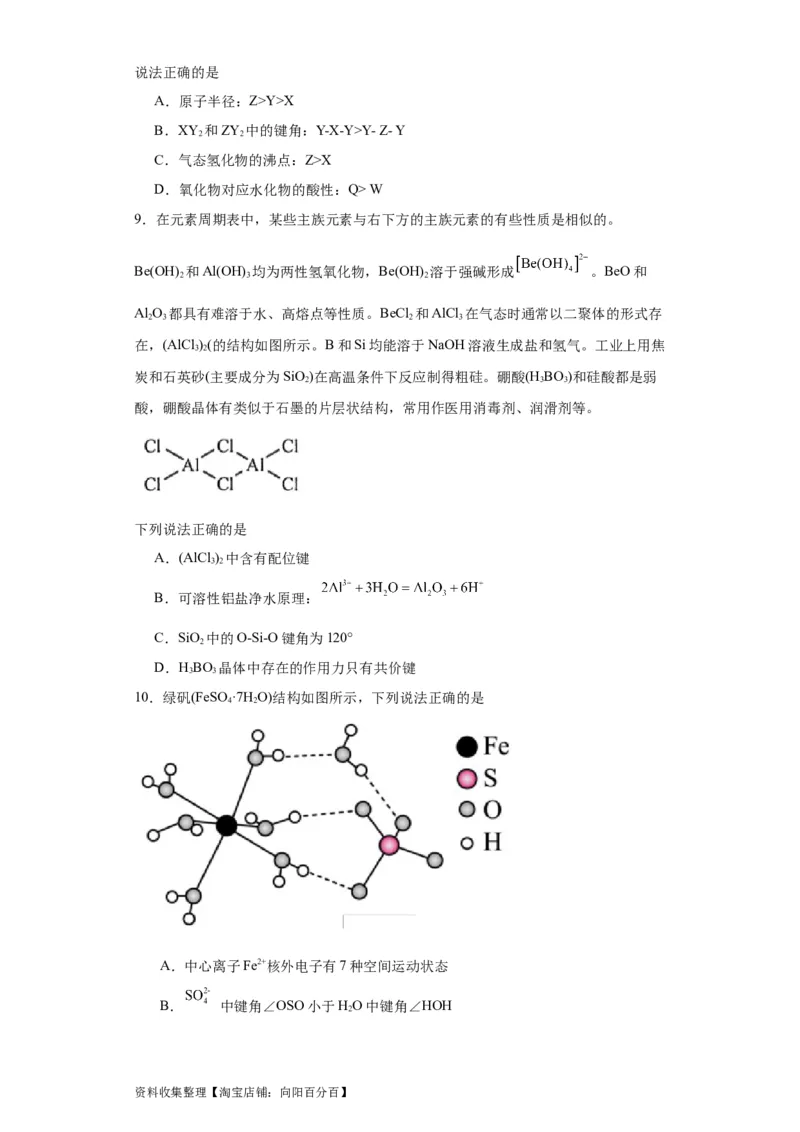
10.绿矾(FeSO ·7H O)结构如图所示,下列说法正确的是
4 2
A.中心离子Fe2+核外电子有7种空间运动状态
B. 中键角∠OSO小于HO中键角∠HOH
2
资料收集整理【淘宝店铺:向阳百分百】C.此结构中HO与Fe2+、HO与 之间的作用力相同
2 2
D.FeSO ·7H O失水后可转为FeSO ·6H O,此过程只破坏了氢键
4 2 4 2
11.下列“类比”结果正确的是
A.第二周期元素氢化物的稳定性:HF>HO>NH ,则第三周期元素氢化物的稳
2 3
定性:HCl>HS>PH
2 3
B.ⅣA族氢化物沸点:GeH >SiH>CH,则VA族元素氢化物沸点:AsH >PH
4 4 4 3 3
>NH
3
C.N≡N键能大,N 性质稳定;则C≡C键能大,CH≡CH性质也稳定
2
D. 和P 都为正四面体形, 中键角为109°28′;则P 中键角也为109°28′
4 4
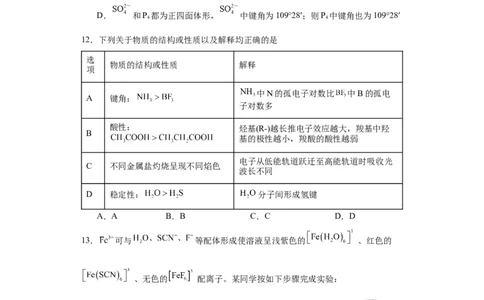
12.下列关于物质的结构或性质以及解释均正确的是
选
物质的结构或性质 解释
项
中N的孤电子对数比 中B的孤电
A 键角:
子对数多
酸性: 烃基(R-)越长推电子效应越大,羧基中羟
B
基的极性越小,羧酸的酸性越弱
电子从低能轨道跃迁至高能轨道时吸收光
C 不同金属盐灼烧呈现不同焰色
波长不同
D 稳定性: 分子间形成氢键
A.A B.B C.C D.D
13. 可与 等配体形成使溶液呈浅紫色的 、红色的
、无色的 配离子。某同学按如下步骤完成实验:
已知:向 的溶液中加入KSCN溶液生成蓝色的 配离子: 不能
与 形成配离子。下列说法不正确的是
A.溶液I中溶液呈黄色可能是由 水解产物的颜色造成
资料收集整理【淘宝店铺:向阳百分百】B.溶液Ⅱ、Ⅲ的颜色分别为红色和无色,说明其中不存在
C.可用 和 溶液检验 溶液中是否含有
D. 中 的键角大于 分子中 的键角
14.水合肼( )是一种无色透明发烟液体,具有强碱性和吸湿性,工业上常用
作抗氧化剂。实验室利用反应
制备水合肼。下列有关说法
正确的是
A.制备时为提高 的转化率,可将 加入到过量NaClO中
B.此反应中 既不是氧化产物也不是还原产物
C. 在空气中会与 反应产生烟雾
D. 中 键角小于 中 键角
15.侯德榜联合制碱法的原理之一是 。
下列关于该原理涉及到的物质说法正确的是
A.NH Cl的电子式为
4
B.CO、 、HO中心原子均为sp3杂化
2 2
C.键角的大小顺序为
D.NaCl晶胞中 的配位数是12
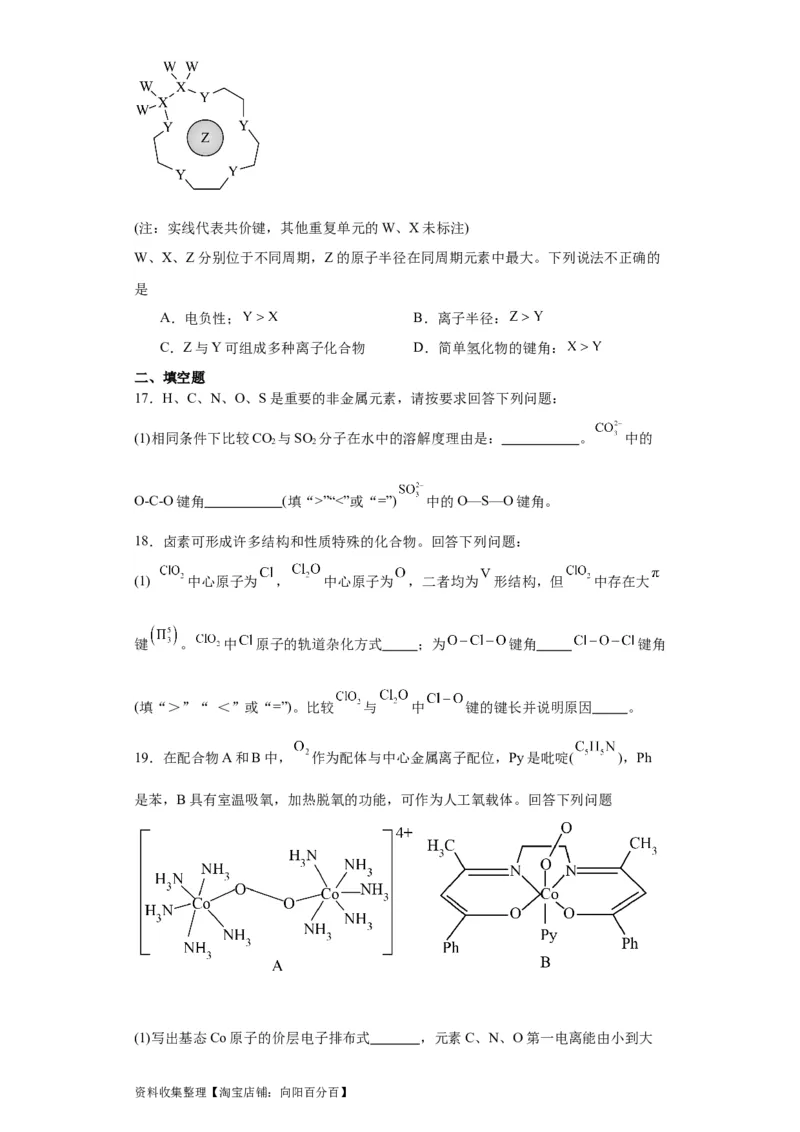
16.科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分
子,具有高效的催化性能,其分子结构示意图如下。
资料收集整理【淘宝店铺:向阳百分百】(注:实线代表共价键,其他重复单元的W、X未标注)
W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。下列说法不正确的
是
A.电负性; B.离子半径:
C.Z与Y可组成多种离子化合物 D.简单氢化物的键角:
二、填空题
17.H、C、N、O、S是重要的非金属元素,请按要求回答下列问题:
(1)相同条件下比较CO 与SO 分子在水中的溶解度理由是: 。 中的
2 2
O-C-O键角 (填“>”“<”或“=”) 中的O—S—O键角。
18.卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1) 中心原子为 , 中心原子为 ,二者均为 形结构,但 中存在大
键 。 中 原子的轨道杂化方式 ;为 键角 键角
(填“>”“ <”或“=”)。比较 与 中 键的键长并说明原因 。
19.在配合物A和B中, 作为配体与中心金属离子配位,Py是吡啶( ),Ph
是苯,B具有室温吸氧,加热脱氧的功能,可作为人工氧载体。回答下列问题
(1)写出基态Co原子的价层电子排布式 ,元素C、N、O第一电离能由小到大
资料收集整理【淘宝店铺:向阳百分百】的顺序为 ,A中O—O键的键长 (填“大于”、“小于”或“等于”)B
中O—O键的键长。
20.载氢体与储氢材料的研究是氢能利用的关键技术。回答以下问题:
(1) PH 和NH 为两种常见的三角锥形气态分子,其键角分别93° 6'和107°,试用价层
3 3
电子对互斥模型分析PH 的键角小于NH 的原因 。NH 的沸点比PH 大但比
3 3 3 3
HO小的原因是: 。
2
21.我国某科研工作者制备了一种高性能的钾离子电池负极材料(Bi-MOF),如图所示。
回答下列问题:
(1) Bi(NO )·5H O中HO的VSEPR模型为 形; 的立体构型为 形,
3 3 2 2
HO的键角 (填“>”、“<”或“=”) 的键角。
2
22.碳元素能形成多种单质,其中石墨和富勒烯( )是两类常见的物质。 以其完
美的球烯受到科学家重视,其结构如下图所示。60个碳原子是等同的,均为近似
杂化,但却有两种不同类型的碳碳键。其中一种为138pm:另一种为145pm。
(1)请在图中标明这2种类型的键的键长 。
(2)石墨中原子和原子之间存在的作用力类型有 。
a.σ键 b.π键 c.极性键 d.非极性键 e.离子键 f.范德华力
(3)石墨、 互为同素异形体,但相同条件下,石墨的熔点比 高得多,原因是
资料收集整理【淘宝店铺:向阳百分百】。
资料收集整理【淘宝店铺:向阳百分百】