文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题03 离子共存、离子检验和推断
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
离子共存、离子检验和推断也是历年高考考查的重要内容。
预计2025年高考对这部分内容的考查,选择题仍主要涉及离子共存、离子的检验与推断三个角度,题
目考查内容主要是元素化合物的性质、化学过程的解释。
因此,在复习时要注意离子不能共存的各种类型,特别是氧化还原、双水解不能共存的情况。离子检
验和推断要考察全面,牢记重要的离子反应、检验方法。
1.(2024·重庆·高考真题)常温下,下列各组离子在指定溶液中能大量共存的是
A.氨水中: B.稀硫酸中:
C. 溶液中: D. 溶液中:
【答案】A
【详解】A.该组离子均与氨水不发生反应,能大量共存,故A正确;
B. 与 反应生成硫酸钡沉淀, 与氢离子反应生成二氧化碳气体,该组离子不能在硫酸中大
量共存,故B错误;
C. 在酸性环境下具有强氧化性,能氧化 ,不能大量共存,故C错误;
D. 中存在 即[Al(OH) ]-离子,能与 发生双水解反应不能大量共存,故D错误;
4
故选:A。
2.(2024·江西·高考真题)白色固体样品X,可能含有AgNO、NH NO 、BaCl 、KCl、NaSO 、
3 4 3 2 2 3
NaCO、Al O 之中的几种或全部。在三个烧杯中各加入适量X。分别加入足量以下三种试剂并微热使之
2 3 2 3
充分反应,实验记录为:
编号 试剂 反应后的不溶物 生成的气体
Ⅰ 蒸馏水 白色 无色、有刺激性气味
Ⅱ 稀盐酸 白色 无色、无味
Ⅲ NaOH溶液 无不溶物 无色、有刺激性气味依据实验现象,下列说法正确的是
A.可能含Al O B.含BaCl C.含NaSO D.不含KCl
2 3 2 2 3
【答案】A
【分析】白色固体样品X,可能含有AgNO、NH NO 、BaCl 、KCl、NaSO 、NaCO、Al O 之中的几种
3 4 3 2 2 3 2 3 2 3
或全部,在三个烧杯中各加入适量X,分别加入足量以下三种试剂并微热使之充分反应,Ⅰ.加入蒸馏
水,微热生成无色有刺激性气味的气体,是微热条件下铵根离子和弱酸根离子发生的双水解反应生成了氨
气和气体,说明一定含NH NO ,反应生成白色沉淀,白色沉淀可能为氧化铝,也可能为AgNO 和
4 3 3
NaSO 、NaCO 反应生成的Ag SO 或Ag CO 沉淀,或BaCl 和NaSO 、NaCO 反应生成的BaSO、
2 3 2 3 2 3 2 3 2 2 3 2 3 3
BaCO 沉淀,Ⅱ.加入稀盐酸反应后的不溶物为白色沉淀,同时生成的气体为无色无味气体,为二氧化碳
3
气体,说明一定含NaCO,一定不含NaSO ,白色沉淀可能为AgNO 生成的AgCl,可能含AgNO、
2 3 2 3 3 3
BaCl ,可能存在Al O;Ⅲ.加入NaOH溶液,无沉淀,有无色刺激性气味的气体生成,说明一定含
2 2 3
NH NO ,可能含AgNO、BaCl 、KCl、NaSO 、NaCO、Al O,据此分析判断。
4 3 3 2 2 3 2 3 2 3
A.分析可知,可能含Al O,故A正确;
2 3
B.分析可知,固体中可能含BaCl ,故B错误;
2
C.加入盐酸生成气体为无色无味,说明不含NaSO ,故C错误;
2 3
D.上述过程中的分析可知,KCl的存在不能确定,故D错误;
故选A。
3.(2024·宁夏四川·高考真题)四瓶无色溶液 ,它们之间的反应关系
如图所示。其中a、b、c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列叙述正确的是
A.a呈弱碱性
B.f可溶于过量的b中
C.c中通入过量的e可得到无色溶液
D.b和d反应生成的沉淀不溶于稀硝酸
【答案】B
【分析】由题意及关系图可知,a与b反应需要加热,且产生的e为无色气体,则a和b分别为 和
的一种,产生的气体e为 ;又由于b和c反应生成白色沉淀f, 不会与其他三种溶液
产生沉淀,故b为 ,a为 ;又由于c既能与b产生沉淀f,又能与d反应产生沉淀f,故c为,d为 ,生成的白色沉淀为 ,无色气体g为 。综上所述,a为 溶液,b为
溶液,c为 溶液,d为 溶液,e为 ,f为 ,g为 。
A.由分析可知,a为 溶液,为强酸弱碱盐的溶液, 水解显酸性,故a显弱酸性,A项错误
B.由分析可知,f为 ,b为 溶液, 为两性氢氧化物,可溶液强碱,故f可溶于过
量的b中,B项正确;
C.由分析可知,c为 溶液,e为 , 溶液通入 会生成 沉淀, 不溶于弱
碱,继续通入 不能得到无色溶液,C项错误;
D.由分析可知,b为 ,d为 ,二者反应生成 沉淀,可溶与稀硝酸,D项错误;
故选B。
4.(2024·浙江·高考真题)在溶液中能大量共存的离子组是
A. B.
C. D.
【答案】D
【详解】A. 三种离子会反生氧化还原反应而不能大量共存,故A不符合题意;
B. 会生成 离子而不能大量共存,故B不符合题意;
C. 会生成 沉淀而不能大量共存,故C不符合题意;
D. 虽然不同程度水解,但水解是微弱的,能大量共存,故D符合题意;
答案D。
5.(2022·天津·高考真题)25℃时,下列各组离子中可以在水溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】D
【详解】A. 与 反应生成次氯酸而不能大量共存,故A不符合题意;
B. 、 、 发生氧化还原反应而不能大量共存,故B不符合题意;
C. 与 反应生成氢氧化铝沉淀和二氧化碳气体而不能大量共存,故C不符合题意;D. 、 、 、 是大量共存,故D符合题意。
综上所述,答案为D。
6.(2022·重庆·高考真题)下列操作中,不会影响溶液中K+、Al3+、Fe3+、Ba2+、Cl-、NO 等离子大量共
存的是
A.加入ZnSO B.加入Fe粉 C.通入NH D.通入CO
4 3 2
【答案】D
【详解】A.向溶液中加入硫酸锌溶液,硫酸根离子会与溶液中的钡离子反应,会影响溶液中离子的大量
共存,故A不符合题意;
B.向溶液中加入铁粉,铁离子会与铁反应生成亚铁离子,会影响溶液中离子的大量共存,故B不符合题
意;
C.向溶液中通入氨气,铝离子、铁离子会与氨水反应生成氢氧化铝、氢氧化铁沉淀,会影响溶液中离子
的大量共存,故C不符合题意;
D.向溶液中通入二氧化碳,二氧化碳与溶液中离子不发生任何反应,不会影响溶液中离子的大量共存,
故D符合题意;
故选D。
7.(2022·湖北·高考真题)下列各组离子在给定溶液中能大量共存的是
A.在 氨水中:
B.在 氯化钠溶液中:
C.在 醋酸溶液中:
D.在 硝酸银溶液中:
【答案】C
【详解】A.氨水显碱性,会与 反应,不能大量共存,A项错误;
B. 会发生氧化还原反应,不能大量共存,B项错误;
C.醋酸显酸性,在醋酸溶液中 均不会发生反应,能大量共存,C项正确;
D.硝酸银中的银离子会与氯离子反应生成沉淀,不能大量共存,D项错误;
答案选C。
8.(2022·全国·高考真题)某白色粉末样品,可能含有 、 、 和 。取少量
样品进行如下实验:
①溶于水,得到无色透明溶液②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。
该样品中确定存在的是
A. B.
C. D.
【答案】A
【详解】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向
①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在NaSO,发生反应SO
2 2 3 2
+2H+=S↓+H O+SO ↑,离心分离,③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为
2 2 2
BaSO,说明固体中存在NaSO ,不能确定是否有NaSO 和NaCO,NaSO 与过量盐酸反应生成二氧化
4 2 4 2 3 2 3 2 3
硫,NaCO 与过量盐酸反应生成二氧化碳,而这些现象可以被NaSO 与过量盐酸反应的现象覆盖掉,综
2 3 2 2 3
上分析,该样品中确定存在的是:NaSO 、NaSO,
2 4 2 2 3
答案选A。
9.(2023·辽宁·高考真题)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别NaCO 与NaHCO
2 3 3
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的BaCl 溶液检验NaSO 是否被氧化
2 2 3
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
【答案】A
【详解】A.石灰水的主要成分为Ca(OH) 能与碳酸钠和碳酸氢钠反应生成碳酸钙,二者均生成白色沉
2
淀,不能达到鉴别的目的,A错误;
B.Fe2+变质后会生成Fe3+,可以利用KSCN溶液鉴别,现象为溶液变成血红色,可以达到检验的目的,B
正确;
C.NaSO 被氧化后会变成NaSO ,加入盐酸酸化的BaCl 后可以产生白色沉淀,可以用来检验NaSO 是
2 3 2 4 2 2 3
否被氧化,C正确;
D.含有醛基的物质可以与银氨溶液反应生成银单质,可以用来检验乙醇中混有的乙醛,D正确;
故答案选A。
10.(2021·海南·高考真题)一次性鉴别等浓度的 、 、 三种溶液,下列方法不可行的
是
A.测定 B.焰色试验C.滴加 溶液 D.滴加饱和 溶液,微热
【答案】C
【详解】A. 溶液显中性, 溶液显酸性, 溶液显碱性,故可以用测定pH的方法鉴
别,故A正确;
B. 的焰色试验中现象为透过蓝色钴玻璃为紫色, 的焰色试验中无现象, 的焰色试验
中现象为黄色,故可以用焰色试验的方法鉴别,故B正确;
C. 、 、 中只有 能与 反应有现象,故 和 不能鉴别,故C错
误;
D.2 + CaCl2+2NH +2H O有刺激性气味气体产生, + =CaCO +2NaOH
3 2 3
有白色沉淀产生,而 不反应无现象,故可以鉴别,故D正确;
故选C。
【策略1】两个方面突破离子共存问题
1.判断离子能否大量共存的“四个要点”:一色、二性、三特殊、四反应。
(1)一色——溶液颜色
离子 Cu2+ Fe3+ Fe2+ MnO Cr O2- CrO2- Cr3+
2 7 4
溶液颜色 蓝色 棕黄色 浅绿色 紫红色 橙红色 黄色 绿色
(2)二性——溶液的酸碱性
①在强酸性溶液中,OH-及弱酸根阴离子(如CO、ClO-、SO、S2-、CHCOO-等)不能大量存在。
3
②在强碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Cu2+、Mg2+、Zn2+、Fe3+等)不能大量存在。
③如HCO、HS-、HSO、HPO、HPO等,在强酸性或强碱性溶液中均不能大量存在。
2
(3)三特殊——三种特殊情况:
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不能
大量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的水
3
解程度仍很小,它们在溶液中仍能大量共存。
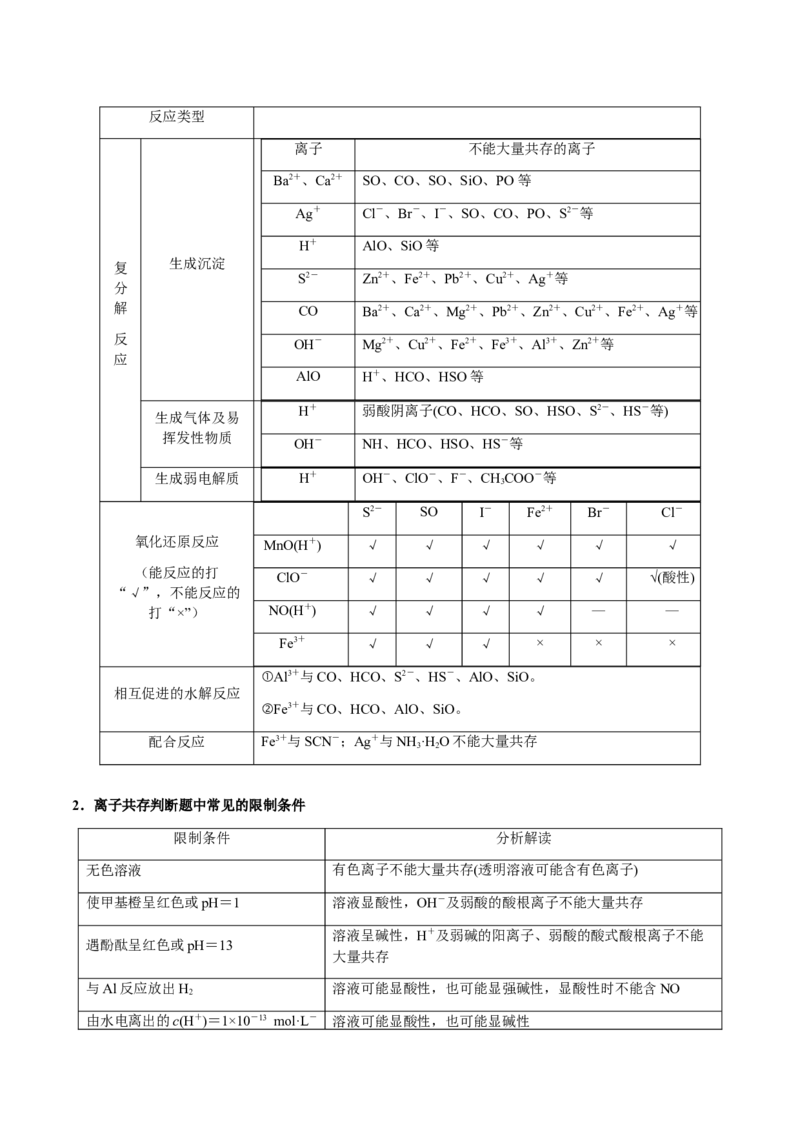
(4)四反应——四种反应类型反应类型
离子 不能大量共存的离子
Ba2+、Ca2+ SO、CO、SO、SiO、PO等
Ag+ Cl-、Br-、I-、SO、CO、PO、S2-等
H+ AlO、SiO等
生成沉淀
复
S2- Zn2+、Fe2+、Pb2+、Cu2+、Ag+等
分
解 CO Ba2+、Ca2+、Mg2+、Pb2+、Zn2+、Cu2+、Fe2+、Ag+等
反 OH- Mg2+、Cu2+、Fe2+、Fe3+、Al3+、Zn2+等
应
AlO H+、HCO、HSO等
H+ 弱酸阴离子(CO、HCO、SO、HSO、S2-、HS-等)
生成气体及易
挥发性物质
OH- NH、HCO、HSO、HS-等
生成弱电解质 H+ OH-、ClO-、F-、CHCOO-等
3
S2- SO I- Fe2+ Br- Cl-
氧化还原反应 MnO(H+) √ √ √ √ √ √
(能反应的打 ClO- √ √ √ √ √ √(酸性)
“√”,不能反应的
打“×”) NO(H+) √ √ √ √ — —
Fe3+ √ √ √ × × ×
①Al3+与CO、HCO、S2-、HS-、AlO、SiO。
相互促进的水解反应
②Fe3+与CO、HCO、AlO、SiO。
配合反应 Fe3+与SCN-;Ag+与NH ·H O不能大量共存
3 2
2.离子共存判断题中常见的限制条件
限制条件 分析解读
无色溶液 有色离子不能大量共存(透明溶液可能含有色离子)
使甲基橙呈红色或pH=1 溶液显酸性,OH-及弱酸的酸根离子不能大量共存
溶液呈碱性,H+及弱碱的阳离子、弱酸的酸式酸根离子不能
遇酚酞呈红色或pH=13
大量共存
与Al反应放出H 溶液可能显酸性,也可能显强碱性,显酸性时不能含NO
2
由水电离出的c(H+)=1×10-13 mol·L- 溶液可能显酸性,也可能显碱性1
通入足量的CO(或NH ) 溶液呈酸性(或碱性)
2 3
因发生氧化还原反应而不能大量共存 能发生氧化还原反应的氧化性离子和还原性离子不能大量共存
“一定”“可能”还是“不能”大量
确定是“可能性”还是“肯定性”
共存
说明该溶液呈酸性[稀释的是溶质,溶质c(H+)减小,而c(OH
加水稀释,减小
-)增大]
某溶液的lg =12 该溶液呈酸性
【策略2】牢记常见离子检验的特征反应及注意事项
(1)常见阳离子的检验
【易错提醒】阳离子检验的注意事项
NaOH溶液可以同时鉴别出若干种阳离子,包括Al3+、Fe3+、Fe2+、Cu2+、NH、Mg2+等多种离子,在阳
离子鉴别中,NaOH溶液是一种应用较广的试剂。若先使用NaOH溶液(必要时可加热)检验出几种离子,
再用其他方法鉴别用NaOH溶液鉴别不出来的离子,整个问题可以较快解决。
(2)常见阴离子的检验【易错提醒】阴离子检验的注意事项
①AgNO 溶液与稀硝酸、BaCl 溶液与稀盐酸这两组试剂,可以鉴别出若干种阴离子,是阴离子鉴别最
3 2
常用的试剂组合。一般说来,若待检的若干种离子中有SO,最好先用BaCl 溶液和盐酸这组试剂,检出包
2
括SO在内的一些离子,其他离子再用AgNO 溶液与稀硝酸等去鉴别。
3
②为了检验某盐中含SO或CO,可以直接加酸(非氧化性酸,如盐酸),根据放出气体的气味等特征现
象判断气体是CO 或SO ,进而确定物质中含CO或SO。
2 2
③灵活运用阴离子检验的知识,有时可以解决某些阳离子的鉴别问题。例如,在一定条件下,可考虑
用卤素离子(如Cl-)检出Ag+,用SO检出Ba2+。
【策略3】坚持“四项基本原则”突破离子推断
1.离子推断的“四项基本原则”
(1)肯定原则:根据实验现象推出溶液中肯定存在或肯定不存在的离子(记住几种常见的有色离子:Fe2
+、Fe3+、Cu2+、MnO、CrO、Cr O)。
2
(2)互斥原则:在肯定某些离子存在的同时,结合离子共存规律,否定一些离子的存在(注意题目中的隐
含条件,如酸性、碱性、指示剂的颜色变化、与铝反应产生H、水的电离情况等)。
2
(3)电中性原则:溶液呈电中性,溶液中有阳离子,必有阴离子,且溶液中阳离子所带正电荷总数与阴
离子所带负电荷总数相等(这一原则可帮助我们确定一些隐含的离子)。
(4)进出原则:通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验
的干扰。
2.电荷守恒在定量型离子推断试题中的应用
离子定量推断试题常根据离子的物质的量(或浓度)定量推断最后一种离子的存在:如果多种离子共
存,且只有一种离子的物质的量未知,可以用电荷守恒来确定最后一种离子是否存在,即阳离子所带的正
电荷总数等于阴离子所带的负电荷总数。1.(2025高三上·辽宁·模拟预测)下列有关实验的叙述正确的是
A.配制 溶液,用托盘天平称取 固体
B.向某溶液中加入 溶液,有白色沉淀生成,说明原溶液中一定含有
C.把红热的木炭加入浓硝酸中,有红棕色气体生成,该现象能证明碳与浓硝酸发生了反应
D.将足量的 通入 溶液中充分反应,取反应后溶液,滴加酸性 溶液,
溶液紫色褪去,证明反应生成了
【答案】A
【详解】A.实验室没有 规格的容量瓶,应该选择 容量瓶,根据计算,用托盘天平称取
的质量为 ,故A正确;
B.能与 沉淀的阴离子有很多,如 、 等,不一定是 ,故B错误;
C.把红热的木炭加入浓硝酸中,有红棕色气体生成,该现象不能证明碳与浓硝酸发生了反应,浓硝酸受
热本身会分解产生二氧化氮气体,故C错误;
D.二氧化硫可以与 反应生成 ,但二氧化硫足量,反应后的混合溶液会有二氧化硫残留,同时溶
液中存在Cl-,此时滴加酸性 溶液,溶液紫色褪去并不能确切证明反应生成了 ,也可能是残留
的二氧化硫或Cl-使溶液褪色,故D错误。
综上所述,答案为A。
2.(2024·广东深圳·一模)将下列离子: 、 、 、 、 、 、 、 、 、
、 、 按可能大量共存的情况,把它们全部分成 、 两组,而且每组中都含有不少于两种阳
离子和两种阴离子。下列离子不会同在一组的是
A. 、 B. 、 C. 、 D. 、
【答案】A
【分析】由给出的离子可知,将能与 共存的分为一组,能与 共存的分为一组,结合离子之间的反
应分为两组,且每组中都含有不少于两种阳离子和两种阴离子,据此分析回答问题;
、 在溶液中不能大量共存,据此可以分为两组:能与 共存的分为一组,为A组,能与 共存
的分为一组,为B组; 、 、 能够与 离子反应,只能与 离子一组;总共有6种阳离
子,A组中已经含有4种,则剩余的2种阳离子 、 只能与 一组; 、 能够与 反应,
只能与 分在一组;因此A组的离子为: ;B组的离子为:
;
剩余的阴离子为: ,由于 组中 具有氧化性,能够氧化 ,所以 只能存在于组, 只能存在于 组;A组有四种阳离子和两种阴离子,分别为:
;B组有四种阴离子和两种阳离子,分别为:
因此 不会同在一组;
故答案为: 。
3.(2025高三上·福建·模拟预测)某白色固体混合物由 中的两种组成,进行
如下实验:
①混合物溶于水,得到澄清透明溶液;
②做焰色试验,透过蓝色钴玻璃可观察到火焰的颜色呈紫色;
③向溶液中加碱溶液,产生白色沉淀。
根据实验现象可判断其组成为
A. B.
C. D.
【答案】C
【详解】根据实验①混合物溶于水,得到澄清透明溶液,而BaCO 难溶于水,即白色固体中一定不含
3
BaCO ;
3
根据实验②做焰色反应时焰色呈紫色(透过蓝色钴玻璃)可确定含有钾元素,即白色固体中含有KCl;
结合实验③向溶液中加碱产生白色沉淀,可知溶液中含有能与OH-反应生成白色沉淀的离子,只能为
Mg2+,即白色固体的另一成分为MgSO ;
4
故本题选C。
4.(2025高三上·湖北·模拟预测)某溶液中只可能含有 、 、 、 、 、 、 、
中的若干种离子,离子浓度均为 。某同学进行了如下实验,下列说法正确的是
A.原溶液中存在 、 、 、
B.原溶液中含有 、不含
C.沉淀 中含有
D.滤液 中大量存在的阳离子有 、 和【答案】A
【分析】试液中只可能含有 、 、 、 、 、 、 、 中的若干种离子,
加入过量稀 HSO 无明显现象,说明该试液中没有 ;再加入过量 Ba(NO ) 溶液有气体产生,因为此
2 4 3 2
时溶液中含有上一步操作所加入的过量 HSO ,结合 离子在酸性条件下具有强氧化性,生成的气体
2 4
为NO,说明原试液中有 Fe2+ 离子存在且被氧化为 Fe3+, 和 会发生反应,不能共存,则溶
液中一定不存在 ,沉淀 A 为 BaSO;向滤液 X 中加入过量的 NaOH 有气体产生,说明原
4
试液中存在 离子,此时产生的气体为 NH ,沉淀 B 为红褐色的 Fe(OH) 沉淀;继续向滤液中通入
3 3
少量 CO 产生沉淀,由于上一步所加 NaOH 有剩余,则所通入少量的 CO 先与 OH− 反应生成 ,
2 2
再与 Ba2+ 反应生成 BaCO ,则沉淀 C 中含有 BaCO ,综上分析可知,原试液中一定存在 、
3 3
Fe2+,一定不存在 、 ,由于存在的离子浓度均为 0.1 mol⋅L−1,根据电荷守恒可知原试液
中一定还存在阴离子 、Cl−,且浓度均为 0.1 mol⋅L−1 的 、Fe2+、Cl−、 恰好满足电荷守
恒,则原试液中 Al3+、K+ 必然不能存在。
A.由分析可知,原溶液中存在 、 、 、 ,A正确;
B.由分析可知,原溶液中不存在 、 ,B错误;
C.由分析可知,沉淀 中含有BaCO ,C错误;
3
D.由分析可知,滤液 中大量存在的阳离子有 、 和 ,D错误;
故选A。
5.(2025高三上·宁夏·模拟预测)某无色溶液可能含有等物质的量的下列某些离子: 、 、 、
、 、 、 ,取溶液分别进行如下实验:①加入 酸化的 溶液产生白色沉淀;
②加入锌粉,有气泡生成;③加入适量 粉末产生白色沉淀。下列说法正确的是
A.由①、②可知该无色溶液中一定有 、 ,可能有
B.该无色溶液中可能有
C.该无色溶液中一定有 、 、 和
D.实验③发生反应的离子方程式只有:
【答案】C
【分析】由于含有 的溶液为黄色,该题干的条件为无色溶液,因此不能存在 ;
①加入 酸化的 溶液产生白色沉淀,可知该沉淀为BaSO,不可能是BaCO ,是由于BaCO
4 3 3会与硝酸反应产生二氧化碳,说明该溶液中含有 ;
②加入锌粉,有气泡生成,说明溶液中含有 ,产生的是氢气,不含 ;
③加入适量 , 与HO反应产生氢氧化钠,NaOH与Mg2+反应产生Mg(OH) 是白色沉淀,说明
2 2
溶液中含有 ;
根据上述可知,溶液中一定含有的离子有: 、 、 ,由于离子的数目相等,即物质的量相等,
溶液为电中性,因此还存在有阴离子,即还存在有 ,综合可知,该无色溶液中一定有 、 、
和 ,一定不存在的离子是: 、 、 ,据此作答。
A.根据上述分析可知,该无色溶液中不含 ,A错误;
B.根据上述分析可知,该无色溶液中一定没有 、 ,B错误;
C.根据上述分析可知,该无色溶液中一定有 、 、 和 ,C正确;
D.实验③加入适量 ,根据分析可知,溶液中存在有 ,也会与氧化钠反应,发生的反应为:
NaO+2H+=2Na++H O,,D错误;
2 2
故选C。
6.(2025高三上·黑龙江哈尔滨·模拟预测)常温下,在下列给定条件的各溶液中,一定能大量共存的离子
组是
A.电解 溶液后的溶液中: 、 、 、
B.使甲基橙呈红色的溶液中: 、 、 、
C.澄清透明溶液中: 、 、 、
D.由水电离产生的 的溶液: 、 、 、
【答案】C
【详解】A.电解 溶液生成单质铜、硫酸和氧气, 与 不能大量共存,A错误;
B.使甲基橙呈红色的溶液显酸性, 与 不能大量共存,B错误;
C.澄清透明溶液中, 、 、 、 互相不反应,可以大量共存,C正确;
D.由水电离产生的 的溶液抑制水的电离,该溶液为酸溶液或碱溶液, 与
不能大量共存,D错误;
故选C。7.(2025高三上·福建泉州·模拟预测)常温下,下列各组粒子在指定溶液中一定能大量共存的是
A.澄清透明溶液:
B.由水电离出 为 的溶液:
C.使甲基橙变红色的溶液:
D.通入足量 的溶液:
【答案】A
【详解】A.该溶液因含MnO 而显紫红色但澄清透明,且 相互间不发生反应,能
大量共存,A符合题意;
B.常温下,由水电离产生的 的溶液,可能是酸性,也可能是碱性,酸性条件下 、
反应生成SO 气体和S沉淀,且酸性条件下 可以氧化 ,不能共存,碱性条件下铵根离子不
2
能大量存在,B不符合题意;
C.使甲基橙变红色的溶液显酸性, 酸性条件下不能存在, 酸性条件下生成硅酸,不能大
量共存,C不符合题意;
D.通入足量NH 的溶液显碱性,Cu2+能结合氨分子生成 ,故不能大量存在,D不符合题
3
意;
故选A。
8.(2025高三上·浙江·模拟预测)下列说法正确的是
A.能使酚酞变红的溶液中可大量存在 、 、 、
B.由水电离的 的溶液中能大量存在 、 、 、
C. 溶液中不能大量共存 、 、 、
D.某卤代烃中滴加 的乙醇溶液后加热,滴入稀硝酸酸化后再滴入几滴 溶液无白色沉
淀,则该卤代烃中不含
【答案】C
【详解】A.使酚酞变红的溶液呈碱性, 、 、 与氢氧根不能大量共存,A错误;
B.水电离的 的溶液为强酸或强碱, 在酸性溶液中不能共存,
与氢氧根反应生成氢氧化钙微溶于水,不能大量共存,B错误;C. 溶液与 、 发生氧化还原反应不能大量共存,C正确;
D. 的乙醇溶液是卤代烃消去反应的条件,如果卤代烃卤原子相连C的相邻C上没有H,不能发生
消去反应,故滴入稀硝酸酸化后再滴入几滴 溶液无白色沉淀不能确定该卤代烃是否含 ,D错
误;
答案选C。
9.(2024·辽宁沈阳·模拟预测)某无色溶液Y可能含有
中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,
忽略 的分解)。下列说法不正确的是
A.溶液Y中一定不存在
B.溶液Y中一定含有 ,且
C.溶液Y中肯定存在
D.溶液Y中可能存在 ,为确定其是否存在,可取溶液1通过焰色试验验证
【答案】B
【分析】无色溶液Y中一定不存在Fe3+。Y和足量的双氧水、盐酸酸化,反应生成气体1、说明溶液中存
在HCO ,根据C元素守恒可知n(HCO )=n(CO)= =0.01 mol;同时得到溶液1和沉淀,沉淀一
2
定是BaSO,则溶液中一定含有Ba2+,一定不存在SO ,一定存在HSO ,HSO 被双氧水氧化生成SO
4
,进而生成BaSO,根据元素守恒可知n(Ba2+)=n(HSO )=n(BaSO)= =0.01 mol。向溶液1中加入
4 4
氢氧化钡生成气体和溶液2,则气体一定是NH ,因此一定含有NH ,其物质的量为n(NH )=n(NH )=
3 3
=0.01 mol,溶液中存在电荷守恒,根据电荷守恒可知溶液中还一定存在Cl-,可能含有Na+。
A.无色溶液Y中一定不存在Fe3+,由于含有Ba2+,Ba2+与SO 会反应产生沉淀,所以溶液Y中一定不存
在SO ,A正确;
B.由分析可知,溶液Y中一定含有Ba2+、 、 、 、Cl-,可能含有Na+,且Ba2+、 、、 的物质的量都为0.01mol,由于溶液中阳离子浓度相同,并根据电荷守恒可知,若溶液Y中
含有Na+,n(Na+)=0.01mol,n(Cl-)=0.02mol,若溶液Y不含Na+,n(Cl-)=0.01mol,B错误;
C.根据上述分析可知溶液Y中肯定存在HCO 、HSO 、Ba2+、NH ,C正确;
D.由分析可知,溶液Y中可能存在Na+,为确定其是否存在,可取溶液1通过焰色试验验证,若溶液1的
焰色呈黄色,则说明溶液Y含有Na+,D正确;
故选B。
10.(2024·安徽·一模)常温下,下列各组离子在指定溶液中能大量共存的是
A.与铝反应产生 的溶液中: 、 、 、
B.新制氯水中: 、 、 、
C.使酚酞变红的溶液中: 、 、 、
D.加入 固体的溶液中: 、 、 、
【答案】C
【详解】A.与铝反应产生H 的溶液为强酸性或强碱性溶液, 在强酸性或强碱性环境中都不能共
2
存,A错误;
B.新制氯水中氯离子和 生成AgCl沉淀,不能大量共存,B错误;
C.使酚酞变红的溶液为碱性, 、 、 、 在碱性溶液中不发生发生,能大量共存,C正确;
D. 和水反应生成NaOH,加入 固体的溶液呈碱性, 不能大量共存,D错误;
故选C。
11.(2024·四川德阳·一模) (铁铵矾)是分析化学中的重要试剂。下列有关1mol·L-1
溶液的叙述正确的是
A.该溶液中, 、 和 可以大量共存
B.该溶液与0.5mol·L-1 溶液相比,
C.可分别用NaOH浓溶液、KSCN溶液检验该溶液中的 和
D.向该溶液滴入 溶液恰好使 完全沉淀的离子方程式为:
【答案】C【详解】A. 含有 ,与 发生氧化还原反应不能共存, ,A错
误;
B.二者铵根浓度均为 ,铵根水解方程式为: , 中还存在
的水解,也水解产生氢离子,促使其溶液中的铵根水解逆向移动,导致 中的铵根浓度大
于 的铵根浓度,B错误;
C. 中的铵根可以和 浓溶液反应生成氨气,同时 可以和 反应生成血红色
,C正确;
D.向 溶液滴入氢氧化钡溶液恰好使硫酸根完全沉淀,铵根离子和铁离子也恰好反应,反应
的离子方程式为: ,D错误;
故选C。
12.(2024·全国·模拟预测)常温下,下列各组离子在指定溶液中能够大量共存的是
A.氨水中: 、 、 、 B.HClO溶液中: 、 、 、
C. 溶液中: 、 、 、 D. 溶液中: 、 、 、
【答案】B
【详解】A. 和氨水易反应生成 ,同时 和 易反应生成微溶物 ,A不符
合题意;
B.酸性 ,所以HClO和 不发生反应,且其他离子间也不发生反应,B符合题
意;
C. 会催化 分解,同时 、 均易与 反应生成对应沉淀,C不符合题意;
D. 和 易反应生成 或 , 与 易发生双水解反应生成沉淀, 与 也可
发生双水解反应或复分解反应生成沉淀,D不符合题意;
选B。
13.(2024·江苏南京·模拟预测)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:Fe3+、Mg2+、 、Cl-
B. =106的溶液中: 、K+、 、
C.碱性溶液中:ClO-、S2-、 、Na+D.与Al反应能放出H 的溶液中:Fe2+、K+、 、
2
【答案】A
【详解】A.澄清透明的溶液中,Fe3+、Mg2+、S 、Cl-四种离子之间不发生任何反应,能大量共存,A正
确;
B. =106的溶液显碱性, 在碱性溶液中不能大量存在,B错误;
C.ClO-具有氧化性,与具有还原性的离子S2-、 可发生氧化还原反应,不能大量共存,C错误;
D.与Al反应能放出H 的溶液可能呈酸性也可能呈碱性,在酸性溶液中,Fe2+、 和H+发生氧化还原反
2
应,在碱性溶液中,Fe2+与OH-发生反应生成沉淀,不能大量共存,D错误;
故选A。
14.(2025·四川·一模)常温常压下,下列指定条件的各组离子一定能大量共存的是
A.透明的溶液中: 、 、 、
B.在酒精中: 、 、 、
C.溶有 的水溶液中: 、 、 、
D.由水电离出 为 的溶液中: 、 、 、
【答案】C
【详解】A. 、 、 能发生氧化还原反应,不能大量共存,故A错误;
B.酒精具有还原性,能被 氧化,不能大量共存,故B错误;
C.该组离子均不与 反应,可以大量共存,故C正确;
D.水电离出 为 ,水的电离被抑制,溶液可能为酸溶液,也可能为碱溶液,若为碱
溶液则 不能大量共存,故D错误;
故选:C。
15.(2025·宁夏陕西·模拟预测)下列名组离子在水溶液中可以大量共存的是
A. B.
C. D.
【答案】B【详解】A. 反应生成硫单质和二氧化硫,不能大量共存,A错误;
B. 互不反应,可以大量共存,B正确;
C. 会生成溴化银沉淀,不能大量共存,C错误;
D. 在 大量存在的溶液中会生成氢氧化铁沉淀,不能大量共存,D错误;
故选B。
16.(2025高一上·湖南怀化·模拟预测)某无色溶液可能含有等物质的量的下列某些离子中的一种或几
种: 、 、 、 、 、 、 ,取溶液分别进行如下实验:
①加入 酸化的 溶液产生白色沉淀;
②加入锌粉,有气泡生成;
③加入适量 粉末产生白色沉淀。
下列说法正确的是
A.该无色溶液中一定没有 ,可能有
B.由①、②可知该溶液可能有
C.该无色溶液中一定有 、 、 和
D.实验③发生反应的离子方程式只有:
【答案】C
【分析】由于含有 的溶液为黄色,该题干的条件为无色溶液,因此不能存在 ;
①加入 酸化的 溶液产生白色沉淀,可知该沉淀为BaSO,不可能是BaCO ,是由于BaCO
4 3 3
会与硝酸反应产生二氧化碳,说明该溶液中含有 ;
②加入锌粉,有气泡生成,说明溶液中含有 ,产生的是氢气,不含 ;
③加入适量 ,NaO与HO反应产生氢氧化钠,NaOH与Mg2+反应产生Mg(OH) 是白色沉淀,说明溶
2 2 2
液中含有 ;
根据上述可知,溶液中一定含有的离子有: 、 、 ,由于离子的数目相等,即物质的量相等,
溶液为电中性,因此还存在有阴离子,即还存在有 ,综合可知,该无色溶液中一定有 、 、
和 ,一定不存在的离子是: 、 、 ,据此作答。
A.根据上述分析可知,该无色溶液中一定没有 、 ,A错误;B.根据上述分析可知,由①、②可知该无色溶液中一定有 、 ,一定没有 ,B错误;
C.根据上述分析可知,该无色溶液中一定有 、 、 和 ,C正确;
D.实验③加入适量 ,根据分析可知,溶液中存在有 ,也会与氧化钠反应,发生的反应为:
NaO+2H+=2Na++H O,D错误;
2 2
答案选C。
17.(2025高三上·天津·模拟预测)某无色溶液中可能含有 、 、 、 ,加入铝粉后,只产
生 ,探究该无色溶液中离子大量共存情况。
(1)加入铝粉产生 ,说明铝具有 (填“氧化性”或“还原性”)。
(2)某同学分析:若 大量存在,则 就不能大量存在。设计实验如下:
i.实验初始,未见明显现象
ii.过一会儿,出现气泡,液面上方呈浅棕色
iii.试管变热,溶液沸腾
①盐酸溶解 薄膜的离子方程式是: 。
②根据现象ii,推测溶液中产生了NO,为进一步确认,进行实验:
实验1 将湿润KI-淀粉试纸置于空气中 未变蓝
实验2 用湿润KI-淀粉试纸检验浅棕色气体试纸 变蓝
a.浅棕色气体是 (化学式)
写出生成浅棕色气体的化学方程式 。
b.实验1的目的是 。
(3)再假设:若 大量存在, 也可能不能大量存在。重新设计实验:
i.实验初始,未见明显现象
ii.过一会儿,出现气泡,有刺激性气味
对“刺激性气味”气体,进行如下实验:用湿润KI-淀粉试纸检验,未变蓝;用蘸有浓盐酸的玻璃棒接近
该气体出现白烟。该气体是 (化学式);产生该气体的离子方程式 。
(4)实验结果证实: 有一定的氧化性,能氧化铝单质,产生含氮化合物(填序号)。a.只在酸性环境中 b.只在碱性环境中 c.在酸性或碱性环境中均
结论:该无色溶液一定能大量存在的是 (离子符号)。
【答案】
(1)还原性
(2) 对比实验,排除氧气使湿润的KI-淀
粉试纸变蓝的可能
(3)
(4)c 、
【分析】无色溶液中可能含有“ 、 、 、 ,”,加入铝粉后,只产生氢气,因为硝酸有氧
化性,则无色溶液中应为氢氧化钠溶液。
(1)加入铝粉产生氢气,铝失去电子,具有还原性。
(2)①氧化铝和盐酸反应生成氯化铝和水,离子方程式为:6H+ + Al O = 2Al3+ + 3H O;
2 3 2
② 液面上显示浅棕色,一定不是氢气,为氮的氧化物,将湿润的碘化钾淀粉试纸置于空气中未变蓝,说
明碘化钾在空气中不能被氧化,而用湿润的碘化钾淀粉试纸检验浅棕色气体试纸变蓝,则碘化钾被氧化,
即二氧化氮与水反应生成硝酸,再氧化碘离子生成碘单质。
a.浅棕色的气体为NO ;NO与空气中的氧气反应生成NO ,化学方程式为: ;
2 2
b.实验1的目的是对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能。
(3)用湿润的碘化钾淀粉试纸检验,未变蓝,用蘸有浓盐酸的玻璃棒接近该气体出现白烟,则该气体为
NH ;由上述分析可知,碱性条件下铝和硝酸根离子发生氧化还原反应生成氨气,离子方程式为:
3
。
(4)经过实验证实硝酸根在酸性或碱性条件下都可以氧化铝,故选c;生成氮的化合物,但是产物中没有
氮的化合物,所以该无色溶液中含有的离子为Na+、OH- 。
18.(2025高三上·辽宁·模拟预测)某强酸性稀溶液中可能存在
中的若干种,现取适量该溶液进行如下实验:
(1)由强酸性条件即可判断原溶液中一定不存在的离子有 。
(2)写出生成气体A的离子方程式 。(3)写出气体A和气体B在催化剂、加热条件下反应生成无毒物质的化学方程式: 。
(4)沉淀A的化学式是 ,沉淀B的颜色是 。
(5)沉淀C中一定有 (填化学式,下同),可能有 。
(6)通过以上分析知,原溶液中一定含有的离子有 。
【答案】
(1) 、
(2)3Fe2++4H++ =3Fe3++NO↑+2HO
2
(3)6NO+4NH 5N+6HO
3 2 2
(4)BaSO 红褐色
4
(5)BaCO Al(OH)
3 3
(6)Fe2+、 、H+、
【分析】强酸性溶液中一定不存在CO 、SiO 。溶液中加入过量硝酸钡溶液有气体A生成,证明一定含
有Fe2+,则原溶液中一定不存在NO ,气体A为NO,同时有沉淀A生成,说明原溶液一定存在 ,一
定不存在Ba2+,沉淀A为BaSO。溶液A中加入过量氢氧化钠溶液、加热,有气体B生成,原溶液中含有
4
,气体B为NH ,沉淀B为Fe (OH) ,由于溶液B中含有过量的硝酸钡、氢氧化钠,溶液B中通入少
3 3
量二氧化碳,生成的沉淀一定含有BaCO ,可能含有沉淀Al (OH) ,综上分析,原溶液中一定有Fe2+、
3 3
、H+、 ,一定没有Ba2+、CO 、 ,不能确定是否含有Al3+、Cl﹣。
(1)由强酸性条件即可判断原溶液中一定不存在的离子有:CO 、SiO ,因为会生成二氧化碳气体、硅
酸沉淀;
(2)溶液中加入过量硝酸钡溶液有气体A生成,证明一定含有Fe2+,气体A为NO,生成气体A的离子方
程式:3Fe2++4H++NO =3Fe3++NO↑+2HO;
2
(3)由分析可知,气体A为NO,气体B为NH ,在催化剂、加热条件下反应生成无毒物质,即反应生成
3
氮气与水,反应化学方程式为:6NO+4NH 5N+6H O;
3 2 2
(4)根据分析,沉淀A的化学式是BaSO,沉淀B为Fe (OH) ,颜色是红褐色;
4 3
(5)由分析可知,沉淀C中一定有BaCO ,可能有Al (OH) ;
3 3
(6)通过分析知,原溶液中一定含有的离子有Fe2+、 、H+、 。
19.(2025高三上·江西宜春·模拟预测)Ⅰ.高铁酸钠 是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠 中铁的化合价为 价,上述反应中体现了高铁酸钠的 (填“氧化性”或
“还原性”)。
(2)写出由 溶液制取 胶体的化学方程式: ,往 胶体中滴加 至过量的实
验现象是 。
Ⅱ.某无色透明溶液由 中的若干种离子组成,为
了确定该溶液的成分,进行如下实验:
①取少量该溶液,往其中加入过量的稀盐酸,有气泡产生,得到甲溶液;
②再往甲溶液中加入硝酸酸化的 溶液,产生白色沉淀乙;
③另取少量原溶液,加入 溶液,有白色沉淀丙产生。
根据上述实验回答下列问题:
(3)原溶液中肯定不存在的离子是 。
(4)原溶液中肯定存在的离子是 。
(5)不能确定原溶液中是否存在的离子是 。
【答案】
(1)+6 氧化性
(2)FeCl +3H O Fe(OH) (胶体)+3HCl Fe(OH) (胶体)先转化为红褐色沉淀,后沉淀溶解得到棕黄色溶
3 2 3 3
液
(3)Cu2+、MnO 、Ag+、Ba2+、Al3+
(4)Na+、CO
(5)SO 、Cl-
【分析】Ⅱ.铜离子、高锰酸根离子在溶液中呈淡蓝色、紫色,则无色溶液中一定不含有铜离子、高锰酸
根离子;取少量该溶液加入过量稀盐酸,有气体生成,得到甲溶液,说明溶液中一定含有碳酸根离子,一
定不含有银离子、钡离子和铝离子;由于步骤①中引入了氯离子,步骤②中再往甲溶液中加入硝酸酸化的
硝酸银溶液,出现白色沉淀说明原溶液中可能含有氯离子;取少量原溶液,向其中加入氢氧化钡溶液,出
现白色沉淀,白色沉淀中一定含碳酸钡,可能含硫酸钡,则溶液中可能含有硫酸根离子;由电荷守恒可
知,溶液中一定含有钠离子,综上可知,溶液中一定含有钠离子、碳酸根离子,一定不含有铜离子、高锰
酸根离子、银离子、钡离子和铝离子,可能含有氯离子和硫酸根离子,据此回答。
(1)由化学式可知,高铁酸钠 中钾元素为+1价、氧元素的化合价为-2价,由化合价代数和为0,铁元素的化合价为+6价;在 反应中,Fe的化合价
由+6价降低为+3价,体现了高铁酸钠的氧化性;
(2)制备氢氧化铁胶体的反应为饱和氯化铁溶液在沸水中发生水解反应生成氢氧化铁胶体和盐酸,反应
的化学方程式为FeCl +3H O Fe(OH) (胶体)+3HCl,向氢氧化铁胶体中加入稀硫酸,胶体会先发生聚沉转
3 2 3
化为氢氧化铁红褐色沉淀,氢氧化铁沉淀与过量硫酸溶液反应生成棕黄色的硫酸铁和水,实验现象为
Fe(OH) (胶体)先转化为红褐色沉淀,后沉淀溶解得到棕黄色溶液;
3
(3)由分析可知,原溶液中肯定不存在的离子Cu2+、MnO 、Ag+、Ba2+、Al3+;
(4)由分析可知,原溶液中肯定存在的离子是Na+、CO ;
(5)由分析可知,不能确定原溶液中是否存在的离子是SO 、Cl-。
20.(2025高三上·江西抚州·模拟预测)某浅绿色溶液X只含下表中四种离子且每种离子浓度均为
(不考虑盐类水解及水电离产生的离子)。
阳离
子
阴离
子
为了确定X组成,进行如下实验:
序号 操作及现象
Ⅰ 取适量溶液X于试管①中,加入足量NaOH溶液,共热,实验过程中无刺激性气味的气体产生
Ⅱ 取适量溶液X于试管②中,滴加足量的稀硫酸,产生无色气泡
Ⅲ 实验Ⅱ结束后,继续向试管②中滴加 溶液,产生白色沉淀
回答下列问题:
(1)根据溶液颜色及实验Ⅰ现象可以排除 种离子存在。
(2)实验Ⅱ中产生无色气泡的离子方程式为 。
(3)根据实验Ⅲ现象, (填“能”或“不能”)确定溶液X中有 存在,理由是 。
(4)根据实验可知,X中含有的四种离子为 (填离子符号)。
(5) 容易转化成 ,其主要原因是 (从结构角度分析);请设计实验检验 溶液中的
是否被氧化为 : (写出操作、现象和结论)。【答案】
(1)3
(2)
(3)不能 实验Ⅱ中添加了硫酸(合理即可)
(4)
(5) 的价层电子排布式为 ,3d轨道处于半充满稳定状态, 的价层电子排布式为 ,易失去1
个电子生成稳定的 (合理即可) 取适量 溶液于试管中,滴加适量KSCN溶液,若溶液变
红,则说明 被氧化为 ,反之则没有(合理即可)
【分析】溶液呈浅绿色,说明有Fe2+,Fe2+与 不能大量共存;加入足量NaOH溶液,共热,实
验过程中无刺激性气味的气体产生,说明不含有 ;取适量溶液X于试管②中,滴加足量的稀硫酸,产
生无色气泡,则溶液中含有 , 在酸性环境中氧化Fe2+,并生成无色的NO;实验Ⅱ结束后,继续
向试管②中滴加BaCl 溶液,产生白色沉淀,不能说明X溶液中还含有 ;由于X溶液中含有四种离
2
子,且离子浓度均相等,根据电荷守恒可知,溶液中还含有 、K+。
【小题1】溶液呈浅绿色,说明有Fe2+,Fe2+与 不能大量共存;加入足量NaOH溶液,共热,
实验过程中无刺激性气味的气体产生,说明不含有 ,故排除了 、 、 这三种离子。
【小题2】有分析可知,加入稀硫酸,产生无色气泡,发生反应为
。
【小题3】实验Ⅱ添加了硫酸,引入了硫酸根离子,故加入氯化钡溶液,产生白色沉淀,不能说明原溶液
含有硫酸根离子。
【小题4】有分析可知,X溶液中含有 。
【小题5】 的价层电子排布式为 ,3d轨道处于半充满稳定状态, 的价层电子排布式为 ,易
失去1个电子生成稳定的 ;实验室常用KSCN溶液检验 ,取适量FeCl 溶液于试管中,滴加适量
2
KSCN溶液,若溶液变红,则说明Fe2+被氧化为Fe3+,反之则没有。