文档内容
专题 04 氧化还原反应
2021年化学高考题
1.(2021·山东高考真题)实验室中利用固体KMnO 进行如图实验,下列说法错误的是
4
A.G与H均为氧化产物 B.实验中KMnO 只作氧化剂
4
C.Mn元素至少参与了3个氧化还原反应 D.G与H的物质的量之和可能为0.25mol
2.(2021·浙江)关于反应KHIO+9HI=2KI+4I+6HO,下列说法正确的是
2 3 6 2 2
A. KHIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7g I 时,转移0.1mol电子
2
D.还原剂与氧化剂的物质的量之比为7:1
KIO
3.(2021·湖南高考真题) 3常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该
Δ
6I +11KCIO +3H O 6KHIO +5KCl+3Cl
方法的第一步反应为 2 3 2 3 2 2 。下列说法错误
的是
Cl 10mole
A.产生22.4L(标准状况) 2时,反应中转移
B.反应中氧化剂和还原剂的物质的量之比为11:6
Cl
C.可用石灰乳吸收反应产生的 2制备漂白粉
IO
D.可用酸化的淀粉碘化钾溶液检验食盐中 3 的存在4.(2021·浙江高考真题)关于反应8NH+6NO=7N+12HO,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
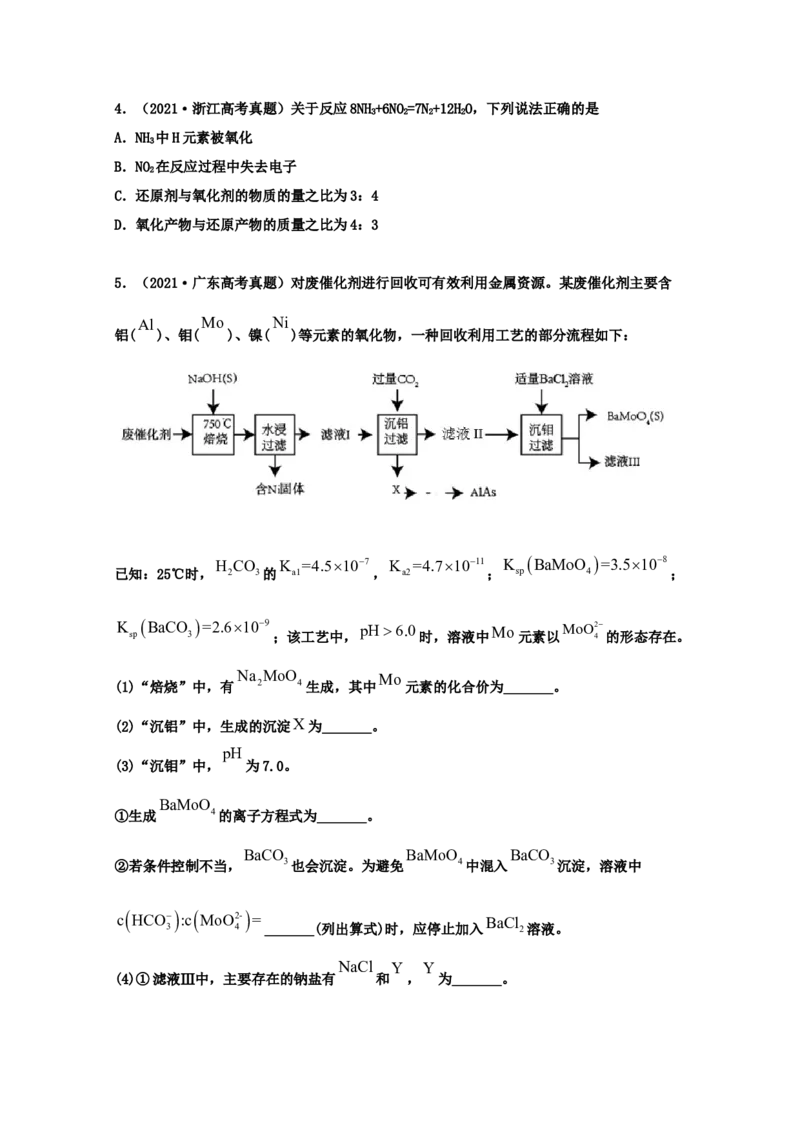
5.(2021·广东高考真题)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含
Al Mo Ni
铝( )、钼( )、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
H CO K =4.5107 K =4.71011 K BaMoO =3.5108
已知:25℃时, 2 3的 a1 , a2 ; sp 4 ;
K BaCO =2.6109 pH6.0 Mo MoO2
sp 3 ;该工艺中, 时,溶液中 元素以 4 的形态存在。
Na MoO Mo
(1)“焙烧”中,有 2 4生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀X为_______。
pH
(3)“沉钼”中, 为7.0。
BaMoO
①生成 4的离子方程式为_______。
BaCO BaMoO BaCO
②若条件控制不当, 3也会沉淀。为避免 4中混入 3沉淀,溶液中
c
HCO
:c
MoO2-
= BaCl
3 4 _______(列出算式)时,应停止加入 2溶液。
NaCl Y Y
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。NaCl CO
②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 2,
可析出Y。
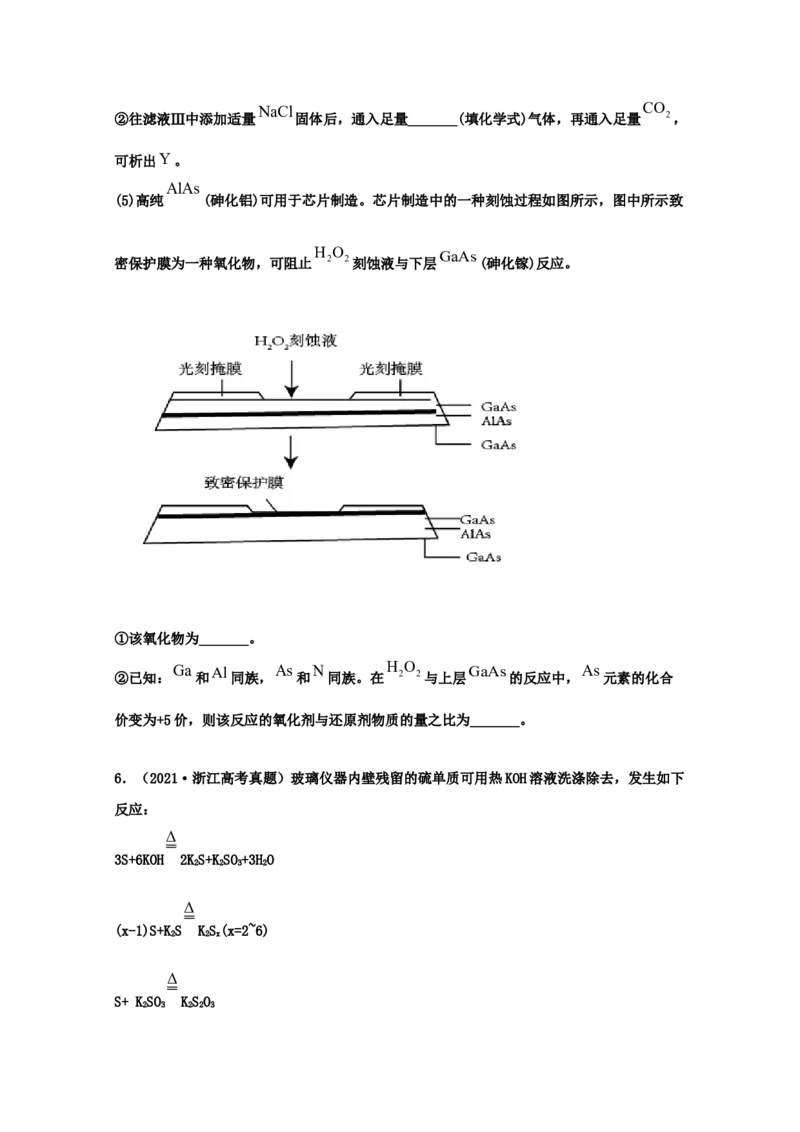
AlAs
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致
H O
GaAs
密保护膜为一种氧化物,可阻止 2 2刻蚀液与下层 (砷化镓)反应。
①该氧化物为_______。
②已知: Ga 和 Al 同族, As 和 N 同族。在 H 2 O 2与上层 GaAs 的反应中, As 元素的化合
价变为+5价,则该反应的氧化剂与还原剂物质的量之比为_______。
6.(2021·浙江高考真题)玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下
反应:
Δ
3S+6KOH 2KS+KSO+3HO
2 2 3 2
Δ
(x-1)S+KS KS(x=2~6)
2 2 x
Δ
S+ KSO KSO
2 3 2 2 3请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS和KSO,则
2 2 3
V=______。
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS 和
2 x
KSO,则x=______。(写出计算过程)
2 2 3
2021年化学高考模拟题
1.(2021·九龙坡区·重庆市育才中学高三三模)下列物质在生活中的应用与氧化还原反
应无关的是
A.用多孔薄膜包裹的CaO用作衣物防潮剂
B.ClO 常用于自来水的杀菌消毒
2
C.用KMnO 溶液浸润的硅藻土吸收水果散发出的乙烯
4
D.呼吸面具中常用NaO 作供氧剂
2 2
2.(2021·南岸区·重庆第二外国语学校高三三模)固体NaS溶于水呈碱性且放出有臭味
2
高温
Na SO+2C Na S+2CO↑
的气体,俗称“臭碱”。工业上可利用反应 2 4 2 2 来制备,下列说法
不正确的是
A.NaS溶液显碱性的原因是:S2-+HO HS-+OH-
2 2 ⇌
B.NaS可以在空气中长期放置会变质
2
C.反应中生成1mol“臭碱”转移电子的物质的量为8mol
D.该反应中氧化剂和还原剂的物质的量比为2:1
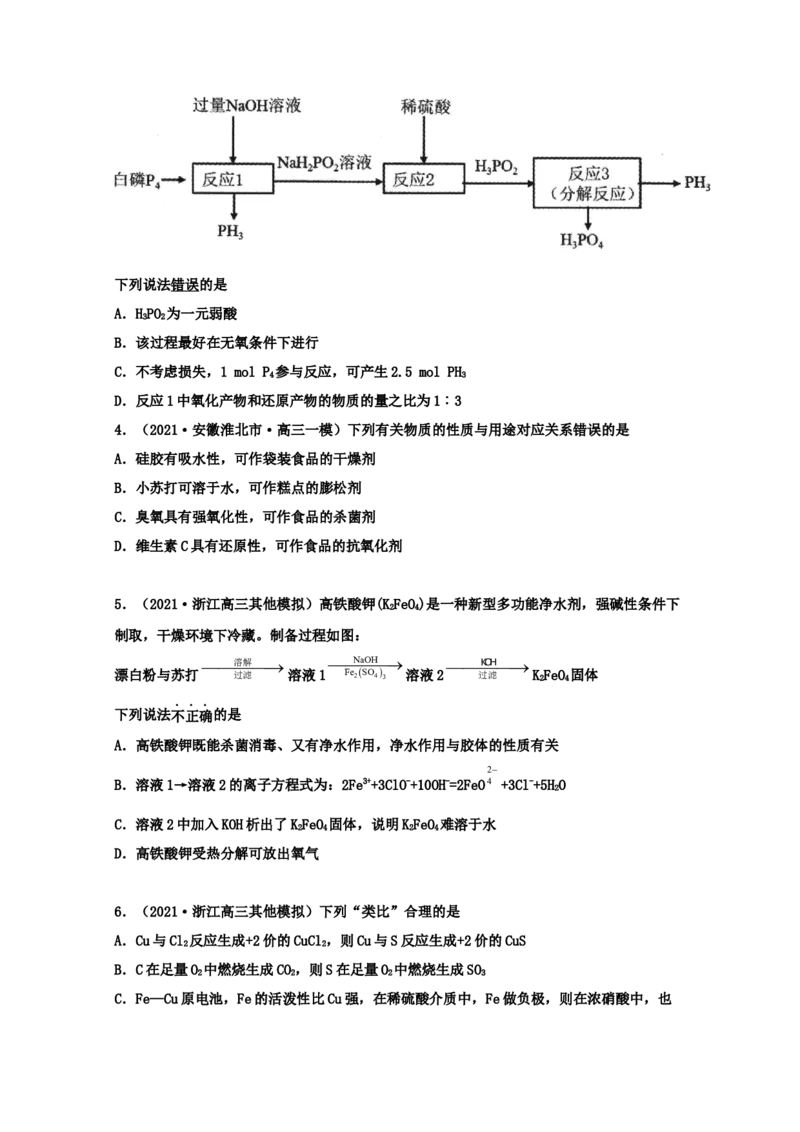
3.(2021·重庆市第十一中学校高三二模)磷化氢(PH)是一种在空气中能自燃的剧毒气体,
3
具有还原性,可作为电子工业原料。PH 的一种工业制法流程如下:
3下列说法错误的是
A.HPO 为一元弱酸
3 2
B.该过程最好在无氧条件下进行
C.不考虑损失,1 mol P 参与反应,可产生2.5 mol PH
4 3
D.反应1中氧化产物和还原产物的物质的量之比为1︰3
4.(2021·安徽淮北市·高三一模)下列有关物质的性质与用途对应关系错误的是
A.硅胶有吸水性,可作袋装食品的干燥剂
B.小苏打可溶于水,可作糕点的膨松剂
C.臭氧具有强氧化性,可作食品的杀菌剂
D.维生素C具有还原性,可作食品的抗氧化剂
5.(2021·浙江高三其他模拟)高铁酸钾(KFeO)是一种新型多功能净水剂,强碱性条件下
2 4
制取,干燥环境下冷藏。制备过程如图:
溶解 NaOH KOH
漂白粉与苏打 过滤 溶液1 Fe 2 SO 4 3 溶液2 过滤 K 2 FeO 4 固体
下列说法不正确的是
A.高铁酸钾既能杀菌消毒、又有净水作用,净水作用与胶体的性质有关
2
B.溶液1→溶液2的离子方程式为:2Fe3++3ClO-+10OH-=2FeO4 +3Cl-+5HO
2
C.溶液2中加入KOH析出了KFeO 固体,说明KFeO 难溶于水
2 4 2 4
D.高铁酸钾受热分解可放出氧气
6.(2021·浙江高三其他模拟)下列“类比”合理的是
A.Cu与Cl 反应生成+2价的CuCl,则Cu与S反应生成+2价的CuS
2 2
B.C在足量O 中燃烧生成CO,则S在足量O 中燃烧生成SO
2 2 2 3
C.Fe—Cu原电池,Fe的活泼性比Cu强,在稀硫酸介质中,Fe做负极,则在浓硝酸中,也是Fe做负极
D.NH 与HCl反应生成NHCl,则HN—NH 也可以与HCl反应生成NHCl
3 4 2 2 2 6 2
高温
7.(2021·浙江高三其他模拟)火法炼铜中涉及反应:2CuFeS+O CuS+2FeS+SO,下
2 2 2 2
列判断正确的是
A.CuFeS 只作还原剂
2
B.SO 既是氧化产物又是还原产物
2
C.消耗1 mol O 时转移电子的物质的量为4 mol
2
D.每生成1 mol CuS同时产生22.4 LSO
2 2
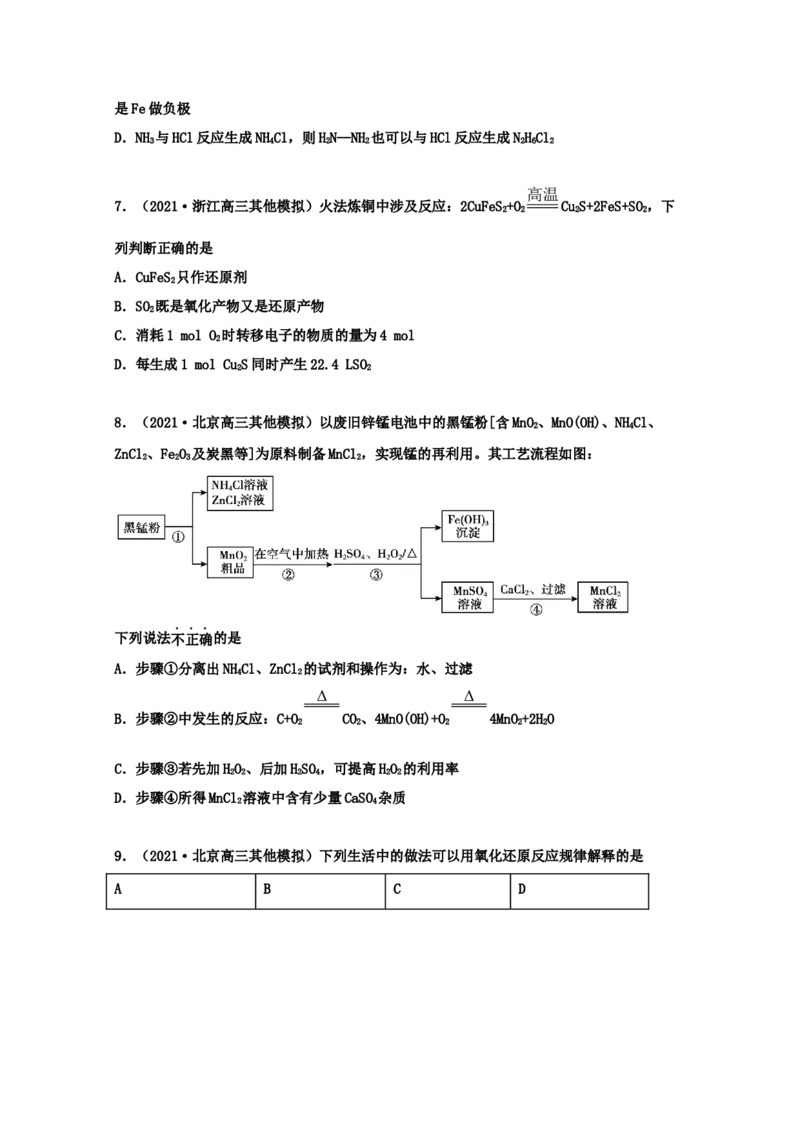
8.(2021·北京高三其他模拟)以废旧锌锰电池中的黑锰粉[含MnO、MnO(OH)、NHCl、
2 4
ZnCl、FeO 及炭黑等]为原料制备MnCl,实现锰的再利用。其工艺流程如图:
2 2 3 2
下列说法不正确的是
A.步骤①分离出NHCl、ZnCl 的试剂和操作为:水、过滤
4 2
Δ Δ
B.步骤②中发生的反应:C+O CO、4MnO(OH)+O 4MnO+2HO
2 2 2 2 2
C.步骤③若先加HO、后加HSO,可提高HO 的利用率
2 2 2 4 2 2
D.步骤④所得MnCl 溶液中含有少量CaSO 杂质
2 4
9.(2021·北京高三其他模拟)下列生活中的做法可以用氧化还原反应规律解释的是
A B C D用纯碱溶液清洗
用铁粉作脱氧保鲜剂 用白醋去除水垢 用明矾净水
油污
A.A B.B C.C D.D
10.(2021·阜新市第二高级中学高三其他模拟)下列叙述不涉及氧化还原反应的是
A.氯碱工业法制NaOH
B.维生素C用作食品抗氧化剂
C.用稀KMnO 溶液消毒
4
D.古代利用明矾溶液清除铜镜表面的铜锈
11.(2021·河南新乡市·新乡县一中高三其他模拟)化学与人类的生活有着密切联系,下
列过程涉及氧化还原反应的是
A.SO 漂白的纸张易变黄 B.长江入海口沙洲的形成
2
C.苹果汁中加入维生素C可防止苹果汁变黄 D.紫甘蓝汁中加入食醋会变为红色
12.(2021·广西南宁市·南宁三中高三三模)2021 年3月,中国国家航天局发布高清火星
影像图,以中国之眼向全世界展示“荧荧火光、离离乱惑”。据载:火星表面富含铁的氧化
物,在气流中形成红棕色尘暴。火星南北极冠覆盖水冰与干冰,随季节消长。下列说法正确
的是
A.水冰与干冰互为同分异构体
B.火星表面含铁氧化物可作颜料入画
C.长征5号火箭只需携带液氢燃料,氧气可来自大气
D.传统的火箭推进剂为偏二甲肼和四氧化二氮,四氧化二氮作还原剂
13.(2021·阜新市第二高级中学高三其他模拟)SF 是有效的应用广泛的选择性有机氟化剂,
4工业上制备SF 的反应为3SCl+4NaF=SF+SCl+4NaCl。下列说法错误的是
4 2 4 2 2
A.SF 为氧化产物,SCl 是还原产物
4 2 2
B.SCl 和SCl 两种物质中硫元素的化合价不同
2 2 2
C.该反应中,参加反应的还原剂和氧化剂物质的量之比为2:1
D.上述反应中,每产生1molSF,转移电子的物质的量为2mol
4
14.(2021·长沙市明德中学高三三模)用酸性KMnO 溶液处理硫化亚铜(CuS)和二硫化亚铁
4 2
MnO- SO2-
(FeS)的混合物时,发生反应I: 4+CuS+H+→Cu2++ 4 +Mn2++HO(未配平)和反应II:
2 2 2
MnO- SO2-
4+FeS+H+→Fe3++ 4 +Mn2++HO(未配平)。下列说法错误的是
2 2
A.反应I中CuS只是还原剂
2
SO2-
B.反应I中每生成1mol 4 ,转移电子的物质的量为10mol
C.反应II中氧化剂与还原剂的物质的量之比为3∶1
D.若反应I和反应II中消耗的KMnO 的物质的量相同,则反应I和反应II中消耗的还原剂
4
的物质的量之比为2∶3
NaN KNO
15.(2021·辽宁高三其他模拟)汽车安全气囊中装有 3和 3固体,发生碰撞时生
成两种金属氧化物和一种单质气体,下列说法正确的是
A.氧化产物与还原产物的质量比为1∶15
1mol NaN 3mol
B.每消耗 3转移 电子
10NaN 2KNO =K O5Na O16N
C.安全气囊中发生的反应为 3 3 2 2 2
NN
D.氮气的电子式为
n n
16.(2021·梅州市梅江区梅州中学)在水溶液中,RO3 和Mn2+发生反应:RO3 +3Mn2+
n
+3HO=R-+3MnO↓+6H+,则RO3 中R元素的化合价和原子最外层电子数分别为
2 2A.+4、6 B.+7、7 C.+5、7 D.+5、5
17.(2021·江苏省如皋中学)室温下,通过下列实验探究NaHS溶液的性质。
实验 实验操作和现象
1 向0.1 mol·L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红
2 向0.1 mol·L-1 NaHS溶液中加入等体积0.1 mol·L-1 NaOH溶液充分混合
3 向0.1 mol·L-1 NaHS溶液中通入过量氯气,无淡黄色沉淀产生
4 向0.1 mol·L-1 NaHS溶液中滴加过量CuCl 溶液,产生黑色沉淀
2
下列有关说法正确的是
A.0.1 mol·L-1NaHS溶液中:c(S2-)>c(HS)
2
B.实验2所得溶液中:c(Na+)=c(S2-)+c(HS-)+c(HS)
2
C.实验3说明HS-不能被氯气氧化
D.实验4反应静置后的上层清液中有c(Cu2+)·c(S2-)=K (CuS)
sp
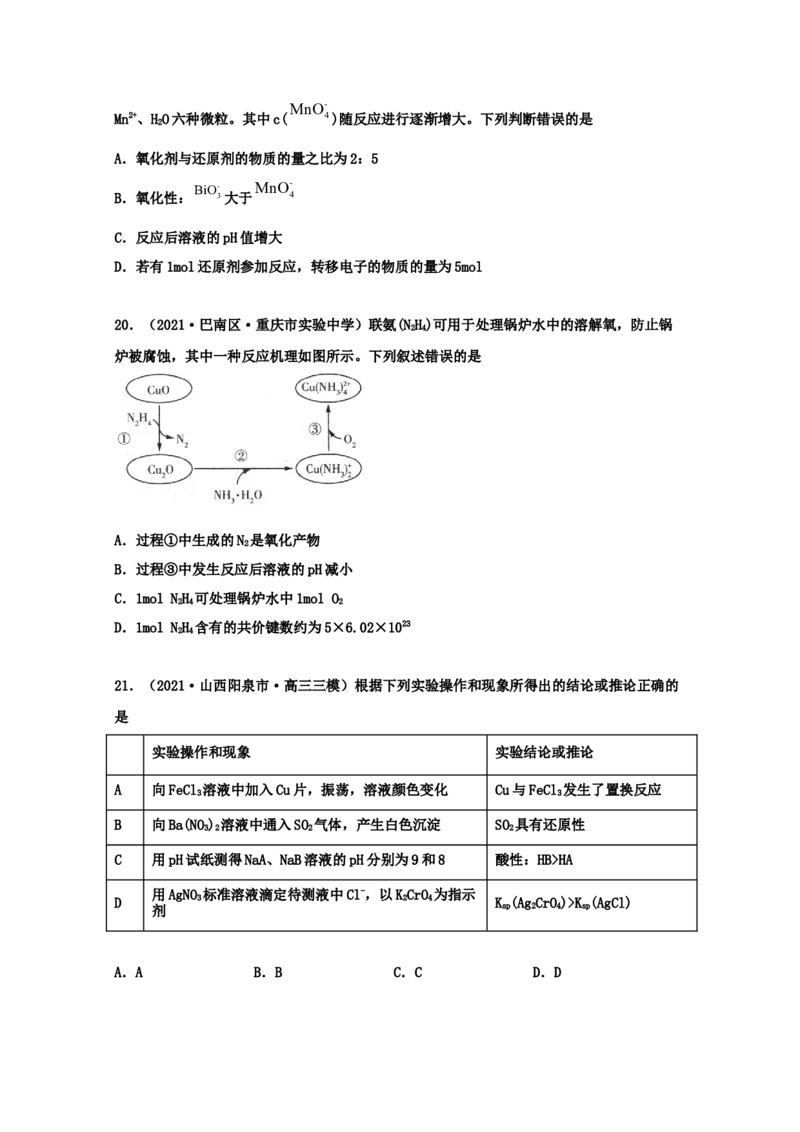
18.(2021·江苏省如皋中学)实验室用下图所示装置制取SO 并验证SO 的部分性质。下列
2 2
有关说法正确的是
A.铜和浓硫酸反应制取SO 时,氧化剂和还原剂的物质的量之比为2:1
2
B.品红溶液褪色,说明SO 的氧化性
2
C.石蕊试液变红但不褪色
-
D.用NaOH溶液吸收少量SO 的离子方程式为SO+OH-=HSO3
2 2
MnO- BiO-
19.(2021·广东汕头市·金山中学高三三模)某离子反应涉及H+、Bi3+、 4、 3、MnO-
Mn2+、HO六种微粒。其中c( 4)随反应进行逐渐增大。下列判断错误的是
2
A.氧化剂与还原剂的物质的量之比为2:5
BiO- MnO-
B.氧化性: 3大于 4
C.反应后溶液的pH值增大
D.若有1mol还原剂参加反应,转移电子的物质的量为5mol
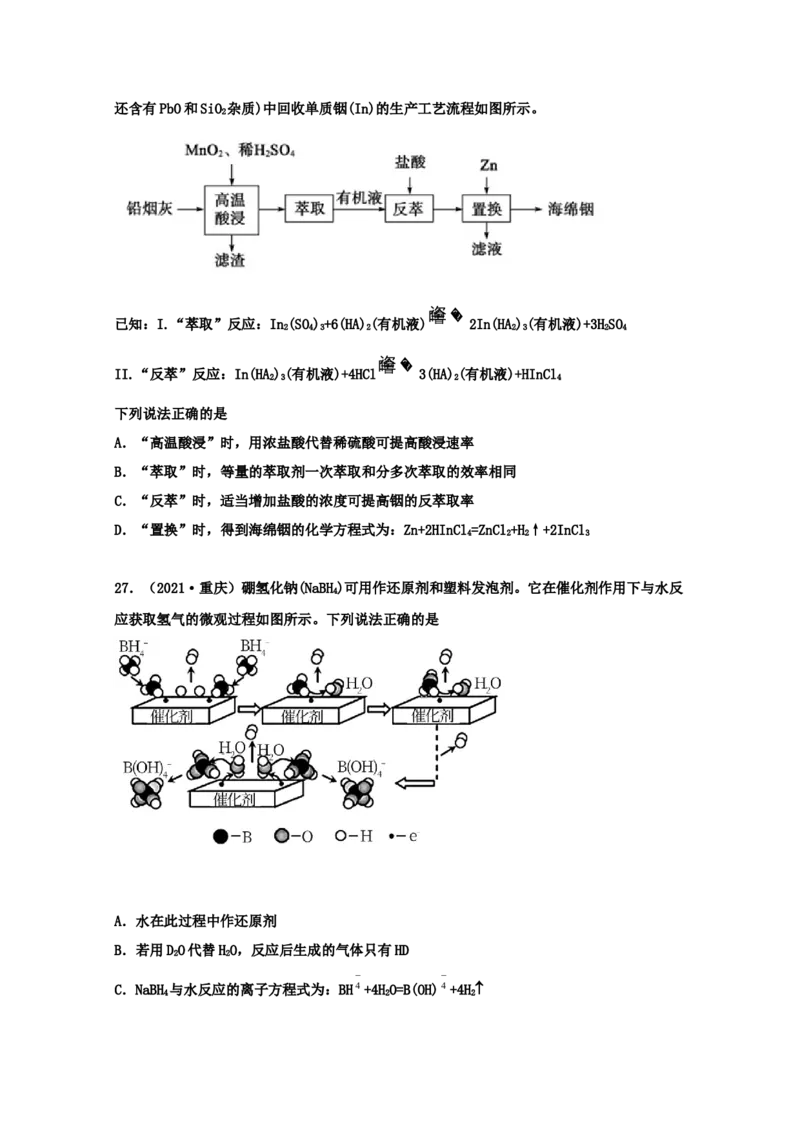
20.(2021·巴南区·重庆市实验中学)联氨(NH)可用于处理锅炉水中的溶解氧,防止锅
2 4
炉被腐蚀,其中一种反应机理如图所示。下列叙述错误的是
A.过程①中生成的N 是氧化产物
2
B.过程③中发生反应后溶液的pH减小
C.1mol NH 可处理锅炉水中1mol O
2 4 2
D.1mol NH 含有的共价键数约为5×6.02×1023
2 4
21.(2021·山西阳泉市·高三三模)根据下列实验操作和现象所得出的结论或推论正确的
是
实验操作和现象 实验结论或推论
A 向FeCl 溶液中加入Cu片,振荡,溶液颜色变化 Cu与FeCl 发生了置换反应
3 3
B 向Ba(NO) 溶液中通入SO 气体,产生白色沉淀 SO 具有还原性
3 2 2 2
C 用pH试纸测得NaA、NaB溶液的pH分别为9和8 酸性:HB>HA
用AgNO 标准溶液滴定待测液中Cl-,以KCrO 为指示
D 3 2 4 K (AgCrO)>K (AgCl)
剂 sp 2 4 sp
A.A B.B C.C D.D22.(2021·安徽安庆一中高三三模)下列文献记载内容涉及非氧化还原反应的是
A.东汉《周易参同契》中记载“胡粉投火中,色坏还为铅”
B.宋代《天工开物》中“凡石灰,经火焚炼为用”
C.西汉时期的《淮南万毕术》中有“曾青得铁,则化为铜”
D.晋代《抱扑子》一书中记载有“丹砂烧之成水银,积变又还成丹砂”
23.(2021·云南昆明市·昆明一中高三其他模拟)下列反应中,反应物用量或浓度变化时,
不会引起产物改变的是
A.Zn与硫酸溶液反应 B.Cu与硝酸溶液反应
C.Al与氢氧化钠溶液反应 D.Cl 与FeBr 溶液反应
2 2
24.(2021·江苏南京市·南京师大附中高三其他模拟)工业上利用炭和水蒸气反应:C(s)
+HO(g)
CO(g)+H(g)、CO(g)+HO(g)
CO(g)+H(g)生成的H 为原料合成氨。
2 2 2 2 2 2
-
在饱和食盐水中先通NH,后通CO,由于HCO3能形成多聚体,所以容易析出NaHCO,过滤后
3 2 3
热分解得纯碱。下列有关说法正确的是
A.增大压强有利于提高上述反应中焦炭的利用率
-
B.NaHCO 溶液中,HCO3能形成多聚体是因为氢键的作用
3
C.若反应体系中,c(CO)=a mol·L-1,c(CO)=b mol·L-1,则c(H)=(a+b) mol·L-1
2 2
D.析出NaHCO 的反应属于氧化还原反应
3
25.(2021·江苏南京市·南京师大附中高三其他模拟)TiO 的“纳米材料”有广泛的应用,
2
工业上可利用TiCl 制取。 TiCl 熔点为-25 ℃,沸点为136.4 ℃。制取TiO 的反应为①
4 4 2
2FeTiO+7Cl+3C=2TiCl+2FeCl+3CO、② TiCl+O=TiO+2Cl。下列说法正确的是
3 2 4 3 2 4 2 2 2
A.基态Ti原子核外价电子排布式为3d24s2
B.Cl、CO 都是含有非极性键的非极性分子
2 2
C.TiCl 晶体是离子晶体,配位数为4
4
D.生成1 mol FeCl 转移电子的物质的量为14 mol
3
26.(2021·山东滨州市·高三二模)用“HSO 浸出一萃取”法从铅烟灰(主要含有InO,
2 4 2 3还含有PbO和SiO 杂质)中回收单质铟(In)的生产工艺流程如图所示。
2
噲垐 ��
已知:I.“萃取”反应:In(SO)+6(HA)(有机液) 2In(HA)(有机液)+3HSO
2 4 3 2 2 3 2 4
噲垐 ��
II.“反萃”反应:In(HA)(有机液)+4HCl 3(HA)(有机液)+HInCl
2 3 2 4
下列说法正确的是
A.“高温酸浸”时,用浓盐酸代替稀硫酸可提高酸浸速率
B.“萃取”时,等量的萃取剂一次萃取和分多次萃取的效率相同
C.“反萃”时,适当增加盐酸的浓度可提高铟的反萃取率
D.“置换”时,得到海绵铟的化学方程式为:Zn+2HInCl=ZnCl+H↑+2InCl
4 2 2 3
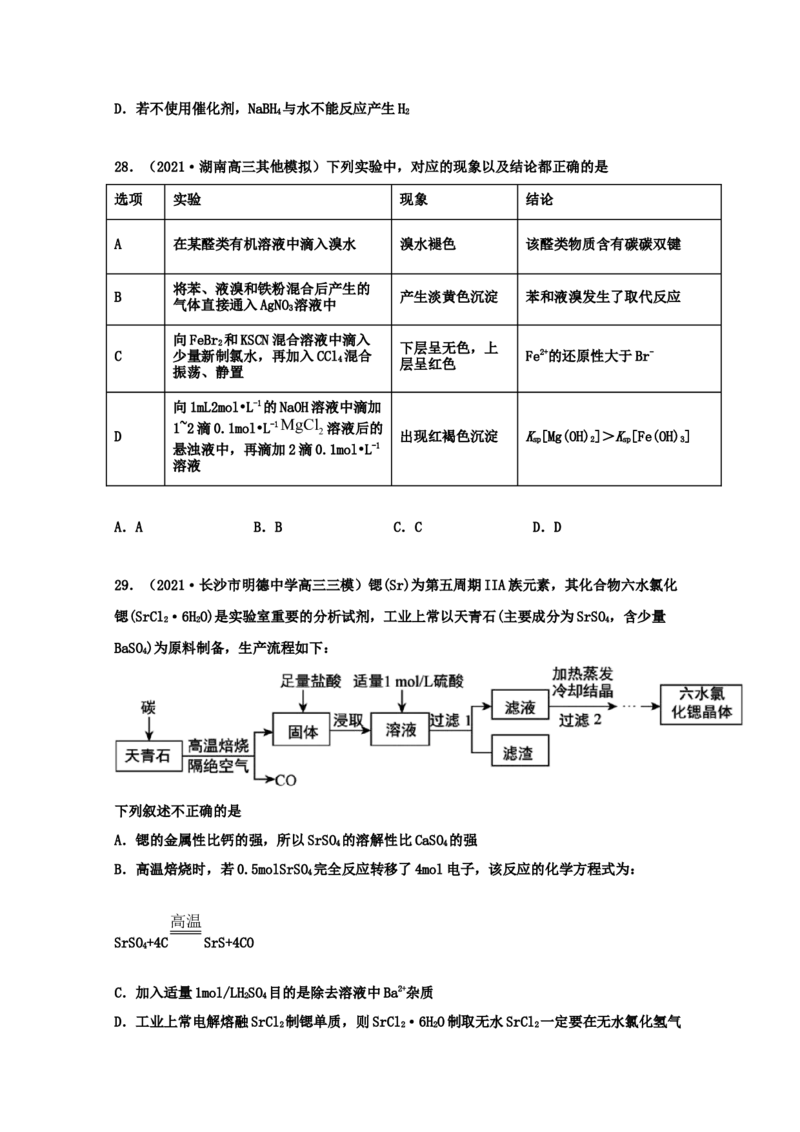
27.(2021·重庆)硼氢化钠(NaBH)可用作还原剂和塑料发泡剂。它在催化剂作用下与水反
4
应获取氢气的微观过程如图所示。下列说法正确的是
A.水在此过程中作还原剂
B.若用DO代替HO,反应后生成的气体只有HD
2 2
C.NaBH 与水反应的离子方程式为:BH4+4HO=B(OH)4+4H
4 2 2D.若不使用催化剂,NaBH 与水不能反应产生H
4 2
28.(2021·湖南高三其他模拟)下列实验中,对应的现象以及结论都正确的是
选项 实验 现象 结论
A 在某醛类有机溶液中滴入溴水 溴水褪色 该醛类物质含有碳碳双键
将苯、液溴和铁粉混合后产生的
B 产生淡黄色沉淀 苯和液溴发生了取代反应
气体直接通入AgNO 溶液中
3
向FeBr 和KSCN混合溶液中滴入
2 下层呈无色,上
C 少量新制氯水,再加入CCl 混合 Fe2+的还原性大于Br-
4 层呈红色
振荡、静置
向1mL2mol•L-1的NaOH溶液中滴加
1~2滴0.1mol•L-1MgCl 溶液后的
D 2 出现红褐色沉淀 K[Mg(OH)]>K[Fe(OH)]
sp 2 sp 3
悬浊液中,再滴加2滴0.1mol•L-1
溶液
A.A B.B C.C D.D
29.(2021·长沙市明德中学高三三模)锶(Sr)为第五周期IIA族元素,其化合物六水氯化
锶(SrCl·6HO)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO,含少量
2 2 4
BaSO)为原料制备,生产流程如下:
4
下列叙述不正确的是
A.锶的金属性比钙的强,所以SrSO 的溶解性比CaSO 的强
4 4
B.高温焙烧时,若0.5molSrSO 完全反应转移了4mol电子,该反应的化学方程式为:
4
高温
SrSO+4C SrS+4CO
4
C.加入适量1mol/LHSO 目的是除去溶液中Ba2+杂质
2 4
D.工业上常电解熔融SrCl 制锶单质,则SrCl·6HO制取无水SrCl 一定要在无水氯化氢气
2 2 2 2流中加热SrCl·6HO失水恒重
2 2
N H H O
NaClO
30.(2021·辽宁高三其他模拟)利用 氧化尿素制备 2 4 2 (水合肼)的实验流
程如图所示:
已知:①氯气与烧碱溶液的反应是放热反应;
N H H O NaClO N
② 2 4 2 有强还原性,能与 剧烈反应生成 2。
下列说法正确的是
A.步骤Ⅰ中为避免温度过高,可采用冰水浴
NaClO NaClO NaClO
B.步骤Ⅰ制备 溶液时,测得产物中 与 3的物质的量之比为5∶1,则
参与反应的氧化剂与还原剂的物质的量之比为3∶5
NaClO
C.步骤Ⅱ中可将尿素水溶液逐滴滴入 碱性溶液中
D.生成水合肼反应的离子方程式为
ClO CONH 2OH=Cl 2H N H H OCO2
2 2 2 4 2 3
31.(2021·湖南高三其他模拟)现有4组标准电极电势:①PbO/PbSO,Eθ=1.69V;②MnO
2 4
4/Mn2+,Eθ=1.51V;③Fe3+/Fe2+,Eθ=0.77V;④Cl/Cl-,Eθ=1.07V。已知电势越高对应物质
2
的氧化性越强,则下列离子方程式或相应的描述中正确的是
2
A.5PbO+2Mn2++2HO+5SO4 =5PbSO↓+2MnO4+4OH-
2 2 4
B.2Fe2++Cl=2Fe3++2Cl-
2
C.酸化高锰酸钾时既可以用硫酸也可以用盐酸
D.氧化性由强到弱的顺序为PbO>MnO4>Cl>Fe3+
2 2
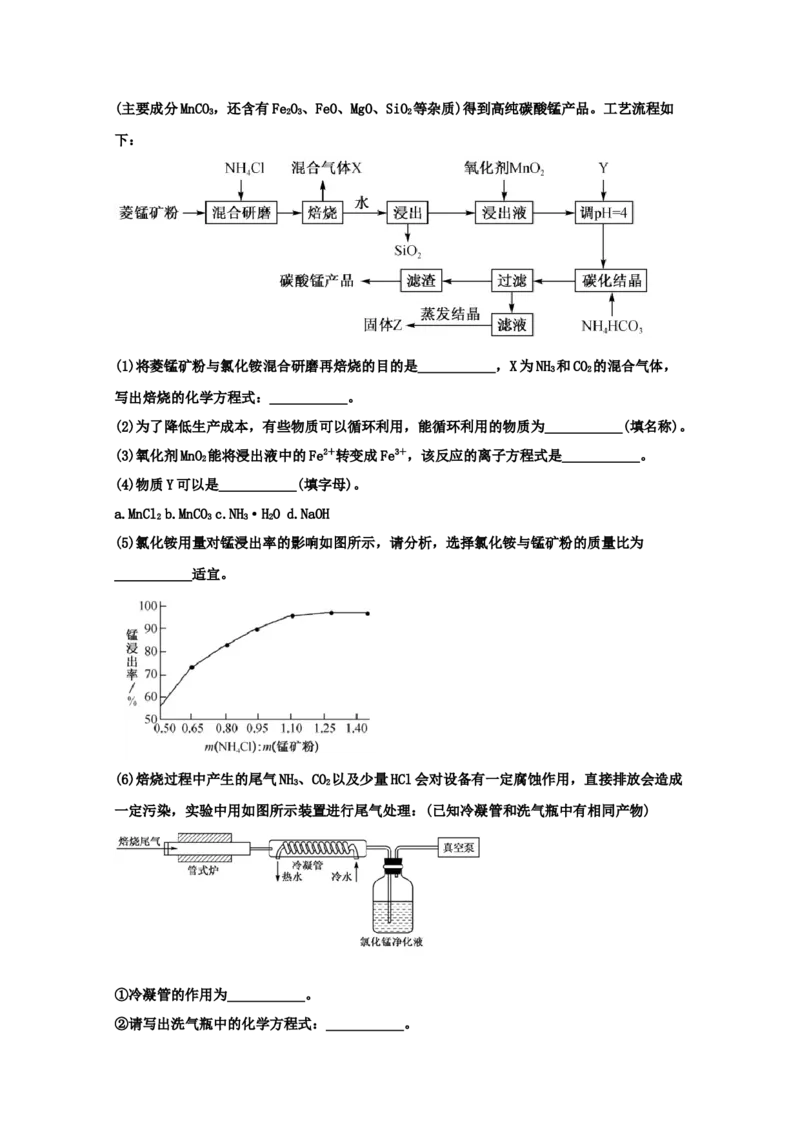
32.(2021·青海高三三模)MnCO 是制造电器材料软磁铁氧体的原料。实验室利用菱锰矿
3(主要成分MnCO,还含有FeO、FeO、MgO、SiO 等杂质)得到高纯碳酸锰产品。工艺流程如
3 2 3 2
下:
(1)将菱锰矿粉与氯化铵混合研磨再焙烧的目的是___________,X为NH 和CO 的混合气体,
3 2
写出焙烧的化学方程式:___________。
(2)为了降低生产成本,有些物质可以循环利用,能循环利用的物质为___________(填名称)。
(3)氧化剂MnO 能将浸出液中的Fe2+转变成Fe3+,该反应的离子方程式是___________。
2
(4)物质Y可以是___________(填字母)。
a.MnCl b.MnCO c.NH·HO d.NaOH
2 3 3 2
(5)氯化铵用量对锰浸出率的影响如图所示,请分析,选择氯化铵与锰矿粉的质量比为
___________适宜。
(6)焙烧过程中产生的尾气NH、CO 以及少量HCl会对设备有一定腐蚀作用,直接排放会造成
3 2
一定污染,实验中用如图所示装置进行尾气处理:(已知冷凝管和洗气瓶中有相同产物)
①冷凝管的作用为___________。
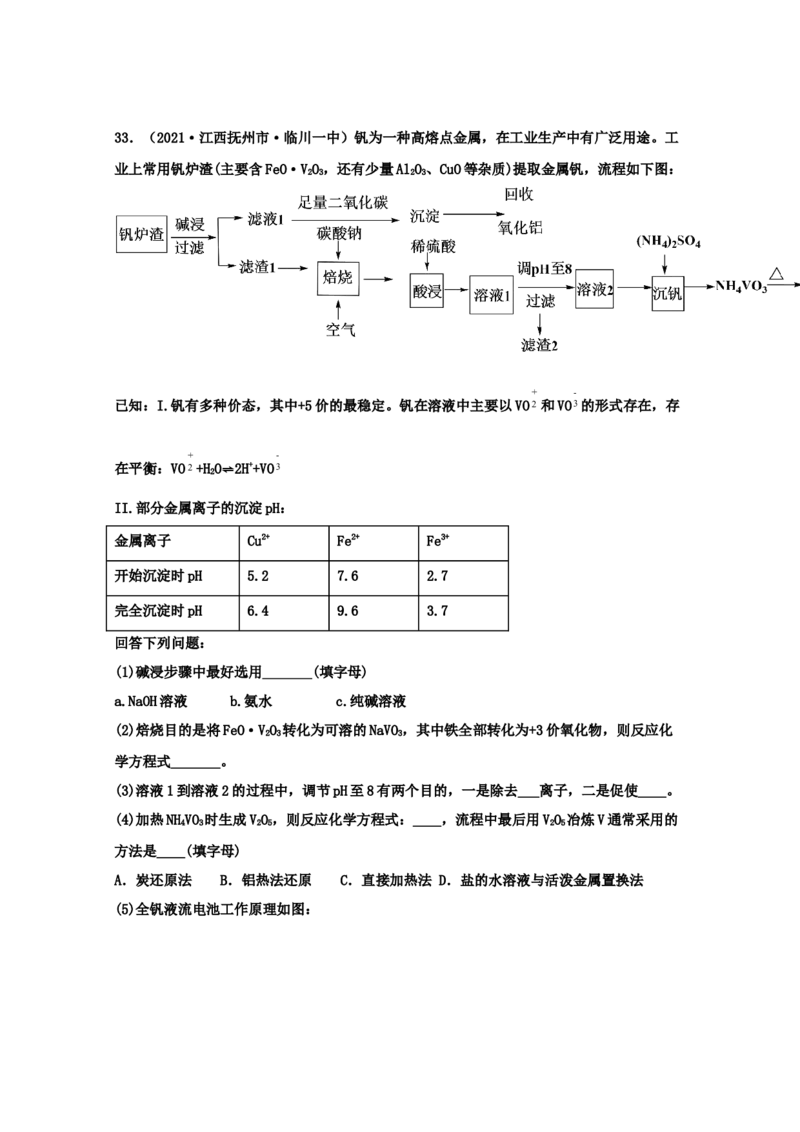
②请写出洗气瓶中的化学方程式:___________。33.(2021·江西抚州市·临川一中)钒为一种高熔点金属,在工业生产中有广泛用途。工
业上常用钒炉渣(主要含FeO·VO,还有少量AlO、CuO等杂质)提取金属钒,流程如下图:
2 3 2 3
+ -
已知:I.钒有多种价态,其中+5价的最稳定。钒在溶液中主要以VO2和VO3的形式存在,存
+ -
在平衡:VO2+H
2
O
⇌
2H++VO3
II.部分金属离子的沉淀pH:
金属离子 Cu2+ Fe2+ Fe3+
开始沉淀时pH 5.2 7.6 2.7
完全沉淀时pH 6.4 9.6 3.7
回答下列问题:
(1)碱浸步骤中最好选用_______(填字母)
a.NaOH溶液 b.氨水 c.纯碱溶液
(2)焙烧目的是将FeO·VO 转化为可溶的NaVO,其中铁全部转化为+3价氧化物,则反应化
2 3 3
学方程式_______。
(3)溶液1到溶液2的过程中,调节pH至8有两个目的,一是除去___离子,二是促使____。
(4)加热NHVO 时生成VO,则反应化学方程式:____,流程中最后用VO 冶炼V通常采用的
4 3 2 5 2 5
方法是____(填字母)
A.炭还原法 B.铝热法还原 C.直接加热法 D.盐的水溶液与活泼金属置换法
(5)全钒液流电池工作原理如图:+
已知各种含钒离子的颜色如下:VO2黄色、VO2+蓝色、V3+绿色、V2+紫色
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是_______。
②当完成储能时,阳极区溶液的颜色是_______。
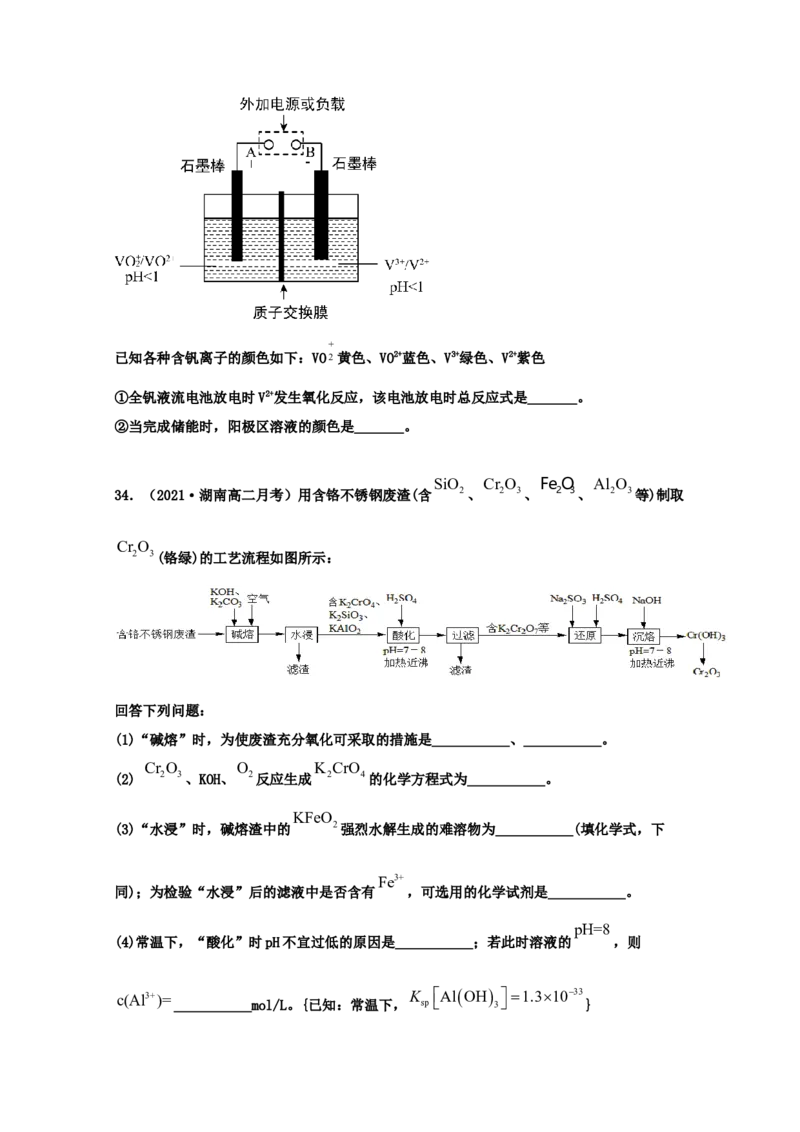
SiO Cr O FeO Al O
34.(2021·湖南高二月考)用含铬不锈钢废渣(含 2、 2 3、 2 3、 2 3等)制取
Cr O
2 3(铬绿)的工艺流程如图所示:
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是___________、___________。
Cr O O K CrO
(2) 2 3、KOH、 2反应生成 2 4的化学方程式为___________。
KFeO
(3)“水浸”时,碱熔渣中的 2强烈水解生成的难溶物为___________(填化学式,下
Fe3+
同);为检验“水浸”后的滤液中是否含有 ,可选用的化学试剂是___________。
pH=8
(4)常温下,“酸化”时pH不宜过低的原因是___________;若此时溶液的 ,则
c(Al3+)=
___________mol/L。{已知:常温下,
K
sp
AlOH
3
1.31033
}(5)“还原”时发生反应的离子方程式为___________。
CrOH
(6)“沉铬”时加热近沸的目的是___________;由 3制取铬绿的方法是___________。