文档内容
专题 04 氧化还原反应
1.(2022·河北省邢台市“五校联盟”部分重点学校高三联考)下列变化不涉及氧化还原反应的是( )
A.食物腐败 B.长期放置的无色浓硝酸变黄
C.石英遇强碱表面变暗 D.长期放置的氯水的酸性增强
2.(2022·辽宁省名校高三第四次联合考试)下列现象或事实涉及氧化还原反应的是( )
A.浓硫酸长期暴露在空气中浓度降低 B.FeSO 溶液使酸性高锰酸钾的紫色褪去
4
C.烧碱溶液长期暴露在空气中变质 D.氯化铁溶液在空气中蒸干不能得到对应的溶质
3.下列反应既属于氧化还原反应又属于化合反应的是
A.NaCO+CO+HO===2NaHCO B.4Fe(OH) +O+2HO===4Fe(OH)
2 3 2 2 3 2 2 2 3
C.2NaO+2CO===2Na CO+O D.Ca(OH) +2NH Cl===CaCl +2NH ↑+2HO
2 2 2 2 3 2 2 4 2 3 2
4.下列表示反应中电子转移的方向和数目正确的是( )
5.下列属于氧化还原反应,且氧化剂和还原剂为同一种物质的是( )
A.MgO+2HCl=MgCl +H O B.C+H O(g) CO+H
2 2 2 2
C.8NH +6NO 7N+12H O D.2NaO+2H O=4NaOH+O ↑
3 2 2 2 2 2 2 2
6.(2022·浙江省新力量联盟高一期中联考)下列变化需要加入氧化剂才能实现的是( )
A.HSO →BaSO B.Fe3+→Fe2+
2 4 4
C.CuO→Cu D.Mn2+→MnO -
4
7.(2023·浙江省温州市高三第一次适应性考试)关于反应3SiO+6C+2N Si N+6CO,下列说法正确的
2 2 3 4是( )
A.C在反应过程中被还原 B.Si N 既是氧化产物又是还原产物
3 4
C.氧化剂和还原剂质量之比为1:3 D.每生成14.0g Si N 共转移1.2mol电子
3 4
8.(2022·浙江省山水联盟高三选考模拟)关于反应CH=CH +KMnO+H SO →MnSO +K SO +CO +H O (没
2 2 4 2 4 4 2 4 2 2
配平),氧化产物和还原产物的物质的量之比是( )
A.5∶6 B.6∶5 C.5∶8 D.8∶5
9.(2022·江苏省连云港市高三联考)黄铁矿在潮湿空气中会被缓慢氧化,发生的主要反应如下(未配平):
a: FeS+ O +H O →SO 2- +Fe2++H+
2 2 2 4
b: Fe2++H++O →Fe3++ H O→
2 2
c: Fe3++FeS + H O→Fe2+ + SO 2-+ H+→
2 2 4
下列说法正确的是( )
A.a反应中氧化产物只有FeSO
4
B.为了验证b反应后溶液中含Fe2+,可选用KSCN溶液和氯水。
C.c反应中每生成1mol Fe2+转移1mol电子
D.长期盛放黄铁矿的纸箱会被腐蚀而发黑
10.(2022·安徽省定远县育才学校高三月考)打印机使用的墨粉中含有Fe O 它的一种制备方法是:将
3 4
FeSO 溶液、Fe (SO ) 溶液按一定比例混合,再加入一定量的 溶液,水浴加热。反应如下:反应a:
4 2 4 3
____ Fe2++____ Fe3++____ ____Fe O+____H O ,下列分析不正确的是( )
3 4 2
A.Fe O 具有磁性
3 4
B.反应a中, 是还原剂, 是氧化剂
C.从左至右,反应a各物质的系数依次为 、 、 、 、
D.Fe O 与盐酸反应,生成盐和水
3 4
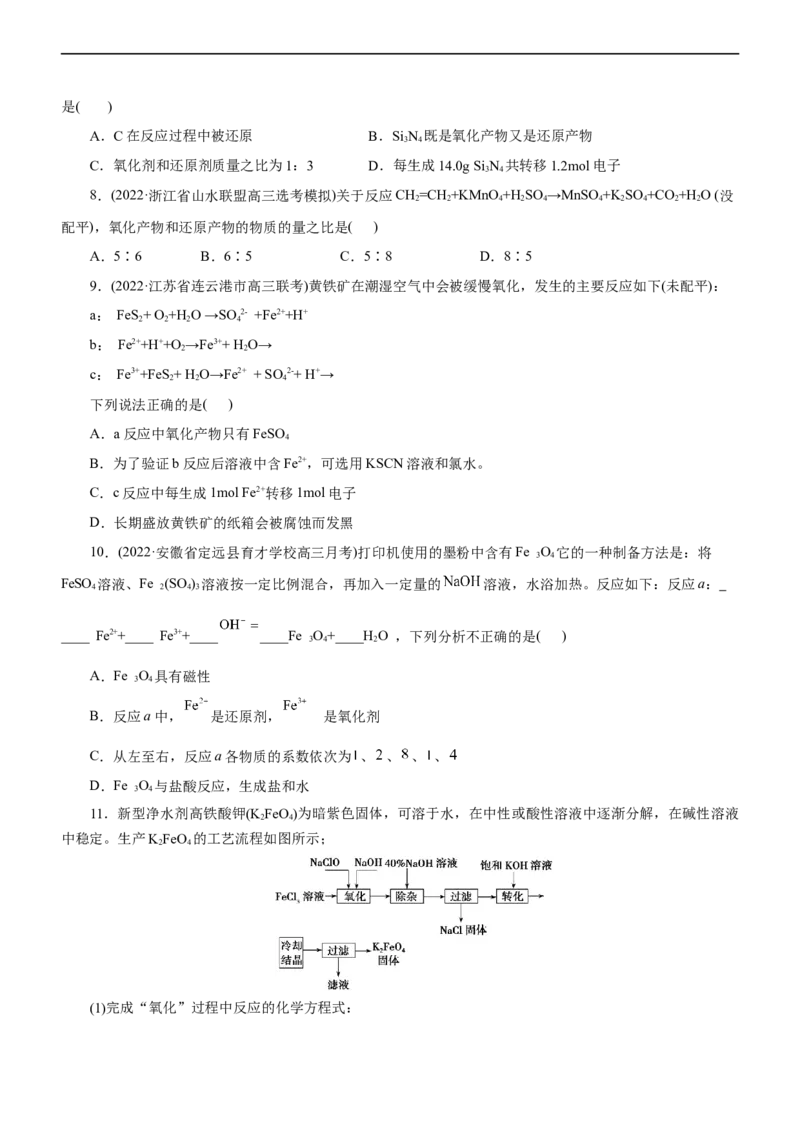
11.新型净水剂高铁酸钾(K FeO)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液
2 4
中稳定。生产KFeO 的工艺流程如图所示;
2 4
(1)完成“氧化”过程中反应的化学方程式:________FeCl +________NaOH+________NaClO―→________NaFeO +________+________。其中氧
3 2 4
化剂是________(填化学式)。
(2)“转化”过程中发生反应的化学方程式为____________________________
__________________________________________________________________。
12.四氧化三铁(Fe O)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域
3 4
多种潜在应用的有力工具。水热法制备 Fe O 纳米颗粒的反应是3Fe2++2SO+O +xOH-===Fe O↓+SO+
3 4 2 2 3 4 4
2HO。请回答下列问题。
2
(1)水热法制备Fe O 纳米颗粒的反应中,还原剂是 。
3 4
(2)反应的离子方程式中x= 。
(3)每生成1 mol Fe O,反应转移的电子为 mol,被Fe2+还原的O 的物质的量为 mol。
3 4 2
13.常温下,二氧化氯(ClO )是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为AI
2
级高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,该反应体系中的物质有 NaCl 、
HO、ClO 、NaClO、Cl、HCl。
2 2 3 2
(1)写出并配平该反应的化学方程式 _____________________________________。
(2)该反应的还原产物是_____________。
(3)在标准状况下,如果反应中生成11.2L氯气,则被氧化的HCl的物质的量为______,转移电子数目为
___________。
(4)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取适量
ClO 通入到含有HS(二元弱酸)的水中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO 与
2 2 2
HS水溶液反应的离子方程式_________________________________。
2
14.黄铜矿(CuFeS)是一种铜铁硫化物矿物,常含微量的金、银等。黄铜矿是冶炼铜及制备铁氧化物的重
2
要矿藏。以黄铜矿为主要原料生产铜、铁红(氧化铁)的工艺流程如下所示:
已知:CuFeS 中Cu为+2价。
2
请回答下列问题:
(1)CuFeS 中Fe的化合价为____________。
2
(2)写出反应Ⅰ的离子方程式:_______________________________,该反应的氧化剂是________。
(3)CuCl 难溶于水,但可与过量的 Cl-反应生成可溶于水的[CuCl ]-。该反应的离子方程式为
2
_______________________________________________。
(4)反应Ⅰ~Ⅳ 4个反应中属于非氧化还原反应的是反应________(选填“Ⅰ~Ⅳ”)。(5)反应Ⅴ中Na[CuCl ]既是氧化剂,又是还原剂,由此可推知“溶液A”中的溶质为________(写出化学式)。
2
15.(2022·宁夏吴忠中学高三月考)高锰酸钾是一种强氧化剂,为紫黑色、细长的棱形结晶或颗粒,带蓝色
的金属光泽,可溶于水。根据所学知识,回答下列问题:
(1)酸性条件下,高锰酸钾可与草酸( )溶液发生反应,其反应为
。
①补上产物,配平化学方程式___________。
②上述反应中HC O 表现的性质有___________。
2 2 4
(2)若将SO 通入硫酸酸化的KMnO 溶液中,溶液褪色,生成Mn2+,此时溶液中仅有一种阴离子。写出发
2 4
生反应的离子方程式:___________,该反应中作还原剂的是___________(填化学式)。
(3)高锰酸钾还可与浓盐酸反应,写出其化学方程式___________,其中浓盐酸表现酸性与还原性的物质的
量之比为:___________。
1.(2023·湖北省荆宜三校高三联考)通过电氧化合成法可制得特殊高价金属化合物高铜酸钠(化学式为
NaCuO)。下列关于该物质的说法错误的是( )
2
A.NaCuO 中 为 价 B.NaCuO 中存在过氧键
2 2
C.NaCuO 在酸性条件下不能稳定存在 D.NaCuO 与氢气反应可能有Cu生成
2 2
2.(2022·湖南省天壹名校联盟高三调研考试)含氰化物的废液乱倒或与酸混合,均易生成有剧毒且易挥发
的氰化氢。工业上,常采用碱性氯化法(Cl 过量)来处理高浓度氰化物污水,将废水中的有害物质转化为无毒物
2
质,发生的总反应为CN-+OH-+Cl→CO+N +Cl-+H O (未配平)。下列说法正确的是( )
2 2 2 2
A.还原性:Cl>N B.氧化剂、还原剂的物质的量之比为2∶5
2 2
C.该反应中,每生成1mol CO 转移2mol电子 D.若将该反应设计成原电池,则CO 在负极区生成
2 2
3.(2022·浙江省台州市高三选考科目教学质量评估)一定条件下,F 与水反应,生成物除了O 外,还会生
2 2
成次氟酸(HFO)、OF 等。下列推测不合理的是( )
2
A.F 与水反应还可能生成HO
2 2 2
B.HFO的分子结构中O原子位于H与F之间,O元素的化合价为-2价
C.HFO不稳定,分解生成HF与O
2
D.OF 是一种强氧化剂,与盐酸反应会生成HF、Cl、O 等
2 2 2
4.(2022·河南省部分重点高中适应检则考试)叠氮酸钠(NaN )可用作医药原料和炸药,工业上可在立窑中
3通过反应NaNO +NaNH NaN +NH↑+ NaOH(未配平)来制备叠氮酸钠,下列说法正确的是( )
3 2 3 3
A.方程式中NaNO 和NaN 的化学计量数之比为1:1
3 3
B.作还原剂的NaNH 占参与反应的 的物质的量的
2
C.每生成67.2LNH ,转移电子的物质的量为16mol
3
D.立窑的衬里适宜选用石英耐火砖
5.(2022·辽宁省名校高一联合考试)高铁酸钾(K FeO)是一种新型、高效、多功能水处理剂,工业上采用
2 4
向KOH溶液中通氯气,然后再加入Fe(NO ) 溶液的方法制备KFeO,发生如下反应:
3 3 2 4
①Cl+KOH=KCl+KClO+KClO+H O (未配平)、②3KClO+2Fe(NO )+10KOH=2KFeO↓+3KCl+6KNO +5H O,下
2 2 3 3 2 4 3 2
列说法正确的是( )
A.若反应①中有标准状况下11.2L Cl 参加反应,则消耗1molKOH
2
B.若反应①中n(Cl-):n(ClO-)=6:1,则氧化剂与还原剂的物质的量之比为1:3
C.氧化性:KFeO>KClO
2 4
D.反应②中每消耗1mol 转移6mol电子
6.(2022·安徽省合肥市五中、七中、十中高三联考)高铁酸钾是一种新型、高效、多功能水处理剂,工业
上采用向KOH溶液中通入氯气,然后再加入Fe(NO ) 溶液的方法制备KFeO,发生反应:
3 3 2 4
①Cl+KOH→KCl+KClO+KClO +H O(未配平);
2 3 2
②2Fe(NO )+3KClO+10KOH=2K FeO+6KNO +3KCl+5H O。
3 3 2 4 3 2
下列说法正确的是( )
A.反应①中每消耗4molKOH,会吸收44.8LCl
2
B.氧化性:KFeO>KClO
2 4
C.若反应①中n(ClO-):n(ClO -)=5:1,则氧化剂与还原剂的物质的量之比为5:3
3
D.若反应①的氧化产物只有KClO,则得到0.2molKFeO 时消耗0.6molCl
2 4 2
7.(2022·湖南省长沙一中高三月考)将SO 气体不断通人Fe (SO ) 溶液中,溶液颜色逐渐变浅,最后至浅
2 2 4 3
绿色,然后往溶液中滴加KCr O 溶液,溶液又变成棕黄色(还原产物为Cr3+)。则下列有关说法错误的是( )
2 2 7
A.氧化性:Cr O2->Fe3+>SO
2 7 2
B.标准状况下,若有6.72LSO 参加反应,则最终能消耗0.1molKCr O
2 2 2 7
C.通入SO 时反应的离子方程式为:SO +2Fe3++2H O= SO 2-+2Fe2++4H+
2 2 2 4
D.随着上述操作的进行,溶液的酸性越来越强
8.(2022·山西省运城市教育局教学研究室高三期中)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”
3
制备,该方法的第一步反应为6I+11KClO +3H O 6KH(IO)+5KCl+3Cl ↑。下列说法错误的是( )
2 3 2 3 2 2A.产生22.4L(标准状况) Cl 时,反应中转移 B.反应中氧化剂和还原剂的物质的量之比为11:
2
6
C.可用酸化的淀粉碘化钾溶液检验食盐中IO -的存在 D.可用澄清石灰水吸收反应产生的Cl 制备漂白
3 2
粉
9.(2022·河南省南阳市高三联考)已知电离平衡常数:HCO>HClO>HCO -,氧化性:HCO>Cl>Br
2 3 3 2 3 2 2
>Fe3+>I。下列有关离子反应或离子方程式的叙述中,正确的是( )
2
A.常温下,中性溶液中,Fe3+、Cl-、Ba2+、I-能大量共存
B.向FeI 的溶液中通入少量氯气充分反应:4Fe2++2I-+3Cl=4 Fe3++ I+6Cl-
2 2 2
C.向NaClOO溶液中通入少量二氧化碳的离子方程式:ClO-+CO +H O═HClO+HCO -
2 2 3
D.向FeBr 溶液中滴加少量氯水,再加入CCl 溶液振荡,静置,有机层呈橙色
2 4
10.(2022·贵州省金沙市高三联考)SO 气体与足量Fe (SO ) 溶液完全反应后,再加入KCr O 溶液,发生
2 2 4 3 2 2 7
如下化学反应:
① ;② 。
则下列有关说法错误的是( )
A.还原性:SO >Fe2+>Cr3+
2
B.标准状况下,若有3.36LSO 参加反应,则最终消耗0.1mol K Cr O
2 2 2 7
C.反应②中,每有0.1mol K Cr O 参加反应,转移电子的数目为0.6N
2 2 7 A
D.由上述反应原理推断:KCr O 能将NaSO 氧化成NaSO
2 2 7 2 3 2 4
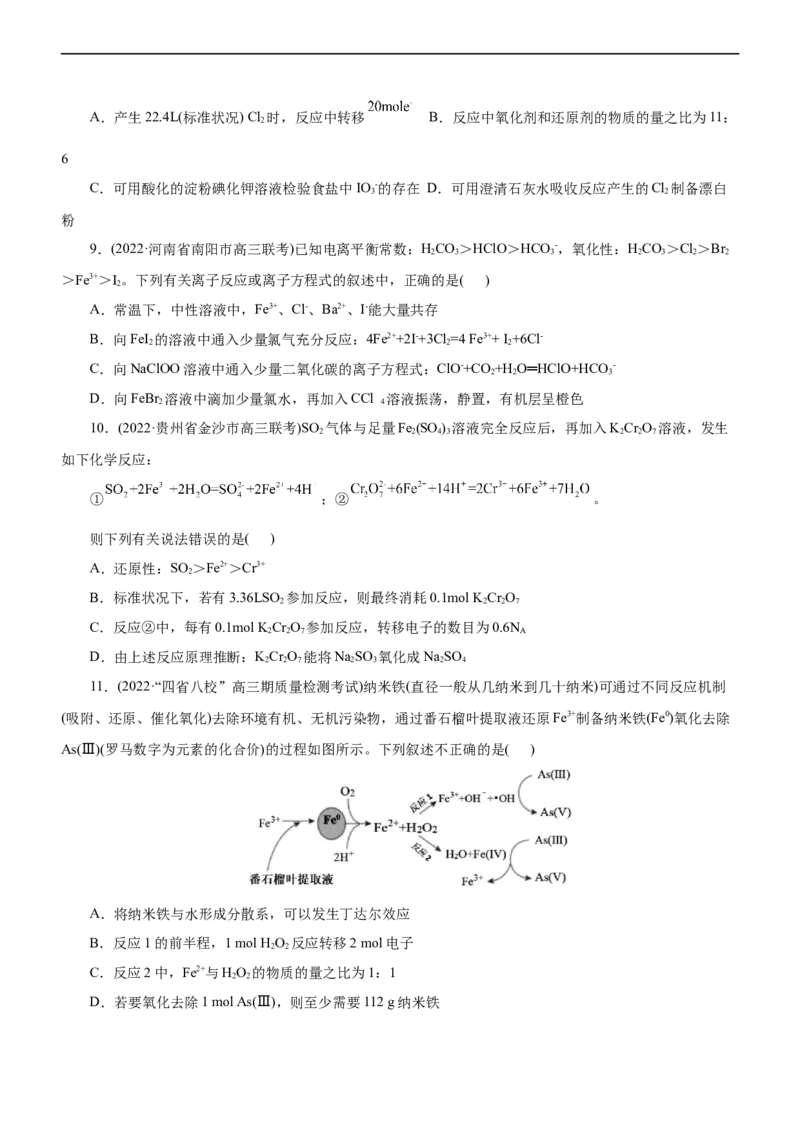
11.(2022·“四省八校”高三期质量检测考试)纳米铁(直径一般从几纳米到几十纳米)可通过不同反应机制
(吸附、还原、催化氧化)去除环境有机、无机污染物,通过番石榴叶提取液还原Fe3+制备纳米铁(Fe0)氧化去除
As(Ⅲ)(罗马数字为元素的化合价)的过程如图所示。下列叙述不正确的是( )
A.将纳米铁与水形成分散系,可以发生丁达尔效应
B.反应1的前半程,1 mol H O 反应转移2 mol电子
2 2
C.反应2中,Fe2+与HO 的物质的量之比为1:1
2 2
D.若要氧化去除1 mol As(Ⅲ),则至少需要112 g纳米铁12.(2023·湘豫名校联考第一轮复习诊断性考试)科学研究发现过二硫酸盐的溶液中存在一定量的过氧化氢,
加热会促进过二硫酸盐的水解,某兴趣小组为探究过二硫酸钠(NaSO)的性质进行了以下实验:
2 2 8
第一步:将少量的MnSO ·H O与过量的NaSO 混合,加入蒸馏水;
4 2 2 2 8
第二步:加热上述混合液,30s后开始出现大量的无色气泡,经验证该气体能使带火星的木条复燃;
第三步:取加热煮沸3min后的溶液,观察发现溶液呈深棕色,里面明显看到悬浮的小颗粒;
……
下列观点正确的是( )
A.分析NaSO 可知硫元素的化合价为+7
2 2 8
B.过二硫酸钠的水解产物中有HSO
2 4
C.3min后的溶液呈深棕色是由于Mn2+被氧化成MnO -
4
D.悬浮的小颗粒直径介于1~100nm之间
13.(2022·湖南省19所名校高三联考)用酸性KMnO 溶液处理硫化亚铜(CuS)和硫化亚铁(FeS)的混合物时,
4 2 2
发生的反应有:
反应Ⅰ: (未配平)
反应Ⅱ: (未配平)
下列说法不正确的是( )
A.反应Ⅰ中每生成1mol SO 2-,转移电子的物质的量为10mol
4
B.FeS 中含有离子键和非极性共价键
2
C.反应Ⅱ中生成的Fe3+可用K[Fe(CN) ]检验其存在
3 6
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO 的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的物质的量
4
之比为3∶2
14.高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):
KMnO +____FeSO +____HSO ===____K SO +____MnSO +____Fe (SO )+____HO。
4 4 2 4 2 4 4 2 4 3 2
下列说法正确的是( )
A.MnO是氧化剂,Fe3+是还原产物
B.Fe2+的还原性强于Mn2+
C.取反应后的溶液加KSCN溶液,可观察到有红色沉淀生成
D.生成1 mol水时,转移2.5 mol电子
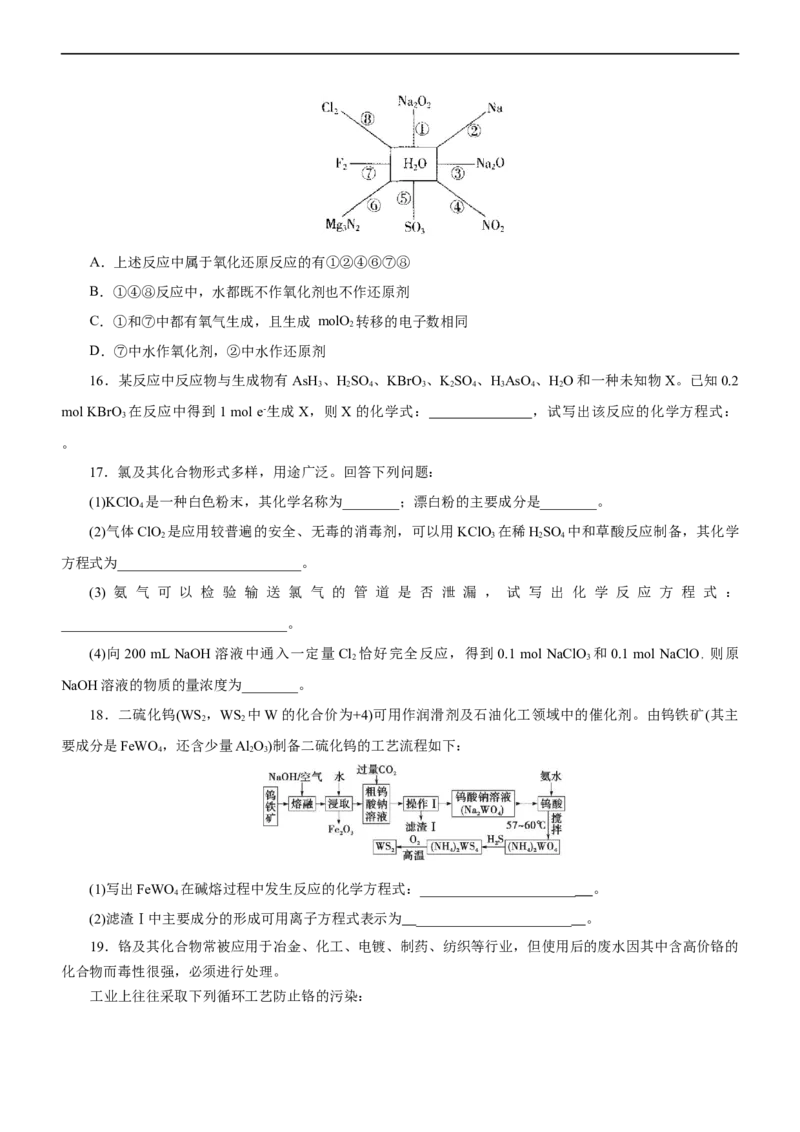
15.(2022·陕西省泾阳县教育局教学研究室高三期中)如图所示,和水相连的物质都能和水发生反应,有关
说法正确的是( )A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①④⑧反应中,水都既不作氧化剂也不作还原剂
C.①和⑦中都有氧气生成,且生成 molO 转移的电子数相同
2
D.⑦中水作氧化剂,②中水作还原剂
16.某反应中反应物与生成物有AsH 、HSO 、KBrO 、KSO 、HAsO 、HO和一种未知物X。已知0.2
3 2 4 3 2 4 3 4 2
mol KBrO 在反应中得到1 mol e-生成X,则X的化学式: ,试写出该反应的化学方程式:
3
。
17.氯及其化合物形式多样,用途广泛。回答下列问题:
(1)KClO 是一种白色粉末,其化学名称为________;漂白粉的主要成分是________。
4
(2)气体ClO 是应用较普遍的安全、无毒的消毒剂,可以用KClO 在稀HSO 中和草酸反应制备,其化学
2 3 2 4
方程式为__________________________。
(3) 氨 气 可 以 检 验 输 送 氯 气 的 管 道 是 否 泄 漏 , 试 写 出 化 学 反 应 方 程 式 :
________________________________。
(4)向200 mL NaOH溶液中通入一定量Cl 恰好完全反应,得到 0.1 mol NaClO 和0.1 mol NaClO 则原
2 3 ,
NaOH溶液的物质的量浓度为________。
18.二硫化钨(WS ,WS 中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由钨铁矿(其主
2 2
要成分是FeWO,还含少量Al O)制备二硫化钨的工艺流程如下:
4 2 3
(1)写出FeWO 在碱熔过程中发生反应的化学方程式:______________________ 。
4
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为 ______________________ 。
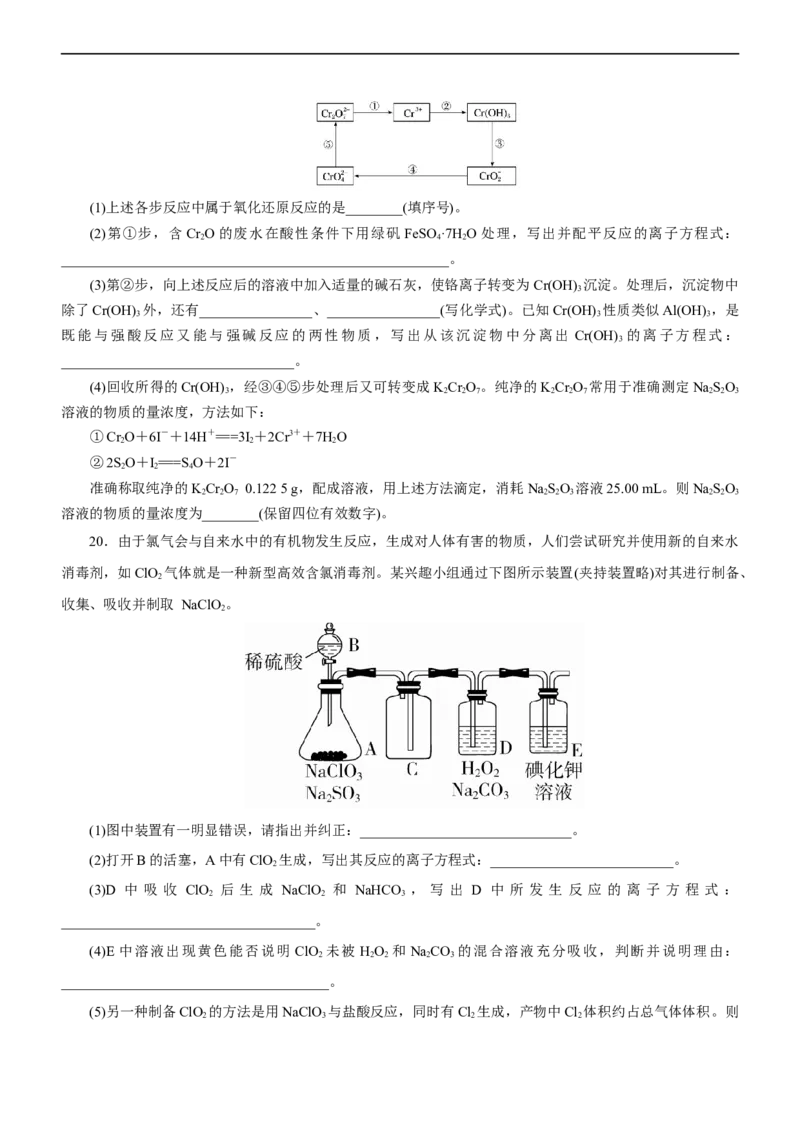
19.铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价铬的
化合物而毒性很强,必须进行处理。
工业上往往采取下列循环工艺防止铬的污染:(1)上述各步反应中属于氧化还原反应的是________(填序号)。
(2)第①步,含Cr O的废水在酸性条件下用绿矾 FeSO ·7H O处理,写出并配平反应的离子方程式:
2 4 2
_______________________________________________________。
(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为 Cr(OH) 沉淀。处理后,沉淀物中
3
除了Cr(OH) 外,还有________________、________________(写化学式)。已知Cr(OH) 性质类似Al(OH) ,是
3 3 3
既能与强酸反应又能与强碱反应的两性物质,写出从该沉淀物中分离出 Cr(OH) 的离子方程式:
3
_________________________________。
(4)回收所得的Cr(OH) ,经③④⑤步处理后又可转变成KCr O 。纯净的KCr O 常用于准确测定NaSO
3 2 2 7 2 2 7 2 2 3
溶液的物质的量浓度,方法如下:
①Cr O+6I-+14H+===3I +2Cr3++7HO
2 2 2
②2SO+I===S O+2I-
2 2 4
准确称取纯净的KCr O 0.122 5 g,配成溶液,用上述方法滴定,消耗NaSO 溶液25.00 mL。则NaSO
2 2 7 2 2 3 2 2 3
溶液的物质的量浓度为________(保留四位有效数字)。
20.由于氯气会与自来水中的有机物发生反应,生成对人体有害的物质,人们尝试研究并使用新的自来水
消毒剂,如ClO 气体就是一种新型高效含氯消毒剂。某兴趣小组通过下图所示装置(夹持装置略)对其进行制备、
2
收集、吸收并制取 NaClO。
2
(1)图中装置有一明显错误,请指出并纠正:______________________________。
(2)打开B的活塞,A中有ClO 生成,写出其反应的离子方程式:__________________________。
2
(3)D 中 吸 收 ClO 后 生 成 NaClO 和 NaHCO , 写 出 D 中 所 发 生 反 应 的 离 子 方 程 式 :
2 2 3
____________________________________。
(4)E 中溶液出现黄色能否说明 ClO 未被 HO 和 NaCO 的混合溶液充分吸收,判断并说明理由:
2 2 2 2 3
______________________________________。
(5)另一种制备ClO 的方法是用NaClO 与盐酸反应,同时有Cl 生成,产物中Cl 体积约占总气体体积。则
2 3 2 2每生成0.5 mol ClO ,转移________ mol e-。
2
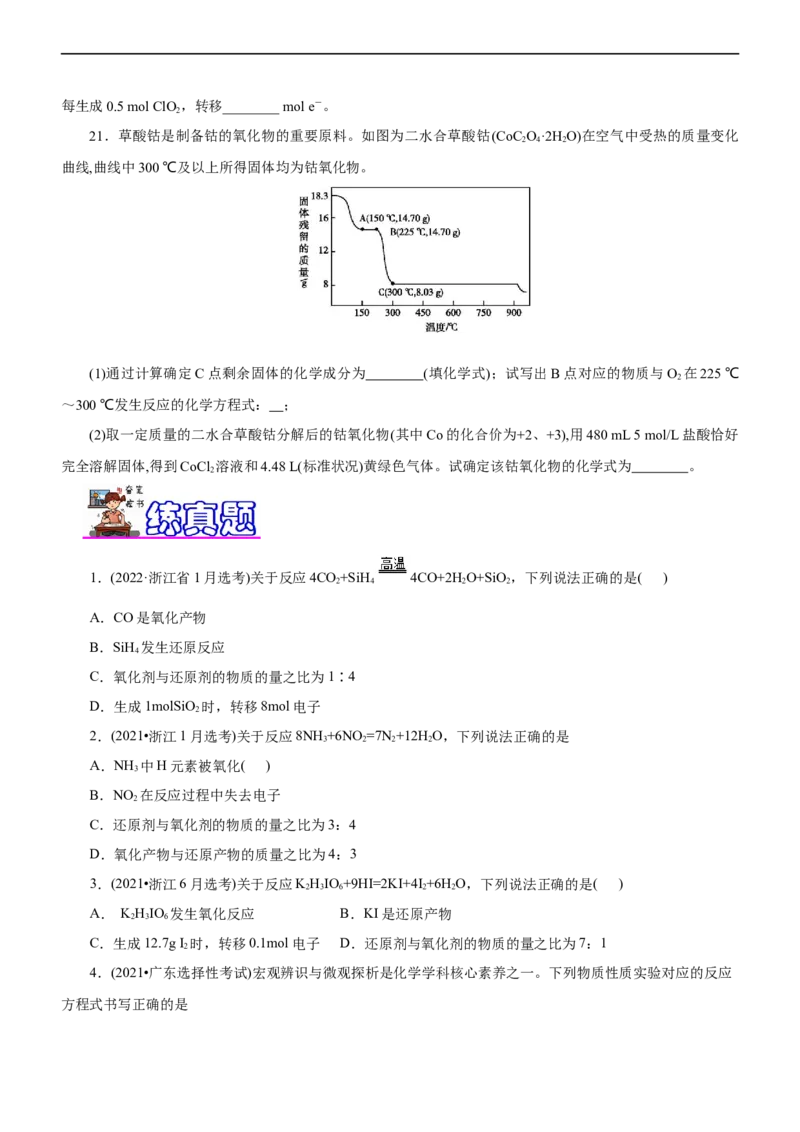
21.草酸钴是制备钴的氧化物的重要原料。如图为二水合草酸钴(CoC O·2H O)在空气中受热的质量变化
2 4 2
曲线,曲线中300 ℃及以上所得固体均为钴氧化物。
(1)通过计算确定C点剩余固体的化学成分为 (填化学式);试写出B点对应的物质与O 在225 ℃
2
~300 ℃发生反应的化学方程式: ;
(2)取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸恰好
完全溶解固体,得到CoCl 溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物的化学式为 。
2
1.(2022·浙江省1月选考)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是( )
2 4 2 2
A.CO是氧化产物
B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4
D.生成1molSiO 时,转移8mol电子
2
2.(2021•浙江1月选考)关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化( )
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
3.(2021•浙江6月选考)关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是( )
2 3 6 2 2
A. KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7:1
2
4.(2021•广东选择性考试)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应
方程式书写正确的是A.NaO 放入水中:NaO+H O=2NaOH+O ↑
2 2 2 2 2 2
B.HO(g)通过灼热铁粉:3HO+2Fe= Fe O+3H
2 2 2 3 2
C.铜丝插入热的浓硫酸中:Cu+H SO = CuSO + H↑
2 4 4 2
D.SO 通入酸性KMnO 溶液中:5SO +2H O+MnO -=5SO 2-+4H++2Mn2+
2 4 2 2 4 4
5.(2021•北京卷)电石中混有CaS、Ca P 等杂质,用电石水解制备乙炔时,乙炔中常混有HS、PH ,可
3 2 2 3
用CuSO 溶液除去这两种杂质,相应的化学方程式是( )
4
i.CuSO +H S=CuS↓+H SO
4 2 2 4
ii.11PH+24CuSO+12H O=3HPO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列说法不正确的是
A.反应i不能说明HS的酸性强于HSO
2 2 4
B.24molCuSO 完全反应时,可氧化11molPH
4 3
C.HS、PH 会干扰KMnO 酸性溶液对乙炔性质的检验
2 3 4
D.CaS的水解方程式:CaS+2H O=Ca(OH) +H S↑;Ca P 水解方程式:Ca P+6H O=3Ca(OH) +2PH↑
2 2 2 3 2 3 2 2 2 3
6.(2020•浙江1月选考)为测定FeC O·2H O(M=180 g·mol−1)样品的纯度,用硫酸溶解6.300 g样品,定容
2 4 2
至250 mL。取25.00 mL溶液,用0.1000 mol·L−1 KMnO 标准溶液滴定至终点。重复实验,数据如下:
4
序号 滴定前读数/mL 滴定终点读数/mL
1 0.00 19.98
2 1.26 22.40
3 1.54 21.56
已知:3MnO+5FeC O·2H O+24H+===3Mn2++5Fe3++10CO↑+22HO
2 4 2 2 2
假设杂质不参加反应。
该样品中FeC O·2H O的质量分数是________%(保留小数点后一位);写出简要计算过程:________
2 4 2