文档内容
专题 05 元素及其化合物的性质与应用
目录
01 模拟基础练
【题型一】常见无机物的性质与用途
【题型二】常见无机物的性质与转化
02 重难创新练
03 真题实战练
题型一 常见无机物的性质与用途
1.下列关于Na、Mg、Al、Fe、Cu的说法正确的是( )
A.常温下,Al、Cu均不与氧气反应
B.Al、Fe的阳离子,只有氧化性没有还原性
C.Na、Mg的单质放置在空气中均只生成氧化物
D.只需用水就可以鉴别MgSO 、Al (SO ) 和NaOH
4 2 4 3
2.下列说法中正确的是( )
A.金属钠可用于冶炼钛等金属 B.氢氧化铁胶体用于消毒净水
C.碳酸钠可用于中和胃酸过多 D.镁条着火可以用CO 灭火
2
3.[原创题]下列关于物质的用途的叙述不正确的是( )
A.工业上用焦炭和石英砂制备粗硅
B.锌的抗腐蚀性较强可用于制造白铁皮
C.氢气与氯气混合点燃可用于工业制盐酸
D.石灰石可用于工业炼铁、制玻璃、水泥的原料
4.(2025· 浙江省杭州市浙南联盟高三联考)物质的性质决定用途。下列说法正确的是( )
A.SO 具有漂白性,葡萄酒中添加 起到漂白作用
2
B.FeCl 溶液具有酸性,可用于腐蚀覆铜板制作印刷电路板
3
C.HNO 具有强氧化性,可清洗附在试管内壁的银镜
3D.维生素C具有氧化性,可用于水果罐头的抗还原剂
5.化学在生活生产中应用广泛,下列有关叙述正确的是( )
A.钢水注入干燥的模具,是为了防止铁与水蒸气高温下产生H 和Fe O
2 2 3
B.利用FeCl 溶液作为“腐蚀液”制作覆铜板电路时发生了置换反应
3
C.硬铝常用于制造飞机的外壳,利用了合金熔点比任一组成金属低的特点
D.过氧化钠可在呼吸面具或潜水艇中作为氧气的来源
6.关于铁及其化合物的性质与用途具有对应关系的是( )
A.Fe具有还原性,可用作抗氧化剂 B.Fe O 具有磁性,可用于炼铁
3 4
C.Fe(OH) 胶体呈红褐色,可用于净水 D.FeCl 溶液呈酸性,可用于刻蚀铜板
3 3
7.下列物质与其主要成分的化学式或者说法对应正确的是( )
A.侯氏制碱法得到的物质是碱式盐——碳酸钠
B.水玻璃很稳定,长期暴露在空气中也不变质
C.丹霞地貌的岩层因含Fe O 而呈红色
2 3
D.卤素主要单质有F、Cl、Br、I 等,都能与氢氧化钠溶液发生歧化反应
2 2 2 2
8.下列说法正确的是( )
A.二氧化硅有很好的导电性,可用于制造光导纤维
B.侯氏制碱法的原理是将氨通入二氧化碳的氯化钠饱和溶液中,使碳酸钠从溶液中析出
C.生铁含碳2%-4.5%,将生铁进一步炼制,就可以得到用途更广泛的钢(含碳0.03%-2%)
D.工业上以海带为原料制碘时,利用CCl 萃取碘水中的碘,分液、蒸馏获得粗碘
4
9.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断
向浓盐酸中加入浓硫酸 浓盐酸易挥发,浓硫酸与水作用放出大
A Ⅰ对,Ⅱ对;有
可制备氯化氢气体 量的热
由于Cu具有还原性,浓HNO 具有氧
3
B Cu能与浓HNO 反应 化性,在任何条件下生成的气体一定是 Ⅰ对,Ⅱ错;无
3
NO
2
硫单质在纯氧中燃烧有
C 部分二氧化硫被氧化为SO Ⅰ对,Ⅱ对;无
少量SO 生成 3
3
硝酸铵和碱石灰共热用
D 铵盐与碱能发生复分解反应 Ⅰ对,Ⅱ对;有
于实验室制备NH
3
题型二 常见无机物的性质与转化
1.(2022·浙江省高三下学期高考选考科目联考)下列说法不正确的是( )A.氯气与溴化亚铁反应可生成溴化铁
B.铁与稀硝酸反应可生成硝酸亚铁
C.硫在纯氧中燃烧可生成三氧化硫
D.铝与二氧化锰反应可制取金属锰
2.(2023·河南省三门峡市高三阶段性考试)下列物质在给定条件下的转化均能一步实现的是( )
A.
B.
C.
D.
3.[原创题]在给定条件下,下列物质间的转化均能一步实现的是( )
A.
B.
C.
D. (粗)
4.在给定条件下,下列选项所示的物质间转化均能实现的是
A.Fe O(s) FeCl (aq) Fe(s)
2 3 3
B.FeS SO HSO
2 2 2 3
C.Fe O FeCl (aq) 无水FeCl
2 3 3 3
D.Fe FeCl (aq) Fe(OH) Fe(OH)
2 2 3
5.下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )选项 X Y Z 箭头上所标数字的反应条件
A SiO NaSiO HSiO ①NaCO 熔融
2 2 3 2 3 2 3
B NaCl NaHCO NaCO ②加热
3 2 3
C N NO HNO ③加热
2 2 3
D C CO CO ④灼热炭粉
2
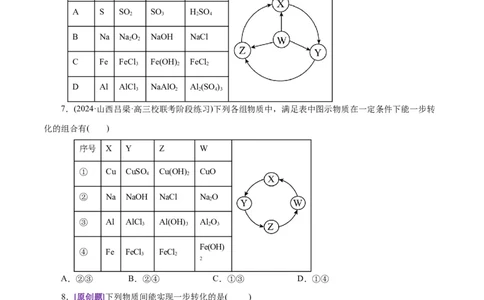
6.如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化
关系的是( )
选项 W X Y Z
A S SO SO HSO
2 3 2 4
B Na NaO NaOH NaCl
2 2
C Fe FeCl Fe(OH) FeCl
3 2 2
D Al AlCl NaAlO Al (SO )
3 2 2 4 3
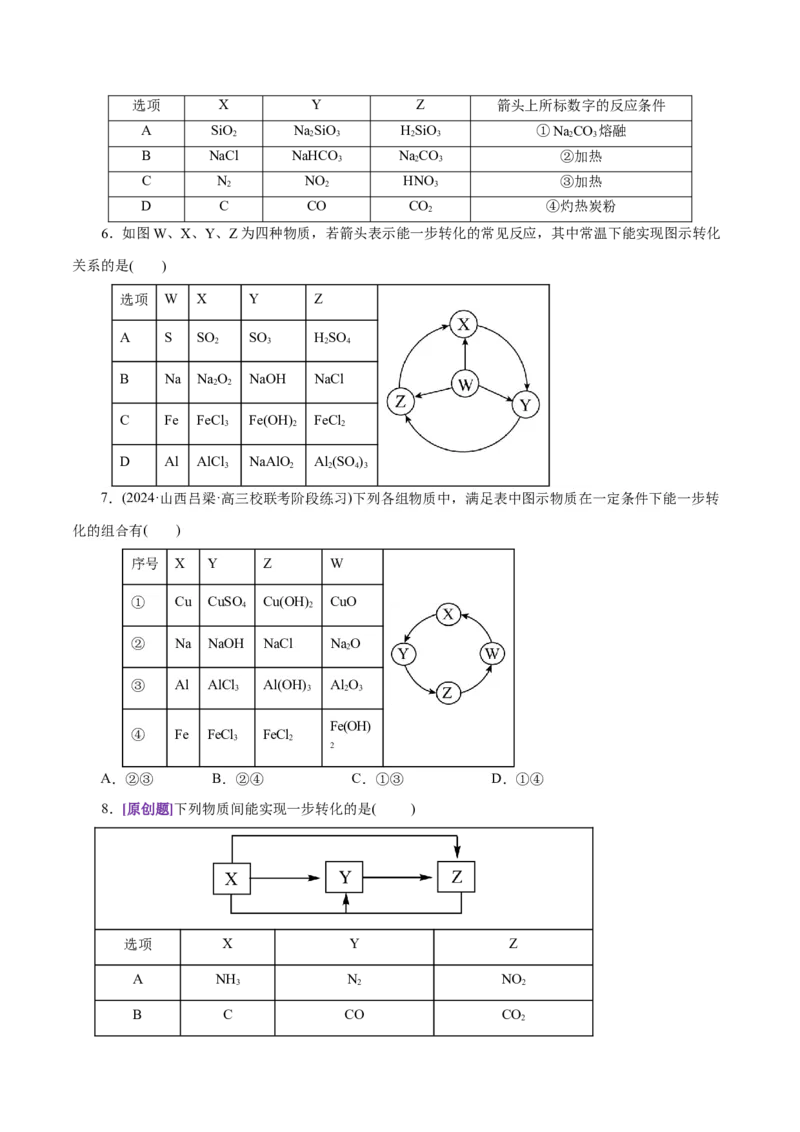
7.(2024·山西吕梁·高三校联考阶段练习)下列各组物质中,满足表中图示物质在一定条件下能一步转
化的组合有( )
序号 X Y Z W
① Cu CuSO Cu(OH) CuO
4 2
② Na NaOH NaCl NaO
2
③ Al AlCl Al(OH) Al O
3 3 2 3
Fe(OH)
④ Fe FeCl FeCl
3 2
2
A.②③ B.②④ C.①③ D.①④
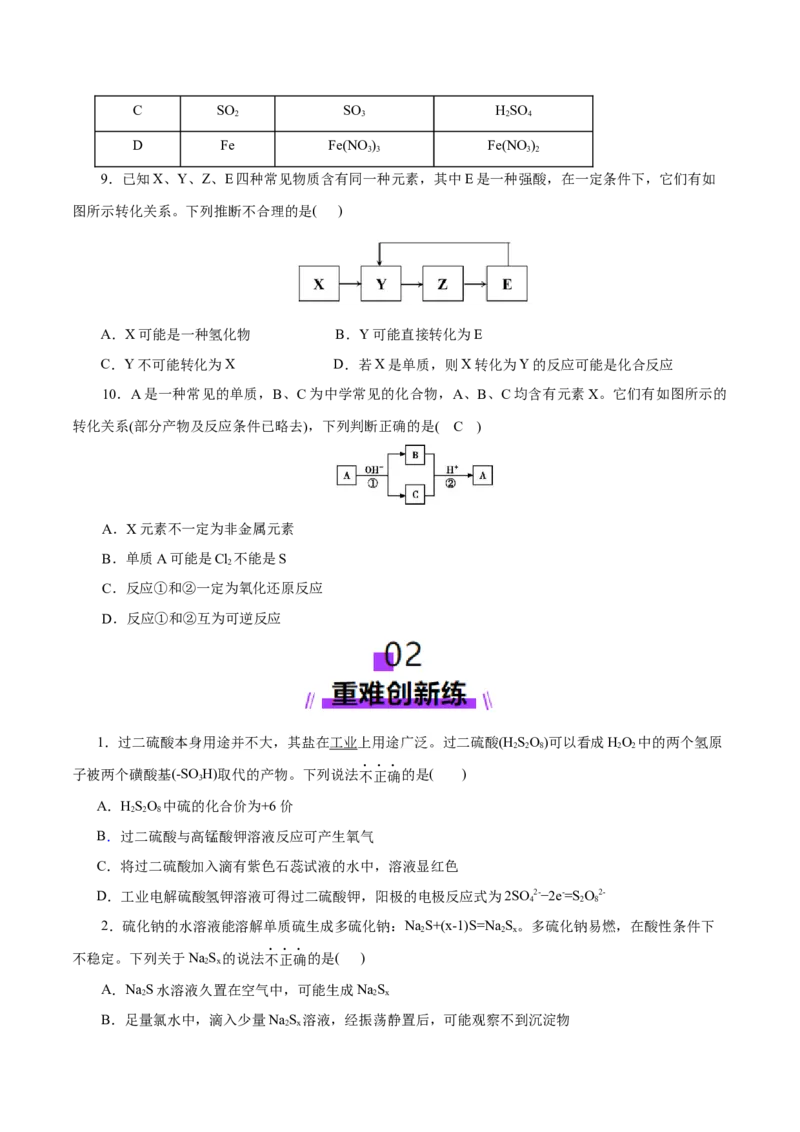
8.[原创题]下列物质间能实现一步转化的是( )
选项 X Y Z
A NH N NO
3 2 2
B C CO CO
2C SO SO HSO
2 3 2 4
D Fe Fe(NO ) Fe(NO )
3 3 3 2
9.已知X、Y、Z、E四种常见物质含有同一种元素,其中E是一种强酸,在一定条件下,它们有如
图所示转化关系。下列推断不合理的是( )
A.X可能是一种氢化物 B.Y可能直接转化为E
C.Y不可能转化为X D.若X是单质,则X转化为Y的反应可能是化合反应
10.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如图所示的
转化关系(部分产物及反应条件已略去),下列判断正确的是( C )
A.X元素不一定为非金属元素
B.单质A可能是Cl 不能是S
2
C.反应①和②一定为氧化还原反应
D.反应①和②互为可逆反应
1.过二硫酸本身用途并不大,其盐在工业上用途广泛。过二硫酸(H SO)可以看成HO 中的两个氢原
2 2 8 2 2
子被两个磺酸基(-SO H)取代的产物。下列说法不正确的是( )
3
A.HSO 中硫的化合价为+6价
2 2 8
B.过二硫酸与高锰酸钾溶液反应可产生氧气
C.将过二硫酸加入滴有紫色石蕊试液的水中,溶液显红色
D.工业电解硫酸氢钾溶液可得过二硫酸钾,阳极的电极反应式为2SO 2-−2e-=S O2-
4 2 8
2.硫化钠的水溶液能溶解单质硫生成多硫化钠:NaS+(x-1)S=Na S。多硫化钠易燃,在酸性条件下
2 2 x
不稳定。下列关于NaS 的说法不正确的是( )
2 x
A.NaS水溶液久置在空气中,可能生成NaS
2 2 x
B.足量氯水中,滴入少量NaS 溶液,经振荡静置后,可能观察不到沉淀物
2 xC.NaS 应在远离火种、热源的阴凉、干燥处密封保存
2 x
D.酸性条件下NaS 发生反应,生成淡黄色沉淀和能使品红溶液褪色的气体
2 x
3. CuCl 的结构式如下图, 时CuCl 会发生分解.下列推测合理的是( )
2 2
A.CuCl 是离子晶体,熔点高,硬度大
2
B.CuCl·H O加热可能生成Cu (OH) Cl
2 2 2 2 2
C.CuCl 分解的产物可能为CuCl和Cl,同类化合物CuI 分解温度更高
2 2 2
D.CuCl 溶于浓盐酸呈绿色,加水稀释溶液变蓝色,是因为 浓度减小
2
4.下列推理合理的是( )
A.NaCl固体与浓HSO 加热可制HCl, 则NaI固体与浓HSO 加热制HI
2 4 2 4
B.NaO 与CO 反应生成NaCO 和O,则NaO 与SO 反应生成NaSO 和O
2 2 2 2 3 2 2 2 2 2 3 2
C.实验室可利用AlCl 与足量氨水反应来制备Al(OH) ,则也可利用CuCl 与足量氨水反应生成
3 3 2
Cu(OH)
2
D.Fe与S反应生成FeS,则Cu与S反应生成Cu S
2
5.工业上曾经通过反应“3Fe+4NaOH Fe O+2H ↑+4Na↑”生产金属钠。下列有关说法正确的是(
3 4 2
)
A.Fe置换出金属Na,还原性:Fe>Na
B. 得到电子,发生氧化反应
C.将生成的气体在空气中冷却可获得钠
D.每生成1molNa,转移的电子数为2×6.02×1023
6.高炉煤气为炼铁过程中的副产品,其主要成分为CO、CO、N。现欲测定高炉煤气中CO 的含量,
2 2 2
将高炉煤气(标准状况下)以流速0.2 L·s-1匀速通入100mL1.80mol·L-1 NaOH溶液中,50s后溶液增重4.4g,
下列分析正确的是( )
A.高炉炼铁时的主要反应为2Fe O+3C 4Fe+3CO
2 3 2
B.为了提高效率,应加快高炉煤气的流速
C.溶液中生成的NaCO 和NaHCO 的物质的量之比为4:1
2 3 3
D.该高炉煤气中CO 的体积分数为2.24%
27.下列“类比”合理的是( )
A.Fe O 中Fe元素显+2、+3价,则Pb O 中Pb显+2、+3价
3 4 3 4
B.SiH 的沸点比CH 高,则PH 的沸点比NH 高
4 4 3 3
C.向Fe(OH) 中加入盐酸生成Fe3+,则向Fe(OH) 中加入氢溴酸也生成Fe3+
3 3
D.NaO 与CO 反应生成NaCO 和O,则NaO 与SO 反应生成NaSO 和O
2 2 2 2 3 2 2 2 2 2 3 2
8.下列“类比”、“推理”合理的是( )
A.Fe与Cl 反应生成FeCl ,则Fe与I 反应生成FeI
2 3 2 3
B.CaO与CO 反应生成CaCO ,CuO与CO 反应生成CuCO
2 3 2 3
C.在NaO 与水反应后的溶液中加入MnO 粉末,会产生大量气体,该气体能使带火星的木条复燃,
2 2 2
则可推测NaO 与水反应有中间产物HO 生成
2 2 2 2
D.Na与水反应生成NaOH和H,则Fe与水蒸气反应生成Fe(OH) 和H
2 3 2
9.+5价V在不同pH下微粒的化学式不同,其微粒与pH关系如表所示。
含钒元素的不同微粒 VO + VO - VO4- VO 3-
2 3 2 7 4
pH 4~6 6~8 8~10 10~12
另外,V价态不同在溶液中颜色不同,如V2+(紫色)、V3+(绿色)、VO2+(蓝色)、VO + (黄色)、VO 3- (无
2 4
色)、VO 3- (红棕色)等。下列说法正确的是( )
5 14
A.VO -转化为VO4-的离子反应为2VO -+H O=VO4-+2H+
3 2 7 3 2 2 7
B.含VO +的溶液中滴加氨水有NH VO 沉淀产生,该过程V元素被还原
2 4 3
C.酸性VO +滴加烧碱溶液,溶液显红棕色时离子反应为5VO ++8OH-=V O 3-+4H O
2 2 5 14 2
D.紫色VSO 溶液中滴加酸性高锰酸钾溶液,溶液颜色出现绿色→蓝色→黄色,两个过程均失去
4
1mol电子
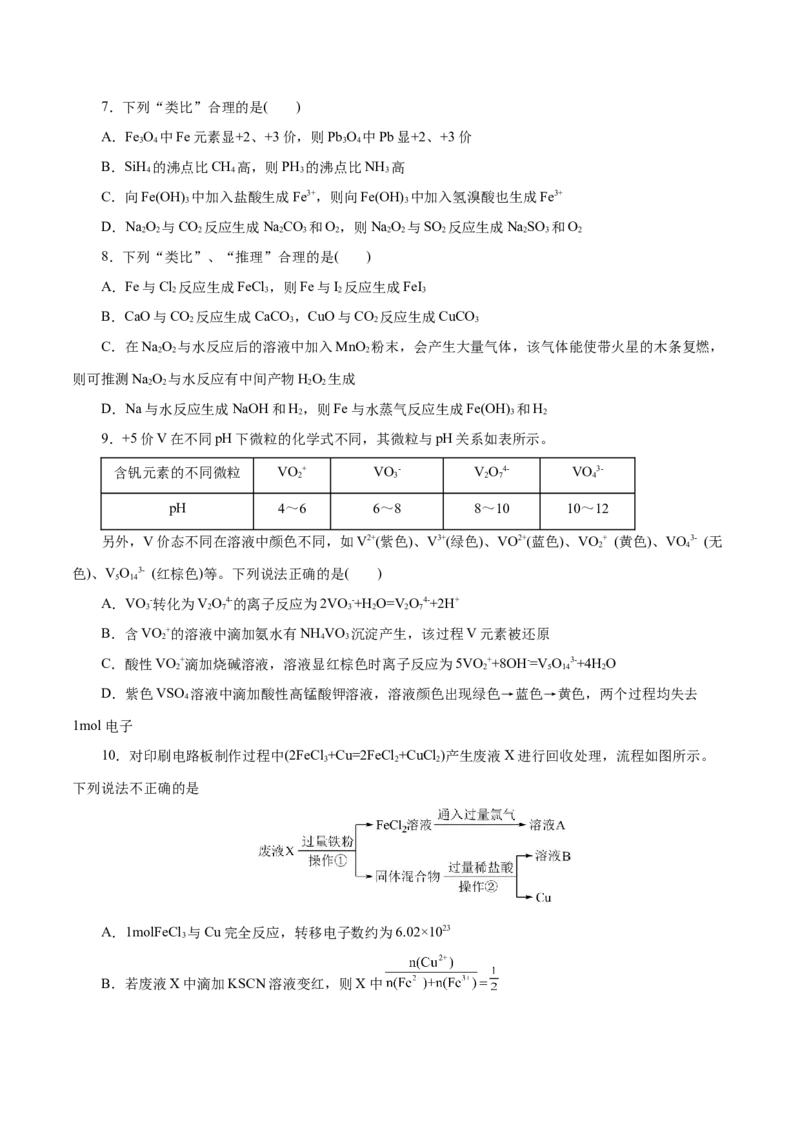
10.对印刷电路板制作过程中(2FeCl +Cu=2FeCl +CuCl )产生废液X进行回收处理,流程如图所示。
3 2 2
下列说法不正确的是
A.1molFeCl 与Cu完全反应,转移电子数约为6.02×1023
3
B.若废液X中滴加KSCN溶液变红,则X中 =C.若向溶液A中、溶液B中分别加入少量铁粉,铁粉均有减少
D.实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和玻璃棒
1.(2023•江苏卷,8,3分)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.实验室探究稀硝酸与铜反应的气态产物:
的
B.工业制硝酸过程中 物质转化:
C.汽车尾气催化转化器中发生的主要反应:2NO+2CO N+2CO
2 2
的
D.实验室制备少量NH 原理:2NH Cl+Ca(OH) CaCl +2NH ↑+2H O
3 4 2 2 3 2
2.(2023•浙江省1月选考,4)物质的性质决定用途,下列两者对应关系不正确的是( )
A. 能使某些色素褪色,可用作漂白剂 B.金属钠导热性好,可用作传热介质
C. 溶液呈碱性,可用作消毒剂 D.Fe O 呈红色,可用作颜料
2 3
3.(2023•浙江省6月选考,4)物质的性质决定用途,下列两者对应关系不正确的是( )
A.铝有强还原性,可用于制作门窗框架
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
4.(2023•浙江省1月选考,5)下列关于元素及其化合物的性质说法不正确的是( )
A. 和乙醇反应可生成H B.工业上煅烧黄铁矿(FeS )生产SO
2 2 2
C.工业上用氨的催化氧化制备NO D.常温下铁与浓硝酸反应可制备NO
2
5.(2022•江苏卷)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将N 转化为NH
2 3
B.侯氏制碱法以HO、NH 、CO、NaCl为原料制备NaHCO 和NH Cl
2 3 2 3 4
C.工业上通过NH 催化氧化等反应过程生产HNO
3 3
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
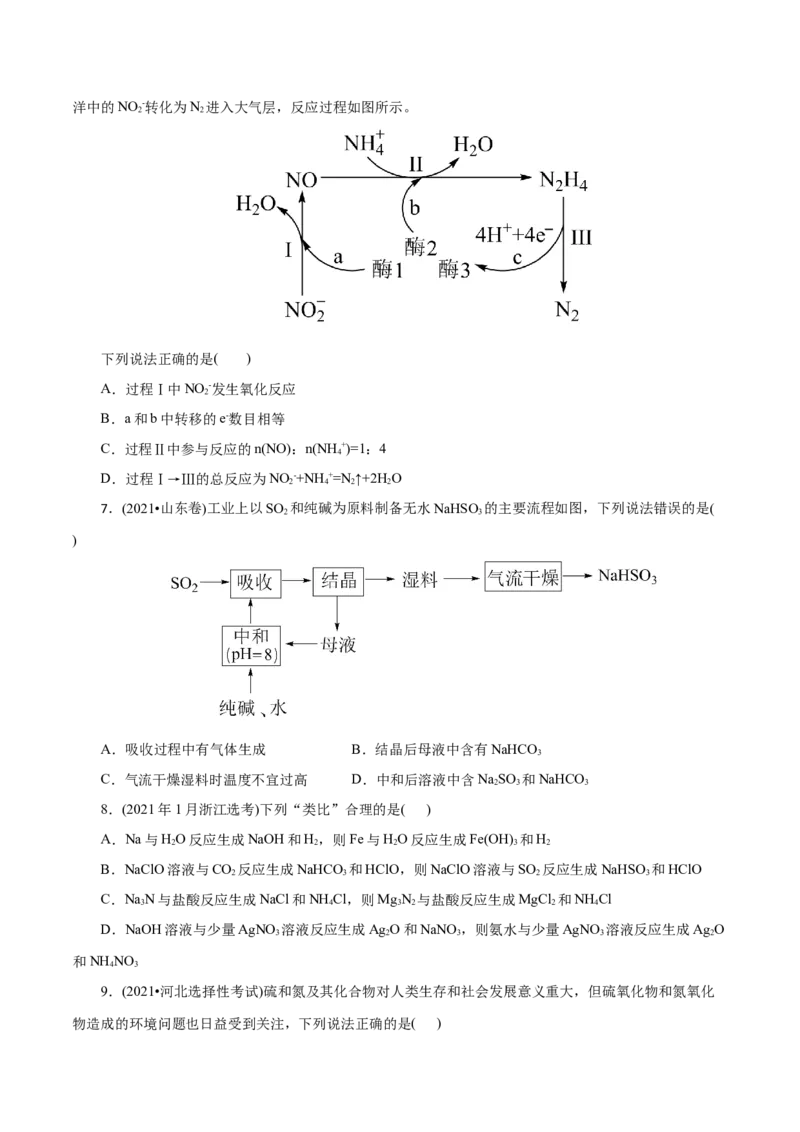
6.(2022•湖南选择性卷,9)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中的NO -转化为N 进入大气层,反应过程如图所示。
2 2
下列说法正确的是( )
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO):n(NH +)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO -+NH+=N ↑+2H O
2 4 2 2
7.(2021•山东卷)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是(
2 3
)
A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高 D.中和后溶液中含NaSO 和NaHCO
2 3 3
8.(2021年1月浙江选考)下列“类比”合理的是( )
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B.NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO 和HClO
2 3 2 3
C.NaN与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D.NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应生成Ag O
3 2 3 3 2
和NH NO
4 3
9.(2021•河北选择性考试)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化
物造成的环境问题也日益受到关注,下列说法正确的是( )A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2
B.汽车尾气中的主要大气污染物为NO、SO 和PM2.5
2
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
10.(2021•河北选择性考试)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3