文档内容
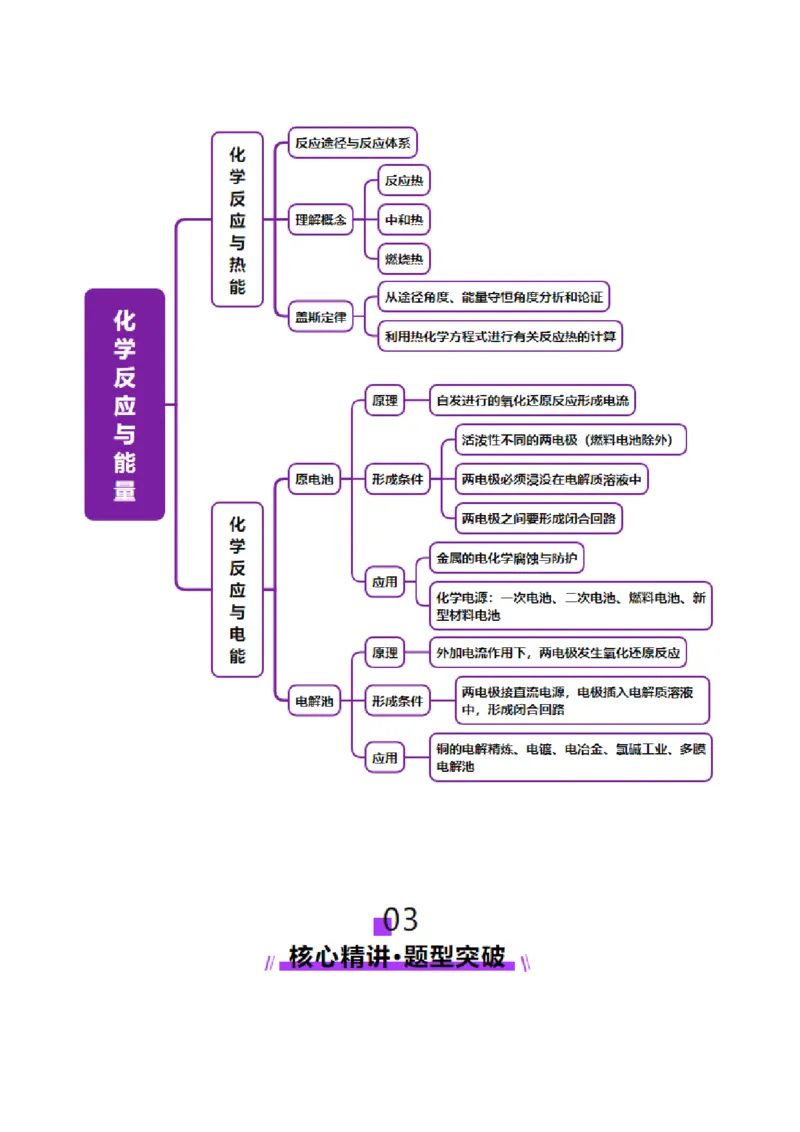
专题 06 化学反应与能量
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 反应热与热化学方程式..............................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.化学反应的热效应.............................................................................................................................................
2.反应热的计算方法.............................................................................................................................................
3.热化学方程式书写.............................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1反应过程中的能量变化...............................................................................................................................
考向2 热化学方程式..............................................................................................................................................
题型二 盖斯定律及其应用.....................................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.盖斯定律.............................................................................................................................................................
2.盖斯定律应用.....................................................................................................................................................
【命题预测】...........................................................................................................................................................
题型三 原电池原理及应用.....................................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.原电池的工作原理.............................................................................................................................................
2.“五类”依据判断原电池电极.........................................................................................................................
3.“三步”突破原电池电极反应式的书写.........................................................................................................
4.解答新型化学电源的步骤.................................................................................................................................【命题预测】...........................................................................................................................................................
题型四 电解原理及应用.........................................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.惰性电极电解电解质溶液的产物判断.............................................................................................................
2.“五类”依据判断电解池电极
3.电解原理的应用.................................................................................................................................................
4.“串联”类装置的解题流程.............................................................................................................................
【命题预测】...........................................................................................................................................................
题型五金属的腐蚀与防护.......................................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1. 金属腐蚀两种类型比较......................................................................................................................................
2.金属电化学保护的两种方法.............................................................................................................................
【命题预测】...........................................................................................................................................................考点要求 考题统计 考情分析
化学反应 2024· 海南卷,8,2分;2024· 重庆卷,13,3分;2024·江
与能量的 苏卷,5,3分;2023•海南卷,7;2022·浙江省6月卷, 化学反应的热效应
变化 18,2分; 的考查,一是在选
择题中单独设题,
2024·北京卷,3,3分;2024·江苏卷,8,3分;2024·安徽
考查反应中的能量
卷,11,3分;2024·福建卷,9,4分;2024·全国甲卷, 变化、反应热的比
6,6分;2024·全国新课标卷,6,6分;2024·河北卷, 较及盖斯定律的计
13,3分;2024·广西卷,1,3分;2024·江西卷,11,3 算;二是在选择题
原电池原
分;2023•全国乙卷,12,6分;2023•全国新课标卷,10, 中某一选项出现,
理及应用
6分;2023•浙江省6月选考,13,2分;2023•海南卷,8, 多与图像分析相结
2分;2022•福建卷,9,3分;2022•辽宁省选择性卷,14, 合;三是在填空题
3分;2022•山东卷,13,3分;2022•广东选择性卷,16,3 中考查,考查盖斯
分; 定律的计算或结合
盖斯定律的热化学
2024· 重庆卷,9,3分;2024·山东卷,13,4分;2024· 海 方程式的书写。
南卷,13,4分;2024· 贵州卷,11,3分;2024·广东卷,
电化学知识是每年
16,3分;2024·甘肃卷,7,3分;2024·湖北卷,14,3
必考,大多是选择
分;2024·辽吉黑卷,12,3分;2024·广东卷,5,2分;
题,个别省份除了
2024·浙江1月卷,13,3分;2024·浙江6月卷,13,3
有选择题,还会有
分;2023•浙江省1月选考,11,2分;2023•湖北省选择性
电解池原 二卷的填空题。题
考试,10,3分;2023•辽宁省选择性考试,7,3分;2023•
理衣应用 干大多以前沿的电
辽宁省选择性考试,11,3分;2023•全国甲卷,12,6分; 化学研究成果为情
2023•山东卷,11,3分;2023•北京卷,5,6分;2023•广 境,设问方式“大
东卷,16,3分;2022•重庆卷,12,3分;2022•全国甲 同小异”。预计
卷,10,6分;2022•全国乙卷,12,6分;2022•海南省选 2025 年仍保持这
择性卷,9,2分;2022•湖北省选择性卷,14,3分;2022· 种命题趋向。
浙江省6月卷,21,2分;题型一 反应热与热化学方程式
1.(2024· 海南卷,8,2分)已知298K,101 kPa时,2H(g)+O(g)=2HO(l) ΔH=-571.6kJ·mol−1,H
2 2 2 2
的临界温度(能够液化的最高温度)为 ,下列说法错误的是( )
A.氢气燃烧热ΔH=-285.8kJ·mol−1
B.题述条件下2 molH 和1 molO ,在燃料电池中完全反应,电功+放热量=571.6kJ
2 2
C.氢能利用的关键技术在于安全储存与运输
D.不同电极材料电解水所需电压不同,产生2gH(g)消耗的电功相同
2
【答案】D
【解析】A项,氢气燃烧热为1mol氢气完全燃烧生成液态水放出的热量,则由热化学方程式可知,氢
气燃烧热 ,故A正确;B项,由题意可知,氢氧燃料电池
中化学能转化为热能和电能,由能量守恒定律可知,2molH 和1 molO ,在燃料电池中完全反应,电功
2 2
+放热量=571.6kJ,故B正确;C项,氢气是易燃易爆的气体,难于安全储存与运输,所以氢能利用的关键
技术在于安全储存与运输,故C正确;D项,不同电极材料电解水所需电压不同,说明所需的电流不同,
所以产生2g氢气所需时间不同,消耗的电功不同,故D错误;故选D。
2.(2024· 重庆卷,13,3分)二氧化碳甲烷重整是CO 资源化利用的重要研究方向,涉及的主要热化
2
学方程式有:
①CO(g)+CH(g) 2CO(g)+2H(g) ΔH =+247kJ·mol−1
2 4 2 1
②CO(g)+H(g) C(s)+HO(g) ΔH =-131kJ·mol−1
2 2 2
③CO(g)+2H(g) C(s)+2HO(g) ΔH =-90kJ·mol−1
2 2 2 3
已知H-H键能为a kJ·mol−1, 键能为b kJ·mol−1, 键能为c kJ·mol−1,则CO(g)中的碳氧键键
能(单位: kJ·mol−1)为( )
A. B.
C. D.
【答案】B【解析】根据盖斯定律反应①+②-③可得反应:CH(g)+HO(g) CO(g)+3H(g),该反应
4 2 2
,根据ΔH=反应物键能和-生成
物键能和可得:ΔH =4c+2b-3a- CO(g)中的碳氧键键能=206,CO(g)中的碳氧键键能=( )
,故B正确;故选B。
3.(2024·江苏卷,5,3分)催化剂能改变化学反应速率而不改变反应的焓变,常见倠化剂有金属及其
氧化物、酸和碱等。倠化反应广泛存在,如豆科植物固氮、石墨制金刚石、CO 和H 制CHOCH (二甲醚)、
2 2 3 3
VO 倠化氧化SO 等。催化剂有选择性,如C H 与O 反应用Ag催化生成 (环氧乙烷)、用
2 5 2 2 4 2
CuCl /PdCl 催化生成CHCHO。催化作用能消除污染和影响环境,如汽车尾气处理、废水中NO -电倠化生
2 2 3 3
成N 、氯自由基催化O 分解形成臭氧空洞。我国在石油催化领域领先世界,高效、经济、绿色是未来催
2 3
化剂研究的发展方向。下列说法正确的是( )
A.豆科植物固氮过程中,固氮酶能提高该反应的活化能
B.C H 与O 反应中,Ag催化能提高生成CHCHO的选择性
2 4 2 3
C.HO 制O 反应中,MnO 能加快化学反应速率
2 2 2 2
D.SO 与O 反应中,VO 能减小该反应的焓变
2 2 2 5
【答案】C
【解析】A项,固氮酶是豆科植物固氮过程的催化剂,能降低该反应的活化能,A错误;B项,根据
题意,催化剂有选择性,如C H 与O 反应用Ag催化生成 (环氧乙烷)、用CuCl /PdCl 催化生
2 4 2 2 2
成CHCHO,则判断Ag催化不能提高生成CHCHO的选择性,B错误;C项,MnO 是HO 制O 反应的
3 3 2 2 2 2
催化剂,能加快化学反应速率,C正确;D项,VO 是SO 与O 反应的催化剂,能加快反应速率,但不能
2 5 2 2
改变该反应的焓变,D错误;故选C。
反应热及其测定——反应热与焓变——反应热的微观实质——反应热的表示(热化学方程式)——反
应热示例(燃烧热)1 .化学 反应的热效应
2 . 反应热的计算方法
(1)利用热化学方程式进行有关计算
根据已知的热化学方程式、已知的反应物或生成物的物质的量、反应吸收或放出的热量,可以把反应
热当作“产物”,计算反应放出或吸收的热量。
(2)根据燃烧热数据,计算反应放出的热量
计算公式:Q=燃烧热×n(可燃物的物质的量)。
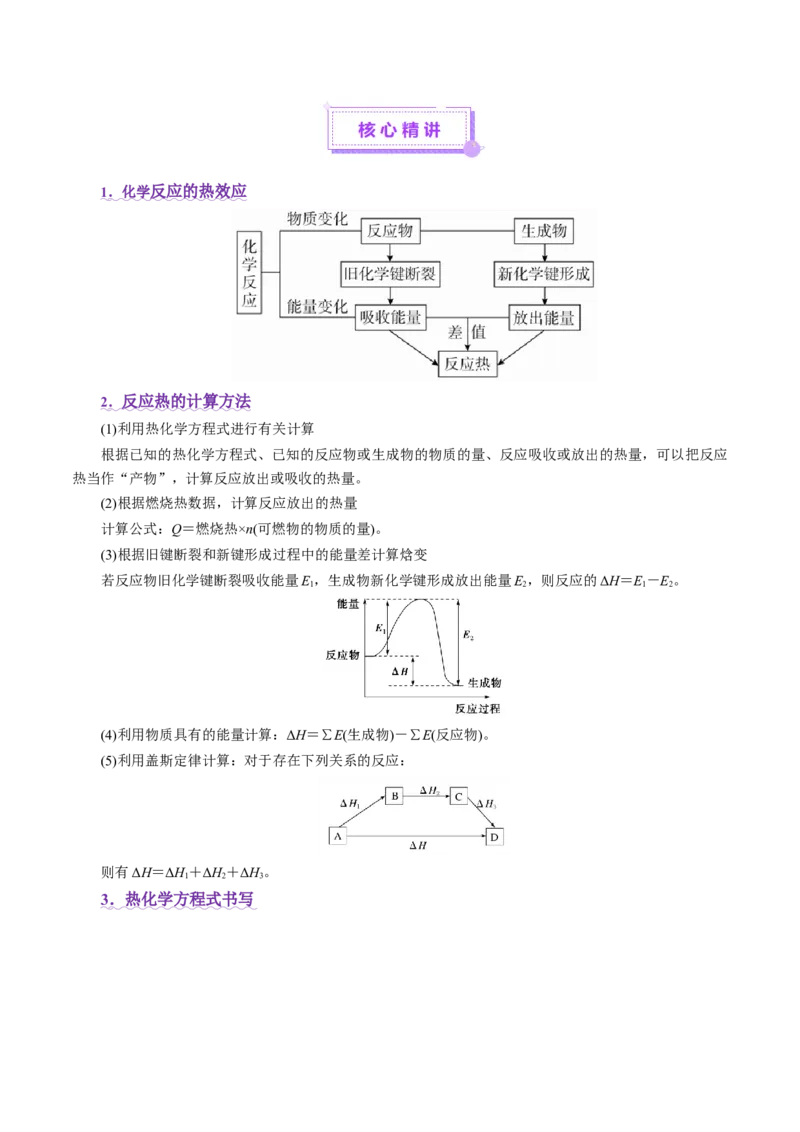
(3)根据旧键断裂和新键形成过程中的能量差计算焓变
若反应物旧化学键断裂吸收能量E,生成物新化学键形成放出能量E,则反应的ΔH=E-E。
1 2 1 2
(4)利用物质具有的能量计算:ΔH=∑E(生成物)-∑E(反应物)。
(5)利用盖斯定律计算:对于存在下列关系的反应:
则有ΔH=ΔH+ΔH+ΔH。
1 2 3
3 .热化学方程式书写【易错警示】
(1)注明反应的温度和压强(25 ℃、101 kPa下进行的反应可不注明)。
(2)注明反应物和生成物的状态:固态(s)、液态(l)、水溶液(aq)、气态(g)。
(3)热化学方程式中各物质的化学计量数只表示物质的物质的量,而不表示分子个数(或原子个数),因
此可以写成分数。
(4)热化学方程式中不用“↑”和“↓”。
(5)由于ΔH与反应物的物质的量有关,所以热化学方程式中物质的化学计量数必须与 ΔH相对应,如
果化学计量数加倍,则ΔH也要加倍。当反应向逆反应方向进行时,其反应热与正反应的反应热数值相等
符号相反。
考向 1 反应过程中的能量变化
1.化学反应H(g)+Cl(g)===2HCl(g)的反应过程如图所示。下列说法错误的是
2 2
A.过程①、②均放出热量
B.光照和点燃条件下的反应热是相同的
C.H(g)+Cl(g)===2HCl(g) ΔH=-183 kJ·mol-1
2 2
D.2mol气态氢原子的能量高于1mol氢气的能量
【答案】A
【解析】A项,过程①为化学键断裂的过程,需要吸收能量,A错误;B项,反应热和反应物、生成物的能量有关,光照和点燃条件下的反应热是相同的,B正确;C项,由图可知,1mol氢气、氯气反应生
成2mol氯化氢气体放出热量862kJ-679kJ=183kJ,故反应热化学方程式为H(g)+Cl(g)===2HCl(g) ΔH=
2 2
-183 kJ·mol-1,C正确;D项,由图可知,2mol气态氢原子的能量高于1mol氢气的能量,D正确。故选
A。
2.已知:①CH(g)+2O(g)=CO (g)+2HO(g)ΔH=-802.3 kJ·mol-1
4 2 2 2 1
②H(g)+Cl (g)=2HCl(g)ΔH=-184.6 kJ·mol-1
2 2 2
③C(s)+ O(g)=CO(g )ΔH=-110.5 kJ·mol-1
2 3
④2SO (g)+O(g) 2SO (g)ΔH=-197.8kJ·mol-1
2 2 3 4
下列说法正确的是( )
A.CH 的燃烧热ΔH为—802.3kJ· mol-1
4
B.1 mol C完全燃烧放出的热量大于110.5kJ
C.1 g H 在Cl 中完全燃烧放出184.6kJ的热量
2 2
D.一定条件下,2 mol SO 与足量O 充分反应放出197.8kJ的热量
2 2
【答案】B
【解析】A项,甲烷的燃烧热为1mol甲烷完全燃烧生成二氧化碳和液态水放出的热量,由反应①可知,
甲烷的燃烧热ΔH小于-802.3kJ· mol-1,故A错误;B项,由反应③可知,1mol碳完全燃烧生成二氧化碳放
出的热量大于110.5kJ,故B正确;C项,由反应②可知,1g氢气在氯气中完全燃烧放出的热量为
×184.6kJ/mol=92.3kJ,故C错误;D项,由反应④可知,二氧化硫转化为三氧化硫的反应为可逆反应,可
逆反应不可能完全反应,则一定条件下,2 mol二氧化硫与足量氧气充分反应放出的热量小于197.8kJ,故
D错误;故选B。
3.根据以下热化学方程式,ΔH 和ΔH 的大小比较错误的是( )
1 2
A.Br (g)+H(g)=2HBr(g) ΔH ,Br (l)+H (g)=2HBr(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 2 1 2
B.2HS(g)+3O(g)=2SO(g)+2HO(l) ΔH ,2HS(g)+O(g)=2S(s)+2HO(l) ΔH ,则有ΔH>ΔH
2 2 2 2 1 2 2 2 2 1 2
C.4Al(s)+3O (g)=2Al O(s) ΔH ,4Fe(s)+3O (g)=2Fe O(s) ΔH ,则有ΔH<ΔH
2 2 3 1 2 2 3 2 1 2
D.C(s)+O(g)=CO (g) ΔH ,C(s)+O(g)=CO(g) ΔH ,则有ΔH<ΔH
2 2 1 2 2 1 2
【答案】B
【解析】A项,依据盖斯定律分析,液态溴变化为气态溴需要吸收热量,反应是放热反应,焓变是负
值,所以△H<△H,A正确;B项,S燃烧生成二氧化硫放热,反应是放热反应,焓变是负值,所以
1 2
△H<△H,B错误;C项,铝活泼性大于铁,能量高于铁,反应是放热反应,焓变是负值,△H<
1 2 1
△H,C正确;D项,碳完全燃烧放出的热量大于不完全燃烧生成CO放出的热量,反应是放热反应,焓
2变是负值,所以△H<△H,D正确;故选B。
1 2
4.以CO和H 为原料合成甲醇是工业上的成熟方法,直接以CO 为原料生产甲醇是目前的研究热点。
2 2
我国科学家用CO 人工合成淀粉时,第一步就需要将CO 转化为甲醇。
2 2
已知:①CO(g)+2H(g)=CH OH(g) ΔH =-90.5kJ/mol
2 3 1
CO(g)+HO(g)=CO(g)+H(g) ΔH =-41.1kJ/mol
2 2 2 2
2H(g)+ O (g)=2HO(g) ΔH =-483.6kJ/mol
② 2 2 2 3
③
下列说法不正确的是( )
A.若温度不变,反应①中生成1 mol CH OH(l)时,放出的热量大于90.5 kJ
3
B.CO 与H 合成甲醇的热化学方程式为:CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=-49.4kJ/mol
2 2 2 2 3 2
C.通过电解制H 和选用高效催化剂,可降低CO 与H 合成甲醇反应的焓变
2 2 2
D.以CO 和HO为原料合成甲醇,同时生成O,该反应需要吸收能量
2 2 2
【答案】C
【解析】A项,1mol CHOH(g)能量高于 1mol CHOH(l),反应物的总能量相同,根据能量守恒定律,
3 3
若温度不变,反应国中生成1mol CHOH(l)时,放出的热量大于90.5kJ,故 A 正确;B项,根据盖斯定律,
3
①—②得CO(g)+3H(g)=CH OH(g)+H O(g) ΔH=ΔH -ΔH =-49.4kJ/mol,故B正确;C项,催化剂可降低
2 2 3 2 1 1
CO 与H 合成甲醇反应的活化能,但不改变反应的焓变,故C错误;D项,已知反应④CO(g)
2 2 2
+3H (g)=CH OH(g)+H O(g) ΔH=-49.4kJ/mol,根据盖斯定律④×2— ×3得2CO(g)+4HO(g)=2CHOH(g)
2 3 2 2 2 3
+3O
2
(g) ΔH=2ΔH
4
-3ΔH
3
=1352kJ/mol>0,,则该反应需要吸收能量③,故 D 正确;故选C。
考向 2 热化学方程式
5.燃烧热指 时, 纯物质完全燃烧生成指定产物时所放出的热量,如C转化为CO(g)、H
2 2
转化为HO(l)。已知丙烷的燃烧热ΔH=-2219.9kJ·mol-1,下列有关丙烷的说法正确的是( )
2
A.丙烷的燃烧反应中,反应物的焓小于生成物的焓
B.C H(g)+7O(g)=6CO(g)+8HO(l) ΔH=-4439.8kJ·mol-1
3 8 2 2
C.C H(g)+5O(g)=3CO (g)+4HO(g) ΔH=-2219.9kJ·mol-1
3 8 2 2 2
D.甲烷的燃烧热ΔH=-890kJ·mol-1,等质量的甲烷、丙烷完全燃烧甲烷放出的热量多
【答案】D
【解析】A项,燃烧为放热反应,焓变为负值,则丙烷的燃烧反应中,反应物的焓大于生成物的焓,
A错误; B项,烷烃的标准燃烧热所指的稳定氧化物是指CO 气体和液态水,反应中为CO气体,B错误;
2
C项,烷烃的标准燃烧热所指的稳定氧化物是指CO 气体和液态水,反应中为气态水,C错误;D项,在
2
101kPa下,甲烷的热值是890.0kJ/mol÷16g/mol=55.625kJ/g,在101kPa下,丙烷的热值是2219.9kJ/
mol÷44g/mol=50.452kJ/g,则等质量的甲烷、丙烷完全燃烧甲烷放出的热量多,D正确;故选D。
6.在25℃和101kPa下,2gH 燃烧生成液态水放出285.8kJ的热量,则下列热化学方程式中书写正确
2
的是A.2H(g)+O(g)=2HO(l) ΔH=-142.9kJ/mol B.H(g)+ O(g)=HO(l) ΔH=-285.8kJ/mol
2 2 2 2 2 2
C.2H(g)+O(g)=2HO(g) ΔH=-571.6kJ/mol D.H(g)+ O(g)=2HO(l) ΔH=+285.8kJ/mol
2 2 2 2 2 2
【答案】B
【解析】A项,1molH 完全燃烧生成液态水放热285.8kJ,则2molH 完全燃烧生成液态水放热
2 2
571.6kJ,A不正确;B项,1molH 完全燃烧生成液态水放热285.8kJ,则热化学方程式为H(g)+
2 2
O(g)=HO(l) ΔH=-285.8kJ/mol,B正确;C项,由题意知,H 燃烧生成液态水,而不是气态水,所以
2 2 2
2H(g)+O(g)=2HO(g) ΔH>-571.6kJ/mol,C不正确;D项,H 燃烧放出热量,而不是吸收热量,所以ΔH
2 2 2 2
<0,D不正确;故选B。
7.根据如图所给信息,得出的结论正确的是( )
A.48 g碳完全燃烧放出热量为1 574 kJ/mol
B.2C(s)+O(g)===2CO(g) ΔH=-221.0 kJ/mol
2
C.2CO(g)===2CO(g)+O(g) ΔH=+283.0 kJ/mol
2 2
D.C(s)+O(g)===CO (s) ΔH=-393.5 kJ/mol
2 2
【答案】B
【解析】48 g C完全燃烧放热为393.5 kJ/mol×4 mol=1 574 kJ,不是1 574 kJ/mol,故A错误;据图示
可知,1 mol C燃烧生成CO放热393.5 kJ-283.0 kJ=110.5 kJ,所以2 mol C燃烧生成CO放热221.0 kJ,
故B正确;1 mol CO燃烧生成1 mol二氧化碳放热283.0 kJ,所以2CO(g)===2CO(g)+O(g) ΔH=+
2 2
566.0 kJ/mol,故C错误;应该生成二氧化碳气体,不是固态,故D错误。
8.[新题型](2025·湖南省三湘名校教育联盟高三第二次大联考)标准状态下,下列物质气态时的相对能
量如下表:物质( ) O H HO HOO H O HO HO
2 2 2 2 2
能量
249 218 39 10 0 0
已知:HO 中氧氧单键的键能为214 kJ·mol−1。下列说法正确的是( )
2 2
A.O 的键能为249 kJ·mol−1
2
B.表中的X=-136
C.HO(g)=2H(g)+O(g) ΔH=-242kJ·mol−1
2
D.H(g)+1/2O (g)=HO(l) ΔH=-242kJ·mol−1
2 2 2
【答案】B
【解析】A项,已知键能是指气态分子中1 mol化学键解离而生成气态原子所吸收的能量。根据表格
中的数据可知,O 的键能为2×249kJ·mol−1=498kJ·mol−1,A项错误;B项,反应HO(g)+HO(g)=H O(g)的
2 2 2
过程中形成氧氧单键,即HO(g)+HO(g)=H O(g) ΔH=-214kJ·mol−1,ΔH=生成物的总能量-反应物的总能
2 2
量 ,X=-136,B项正确;C项,水分解应该属于吸热过程,C项错误;
D项,依题意可得,H(g)+1/2O (g)=HO(g) ΔH=-242kJ·mol−1,D项错误;故选B。
2 2 2
题型二 盖斯定律及其应用
1.(2024·福建卷,14节选)SiHCl 是制造多晶硅的原料,可由 Si和SiCl 耦合加氢得到,相关反应如
3 4
下:
Ⅰ.SiCl (g)+H(g)= SiHCl (g)+HCl(g) ΔH =52kJ·mol−1
4 2 3 1
Ⅱ.Si(s)+3HCl(g)= SiHCl (g)+H(g) ΔH =-236kJ·mol−1
3 2 2
Ⅲ.Si(s)+SiCl (g)+2H(g)=2SiH Cl(g) ΔH =16kJ·mol−1
4 2 2 2 3
(1)生成SiHCl 的总反应:
3
Ⅳ.Si(s)+3SiCl (g)+2H(g)=4SiHCl (g) ΔH =______kJ·mol−1
4 2 3 4
【答案】(1)-80
【解析】(1)根据盖斯定律可知,ΔH=ΔH+3ΔH =-236kJ·mol−1+3×(+52kJ·mol−1)=-80kJ·mol−1。
4 2 1
2.(2024·江西卷,16节选)石油开采的天然气含有HS。综合利用天然气制氢是实现“碳中和”的重
2
要途径。CH 和HS重整制氢的主要反应如下:
4 2
反应Ⅰ:CH(g)+2HS(s) CS(g)+4H(g) ΔH =+260kJ/mol
4 2 2 2 1
反应Ⅱ:CH(g) C(s)+2H(g) ΔH =+90kJ/mol
4 2 2反应Ⅲ:2HS(g) S(g)+2H(g) ΔH =+181kJ/mol
2 2 2 3
回答下列问题:
(2)反应Ⅳ:CS(g) S(g)+C(s)ㅤΔH=_______kJ/mol。
2 2 4
【答案】(2)+11
【解析】 (2)根据盖斯定律可知,反应Ⅱ+Ⅲ﹣Ⅰ=Ⅳ,则CS(g) S(g)+C(s)ㅤΔH=ΔH+ΔH ﹣
2 2 4 2 3
ΔH=(90+181-260)kJ/mol=+11kJ/mol。
1
3.(2024·安徽卷,17,15节选)乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。
回答下列问题:
(1) C H 氧化脱氢反应:
2 6
2C H(g)+O(g)=2C H(g)+2HO(g) ΔH =-209.8kJ·mol−1
2 6 2 2 4 2 1
C H(g)+CO(g)=C H(g)+2HO(g)+ CO(g) ΔH =178.1kJ·mol−1
2 6 2 2 4 2 2
计算:2CO(g)+O(g) 2CO(g) ΔH =_______kJ·mol−1
2 2 3
【答案】(1)-566
【解析】(1)将两个反应依次标号为反应①和反应②,反应①-反应②×2可得目标反应,则ΔH=ΔH -
3 1
2ΔH=(-209.8-178.1×2)kJ/mol=-566kJ/mol。
2
4.(2024·广西卷,17节选)二氯亚砜(SOCl)是重要的液态化工原料。回答下列问题:
2
(1)合成SOCl 前先制备SCl。有关转化关系为:
2 2
的
则S(s)+Cl(g)=SCl(l) ΔH=_______ kJ·mol−1。
2 2 3
【答案】(1)-50
【 解 析 】 (1) 由 盖 斯 定 律 可 知 , 2S(s) + 2Cl(g)=2SCl(l) 的 焓 变 为
2 2
, 则 S(s) + Cl(g)=SCl(l) 的
2 2
。1 .盖斯定律
(1)内容:一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。
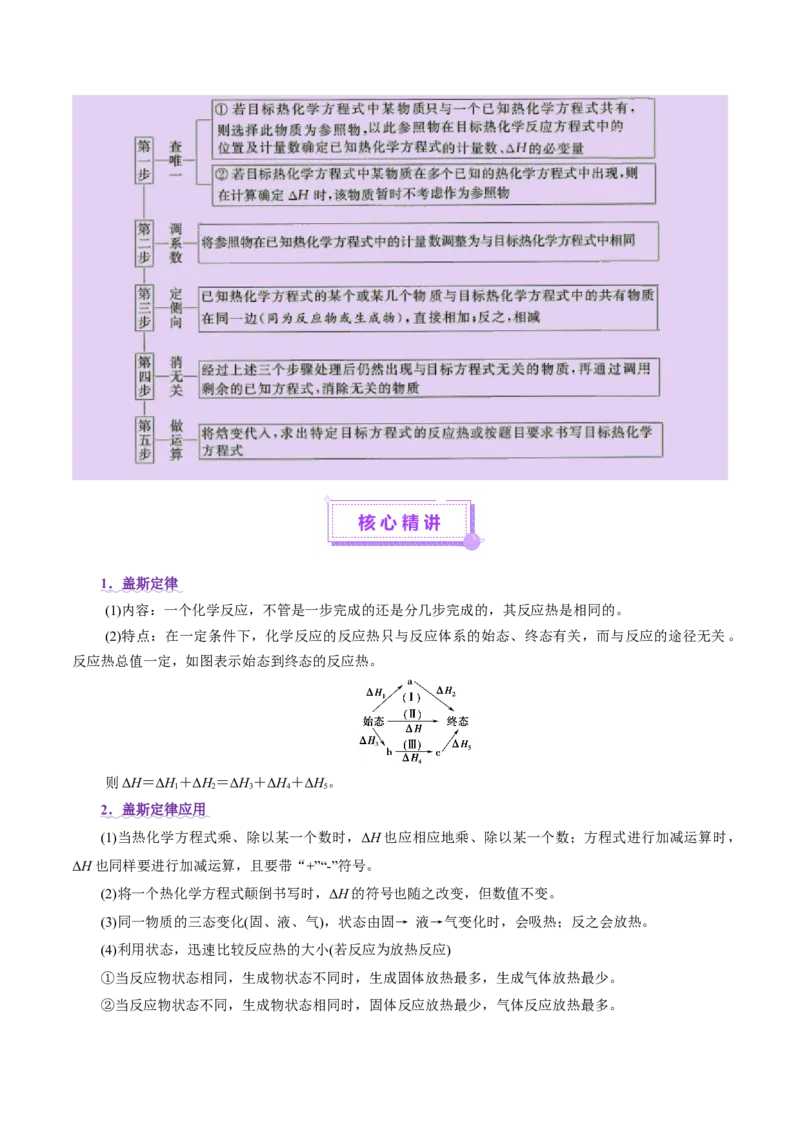
(2)特点:在一定条件下,化学反应的反应热只与反应体系的始态、终态有关,而与反应的途径无关。
反应热总值一定,如图表示始态到终态的反应热。
则ΔH=ΔH+ΔH=ΔH+ΔH+ΔH。
1 2 3 4 5
2 .盖斯定律应用
(1)当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,
ΔH也同样要进行加减运算,且要带“+”“-”符号。
(2)将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。
(3)同一物质的三态变化(固、液、气),状态由固→ 液→气变化时,会吸热;反之会放热。
(4)利用状态,迅速比较反应热的大小(若反应为放热反应)
①当反应物状态相同,生成物状态不同时,生成固体放热最多,生成气体放热最少。
②当反应物状态不同,生成物状态相同时,固体反应放热最少,气体反应放热最多。③在比较反应热(ΔH)的大小时,应带符号比较。对于放热反应,放出的热量越多,ΔH反而越小。
1.在一定温度压强下,依据图示关系,下列说法不正确的是( )
A.C(石墨)+ CO (g) =2CO(g) ΔH=ΔH-ΔH
2 1 2
B.1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g) ,前者放热多
2 2
C.ΔH=ΔH-ΔH
5 1 3
D.化学反应的△H,只与反应体系的始态和终态有关,与反应途径无关
【答案】B
【解析】A项,由题干信息可知,反应I:C(石墨)+ (g)=CO(g) ΔH 反应II:CO(g)+
1
(g)=CO (g) ΔH,则反应I-反应II得C(石墨)+ CO (g) =2CO(g),根据盖斯定律可知ΔH=ΔH-ΔH,A正确;
2 2 2 1 2
B项,由题干信息可知,C(石墨)= C(金刚石) ΔH<0,即1molC(石墨)具有的总能量低于1molC(金刚石),
5
则1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g),后者放热多,B错误;C项,由
2 2
题干信息可知,反应I:C(石墨)+ (g)=CO(g) ΔH,反应III:C(金刚石)+ (g)=CO(g) 则反应I-反应
1
III得C(石墨)= C(金刚石),根据盖斯定律可知,ΔH=ΔH-ΔH,C正确;D项,根据盖斯定律可知,化学
5 1 3
反应的△H,只与反应体系的始态和终态有关,与反应途径无关,D正确;故选B。
2.2 mol金属钠和l mol氯气反应的能量关系如图所示,下列说法不正确的是( )
A.原子失电子为吸热过程,相同条件下,K(s)的( H'+△H')-( H+△H)
2 3 4 5 6 7
D.2Na(s)+Cl
2
(g)=2NaCl(s)在较低△温度下自发进行
【答案】C
【解析】A项,原子失电子为吸热过程,相同条件下,K与Na同一主族,电离能同主族从上到下逐渐
减小,K(s)的( H'+△H')0,d<0 D.d=b+c,d<0
【答案】B
【解析】A项,根据③式是电离方程式,③= - ,ΔH=c=a-b,由于a②0。故C不正确。D项,反应④是反应①的逆过程,故d=-
a>0。故不正确。故选B。
4.已知[ΔH、ΔH、ΔH 对应的反应中O(g)已省略,且ΔH>ΔH]:
2 3 5 2 2 5
下列说法正确的是( )
A.ΔH>0 B.ΔH 的值是CHCHCHCH(g)的燃烧热
1 3 3 2 2 3C.ΔH+ΔH=ΔH+ΔH D.稳定性:正丁烷>异丁烷
1 2 3 4
【答案】C
【解析】A项,ΔH、ΔH 分别表示异丁烷与正丁烷的燃烧热,若ΔH>ΔH,说明燃烧1 mol两种物
2 3 2 5
质时前者释放的热量较后者少,由此知异丁烷的能量较低,则正丁烷转化为异丁烷是放热反应,故A错误;
B项,燃烧热是1mol纯物质完全燃烧生成指定产物时放出的热量,含H元素的物质燃烧生成的指定产物为
液态水,所以ΔH 的值不是正丁烷的燃烧热,故B错误;C项,ΔH+ΔH 和ΔH+ΔH 的始态和终态相同,
3 1 2 3 4
由盖斯定律可知,ΔH+ΔH=ΔH+ΔH,故C正确;D项,相同条件下,能量越低越稳定,则稳定性:正丁
1 2 3 4
烷<异丁烷,故D错误;故选C。
5.天然气使用前需要脱硫,发生下列反应:
①HS(g)+ O(g)=SO(g)+HO(g) H
2 2 2 2 1
△
②2HS(g)+SO (g)= S(g)+2HO(g) H
2 2 2 2 2
△
③HS(g)+ O(g)=S(g)+HO(g) H
2 2 2 3
△
④2S(g)=S(g) H
2 4
则△H 的正确表达式为( )
4 △
A.△H= ( H+△H-3 H) B.△H= (3 H- H- H)
4 1 2 3 4 3 1 2
△ △ △ △ △
C.△H= ( H- H+3 H) D.△H= ( H- H-3 H)
4 1 2 3 4 1 2 3
△ △ △ △ △ △
【答案】A
【解析】根据盖斯定律,①× -③× 得⑤: S(g)+ O(g)= SO (g) H= ( H- H);根据盖斯
2 2 5 1 3
△ △ △
定律,②× -③× 得⑥: SO (g)+ S(g)= O(g) + S (g) H= ( H-2 H);⑤+⑥得:2S(g) =S (g)
2 2 2 6 2 3 2
△ △ △
H= ( H+ H-3 H),故选A。
4 1 2 3
△ △ △ △6.在一定条件下,Xe(g)与F(g)反应生成XeF (g)(n=2,4,6)的平衡气体。 时主要为XeF (g),
2 n 6
时主要为XeF (g),高温时生成XeF (g)。其变转化关系如下:
4 2
下列说法不正确的是( )
A.ΔH<0,ΔH<0 B.ΔH-ΔH=ΔH C.ΔH>0 D.ΔH-ΔH=ΔH-ΔH
1 5 5 4 3 3 4 6 1 3
【答案】C
【解析】A项,根据图示可知,ΔH 对应的反应Xe(g)+F(g) XeF (g)和ΔH 对应的反应
1 2 2 5
Xe(g)+3F(g) XeF (g)都是化合反应,一般化合反应是放热的,所以ΔH<0,ΔH<0,故A正确;B
2 6 1 5
项,ΔH 对应的反应是Xe(g)+3F(g) XeF (g),ΔH 对应的反应是Xe(g)+2F(g) XeF (g),ΔH
5 2 6 4 2 4 3
对应的反应是XeF (g)+F (g) XeF (g),Xe(g)+3F(g) XeF (g)和Xe(g)+2F(g) XeF (g)相
4 2 6 2 6 2 4
减即可得到反应XeF (g)+F (g) XeF (g),所以ΔH-ΔH=ΔH,故B正确;C项,ΔH 对应的反应
4 2 6 5 4 3 3
XeF (g)+F (g) XeF (g)是化合反应,一般化合反应是放热的,所以ΔH<0,故C错误;D项,ΔH
4 2 6 3 4
对应的反应是Xe(g)+2F(g) XeF (g),ΔH 对应的反应是XeF (g)+2F (g) XeF (g),两反应相减
2 4 6 2 2 6
得到反应Xe(g)+XeF(g) XeF (g)+XeF(g);ΔH 对应的反应是Xe(g)+F(g) XeF (g),ΔH 对应
6 4 2 1 2 2 3
的反应是XeF (g)+F (g) XeF (g),两反应相减也得到反应Xe(g)+XeF(g) XeF (g)+XeF(g),所
4 2 6 6 4 2
以ΔH-ΔH=ΔH-ΔH,故D正确;故选C。
4 6 1 3
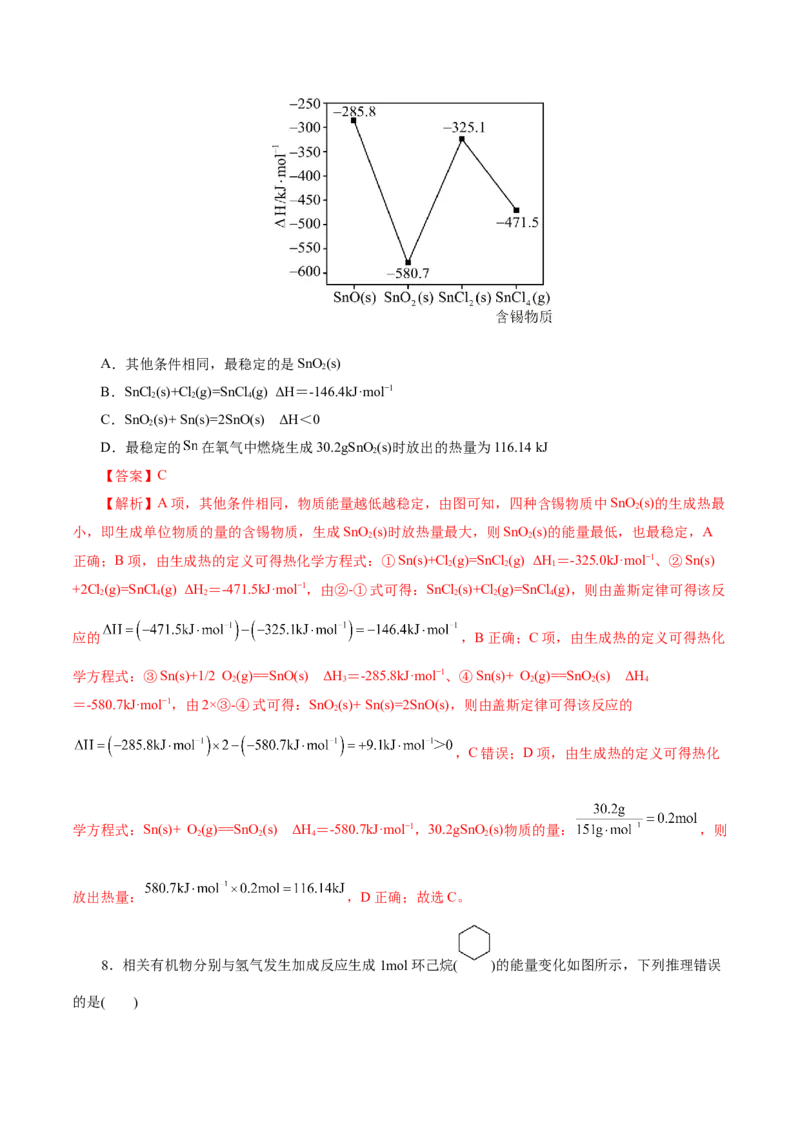
7.[新考法](2025·陕西省部分学校高三质检)生成热是指由标准状况(101kPa,273K)下最稳定单质生成
标准状况下单位物质的量的化合物的热效应或焓变(ΔH)。最稳定的单质的标准生成热规定为零。几种含锡
物质的生成热如图所示。下列叙述错误的是( )A.其他条件相同,最稳定的是SnO(s)
2
B.SnCl(s)+Cl(g)=SnCl(g) ΔH=-146.4kJ·mol−1
2 2 4
C.SnO(s)+ Sn(s)=2SnO(s) ΔH<0
2
D.最稳定的 在氧气中燃烧生成30.2gSnO(s)时放出的热量为116.14 kJ
2
【答案】C
【解析】A项,其他条件相同,物质能量越低越稳定,由图可知,四种含锡物质中SnO (s)的生成热最
2
小,即生成单位物质的量的含锡物质,生成SnO (s)时放热量最大,则SnO (s)的能量最低,也最稳定,A
2 2
正确;B项,由生成热的定义可得热化学方程式:①Sn(s)+Cl(g)=SnCl(g) ΔH=-325.0kJ·mol−1、②Sn(s)
2 2 1
+2Cl(g)=SnCl(g) ΔH=-471.5kJ·mol−1,由②-①式可得:SnCl(s)+Cl(g)=SnCl(g),则由盖斯定律可得该反
2 4 2 2 2 4
应的 ,B正确;C项,由生成热的定义可得热化
学方程式:③Sn(s)+1/2 O(g)==SnO(s) ΔH=-285.8kJ·mol−1、④Sn(s)+ O(g)==SnO(s) ΔH
2 3 2 2 4
=-580.7kJ·mol−1,由2×③-④式可得:SnO(s)+ Sn(s)=2SnO(s),则由盖斯定律可得该反应的
2
,C错误;D项,由生成热的定义可得热化
学方程式:Sn(s)+ O(g)==SnO(s) ΔH=-580.7kJ·mol−1,30.2gSnO(s)物质的量: ,则
2 2 4 2
放出热量: ,D正确;故选C。
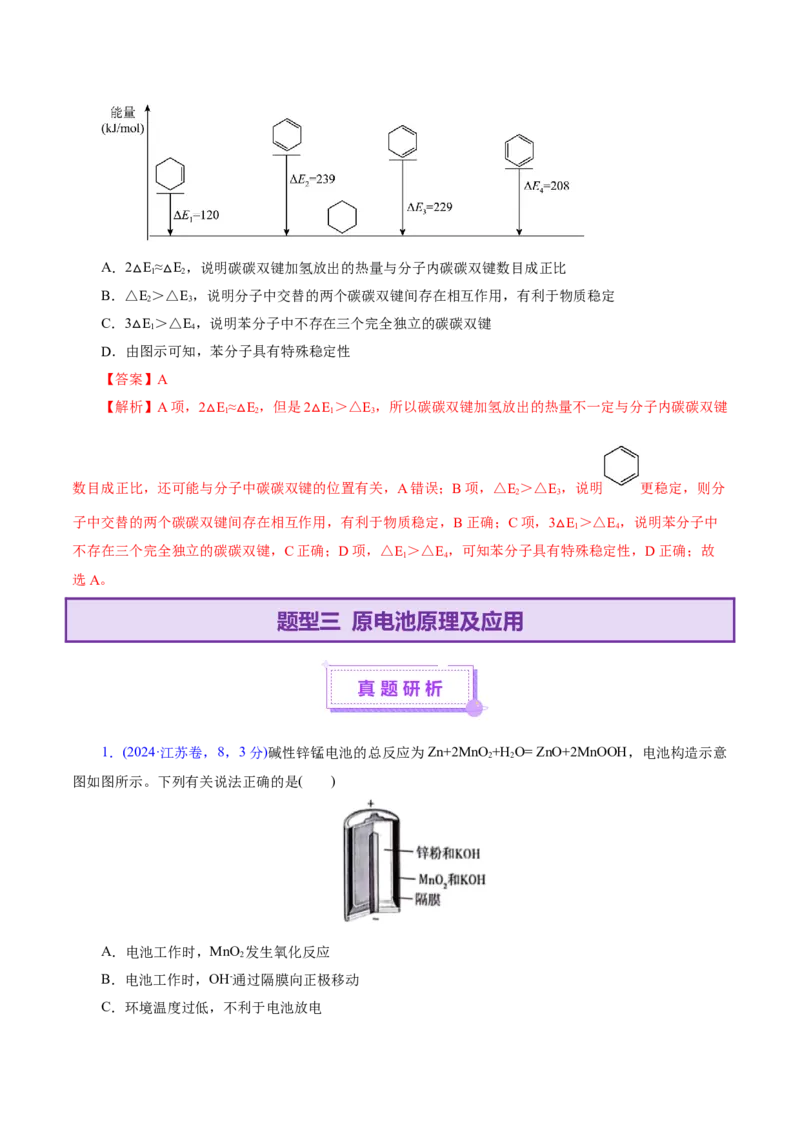
8.相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图所示,下列推理错误
的是( )A.2 E≈ E,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.△△E
2
>△△E
3
,说明分子中交替的两个碳碳双键间存在相互作用,有利于物质稳定
C.3 E>△E,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.由
△
图示可知,苯分子具有特殊稳定性
【答案】A
【解析】A项,2 E≈ E,但是2 E>△E,所以碳碳双键加氢放出的热量不一定与分子内碳碳双键
1 2 1 3
△ △ △
数目成正比,还可能与分子中碳碳双键的位置有关,A错误;B项,△E>△E,说明 更稳定,则分
2 3
子中交替的两个碳碳双键间存在相互作用,有利于物质稳定,B正确;C项,3 E>△E,说明苯分子中
1 4
不存在三个完全独立的碳碳双键,C正确;D项,△E
1
>△E
4
,可知苯分子具有△特殊稳定性,D正确;故
选A。
题型三 原电池原理及应用
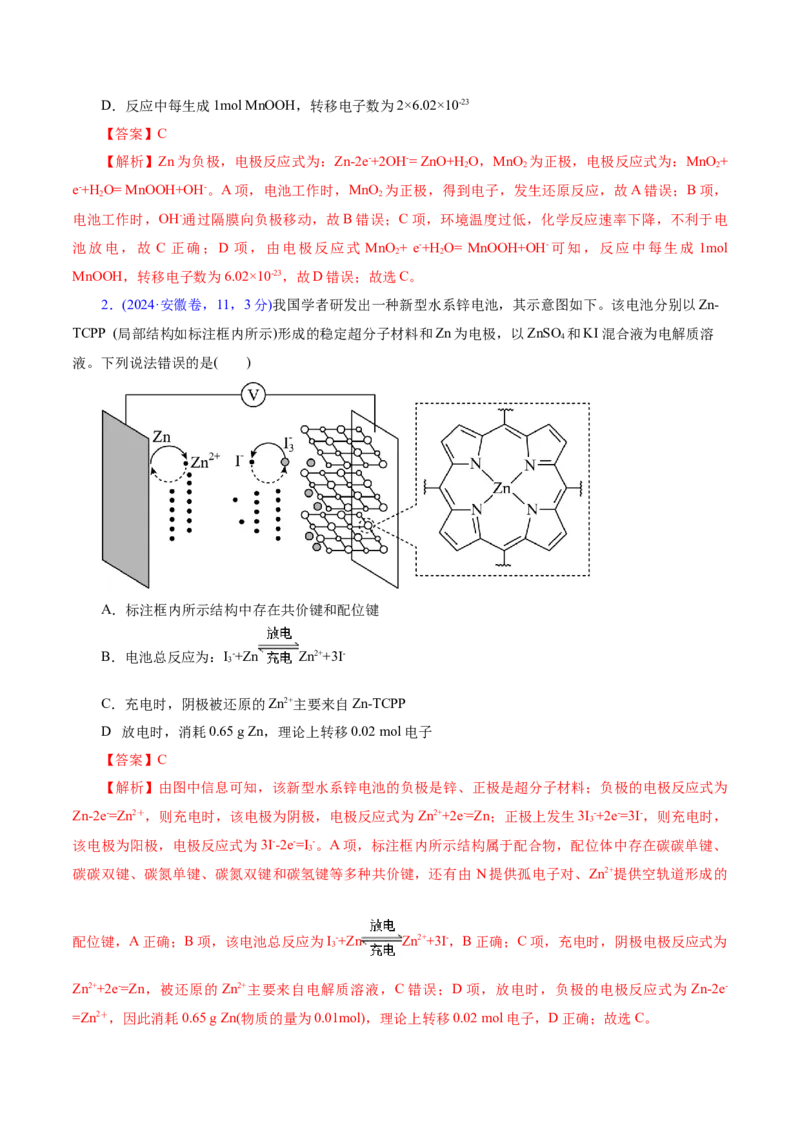
1.(2024·江苏卷,8,3分)碱性锌锰电池的总反应为Zn+2MnO +H O= ZnO+2MnOOH,电池构造示意
2 2
图如图所示。下列有关说法正确的是( )
A.电池工作时,MnO 发生氧化反应
2
B.电池工作时,OH-通过隔膜向正极移动
C.环境温度过低,不利于电池放电D.反应中每生成1mol MnOOH,转移电子数为2×6.02×10-23
【答案】C
【解析】Zn为负极,电极反应式为:Zn-2e-+2OH-= ZnO+H O,MnO 为正极,电极反应式为:MnO +
2 2 2
e-+H O= MnOOH+OH-。A项,电池工作时,MnO 为正极,得到电子,发生还原反应,故A错误;B项,
2 2
电池工作时,OH-通过隔膜向负极移动,故B错误;C项,环境温度过低,化学反应速率下降,不利于电
池放电,故 C 正确;D 项,由电极反应式 MnO + e-+H O= MnOOH+OH-可知,反应中每生成 1mol
2 2
MnOOH,转移电子数为6.02×10-23,故D错误;故选C。
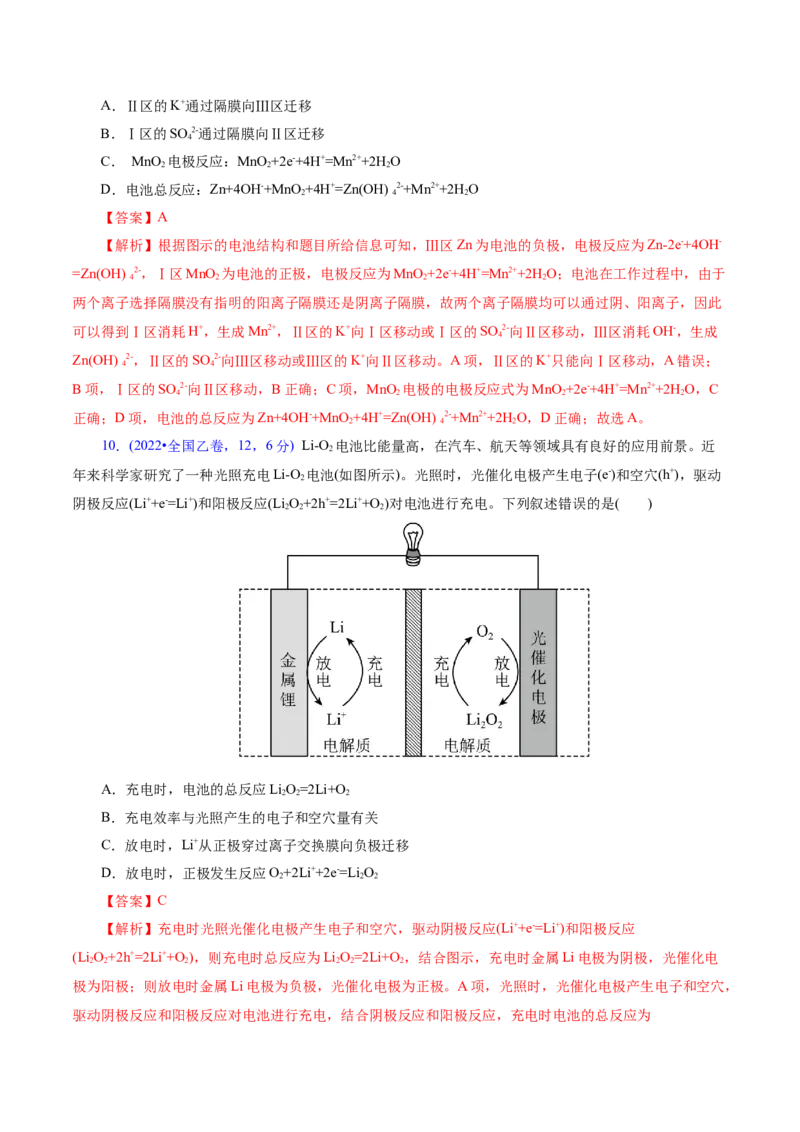
2.(2024·安徽卷,11,3分)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以Zn-
TCPP (局部结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO 和KI混合液为电解质溶
4
液。下列说法错误的是( )
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:I-+Zn Zn2++3I-
3
C.充电时,阴极被还原的Zn2+主要来自Zn-TCPP
.
D 放电时,消耗0.65 g Zn,理论上转移0.02 mol电子
【答案】C
【解析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为
Zn-2e-=Zn2+,则充电时,该电极为阴极,电极反应式为Zn2++2e-=Zn;正极上发生3I-+2e-=3I-,则充电时,
3
该电极为阳极,电极反应式为3I--2e-=I -。A项,标注框内所示结构属于配合物,配位体中存在碳碳单键、
3
碳碳双键、碳氮单键、碳氮双键和碳氢键等多种共价键,还有由 N提供孤电子对、Zn2+提供空轨道形成的
配位键,A正确;B项,该电池总反应为I-+Zn Zn2++3I-,B正确;C项,充电时,阴极电极反应式为
3
Zn2++2e-=Zn,被还原的Zn2+主要来自电解质溶液,C错误;D项,放电时,负极的电极反应式为 Zn-2e-
=Zn2+,因此消耗0.65 g Zn(物质的量为0.01mol),理论上转移0.02 mol电子,D正确;故选C。3.(2024·福建卷,9,4分)一种兼具合成功能的新型锂电池工作原理如图。电解质为含Li+有机溶液。
放电过程中产生(CFSO )NLi,充电过程中电解LiCl产生Cl。下列说法正确的是( )
3 2 2
A.交换膜为阴离子交换膜
B.电解质溶液可替换为LiCl水溶液
C.理论上每生成1molCl ,需消耗2molLi
2
D.放电时总反应:6Li+N+4CF SO Cl=2(CF SO )NLi+4LiCl
2 3 2 3 2
【答案】D
【解析】放电过程中产生(CFSO )NLi,由图可知,放电过程中氮气得到电子发生还原反应生成
3 2
LiN,LiN又转化为(CFSO )NLi和LiCl,则左侧电极为正极,右侧电极为负极。A项,放电过程中负极
3 3 3 2
锂失去电子形成锂离子,锂离子通过阳离子交换膜进入左侧生成(CFSO )NLi,A错误;B项,锂为活泼金
3 2
属,会和水反应,故电解质溶液不能为水溶液,B错误;C项,充电过程中电解LiCl失去电子发生氧化反
应产生 Cl :2Cl--2e-=Cl↑,锂离子在阴极得到电子发生还原生成锂单质:2Li++2e-=2Li,则每生成
2 2
1molCl ,同时生成2mol Li;放电过程中,消耗6molLi,同时生成4mol LiCl,则整个充放电过程来看,理
2
论上每生成1molCl ,需消耗1mol Li,C错误;D项,放电过程中,正极氮气得到电子发生还原反应生成
2
LiN,LiN 又转化为(CFSO )NLi 和 LiCl,负极锂失去电子发生氧化反应生成锂离子,总反应为
3 3 3 2
6Li+N+4CF SO Cl=2(CF SO )NLi+4LiCl,D正确;故选D。
2 3 2 3 2
4.(2024·全国甲卷,6,3分)科学家使用δ-MnO 研制了一种MnO -Zn可充电电池(如图所示)。电池工
2 2
作一段时间后,MnO 电极上检测到MnOOH和少量ZnMn O。下列叙述正确的是( )
2 2 4
A.充电时,Zn2+向阳极方向迁移
B.充电时,会发生反应Zn+2MnO =ZnMn O
2 2 4C.放电时,正极反应有MnO +H O+e-=MnOOH+OH-
2 2
D.放电时,Zn电极质量减少0.65g,MnO 电极生成了0.020molMnOOH
2
【答案】C
【解析】Zn具有比较强的还原性,MnO 具有比较强的氧化性,自发的氧化还原反应发生在Zn与
2
MnO 之间,所以MnO 电极为正极,Zn电极为负极,则充电时MnO 电极为阳极、Zn电极为阴极。A项,
2 2 2
充电时该装置为电解池,电解池中阳离子向阴极迁移,即Zn2+向阴极方向迁移,A不正确;B项,放电时,
负极的电极反应为Zn-2e-=Zn2+,则充电时阴极反应为Zn2++2e-=Zn,即充电时Zn元素化合价应降低,而
选项中Zn元素化合价升高,B不正确;C项,放电时MnO 电极为正极,正极上检测到MnOOH和少量
2
ZnMn O,则正极上主要发生的电极反应是MnO +H O+e-=MnOOH+OH-,C正确;D项,放电时,Zn电
2 4 2 2
极质量减少0.65g(物质的量为0.010mol),电路中转移0.020mol电子,由正极的主要反应MnO +H O+e-
2 2
=MnOOH+OH-可知,若正极上只有MnOOH生成,则生成MnOOH的物质的量为0.020mol,但是正极上
还有ZnMn O 生成,因此,MnOOH的物质的量小于0.020mol,D不正确;故选C。
2 4
5.(2024·全国新课标卷,6,3分)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗
血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电
池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为2C H O+O =2C H O
6 12 6 2 6 12 7
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的Na+在电场驱动下的迁移方向为b→a
【答案】C
【解析】由题中信息可知,b 电极为负极,发生反应 Cu O+2OH--2e-=2CuO+H O,然后再发生
2 2
C H O+2CuO= C H O+Cu O;a电极为正极,发生反应O+2H O+4e-=4OH-,在这个过程中发生的总反应
6 12 6 6 12 7 2 2 2
为2C H O+O =2C H O 。A项,由题中信息可知,当电池开始工作时,a电极为电池正极,血液中的O
6 12 6 2 6 12 7 2
在a电极上得电子生成OH-,电极反应式为O+2H O+4e-=4OH-;b电极为电池负极, Cu O在b电极上失
2 2 2电子转化成CuO,电极反应式为Cu O+2OH--2e-=2CuO+H O,然后葡萄糖被CuO氧化为葡萄糖酸,CuO被
2 2
还原为Cu O,则电池总反应为2C H O+O =2C H O ,A正确;B项,b电极上CuO将葡萄糖被CuO氧化
2 6 12 6 2 6 12 7
为葡萄糖酸后被还原为Cu O,Cu O在b电极上失电子转化成CuO,在这个过程中CuO的质量和化学性质
2 2
保持不变,因此,CuO 通过 Cu(Ⅱ)和 Cu(Ⅰ)相互转变起催化作用,B 正确;C 项,根据反应
2C H O+O =2C H O 可知,1mol C H O 参加反应时转移2 mol电子,18 mg C H O 的物质的量为0.1
6 12 6 2 6 12 7 6 12 6 6 12 6
mmol,则消耗18 mg葡萄糖时,理论上a电极有0.2 mmol电子流入,C错误;D项,原电池中阳离子从负
极移向正极迁移,故Na+迁移方向为b→a,D正确。故选C。
6.(2024·河北卷,13,3分)我国科技工作者设计了如图所示的可充电Mg-CO 电池,以Mg(TFSI) 为
2 2
电解质,电解液中加入1,3-丙二胺( )以捕获CO,使放电时CO 还原产物为MgC O。该设计克服了
2 2 2 4
MgCO 导电性差和释放CO 能力差的障碍,同时改善了Mg2+的溶剂化环境,提高了电池充放电循环性能。
3 2
下列说法错误的是( )
A.放电时,电池总反应为Mg+2CO= MgC O
2 2 4
B.充电时,多孔碳纳米管电极与电源正极连接
C.充电时,电子由Mg电极流向阳极,Mg2+向阴极迁移
D.放电时,每转移1mol电子,理论上可转化1mol CO
2
【答案】C
【解析】放电时CO 转化为MgC O,碳元素化合价由+4价降低为+3价,发生还原反应,所以放电时,
2 2 4
多孔碳纳米管电极为正极、Mg电极为负极,则充电时多孔碳纳米管电极为阳极、Mg电极为阴极:
电极 过程 电极反应式
放电 Mg-2e-=Mg2+
Mg电极
充电 Mg2++2e-= Mg
放电 Mg2++2CO+2e-=MgC O
2 2 4
多孔碳纳米管电极
MgC O-2e-= Mg2+
充电 2 4
+2CO ↑
2A项,放电时正极反应式为Mg2++2CO+2e-=MgC O、负极反应式为Mg-2e-=Mg2+,将放电时正、负电
2 2 4
极反应式相加,可得放电时电池总反应:Mg+2CO= MgC O,A正确;B项,充电时,多孔碳纳米管电极
2 2 4
上发生失电子的氧化反应,则多孔碳纳米管在充电时是阳极,与电源正极连接,B正确;C项,充电时,
Mg电极为阴极,电子从电源负极经外电路流向Mg电极,同时Mg2+向阴极迁移,C错误;D项,根据放电
时的电极反应式Mg2++2CO+2e-=MgC O 可知,每转移2mol电子,有2mol CO 参与反应,因此每转移
2 2 4 2
1mol电子,理论上可转化1mol CO,D正确;故选C。
2
7.(2024·广西卷,1,3分)某新型钠离子二次电池(如图)用溶解了NaPF 的二甲氧基乙烷作电解质溶液。
6
放电时嵌入PbSe中的Na变成Na+后脱嵌。下列说法错误的是( )
A.外电路通过1mol电子时,理论上两电极质量变化的差值为23g
B.充电时,阳极电极反应为:NaV(PO )-xe-=Na V(PO )+xNa+
3 2 4 3 3-x 2 4 3
C.放电一段时间后,电解质溶液中的Na+浓度基本保持不变
D.电解质溶液不能用NaPF 的水溶液替换
6
【答案】A
【解析】放电时嵌入PbSe中的Na变成Na+后脱嵌,则右侧电极为负极,Na失电子生成Na+;Na+透过
允许Na+通过的隔膜从右侧进入左侧,则左侧为正极。A项,外电路通过1mol电子时,负极有1molNa失
电子生成Na+进入右侧溶液,溶液中有1molNa+从右侧进入左侧,并与正极的Na V(PO ) 结合,则理论上
3-x 2 4 3
两电极质量变化的差值为2mol×23g/mol=46g,A错误;B项,充电时,左侧电极为阳极,NaV(PO ) 失电
3 2 4 3
子生成Na V(PO ),则阳极电极反应为:NaV(PO )-xe-=Na V(PO )+xNa+,B正确;C项,放电一段时
3-x 2 4 3 3 2 4 3 3-x 2 4 3
间后,负极产生的Na+的物质的量与负极区通过隔膜进入左极区的Na+的物质的量相同,进入左极区的
Na+与参加左侧正极反应的Na+的物质的量相同,所以电解质溶液中的Na+浓度基本保持不变,C正确;D
项,Na能与水反应,所以电解质溶液不能用NaPF 的水溶液替换,D正确;故选A。
6
8.(2024·江西卷,11,3分)我国学者发明了一种新型多功能甲醛﹣硝酸盐电池,可同时处理废水中的
甲醛和硝酸根离子(如图)。下列说法正确的是( )A.CuAg电极反应为2HCHO+2H O﹣4e﹣═2HCOO﹣+H ↑+2OH﹣
2 2
B.CuRu电极反应为NO -+6HO+8e﹣═NH ↑+9OH﹣
3 2 3
C.放电过程中,OH﹣通过质子交换膜从左室传递到右室
D.处理废水过程中溶液pH不变,无需补加KOH
【答案】B
【解析】由原电池中电子移动方向可知,CuAg为负极,HCHO失去电子生成HCOO-和H ,电极方程
2
式为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,CuRu为正极,NO -得到电子生成NH ,电极方程式为:
2 2 3 3
NO -+6HO+8e﹣═NH ↑+9OH﹣。A项,CuAg为负极,HCHO失去电子生成HCOO-和H ,根据得失电子守
3 2 3 2
恒和电荷守恒配平电极方程式为:2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,A错误;B项,CuRu为正极,
2 2
NO -得到电子生成NH ,根据得失电子守恒和电荷守恒配平电极方程式为:NO -+6HO+8e﹣═NH ↑+9OH
3 3 3 2 3
﹣,B 正确;C 项,质子交换膜只允许 H+通过,C 错误;D 项,由分析可知,负极电极方程式为:
2HCHO+4OH-﹣2e﹣═2HCOO﹣+H ↑+2H O,正极电极方程式为:NO -+6HO+8e﹣═NH ↑+9OH﹣,总反应为
2 2 3 2 3
8HCHO+ NO -+7OH-=NH↑+8HCOO-+4 H ↑+2H O,处理废水过程中消耗 OH-,溶液 pH 减小,需补加
3 3 2 2
KOH,D错误;故选B。
9.(2022•全国甲卷10,6分)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,
2
Zn2+以Zn(OH) 2-存在)。电池放电时,下列叙述错误的是( )
4A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 2-通过隔膜向Ⅱ区迁移
4
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O
2 4 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) 2-,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于
4 2 2 2
两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此
可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 2-向Ⅱ区移动,Ⅲ区消耗OH-,生成
4
Zn(OH) 2-,Ⅱ区的SO 2-向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。A项,Ⅱ区的K+只能向Ⅰ区移动,A错误;
4 4
B项,Ⅰ区的SO 2-向Ⅱ区移动,B正确;C项,MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C
4 2 2 2
正确;D项,电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O,D正确;故选A。
2 4 2
10.(2022•全国乙卷,12,6分) Li-O 电池比能量高,在汽车、航天等领域具有良好的应用前景。近
2
年来科学家研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动
2
阴极反应(Li++e-=Li+)和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是( )
2 2 2
A.充电时,电池的总反应LiO=2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应O+2Li++2e-=Li O
2 2 2
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(Li O+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化电
2 2 2 2 2 2
极为阳极;则放电时金属Li电极为负极,光催化电极为正极。A项,光照时,光催化电极产生电子和空穴,
驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为LiO=2Li+O ,A正确;充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空
2 2 2
穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;C项,放电时,金属Li电极为负极,光催
化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;D项,放电时总反应为2Li+O=Li O,正
2 2 2
极反应为O+2Li++2e-=Li O,D正确;故选C。
2 2 2
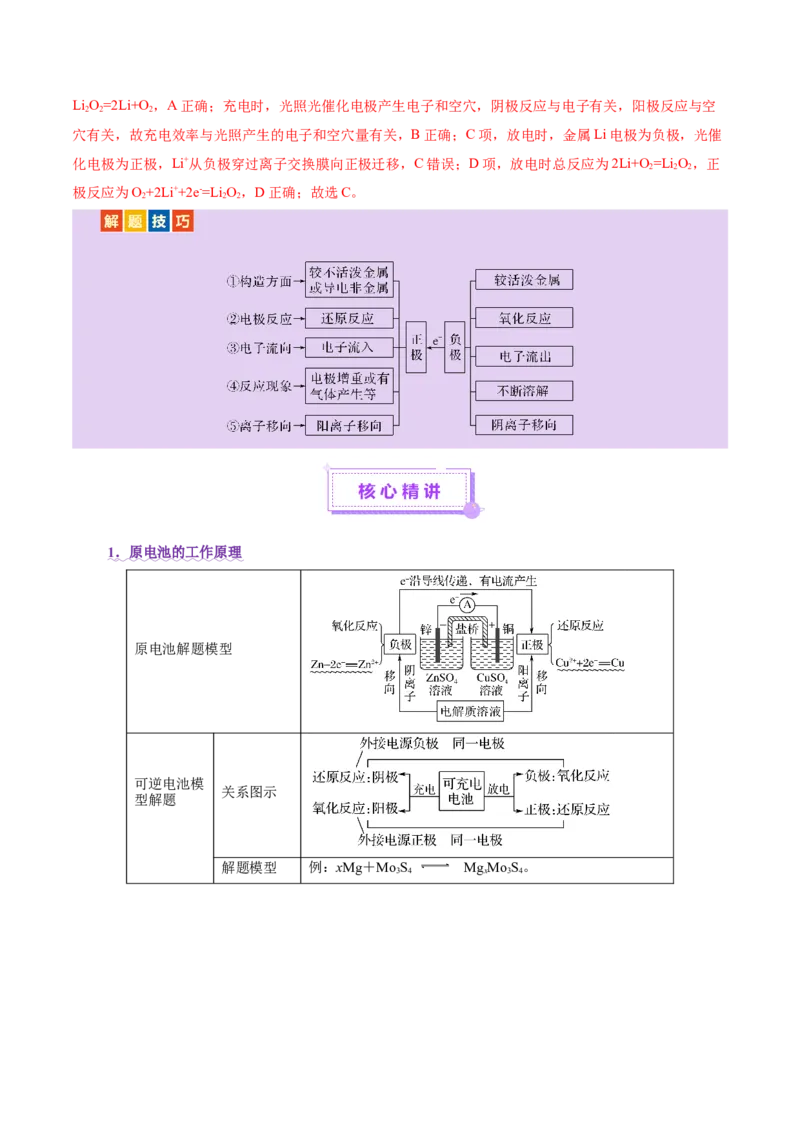
1 .原电池的工作原理
原电池解题模型
可逆电池模
关系图示
型解题
解题模型 例:xMg+MoS MgMoS。
3 4 x 3 42 .“五类”依据判断原电池电极
判断依据
电极材料 电极反应 电子流向 离子移向 电极现象
电极
负极 活泼金属 氧化反应 流出 阴离子移向 电极质量减小
不活泼金属 电极增重或质
正极 还原反应 流入 阳离子移向
或非金属 量不变
3 .“三步”突破原电池电极反应式的书写
第一步:分析氧化还原反应
根据氧化还原反应,分析元素化合价的升降,确定正负极反应物质及电子得失数目
第二步:注意电解质溶液环境
分析电解质溶液的酸碱性及离子参加反应的情况,确定电极反应,写出电极反应式
第三步:合并正、负电极反应
调整两极反应式中得失电子数目相等并叠加,消去电子,得出总反应式
4 .解答新型化学电源的步骤
(1)判断电池类型→确认电池原理→核实电子、离子移动方向。
(2)确定电池两极→判断电子、离子移动方向→书写电极反应和电池反应。
(3)充电电池→放电时为原电池→失去电子的为负极反应。
(4)电极反应→总反应离子方程式减去较简单一极的电极反应式→另一电极反应式。
1.钠离子电池因具有安全性高、能量密度大等特点而具有良好的发展前景。某钠离子电池工作原理
如图所示,下列有关说法中正确的是( )A.②表征的是放电时的电子流向
B.放电时,M极电极反应式为MoO +xe-+xNa+=Na MoO
3 x 3
C.若使用氢氧燃料电池给该电池充电,氢电极应连接M极
D.充电时,外电路中每转移0.2mole-,理论上N极将减重4.6g
【答案】B
【解析】A项,由电池的工作原理图可知放电时Na转变为Na+ ,N极为负极,M极为正极。②表征
的是充电时电子的流向,A项错误;B项,放电时,M极的电极反应式为MoO +xe-+xNa+=Na MoO ,B项
3 x 3
正确;C项,若使用氢氧燃料电池给该电池充电,氢电极应连接该电池负极,即N极,C项错误;D项,
充电时,由电子守恒可知外电路每转移0.2 mole- ,理论上N极将增重4.6 g,D项错误;故选B。
2.[原创题]《中国锂硫电池市场现状深度调研与发展趋势(2022-2028年)》主要研究分析了锂硫电池行
业市场运行态势并对锂硫电池行业发展趋势作出预测。一种锂硫电池的工作原理如图所示,其中电极a常
用掺有石墨烯的S 材料,电池反应为:16Li+xS=8Li S(2≤x≤8)。下列说法正确的是( )
8 8 2 x
下列说法中正确的是
A.放电时,锂电极的电势高
B.电解质溶液可以用无机物水溶液代替
C.电池充电时间越长,电池中的LiS 量越多
2 xD.电池工作时,外电路中流过0.2mol电子,负极材料减重1.4g
【答案】D
【解析】由电池反应16Li+xS=8Li S(2≤x≤8)可知负极锂失电子发生氧化反应,电极反应为:Li-e-
8 2 x
=Li+,Li+移向正极,所以B电极为负极,A电极为正极;原电池的正极发生还原反应:3LiS+2Li++2e-
2 8
=4Li S、2LiS+2Li++2e-=3Li S、LiS+2Li++2e-=2Li S。A项,放电时,锂电极为负极,电势低,A错误;
2 6 2 6 2 4 2 4 2 2
B项,锂化学性质活泼,能和水反应,电解质溶液不可以用无机物水溶液代替,B错误;C项,充电时A
为阳极,与放电时的电极反应相反,则充电时间越长,电池中的LiS 量就会越少,C错误;D项,负极反
2 x
应为:Li-e - =Li +,当外电路流过0.2mol电子时,消耗的锂为0.2mol,负极减重的质量为0.2mol×7g/
mol=1.4g,故D正确;故选D。
3.我国某科研团队借助氧化还原介质RM,将Li-CO 电池的放电电压提高至3V以上,该电池的工作
2
原理如图。下列说法正确的是( )
A.LiFePO 电极的电势比多孔碳电极的高
4
B.负极反应:LiFePO - xe-= Li FePO +xLi+
4 1-x 4
C.RM和 均为该电池反应的催化剂
D.LiFePO 电极每减重7 g,就有22 g CO 被固定
4 2
【答案】B
【解析】由图可知,原电池中阳离子向正极移动,则左侧电极为负极、右侧电极为正极。A项,
LiFePO 电极为负极、多孔电极为正极,故LiFePO 电极的电势比多孔碳电极的低,A错误;B项,左侧电
4 4
极为负极,LiFePO 失去电子发生氧化反应,负极反应:LiFePO - xe-= Li FePO +xLi+,B正确;C项,由
4 4 1-x 4
图可知,RM为该电池反应的催化剂, 为该电池反应的中间产物,C错误;D项,由负极电极反
应可知,LiFePO 电极每减重7 g则转移1mol电子,反应中碳元素化合价由+4变为+3,则根据电子守恒可
4
知,有1mol即44 g CO 被固定,D错误;故选B。
2
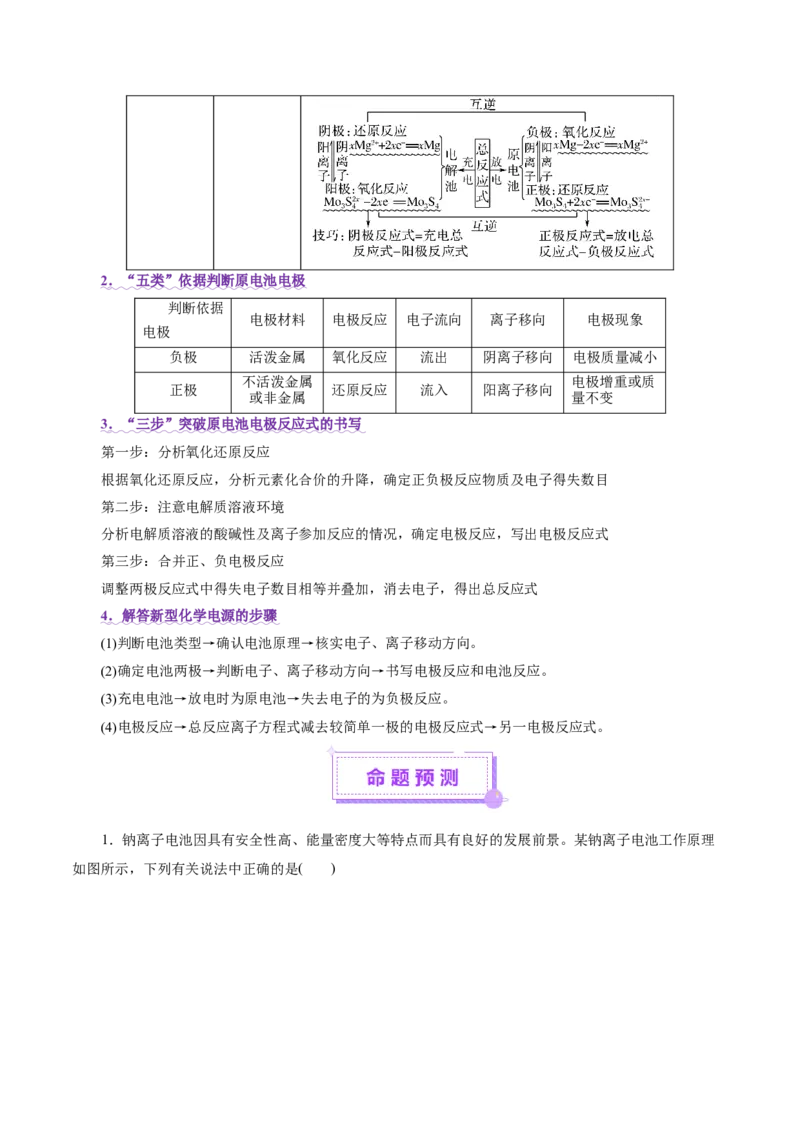
4.科学家开发了一种绿色环保“全氢电池”,其工作原理如图所示。下列说法错误的是( )A.吸附层a发生的电极反应: H-2e-+2OH-=2H O
2 2
B.离子交换膜只允许Na+通过
C.一段时间后右极室pH增大
D.“全氢电池”将酸碱反应的中和能转化为电能
【答案】B
【解析】吸附层a吸收H,作阳极,发生的电极反应:H-2e-+2OH-=2H O,吸附层b释放H,作阴极,
2 2 2 2
发生的电极反应:2H++2e-=H ↑,离子交换膜为阳离子交换膜,从左边移动到右边。A项,吸附层a吸收H
2 2
为阳极,电极反应:H-2e-+2OH-=2H O,A正确;B项,H+在吸附层b参加反应,离子交换膜还允许H+通
2 2
过,B错误;C项,右极室发生的电极反应:2H++2e-=H ↑,一段时间后,pH增大,C正确;D项,将正、
2
负电极反应叠加可知,实际发生的是H++OH-=H O,全氢电池工作时,将酸碱反应的中和能转化为电能,
2
D正确;故选B。
题型四 电解原理及应用
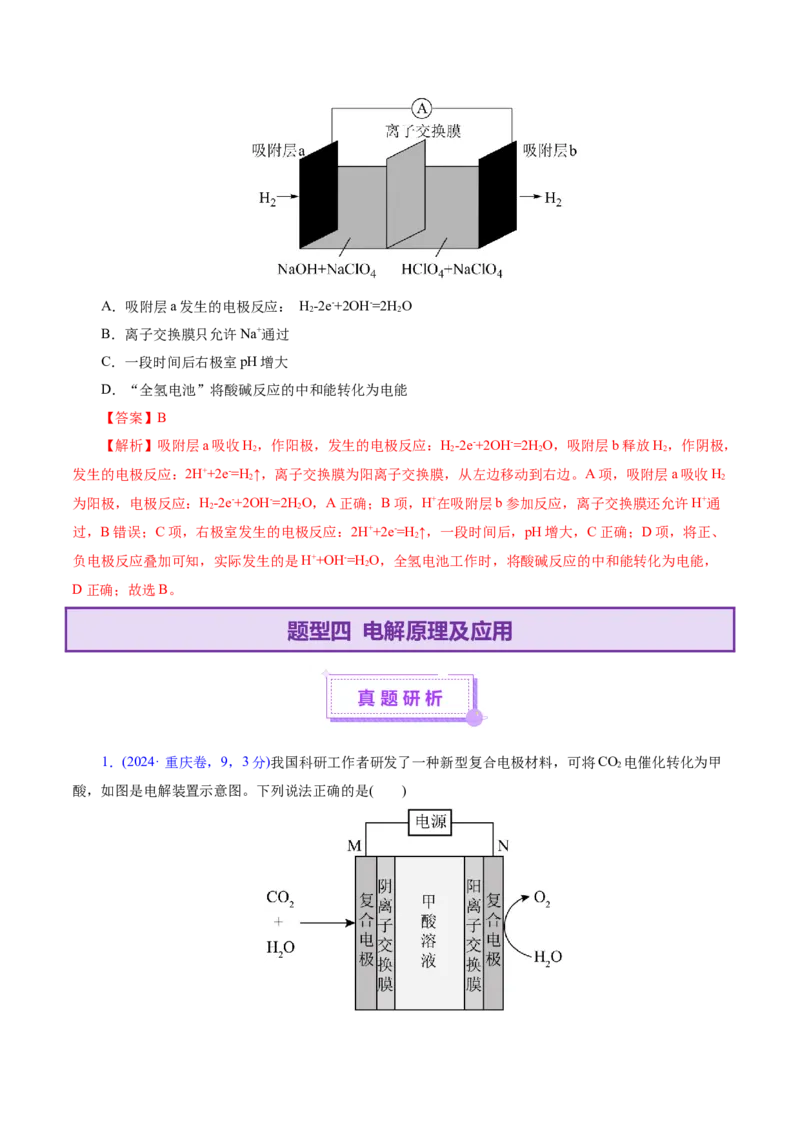
1.(2024· 重庆卷,9,3分)我国科研工作者研发了一种新型复合电极材料,可将CO 电催化转化为甲
2
酸,如图是电解装置示意图。下列说法正确的是( )A.电解时电极N上产生OH- B.电解时电极M上发生氧化反应
C.阴、阳离子交换膜均有两种离子通过 D.总反应为2CO+2H O 2HCOOH+O
2 2 2
【答案】D
【解析】催化电极 M 上二氧化碳得到电子发生还原反应和水生成甲酸根离子和氢氧根离子:
CO+2H O+2e-=HCOO-+OH-,甲酸根离子和氢氧根离子通过阴离子膜加入中间室,氢氧根离子和氢离子
2 2
生成水、甲酸根离子和氢离子生成甲酸,则M是阴极,那么N是阳极,阳极水失去电子发生氧化反应生成
氧气:2HO-4e-=O↑+4H+,氢离子通过阳离子膜进入中间室。A项,酸性条件下,电解时电极N上水失
2 2
去电子发生氧化反应生成氧气:2HO-4e-=O↑+4H+,A错误;B项,催化电极M上二氧化碳得到电子发
2 2
生还原反应生成甲酸,B错误;C项,阳离子交换膜有1种离子通过,C错误;D项,总反应为二氧化碳和
水生成甲酸和氧气,D正确;故选D。
2.(2024·山东卷,13,4分)以不同材料修饰的Pt为电极,一定浓度的NaBr溶液为电解液,采用电解
和催化相结合的循环方式,可实现高效制H 和O,装置如图所示。下列说法错误的是( )
2 2
A.电极a连接电源负极
B.加入Y的目的是补充NaBr
C.电解总反应式为Br-+3H O BrO -+3H ↑
2 3 2
D.催化阶段反应产物物质的量之比n(Z) ∶n(Br-)=3∶2
【答案】B
【解析】电极b上Br-发生失电子的氧化反应转化成BrO -,电极b为阳极,电极反应为Br- -6e-+3H O=
3 2
BrO -+6H+;则电极a为阴极,电极a的电极反应为6H++6e-=3H ↑;电解总反应式为Br-+3H O BrO -
3 2 2 3
+3H ↑;催化循环阶段BrO -被还原成Br-循环使用、同时生成O,实现高效制H 和O,即Z为O。A项,
2 3 2 2 2 2
电极a为阴极,连接电源负极,A项正确;B项,根据分析电解过程中消耗HO和Br-,而催化阶段BrO -
2 3
被还原成Br-循环使用,故加入Y的目的是补充HO,维持NaBr溶液为一定浓度,B项错误;C项,根据
2
分析电解总反应式为Br-+3H O BrO -+3H ↑,C项正确;D项,催化阶段,Br元素的化合价由+5价降
2 3 2
至-1价,生成1molBr-得到6mol电子,O元素的化合价由-2价升至0价,生成1molO 失去4mol电子,根
2
据得失电子守恒,反应产物物质的量之比n(O ) ∶n(Br-)=6∶4=3∶2,D项正确;故选B。
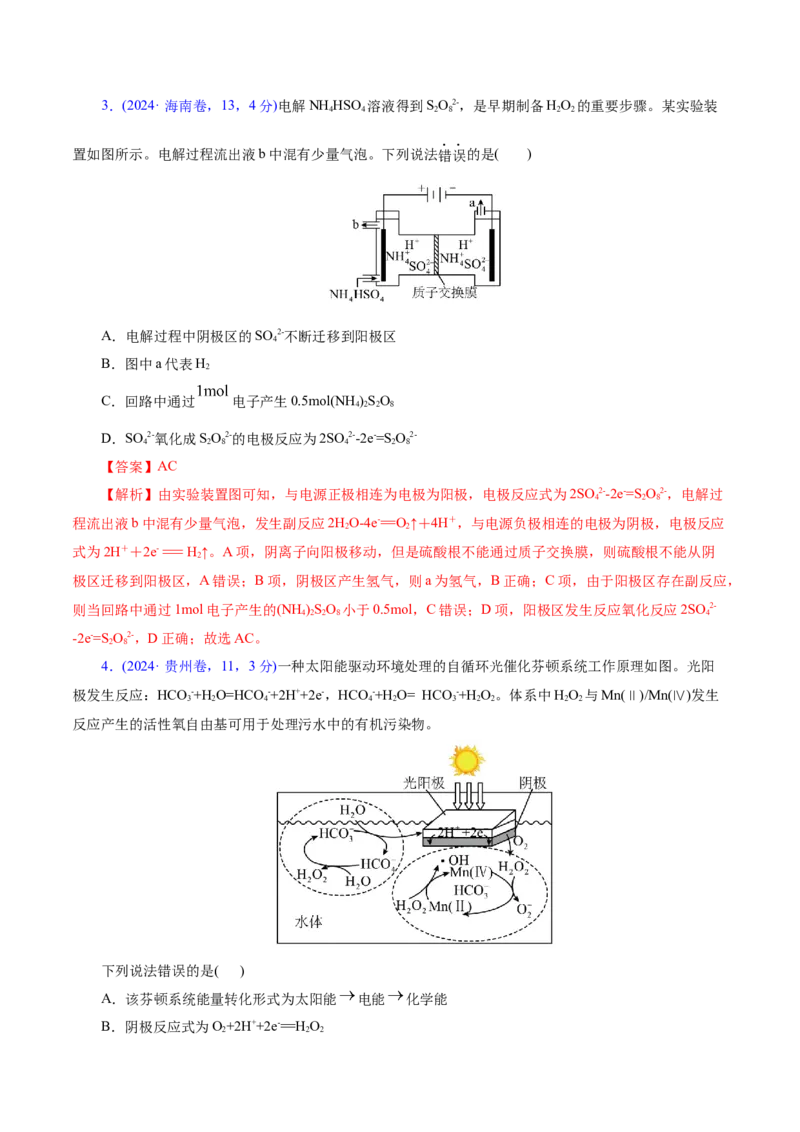
23.(2024· 海南卷,13,4分)电解NH HSO 溶液得到SO2-,是早期制备HO 的重要步骤。某实验装
4 4 2 8 2 2
置如图所示。电解过程流出液b中混有少量气泡。下列说法错误的是( )
A.电解过程中阴极区的SO 2-不断迁移到阳极区
4
B.图中a代表H
2
C.回路中通过 电子产生0.5mol(NH )SO
4 2 2 8
D.SO 2-氧化成SO2-的电极反应为2SO 2--2e-=SO2-
4 2 8 4 2 8
【答案】AC
【解析】由实验装置图可知,与电源正极相连为电极为阳极,电极反应式为2SO 2--2e-=SO2-,电解过
4 2 8
程流出液b中混有少量气泡,发生副反应2HO-4e-=O↑+4H+,与电源负极相连的电极为阴极,电极反应
2 2
式为2H++2e-=H↑。A项,阴离子向阳极移动,但是硫酸根不能通过质子交换膜,则硫酸根不能从阴
2
极区迁移到阳极区,A错误;B项,阴极区产生氢气,则a为氢气,B正确;C项,由于阳极区存在副反应,
则当回路中通过1mol电子产生的(NH )SO 小于0.5mol,C错误;D项,阳极区发生反应氧化反应2SO 2-
4 2 2 8 4
-2e-=SO2-,D正确;故选AC。
2 8
4.(2024· 贵州卷,11,3分)一种太阳能驱动环境处理的自循环光催化芬顿系统工作原理如图。光阳
极发生反应:HCO -+H O=HCO -+2H++2e-,HCO -+H O= HCO -+H O。体系中HO 与Mn(Ⅱ)/Mn(Ⅳ)发生
3 2 4 4 2 3 2 2 2 2
反应产生的活性氧自由基可用于处理污水中的有机污染物。
下列说法错误的是( )
A.该芬顿系统能量转化形式为太阳能 电能 化学能
B.阴极反应式为O+2H++2e-=HO
2 2 2C.光阳极每消耗1molHO,体系中生成2mol HO
2 2 2
D.HO 在Mn(Ⅱ)/Mn(Ⅳ)的循环反应中表现出氧化性和还原性
2 2
【答案】C
【解析】该装置为电解池,光阳极上水失电子生成氧气和氢离子,电极反应式为2HO-2e-=HO +
2 2 2
2H+,阴极上氧气和氢离子得电子生成过氧化氢,电极反应式为 O+2H++2e-=HO 。A项,该装置为电解
2 2 2
池,利用光能提供能量转化为电能,在电解池中将电能转化为化学能,A正确;B项,由图可知,阴极上
氧气和氢离子得电子生成过氧化氢,电极反应式为O+2H++2e-=HO ,B正确;C项,光阳极上水失电子
2 2 2
生成氧气和氢离子,电极反应式为2HO-2e-=HO +2H+,每消耗1molHO,则体系中生成0.5mol HO ,
2 2 2 2 2 2
C错误;D项,由Mn(Ⅳ)和过氧化氢转化为Mn(Ⅱ)过程中,锰元素化合价降低,HO 做还原剂,表现还原
2 2
性,由Mn(Ⅱ)转化为Mn(Ⅳ)时,HO 中O元素化合价降低,做氧化剂,表现氧化性,D正确;故选C。
2 2
5.(2024·广东卷,16,3分)一种基于氯碱工艺的新型电解池(下图),可用于湿法冶铁的研究。电解过
程中,下列说法不正确的是( )
A.阳极反应:2Cl--2e-= Cl ↑
2
B.阴极区溶液中OH-浓度逐渐升高
C.理论上每消耗1molFe O,阳极室溶液减少
2 3
D.理论上每消耗1molFe O,阴极室物质最多增加
2 3
【答案】C
【解析】右侧溶液为饱和食盐水,右侧电极产生气体,则右侧电极为阳极,Cl-放电产生氯气,电极反
应为:2Cl--2e-= Cl ↑;左侧电极为阴极,发生还原反应,Fe O 在碱性条件下转化为Fe,电极反应为:
2 2 3
Fe O+6e-+3H O=2Fe+6OH-;中间为阳离子交换膜,Na+由阳极向阴极移动。A项,阳极反应为:2Cl--2e-
2 3 2
= Cl ↑,A正确;B项,阴极反应为:Fe O+6e-+3H O=2Fe+6OH-,消耗水产生OH-,阴极区溶液中OH-
2 2 3 2
浓度逐渐升高,B正确;C项,理论上每消耗1molFe O,转移6mol电子,产生3mol Cl ,同时有6mol
2 3 2
Na+由阳极转移至阴极,则阳极室溶液减少 ,C错误;D项,理论上每消耗1molFe O,转移6mol电子,有6mol Na+由阳极转移至阴极,阴极室物质最多增加 ,D正确;
2 3
故选C。
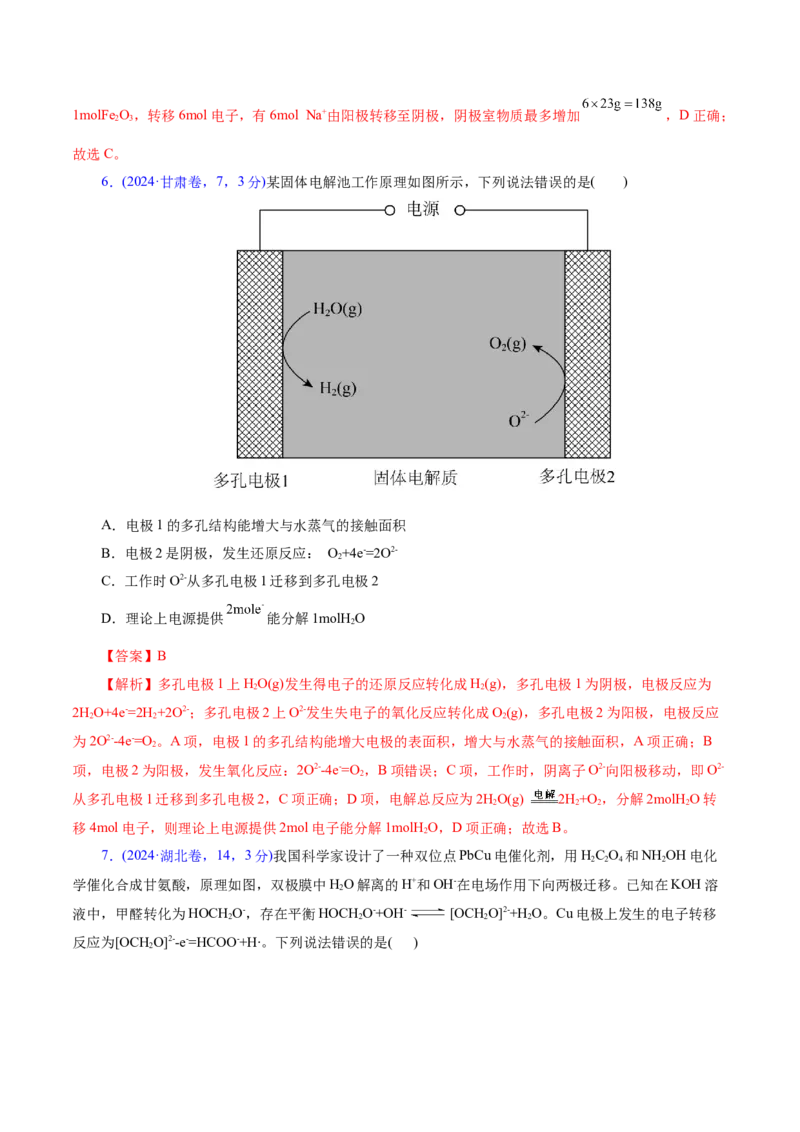
6.(2024·甘肃卷,7,3分)某固体电解池工作原理如图所示,下列说法错误的是( )
A.电极1的多孔结构能增大与水蒸气的接触面积
B.电极2是阴极,发生还原反应: O+4e-=2O2-
2
C.工作时O2-从多孔电极1迁移到多孔电极2
D.理论上电源提供 能分解1molH O
2
【答案】B
【解析】多孔电极1上HO(g)发生得电子的还原反应转化成H(g),多孔电极1为阴极,电极反应为
2 2
2HO+4e-=2H +2O2-;多孔电极2上O2-发生失电子的氧化反应转化成O(g),多孔电极2为阳极,电极反应
2 2 2
为2O2--4e-=O 。A项,电极1的多孔结构能增大电极的表面积,增大与水蒸气的接触面积,A项正确;B
2
项,电极2为阳极,发生氧化反应:2O2--4e-=O ,B项错误;C项,工作时,阴离子O2-向阳极移动,即O2-
2
从多孔电极1迁移到多孔电极2,C项正确;D项,电解总反应为2HO(g) 2H+O ,分解2molH O转
2 2 2 2
移4mol电子,则理论上电源提供2mol电子能分解1molH O,D项正确;故选B。
2
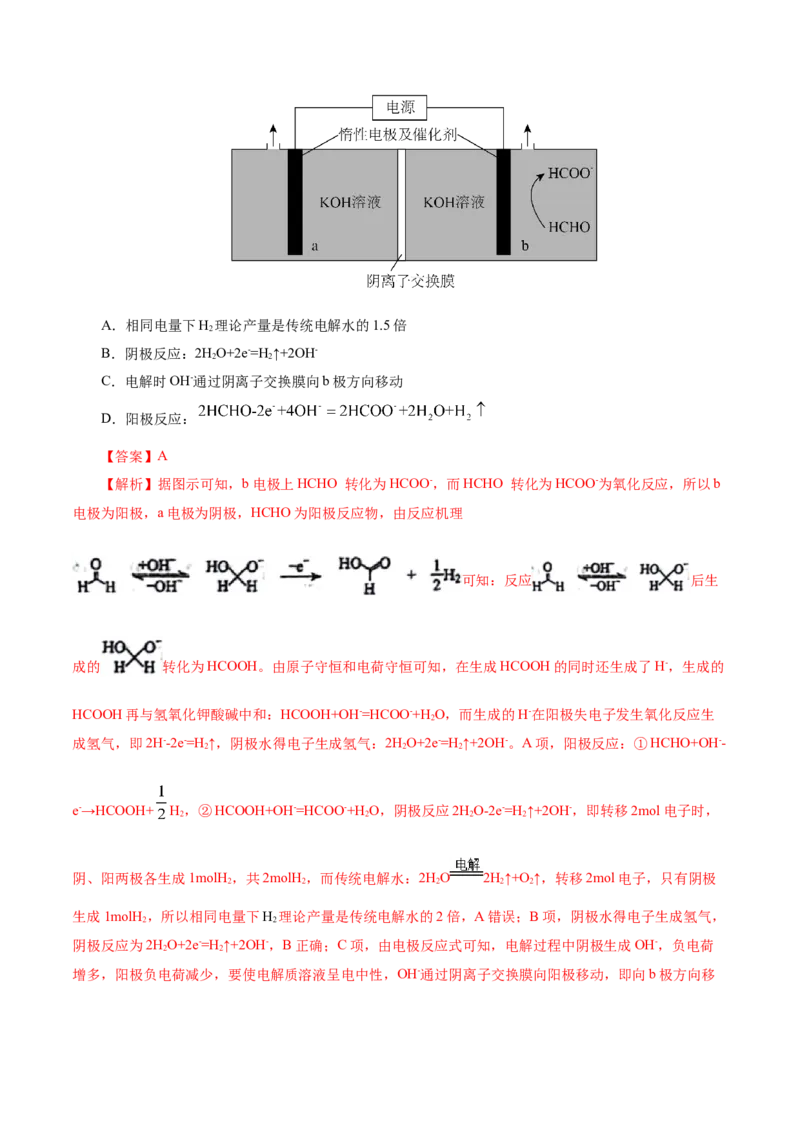
7.(2024·湖北卷,14,3分)我国科学家设计了一种双位点PbCu电催化剂,用HC O 和NH OH电化
2 2 4 2
学催化合成甘氨酸,原理如图,双极膜中HO解离的H+和OH-在电场作用下向两极迁移。已知在KOH溶
2
液中,甲醛转化为HOCH O-,存在平衡HOCH O-+OH- [OCH O]2-+H O。Cu电极上发生的电子转移
2 2 2 2
反应为[OCH O]2--e-=HCOO-+H∙。下列说法错误的是( )
2A.电解一段时间后阳极区c(OH-)减小
B.理论上生成1molH N+CHCOOH双极膜中有4molH O解离
3 2 2
为
C.阳极总反应式 2HCHO-2e-+4OH-=2HCOO-+H ↑+2H O
2 2
D.阴极区存在反应HC O+2e-+2H+=OHC—COOH+H O
2 2 4 2
【答案】B
【解析】在KOH溶液中HCHO转化为HOCH O-:HCHO+OH-→HOCH O-,存在平衡HOCH O-+OH-
2 2 2
[OCH O]2-+H O,Cu电极上发生的电子转移反应为[OCH O]2--e-=HCOO-+H∙,H∙结合成H,Cu电极
2 2 2 2
为阳极;PbCu电极为阴极,首先HOOC—COOH在Pb上发生得电子的还原反应转化为OHC—COOH:
HC O+2e-+2H+=OHC—COOH+H O,OHC—COOH与HO—N+H 反应生成HOOC—CH=N—OH:OHC—
2 2 4 2 3
COOH+HO—N+H→HOOC—CH=N—OH+H O+H+,HOOC—CH=N—OH发生得电子的还原反应转化成
3 2
HN+CHCOOH:HOOC—CH=N—OH+4e-+5H+=H N+CHCOOH+H O。A项,电解过程中,阳极区消耗
3 2 3 2 2
OH-、同时生成HO,故电解一段时间后阳极区c(OH-)减小,A正确;B项,阴极区的总反应为
2
HC O+HO—N+H+6e-+6H+= H N+CHCOOH+3H O,1molH O解离成1molH+和1molOH-,故理论上生成
2 2 4 3 3 2 2 2
1molH N+CHCOOH双极膜中有6molH O解离,B错误;C项,结合装置图,阳极总反应为2HCHO-2e-
3 2 2
+4OH-=2HCOO-+H ↑+2H O,C正确;D项,阴极区的Pb上发生反应HC O+2e-+2H+=OHC—
2 2 2 2 4
COOH+H O,D正确;故选B。
2
8.(2024·辽吉黑卷,12,3分) “绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、
反应速率缓慢的问题,科技工作者设计耦合HCHO高效制H 的方法,装置如图所示。部分反应机理为:
2
。下列说法错误的是( )A.相同电量下H 理论产量是传统电解水的1.5倍
2
B.阴极反应:2HO+2e-=H ↑+2OH-
2 2
C.电解时OH-通过阴离子交换膜向b极方向移动
D.阳极反应:
【答案】A
【解析】据图示可知,b电极上HCHO 转化为HCOO-,而HCHO 转化为HCOO-为氧化反应,所以b
电极为阳极,a电极为阴极,HCHO为阳极反应物,由反应机理
可知:反应 后生
成的 转化为HCOOH。由原子守恒和电荷守恒可知,在生成HCOOH的同时还生成了H-,生成的
HCOOH再与氢氧化钾酸碱中和:HCOOH+OH-=HCOO-+H O,而生成的H-在阳极失电子发生氧化反应生
2
成氢气,即2H--2e-=H ↑,阴极水得电子生成氢气:2HO+2e-=H ↑+2OH-。A项,阳极反应:①HCHO+OH--
2 2 2
e-→HCOOH+ H,②HCOOH+OH-=HCOO-+H O,阴极反应2HO-2e-=H ↑+2OH-,即转移2mol电子时,
2 2 2 2
阴、阳两极各生成1molH ,共2molH ,而传统电解水:2HO 2H↑+O ↑,转移2mol电子,只有阴极
2 2 2 2 2
生成1molH ,所以相同电量下H 理论产量是传统电解水的2倍,A错误;B项,阴极水得电子生成氢气,
2 2
阴极反应为2HO+2e-=H ↑+2OH-,B正确;C项,由电极反应式可知,电解过程中阴极生成OH-,负电荷
2 2
增多,阳极负电荷减少,要使电解质溶液呈电中性,OH-通过阴离子交换膜向阳极移动,即向b极方向移动,C正确;D项,阳极反应涉及到:①HCHO+OH--e-→HCOOH+ H,②HCOOH+OH-=HCOO-+H O,
2 2
由(①+②)×2得阳极反应为:2HCHO+4OH--2e-=2HCOO-+2H O+H↑,故D正确;故选A。
2 2
1.电化学题解题策略
2.电极反应式的书写
1 .惰性电极电解电解质溶液的产物判断 (图示)
2 .“五类”依据判断电解池电极
判断依据
电极材料 电极反应 电子流向 离子移向 电极现象
电极
电极溶解或
阳极 与电源正极相连 氧化反应 流出 阴离子移向
pH减小
电极增重或
阴极 与电源负极相连 还原反应 流入 阳离子移向
pH增大3 .电解原理的应用
(1)电解饱和食盐水。
阳极反应式:2Cl--2e-===Cl↑(氧化反应) 阴极反应式:2H++2e-===H ↑(还原反应)
2 2
总反应方程式:2NaCl+2HO 2NaOH+H↑+Cl↑
2 2 2
离子反应方程式:2Cl-+2HO 2OH-+H↑+Cl↑
2 2 2
2.电镀和电解精炼铜
电镀(Fe上镀Cu) 电解精炼铜
电极材料 镀层金属铜 粗铜(含Zn、Fe、Ni、Ag、Au等杂质)
阳极 Cu-2e-===Cu2+,Zn-2e-===Zn2+,
电极反应 Cu-2e-===Cu2+
Fe-2e-===Fe2+,Ni-2e-===Ni2+
电极材料 待镀金属Fe 纯铜
阴极
电极反应 Cu2++2e-===Cu
电解质溶液 含Cu2+的盐溶液
电解精炼铜时,粗铜中的Ag、Au等不反应,沉积在电解槽底部形成阳极泥,阳极泥可作为
提炼金、银等金属的原料
(4)电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等
总方程式 阳极、阴极反应式
冶炼钠 2NaCl(熔融)=====2Na+Cl↑ 2Cl--2e-===Cl↑,2Na++2e-===2Na
2 2
冶炼镁 MgCl (熔融)=====Mg+Cl↑ 2Cl--2e-===Cl↑,Mg2++2e-===Mg
2 2 2
冶炼铝 2Al O(熔融)=====4Al+3O↑ 6O2--12e-===3O ↑,4Al3++12e-===4Al
2 3 2 2
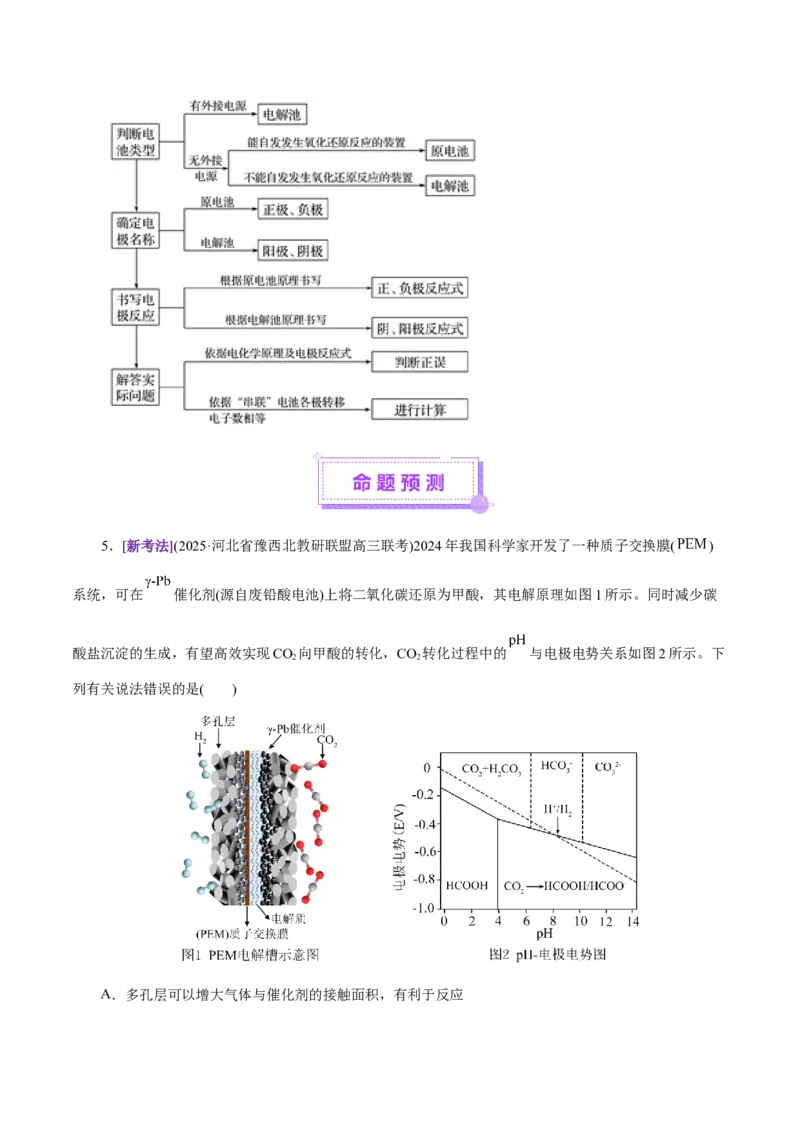
4 .“串联”类装置的解题流程5.[新考法](2025·河北省豫西北教研联盟高三联考)2024年我国科学家开发了一种质子交换膜( )
系统,可在 催化剂(源自废铅酸电池)上将二氧化碳还原为甲酸,其电解原理如图1所示。同时减少碳
酸盐沉淀的生成,有望高效实现CO 向甲酸的转化,CO 转化过程中的 与电极电势关系如图2所示。下
2 2
列有关说法错误的是( )
A.多孔层可以增大气体与催化剂的接触面积,有利于反应B.外电路每转移 电子,有 的 自右侧经过质子交换膜到左侧
C.在pH=2的条件下,可发生CO+2H++2e-=HCOOH
2
D.pH=12时,可生成碳酸盐沉淀,不利于甲酸的生成
【答案】B
【解析】A项,多孔材料具有许多微小的孔隙,这些孔隙可以增加催化剂与反应气体的接触面积,使
得反应物分子更容易与催化剂活性位点接触,从而提高反应速率,有利于反应进行,A正确;B项,由图
可知,CO 在正极得到电子生成HCOOH,右侧为正极,左侧为负极,原电池中阳离子向正极移动,外电
2
路每转移1mol电子,有1mol的H+自左侧经过质子交换膜到右侧,B错误;C项,由图2可知,CO 在正
2
极得到电子生成了HCOOH,根据得失电子守恒和电荷守恒配平电极方程式为:CO+2H++2e-=HCOOH,C
2
正确;D项,由图2可知,pH=12时,CO 在正极得到电子生成了CO2-,可生成碳酸盐沉淀,不利于甲酸
2 3
的生成,D正确;故选B。
6.[新题型](2025·河北省石家庄市百校高三联考)如图1所示为一种用双氧水去除废水中的持久性有机
污染物的工作原理,工作10min时,Fe2+、HO 电极产生量(mmol-1)与电流强度关系如图2所示:
2 2
下列说法正确的是( )
A.图1装置需不断补充Fe3+
B.Pt电极为阳极,苯酚在Pt电极失电子生成CO
2
C.据图2可知电流强度越高,去除苯酚的效果越好
D.若处理47.0g苯酚,理论上消耗14molH O
2 2
【答案】D
【解析】图可知,HMC-3电极上铁元素、氧元素价态降低得电子,故HMC-3电极为阴极,电极反应
式分别为O+2e-+2H+=H O,Fe3++e-=Fe2+,后发生反应Fe2++H O+H+=Fe3++•OH+H O,•OH氧化苯酚,反
2 2 2 2 2 2
应为C HOH+28•OH=6CO ↑+17H O,Pt电极为阳极,电极反应式为HO-e-=•OH+H+。A项,HMC-3电极
6 5 2 2 2
为阴极Fe3++e-=Fe2+,后发生反应Fe2++H O+H+=Fe3++•OH+H O,反应前后Fe3+的量保持不变,A错误;B
2 2 2项,Pt电极为阳极,电极反应式为HO-e-=•OH+H+,•OH氧化苯酚,反应为
2
C HOH+28•OH=6CO ↑+17H O,B错误;C项,电流强度过高,产生的过氧化氢过多,过量的过氧化氢会
6 5 2 2
氧化亚铁离子,导致生成的羟基自由基减少,使得降解去除废水中的持久性有机污染物的效率下降,C错
误;D项,根据反应C HOH+28•OH=6CO ↑+17H O,苯酚转化为二氧化碳,1mol的苯酚发生反应,要消
6 5 2 2
耗28mol的·OH,而28mol的·OH需要28mol的过氧化氢,47.0g苯酚的物质的量为 ,理
论上消耗14molH O,D正确;故选D。
2 2
7.(2025·浙江省嘉兴市高三基础测试)以Pt为电极,一定浓度的NaBr溶液为电解液,采用电解和催化
相结合的循环方式,可实现高效制H 和O,装置如图所示。下列说法不正确的是( )
2 2
A.X为H,Y为NaBr,Z为O
2 2
B.电极b连接电源正极
C.电解总反应式为Br-+3H O BrO-+3H ↑
2 3 2
D.催化阶段反应产物物质的量之比n(Z) :n(Br-)=3∶2
【答案】A
【解析】电极b上Br-发生失电子的氧化反应转化成BrO-,电极b为阳极,电极反应为Br--6e-
3
+3H O=BrO-+6H+;则电极a为阴极,电极a的电极反应为6H++6e-=3H ↑;电解总反应式为Br-+3H O
2 3 2 2
BrO-+3H ↑;催化循环阶段BrO-被还原成Br-循环使用、同时生成O,实现高效制H 和O,即Z为O。A
3 2 3 2 2 2 2
项,电解过程中消耗HO和Br-,而催化阶段被还原成Br-循环使用,故加入Y的目的是补充HO,维持
2 2
NaBr溶液为一定浓度,Y为HO,电极a为阴极,电极a的电极反应为6H++6e-=3H ↑,X为H,催化循环
2 2 2
阶段BrO-被还原成Br-循环使用、同时生成Z为O,A错误;B项,电极b为阳极,连接电源正极,B正
3 2
确;C项,电解总反应式为Br-+3H O BrO-+3H ↑,C正确;D项,催化阶段,Br元素的化合价由+5
2 3 2
价降至-1价,生成1mol Br-得到6mol电子,O元素的化合价由-2价升至0价,生成1molO 失去4mol电子,
2根据得失电子守恒,反应产物物质的量之比n(O ) :n(Br-)=6∶4=3∶2,D正确;故选A。
2
8.基于甲烷蒸汽重整工业制氢面临着大量的“碳排放”,我国科技工作者发明了一种电化学分解甲
烷的方法,从而实现了碳和水的零排放方式生产氢气。电化学反应机理如下图所示。下列判断正确的是(
)
A.上述电化学装置中电解质可使用水溶液
B.阳极反应:CH-4e-+2O2-=CO +2H
4 2 2
C. 既是阴极的生成物,也是阴极的反应物
D.理论上阳极生成1.5mol气体,电路中转移8mol电子
【答案】B
【解析】A项,O2-在水中不存在,A错误;B项,由Ni-YSZ电极上生成CO 可知,该电极为阳极,是
2
CH 失电子生成CO,B正确;C项,CO+O2-=CO 2-,该反应不是阴极反应,阴极反应为CO2-+4e-
4 2 2 3 3
=C+3O2-,C错误;D项,阳极不仅生成氧化产物CO,还生成还原产物H,由阳极反应可知,理论上阳极
2 2
生成1.5mol气体(即0.5molCO 和1molH ),转移2mol电子,D错误。故选B。
2 2
9.科学家利用多晶铜高效催化电解CO 制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不
2
变。下列说法正确的是( )
A.铂电极为阳极,产生的气体是O 和CO
2 2
B.铜电极的电极反应式为2CO+12HCO-+12e-=C H+12CO 2-+4H O
2 3 2 4 3 2
C.通电过程中,溶液中HCO -通过阴离子交换膜向右槽移动
3D.当电路中通过0.6 mol电子时,理论上能产生C H1.12L
2 4
【答案】A
【解析】该电解池的总反应方程式为2CO+2H O=C H+3O ,铜电极为阴极,该电极的电极方程式为
2 2 2 4 2
14CO+8H O+12e-=C H+12HCO- , 铂 电 极 为 阳 极 , 该 电 极 的 电 极 方 程 式 为 12HCO --12e-
2 2 2 4 3 3
=12CO ↑+3O ↑+6H O。A项,铂电极为阳极,产生的气体是O 和CO ,故A正确;B项,铜电极的电极方
2 2 2 2 2
程式为14CO+8H O+12e-=C H+12HCO-,故B错误;C项,HCO -在铂电极发生反应,并且电解前后电解
2 2 2 4 3 3
液浓度几乎不变,所以溶液中HCO -通过阴离子交换膜向左槽移动,故C错误;D项,由铜电极电极方程
3
式分析可知,当电路中通过0.6 mol电子时,理论上能产生0.05mol C H ,在标况下,0.05molC H 的体积
2 4 2 4
为1.12L,该题目没有说明条件为标况,故D错误;故选A。
10.通过NO协同耦合反应,实现了NO的电催化歧化,并同时合成了双氮产物(NH 和硝酸盐)是实现
3
可持续固氮的一种极具潜力的方法,装置如图。下列说法正确的是( )
A.电解液E为阳极电解液,呈酸性
B.电极B的电极反应:NO+2H O-3e-= HNO-+3H+
2 3
C.中间层的OH-、 分别透过选择性离子膜向A、B极迁移
D.若电解一段时间后,取两极所有产物于溶液中反应,可得硝酸盐和硝酸
【答案】D
【解析】由图可知,A 极氮元素价态降低得电子,故 A 极为阴极,电极反应式为 NO+5H++5e-
=NH+H O,B极为阳极,电极反应式为NO+2H O-3e-=NO-+4H+。A项,根据以上分析,A极为阴极,电
3 2 2 3
极反应式为NO+5H++5e-=NH+H O,则电解液E为阴极电解液,呈酸性,故A错误;B项,B极为阳极,
3 2
电极反应式为NO+2H O-3e-= NO -+4H+,故B错误;C项,由两极反应式可知,阳极区产生氢离子,阴极
2 3
区消耗氢离子,故中间层的OH-、H+分别透过选择性离子膜向B、A极迁移,故C错误;D项,由图可知,
A极NO→NH ~5e-,B极NO→NO -~3e-,根据电子得失守恒,电解一段时间后,取两极所有产物于溶液
3 3
中反应,可得硝酸盐和硝酸,故D正确;故选D。
11.利用电解池原理可将CO 转化为燃料或者化学品。下图通过将CO 与辛胺反应耦合,实现了两电
2 2
极体系中产物的高选择性合成。下列说法正确的是( )
A.装置中b电极为阴极,发生还原反应
B.电极a的电极反应可能为:CO+H O+2e- =HCOO-+OH-
2 2
C.中间的离子交换膜一定是质子交换膜
D.电解过程中,a、b两极反应物物质的量之比为2∶1
【答案】B
【解析】利用电解池原理可将CO 转化为燃料或者化学品,反应过程中碳元素的化合价降低,得到电
2
子,则a极为阴极,CO 转化为燃料或者化学品,b极为阳极,辛胺转化为辛氰。A项,装置中b电极为阳
2
极,失去电子,发生氧化反应,故 A错误;B项,电极 a为阴极,电极反应可能为::CO+H O+2e-
2 2
=HCOO-+OH-,故B正确;C项,若电解液中性时,中间的离子交换膜是质子交换膜,若电解液碱性时,
中间的离子交换膜是阴离子交换膜,故C错误;D项,电解过程中,a极CO 转化为燃料或者化学品,b极
2
辛胺转化为辛氰,由于电极a的产物不确定,则反应物物质的量之比不确定,故D错误;故选B。
题型五 电化学腐蚀与防护
1.(2024·广东卷,5,2分)我国自主设计建造的浮式生产储御油装置“海葵一号”将在珠江口盆地海
域使用,其钢铁外壳镶嵌了锌块,以利用电化学原理延缓外壳的腐蚀。下列有关说法正确的是( )
A.钢铁外壳为负极 B.镶嵌的锌块可永久使用
C.该法为外加电流法 D.锌发生反应:
【答案】D
【解析】钢铁外壳镶嵌了锌块,由于金属活动性Zn>Fe,即锌块为负极,钢铁为正极,形成原电池,
Zn失去电子,发生还原反应,Zn-2e-=Zn2+,从而保护钢铁,延缓其腐蚀。A项,由于金属活动性Zn>
Fe,钢铁外壳为正极,锌块为负极,故A错误;B项,Zn失去电子,发生还原反应,Zn-2e-=Zn2+,镶嵌
的锌块会被逐渐消耗,需根据腐蚀情况进行维护和更换,不能永久使用,故B错误;C项,该方法为牺牲
阳极的阴极保护法,故C错误;D项,Zn失去电子,发生还原反应:Zn-2e-=Zn2+,故D正确;故选D。2.(2024·浙江1月卷,13,3分)破损的镀锌铁皮在氨水中发生电化学腐蚀,生成[Zn(NH )]2+和H,下
3 4 2
列说法不正确的是( )
A.氨水浓度越大,腐蚀趋势越大
B.随着腐蚀的进行,溶液pH变大
C.铁电极上的电极反应式为: 2NH +2e-=H↑+2NH -
3 2 2
D.每生成标准状况下22.4mLH ,消耗0.010 mol Zn
2
【答案】C
【解析】A项,氨水浓度越大,越容易生成[Zn(NH )]2+,腐蚀趋势越大,A正确;B项,腐蚀的总反
3 4
应为Zn+4NH •H O=[Zn(NH )]2++H ↑+2H O+2OH-,有OH-离子生成,溶液pH变大,B正确;C项,该电
3 2 3 4 2 2
化学腐蚀中Zn作负极,Fe作正极,正极上氢离子得电子生成氢气,铁电极上的电极反应式为:2HO+2e-
2
=H↑+2OH-,C错误;D项,根据得失电子守恒,每生成标准状况下22.4mLH ,转移电子数为
2 2
,消耗0.010 mol Zn,D正确;故选C。
3.(2024·浙江6月卷,13,3分)金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有
关。下图为两种对海水中钢闸门的防腐措施示意图:
下列说法正确的是( )
A.图1、图2中,阳极材料本身均失去电子
B.图2中,外加电压偏高时,钢闸门表面可发生反应:O+2H O+4e-=4OH-
2 2
C.图2中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
【答案】B
【解析】A项,图1为牺牲阳极的阴极瓮中保护法,牺牲阳极一般为较活泼金属,其作为原电池的负
极,其失去电子被氧化;图2为外加电流的阴极保护法,阳极材料为辅助阳极,其通常是惰性电极,其本
身不失去电子,电解质溶液中的阴离子在其表面失去电子,如海水中的Cl-,A不正确;B项,图2中,外
加电压偏高时,钢闸门表面积累的电子很多,除了海水中的H+放电外,海水中溶解的O 也会竞争放电,
2故可发生O+2H O+4e-=4OH-,B正确;C项,图2为外加电流的阴极保护法,理论上只要能对抗钢闸门
2 2
表面的腐蚀电流即可,当钢闸门表面的腐蚀电流为零时保护效果最好;腐蚀电流会随着环境的变化而变化,
若外加电压保持恒定不变,则不能保证抵消腐蚀电流,不利于提高对钢闸门的防护效果,C不正确;D项,
图1、图2中,当钢闸门表面的腐蚀电流为零时,说明从牺牲阳极或外加电源传递过来的电子阻止了Fe-2e-
=Fe2+的发生,钢闸门不发生化学反应,但是牺牲阳极和发生了氧化反应,辅助阳极上也发生了氧化反应,
D不正确;故选B。
1 .金属腐蚀两种类型比较
(1)析氢腐蚀和吸氧腐蚀的比较
类型 析氢腐蚀 吸氧腐蚀
条件 水膜呈酸性 水膜呈弱酸性或中性
正极反应 2H++2e-===H ↑ O+2HO+4e-===4OH-
2 2 2
负极反应 Fe-2e-===Fe2+
Fe2++2OH-===Fe(OH) ↓
2
其他反应 4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
Fe(OH) 失去部分水转化为铁锈
3
2 .金属电化学保护的两种方法1.(2025· 江浙皖高中发展共同体高三联考)下列关于电化学腐蚀、防护与利用的说法正确的是( )
A.铜板打上铁铆钉后,铜 B.牺牲阳极防护输水 C.连接锌棒后,电子由
D.外加电流保护
板更易被腐蚀 管腐蚀 铁管道流向锌
【答案】B
【解析】A项,形成Fe - Cu原电池,Cu作正极被保护,Cu不易被腐蚀,A错误;B项,镁比铁活泼,
此为牺牲阳极的阴极保护法,B正确;C项,锌比铁活泼,形成锌-铁原电池,锌作负极,电子由锌流向铁
管道,C错误;D项,此为外加电源的阴极保护法,被保护金属钢制管桩应与电源负极相连,D错误;故
选B。
2.(2025·浙江省强基联盟高三10月联考)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐
蚀。在题图所示的情境中,下列有关说法正确的是( )
A.阴极的电极反应式为Fe-2e-=Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【解析】A项,阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;B项,
阳极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe的
活动性强,故B错误;C项,金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电
子,自身金属不再失电子从而被保护,故C正确;D项,海水中的离子浓度大于河水中的离子浓度,离子
浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D错误;故选C。
3.(2025·浙江省新阵地教育联盟高三第一次联考)我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,防护原理如图所示。下列说法不正确的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应式为2HO+2e-=H↑+2OH-
2 2
C.把锌环换成锡环后,断电时,仍能防止铁帽被腐蚀
D.断电时,正极上的电极反应式为O+2H O+4e-=4OH-
2 2
【答案】C
【解析】根据电源和直流电方向可知,锌环作阳极、铁帽作阴极。A项,通电时锌环与电源的正极相
连,作阳极,发生氧化反应,A正确;B项,通电时铁作阴极,水中氢离子放电,电极反应式为2HO+2e-
2
=H↑+2OH-,B正确;C项,因铁比锡活泼,断电时构成原电池,锡作正极,而铁作负极被消耗,所以
2
铁帽被腐蚀,C错误;D项,断电时构成原电池,铁作正极氧气得电子,即正极上的电极反应式为
O+2H O+4e-=4OH-,D正确; 故选C。
2 2
4.如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。下列说法正确的是( )
A.铁闸主要发生的是析氢腐蚀 B.将铁闸与石墨相连可保护铁闸
C.铁腐蚀时的电极反应式:Fe-3e-===Fe3+ D.图中生成铁锈最多的是乙区域
【答案】D
【解析】海水溶液为弱碱性,铁闸主要发生吸氧腐蚀,A错误;将铁闸与石墨相连,铁比碳活泼,铁
作负极失电子,可以加快海水对铁闸的腐蚀,B错误;铁腐蚀时作负极失电子生成亚铁离子,电极反应式:
Fe-2e-===Fe2+,C错误;在乙区域,氧气含量高,海水与氧气接触,与 Fe最易形成原电池,发生的吸氧
腐蚀的程度最大,生成铁锈最多,故D正确。
5.点蚀又称为孔蚀,是一种集中于金属表面很小的范围并深入到金属内部的腐蚀形态。某铁合金钝
化膜破损后的孔蚀如图,下列说法正确的是( )A.为防止孔蚀发生可以将外接电源正极与金属相连
B.蚀孔外每吸收2.24LO ,可氧化0.2molFe
2
C.由于孔蚀中Fe3+水解导致电解质酸性增强
D.孔隙中可以发生析氢腐蚀
【答案】D
【解析】A项,为防止孔蚀发生可以将外接电源负极与金属相连,A错误;B项,2.24LO 没有指明是
2
否为标准状况,不一定为0.1molO,B错误;C项,封闭环境中由于Fe2+水解导致酸性增强,C错误;D项,
2
由于孔隙中介质的酸性增强有HCl存在,可发生析氢腐蚀,D正确;故选D。