文档内容
专题 10 水溶液中的离子平衡
1.(2022·浙江卷) 时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,
B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
【答案】C
【解析】A.醋酸的酸性大于苯酚,则醋酸根离子的水解程度较小,则相同温度下,等pH的C HONa和
6 5
CHCOONa溶液中c(C HO-)1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子方程
式为:H++OH-=H O和CHCOOH+OH-=CH COO-+H O,B错误;
2 3 3 2
C.滴定前盐酸和醋酸的浓度相同,故滴定过程中,根据物料守恒可知:
,C正确;
D.向 浓度均为 的盐酸和醋酸的混合溶液中逐滴加入 的 溶液,当盐酸的体
积为20ml时,溶液为氯化钠和醋酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH
溶液的体积为30mL时,溶液为NaCl和等浓度的CHCOONa、CHCOOH,根据Ka=1.8×10-5>Kh=
3 3
可知,此时溶液仍然呈酸性,需继续滴加NaOH溶液,故有
,D正确;
故答案为:B。
3.(2022·全国乙卷)常温下,一元酸 的 。在某体系中, 与 离子不能穿过隔膜,
未电离的 可自由穿过该膜(如图所示)。设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
【答案】B
【解析】A.常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A错误;
B.常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
则 =1.0×10-3,解得 = ,B正确;
C.根据题意,未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,C错误;
D.常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,K = =1.0×10-3,c (HA)=c(HA)
a 总
+c(A-), =1.0×10-3,溶液I中c (HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中
总
c(H+)=0.1mol/L,K = =1.0×10-3,c (HA)=c(HA)+c(A-), =1.0×10-3,溶液II
a 总
中c (HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c
总 总(HA)之比为[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误;
答案选B。
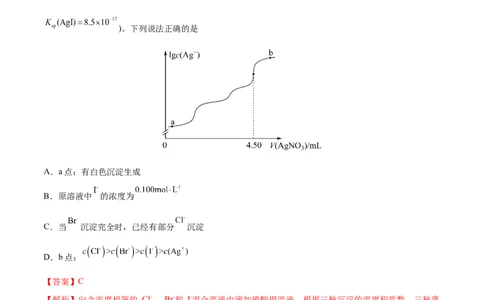
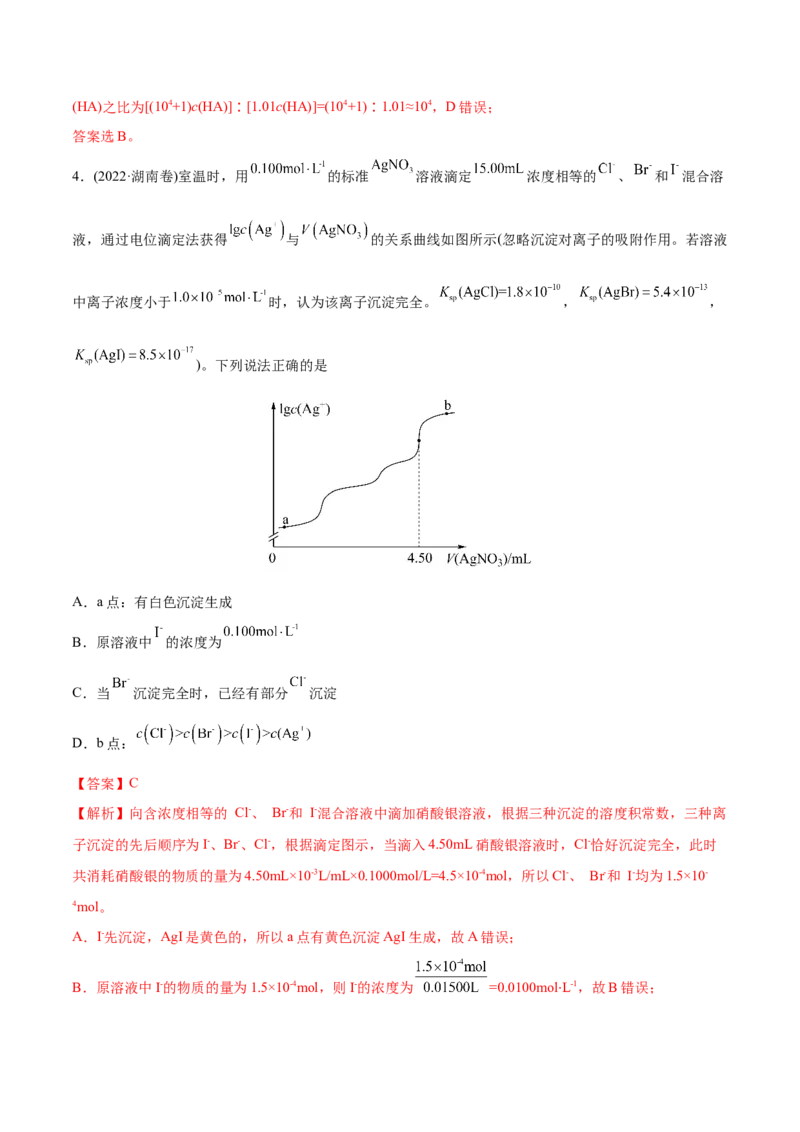
4.(2022·湖南卷)室温时,用 的标准 溶液滴定 浓度相等的 、 和 混合溶
液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶液
中离子浓度小于 时,认为该离子沉淀完全。 , ,
)。下列说法正确的是
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
【答案】C
【解析】向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积常数,三种离
子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,此时
共消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-
4mol。
A.I-先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;
B.原溶液中I-的物质的量为1.5×10-4mol,则I-的浓度为 =0.0100molL-1,故B错误;
⋅C.当Br-沉淀完全时(Br-浓度为1.0×10-5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若
Cl-已经开始沉淀,则此时溶液中的c(Cl-)= =3.3×10-3mol/L,原溶液中的c(Cl-)=
c(I-)=0.0100molL-1,则已经有部分Cl-沉淀,故C正确;
⋅
D.b点加入了过量的硝酸银溶液,Ag+浓度最大,则b点各离子浓度为: ,故
D错误;
故选C。
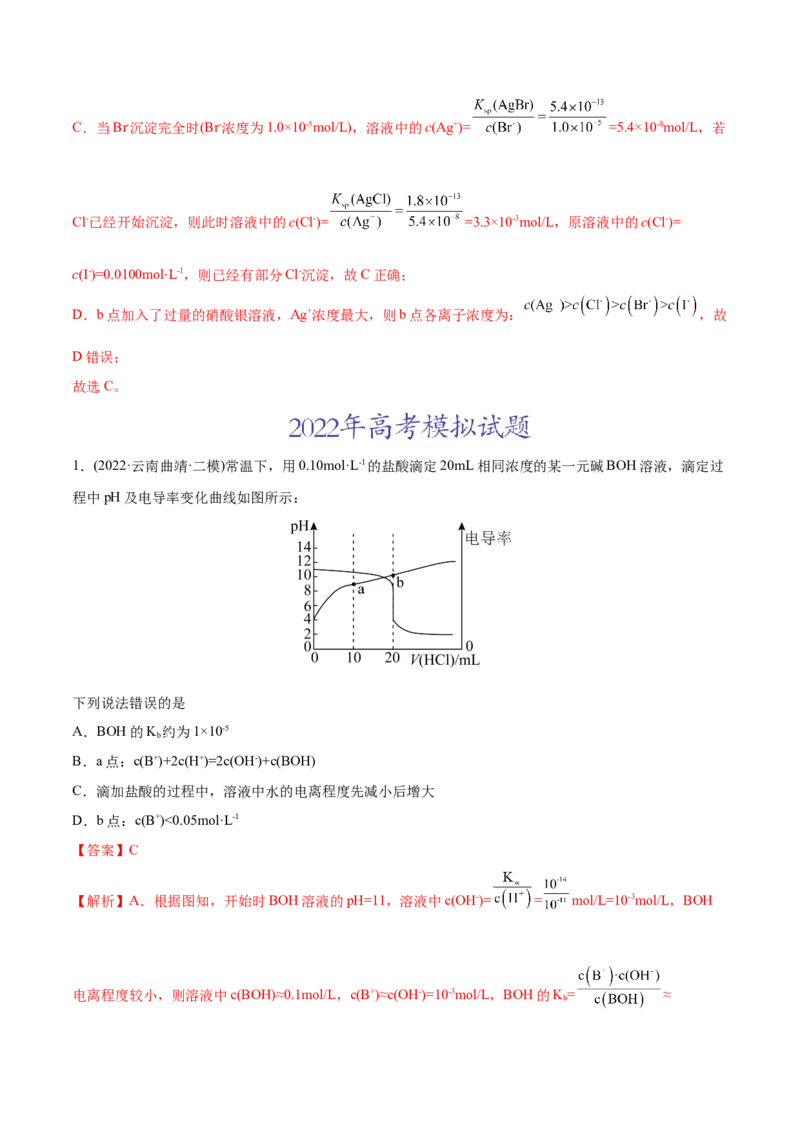
1.(2022·云南曲靖·二模)常温下,用0.10mol·L-1的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过
程中pH及电导率变化曲线如图所示:
下列说法错误的是
A.BOH的K 约为1×10-5
b
B.a点:c(B+)+2c(H+)=2c(OH-)+c(BOH)
C.滴加盐酸的过程中,溶液中水的电离程度先减小后增大
D.b点:c(B+)<0.05mol·L-1
【答案】C
【解析】A.根据图知,开始时BOH溶液的pH=11,溶液中c(OH-)= = mol/L=10-3mol/L,BOH
电离程度较小,则溶液中c(BOH)≈0.1mol/L,c(B+)≈c(OH-)=10-3mol/L,BOH的K= ≈
b=10-5,A正确;
B.a点等浓度的BOH和BCl混合溶液,存在电荷守恒c(B+ )+c(H+)=c(OH- )+c(Cl- )、存在物料守恒c(B+ )
+c(BOH)=2c(Cl- ),所以存在c(B+ )+2c(H+)=2c(OH- )+c( BOH),B正确;
C. 随着盐酸的滴加,一开始BOH电离的OH-浓度越来越小,对水的电离的抑制作用也越来越小,水的电
离程度增大,B+浓度越来越大,B+水解对水的电离起促进作用,当恰好完全反应生成BCl时,水的电离程
度最大,继续滴加盐酸,由于HCl电离出的H+对水的电离和B+水解均起到抑制作用,导致水的电离程度
又减小,即滴加盐酸的过程中,溶液中水的电离程度先增大后减小,C错误;
D. 由A项分析可知,BOH是弱碱,b点为BOH与HCl恰好完全反应,由于B+发生水解,故b点
c(B+)<0.05mol·L-1,D正确;
故答案为:C。
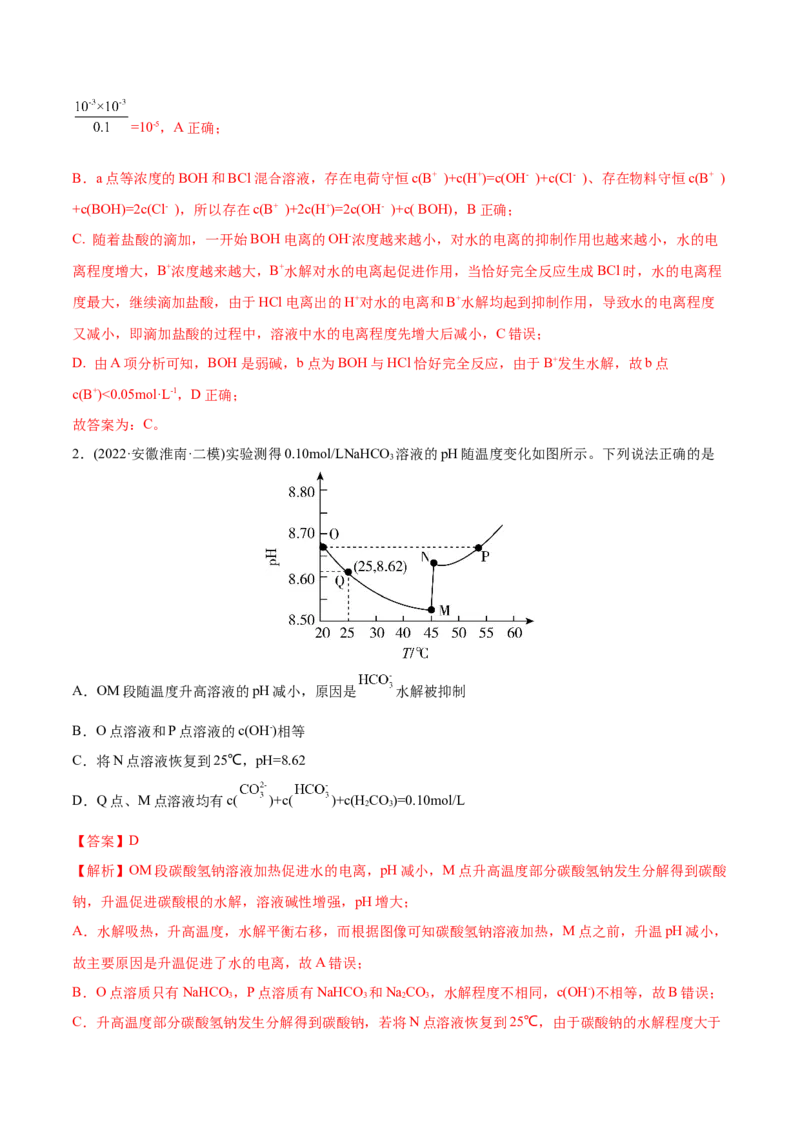
2.(2022·安徽淮南·二模)实验测得0.10mol/LNaHCO 溶液的pH随温度变化如图所示。下列说法正确的是
3
A.OM段随温度升高溶液的pH减小,原因是 水解被抑制
B.O点溶液和P点溶液的c(OH-)相等
C.将N点溶液恢复到25℃,pH=8.62
D.Q点、M点溶液均有c( )+c( )+c(H CO)=0.10mol/L
2 3
【答案】D
【解析】OM段碳酸氢钠溶液加热促进水的电离,pH减小,M点升高温度部分碳酸氢钠发生分解得到碳酸
钠,升温促进碳酸根的水解,溶液碱性增强,pH增大;
A.水解吸热,升高温度,水解平衡右移,而根据图像可知碳酸氢钠溶液加热,M点之前,升温pH减小,
故主要原因是升温促进了水的电离,故A错误;
B.O点溶质只有NaHCO ,P点溶质有NaHCO 和NaCO,水解程度不相同,c(OH-)不相等,故B错误;
3 3 2 3
C.升高温度部分碳酸氢钠发生分解得到碳酸钠,若将N点溶液恢复到25℃,由于碳酸钠的水解程度大于碳酸氢钠,故混合溶液pH应大于8.62,故C错误;
D.Q点、M点溶液均存在物料守恒:c( )+c( )+c(H CO)=0.10mol/L,故D正确;
2 3
故选:D。
3.(2022·安徽马鞍山·三模)MOH是一种一元弱碱,25℃时, 在20.0mL 0.1 mol·L-1MOH溶液中滴加0.1
mol·L-1盐酸V mL, 混合溶液的pH与 的关系如图所示。下列说法错误的是
A.x=3.75
B.a点时,V=10.0 mL
C.25℃时, MOH的电离常数K 的数量级为10-4
b
D.V=20.0 mL时,溶液存在关系: 2c(H+) + c(M+) = c(MOH) +2c(OH-)+ c(Cl-)
【答案】B
【解析】由图可知,a点时pH=10.75,故c(OH-)=10-3.25,当 =0,故c(M+)=c(MOH),
。
A.由分析知 ,当pH=7时,c(OH-)=10-7,则 ,故x=3.75,A项正确;
B.当V=10.0 mL,若不考虑电离和水解,则溶液中溶质为c(MOH)=c(MCl),由于M+的水解程度和MOH的电离程度不同,则c(MOH)≠c(MCl),故 ,B项错误;
C.由分析知 ,故MOH的电离常数K 数量级为10-4,C项正确;
b
D.当V=20.0 mL时,由电荷守恒可知:c(H+) + c(M+) =c(OH-)+ c(Cl-),由质子守恒可知:c(H+)= c(OH-)+
c(MOH),用电荷守恒与质子守恒相加即可得到2c(H+) + c(M+) = c(MOH) +2c(OH-)+ c(Cl-),D项正确;
答案选B。
4.(2022·安徽芜湖·三模)常温下,将0.2mol·L-1NH Cl溶液与0.2mol·L-1NaHA溶液等体积混合后(忽略体积
4
变化),所得混合溶液的pH为7.8。当向混合液中加入盐酸或NaOH溶液时,溶液中的粒子分布系数(δ)随
溶液pH的变化如图所示(无NH 逸出)。已知δ(x)= 或δ(x)= ;
3
a、b、c、d、e分别表示NH 、NH ·H O、HA-、A2-、HA中的一种。下列有关描述正确的是
3 2 2
A.常温下,K (NH ·H O)<K (H A)
b 3 2 a1 2
B.由图可知,曲线a表示的是HA,曲线e表示的是NH ·H O
2 3 2
C.常温下,向该混合溶液中逐滴加入NaOH溶液时,c(NH )、c(HA-)均逐渐减小
D.常温下,向该混合溶液中逐滴加入HCl溶液至pH=7时:c(Na+)+c(H A)=c(Cl-)+c(A2-)+c(NH ·H O)
2 3 2
【答案】D
【解析】已知NH ·H O +OH-,HA HA-+H+,HA- A2-+H+,随着pH值的增大,NH ·H O浓度
3 2 2 3 2
增大, 浓度减小,HA浓度减小,HA-浓度先增大后减小,A2-浓度增大,故题干图示中,a代表
2HA,b代表HA-,c代表 ,d代表NH ·H O,e代表A2-,据此分析解题。
2 3 2
A.由题干信息可知,将0.2mol·L-1NH Cl溶液与0.2mol·L-1NaHA溶液等体积混合后(忽略体积变化),所得
4
混合溶液的pH为7.8,说明HA-的水解大于 的水解,即K (HA-)>K ( ),即 >
h h
,则常温下,K (NH ·H O)>K (H A),A错误;
b 3 2 a1 2
B.由图可知,曲线a表示的是HA,曲线d表示的是NH ·H O,曲线e表示的是A2-,B错误;
2 3 2
C.由分析可知,常温下,向该混合溶液中逐滴加入NaOH溶液时,c( )逐渐减小,而c(HA-)先增大后
减小,C错误;
D.常温下,向该混合溶液中逐滴加入HCl溶液至pH=7即①c(H+)=c(OH-)时,根据电荷守恒可知:
②c(Na+)+ c(NH )+c(H+)=c(Cl-)+2c(A2-)+c(OH-)+c(HA-),根据物料守恒有:③c(NH )+ c(NH ·H O)= c(A2-)
3 2
+ c(H A)+c(HA-),则联合①②③可得:c(Na+)+c(H A)=c(Cl-)+c(A2-)+c(NH ·H O),D正确;
2 2 3 2
故答案为:D。
5.(2022·安徽淮北·二模) 为二元弱酸,在25℃时,溶液中 及HA-浓度的负对数pc随溶液pH变化
的关系如图所示[已知:溶液中始终保持 ]。下列有关叙述错误的是
A.HA的K 为1.0×10-3
2 a1
B.b点:
C.由a点到c点的过程中,水的电离程度一直增大
D.NaHA溶液呈碱性【答案】D
【解析】pH为0时,溶液中主要是HA,以HA的一级电离为主,故c(HA-)=10-4mol/L,ab所在曲线为
2 2
HA-的曲线,另一条线为A2-的曲线,c(HA)近似为0.1mol/L, 。
2
A.由分析可知,K =10-3,A正确;
a1
B.b点溶液显酸性,氢氧根浓度很小,根据图知,c(HA-)>c(A2-),故c(HA-)>c(A2-)>c(OH-),B正确;
C.由a点经b点到c点的过程中,溶液一直呈酸性,且酸性越来越弱,酸抑制水电离程度越来越弱,故水
的电离程度一直增大,C正确;
D.pH=4.4时,c(HA-)=c(A2-),故 ,HA-的水解平衡常数
,故NaHA溶液显酸性, D错误;
故选D。
6.(2022·安徽合肥·三模)常温下,保持某含少量CaCO 浊液的水体中HCO 与空气中CO 的平衡,调节水
3 2 3 2
体pH,水体中-lg[c(X)]与pH的关系如下图所示(其中X为HCO、HCO 、CO 或Ca2+)。下列说法错误的
2 3 3
是
A.曲线II表示-lg[c(CO )]与pH的关系
B.该温度下,HCO 的电离常数K 的数量级为10-7
2 3 a1
C.a点的水体中:c(Ca2+)>c(HCO )>c(CO )
D.向水体中加入适量Ca(OH) 固体,可使溶液由b点变到c点
2【答案】D
【解析】根据图象分析,随着pH的增大,溶液的碱性增强, 、 的浓度都逐渐增大,-lg[c(X)]均
减小,随着 浓度增大,逐渐生成CaCO 沉淀,溶液中Ca2+逐渐减小,-lg[c(X)]逐渐增大,由于碳酸分
3
步电离,第一步电离产生 ,第二步电离时产生 ,且以第一步电离为主,则起始时 的浓度
大于 ,因此曲线Ⅲ代表 与pH的关系,曲线Ⅱ为 与pH的关系,曲线Ⅰ为
与pH的关系,。
A.由上述分析可知,曲线Ⅱ为 与pH的关系,选项A正确;
B.由图可知,a点时 ,此时HCO 的电离常数 ,数量
2 3
级为 ,选项B正确;
C.曲线Ⅲ代表 与pH的关系,曲线Ⅱ为 与pH的关系,曲线Ⅰ为
与pH的关系,经过a点作一条垂直与pH轴的直线,曲线Ⅱ在最上面,曲线Ⅲ在最下面,
因此a点的水体中: ,选项C正确;
D. ,向水体中加入适量Ca(OH) 固体, 、 减小,
2
增大,不能使溶液由b点变到c点,选项D错误;
答案选D。
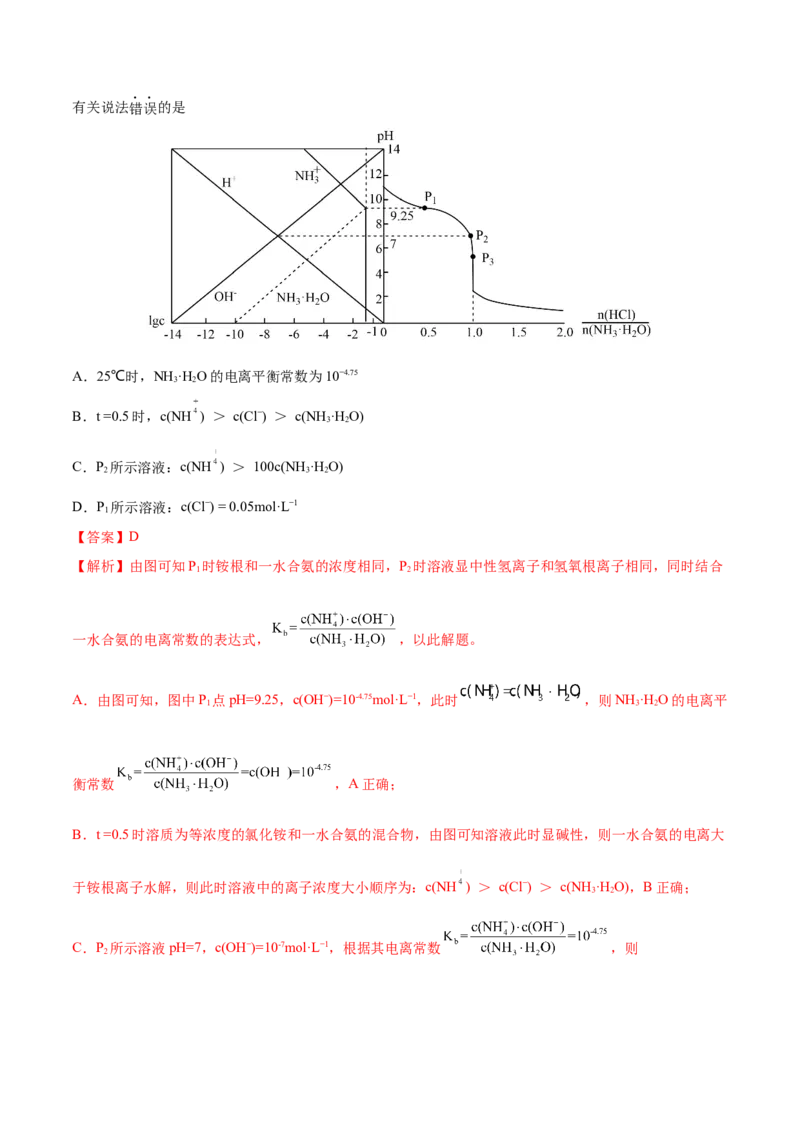
7.(2022·安徽黄山·二模)25℃时,将HCl气体缓慢通入0.1 mol·L−1的氨水中,溶液的pH、体系中粒子浓度
的对数值(lgc)与反应物的物质的量之比[ ]的关系如下图所示。若忽略溶液体积变化,下列有关说法错误的是
A.25℃时,NH ·H O的电离平衡常数为10−4.75
3 2
B.t =0.5时,c(NH ) > c(Cl−) > c(NH ·H O)
3 2
C.P 所示溶液:c(NH ) > 100c(NH ·H O)
2 3 2
D.P 所示溶液:c(Cl−) = 0.05mol·L−1
1
【答案】D
【解析】由图可知P 时铵根和一水合氨的浓度相同,P 时溶液显中性氢离子和氢氧根离子相同,同时结合
1 2
一水合氨的电离常数的表达式, ,以此解题。
A.由图可知,图中P 点pH=9.25,c(OH−)=10-4.75mol·L−1,此时 ,则NH ·H O的电离平
1 3 2
衡常数 ,A正确;
B.t =0.5时溶质为等浓度的氯化铵和一水合氨的混合物,由图可知溶液此时显碱性,则一水合氨的电离大
于铵根离子水解,则此时溶液中的离子浓度大小顺序为:c(NH ) > c(Cl−) > c(NH ·H O),B正确;
3 2
C.P 所示溶液pH=7,c(OH−)=10-7mol·L−1,根据其电离常数 ,则
2,故c(NH ) > 100c(NH ·H O),C正确;
3 2
D.P 所示溶液中电荷守恒, ,由图可知P 点时 ,且c(
1 1
)=10-1mol·L−1, ,则 ,
,D错误;
故选D。
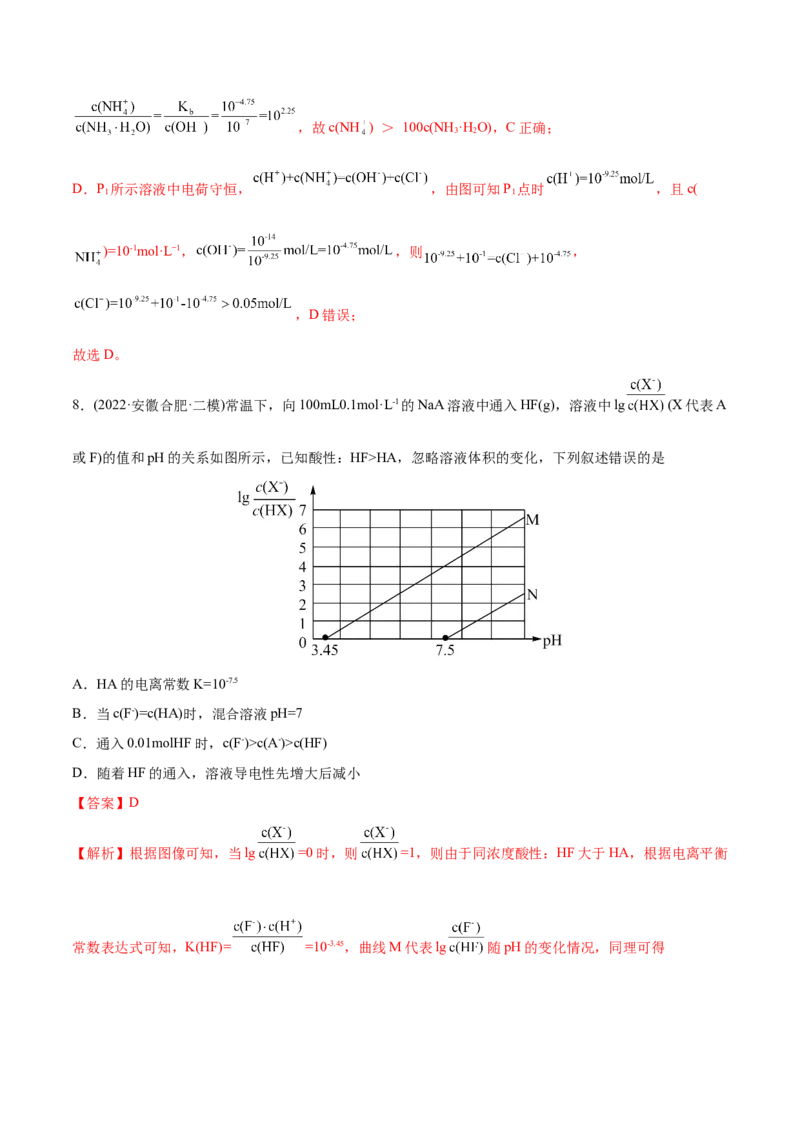
8.(2022·安徽合肥·二模)常温下,向100mL0.1mol·L-1的NaA溶液中通入HF(g),溶液中lg (X代表A
或F)的值和pH的关系如图所示,已知酸性:HF>HA,忽略溶液体积的变化,下列叙述错误的是
A.HA的电离常数K=10-7.5
B.当c(F-)=c(HA)时,混合溶液pH=7
C.通入0.01molHF时,c(F-)>c(A-)>c(HF)
D.随着HF的通入,溶液导电性先增大后减小
【答案】D
【解析】根据图像可知,当lg =0时,则 =1,则由于同浓度酸性:HF大于HA,根据电离平衡
常数表达式可知,K(HF)= =10-3.45,曲线M代表lg 随pH的变化情况,同理可得K(HA)=10-7.5,即曲线N表示lg 随pH的变化情况。
A.HA的电离常数K=10-7.5,A正确;
B.根据溶液中的电荷守恒可得c(Na+)+c(H+)=c(A-)+c(F-)+c(OH-),根据物料守恒c(A-)+c(HA)=c(Na+),
若溶液中c(F-)=c(HA),联立方程可得,得出c(H+)= c(OH-),即pH=7,B正确;
C.通入HF,发生反应为:HF+NaA=HA+NaF,通入0.01molHF时,HF与NaA恰好完全反应,溶液的溶
质为等浓度的HA和NaF,因为HA的电离平衡常数为K(HA)=10-7.5,根据HF的电离平衡常数可知,NaF
的水解平衡常数K(NaF)= ,推出溶液HA的电离程度大于F-的水解程度,所以离
h
子浓度大小关系为:c(F-)>c(A-)>c(HF) ,C正确;
D.通入HF,发生反应为:HF+NaA=HA+NaF,随着HF的增多,溶液中A-不断转化为F-,水解程度减弱,
总离子浓度增大,即溶液的导电性增大,当NaA恰好与HF反应完后,溶液中溶质为HF、HA和NaF,HF
会更多的电离出H+与F-,导电性也会增大,D错误;
故选D。
9.(2022·河南洛阳·三模)常温下,向10 mL一定浓度的硝酸银溶液中,逐滴加入0.1 mol·L-1的氨水,反应
过程中- 1gc(Ag+ )或-1gc([(Ag(NH)]+ )与加入氨水体积的关系如图所示。下列说法错误的是
3 2
A.常温下,K (AgOH)的数量级为10-8
sp
B.原硝酸银溶液的浓度是0.1 mol·L-1
C.溶液m点c( )-c(Ag+)-c( )=0.01 mol·L-1
D.溶液b点 的浓度大于溶液m点的 浓度【答案】C
【解析】向10mL一定浓度的硝酸银溶液中,逐滴加入0.1mol•L-1的氨水,首先发生反应:Ag+
+NH•H O=AgOH↓+NH +,継而发生AgOH+2NH•H O= +2H O+OH-;b点-1gc(Ag+ )达到最大值,
3 2 4 3 2 2
可认为此时Ag+与NH •H O恰好完全反应,阴离子完全沉淀,据此来分析。
3 2
A.b点溶液溶质为NH NO ,Ag+完全沉淀,存在沉淀溶解平衡AgOH(s)=Ag+(aq)+OH-(aq),所以可以近似
4 3
地认为c(Ag+)=c(OH-),此时-1gc(Ag+)=4,则c(Ag+)=c(OH-)=1×10-4mol,K (AgOH)=c(Ag+)•c(OH-)=1×10-8,
sp
A正确;
B.b点完全反应,此时加入的氨水为10mL,氨水的浓度0.1mol/L,原硝酸银溶液也为10mL,根据方程式
Ag++NH•H O=AgOH↓+NH +可知,硝酸银溶液的浓度为0.1mol/L,B正确;
3 2 4
C.m点溶液存在电荷守恒c(OH-)+c( )=c(Ag+)+c[ ]+c( )+c(H+),此时加入了过量的氨水,
溶液应呈碱性,则有:c( )-c(Ag+)-c( )= c[ ]+c(H+)-c(OH-)=10-2+c(H+)-c(OH-)<10-2mol/L,C
错误;
D.b点溶液溶质为NH NO ,b到m过程发生反应AgOH+2NH•H O= +2H O+OH-,随着氨水的
4 3 3 2 2
加入,并没有引入铵根离子,虽然碱性增强铵根离子的水解受到促进,则铵根离子的浓度减小,即b点铵
根离子的浓度大于溶液m点铵根离子的浓度,D正确;
故答案为:C。
10.(2022·河南开封·三模)谷氨酸[ HOOC(CH )CH(NH)COOH,用HR表示]是人体内的基本氨基酸之一,
2 2 2 2
在水溶液中存在如下平衡:HR HR- R2-。常温下,向一定浓度的HR溶液中滴加
2 2
NaOH溶液,混合溶液中lgx[x表示 或 ]随pOH[pOH=- lgc(OH- )] 的变化如图所示。下列说
法正确的是A.K=1×10-9.7
1
B.pH=7时,c(HR-)>c(HR)>c(R2-)
2
C.曲线II表示pOH与lg 的变化关系
D.M点时,c(H+ )+c(Na+ )=c(OH-)+3c(HR-)
【答案】D
【解析】由题意可知,k>k,一级电离时酸性最强,故曲线Ⅰ表示随pOH和lg 关系,曲线Ⅱ表示
1 2
随pOH和lg 关系。
A.k= ,当 ,pOH=9.7,则氢离子浓度为10-4.3mol/L,A项错误;
1
B.pH=7时,pOH=7,由曲线Ⅰ可知, 时, >0,则c(HR-)>c(R2-),由曲线Ⅱ可知,
<0,则c(HR-)>c(HR),但c(HR)和c(R2-)的大小关系无法判断,B项错误;
2 2
C.曲线Ⅱ表示随pOH和lg 关系,C项错误;
D.M点时, =0,c(HR-)=c(R2-),依据电荷守恒,c(H+ )+c(Na+ )=c(OH-)+c(HR-)+ 2c(R2-),则有
c(H+ )+c(Na+ )=c(OH-)+3c(HR-),D项正确。
故选D。
11.(2022·河南洛阳·二模)三甲胺[N(CH )]是一种一元有机弱碱,可简写为MOH。常温下,向
3 320mL0.5mol/LMOH溶液中逐滴加入浓度为0.25mol/L的HC1溶液,溶液中 ,
、中和率(中和率=被中和的MOH的物质的量/反应前MOH的总物质的量)的变化如图
所示。下列说法不正确的是
A.a点时,
B.b点时,
C.溶液中水的电离程度:c点>d点
D.三甲胺[N(CH )]的电离常数为
3 3
【答案】A
【解析】A.根据图示,a点中和率小于50%,根据物料守恒 ,故A错误;
B.b点时中和率为50%,溶质为等浓度的MOH和MCl,溶液呈碱性,说明MOH电离大于MCl水解,所
以 ,故B正确;
C.c点溶液中和率为100%,溶质只有MCl,d点盐酸过量,盐酸抑制水电离,所以水的电离程度c点>d
点,故C正确;
D.根据a点, 时c(OH-)=10-4.2,三甲胺[N(CH )]的电离常数 为 ,故D
3 3
正确;
选A。
11.(2022·河南新乡·三模)已知:AgA、Ag B都是难溶盐。室温下,向体积均为10mL、浓度均为
20.1mol·L-1的NaA溶液、NaB溶液中分别滴加0.1mol·L-1的AgNO 溶液,溶液中pX与AgNO 溶液体积的
2 3 3
关系如图所示[已知:pX=—lgc(A—)或—lgc(B2—)]。下列推断错误的是
A.室温下,K (Ag B)=4×10-3a
sp 2
B.对应溶液中c(Ag+):e>f
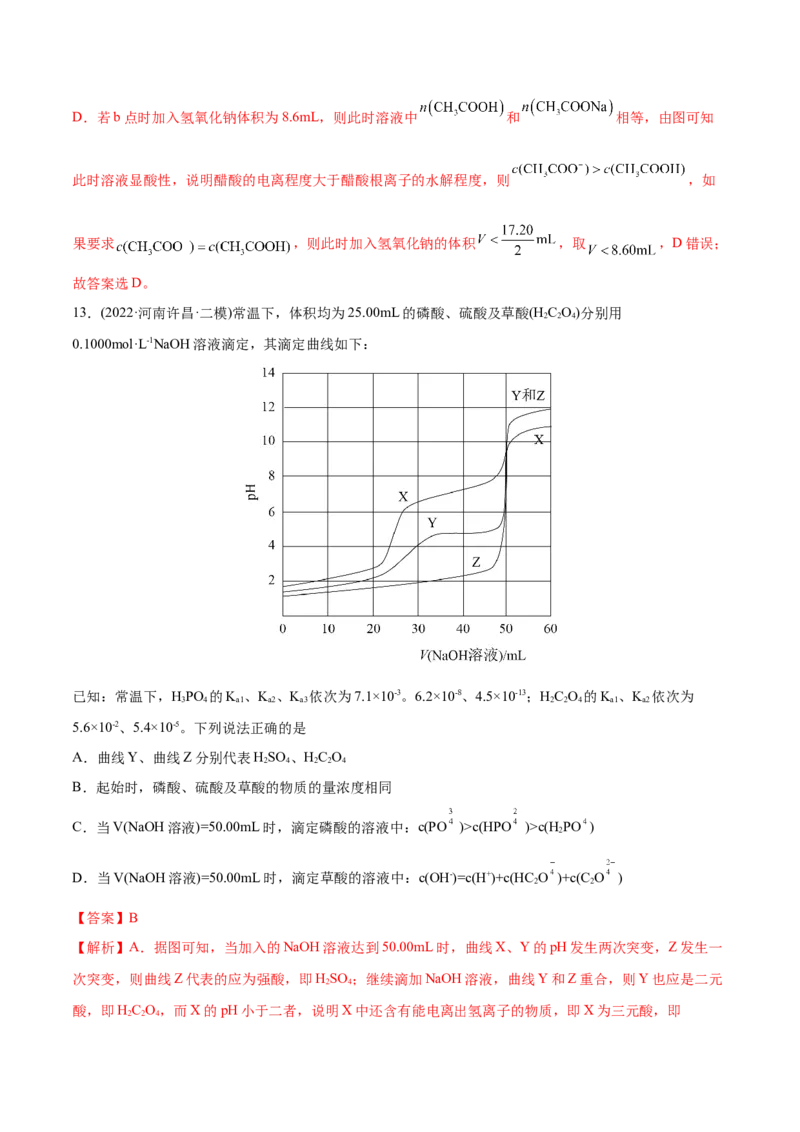
C.室温下,溶解度:S(AgA)c(HPO )>c(H PO )
2
D.当V(NaOH溶液)=50.00mL时,滴定草酸的溶液中:c(OH-)=c(H+)+c(HC O )+c(C O )
2 2
【答案】B
【解析】A.据图可知,当加入的NaOH溶液达到50.00mL时,曲线X、Y的pH发生两次突变,Z发生一
次突变,则曲线Z代表的应为强酸,即HSO ;继续滴加NaOH溶液,曲线Y和Z重合,则Y也应是二元
2 4
酸,即HC O,而X的pH小于二者,说明X中还含有能电离出氢离子的物质,即X为三元酸,即
2 2 4HPO ,A错误;
3 4
B.加入的50.00mLNaOH溶液后Y和Z重合,说明二者均完全反应,所以HSO 和HC O 的起始浓度相
2 4 2 2 4
同,滴定HPO 时依次发生反应HPO +NaOH=NaH PO +H O、NaH PO +NaOH=Na HPO +H O、
3 4 3 4 2 4 2 2 4 2 4 2
NaHPO +NaOH=Na PO +H O,每一步反应恰好进行完时pH发生一次突变,据图可知第二次突变时加入的
2 4 3 4 2
NaOH溶液为50.00mL,即反应掉“2个氢离子”时消耗的NaOH和另外两种二元酸相同,所以HPO 的起
3 4
始浓度与另外两种酸也相同,B正确;
C.V(NaOH溶液)=50.00mL时,滴定磷酸的溶液中溶质为NaHPO ,存在HPO 的电离和水解,据图可知
2 4
此时溶液显碱性,所以水解程度大于电离程度,且水解和电离都是微弱的,所以溶液中c(HPO )>c(HPO
2
)>c(PO ),C错误;
D.当V(NaOH溶液)=50.00mL时,滴定草酸的溶液中溶质为NaC O,存在质子守恒:c(OH-)=c(H+)
2 2 4
+c(HC O )+2c(H C O),且C O 由NaC O 电离产生,c(C O )远大于c(OH-),D错误;
2 2 2 4 2 2 2 4 2
综上所述答案为B。
14.(2022·山西太原·二模)某温度下,25 mL含KX和KY的混合溶液,用0.1000 mol·L-1的硝酸银标准溶液
对该混合液进行电位滴定(Y-与H+的反应可以忽略),获得电动势(E)和硝酸银标准溶液体积(V)的电位滴定曲
线如图所示。
已知:Ⅰ.Ag+与Y-反应过程为:①Ag++2Y-=[AgY]- 、②[AgY ]-+Ag+=2AgY↓
2 2
Ⅱ.该温度下,K (AgY)=2 ×10-16,K (AgX)=2 ×10-10。
sp sp
下列说法不正确的是
A.若HY为弱酸,则从开始到B点,水的电离程度不断减小
B.原混合溶液中c(KX )=0.02000 mol·L-1
C.若反应①的平衡常数为K,反应②的平衡常数为K,则 =K 2 (AgY)
1 2 spD.AgX(s)+Y-(aq) AgY(s)+X-(aq)的平衡常数为106
【答案】B
【解析】A.溶度积小的先生成沉淀,根据反应的方程式可知,B点生成AgY,若HY为弱酸,Y-被消耗,
HY的电离程度增大,H+浓度增大,抑制水的电离,则从开始到B点,水的电离程度不断减小,故A正确;
B.B点KY完全和AgNO 反应生成AgY,则 KX和硝酸银完全反应消耗V(AgNO )=(12.50-
3 3
5.00)mL=7.50mL,BC段发生反应 Ag++X-= AgX↓,则原溶液中c(X-)= 0.1000 mol·L-1×7.5×10-3L=7.5×10-
4mol,则c(KX )= 7.5×10-4mol ÷0.025L=0.03000 mol·L-1,故B错误;
C.①的平衡常数为K= ,反应②的平衡常数为K= ,K×K =
1 2 1 2
,Ag++Y-═AgY↓,K (AgY)=c(Ag+)×c(Y-)= ,则 =K 2 (AgY),故C正确;
sp sp
D.AgX(s)+Y-(aq) AgY(s)+X-(aq)的平衡常数为 = = =106,故D正确;
⇌
答案选B。
15.(2022·山西太原·一模)已知HA为一元弱酸,K 为HA的电离常数,25℃时,某混合溶液中c(HA)
a
+c(A-)=0.1 mol·L-1, lgc(HA)、lgc(A-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。下列说法错误的是
A.O点时,pH = 7
B.K(HA)的数量级为10-5
a
C.M点时,存在c(H+)=c(OH-)+ (A-)
C
D.该体系中,c(HA)= mol·L-1
【答案】C【解析】pH=-lgc(H+),所以随pH升高直线减小的是lgc(H+),则直线升高的是lgc(OH-),而pH升高时,
HA会与氢氧根发生反应HA+OH-=H O+A-,所以开始几乎不变,后续随pH增大而减少的是lgc(HA),随
2
pH增大而增加,后续几乎不变的是lgc(A-)。
A.据图可知O点处lgc(H+)=lgc(OH-),即c(H+)=c(OH-),溶液呈中性,温度为25℃,所以pH=7,A正确;
B.K(HA)= ,据图可知N点处c(A-)=c(HA),pH=4.74,即c(H+)=10-4.74mol/L,所以K(HA)=10-
a a
4.74,数量级为10-5,B正确;
C.据图可知M点处c(A-)=c(H+),C错误;
D.该体系中c(HA)+c(A-)=0.1 mol·L-1,即c(A-)=0.1mol/L-c(HA),c(HA)= = ,
解得c(HA)= mol/L,D正确;
综上所述答案为C。
16.(2022·吉林长春·二模)25 °C时,用0.1 mol·L-1 NaOH溶液滴定同浓度的HA溶液,HA被滴定分数
2 2
、pH及微粒分布分数 ,X表示HA、HA-或A2-]的关系如图所示:
2
下列说法正确的是
A.25 °C时,HA第一步电离平衡常数K ≈10-7
2 a1
B.c点溶液中: c(Na+)=2c(HA- )+ c(A2-)C.b点溶液中: c(Na+ )>c(HA- )> c(A2- )>c(H+ )> c(HA)>c(OH- )
2
D.a、b、c、d四点溶液中水的电离程度: c>d>b>a
【答案】B
【解析】由图可知,a、b、c、d所在实线为0.1 mol•L-1NaOH溶液滴定二元弱酸HA的滴定曲线,当
2
<1时,HA部分反应,溶液中溶质为NaHA和HA;当 =1时,反应生成NaHA,
2 2
NaHA溶液显酸性;当2> >1时,溶液中溶质为NaHA和NaA;当 =2时,反应生成
2
NaA,NaA溶液显碱性。
2 2
A. 25 °C时,pH=7时,c点c(HA- )= c(A2-),HA第二步电离平衡常数K = ≈10-
2 a2
7,HA第一步电离平衡常数K >10-7,故A错误;
2 a1
B.c点溶液中,溶液中溶质为NaHA和NaA,且c(HA-)=c(A2- ),由电荷守恒可知c(Na+)+c(H+)═c(HA-)
2
+c(OH-)+2c(A2- ),pH=7,c(H+)═c(OH-),故c(Na+)═c(HA-)+2c(A2- )═3c(HA-)==3c(A2- )= 2c(HA- )+ c(A2-),故
B正确;
C.b点溶液中,由图象可知c(Na+)>c(HA-)>c(A2- )>c(HA),b点pH<7,c(H+ )>c(OH- ),HA被滴定分
2 2
数 >1,c(OH- )> c(HA),故C错误;
2
D.未加氢氧化钠溶液时,HA电离出氢离子,抑制水的电离,加入氢氧化钠溶液,酸逐渐被中和为盐,
2
对水的抑制程度减弱,生成的NaHA、NaA能水解,促进水的电离,当酸碱恰好中和为NaA,即d点附
2 2
近(pH突变),对水的电离促进程度最大,故a、b、c、d四点溶液中水的电离程度:d>c>b>a,故D错误;
故选B。
17.(2022·陕西汉中·二模)常温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1的HPO 溶液,滴定过
3 2
程中混合溶液的pH随加入的NaOH溶液体积变化关系如图所示,下列说法不正确的是A.常温下,K (H PO )的数量级为10—5
a 3 2
B.B点对应的溶液中:2[c(H+)—c(OH—)]=c(H PO )—c(H PO )
2 3 2
C.HPO 为一元弱酸
3 2
D.滴定至V=20mL的过程中,溶液中由水电离出的c( H+)·(OH—)不变
【答案】D
【解析】由图可知,未加入氢氧化钠溶液时,0.1mol·L-1的HPO 溶液pH为3说明HPO 为弱酸,加入
3 2 3 2
20mL0.1mol·L-1氢氧化钠溶液时,20mL0.1mol·L-1的HPO 溶液恰好完全反应说明HPO 为一元弱酸,所得
3 2 3 2
NaH PO 溶液呈碱性。
2 2
A.由分析可知,0.1mol·L-1的HPO 溶液pH为3,则K (H PO )= =1.0×10—5,数量级
3 2 a 3 2
为10—5,故A正确;
B.由图可知,B点时氢氧化钠溶液与HPO 溶液反应得到等浓度的HPO 和NaH PO 混合溶液,溶液中存
3 2 3 2 2 2
在电荷守恒关系c(Na+)+ c(H+)= c(OH—)+c(H PO )和物料守恒关系2 c(Na+)= c(H PO )+c(H PO ),整合可
2 2 3 2
得2[c(H+)—c(OH—)]=c(H PO )—c(H PO ),故B正确;
2 3 2
C.由分析可知,HPO 为一元弱酸,故C正确;
3 2
D.由分析可知,HPO 为一元弱酸,加入20mL0.1mol·L-1氢氧化钠溶液时,20mL0.1mol·L-1的HPO 溶液
3 2 3 2
恰好完全反应说明HPO 为一元弱酸,所得NaH PO 溶液呈碱性,则HPO 离子在溶液中水解促进水的电
3 2 2 2 2
离,溶液中由水电离出的c( H+)·(OH—)增大,故D错误;
故选C。
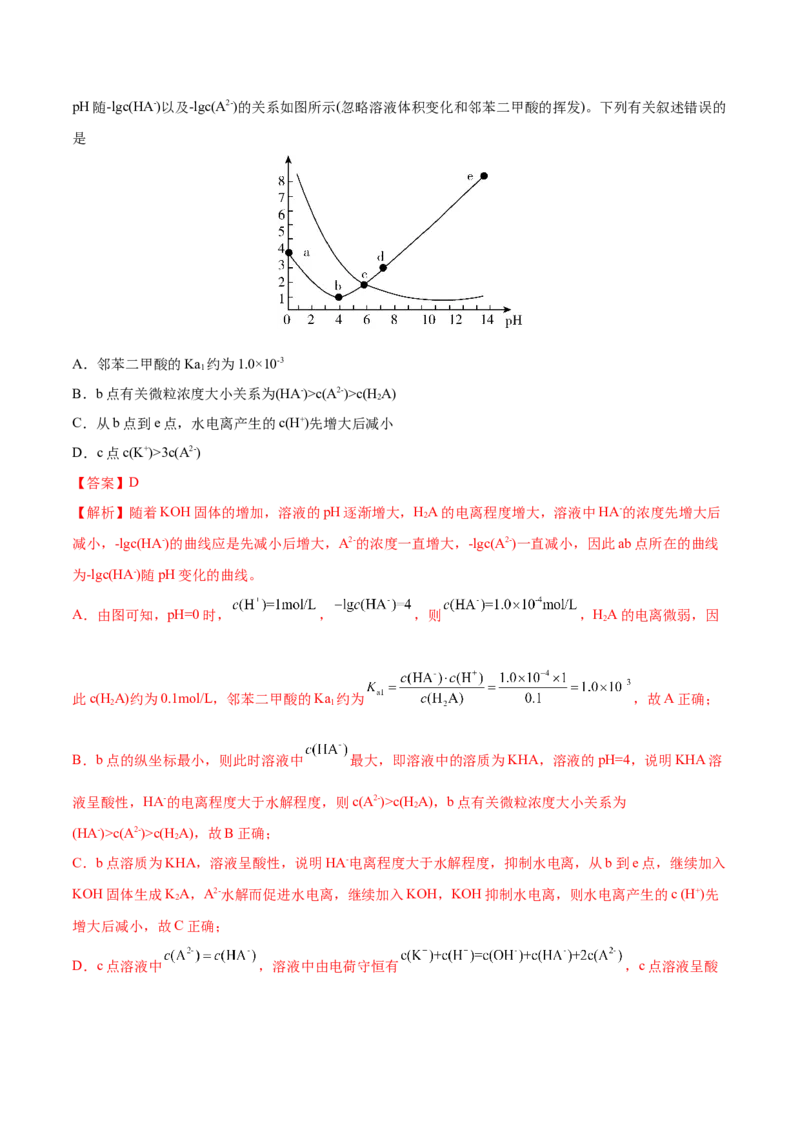
18.(2022·陕西宝鸡·三模)25℃时,向25mL0.lmol·L-1邻苯二甲酸(H A)溶液中加入KOH固体,混合溶液的
2pH随-lgc(HA-)以及-lgc(A2-)的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发)。下列有关叙述错误的
是
A.邻苯二甲酸的Ka 约为1.0×10-3
1
B.b点有关微粒浓度大小关系为(HA-)>c(A2-)>c(H A)
2
C.从b点到e点,水电离产生的c(H+)先增大后减小
D.c点c(K+)>3c(A2-)
【答案】D
【解析】随着KOH固体的增加,溶液的pH逐渐增大,HA的电离程度增大,溶液中HA-的浓度先增大后
2
减小,-lgc(HA-)的曲线应是先减小后增大,A2-的浓度一直增大,-lgc(A2-)一直减小,因此ab点所在的曲线
为-lgc(HA-)随pH变化的曲线。
A.由图可知,pH=0时, , ,则 ,HA的电离微弱,因
2
此c(HA)约为0.1mol/L,邻苯二甲酸的Ka 约为 ,故A正确;
2 1
B.b点的纵坐标最小,则此时溶液中 最大,即溶液中的溶质为KHA,溶液的pH=4,说明KHA溶
液呈酸性,HA-的电离程度大于水解程度,则c(A2-)>c(H A),b点有关微粒浓度大小关系为
2
(HA-)>c(A2-)>c(H A),故B正确;
2
C.b点溶质为KHA,溶液呈酸性,说明HA-电离程度大于水解程度,抑制水电离,从b到e点,继续加入
KOH固体生成KA,A2-水解而促进水电离,继续加入KOH,KOH抑制水电离,则水电离产生的c (H+)先
2
增大后减小,故C正确;
D.c点溶液中 ,溶液中由电荷守恒有 ,c点溶液呈酸性, ,则 ,故D错误;
答案选D。