文档内容
专题 15 化学反应原理综合题
1.工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NO )、SO 、CO等有害气体,对废气进行脱硝、脱
x 2
硫处理可实现绿色环保、废物利用。
(1)利用氢气还原法脱硝。
已知:①H 的燃烧热为285.8kJ/mol
2
②
写出在催化剂存在下,H 还原NO 生成液态水和无毒物质的热化学方程式:_______。
2 2
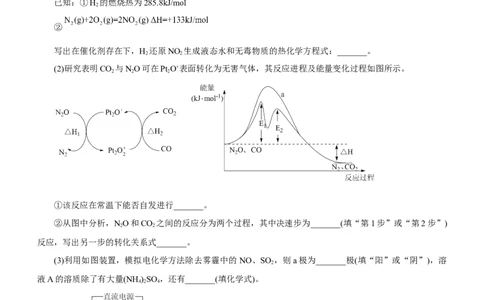
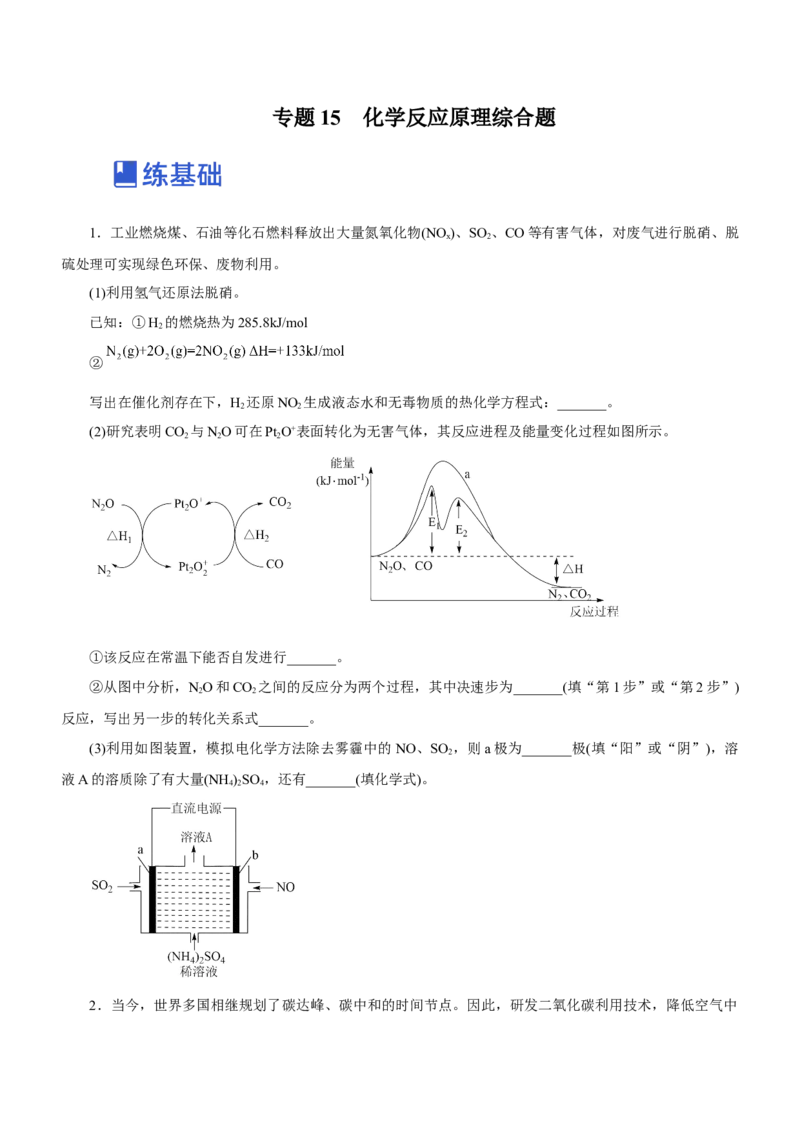
(2)研究表明CO 与NO可在Pt O+表面转化为无害气体,其反应进程及能量变化过程如图所示。
2 2 2
①该反应在常温下能否自发进行_______。
②从图中分析,NO和CO 之间的反应分为两个过程,其中决速步为_______(填“第1步”或“第2步”)
2 2
反应,写出另一步的转化关系式_______。
(3)利用如图装置,模拟电化学方法除去雾霾中的NO、SO ,则a极为_______极(填“阳”或“阴”),溶
2
液A的溶质除了有大量(NH )SO ,还有_______(填化学式)。
4 2 4
2.当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)以CO 与NH 为原料可合成尿素[CO(NH)]回收CO 并为农业服务,
2 3 2 2 2
已知:反应I.2NH(g)+CO (g)=NH CONH (s) △H=-159.47kJ•mol-1
3 2 2 2 4
反应Ⅱ.NHCONH (s)=CO(NH )(s)+HO(g) △H=+116.49kJ•mol-1
2 2 4 2 2 2
在相同条件下,反应2NH (g)+CO (g)=CO(NH )(s)+HO(g)正反应的活化能E 为225.36kJ/mol,则逆反应的
3 2 2 2 2 a
活化能E 为_____。
a
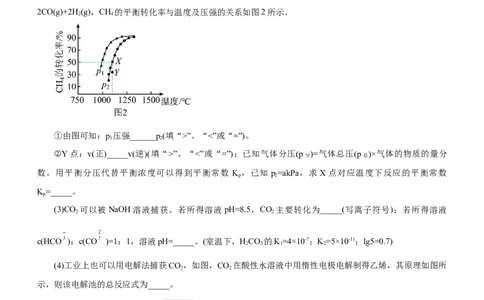
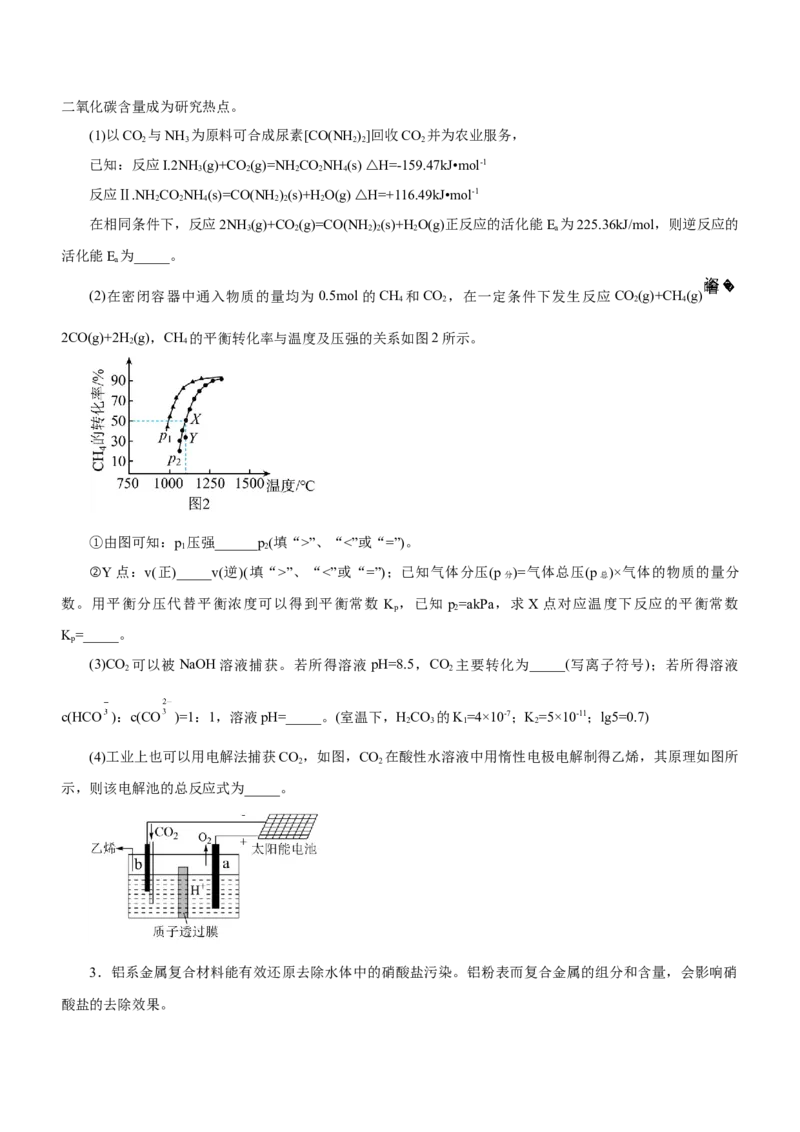
(2)在密闭容器中通入物质的量均为 0.5mol的CH 和CO ,在一定条件下发生反应CO(g)+CH (g)
4 2 2 4
2CO(g)+2H(g),CH 的平衡转化率与温度及压强的关系如图2所示。
2 4
①由图可知:p 压强______p(填“>”、“<”或“=”)。
1 2
②Y点:v(正)_____v(逆)(填“>”、“<”或“=”);已知气体分压(p
分
)=气体总压(p
总
)×气体的物质的量分
数。用平衡分压代替平衡浓度可以得到平衡常数 K ,已知p=akPa,求X点对应温度下反应的平衡常数
p 2
K=_____。
p
(3)CO 可以被NaOH溶液捕获。若所得溶液 pH=8.5,CO 主要转化为_____(写离子符号);若所得溶液
2 2
c(HCO ):c(CO )=1:1,溶液pH=_____。(室温下,HCO 的K=4×10-7;K=5×10-11;lg5=0.7)
2 3 1 2
(4)工业上也可以用电解法捕获CO ,如图,CO 在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所
2 2
示,则该电解池的总反应式为_____。
3.铝系金属复合材料能有效还原去除水体中的硝酸盐污染。铝粉表而复合金属的组分和含量,会影响硝
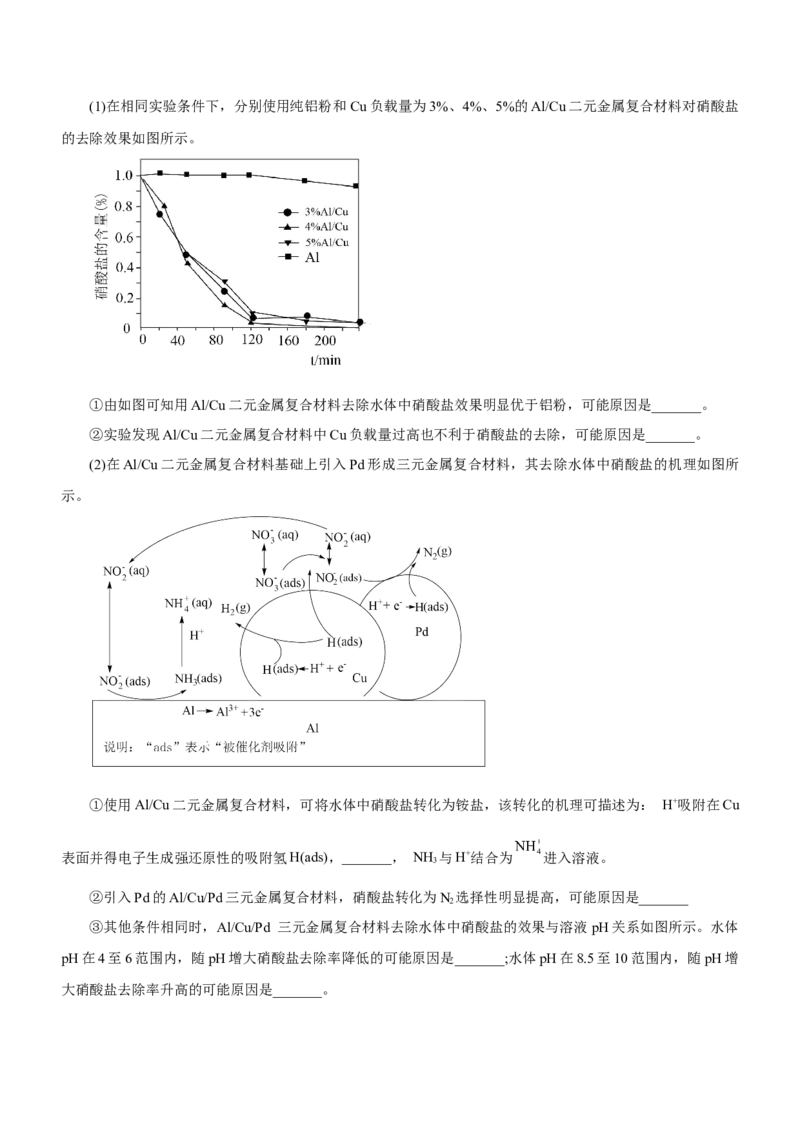
酸盐的去除效果。(1)在相同实验条件下,分别使用纯铝粉和Cu负载量为3%、4%、5%的Al/Cu二元金属复合材料对硝酸盐
的去除效果如图所示。
①由如图可知用Al/Cu二元金属复合材料去除水体中硝酸盐效果明显优于铝粉,可能原因是_______。
②实验发现Al/Cu二元金属复合材料中Cu负载量过高也不利于硝酸盐的去除,可能原因是_______。
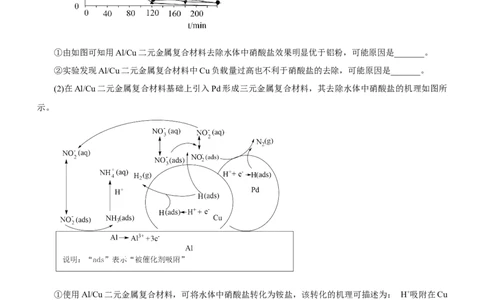
(2)在Al/Cu二元金属复合材料基础上引入Pd形成三元金属复合材料,其去除水体中硝酸盐的机理如图所
示。
①使用Al/Cu二元金属复合材料,可将水体中硝酸盐转化为铵盐,该转化的机理可描述为: H+吸附在Cu
表面并得电子生成强还原性的吸附氢H(ads),_______, NH 与H+结合为 进入溶液。
3
②引入Pd的Al/Cu/Pd三元金属复合材料,硝酸盐转化为N 选择性明显提高,可能原因是_______
2
③其他条件相同时,Al/Cu/Pd 三元金属复合材料去除水体中硝酸盐的效果与溶液pH关系如图所示。水体
pH在4至6范围内,随pH增大硝酸盐去除率降低的可能原因是_______;水体pH在8.5至10范围内,随pH增
大硝酸盐去除率升高的可能原因是_______。4.甲醇是重要的化工原料,研究甲醇的制备及用途在工业上有重要的意义。
一种工业制备甲醇的反应为
(1)向某容器中通入一定量 CO 和H 发生反应,达到平衡后,下列措施能提高CHOH平衡产率的有
2 2 3
_______(填标号)。
a.恒压下,充入惰性气体 b.加入高效催化剂
c.恒容下,充入CO d.适当升高温度
2
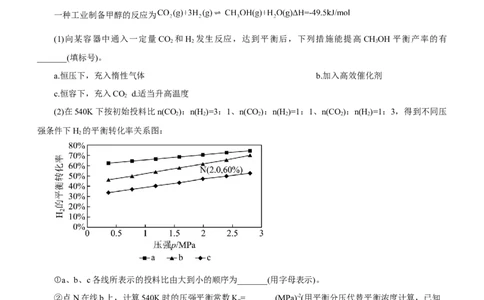
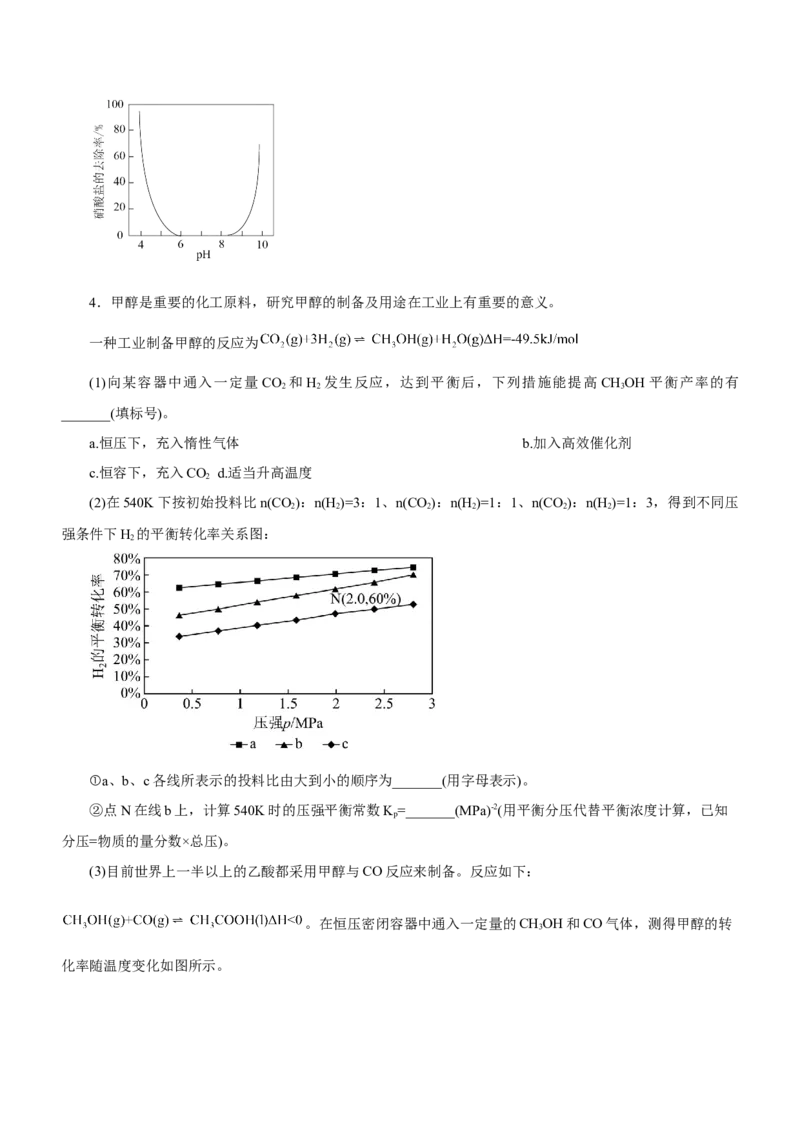
(2)在540K下按初始投料比n(CO):n(H )=3:1、n(CO):n(H )=1:1、n(CO):n(H )=1:3,得到不同压
2 2 2 2 2 2
强条件下H 的平衡转化率关系图:
2
①a、b、c各线所表示的投料比由大到小的顺序为_______(用字母表示)。
②点N在线b上,计算540K时的压强平衡常数K=_______(MPa)-2(用平衡分压代替平衡浓度计算,已知
p
分压=物质的量分数×总压)。
(3)目前世界上一半以上的乙酸都采用甲醇与CO反应来制备。反应如下:
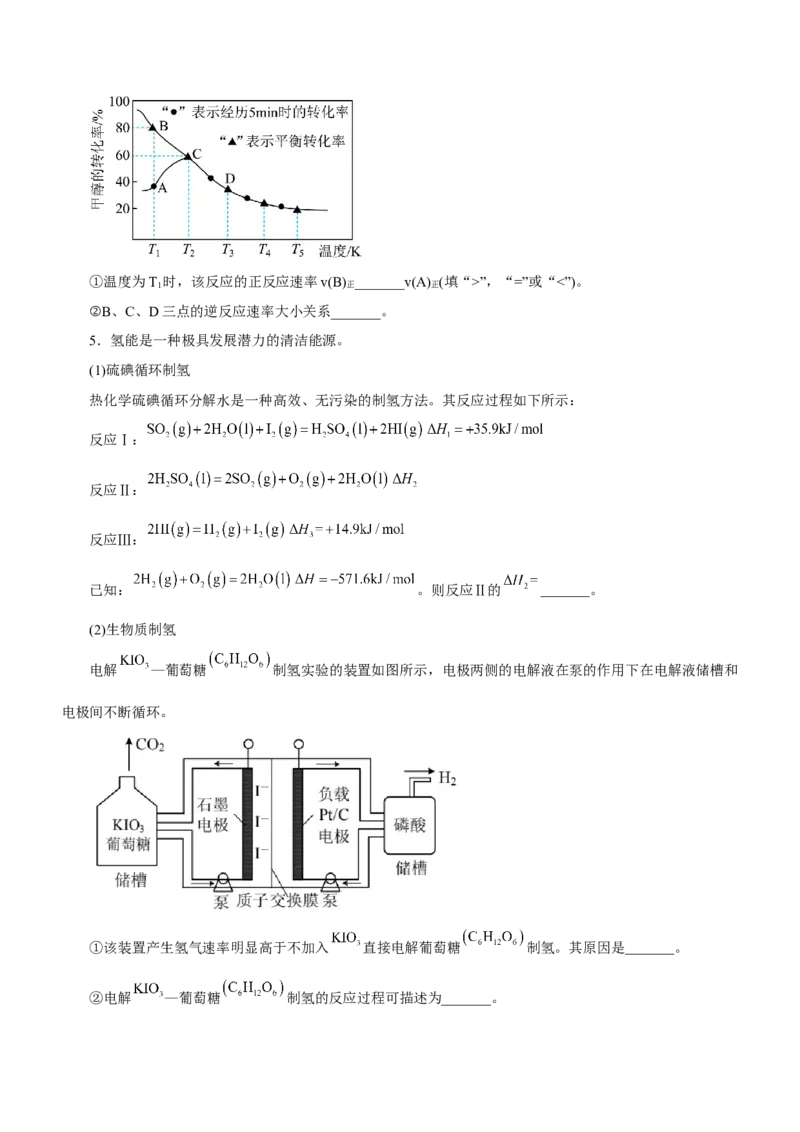
。在恒压密闭容器中通入一定量的CHOH和CO气体,测得甲醇的转
3
化率随温度变化如图所示。①温度为T 时,该反应的正反应速率v(B) _______v(A) (填“>”,“=”或“<”)。
1 正 正
②B、C、D三点的逆反应速率大小关系_______。
5.氢能是一种极具发展潜力的清洁能源。
(1)硫碘循环制氢
热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下所示:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
已知: 。则反应Ⅱ的 _______。
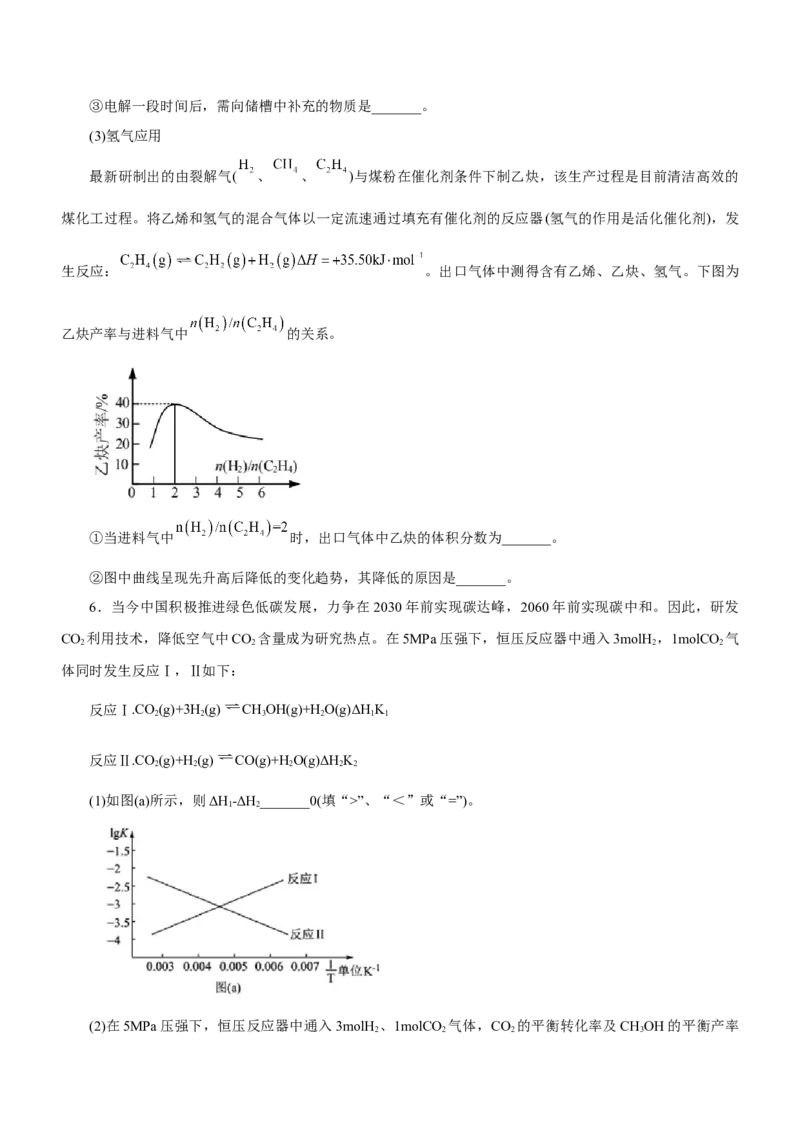
(2)生物质制氢
电解 —葡萄糖 制氢实验的装置如图所示,电极两侧的电解液在泵的作用下在电解液储槽和
电极间不断循环。
①该装置产生氢气速率明显高于不加入 直接电解葡萄糖 制氢。其原因是_______。
②电解 —葡萄糖 制氢的反应过程可描述为_______。③电解一段时间后,需向储槽中补充的物质是_______。
(3)氢气应用
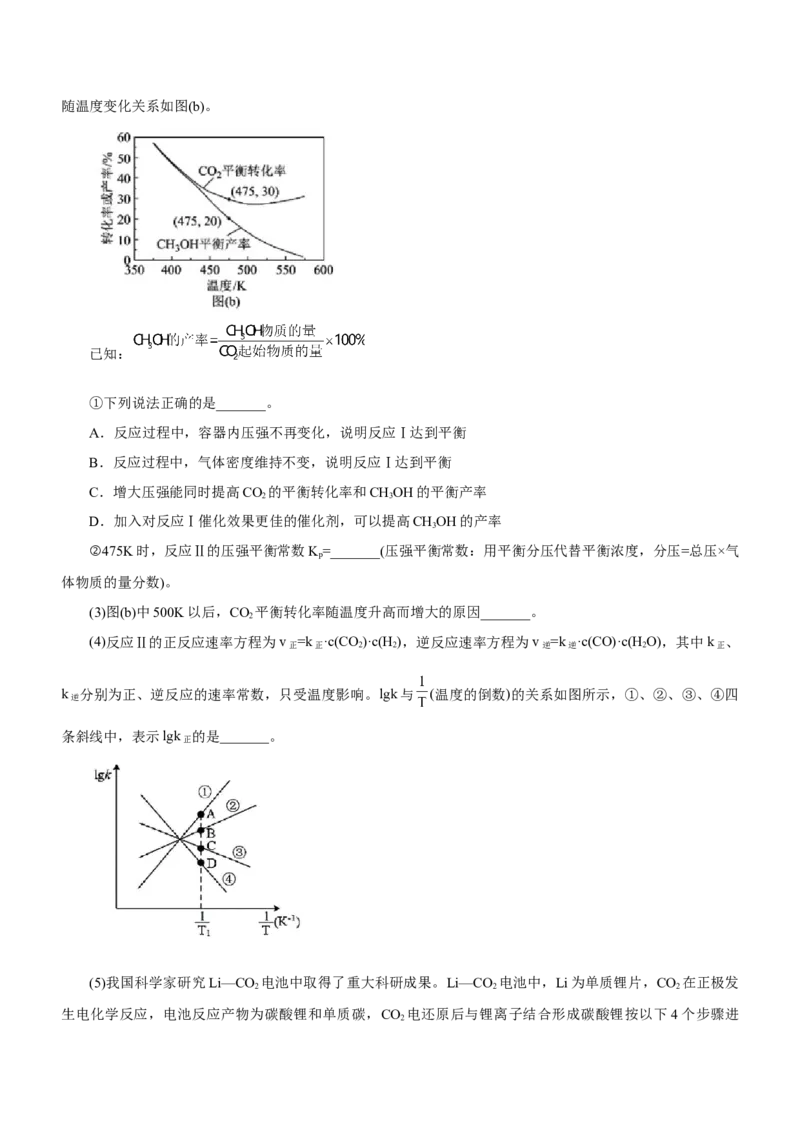
最新研制出的由裂解气( 、 、 )与煤粉在催化剂条件下制乙炔,该生产过程是目前清洁高效的
煤化工过程。将乙烯和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),发
生反应: 。出口气体中测得含有乙烯、乙炔、氢气。下图为
乙炔产率与进料气中 的关系。
①当进料气中 时,出口气体中乙炔的体积分数为_______。
②图中曲线呈现先升高后降低的变化趋势,其降低的原因是_______。
6.当今中国积极推进绿色低碳发展,力争在 2030年前实现碳达峰,2060年前实现碳中和。因此,研发
CO 利用技术,降低空气中CO 含量成为研究热点。在5MPa压强下,恒压反应器中通入3molH ,1molCO 气
2 2 2 2
体同时发生反应Ⅰ,Ⅱ如下:
反应Ⅰ.CO (g)+3H(g) CHOH(g)+H O(g)ΔH K
2 2 3 2 1 1
反应Ⅱ.CO (g)+H(g) CO(g)+HO(g)ΔH K
2 2 2 2 2
(1)如图(a)所示,则ΔH-ΔH _______0(填“>”、“<”或“=”)。
1 2
(2)在5MPa压强下,恒压反应器中通入3molH 、1molCO 气体,CO 的平衡转化率及CHOH的平衡产率
2 2 2 3随温度变化关系如图(b)。
已知:
①下列说法正确的是_______。
A.反应过程中,容器内压强不再变化,说明反应Ⅰ达到平衡
B.反应过程中,气体密度维持不变,说明反应Ⅰ达到平衡
C.增大压强能同时提高CO 的平衡转化率和CHOH的平衡产率
2 3
D.加入对反应Ⅰ催化效果更佳的催化剂,可以提高CHOH的产率
3
②475K时,反应Ⅱ的压强平衡常数K=_______(压强平衡常数:用平衡分压代替平衡浓度,分压=总压×气
p
体物质的量分数)。
(3)图(b)中500K以后,CO 平衡转化率随温度升高而增大的原因_______。
2
(4)反应Ⅱ的正反应速率方程为v =k ·c(CO)·c(H),逆反应速率方程为v =k ·c(CO)·c(H O),其中k 、
正 正 2 2 逆 逆 2 正
k 分别为正、逆反应的速率常数,只受温度影响。lgk与 (温度的倒数)的关系如图所示,①、②、③、④四
逆
条斜线中,表示lgk 的是_______。
正
(5)我国科学家研究Li—CO 电池中取得了重大科研成果。Li—CO 电池中,Li为单质锂片,CO 在正极发
2 2 2
生电化学反应,电池反应产物为碳酸锂和单质碳,CO 电还原后与锂离子结合形成碳酸锂按以下4个步骤进
2行,写出步骤Ⅲ的离子方程式_______。
Ⅰ.
Ⅱ.
Ⅲ.……
Ⅳ.
7.中国自古有“信口雌黄”、“雄黄入药”之说。雌黄 和雄黄 都是自然界中常见的砷化物,
早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
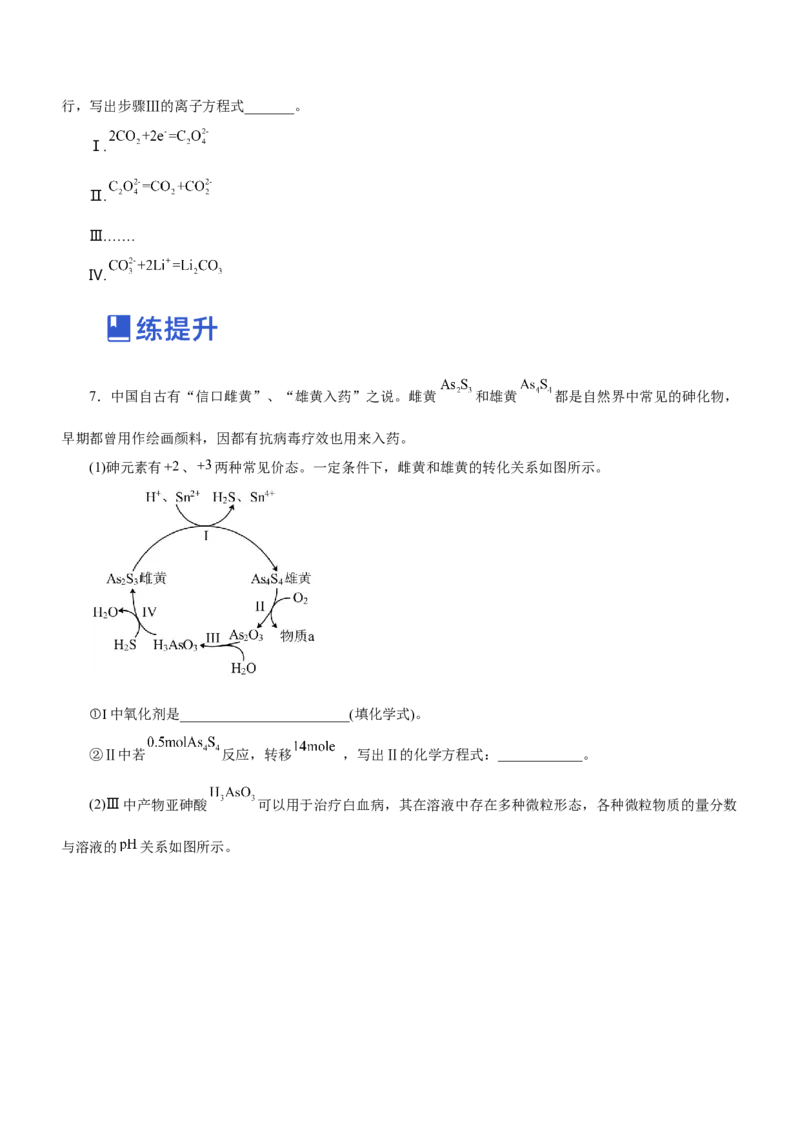
(1)砷元素有 、 两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。
①I中氧化剂是________________________(填化学式)。
②Ⅱ中若 反应,转移 ,写出Ⅱ的化学方程式:____________。
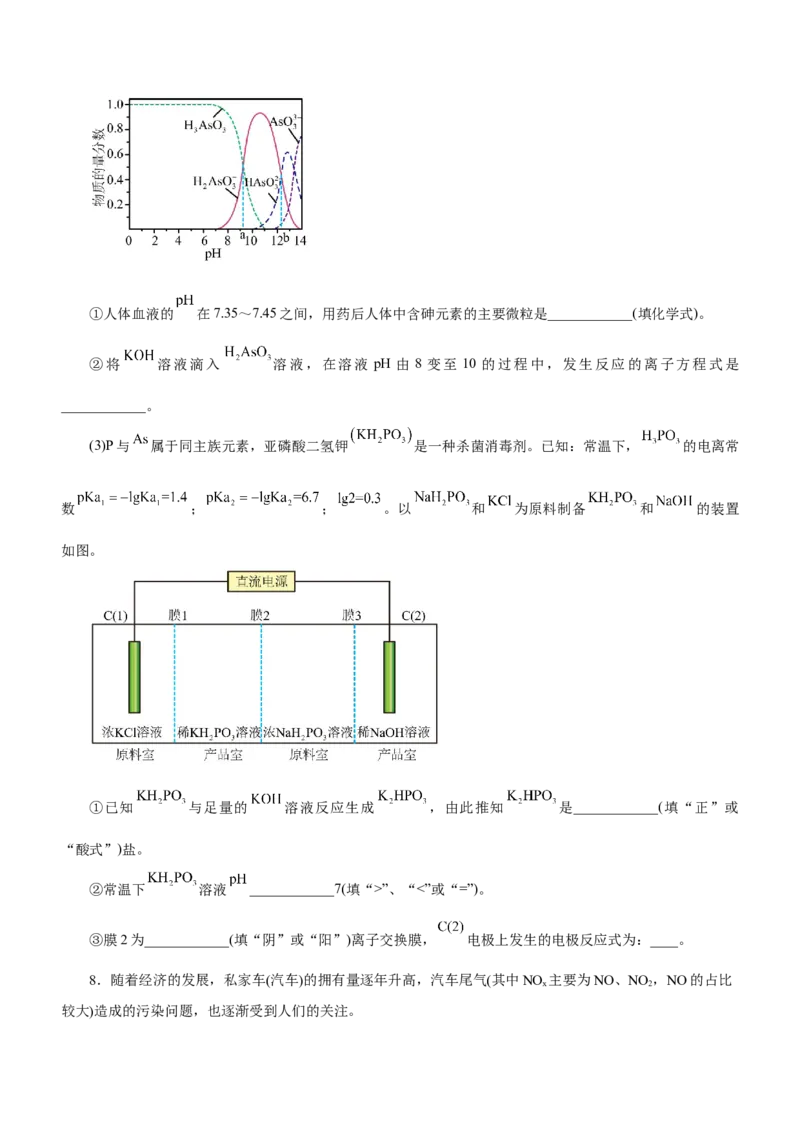
(2)Ⅲ中产物亚砷酸 可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数
与溶液的 关系如图所示。①人体血液的 在7.35~7.45之间,用药后人体中含砷元素的主要微粒是____________(填化学式)。
②将 溶液滴入 溶液,在溶液 pH 由 8 变至 10 的过程中,发生反应的离子方程式是
____________。
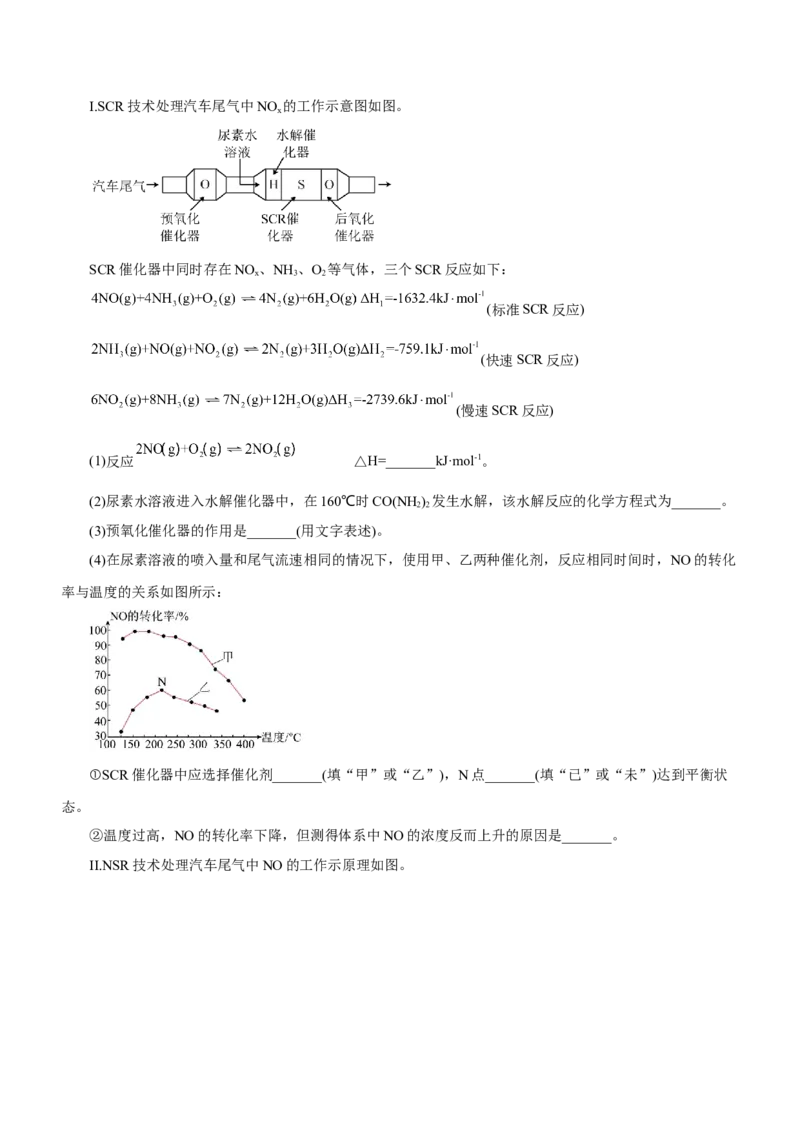
(3)P与 属于同主族元素,亚磷酸二氢钾 是一种杀菌消毒剂。已知:常温下, 的电离常
数 ; ; 。以 和 为原料制备 和 的装置
如图。
①已知 与足量的 溶液反应生成 ,由此推知 是____________(填“正”或
“酸式”)盐。
②常温下 溶液 ____________7(填“>”、“<”或“=”)。
③膜2为____________(填“阴”或“阳”)离子交换膜, 电极上发生的电极反应式为:____。
8.随着经济的发展,私家车(汽车)的拥有量逐年升高,汽车尾气(其中NO 主要为NO、NO ,NO的占比
x 2
较大)造成的污染问题,也逐渐受到人们的关注。I.SCR技术处理汽车尾气中NO 的工作示意图如图。
x
SCR催化器中同时存在NO 、NH 、O 等气体,三个SCR反应如下:
x 3 2
(标准SCR反应)
(快速SCR反应)
(慢速SCR反应)
(1)反应 △H=_______kJ·mol-1。
(2)尿素水溶液进入水解催化器中,在160℃时CO(NH) 发生水解,该水解反应的化学方程式为_______。
2 2
(3)预氧化催化器的作用是_______(用文字表述)。
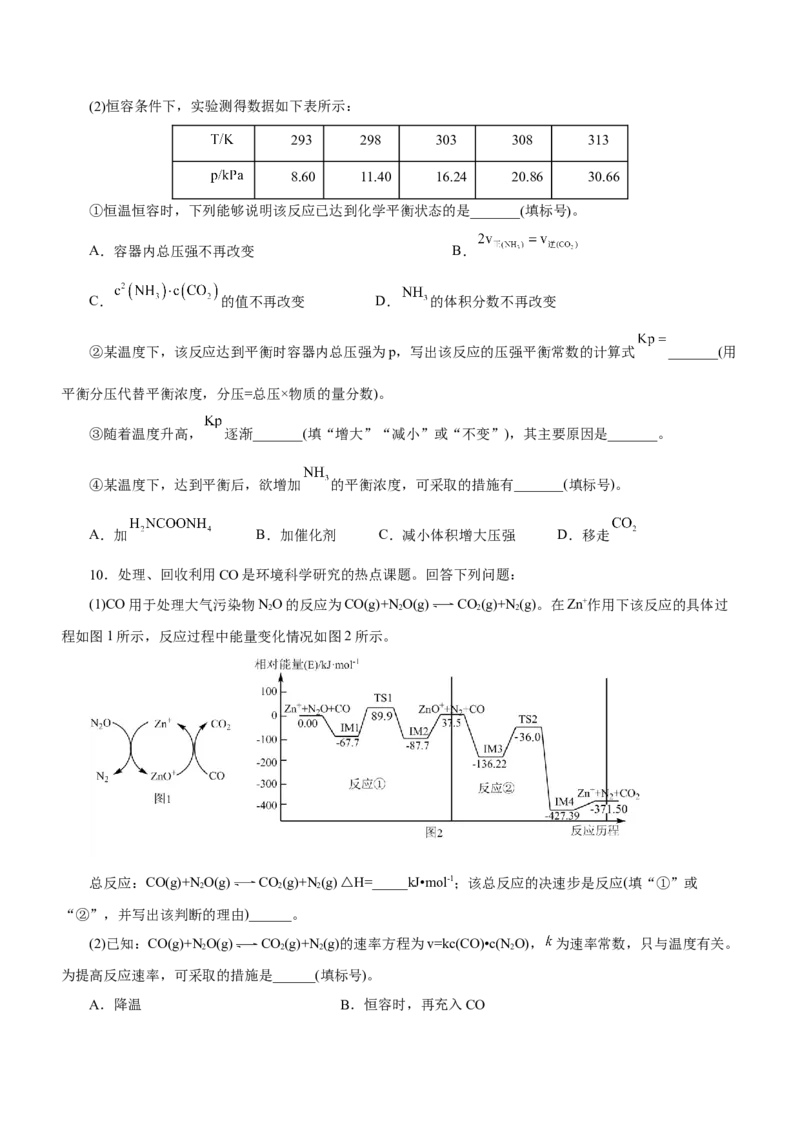
(4)在尿素溶液的喷入量和尾气流速相同的情况下,使用甲、乙两种催化剂,反应相同时间时,NO的转化
率与温度的关系如图所示:
①SCR催化器中应选择催化剂_______(填“甲”或“乙”),N点_______(填“已”或“未”)达到平衡状
态。
②温度过高,NO的转化率下降,但测得体系中NO的浓度反而上升的原因是_______。
II.NSR技术处理汽车尾气中NO的工作示原理如图。(5)富氧条件下,NO 被储存为Ba(NO ),发生反应的化学方程式为_______;贫氧条件下,NO 被H 还原
x 3 2 x 2
时,n(NO ):n(H )=_______。
x 2
Ⅲ.在汽车排气系统安装三元催化转化器,可发生反应: 。在一
定温度下,向容积为2L的恒容密闭容器中充入等物质的量的NO(g)和CO(g)发生上述反应,反应过程中c(NO)
随时间变化曲线如图所示。
(6) 此温度下,该反应的平衡常数为_______,若在反应达到平衡后,在其他条件保持不变时,向容器中
再充入0.5 mol NO(g)和0.5molCO(g),则此时v _______(填“>”“<”或“=”)v 。
2 正 逆
9.氨基甲酸铵 为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行
探究。
已知:I.
II.
III.
回答下列问题:
(1)写出 分解生成 与 气体的热化学方程式:_______。(2)恒容条件下,实验测得数据如下表所示:
293 298 303 308 313
8.60 11.40 16.24 20.86 30.66
①恒温恒容时,下列能够说明该反应已达到化学平衡状态的是_______(填标号)。
A.容器内总压强不再改变 B.
C. 的值不再改变 D. 的体积分数不再改变
②某温度下,该反应达到平衡时容器内总压强为p,写出该反应的压强平衡常数的计算式 _______(用
平衡分压代替平衡浓度,分压=总压×物质的量分数)。
③随着温度升高, 逐渐_______(填“增大”“减小”或“不变”),其主要原因是_______。
④某温度下,达到平衡后,欲增加 的平衡浓度,可采取的措施有_______(填标号)。
A.加 B.加催化剂 C.减小体积增大压强 D.移走
10.处理、回收利用CO是环境科学研究的热点课题。回答下列问题:
(1)CO用于处理大气污染物NO的反应为CO(g)+NO(g) CO(g)+N(g)。在Zn+作用下该反应的具体过
2 2 2 2
程如图1所示,反应过程中能量变化情况如图2所示。
总反应:CO(g)+NO(g) CO(g)+N(g) △H=_____kJ•mol-1;该总反应的决速步是反应(填“①”或
2 2 2
“②”,并写出该判断的理由)______。
(2)已知:CO(g)+NO(g) CO(g)+N(g)的速率方程为v=kc(CO)•c(N O), 为速率常数,只与温度有关。
2 2 2 2
为提高反应速率,可采取的措施是______(填标号)。
A.降温 B.恒容时,再充入COC.恒压时,再充入NO D.减压
2
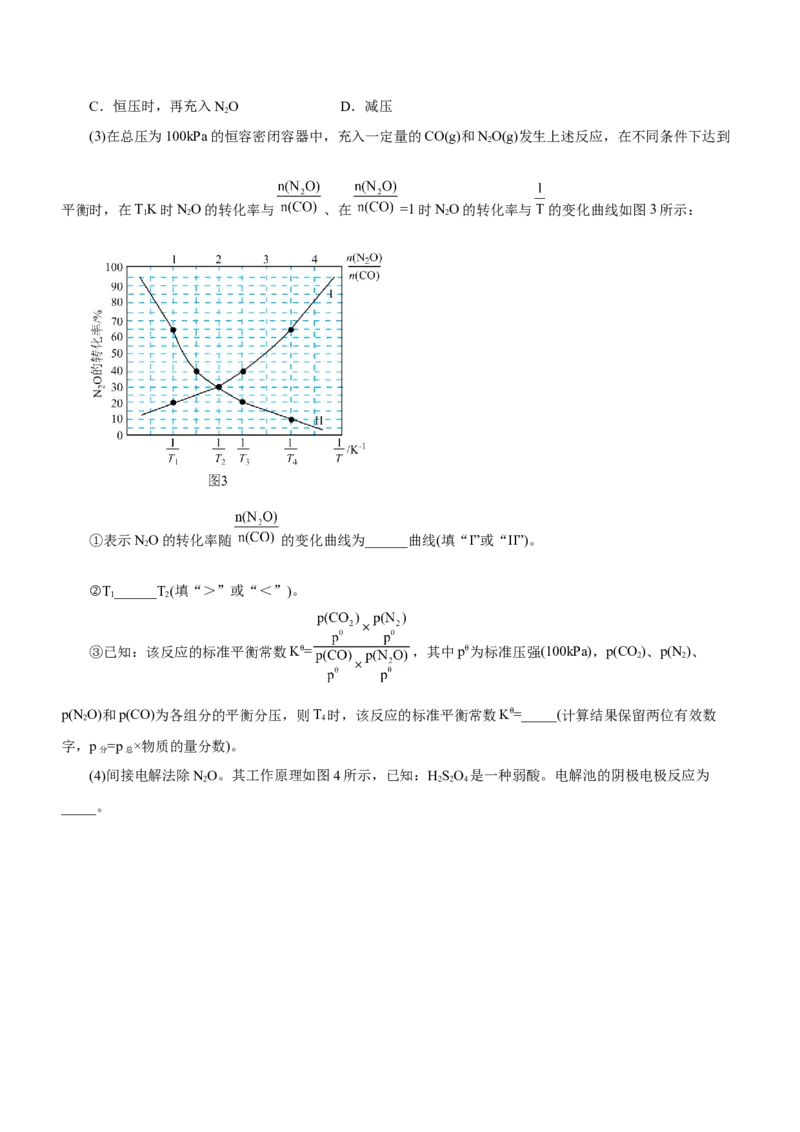
(3)在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和NO(g)发生上述反应,在不同条件下达到
2
平衡时,在TK时NO的转化率与 、在 =1时NO的转化率与 的变化曲线如图3所示:
1 2 2
①表示NO的转化率随 的变化曲线为______曲线(填“I”或“II”)。
2
②T ______T(填“>”或“<”)。
1 2
③已知:该反应的标准平衡常数Kθ= ,其中pθ为标准压强(100kPa),p(CO)、p(N )、
2 2
p(N O)和p(CO)为各组分的平衡分压,则T 时,该反应的标准平衡常数Kθ=_____(计算结果保留两位有效数
2 4
字,p =p ×物质的量分数)。
分 总
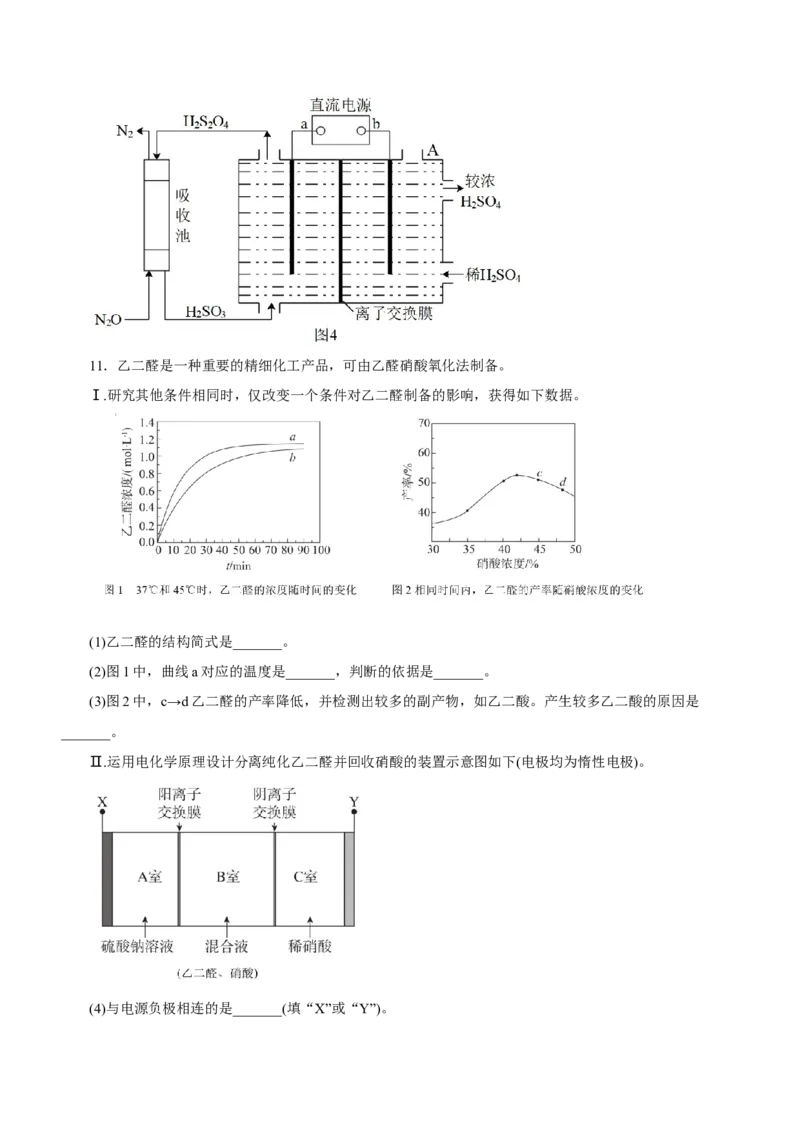
(4)间接电解法除NO。其工作原理如图4所示,已知:HSO 是一种弱酸。电解池的阴极电极反应为
2 2 2 4
_____。11.乙二醛是一种重要的精细化工产品,可由乙醛硝酸氧化法制备。
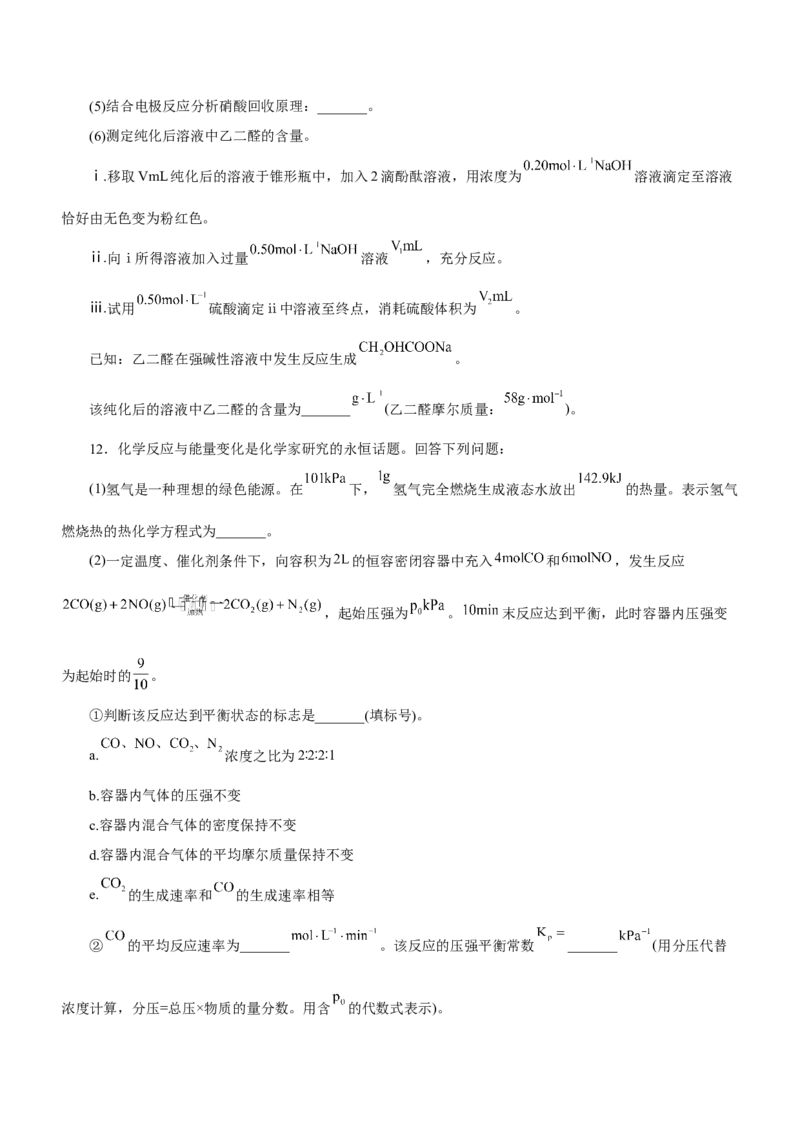
Ⅰ.研究其他条件相同时,仅改变一个条件对乙二醛制备的影响,获得如下数据。
(1)乙二醛的结构简式是_______。
(2)图1中,曲线a对应的温度是_______,判断的依据是_______。
(3)图2中,c→d乙二醛的产率降低,并检测出较多的副产物,如乙二酸。产生较多乙二酸的原因是
_______。
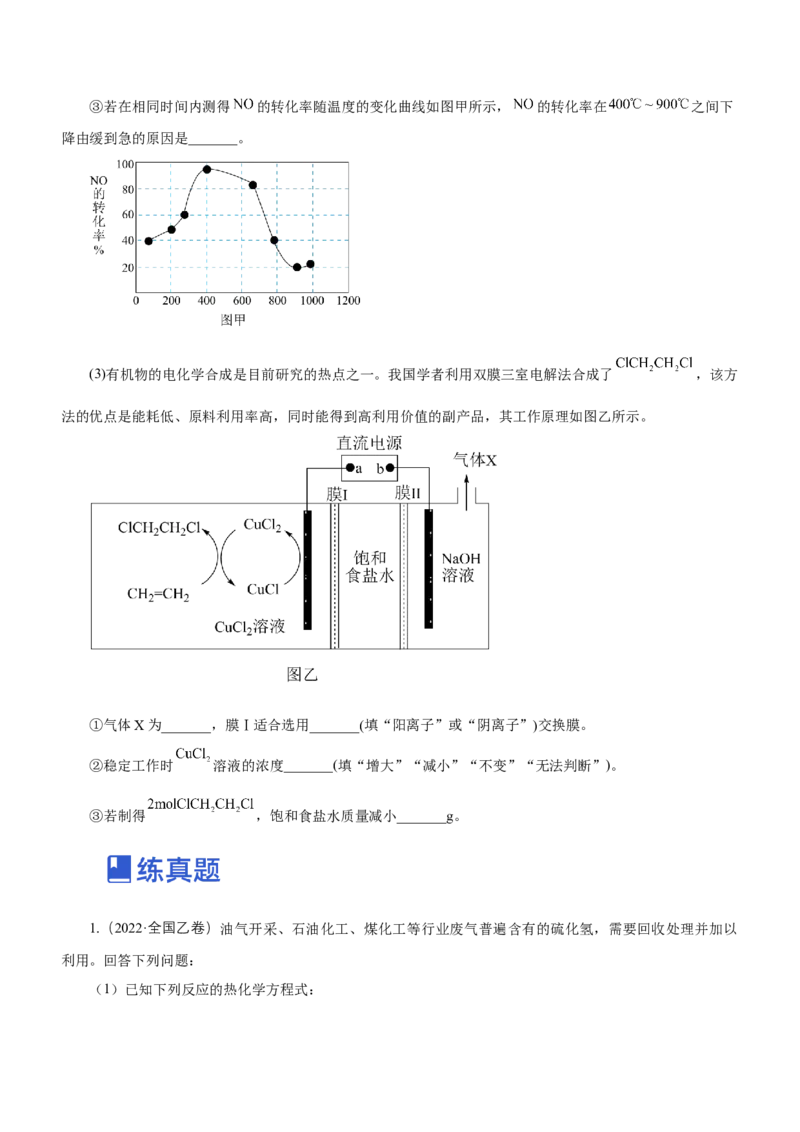
Ⅱ.运用电化学原理设计分离纯化乙二醛并回收硝酸的装置示意图如下(电极均为惰性电极)。
(4)与电源负极相连的是_______(填“X”或“Y”)。(5)结合电极反应分析硝酸回收原理:_______。
(6)测定纯化后溶液中乙二醛的含量。
ⅰ.移取VmL纯化后的溶液于锥形瓶中,加入2滴酚酞溶液,用浓度为 溶液滴定至溶液
恰好由无色变为粉红色。
ⅱ.向ⅰ所得溶液加入过量 溶液 ,充分反应。
ⅲ.试用 硫酸滴定ⅱ中溶液至终点,消耗硫酸体积为 。
已知:乙二醛在强碱性溶液中发生反应生成 。
该纯化后的溶液中乙二醛的含量为_______ (乙二醛摩尔质量: )。
12.化学反应与能量变化是化学家研究的永恒话题。回答下列问题:
(1)氢气是一种理想的绿色能源。在 下, 氢气完全燃烧生成液态水放出 的热量。表示氢气
燃烧热的热化学方程式为_______。
(2)一定温度、催化剂条件下,向容积为 的恒容密闭容器中充入 和 ,发生反应
,起始压强为 。 末反应达到平衡,此时容器内压强变
为起始时的 。
①判断该反应达到平衡状态的标志是_______(填标号)。
a. 浓度之比为2∶2∶2∶1
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.容器内混合气体的平均摩尔质量保持不变
e. 的生成速率和 的生成速率相等
② 的平均反应速率为_______ 。该反应的压强平衡常数 _______ (用分压代替
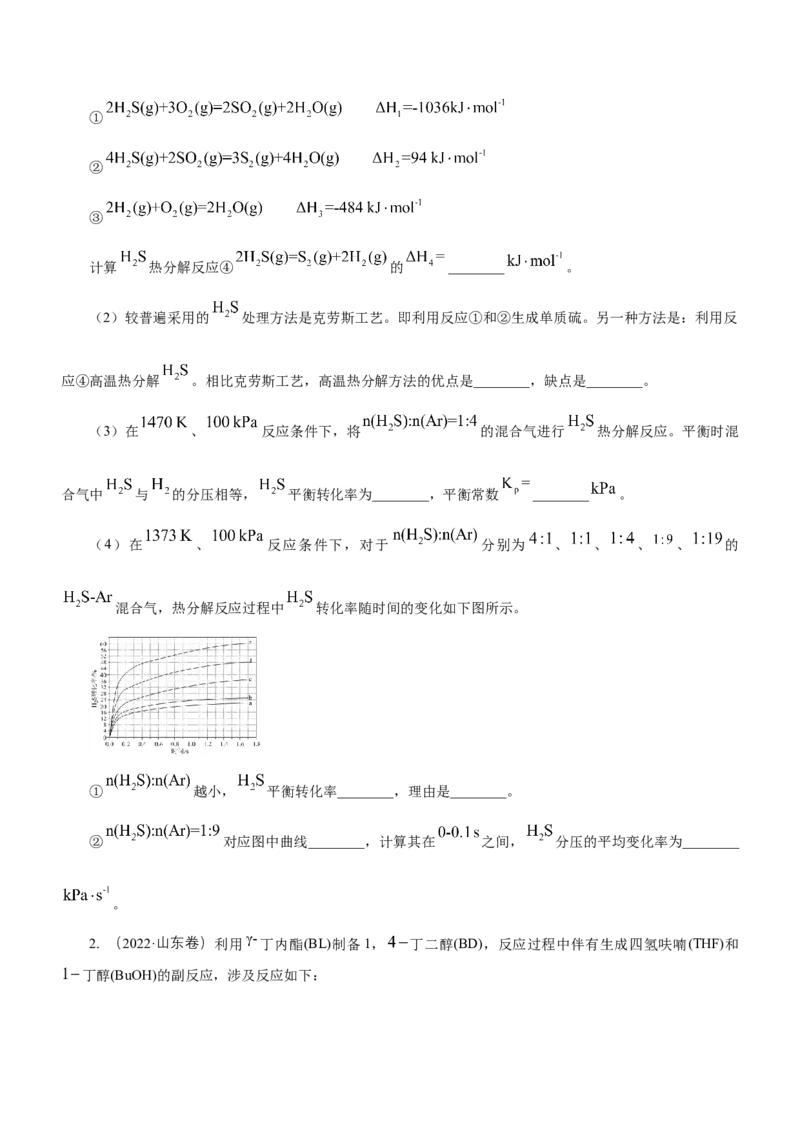
浓度计算,分压=总压×物质的量分数。用含 的代数式表示)。③若在相同时间内测得 的转化率随温度的变化曲线如图甲所示, 的转化率在 之间下
降由缓到急的原因是_______。
(3)有机物的电化学合成是目前研究的热点之一。我国学者利用双膜三室电解法合成了 ,该方
法的优点是能耗低、原料利用率高,同时能得到高利用价值的副产品,其工作原理如图乙所示。
①气体X为_______,膜Ⅰ适合选用_______(填“阳离子”或“阴离子”)交换膜。
②稳定工作时 溶液的浓度_______(填“增大”“减小”“不变”“无法判断”)。
③若制得 ,饱和食盐水质量减小_______g。
1.(2022·全国乙卷)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以
利用。回答下列问题:
(1)已知下列反应的热化学方程式:①
②
③
计算 热分解反应④ 的 ________ 。
(2)较普遍采用的 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反
应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是________,缺点是________。
(3)在 、 反应条件下,将 的混合气进行 热分解反应。平衡时混
合气中 与 的分压相等, 平衡转化率为________,平衡常数 ________ 。
(4)在 、 反应条件下,对于 分别为 、 、 、 、 的
混合气,热分解反应过程中 转化率随时间的变化如下图所示。
① 越小, 平衡转化率________,理由是________。
② 对应图中曲线________,计算其在 之间, 分压的平均变化率为________
。
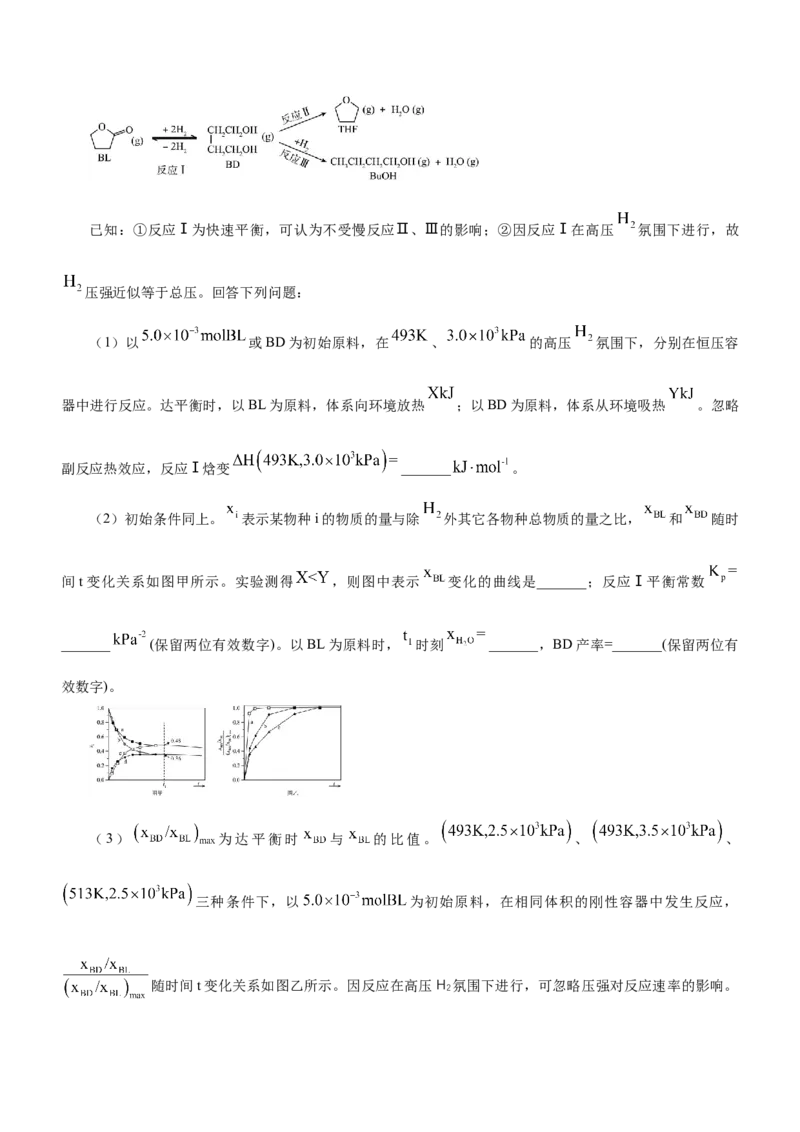
2. (2022·山东卷)利用 丁内酯(BL)制备1, 丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和
丁醇(BuOH)的副反应,涉及反应如下:已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压 氛围下进行,故
压强近似等于总压。回答下列问题:
(1)以 或BD为初始原料,在 、 的高压 氛围下,分别在恒压容
器中进行反应。达平衡时,以BL为原料,体系向环境放热 ;以BD为原料,体系从环境吸热 。忽略
副反应热效应,反应Ⅰ焓变 _______ 。
(2)初始条件同上。 表示某物种i的物质的量与除 外其它各物种总物质的量之比, 和 随时
间t变化关系如图甲所示。实验测得 ,则图中表示 变化的曲线是_______;反应Ⅰ平衡常数
_______ (保留两位有效数字)。以BL为原料时, 时刻 _______,BD产率=_______(保留两位有
效数字)。
(3) 为达平衡时 与 的比值。 、 、
三种条件下,以 为初始原料,在相同体积的刚性容器中发生反应,
随时间t变化关系如图乙所示。因反应在高压 H 氛围下进行,可忽略压强对反应速率的影响。
2曲线a、b、c中, 最大的是_______(填代号);与曲线b相比,曲线c达到 所
需时间更长,原因是_______。
3.(2022·浙江卷)工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足
不同需求的原料气。请回答:
(1)在C和O 的反应体系中:
2
反应1:C(s)+O(g)=CO (g)ΔH =-394kJ·mol-1
2 2 1
反应2:2CO(g)+O(g)=2CO (g)ΔH =-566kJ·mol-1
2 2 2
反应3:2C(s)+O(g)=2CO(g)ΔH 。
2 3
①设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是______。
②一定压强下,随着温度的升高,气体中CO与CO 的物质的量之比______。
2
A.不变B.增大C.减小D.无法判断
(2)水煤气反应:C(s)+HO(g)=CO(g)+H (g)ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量
2 2
的空气和水蒸气与煤炭反应,其理由是________。
(3)一氧化碳变换反应:CO(g)+HO(g)=CO(g)+H(g)ΔH=-41kJ·mol-1。
2 2 2
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPa、
p(H O)=0.25MPa、p(CO)=0.75MPa和p(H )=0.75MPa,则反应的平衡常数K的数值为________。
2 2 2
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中水蒸
气和CO的物质的量之比为________。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是________。
A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气
④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过程如
图2所示。用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:________;步骤Ⅱ:________。
4.(2022·浙江卷)主要成分为H S的工业废气的回收利用有重要意义。
2
( 1 ) 回 收 单 质 硫 。 将 三 分 之 一 的 H S 燃 烧 , 产 生 的 SO 与 其 余 H S 混 合 后 反 应 :
2 2 2
。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
、 、 ,计算该温度下的平
衡常数K_______。
(2)热解H S制H 。根据文献,将H S和CH 的混合气体导入石英管反应器热解(一边进料,另一边出
2 2 2 4
料),发生如下反应:
Ⅰ.
Ⅱ.
总反应:
Ⅲ.
投料按体积之比 ,并用N 稀释;常压,不同温度下反应相同时间后,测得H 和
2 2
CS 体积分数如下表:
2
温度/ 950 1000 1050 1100 1150
0.5 1.5 3.6 5.5 8.5
0.0 0.0 0.1 0.4 1.8
请回答:
①反应Ⅲ能自发进行的条件是_______。②下列说法正确的是_______。
A.其他条件不变时,用Ar替代N 作稀释气体,对实验结果几乎无影响
2
B.其他条件不变时,温度越高,H S的转化率越高
2
C.由实验数据推出H S中的S-H键强于CH 中的C-H键
2 4
D.恒温恒压下,增加N 的体积分数,H 的浓度升高
2 2
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意图
_______。
④在 ,常压下,保持通入的H S体积分数不变,提高投料比 ,H S的转化率
2 2
不变,原因是_______。
⑤在 范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该变化规律并
分析原因_______。
5.(2021·湖北卷)丙烯是一种重要的化工原料,可以在催化剂作用下,由丙烷直接脱氢或氧化脱氢制
备。
反应Ⅰ(直接脱氢):C H(g)=C H(g)+H(g)△H=+125kJ·mol-1
3 8 3 6 2 1
反应Ⅱ(氧化脱氢):C H(g)+ O(g)=C H(g)+HO(g)△H=-118kJ·mol-1
3 8 2 3 6 2 2
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
___kJ。
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入C H 和N 的混合气体(N 不参与反应),从平
3 8 2 2
衡移动的角度判断,达到平衡后“通入N”的作用是___。在温度为T 时,C H 的平衡转化率与通入气体中C H
2 1 3 8 3 8
的物质的量分数的关系如图a所示,计算T 时反应Ⅰ的平衡常数K=__kPa(以分压表示,分压=总压×物质的量
1 p
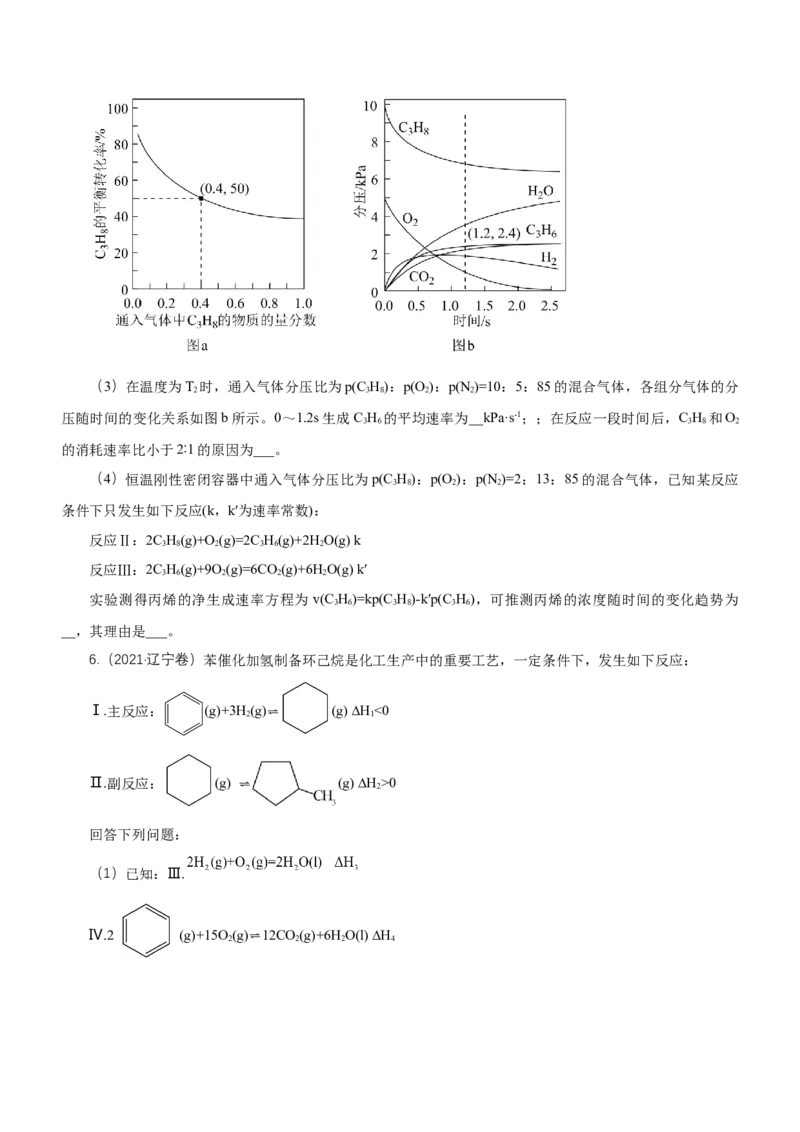
分数,保留一位小数)。(3)在温度为T 时,通入气体分压比为p(C H):p(O ):p(N )=10:5:85的混合气体,各组分气体的分
2 3 8 2 2
压随时间的变化关系如图b所示。0~1.2s生成C H 的平均速率为__kPa·s-1;;在反应一段时间后,C H 和O
3 6 3 8 2
的消耗速率比小于2∶1的原因为___。
(4)恒温刚性密闭容器中通入气体分压比为p(C H):p(O ):p(N )=2:13:85的混合气体,已知某反应
3 8 2 2
条件下只发生如下反应(k,k′为速率常数):
反应Ⅱ:2C H(g)+O(g)=2C H(g)+2HO(g) k
3 8 2 3 6 2
反应Ⅲ:2C H(g)+9O(g)=6CO (g)+6HO(g) k′
3 6 2 2 2
实验测得丙烯的净生成速率方程为 v(C H)=kp(C H)-k′p(C H),可推测丙烯的浓度随时间的变化趋势为
3 6 3 8 3 6
__,其理由是___。
6.(2021·辽宁卷)苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反应:
Ⅰ.主反应: (g)+3H
2
(g)⇌ (g) ∆H
1
<0
Ⅱ.副反应: (g) ⇌ (g) ∆H 2 >0
回答下列问题:
(1)已知:Ⅲ.
Ⅳ.2 (g)+15O
2
(g)⇌12CO
2
(g)+6H
2
O(l) ∆H
4Ⅴ. (g)+9O(g)=6CO (g)+6HO(l) ∆H
2 2 2 5
则 _______(用 、 和 表示)。
(2)有利于提高平衡体系中环己烷体积分数的措施有_______。
A.适当升温 B.适当降温 C.适当加压 D.适当减压
(3)反应Ⅰ在管式反应器中进行,实际投料往往在 的基础上适当增大 用量,其目
的是_______。
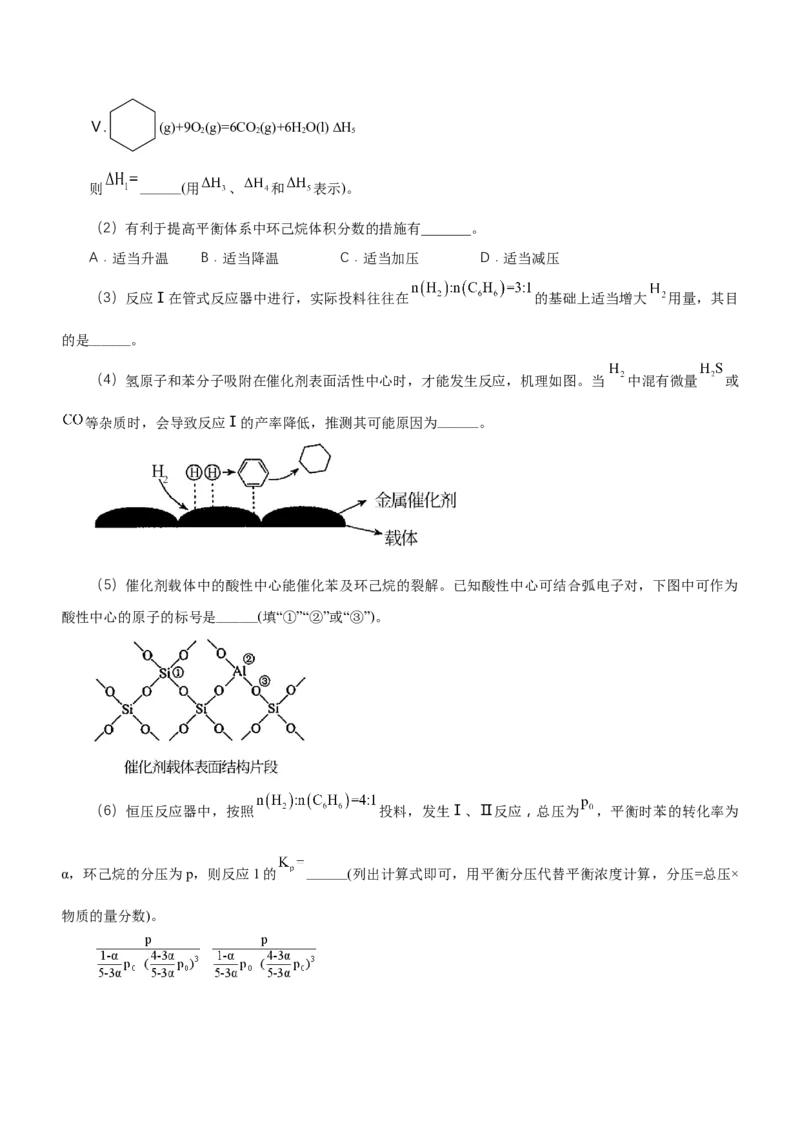
(4)氢原子和苯分子吸附在催化剂表面活性中心时,才能发生反应,机理如图。当 中混有微量 或
等杂质时,会导致反应Ⅰ的产率降低,推测其可能原因为_______。
(5)催化剂载体中的酸性中心能催化苯及环己烷的裂解。已知酸性中心可结合弧电子对,下图中可作为
酸性中心的原子的标号是_______(填“①”“②”或“③”)。
(6)恒压反应器中,按照 投料,发生Ⅰ、Ⅱ反应,总压为 ,平衡时苯的转化率为
α,环己烷的分压为p,则反应1的 _______(列出计算式即可,用平衡分压代替平衡浓度计算,分压=总压×
物质的量分数)。