文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题20 化学反应机理与反应历程图像分析
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
近几年高考中,化学反应机理与反应历程试题频繁出现,题目主要以图示的形式来描述某一化学变化
所经由的全部反应,就是把一个复杂反应分解成若干个反应,然后按照一定规律组合起来,从而达到阐述
复杂反应内在联系的目的。
预计在2025年高考中,会以选择题的形式出现,以及在化学反应原理大题中有所涉及,其中以催化剂
的催化反应机理和能垒图像为情境载体进行命题的可能性很大。由于陌生度高,思维转化大,且命题视角
在不断地创新和发展,成为大多数考生的失分点。所以,很有必要对这两类题型的解题模型进行掌握。
1.(2024·广西·高考真题)烯烃进行加成反应的一种机理如下:
此外,已知实验测得 与 进行加成反应的活化能依次减小。下
列说法错误的是
A.乙烯与HCl反应的中间体为
B.乙烯与氯水反应无 生成
C.卤化氢与乙烯反应的活性:
D.烯烃双键碳上连接的甲基越多,与 的反应越容易
【答案】B
【详解】A.HCl中氢带正电荷、氯带负电荷,结合机理可知,乙烯与HCl反应的中间体为氢和乙烯形成
正离子: ,A正确;
B.氯水中存在HClO,其结构为H-O-Cl,其中Cl带正电荷、OH带负电荷,结合机理可知,乙烯与氯水
反应可能会有 生成,B错误;
C.由机理,第一步反应为慢反应,决定反应的速率,溴原子半径大于氯,HBr中氢溴键键能更小,更容
易断裂,反应更快,则卤化氢与乙烯反应的活性: ,C正确;D.已知实验测得 与 进行加成反应的活化能依次减小;则烯
烃双键碳上连接的甲基越多,与 的反应越容易,D正确;
故选B。
2.(2023·重庆·高考真题) 和 均可发生水解反应,其中 的水解机理示意图如下:
下列说法正确的是
A. 和 均为极性分子 B. 和 中的 均为 杂化
C. 和 的水解反应机理相同 D. 和 均能与 形成氢键
【答案】D
【详解】A. 中中心原子N周围的价层电子对数为:3+ =4,故空间构型为三角锥形,其分子
中正、负电荷中心不重合,为极性分子,而 中中心原子周围的价层电子对数为:4+ =4,是
正四面体形结构,为非极性分子,A错误;
B. 和 中中心原子N周围的价层电子对数均为:3+ =4,故二者 均为 杂化,B错
误;
C.由题干NCl 反应历程图可知,NCl 水解时首先HO中的H原子与NCl 上的孤电子对结合,O与Cl结
3 3 2 3
合形成HClO,而SiCl 上无孤电子对,故SiCl 的水解反应机理与之不相同,C错误;
4 4
D. 和 分子中均存在N-H键和孤电子对,故均能与 形成氢键,D正确;
故答案为:D。
3.(2024·浙江·高考真题)酯在 溶液中发生水解反应,历程如下:
已知:①
② 水解相对速率与取代基R的关系如下表:
取代基R
水解相对速率 1 290 7200
下列说法不正确的是
A.步骤I是 与酯中 作用
B.步骤III使I和Ⅱ平衡正向移动,使酯在 溶液中发生的水解反应不可逆
C.酯的水解速率:
D. 与 反应、 与 反应,两者所得醇和羧酸盐均不同
【答案】D
【详解】A.步骤Ⅰ是氢氧根离子与酯基中的 作用生成羟基和O-,A正确;
B.步骤Ⅰ加入氢氧根离子使平衡Ⅰ正向移动,氢氧根离子与羧基反应使平衡Ⅱ也正向移动,使得酯在
NaOH溶液中发生的水解反应不可逆,B正确;
C.从信息②可知,随着取代基R上Cl个数的增多,水解相对速率增大,原因为Cl电负性较强,对电子的
吸引能力较强,使得酯基的水解速率增大,F的电负性强于Cl,FCH 对电子的吸引能力更强,因此酯的水
2
解速率 ,C正确;
D. 与氢氧根离子反应,根据信息①可知,第一步反应后18O既存在于羟基中也存在于
O-中,随着反应进行,最终18O存在于羧酸盐中,同理 与18OH-反应,最终18O存在于羧
酸盐中,两者所得醇和羧酸盐相同,D错误;
故选D。
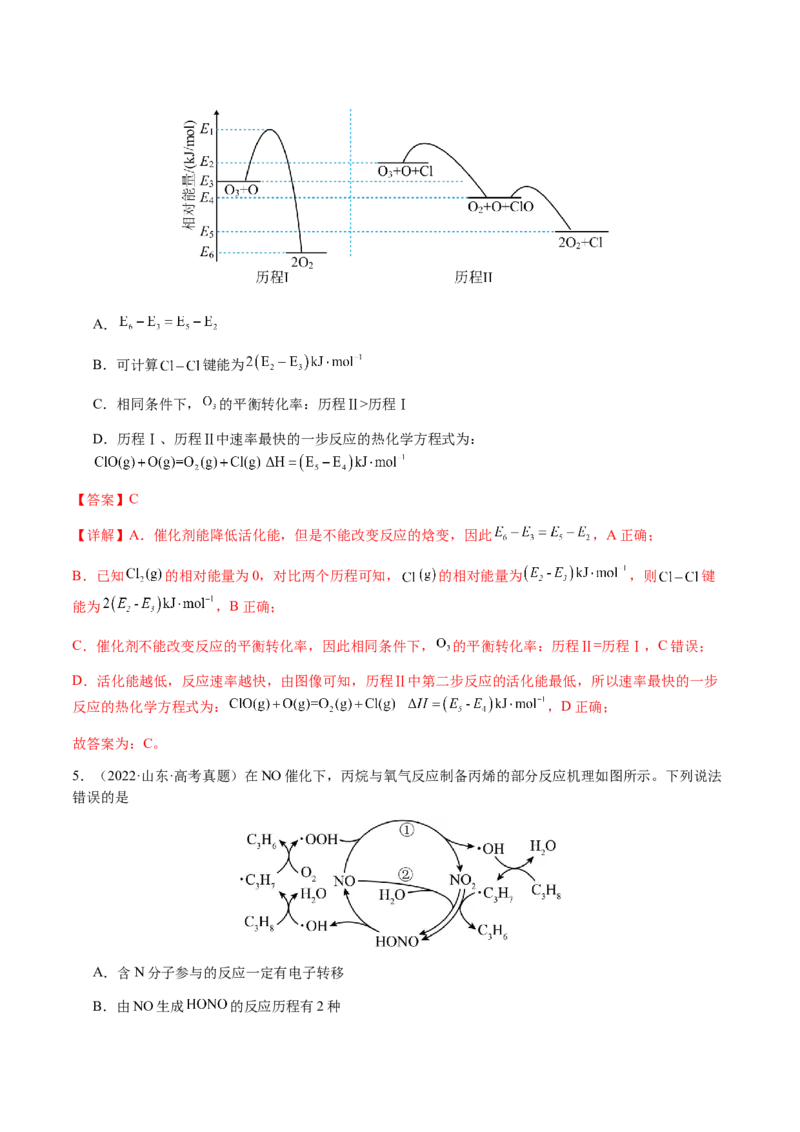
4.(2023·浙江·高考真题)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知
和 的相对能量为0],下列说法不正确的是A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【详解】A.催化剂能降低活化能,但是不能改变反应的焓变,因此 ,A正确;
B.已知 的相对能量为0,对比两个历程可知, 的相对能量为 ,则 键
能为 ,B正确;
C.催化剂不能改变反应的平衡转化率,因此相同条件下, 的平衡转化率:历程Ⅱ=历程Ⅰ,C错误;
D.活化能越低,反应速率越快,由图像可知,历程Ⅱ中第二步反应的活化能最低,所以速率最快的一步
反应的热化学方程式为: ,D正确;
故答案为:C。
5.(2022·山东·高考真题)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法
错误的是
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【详解】A.根据反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO +∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中N元
2 2 2 3 7 3 6 2
素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反应,一定有
电子转移,A项正确;
B.根据图示,由NO生成HONO的反应历程有2种,B项正确;
C.NO是催化剂,增大NO的量,C H 的平衡转化率不变,C项正确;
3 8
D.无论反应历程如何,在NO催化下丙烷与O 反应制备丙烯的总反应都为2C H+O
2 3 8 2
2C H+2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误;
3 6 2
答案选D。
6.(2024·贵州·高考真题)AgCN与 可发生取代反应,反应过程中 的C原子和N原子均可
进攻 ,分别生成腈 和异腈 两种产物。通过量子化学计算得到的反应
历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是
A.从 生成 和 的反应都是放热反应
B.过渡态TS1是由 的C原子进攻 的 而形成的
C.Ⅰ中“ ”之间的作用力比Ⅱ中“ ”之间的作用力弱
D.生成 放热更多,低温时 是主要产物
【答案】D【详解】A.由反应历程及能量变化图可知,两种路径生成的产物的总能量均低于反应物,故从
生成 和 的反应都是放热反应,A项正确;
B.与Br原子相连的C原子为 ,由反应历程及能量变化图可知,过渡态TS1是由CN-的C原子进攻
的 ,形成碳碳键,B项正确;
C.由反应历程及能量变化图可知,后续物Ⅰ、Ⅱ转化为产物,分别断开的是 和 ,且后者吸
收更多的能量,故Ⅰ中“ ”之间的作用力比Ⅱ中“ ”之间的作用力弱,C项正确;
D.由于生成 所需要的活化能高,反应速率慢,故低温时更容易生成 ,为主要产
物,D项错误;
故选D。
7.(2024·广东·高考真题)对反应 (I为中间产物),相同条件下:
①加入催化剂,反应达到平衡所需时间大幅缩短;
②提高反应温度, 增大, 减小。
基于以上事实,可能的反应历程示意图(——为无催化剂,------为有催化剂)为
A. B. C. D.
【答案】A
【详解】提高反应温度, 增大,说明反应 的平衡逆向移动,即该反应为放热反
应, 减小,说明S生成中间产物I的反应平衡正向移动,属于吸热反应,由此可排除C、D选
项,加入催化剂,反应达到平衡所需时间大幅缩短,即反应的决速步骤的活化能下降,使得反应速率大幅
加快,活化能大的步骤为决速步骤,符合条件的反应历程示意图为A,故A正确,
故选A。
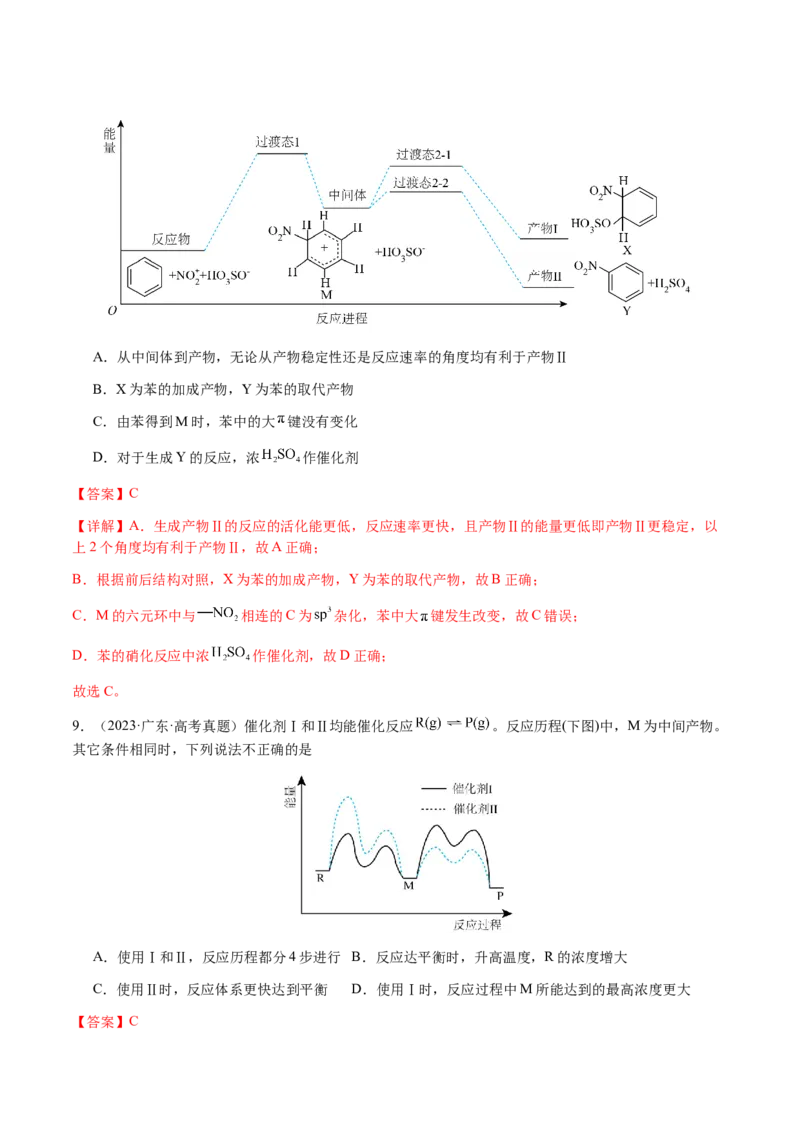
8.(2024·北京·高考真题)苯在浓 和浓 作用下,反应过程中能量变化示意图如下。下列说法
不正确的是A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大 键没有变化
D.对于生成Y的反应,浓 作催化剂
【答案】C
【详解】A.生成产物Ⅱ的反应的活化能更低,反应速率更快,且产物Ⅱ的能量更低即产物Ⅱ更稳定,以
上2个角度均有利于产物Ⅱ,故A正确;
B.根据前后结构对照,X为苯的加成产物,Y为苯的取代产物,故B正确;
C.M的六元环中与 相连的C为 杂化,苯中大 键发生改变,故C错误;
D.苯的硝化反应中浓 作催化剂,故D正确;
故选C。
9.(2023·广东·高考真题)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。
其它条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行 B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡 D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
【答案】C【详解】A.由图可知两种催化剂均出现四个波峰,所以使用Ⅰ和Ⅱ,反应历程都分4步进行,A正确;
B.由图可知该反应是放热反应,所以达平衡时,升高温度平衡向左移动,R的浓度增大,B正确;
C.由图可知Ⅰ的最高活化能小于Ⅱ的最高活化能,所以使用Ⅰ时反应速率更快,反应体系更快达到平
衡,C错误;
D.由图可知在前两个历程中使用Ⅰ活化能较低反应速率较快,后两个历程中使用Ⅰ活化能较高反应速率
较慢,所以使用Ⅰ时,反应过程中M所能达到的最高浓度更大,D正确;
故选C。
10.(2023·浙江·高考真题)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】C
【详解】A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的热量,
反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;
B.短时间里反应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,
其活化能越小,则反应活化能:反应I<反应Ⅱ,故B正确;
C.产物I和产物II存在可逆反应,则产物II和产物I的比值即该可逆反应的平衡常数K,由于平衡常数只
与温度有关,所以增加HCl浓度平衡时产物II和产物I的比例不变,故C错误;
D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,故D正确。
综上所述,答案为C。
11.(2023·西藏四川·高考真题)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:(3) 分别与 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以 示
例)。
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是 (填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则 与 反应的能量变
化应为图中曲线 (填“c”或“d”)。
(ⅲ) 与 反应,氘代甲醇的产量 (填“>”“<”或“=”)。若 与
反应,生成的氘代甲醇有 种。
【答案】(3)Ⅰ c < 2
【详解】(3)(ⅰ)步骤Ⅰ涉及的是碳氢键的断裂和氢氧键的形成,步骤Ⅱ中涉及碳氧键形成,所以符合题
意的是步骤Ⅰ;
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则此时正反应活化能会增
大,根据图示可知, 与 反应的能量变化应为图中曲线c;
(ⅲ) 与 反应时,因直接参与化学键变化的元素被替换为更重的同位素时,步骤Ⅰ的活化能增
大,反应速率会变慢,则CHDOD更难获得,故产率: < ;根据反应机理可知,若
2
与 反应,生成的氘代甲醇可能为 或 共2种,故答案为:<;2。
12.(2023·湖北·高考真题)纳米碗 是一种奇特的碗状共轭体系。高温条件下, 可以由
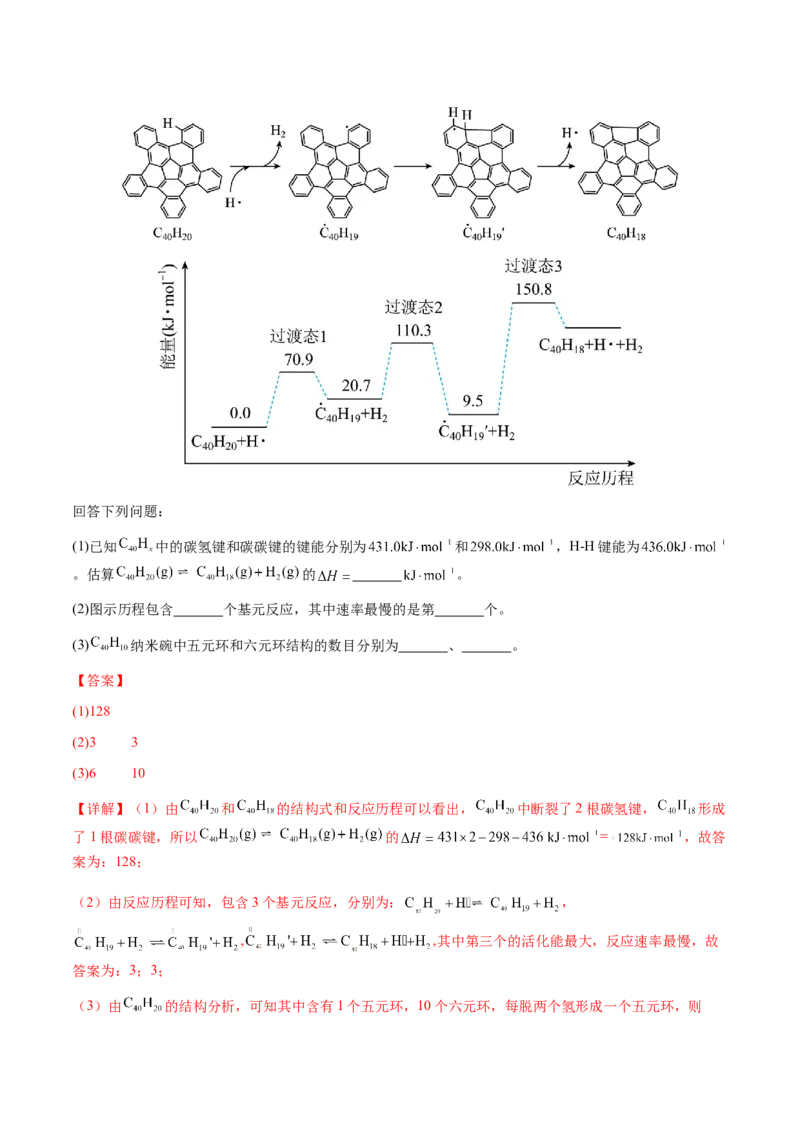
分子经过连续5步氢抽提和闭环脱氢反应生成。 的反应机理和能量
变化如下:回答下列问题:
(1)已知 中的碳氢键和碳碳键的键能分别为 和 ,H-H键能为
。估算 的 。
(2)图示历程包含 个基元反应,其中速率最慢的是第 个。
(3) 纳米碗中五元环和六元环结构的数目分别为 、 。
【答案】
(1)128
(2)3 3
(3)6 10
【详解】(1)由 和 的结构式和反应历程可以看出, 中断裂了2根碳氢键, 形成
了1根碳碳键,所以 的 = ,故答
案为:128;
(2)由反应历程可知,包含3个基元反应,分别为: ,
, ,其中第三个的活化能最大,反应速率最慢,故
答案为:3;3;
(3)由 的结构分析,可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则总共含有6个五元环,10个六元环,故答案为:6;10;
13.(2023·重庆·高考真题)银及其化合物在催化与电化学等领域中具有重要应用。
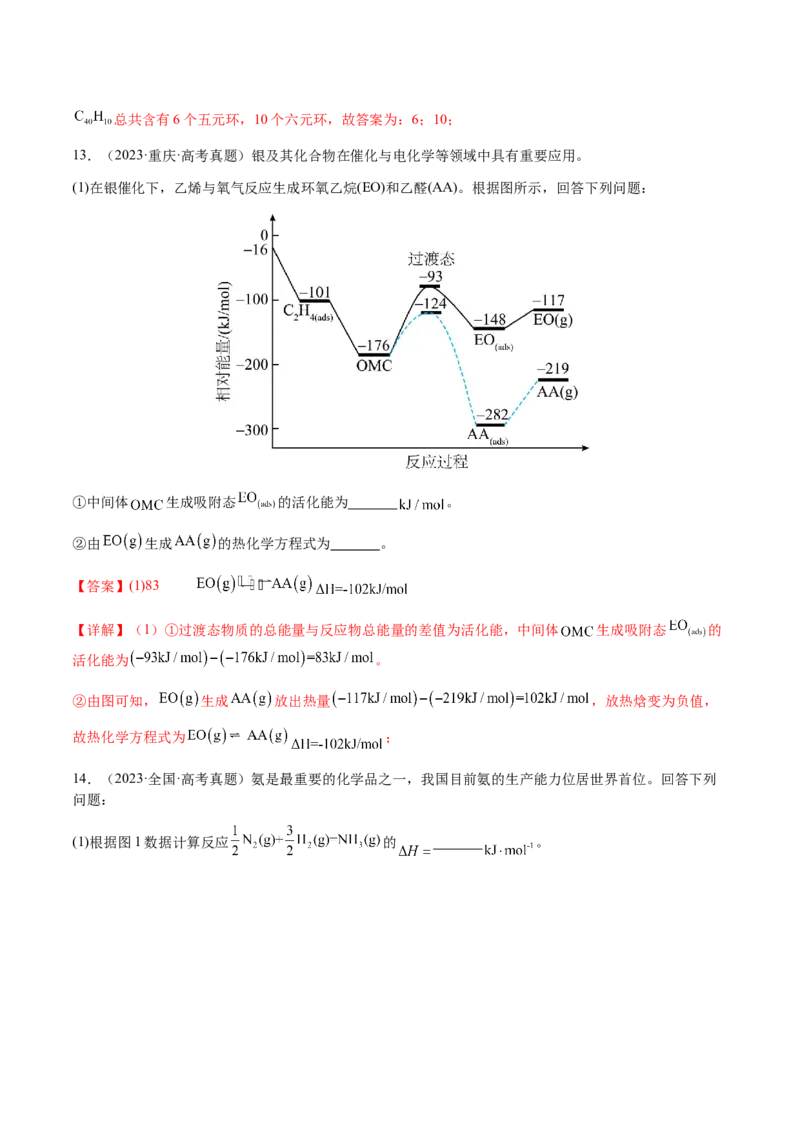
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:
①中间体 生成吸附态 的活化能为 。
②由 生成 的热化学方程式为 。
【答案】(1)83
【详解】(1)①过渡态物质的总能量与反应物总能量的差值为活化能,中间体 生成吸附态 的
活化能为 。
②由图可知, 生成 放出热量 ,放热焓变为负值,
故热化学方程式为 ;
14.(2023·全国·高考真题)氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列
问题:
(1)根据图1数据计算反应 的 。(2)研究表明,合成氨反应在 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位, 表示被吸附
于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为 (填步骤前的标
号),理由是 。
【答案】
(1)
(2)(ⅱ) 在化学反应中,最大的能垒为速率控制步骤,而断开化学键的步骤都属于能垒,由于 的
键能比H-H键的大很多,因此,在上述反应机理中,速率控制步骤为(ⅱ)
【详解】(1)在化学反应中,断开化学键要消耗能量,形成化学键要释放能量,反应的焓变等于反应物
的键能总和与生成物的键能总和的差,因此,由图1数据可知,反应 的
。
(2)由图1中信息可知, 的 ,则 的键能为 ;
的 ,则H-H键的键能为 。在化学反应中,最大的能垒为速率
控制步骤,而断开化学键的步骤都属于能垒,由于 的键能比H-H键的大很多,因此,在上述反应机
理中,速率控制步骤为(ⅱ)。
一、基元反应、过渡态理论
1.基元反应和有效碰撞理论
(1)基元反应:大多数化学反应往往经历多个反应步骤才能实现,其中每一步反应都称为基元反应。
反应历程:基元反应反映了化学反应的历程,反应历程又称反应机理。
如:2HI===H +I 实际上经过下列两步反应完成:①2HI→H +2I·
2 2 2
②2I·→I
2
(2)许多化学反应都不是基元反应,而是由两个或多个基元步骤完成的。假设反应:A +B===AB是分
2 2两个基元步骤完成的:
第一步 A 2A (慢反应)
2
第二步 2A+B AB (快反应)
2
对于总反应来说,决定反应速率的肯定是第一个基元步骤,即这种前一步的产物作为后一步的反应物
的连串反应的。决定速率的步骤是最慢的一个基元步骤。
如:过氧化氢 HO 在水溶液中把溴化氢 HBr 氧化为溴 Br 的反应:HO + 2H+ +2Br- Br +
2 2 2 2 2 2
2HO,反应机理为:
2
HO+H++Br- HBrO+HO (慢反应)
2 2 2
HBrO+Br-+H+ Br +HO (快反应)
2 2
决定速率的就是第一个反应,且这个反应中HBrO不是最终产物,称为反应的中间产物或中间体。
(3)有效碰撞
①基元反应发生的先决条件是反应物的分子必须发生碰撞。
②反应物分子的每一次碰撞并不是都能发生反应,能够发生化学反应的碰撞叫作有效碰撞。发生有效
碰撞的两个条件是反应物分子能量足够和取向合适。
2.过渡态理论
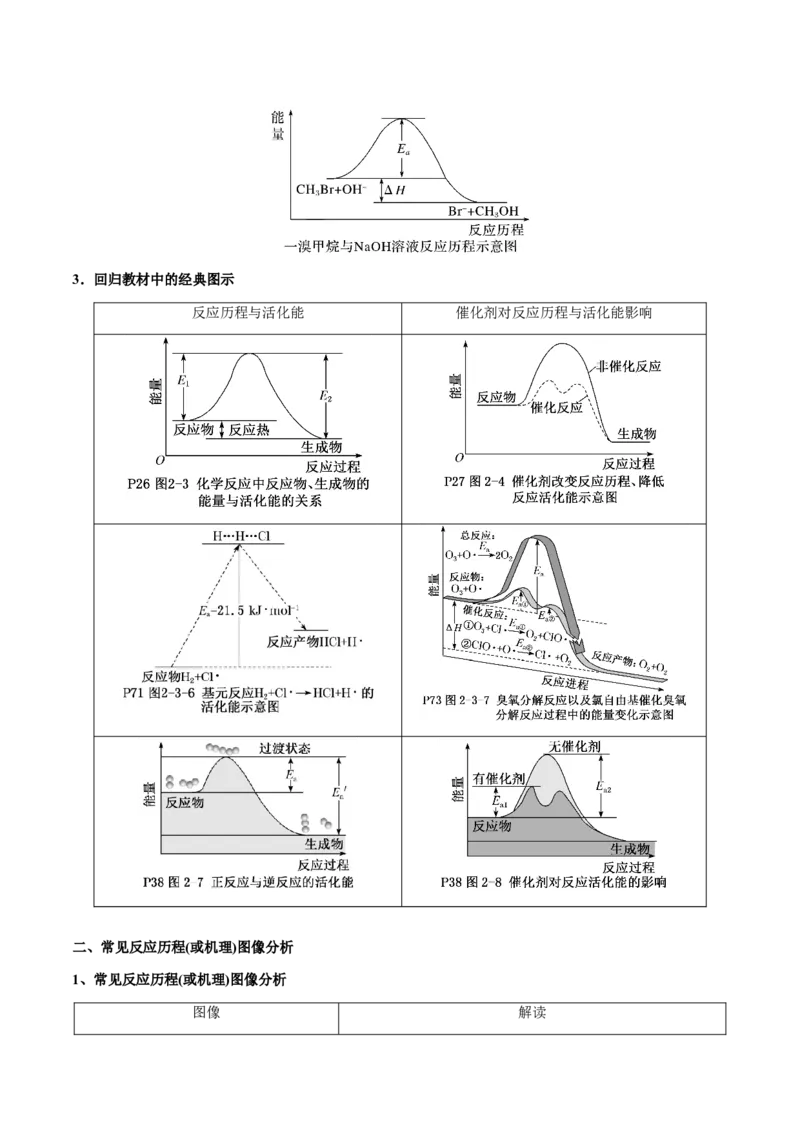
(1)如图所示是两步完成的化学反应,分析并回答下列问题。
①该反应的反应物为A、B,中间体为C,生成物为D。
②由A、B生成C的反应为吸热反应,由C生成D的反
应为放热反应,总反应为放热反应。
③第一步为慢反应,第二步为快反应,决定总反应快慢
的是第一步反应。
(2)基元反应过渡状态理论认为,基元反应在从反应物到产物的变化过程中要经历一个中间状态,这个
状态称为过渡态。
AB+C [A…B…C] A+BC
反应物 过渡态 产物
(3)过渡态是处在反应过程中具有最高能量的一种分子构型,过渡态能量与反应物的平均能量的差值相
当于活化能。
如:一溴甲烷与 NaOH 溶液反应的历程可以表示为:CHBr+OH- [Br…CH…OH] Br-+
3 3
CHOH
3
反应物 过渡态 产物3.回归教材中的经典图示
反应历程与活化能 催化剂对反应历程与活化能影响
二、常见反应历程(或机理)图像分析
1、常见反应历程(或机理)图像分析
图像 解读催化剂与化学反应:
(1)在无催化剂的情况下:E 为正反应的活化能;E 为逆反应
1 2
的活化能;E-E 为此反应的焓变(ΔH)。
1 2
(2)有催化剂时,总反应分成了两个反应步骤(也可能为多
个,如模拟演练题1中图像所表示的),反应①为吸热反应,
产物为总反应的中间产物,反应②为放热反应,总反应为放
热反应。
(3)催化剂的作用:降低E、E,但不影响ΔH,反应是放热
1 2
反应还是吸热反应取决于起点(反应物)能量和终点(生成物)能
量的相对大小
“环式”反应:
对于“环式”反应过程图像,位于“环上”的物质一般是催
化剂或中间体,如⑤、⑥、⑦和⑧,“入环”的物质为反应
物,如①和④,“出环”的物质为生成物,如②和③
催化剂与中间产物:
催化剂:在连续反应中从一开始就参与了反应,在最后又再
次生成,所以仅从结果上来看似乎并没有发生变化,实则是
消耗多少后续又生成了多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又
作为反应物被消耗,所以仅从结果上来看似乎并没有生成,
实则是生成多少后续有消耗多少。
例1:在含少量 I-的溶液中,HO 分解的机理为:
2 2
HO + I- → H O + IO- 慢
2 2 2
HO + IO-→ O + I- +H O 快
2 2 2 2
在该反应中I-为催化剂, IO-为中间产物。
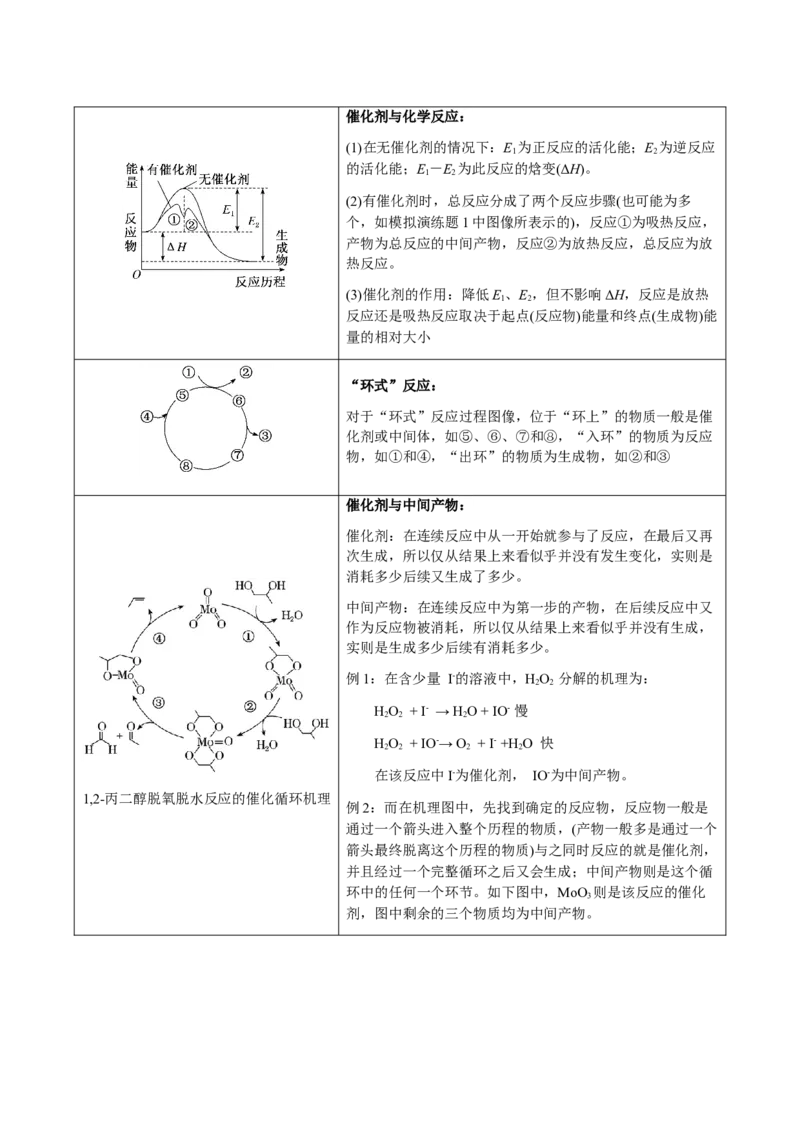
1,2-丙二醇脱氧脱水反应的催化循环机理
例2:而在机理图中,先找到确定的反应物,反应物一般是
通过一个箭头进入整个历程的物质,(产物一般多是通过一个
箭头最终脱离这个历程的物质)与之同时反应的就是催化剂,
并且经过一个完整循环之后又会生成;中间产物则是这个循
环中的任何一个环节。如下图中,MoO 则是该反应的催化
3
剂,图中剩余的三个物质均为中间产物。能垒与决速步骤:
能垒:简单可以理解为从左往右进行中,向上爬坡最高的为
能垒,而包含此能垒的反应我们称之为决速步骤,也成为慢
反应。
例如图中,从第一个中间态到过渡态2的能量就是能垒,而
HCOO*+H*=CO +2H*是在Rh做催化剂时该历程的决速步
2
骤。
注意:
①能垒越大,反应速率越小,即多步反应中能垒最大的反应
为决速反应。
②用不同催化剂催化化学反应,催化剂使能垒降低幅度越
大,说明催化效果越好。
③相同反应物同时发生多个竞争反应,其中能垒越小的反
应,反应速率越大,产物占比越高。
2.催化反应机理题的解题思路
(1)通览全图,找准一“剂”三“物”
一“剂”指催 催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物种一定
化剂 在机理图中的主线上.
反应物 通过一个箭头进入整个历程的物质是反应物;
三“物”指反
生成物 通过一个箭头最终脱离整个历程的物质一般多是产物;
应物、生成
物、中间物种 通过一个箭头脱离整个历程,但又生成生成物的是中间体,通过二个箭头
(或中间体) 中间体 进入整个历程的中间物质也是中间体,中间体有时在反应历程中用“[ ]”
标出;
(2)逐项分析得答案:根据第一步由题给情境信息,找出催化剂、反应物、生成物、中间体,再结合每
一选项设计的问题逐项分析判断,选出正确答案。
(3)重新认识催化剂
①催化剂具有的三大特征
催化剂是通过降低反应活化能,从而改变了反应的途径,此即催化剂加速化学反应的主要原因所在。
总结起来,催化剂的特征主要表现在这样几个方面:
第一,催化剂可以改变反应速率,但其自身在反应前后的组成、质量和化学性质不变。
第二,催化剂不改变化学平衡。即催化剂既能加快正向反应的速率,也能加快逆向反应的速率,从而
缩短化学反应达到平衡的时间。第三,催化剂具有特殊的选择性,不同类型的反应,需要选择不同的催化剂。同一种反应物,使用不
同的催化剂,可以得到不同的产物。
②常见催化剂的四大误区
实际上,催化剂不是不参加化学反应,而是在化学反应前后,催化剂的化
学性质基本不变。例如在铜催化乙醇生成乙醛的反应中,铜参与反应的原
理如下:
误区 催化剂不参
1 加化学反应 第一步为2Cu+O===2CuO,
2
第二步为CuO+CHCHOH→Cu+CHCHO+HO,这两步反应方程式的加
3 2 3 2
和为O+2CHCHOH→CH CHO+2HO。显然催化剂参与了化学反应。
2 3 2 3 2
一种反应只 实际上一个反应可以有多种催化剂,只是我们常选用催化效率高的,对环
误区
有一种催化 境污染小,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也
2
剂 可以是氯化铁,当然还可以硫酸铜等。
催化剂都是
误区 实际上,催化剂有正催化剂与负催化剂,正催化剂加快化学反应速率,负
加快化学反
3 催化剂是减慢化学反应速率的。
应速率
催化剂的效 实际上,催化剂参与了化学反应,是第一反应物。既然是反应物,催化剂
误区
率与催化剂 的表面积,催化剂的浓度大小必然影响化学反应速率。比如用酵母催化剂
4
的量无关 做食品,酵母量大自然面就膨大快。催化剂的用量是会改变催化效率的。
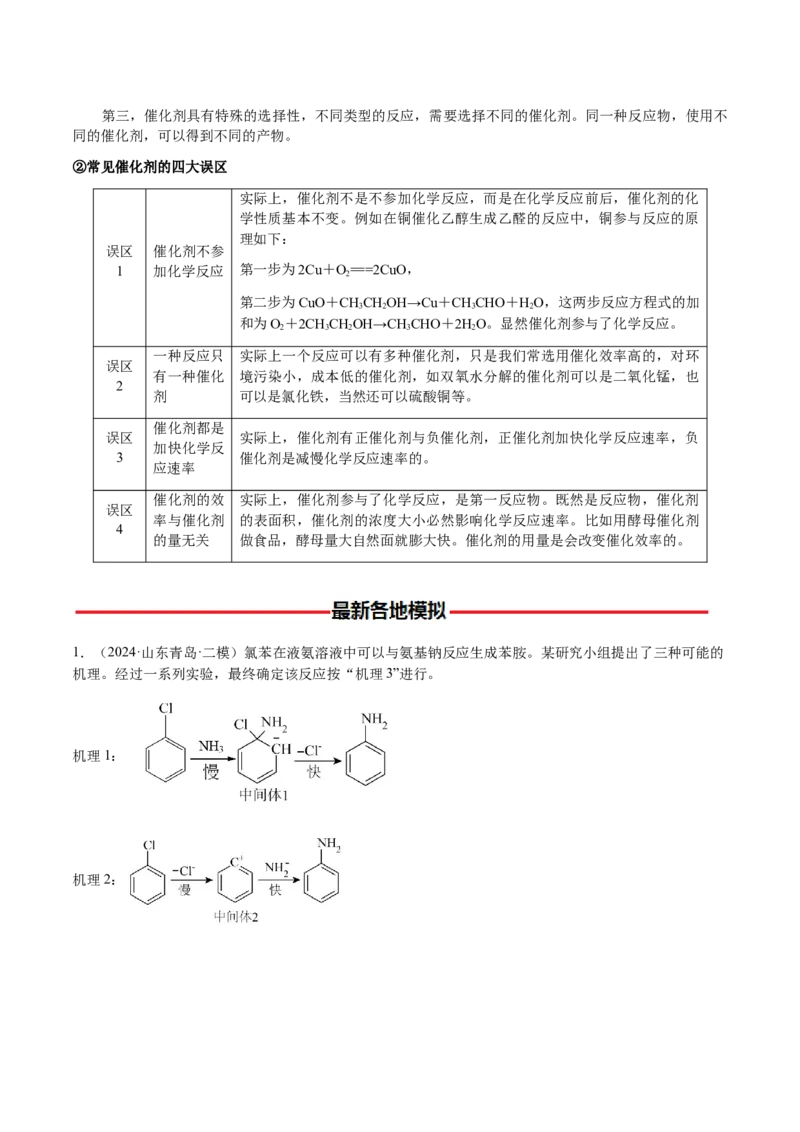
1.(2024·山东青岛·二模)氯苯在液氨溶液中可以与氨基钠反应生成苯胺。某研究小组提出了三种可能的
机理。经过一系列实验,最终确定该反应按“机理3”进行。
机理1:
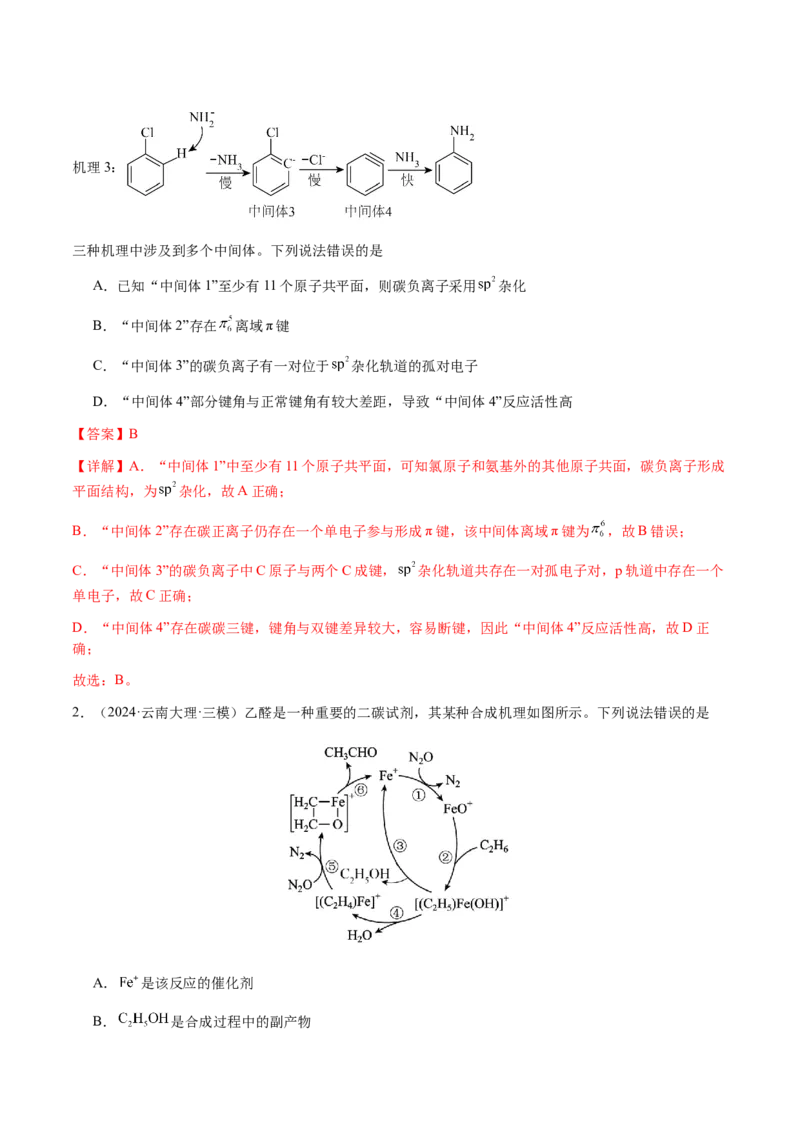
机理2:机理3:
三种机理中涉及到多个中间体。下列说法错误的是
A.已知“中间体1”至少有11个原子共平面,则碳负离子采用 杂化
B.“中间体2”存在 离域π键
C.“中间体3”的碳负离子有一对位于 杂化轨道的孤对电子
D.“中间体4”部分键角与正常键角有较大差距,导致“中间体4”反应活性高
【答案】B
【详解】A.“中间体1”中至少有11个原子共平面,可知氯原子和氨基外的其他原子共面,碳负离子形成
平面结构,为 杂化,故A正确;
B.“中间体2”存在碳正离子仍存在一个单电子参与形成π键,该中间体离域π键为 ,故B错误;
C.“中间体3”的碳负离子中C原子与两个C成键, 杂化轨道共存在一对孤电子对,p轨道中存在一个
单电子,故C正确;
D.“中间体4”存在碳碳三键,键角与双键差异较大,容易断键,因此“中间体4”反应活性高,故D正
确;
故选:B。
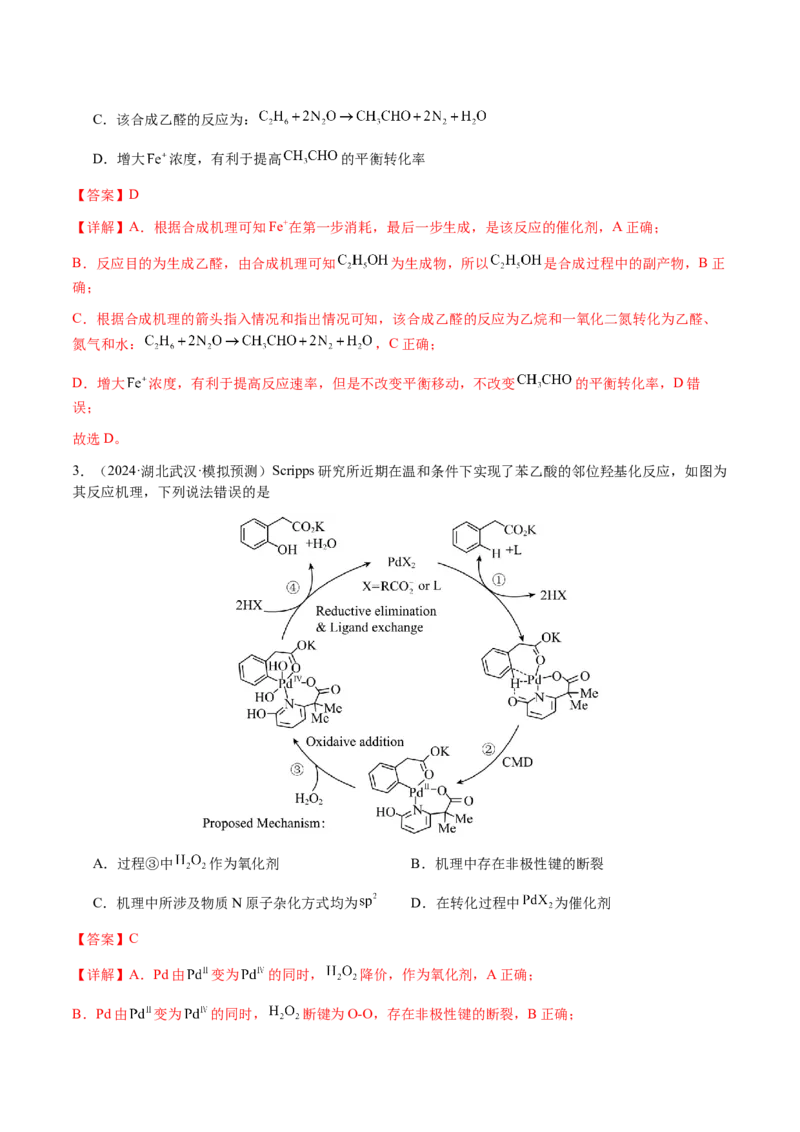
2.(2024·云南大理·三模)乙醛是一种重要的二碳试剂,其某种合成机理如图所示。下列说法错误的是
A. 是该反应的催化剂
B. 是合成过程中的副产物C.该合成乙醛的反应为:
D.增大 浓度,有利于提高 的平衡转化率
【答案】D
【详解】A.根据合成机理可知Fe+在第一步消耗,最后一步生成,是该反应的催化剂,A正确;
B.反应目的为生成乙醛,由合成机理可知 为生成物,所以 是合成过程中的副产物,B正
确;
C.根据合成机理的箭头指入情况和指出情况可知,该合成乙醛的反应为乙烷和一氧化二氮转化为乙醛、
氮气和水: ,C正确;
D.增大 浓度,有利于提高反应速率,但是不改变平衡移动,不改变 的平衡转化率,D错
误;
故选D。
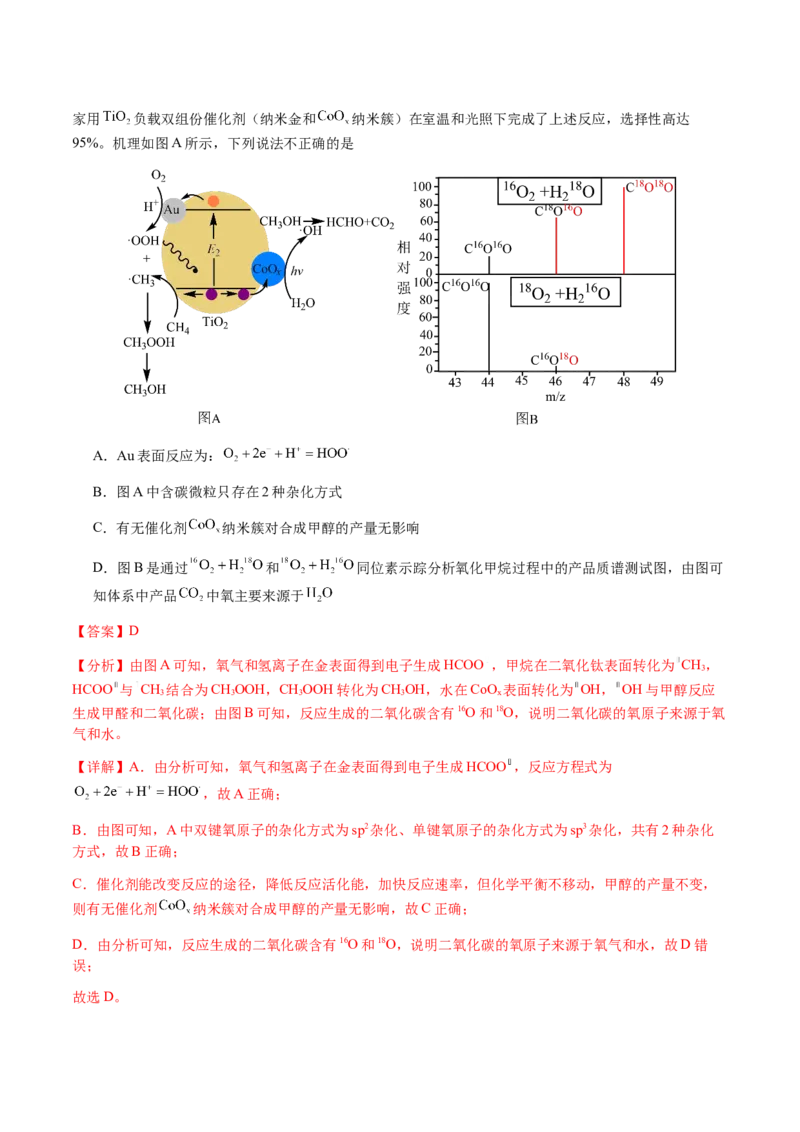
3.(2024·湖北武汉·模拟预测)Scripps研究所近期在温和条件下实现了苯乙酸的邻位羟基化反应,如图为
其反应机理,下列说法错误的是
A.过程③中 作为氧化剂 B.机理中存在非极性键的断裂
C.机理中所涉及物质N原子杂化方式均为 D.在转化过程中 为催化剂
【答案】C
【详解】A.Pd由 变为 的同时, 降价,作为氧化剂,A正确;
B.Pd由 变为 的同时, 断键为O-O,存在非极性键的断裂,B正确;C.机理中所涉及物质N原子杂化方式为 、 ,C错误;
D.PdCl 在反应物苯乙酸前参与反应,后生成,为催化剂,D正确。
2
故选C。
4.(2025·安徽合肥·模拟预测)一种利用Al/Cu/Pd三元金属颗粒复合材料去除水体中硝酸盐的技术机理如
图所示。下列说法中错误的是
A.随水体pH增大,硝酸盐去除率降低
B.H( ads)可以促进 的脱氧,从而产生N
2
C.该机理中三种金属均给出电子,体现还原性
D.金属铝表面的反应过程可表示为:2Al+ (ads) +7H+= 2Al3+ + NH (ads) +2H O
3 2
【答案】C
【详解】A.随水体pH增大,则溶液碱性增强,导致铝催化剂和碱反应,催化效率降低,硝酸盐去除率降
低,A正确;
B.由图可知,H( ads)可以和 ( ads)反应生成氮气,故可促进 的脱氧,从而产生N,B正确;
2
C.由图可知,该机理中是铝离子给出电子体现还原性,而Cu、Pd没有失去电子,C错误;
D.金属铝表面的反应为在酸性条件下, (ads)和铝在铝表面生成铝离子、NH (ads) ,根据质量守恒可
3
知,还会生成HO,可表示为:2Al+ (ads) +7H+= 2Al3+ + NH (ads) +2H O,D正确;
2 3 2
故选C。
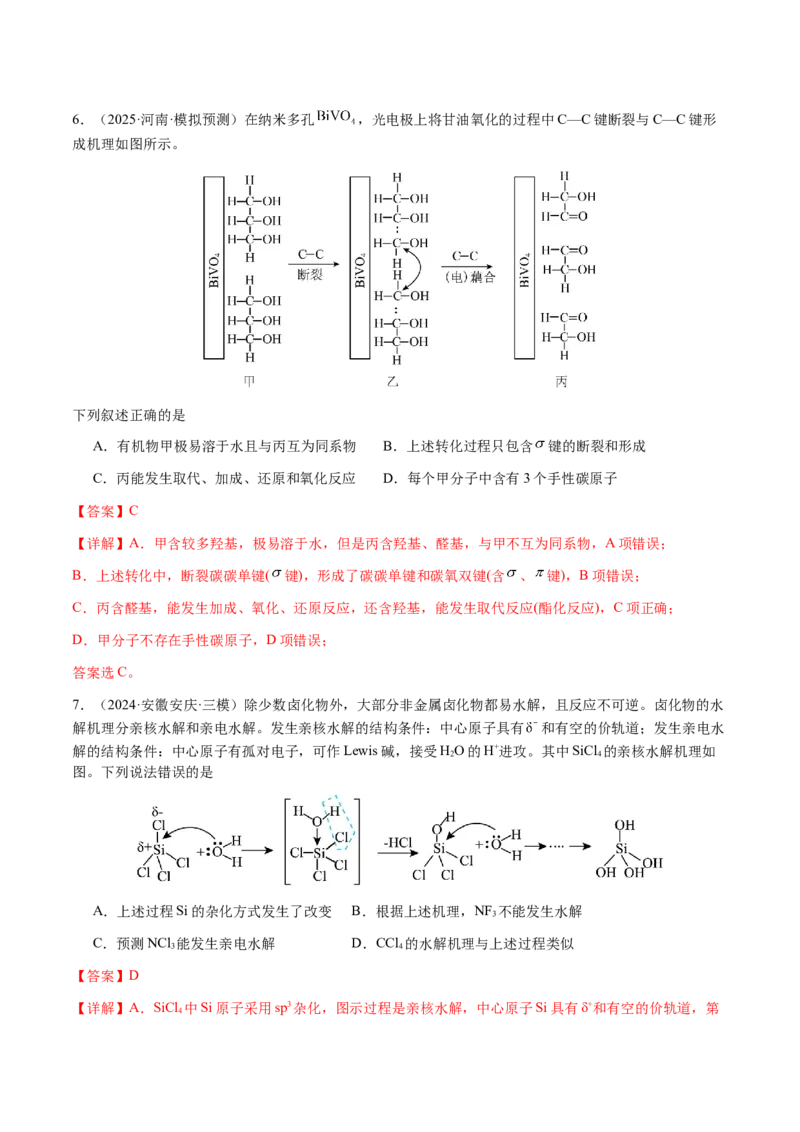
5.(2024·黑龙江哈尔滨·二模)甲烷与氧气直接选择性转化为甲醇是当今催化领域的“梦想反应”,科学家用 负载双组份催化剂(纳米金和 纳米簇)在室温和光照下完成了上述反应,选择性高达
95%。机理如图A所示,下列说法不正确的是
A.Au表面反应为:
B.图A中含碳微粒只存在2种杂化方式
C.有无催化剂 纳米簇对合成甲醇的产量无影响
D.图B是通过 和 同位素示踪分析氧化甲烷过程中的产品质谱测试图,由图可
知体系中产品 中氧主要来源于
【答案】D
【分析】由图A可知,氧气和氢离子在金表面得到电子生成HCOO ,甲烷在二氧化钛表面转化为 CH,
3
HCOO 与 CH 结合为CHOOH,CHOOH转化为CHOH,水在CoO 表面转化为 OH, OH与甲醇反应
3 3 3 3 x
生成甲醛和二氧化碳;由图B可知,反应生成的二氧化碳含有16O和18O,说明二氧化碳的氧原子来源于氧
气和水。
【详解】A.由分析可知,氧气和氢离子在金表面得到电子生成HCOO ,反应方程式为
,故A正确;
B.由图可知,A中双键氧原子的杂化方式为sp2杂化、单键氧原子的杂化方式为sp3杂化,共有2种杂化
方式,故B正确;
C.催化剂能改变反应的途径,降低反应活化能,加快反应速率,但化学平衡不移动,甲醇的产量不变,
则有无催化剂 纳米簇对合成甲醇的产量无影响,故C正确;
D.由分析可知,反应生成的二氧化碳含有16O和18O,说明二氧化碳的氧原子来源于氧气和水,故D错
误;
故选D。6.(2025·河南·模拟预测)在纳米多孔 ,光电极上将甘油氧化的过程中C—C键断裂与C—C键形
成机理如图所示。
下列叙述正确的是
A.有机物甲极易溶于水且与丙互为同系物 B.上述转化过程只包含 键的断裂和形成
C.丙能发生取代、加成、还原和氧化反应 D.每个甲分子中含有3个手性碳原子
【答案】C
【详解】A.甲含较多羟基,极易溶于水,但是丙含羟基、醛基,与甲不互为同系物,A项错误;
B.上述转化中,断裂碳碳单键( 键),形成了碳碳单键和碳氧双键(含 、 键),B项错误;
C.丙含醛基,能发生加成、氧化、还原反应,还含羟基,能发生取代反应(酯化反应),C项正确;
D.甲分子不存在手性碳原子,D项错误;
答案选C。
7.(2024·安徽安庆·三模)除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化物的水
解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有 和有空的价轨道;发生亲电水
解的结构条件:中心原子有孤对电子,可作Lewis碱,接受HO的H+进攻。其中SiCl 的亲核水解机理如
2 4
图。下列说法错误的是
A.上述过程Si的杂化方式发生了改变 B.根据上述机理,NF 不能发生水解
3
C.预测NCl 能发生亲电水解 D.CCl 的水解机理与上述过程类似
3 4
【答案】D
【详解】A.SiCl 中Si原子采用sp3杂化,图示过程是亲核水解,中心原子Si具有δ+和有空的价轨道,第
4一步产物中Si原子的杂化方式为sp3d杂化,杂化方式发生改变,A正确;
B.由于F的电负性强,N具有δ+,但没有空的价层轨道,不能发生亲核水解,中心N原子具有δ+,也不
能接受HO的H+进攻,不能发生亲电水解,故NF 不能发生水解,B正确;
2 3
C.NCl 中中心原子N原子含有1个孤电子对,且N具有δ-,能接受HO的H+进攻,发生亲电水解,生成
3 2
NH 和HClO,C正确;
3
D.C原子最外层为L层,没有d轨道接受水分子中的孤电子对,所以CCl 不能发生类似SiCl 的水解反
4 4
应,D错误;
故答案为:D。
8.(2024·湖北黄冈·二模)消除天然气中 是能源领域的热点,利用 表面吸附 时,研究表
明有两种机理途径,如图所示。
下列说法错误的是
A.途径1历程中最大能垒为
B.使用催化剂该吸附过程释放能量减少
C. 的速率:途径1<途径2
D. 在吸附过程中提供了 原子
【答案】B
【详解】A.由图示可知,途径1历程中最大能垒为(-362.6kJ/mol)-(-567.1 kJ/mol)= ,故A正
确;
B.催化剂只能改变化学反应速率,不能影响吸附过程中释放的能量,故B错误;
C.活化能越大、反应速率越小,则 的速率:途径1<途径2,故C正确;
D.吸附过程中有氧原子参加,而HS中不含氧原子,所以 在吸附过程中提供了 原子,故D正
2
确;
故答案为:B。9.(2025·北京·模拟预测)烯烃可与卤素发生加成反应,涉及环正离子中间体,历程如下:
已知:①反应机理表明,此反应是分两步的加成反应,卤素离子从背面进攻。
②反应中,能否形成环正离子与卤素电负性,半径相关。
下列说法不正确的是
A.加成过程中,Br-Br键受到��电子云的作用,使键具有一定极性
B.乙烯与溴水反应,产物存在BrCHCHOH
2 2
C.烯烃与HOCl的加成也可能通过环正离子机理进行
D.此加成过程,顺式产物与反式产物含量相当
【答案】D
【详解】A.根据反应历程可知,加成过程中,Br-Br键受到��电子云的作用,使键具有一定极性,即含
有带正、负电荷的溴离子,A正确;
B.溴水中有Br 单质,水分子,加成过程中通过第一步生成环正离子后,可能带负电的氢氧根从背面进攻
2
生成BrCHCHOH,B正确;
2 2
C.HOCl也会变为带正电荷的卤素离子和带负电荷的氢氧根,故烯烃与HOCl的加成也可能通过环正离子
机理进行,C正确;
D.由于加成过程中第一步是慢反应,第二步是快反应,故反式产物比顺式产物多,D错误;
故选D。
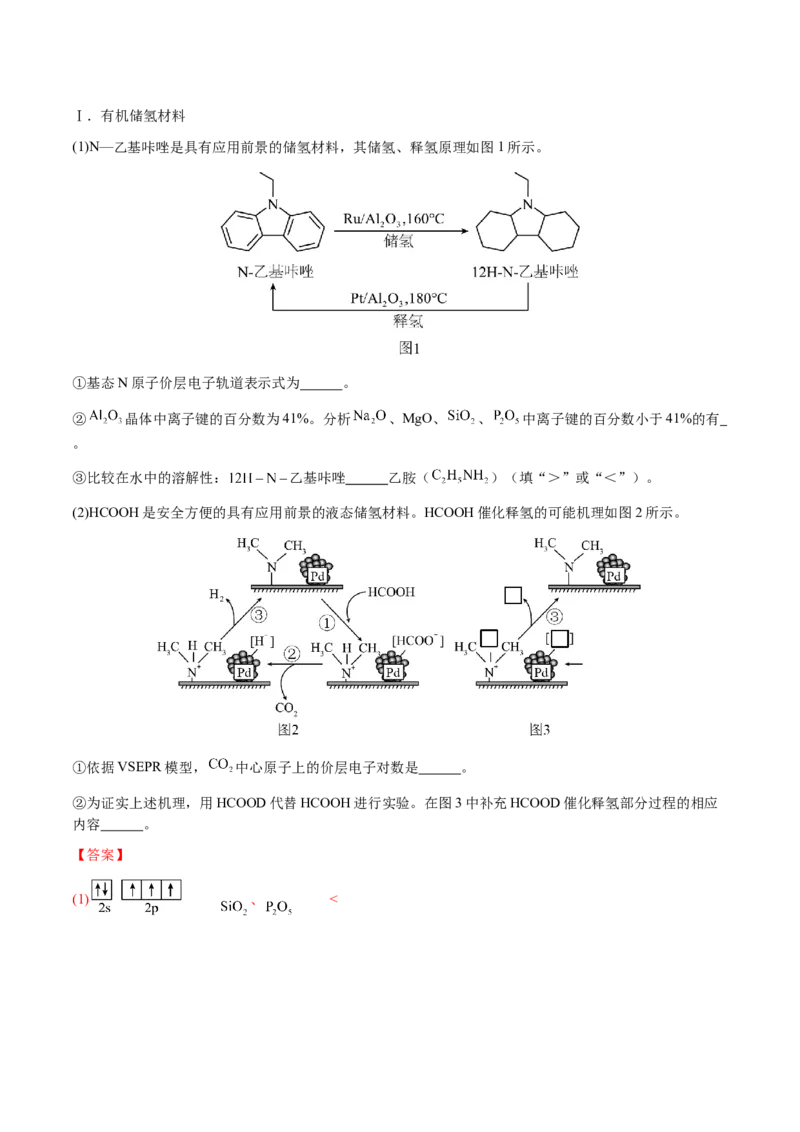
10.(2024·河北沧州·三模)苯甲酸苯甲酯可以用作香料、食品添加剂及一些香料的溶剂,还可以用作塑
料、涂料的增塑剂,其合成机理如下图所示,下列说法不正确的是A.总反应:
B.物质B中碳原子、氧原子的杂化类型相同
C.苯甲酸苯甲酯中除氢原子外的其他所有原子可能共平面
D.该过程中存在极性键和非极性键的断裂和形成
【答案】A
【详解】A.在总反应流程中,物质 先被消耗掉后又重新生成,因此物质D才是总反应的催化剂,总反
应为: ,A错误;
B.酯基中双键氧原子采取 杂化,单键氧原子采取 杂化,物质 中碳原子、氧原子均存在 杂化和
杂化,两者的杂化类型相同,B正确;
C.苯环为平面结构,直接与苯环相连的原子在苯环平面内,次相连的原子以单键连接,可旋转至苯环平
面内,因此,苯甲酸苯甲酯中除氢原子外的其他所有原子可能共平面,C正确;
D. 参与反应断裂非极性键,生成 时,存在碳碳键非极性键的生成; 过程中,断裂 极
性键,并形成 极性键,因此,该过程中存在极性键和非极性键的断裂和形成,D正确。
故答案选A。
11.(2024·黑龙江牡丹江·一模)除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化
物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有 δ+ 和有空的价轨道。发
生亲电水解的结构条件:中心原子有孤对电子,可作 Lewis 碱,接受 HO 的 H+ 进攻。NCl 和SiCl 均可
2 3 4发生水解反应,其中NCl 的水解机理示意图如下:
3
下列说法正确的是
A.NCl 和SiCl 的水解反应机理相同 B.PCl 的水解产物为HPO
3 4 3 3 4
C.由上述理论可知NF 不能发生水解 D.CCl 的水解历程与SiCl 相似
3 4 4
【答案】C
【详解】A.由题意可知,NCl 中的中心N原子有孤对电子,发生亲电水解,而SiCl 的中心原子Si具有
3 4
δ+ 且有空的价轨道,发生亲核水解,所以二者的水解反应机理不同,A错误;
B.PCl 的中心原子P具有 δ+ 且有空的3d轨道,发生亲核水解,故其水解产物为HPO 和HCl,B错
3 3 3
误;
C.由于F的电负性较强,N具有δ+ ,但没有空的价层轨道,不能发生亲核水解,中心N原子具有δ+,
也不能接受 HO 的 H+ 进攻,故也不能发生亲电水解,C正确;
2
D.CCl 的C原子s、p轨道电子都已成键,没有空的价层轨道,CCl 不发生亲核水解,D错误;
4 4
故选C。
12.(2024·广东江门·三模)利用无机物离子 和 (下图简写为 ),实现
了水在催化剂作用下制氧气。用 进行同位素标记实验,证明了产物氧气中的氧原子完全来自水。其
相关机理如下图所示:
下列说法错误的是
A. 在反应中作氧化剂
B.催化氧化水的反应为C.进行同位素标记实验前需排尽体系中的空气
D.若 参与反应,则 中存在
【答案】B
【详解】A.根据图示,CeⅣ→CeⅢ,Ce元素化合价降低, 在反应中作氧化剂,故A正确;
B.根据图示,催化氧化水的反应中没有氢气生成,故B错误;
C.空气中含有氧气,为避免空气中氧气对生成氧气的检验产生影响,进行同位素标记实验前需排尽体系
中的空气,故C正确;
D.由图可知, 与HO反应生成 和H+,根据元素守恒,若H18O参与反应,
2 2
则[(L)RuⅢOOH]6-中存在18O,故D正确;
选B。
13.(2025·重庆九龙坡·二模)尿素 是一种高效化肥,也是一种化工原料。
(1)尿素 技术可用于汽车尾气的处理,该过程中会生成 ,反应如下。
Ⅰ.
Ⅱ.
一定温度下,向恒容容器中投入足量 和一定量的 ,当上述反应达到平衡时,测得
、 。则 (用含p、q的代数式表示,下同),反
应Ⅰ的平衡常数为 。
(2)工业上以 和 为原料合成尿素,图1是反应历程及能量变化,历程中的所有物质均为气态。
①该反应历程中,若 ,则 。
【答案】(1)p-2q p (p-2q) (2)66.5【详解】(1) ,
,则c(HNCO)=(p-2q)mol/L,则反应I的
平衡常数K=c ( NH ) ×c ( HNCO ) =p (p-2q) ( mol/L )2。
3
(2)从图分析,过渡态3的相对能量为241-87=154kJ/mol,则ΔE=154-87.5=66.5kJ/mol。
1
14.(2024·山东泰安·三模)我国高度重视双碳工作实施和目标实现,致力研发二氧化碳综合利用的措施
和途径。
已知: I.CO(g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 3 2 1
II.CO(g)+H(g) CO(g)+HO(g) ΔH₂=+41.2kJ⋅mol-1
2 2 2
Ⅲ.相关化学键的键能数据如表所示。
化学键 C=O H—H C—H C—O O—H
键能/(kJ·mol⁻¹) 803.0 436.0 413.4 351 462.8
回答下列问题:
(1)一氧化碳与氢气合成甲醇气的热化学方程式为 。
(2)研究表明,反应Ⅱ在催化剂上的反应机理如下。其中各物种吸附在催化剂表面活性位的原子用*标注,
如*CO表示CO中C原子吸附在催化剂表面。
I.CO(g)+H(g)+HO(g)= CO (g)+H(g)+HO
2 2 2 2 2 2
II.CO(g)+H(g)+HO*=*COOH+2H*+HO*;
2 2 2
III.*COOH+2H*+HO*= COOH+H*+H O*;
2
iV.*COOH+H*+H O*=*CO+HO*+H*+HO(g);
2 2 2
V.*CO+*OH+H*+H O(g)= *CO+H O*+HO(g);
2 2 2
Vi.*CO+HO*+HOg= CO(g)+2H O(g)。
2 2 2
①HO的作用为生成物和 。
2
②该历程中,脱附和吸附的能量很低,速率控制步骤(即速率最慢步骤)为并骤 (填序号),理由是
。
【答案】
(1)
(2)催化剂 ⅱ 步骤ⅱ和步骤ⅳ中存在断键过程,且步骤ⅱ中断键需要的能量更大【详解】(1)由键能数据计算得,
,反应Ⅰ-反应Ⅱ
得目标反应 ;
(2)①由反应机理可知,部分 作总反应生成物,部分水参加反应后被生成,作催化剂;
②步骤ⅱ为断裂 中 键、 中 键和 中 键,并形成 中 键,步骤ⅳ为断
裂 中 键,步骤ⅱ中断键需要的能量更多,则速率控制步骤为步骤ⅱ;
15.(2024·安徽池州·三模)甲醇是最为常见、应用场景最为广泛的基础化学品之一,甲醇与乙烯、丙烯
和氨是用于生产所有其他化学品的四种关键基础化学品。
(1)已知反应I: ;
反应Ⅱ: ;
则反应Ⅲ: ;
(2)常温常压下利用 催化剂实现二氧化碳加氢制甲醇的反应历程和能量变化图如下(其中吸附
在催化剂表面上的粒子用*标注)
转化历程中决速步骤的反应方程式为 。
【答案】
(1)-90
(2) (或合理答案)
【详解】(1)根据盖斯定律,反应Ⅲ=反应II-反应I,则 ;
(2)该转化历程中活化能越大反应速率越慢,故起决速步骤的方程式为
;
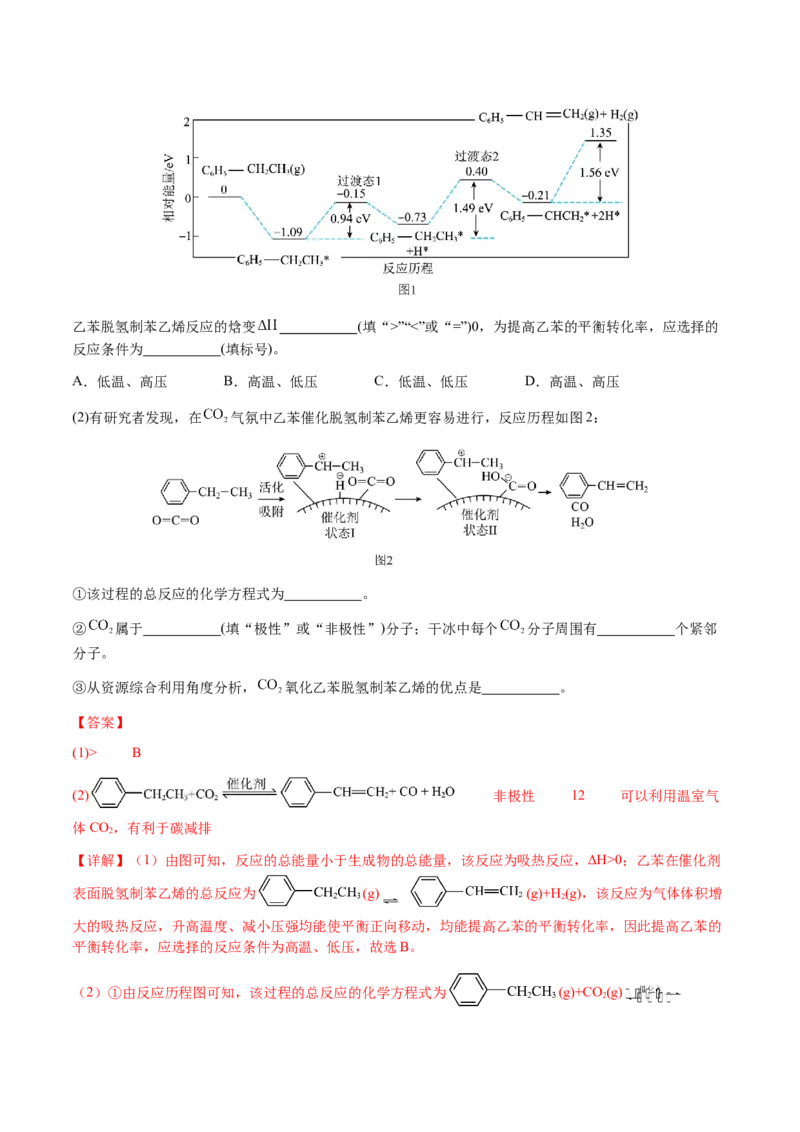
16.(2024·北京朝阳·二模)氢的有效储存与释放是氢能应用的关键问题之一。Ⅰ.有机储氢材料
(1)N—乙基咔唑是具有应用前景的储氢材料,其储氢、释氢原理如图1所示。
①基态N原子价层电子轨道表示式为 。
② 晶体中离子键的百分数为41%。分析 、MgO、 、 中离子键的百分数小于41%的有
。
③比较在水中的溶解性: 乙基咔唑 乙胺( )(填“>”或“<”)。
(2)HCOOH是安全方便的具有应用前景的液态储氢材料。HCOOH催化释氢的可能机理如图2所示。
①依据VSEPR模型, 中心原子上的价层电子对数是 。
②为证实上述机理,用HCOOD代替HCOOH进行实验。在图3中补充HCOOD催化释氢部分过程的相应
内容 。
【答案】
(1) 、 <(2)2
【详解】(1)①基态N为7号元素,其原子价层电子轨道表示式为 。
②硅磷电负性大于铝,则硅氧、磷氧键的离子成分小于铝氧键,故 、MgO、 、 中离子键的
百分数小于41%的有 、 。
③ 能和水形成氢键,而 乙基咔唑不能形成氢键,则在水中的溶解性: 乙基咔
唑小于乙胺;
(2)①CO 分子中C原子的价层电子对数为2+ =2。
2
②由反应历程可知,HCOOD中D原子和氮结合、HCOOD中H原子和Pd结合,然后在③反应中H和D结
合生成氢气,故图示为: ;
17.(2024·广东湛江·二模)二氧化碳的捕集和资源化利用是缓解温室效应的重要战略方向。回答下列问
题:
(1)我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应ⅰ。
反应ⅱ。
和 合成甲醇的热化学方程式为 。
(2)在催化剂 的作用下, 的微观反应历程和相对能量( )如图所示,
其中吸附在催化剂表面上的物种用“*”标注。已知: 表示 , 表示 , 表示 。
历程Ⅰ:
反应甲:历程Ⅱ:
反应乙:
历程Ⅲ:
反应丙:
①历程Ⅲ中的反应丙可表示为 。
②决定 的总反应速率的是历程 (填“Ⅰ”、“Ⅱ”或
“Ⅲ”)。
【答案】
(1)
(2) Ⅲ
【详解】(1)已知,反应ⅰ: ;反应
ⅱ: ;根据盖斯定律可知,由反应ⅰ-反应ⅱ可
得, 和 合成甲醇的热化学方程式为
。
(2)①已知总反应为 ,历程Ⅰ反应甲: ,历程
Ⅱ反应乙: ,则总反应-反应甲-反应乙可得历程Ⅲ中的反应丙,可表示为
。
②历程Ⅰ的活化能为-0.05eV-(-0.37eV)=0.32eV,历程Ⅱ的活化能为0.38eV-(-0.41eV)=0.8eV,历程Ⅲ的活化
能为0.63eV-(-0.85eV)=1.48eV,活化能越大,反应速率越慢,总反应的反应速率应最慢的反应决定,则决
定 的总反应速率的是历程Ⅲ。
18.(2024·广东·一模)苯乙烯是生产塑料和合成橡胶的重要有机原料,可由乙苯催化脱氢获得。
(1)科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历
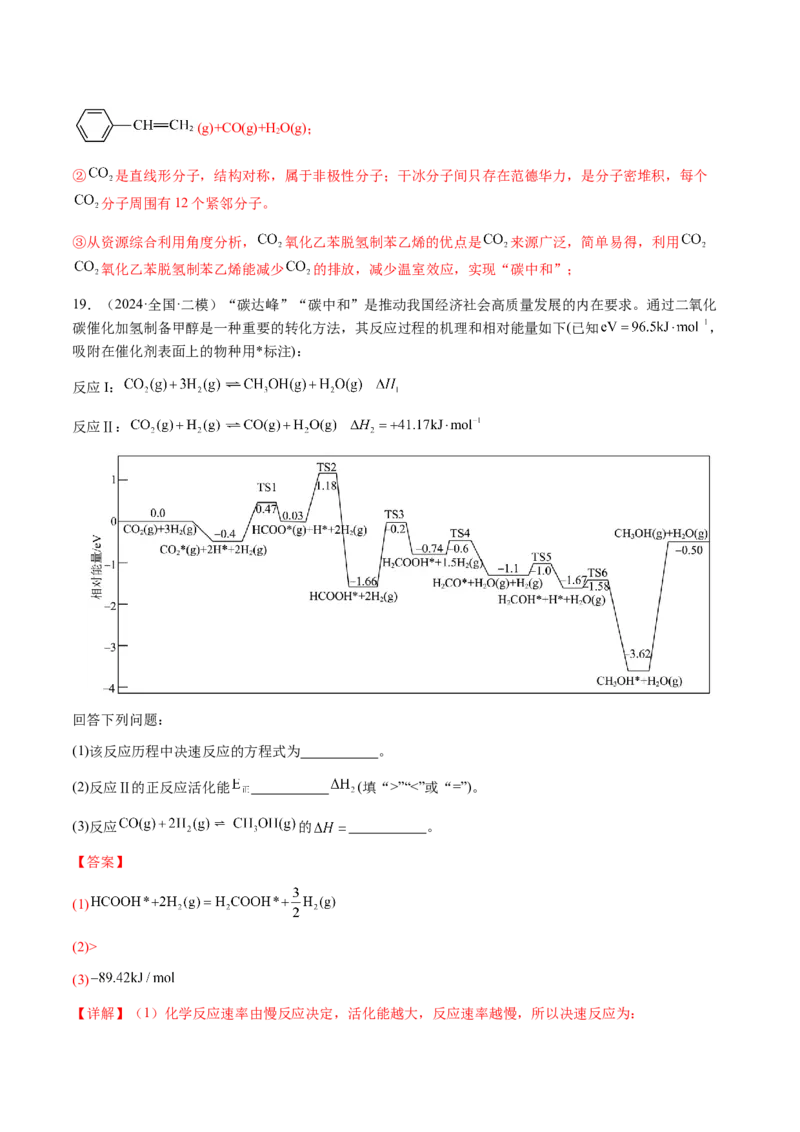
程如图1所示(吸附在催化剂表面的物质用*标注):乙苯脱氢制苯乙烯反应的焓变 (填“>”“<”或“=”)0,为提高乙苯的平衡转化率,应选择的
反应条件为 (填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
(2)有研究者发现,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图2:
①该过程的总反应的化学方程式为 。
② 属于 (填“极性”或“非极性”)分子;干冰中每个 分子周围有 个紧邻
分子。
③从资源综合利用角度分析, 氧化乙苯脱氢制苯乙烯的优点是 。
【答案】
(1)> B
(2) 非极性 12 可以利用温室气
体CO,有利于碳减排
2
【详解】(1)由图可知,反应的总能量小于生成物的总能量,该反应为吸热反应,ΔH>0;乙苯在催化剂
表面脱氢制苯乙烯的总反应为 (g) (g)+H(g),该反应为气体体积增
2
大的吸热反应,升高温度、减小压强均能使平衡正向移动,均能提高乙苯的平衡转化率,因此提高乙苯的
平衡转化率,应选择的反应条件为高温、低压,故选B。
(2)①由反应历程图可知,该过程的总反应的化学方程式为 (g)+CO (g)
2(g)+CO(g)+HO(g);
2
② 是直线形分子,结构对称,属于非极性分子;干冰分子间只存在范德华力,是分子密堆积,每个
分子周围有12个紧邻分子。
③从资源综合利用角度分析, 氧化乙苯脱氢制苯乙烯的优点是 来源广泛,简单易得,利用
氧化乙苯脱氢制苯乙烯能减少 的排放,减少温室效应,实现“碳中和”;
19.(2024·全国·二模)“碳达峰”“碳中和”是推动我国经济社会高质量发展的内在要求。通过二氧化
碳催化加氢制备甲醇是一种重要的转化方法,其反应过程的机理和相对能量如下(已知 ,
吸附在催化剂表面上的物种用*标注):
反应I:
反应Ⅱ:
回答下列问题:
(1)该反应历程中决速反应的方程式为 。
(2)反应Ⅱ的正反应活化能 (填“>”“<”或“=”)。
(3)反应 的 。
【答案】
(1)
(2)>
(3)
【详解】(1)化学反应速率由慢反应决定,活化能越大,反应速率越慢,所以决速反应为:;
(2)反应Ⅱ为吸热反应, ,所以 ;
(3) ,反应 的
;
20.(2024·陕西西安·三模)2023年杭州亚运会主火炬塔首次使用废碳再生的“绿色甲醇”作为燃料,实
现了循环内的零排放。“零碳甲醇”作为公认的新型清洁可再生能源,不易爆炸、储运安全便捷。
甲醇的制备方法有二氧化碳加氢法、电催化法、甲烷催化氧化法等。回答下列问题:
Ⅰ.二氧化碳加氢制甲醇:
① kJ/mol
② kJ/mol
③
已知:甲醇的选择性
(1) ,该反应自发进行的条件是 。
(2)一定温度下,在恒容密闭反应器中,反应③达到平衡,下列措施中能使平衡体系中 增大且加
快化学反应速率的是___________ (填字母)。
A.升高温度 B.充入 ,使体系压强增大
C.再充入1 mol D.将 从体系中分离出去
(3)恒温恒容条件下,原料气 、 以物质的量浓度之比为1∶3投料时,控制合适条件(不考虑反
应③),甲醇的选择性为60%。已知初始压强为4MPa, ,达到平衡时,
mol/L,则该过程中 的平衡转化率为 %,该条件下反应②的 (保留三位有
效数字)。
Ⅱ.电催化法
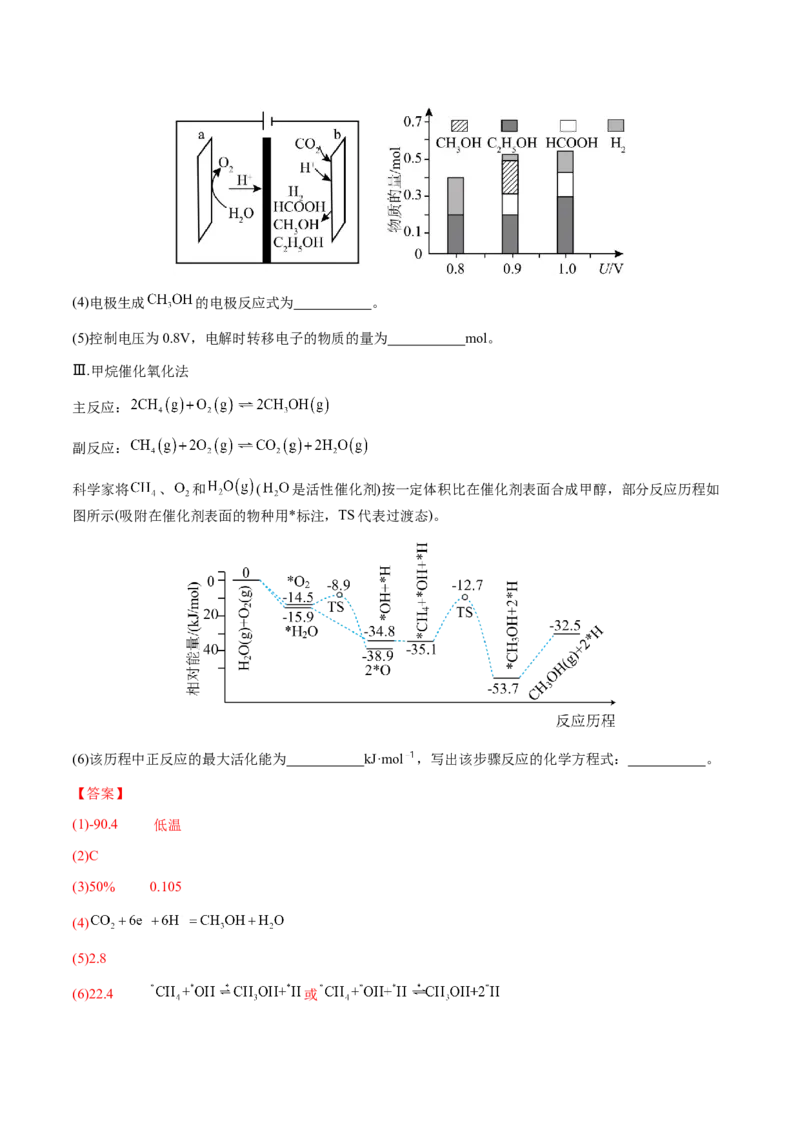
一种基于铜基金属簇催化剂电催化还原 制备甲醇的装置如左下图所示。控制其他条件相同,将一定量
的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如右下图所示。(4)电极生成 的电极反应式为 。
(5)控制电压为0.8V,电解时转移电子的物质的量为 mol。
Ⅲ.甲烷催化氧化法
主反应:
副反应:
科学家将 、 和 ( 是活性催化剂)按一定体积比在催化剂表面合成甲醇,部分反应历程如
图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。
(6)该历程中正反应的最大活化能为 kJ·mol ,写出该步骤反应的化学方程式: 。
【答案】
(1)-90.4 低温
(2)C
(3)50% 0.105
(4)
(5)2.8
(6)22.4 或【详解】(1)由盖斯定律可知, ;反应③是气体
体积减小放热反应,当 时反应能自发进行,则该反应自发进行的条件是低温,故答案
为:-90.4;低温。
(2)③
A.反应③正反应放热,升高温度,平衡逆向移动, 减小,故A错误;
B.恒容条件下充入 ,使体系压强增大,反应物浓度不变,反应速率不变,平衡不移动,
不变,故B错误;
C.再充入 ,H 浓度增大,反应速率加快,平衡正向移动, 增大,故C正确;
2
D.将 从体系中分离出去,由于浓度减小因此所有物质的反应速率减慢,故D错误;
故答案为:C。
(3)恒温恒容条件下, 、 物质的量浓度之比为1∶3,起始时 ,达到平衡
时, mol/L,假设体积为1L,生成的甲醇为xmol,甲醇的选择性为 ,解得
,根据已知条件列出“三段式”:
平衡转化率为 , ,初始压强为4MPa,根据
,有 ,该条件下反应②
,故答案为:50%;0.105。
(4)根据图示,a电极为阳极,b电极为阴极,b极上生成CHOH的电极反应式为
3,故答案为: 。
(5)由图知,控制电压为0.8V时,阴极生成0.2molC HOH和0.2molH,阴极的电极反应式为2CO+12e-
2 5 2 2
+12H+=C HOH+3H O、2H++2e-=H ↑,电解时转移电子物质的量为0.2mol×12+0.2mol×2=2.8mol,故答案
2 5 2 2
为:2.8。
(6)如图可知,该历程中正反应的最大活化能步骤 到 ,活化能为
,该步骤反应的化学方程式为 或
,故答案为22.4; 或
。