文档内容
专题 20 化学键
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 化学键与物质构成
考点二 共价键及其分类
考点三 配位键、配合物、超分子
考点一 化学键与物质构成
1.(2023·浙江·校联考二模)下列化学用语表示正确的是
A.中子数为10的氧原子: B.基态钠离子的电子排布式:
C. 的VSEPR模型为平面三角形 D. 的形成过程:
【答案】C
【解析】A.原子核内有10个中子的氧原子: ,A错误;B.基态钠离子的电子排布式: ,B
错误;C. 的中心S原子价层电子对数为 ,发生sp2杂化,则VSEPR模型为平面三角形,
C正确;D. 的形成过程中钠原子失去电子生成钠离子,氯原子得到电子转化成氯离子,两者通过静
电作用形成氯化钠 ,D错误;故选C。
2.(2023·福建厦门·厦门双十中学校考模拟预测)一定条件下,H 与HCO 在活性Fe O 表面转化为
2 3 4-x
HCOO-,其部分反应机理如图所示。
下列说法正确的是
A.吸附在Fe O 上的两个氢原子带相同电荷
3 4-x
B.生成1molHCOO-理论上转移电子2mol
C.步骤Ⅰ中HCO 发生氧化反应
1
原创精品资源学科网独家享有版权,侵权必究!D.反应过程中只有极性键的断裂与生成
【答案】B
【解析】A.由图可知,吸附在Fe O 上的两个氢原子分别于铁、氧结合,故带不相同电荷,A错误;B.
3 4-x
反应中HCO 转化为HCOO-,根据碳元素化合价变化可知,电子转移为2e-~HCOO-,则生成1molHCOO-理
论上转移电子2mol,B正确;C.步骤Ⅰ中HCO 失去氧,发生还原反应,C错误;D.反应过程中氢气和
HCO 转化为HCOO-和水,反应中存在氢氢键、氢氧键断裂,氢氧键、碳氢键的生成,故还存在氢氢非极
性键断裂,D错误;故选B。
3.(2023·江西赣州·统考模拟预测)短周期元素W 、X、Y、Z的原子序数依次增大。W与Z同主族,Z
的最外层电子数是Y的最外层电子数的2倍,常温下,Y的单质遇浓硝酸时会发生钝化,X的质子数比Y
的少2。下列说法正确的是
A.金属性:X< Y
B.原子半径:Z>>Y> X> W
C.XZ的水溶液显酸性
2
D.化合物XZW 中既含离子键又含共价键
2 3
【答案】D
【分析】短周期元素W 、X、Y、Z的原子序数依次增大;常温下,Y的单质遇浓硝酸时会发生钝化,则
Y为铝;Z的最外层电子数是Y的最外层电子数的2倍,Z最外层电子为6,且原子序数大于铝,为硫,W
与Z同主族,W为氧;X的质子数比Y的少2,则X为11号钠;
【解析】A.同周期从左到右,金属性减弱,非金属性变强,金属性:X> Y,A项错误;B.电子层数越
多半径越大,电子层数相同时,核电荷数越大,半径越小;原子半径:X> Y> Z > W,B项错误;C.NaS
2
为强碱弱酸盐,硫离子水解导致水溶液显碱性,C项错误;D.化合物NaSO 是由钠离子和亚硫酸根离子
2 3
构成的离子化合物,亚硫酸根离子中含有硫氧共价键,D项正确;故选D。
4.(2023·江苏·统考高考真题)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是
氢元素的3种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成 、
、 、 、 等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法
制氢反应中, 与足量 反应生成 和 吸收131.3kJ的热量。 在金属冶炼、
新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。我国科学
家在氢气的制备和应用等方面都取得了重大成果。下列说法正确的是
A. 、 、 都属于氢元素
B. 和 的中心原子轨道杂化类型均为
C. 分子中的化学键均为极性共价键
D. 晶体中存在Ca与 之间的强烈相互作用
【答案】A【解析】A. 、 、 都属于氢元素,三者互为同位素,统称为氢元素,A正确;B. 和 的
中心原子轨道杂化类型均为 ,B错误;C. 分子中的化学键既存在O-H极性共价键,也存在O-O
非极性共价键,C错误;D. 晶体中存在Ca2+与 之间的离子键,为强烈相互作用,D错误。故选
A。
5.(2023·上海嘉定·统考二模)下列物质中只含有非极性共价键的是
A.NaOH B.I C.KCl D.HS
2 2
【答案】B
【解析】A.NaOH中存离子键和极性共价键,选项A不合题意;B.I 中只存在非极性共价键,选项B符
2
合题意;C.KCl中只存在离子键,选项C不合题意;D.HS中只含有极性共价键,选项D不符合题意;
2
答案选B。
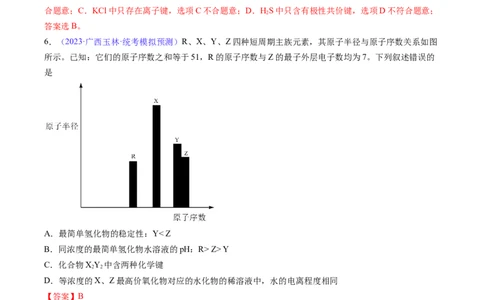
6.(2023·广西玉林·统考模拟预测)R、X、Y、Z四种短周期主族元素,其原子半径与原子序数关系如图
所示。已知:它们的原子序数之和等于51,R的原子序数与Z的最子外层电子数均为7。下列叙述错误的
是
A.最简单氢化物的稳定性:Y< Z
B.同浓度的最简单氢化物水溶液的pH:R> Z> Y
C.化合物XY 中含两种化学键
2 2
D.等浓度的X、Z最高价氧化物对应的水化物的稀溶液中,水的电离程度相同
【答案】B
【分析】由图示可知,X、Y、Z在第三周期且Y、Z相邻,R的原子序数与Z的最外层电子数相等,若Z
的最外层电子数为6,则R、X、Y、Z分别为C、Si、P、S、X与Y也相邻了,不符合题干条件;若Z的
最外层电子数为7,依据R、X、Y、Z的原子序数之和等于51,则R、X、Y、Z分别为N、Na、S、C1,
符合题干条件。
【解析】A.非金属性:SZ>Y>X
B.最简单氢化物的稳定性:Y>Z
C. 的乙、丙、已溶液中,由水电离出的 相同
D.甲、乙、丙中均含有极性键和离子键
【答案】D
【分析】戊的水溶液能使pH试纸变蓝,可知戊为NH ;结合原子序数大小可知X为H,Y为N,甲和丙
3
均为焰色试验呈黄色的盐,可知两者均含Na元素,甲、乙反应生成物中含水,则可知四种元素中有一种
为O,结合以上分析可知Z为O,则知X、Y、Z、M分别为H、N、O、Na,甲~己分别为 、
、 、 、 、 。
【解析】A.原子半径:Na>N>O>H,A项错误;B.非金属性:O>N,最简单氢化物的稳定性:
,B项错误;C. 促进水的电离, 对水的电离没有影响, 抑制水的电离,
C项错误;D. 、 、 均含有极性键和离子键,D项正确;故选:D。
8.(2023·四川巴中·统考模拟预测)一种外用消炎药主要成分的结构如图所示。分子结构中的苯环和甲基
部分已给出,X、Y、Z、W、M为原子序数依次增大的短周期主族元素,其中X的简单氢化物分子空间结
构为三角锥形,W与Y同主族。下列说法错误的是
A.简单氢化物的沸点:Y>X>M
B.最高价氧化物对应水化物的酸性:M>W
C.Y与Z形成的化合物一定含有离子键和共价键
D.WY 不能够使紫色石蕊试液褪色
2
【答案】C
【分析】X、Y、Z、W、M为原子序数依次增大的短周期主族元素,其中X的简单氢化物分子空间结构为三角锥形,W与Y同主族,且根据价键可推知W为S、Y为O、X为N,则原子序数大于S的M为Cl,Z
离子带一个单位正电荷,为Na。
【解析】A.NH 、HO均存在氢键,且HO形成的氢键强度大于NH ,简单氢化物的沸点:HO>NH >
3 2 2 3 2 3
HCl,故A正确;B.非金属性越强最高价氧化物的水化物的酸性越强,最高价氧化物对应水化物的酸性:
HClO>HSO ,故B正确;C.O与Na形成的化合物NaO,只含有离子键,故C错误;D.WY 为
4 2 4 2 2
SO ,溶于水生成亚硫酸呈酸性,能够使紫色石蕊试液变红,但不褪色,故D正确;故选C。
2
9.(2023·河南南阳·南阳中学校考三模)X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子
序数总和等于49。它们的化合物在常温下有如下转化关系:
已知:乙、戊分子都含有10个电子。甲为三元化合物,其他化合物均为二元化合物。下列说法正确的是
A.简单阴离子结合质子能力: Q>W
B.常温下,0. 1 mol·L-1简单氢化物水溶液的pH: Q>W>Z> Y
C.最高价氧化物对应水化物的酸性: Q>W
D.化合物WQ 中含极性键、非极性键和离子键
2 2
【答案】C
【分析】丁能够使品红溶液褪色,加热后又变红色,说明丁是SO ,丙和戊两种气体混合冒白烟,戊是二
2
元化合物且是10电子物质,确定是NH ,丙是二元化合物是HCl,乙是液态10电子物质确定是HO,X、
3 2
Y、Z、W、Q元素分别是H、N、O、S、Cl,原子序数总和为49,甲是三元液态化合物,与水反应生成
HCl、SO 两种物质,说明甲是SOCl 。
2 2
【解析】A.简单阴离子结合质子能力S2-大于Cl-离子,故A错误;B.0. 1 mol·L-1简单氢化物水溶液的
pH:NH >H O>HS>HCl,故B错误;C.最高价氧化物对应水化物的酸性:HClO>H SO ,故C正确;
3 2 2 4 2 4
D.SCl 中没有离子键,故D错误;答案选C。
2 2
10.(2023·山东德州·统考二模)胍( )是一元强碱,分子构型为平面型,其盐酸盐(
)是核酸检测液的主要成分。下列说法错误的是
A.胍中C、N杂化方式均为sp2 B.胍具有很强的吸湿性
C.胍的熔点低于胍盐 D.胍盐中含有的化学键均为极性键
【答案】AD
【解析】A.胍中C形成3条σ键,无孤电子对为sp2杂化,氨基中的N形成3条σ键,同时含有一对孤电子对,为sp3杂化,A错误;B.胍为吸湿性很强的无色晶体,B正确;C.胍为分子晶体,而胍盐为离子
晶体,因此胍的熔点低于胍盐,C正确;D.胍盐中含有离子键,D错误;故答案选AD。
考点二 共价键及其分类
1.(2023·黑龙江大庆·大庆市东风中学校考模拟预测)下列说法正确的是
A.基态 Cr 原子有 6 个未成对电子
B.元素 Ga 的核外电子排布式为 ,位于元素周期表中 p 区
C.NH 中 N—H 间的键角比 CH 中 C—H 间的键角大
3 4
D.XY 分子为 V 形,则 X 原子一定为 sp2 杂化
2
【答案】A
【解析】A.铬为24号元素,基态Cr原子价电子排布为3d54s1,基态 Cr 原子有 6 个未成对电子,A正
确;B..元素Ga为31号元素,位于元素周期表中p区,其核外电子排布式为[Ar]3d104s24p1,B错误;
C.NH 是三角锥形含有1对孤电子对,CH 是正四面体形无孤电子对,因此NH 中N-H间的键角比CH
3 4 3 4
中C-H间的键角小,C错误;D.XY 分子中原子个数比为1:2,XY 分子为 V 形,则X原子不一定
2 2
为sp2杂化,也可能含有2对孤电子对为sp3杂化,D错误;故选A。
2.(2023·海南·校联考一模)化合物ClF 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等,能与
3
NH 发生反应: 。下列叙述正确的是
3
A. 的电子式为
B.上述反应产生 时,转移
C. 键的键长比 键的键长短
D. 晶体中存在离子键、 键、配位键
【答案】D
【解析】A.NH 是共价化合物,其电子式为 ,A错误;B.分析反应
3
可知,该反应过程中转移电子为6e-,故上述反应产生1molCl 时,转移
2
6mole-,B错误;C.已知Cl的原子半径大于F的原子半径,故 键的键长比 键的键长长,C错
误;D.NH F晶体中存在 和F-之间的离子键、 内部的N-H均为 键,还存在一个N→H配位键,
4
D正确;故答案为:D。
3.(2023·辽宁·校联考三模) -二碘四硅双环 丁烷分子如图,该分子中四个硅原子共面且其中两
个硅原子间形成 电子单键(特殊 键)。有关该分子的说法中错误的是A.电负性:
B.该分子中砫原子的杂化方式是
C.键角1>键角2
D.该分子形成的晶体中存在的化学键有极性键、非极性键和 键
【答案】B
【解析】A.同周期主族元素电负性由左至右逐渐增大,同主族元素电负性由上至下逐渐减小,根据这种
周期性变化规律,所以电负性:C> H> Si,选项A正确;B.未形成π电子单键的硅原子均形成4个 键且
没有孤对电子,为sp3杂化,形成π电子单键的硅原子形成3个 键且没有孤对电子,为sp2,所以该分子
中硅原子的杂化方式是sp3、sp2,选项B错误;C.键角1处硅原子为sp2杂化,键角2处硅原子为sp3杂化,
所以键角1 >键角2,选项C正确;D.由图可知,该分子中存在C - Si极性键,Si - Si诽极性键和Si - Si键
形成的π电子单.键,故该分子形成的晶体中存在的化学键有极性键、非极性键和π键,选项D正确;答案
选B。
4.(2023·北京海淀·101中学校考三模)甲磺酸 是一种强酸。下列说法正确的是
A.推测甲磺酸难溶于水 B.该分子中心原子S的价层电子对数为6
C.分子中所有化学键均为极性共价键 D.该分子中硫氧键的键长均相同
【答案】C
【解析】A.该物质中有-OH可与水形成氢键,其溶解性较大,A项错误;B.S的价层电子对=4+0=4对,
B项错误;C.分子中有C-H、C-S、S=O、S-O、O-H均为极性键,C项正确;D.分子中S=O和S-O键键
长不同,D项错误;故选C。
5.(2023·广东汕头·统考三模)尿素可以减少柴油机尾气氮氧化物的排放,发生反应:
,设 为阿伏伽德罗常数,下列有关说法正确的是
A. 均为非极性分子
B.标况下, 含有电子数C. 中含有 键数目为
D.反应过程中生成 时转移电子数为
【答案】C
【解析】A.N、CO 均为直线形分子,分子中正负电荷中心重合,故均为非极性分子,HO为V形结构,
2 2 2
分子正负电荷中心不重合,属于极性分子,A错误;B.已知1分子NO 中含有(7+2×8)=23个电子,故标
2
况下, 即 =1molNO 中含有电子数为 ,B错误;C.已知CO(NH) 中含有一个
2 2 2
C=O双键,其余原子间均为单键,即1分子CO(NH) 中含有1个 键,故 中含有 键数目
2 2
为 ,C正确;D.反应中 转移电子数为:16mol电子,则
反应过程中生成 即 =1mol时转移电子数为 ,D错误;故答案为:C。
6.(2023·河北·张家口市宣化第一中学校联考二模)四氯化碳是常用的不燃溶剂,由如下反应制备:
。下列说法正确的是
A.CS 的熔沸点比CO 的低 B.CCl 的热稳定性比CF 的高
2 2 4 4
C.该制备反应是熵增过程 D.CS 的键角大于CCl 的键角
2 4
【答案】D
【解析】A.CS 和CO 均为分子晶体,结构相似,CS 的相对分子质量比CO 大,分子间作用力较大,故
2 2 2 2
CS 的熔沸点比CO 高,故A错误;B.氢化物共价键的键能越大,对应的氢化物越稳定,Cl的原子半径
2 2
大于F,键长:C-Cl>C-F,键能:CCl < CF,所以CCl 的热稳定性比CF 的低,故B错误;C.该正反应
4 4 4 4
是气体分子数减小的反应,是熵减过程,故C错误;D.CCl 分子为正四面体型,键角为109°28′,CS 分
4 2
子为直线型,键角为180°,即CS 的键角大于CCl 的键角,故D正确;故选:D。
2 4
7.(2023·海南·校联考一模)过氧乙酸( )能有效灭活病毒,在一定条件下可通过反应
制备。设 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有的 键数目为
B.该反应中消耗 时转移 电子
C. 中含有的中子数为
D. 溶液中含有的 数目为
【答案】A
【解析】A.已知一分子CHCOOH中含有7个 键,故 中含有的 键数目为
3
= ,A正确;B.HO 中O的化合价为-1价,CHCOOOH中有2个O的化合价
2 2 3
为-1价,故该反应中为非氧化还原反应,不存在电子的转移,B错误;C. 中含有的中子数为=1.7 ,C错误;D.已知CHCOOH为弱酸,其在水溶液中只有部分
3
电离,故100mL0.1mol/LCH COOH溶液中含有的CHCOO-数目小于 ,D错误;故答案为:A。
3 3
8.(2023·广东梅州·统考二模)PCl 是合成各种有机农药的原料。下列判断错误的是
3
A.PCl 分子中P原子为sp2杂化,分子呈平面三角形
3
B.P的电负性小于S,而P的第一电离能大于S的第一电离能
C.PCl 的键角小于BCl 的键角
3 3
D.PCl 分子的稳定性低于PF 分子,因为P-F键的键能大
3 3
【答案】A
【解析】A. 中P原子的价层电子对数为4,P原子为 杂化,含有3个 键和 =1对孤电子对,
所以空间结构为三角锥形,A项错误;B.P的电负性小于S,但是基态P原子的价电子排布式为 ,
3p轨道有3个电子,为半充满稳定状态,所以P的第一电离能大于S的第一电离能,B项正确;C.由A
项知, 的空间结构为三角锥形, 中B为 杂化,空间结构为平面三角形, 的键角较大,C
项正确;D.因为氟原子的半径小,P—F键的键长较短,键能较大,所以 的稳定性较强,D项正确;
故选A。
9.(2023·辽宁大连·大连八中校考模拟预测)三硫化四磷( )是黄绿色针状晶体,易燃、有毒,分子结
构如图所示。下列有关 的说法中正确的是
A. 中仅P原子最外层均满足8电子稳定结构
B.键角:
C. 中P原子为 杂化,S原子为 杂化
D. 分子中含有6mol极性共价键
【答案】D
【解析】A.P最外层5个电子,形成了3个共价键,S最外层6个电子,形成了2个键,因此都满足8电
子稳定结构,不仅仅是P原子,故A错误;B. 均采用sp3杂化,PCl 的中心原子有一对孤电子,
3
而 无孤电子对,因为孤电子对对成键电子对有排斥力,所以导致Cl-P-Cl键角更小,即键角比较:
,故B错误;C.S原子价层电子对数是4,则S原子是sp3杂化,故C错误;D.根据结构简式
可知1mol 分子中含有6mol极性共价键,3mol非极性共价键,故D正确;答案选D。
10.(2023·河北·张家口市宣化第一中学校联考二模)向Co2+盐溶液中加入过量的KNO 溶液,并以少量
2醋酸酸化,加热后从溶液中析出K[Co(NO )]。下列有关说法错误的是
3 2 6
A.基态Co2+核外电子排布式为[Ar]3d7
B. 的空间构型为V形
C.醋酸分子中σ键与π键数目之比为3∶1
D.配离子 中Co2+提供空轨道
【答案】CD
【解析】A.Co的原子序数是27,其原子基态核外电子排布式为 ,A项正确;B. 中心原子N
的价层电子对数为3,且含有1个孤电子对,空间构型为V形,B项正确;C.单键全为σ键,双键中一个
σ键,一个 键, 中σ键与 键数目之比为7:1,C项错误;D.配离子 中
提供空轨道,D项错误;答案选CD。
考点三 配位键、配合物、超分子
1.(2023·河北邢台·邢台市第二中学校联考三模)近年来,光催化剂的研究是材料领域的热点。一种Ru
配合物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法错误的是
A.Ru配合物中第二周期元素的电负性:O>N>C
B.吡啶( ,原子在同一平面)中C、N原子的杂化方式分别为 、
C.该配合物中Ru的配位数是6
D. 中P的价层电子对数为4,空间结构为正四面体形
【答案】B
【解析】A.第二周期主族元素从左向右电负性逐渐增强,因此电负性:O>N>C,故A正确;B.
中原子在同一平面,则C、N原子的价层电子对数均为3,杂化方式均为 ,故B错误;C.根据图中
Ru与周围的原子得到该配合物中Ru的配位数是6,故C正确;D. 中P的价层电子对数为4,无孤对
电子,空间结构为正四面体形,故D正确。综上所述,答案为B。
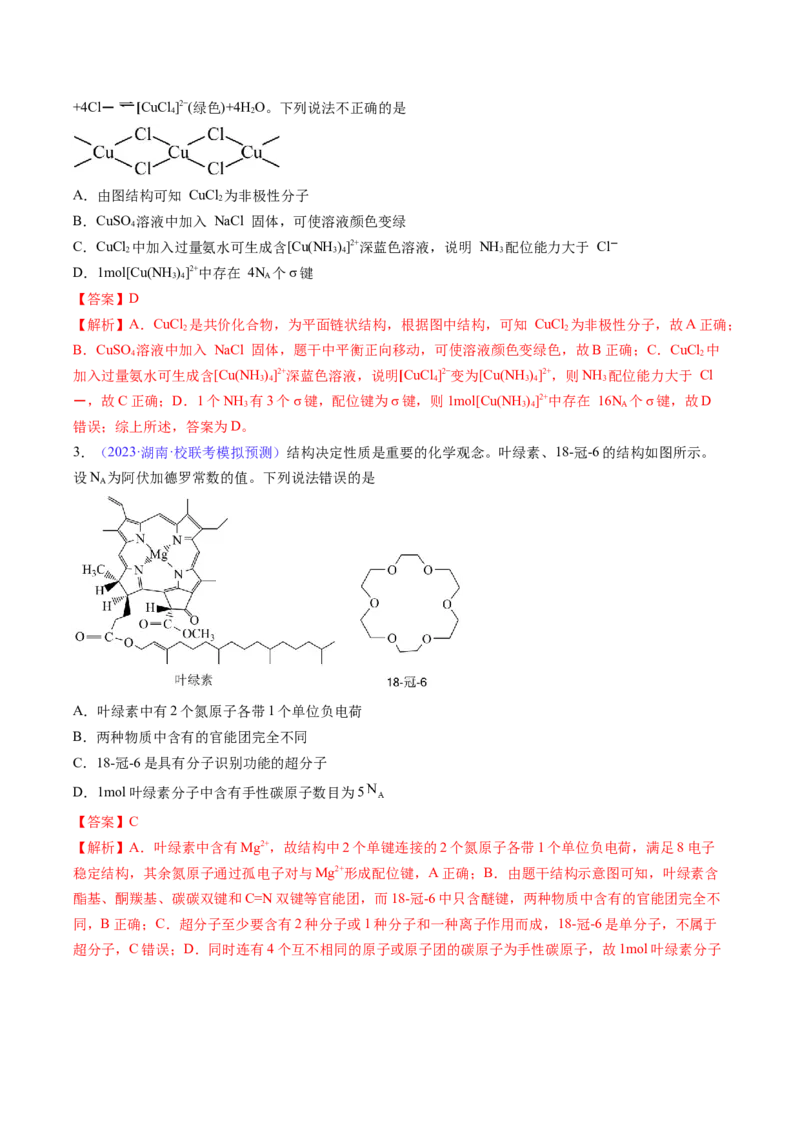
2.(2023·浙江绍兴·统考二模)X 射线研究表明 CuCl 是共价化合物,为平面链状结构,以(CuCl )n形式
2 2
存在,如图所示。CuCl 易溶于水、乙醇、丙酮和氨水等,其水溶液常呈绿色,原因是[Cu(H O) ]2+(蓝色)
2 2 4+4Cl- [CuCl ]2−(绿色)+4H O。下列说法不正确的是
4 2
A.由图结构可知 CuCl 为非极性分子
2
B.CuSO 溶液中加入 NaCl 固体,可使溶液颜色变绿
4
C.CuCl 中加入过量氨水可生成含[Cu(NH )]2+深蓝色溶液,说明 NH 配位能力大于 Cl-
2 3 4 3
D.1mol[Cu(NH)]2+中存在 4N 个σ键
3 4 A
【答案】D
【解析】A.CuCl 是共价化合物,为平面链状结构,根据图中结构,可知 CuCl 为非极性分子,故A正确;
2 2
B.CuSO 溶液中加入 NaCl 固体,题干中平衡正向移动,可使溶液颜色变绿色,故B正确;C.CuCl 中
4 2
加入过量氨水可生成含[Cu(NH )]2+深蓝色溶液,说明[CuCl ]2−变为[Cu(NH )]2+,则NH 配位能力大于 Cl
3 4 4 3 4 3
-,故C正确;D.1个NH 有3个σ键,配位键为σ键,则1mol[Cu(NH)]2+中存在 16N 个σ键,故D
3 3 4 A
错误;综上所述,答案为D。
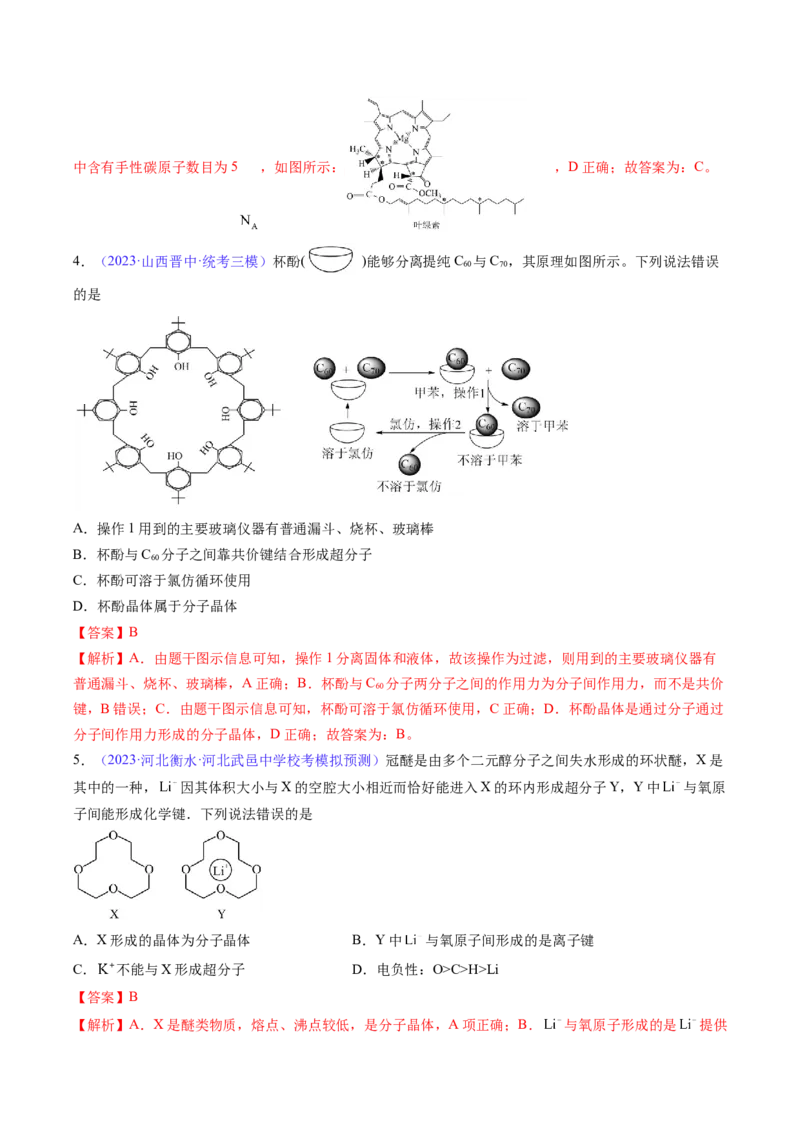
3.(2023·湖南·校联考模拟预测)结构决定性质是重要的化学观念。叶绿素、18-冠-6的结构如图所示。
设N 为阿伏加德罗常数的值。下列说法错误的是
A
A.叶绿素中有2个氮原子各带1个单位负电荷
B.两种物质中含有的官能团完全不同
C.18-冠-6是具有分子识别功能的超分子
D.1mol叶绿素分子中含有手性碳原子数目为5
【答案】C
【解析】A.叶绿素中含有Mg2+,故结构中2个单键连接的2个氮原子各带1个单位负电荷,满足8电子
稳定结构,其余氮原子通过孤电子对与Mg2+形成配位键,A正确;B.由题干结构示意图可知,叶绿素含
酯基、酮羰基、碳碳双键和C=N双键等官能团,而18-冠-6中只含醚键,两种物质中含有的官能团完全不
同,B正确;C.超分子至少要含有2种分子或1种分子和一种离子作用而成,18-冠-6是单分子,不属于
超分子,C错误;D.同时连有4个互不相同的原子或原子团的碳原子为手性碳原子,故1mol叶绿素分子中含有手性碳原子数目为5 ,如图所示: ,D正确;故答案为:C。
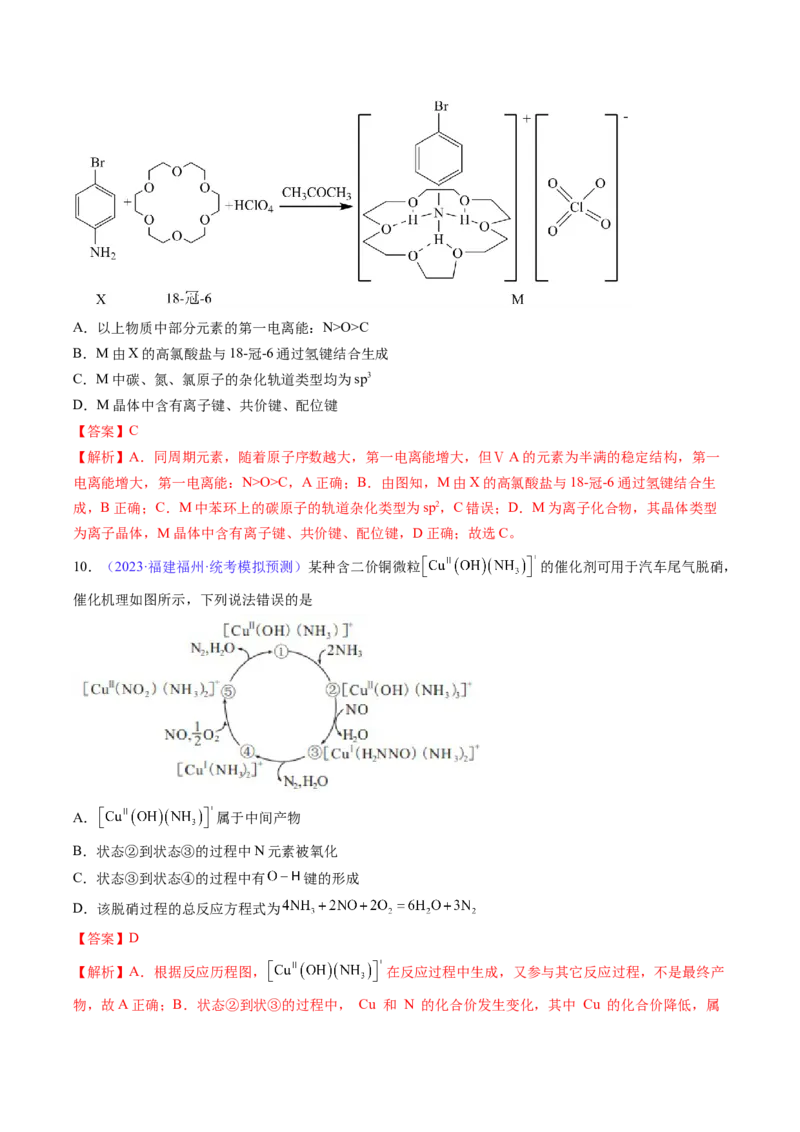
4.(2023·山西晋中·统考三模)杯酚( )能够分离提纯C 与C ,其原理如图所示。下列说法错误
60 70
的是
A.操作1用到的主要玻璃仪器有普通漏斗、烧杯、玻璃棒
B.杯酚与C 分子之间靠共价键结合形成超分子
60
C.杯酚可溶于氯仿循环使用
D.杯酚晶体属于分子晶体
【答案】B
【解析】A.由题干图示信息可知,操作1分离固体和液体,故该操作为过滤,则用到的主要玻璃仪器有
普通漏斗、烧杯、玻璃棒,A正确;B.杯酚与C 分子两分子之间的作用力为分子间作用力,而不是共价
60
键,B错误;C.由题干图示信息可知,杯酚可溶于氯仿循环使用,C正确;D.杯酚晶体是通过分子通过
分子间作用力形成的分子晶体,D正确;故答案为:B。
5.(2023·河北衡水·河北武邑中学校考模拟预测)冠醚是由多个二元醇分子之间失水形成的环状醚,X是
其中的一种, 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原
子间能形成化学键.下列说法错误的是
A.X形成的晶体为分子晶体 B.Y中 与氧原子间形成的是离子键
C. 不能与X形成超分子 D.电负性:O>C>H>Li
【答案】B
【解析】A.X是醚类物质,熔点、沸点较低,是分子晶体,A项正确;B. 与氧原子形成的是 提供空轨道、氧原子提供孤电子对的配位键,B项错误;C. 半径比 大许多,其体积比X的空腔大,无
法进入空腔内,不能形成超分子,C项正确;D.由同周期电负性递变规律知,电负性:O>C>Li,由烃中
碳元素显负价而氢元素显+1价知,电负性:C>H,非金属元素的电负性大于金属元素的电负性,故电负性:
O>C>H>Li,D项正确;故选B。
6.(2023·黑龙江哈尔滨·哈尔滨三中校考模拟预测)在超分子化学中,常用Cu+模板合成各种拓扑结构分
子,图1为诺贝尔得主Auvage教授利用亚铜离子为模板合成的索烃结构。Cu也可与Zn、Sn及S构成四元
半导体化合物的四方晶胞,结构如图2所示,下列说法错误的是
A.索烃分子既有极性键又有非极性键
B.1mol索烃中所含的配位键的数量为8N
A
C.半导体化合物中Zn原子与Sn原子个数比为1:2
D.在四方晶胞中Sn位于S原子组成的四面体空隙中
【答案】C
【解析】A.索烃分子中C、N之间,C、H之间,C、O之间,形成极性键,C、C之间形成非极性键,既
有极性键又有非极性键,A正确;B.索烃中每个Cu+形成4个配位键,1mol索烃中所含的配位键的数量
为8N ,B正确;C.根据均摊法,半导体化合物中Zn原子个数为 ,Sn原子个数为
A
,个数之比为1:1,C错误;D.根据晶胞结构,在四方晶胞中Sn位于S原子组成的四面体
空隙中,D正确;故选C。
7.(2023·广东汕头·金山中学校考三模)某补铁剂的主要成分为琥珀酸亚铁,邻二氮菲(phen)可与Fe2+反
应生成稳定的螯合物,用于测定Fe2+的含量,反应原理为 。邻二氮菲与琥珀酸
亚铁结构简式如图所示,下列说法正确的是
A.琥珀酸亚铁中碳原子均为sp3杂化B. 中,Fe2+的配位数为3
C. 中,存在离子键、配位键和共价键
D.phen与Fe2+形成配合物的反应受到溶液pH的影响
【答案】D
【解析】A.琥珀酸亚铁中饱和碳原子均为sp3杂化,而形成羰基的不饱和碳原子采用sp2杂化,A错误;
B.邻二氮菲分子中含有2个N原子,每个N原子可以形成配位键,在 中,Fe2+与3个邻二
氮菲结合,其中含有2个N原子与Fe2+形成配位键,故Fe2+的配位数为6,B错误;C.在阳离子
中存在配位键和共价键,但不存在离子键,C错误;D.pH<2时,H+浓度大,邻二氮菲中
的N原子优先与H+形成配位键,导致与Fe2+的配位能力减弱,pH>9时,OH-浓度大,与Fe2+反应生成
Fe(OH) ,影响Fe2+与邻二氮菲配位,故phen与Fe2+形成配合物的反应受到溶液pH的影响,D正确;故合
2
理选项是D。
8.(2023·浙江金华·浙江省丽水中学校联考一模)下列关于超分子和配合物的叙述不正确的是
A.[Cr(NH )(H O) Cl]2+中三价铬离子提供空轨道,N、O、Cl提供孤电子对与三价铬离子形成配位键,其
3 3 2 2
中心离子的配位数为6
B.配合物[TiCl(H O) ]Cl ·H O中存在离子键、共价键、配位键,若加入足量AgNO 溶液,所有Cl-均被完
2 5 2 2 3
全沉淀
C.超分子是两种或两种以上的分子通过分子间相互作用形成的分子聚集体,包括离子
D.人体细胞和细胞器的双分子膜体现了超分子的自组装的特征
【答案】B
【解析】A.[Cr(NH )(H O) Cl]2+中Cr3+具有空轨道,N、O、Cl具有孤电子对,能够形成配位键,其中心
3 3 2 2
离子的配位数为6,故A正确;B.加入足量AgNO 溶液,配合物[TiCl(H O) ]Cl ·H O中外界离子Cl-离子
3 2 5 2 2
与Ag+反应,内配位离子Cl-不与Ag+反应,故B错误;C.超分子是两种或两种以上的分子通过分子间相
互作用形成的分子聚集体,包括离子,故C正确;D.人体细胞和细胞器的双分子膜体现了超分子的自组
装的特征,故D正确;故选B。
9.(2023·安徽马鞍山·统考三模)化合物M是一种新型超分子晶体材料,由对溴苯胺(X)、18-冠-6和
HClO 在CHCOCH 中反应制得(如图)。下列叙述错误的是
4 3 3A.以上物质中部分元素的第一电离能:N>O>C
B.M由X的高氯酸盐与18-冠-6通过氢键结合生成
C.M中碳、氮、氯原子的杂化轨道类型均为sp3
D.M晶体中含有离子键、共价键、配位键
【答案】C
【解析】A.同周期元素,随着原子序数越大,第一电离能增大,但ⅤA的元素为半满的稳定结构,第一
电离能增大,第一电离能:N>O>C,A正确;B.由图知,M由X的高氯酸盐与18-冠-6通过氢键结合生
成,B正确;C.M中苯环上的碳原子的轨道杂化类型为sp2,C错误;D.M为离子化合物,其晶体类型
为离子晶体,M晶体中含有离子键、共价键、配位键,D正确;故选C。
10.(2023·福建福州·统考模拟预测)某种含二价铜微粒 的催化剂可用于汽车尾气脱硝,
催化机理如图所示,下列说法错误的是
A. 属于中间产物
B.状态②到状态③的过程中N元素被氧化
C.状态③到状态④的过程中有 键的形成
D.该脱硝过程的总反应方程式为
【答案】D
【解析】A.根据反应历程图, 在反应过程中生成,又参与其它反应过程,不是最终产
物,故A正确;B.状态②到状③的过程中, Cu 和 N 的化合价发生变化,其中 Cu 的化合价降低,属于还原反应,而N元素化合价升高,属于氧化反应,故B正确;C.状态③到状态④的变化过程中有HO
2
生成,即有O-H键的形成,故 C 正确;D.由图可知,反应由2NH 、2NO、 参与,生成2N、
3 2
3HO,则脱硝过程的总反应方程式为 ,故D错误;答案选D。
2