文档内容
专题 32 难溶电解质的溶解平衡
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 沉淀溶解平衡、影响因素及应用
考点二 溶度积常数及应用
考点一 沉淀溶解平衡、影响因素及应用
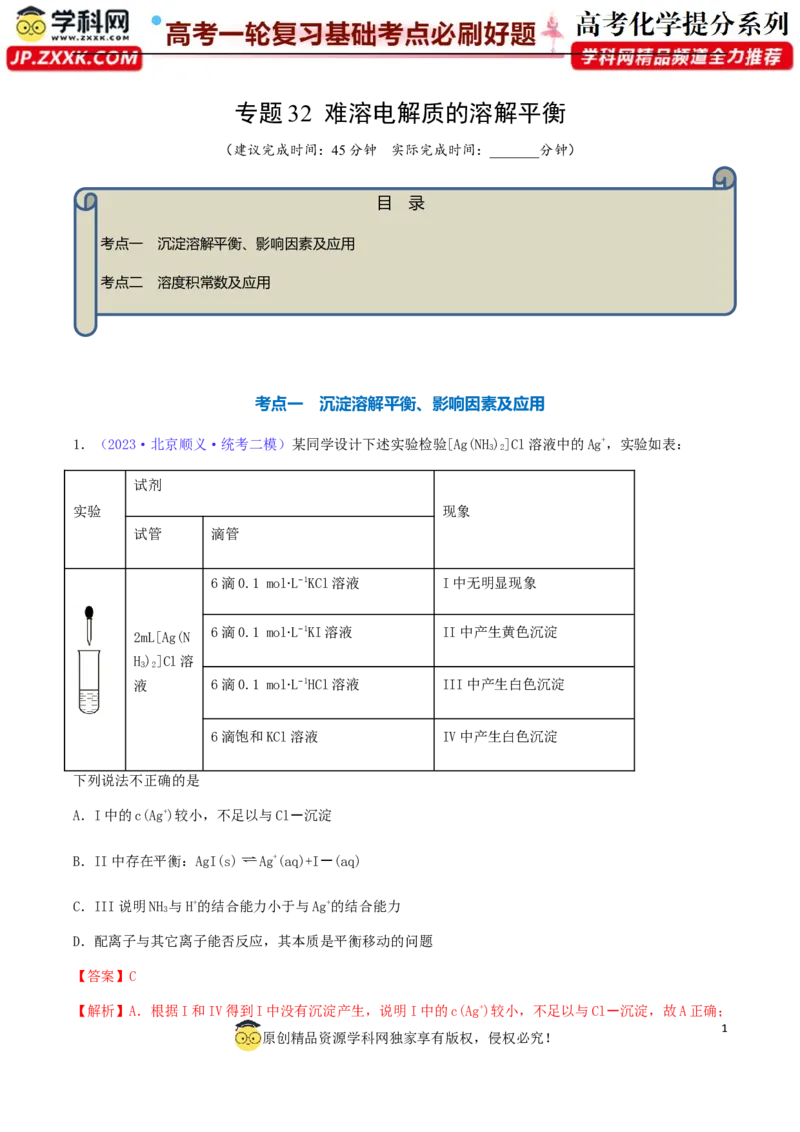
1.(2023·北京顺义·统考二模)某同学设计下述实验检验[Ag(NH)]Cl溶液中的Ag+,实验如表:
3 2
试剂
实验 现象
试管 滴管
6滴0.1 mol∙L−1KCl溶液 I中无明显现象
2mL[Ag(N
6滴0.1 mol∙L−1KI溶液 II中产生黄色沉淀
H)]Cl溶
3 2
液 6滴0.1 mol∙L−1HCl溶液 III中产生白色沉淀
6滴饱和KCl溶液 IV中产生白色沉淀
下列说法不正确的是
A.I中的c(Ag+)较小,不足以与Cl-沉淀
B.II中存在平衡:AgI(s) Ag+(aq)+I-(aq)
C.III说明NH 与H+的结合能力小于与Ag+的结合能力
3
D.配离子与其它离子能否反应,其本质是平衡移动的问题
【答案】C
【解析】A.根据I和IV得到I中没有沉淀产生,说明I中的c(Ag+)较小,不足以与Cl-沉淀,故A正确;
1
原创精品资源学科网独家享有版权,侵权必究!B.II中产生黄色沉淀即生成AgI沉淀,AgI沉淀存在溶解平衡即:AgI(s) Ag+(aq)+I-(aq),故B正确;
C.根据I和III的现象,产生的沉淀说明[Ag(NH)]Cl和氢离子反应,有大量银离子生成,银离子和氯离
3 2
子反应生成AgCl沉淀,说明III中NH 与H+的结合能力大于与Ag+的结合能力,故C错误;D.根据I和II
3
的现象,可以得出配离子与其它离子能否反应,其本质是平衡移动的问题,故D正确。答案为C。
2.(2023·青海海东·统考三模)将足量AgCl(s)溶解在水中,形成悬浊液。已知:AgCl(s) Ag+
(aq)+Cl-(aq) ΔH>0,下列叙述错误的是
A.加热悬浊液,使其温度升高,则K (AgCl)增大
sp
B.加少量水稀释,上述平衡正向移动,c(Ag+)不变
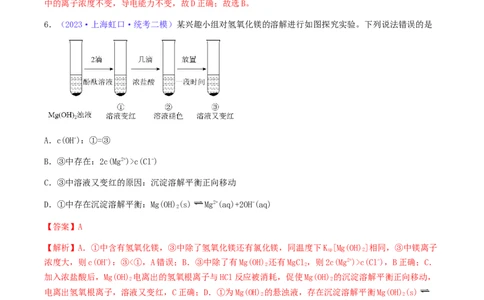
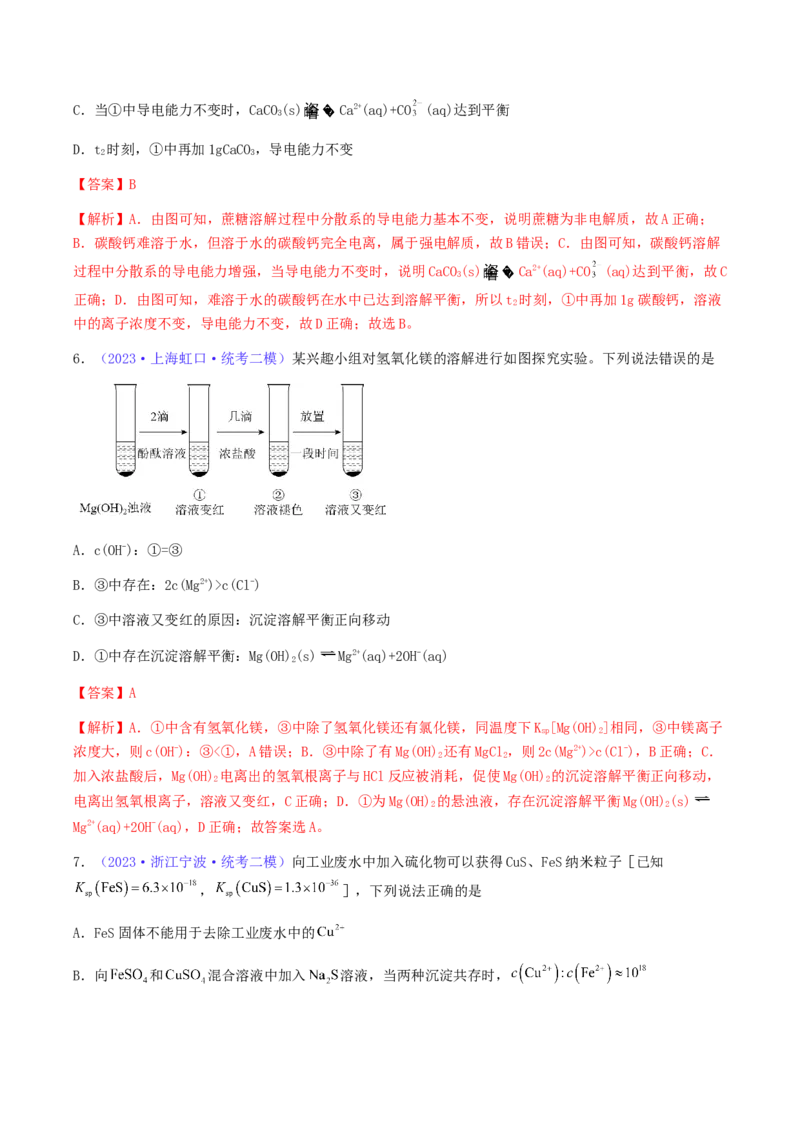
C.向悬浊液中通入少量氨气,Q(AgCl)c(Cl-)
C.③中溶液又变红的原因:沉淀溶解平衡正向移动
D.①中存在沉淀溶解平衡:Mg(OH)(s) Mg2+(aq)+2OH-(aq)
2
【答案】A
【解析】A.①中含有氢氧化镁,③中除了氢氧化镁还有氯化镁,同温度下K [Mg(OH)]相同,③中镁离子
sp 2
浓度大,则c(OH-):③<①,A错误;B.③中除了有Mg(OH) 还有MgCl,则2c(Mg2+)>c(Cl-),B正确;C.
2 2
加入浓盐酸后,Mg(OH) 电离出的氢氧根离子与HCl反应被消耗,促使Mg(OH) 的沉淀溶解平衡正向移动,
2 2
电离出氢氧根离子,溶液又变红,C正确;D.①为Mg(OH) 的悬浊液,存在沉淀溶解平衡Mg(OH)(s)
2 2
Mg2+(aq)+2OH-(aq),D正确;故答案选A。
7.(2023·浙江宁波·统考二模)向工业废水中加入硫化物可以获得CuS、FeS纳米粒子[已知
, ],下列说法正确的是
A.FeS固体不能用于去除工业废水中的
B.向 和 混合溶液中加入 溶液,当两种沉淀共存时,C.向CuS饱和溶液中加入 固体,CuS的溶解平衡逆向移动,滤液中一定存在
D.已知 溶液中 ,可判断CuS易溶于稀盐酸
【答案】C
【解析】A.根据 可知,FeS固体能用于去除工业废水中的 ,故A错误;B.向
和 混合溶液中加入 溶液,当两种沉淀共存时,
,故B错误;C.CuS存在溶解平衡
,向CuS饱和溶液中加入 固体,铜离子浓度增大,因此CuS的溶解平衡
逆向移动,根据溶度积常数得到滤液中一定存在 ,故C正确;D.若要溶解
,则 ,平衡常数很小,反应几乎
不能发生,可判断CuS难溶于稀盐酸,故D错误。综上所述,答案为C。
8.(2023·海南海口·统考模拟预测)已知:向难溶电解质饱和溶液中加入与该电解质没有相同离子的
强电解质时,使难溶物溶解度增大的效应称为盐效应。常温下,在含大量BaSO 固体的浊液中加入0.01mol
4
下列物质(忽略体积变化),溶液中c(Ba2+)由大到小的排序正确的是
①BaSO ②NaSO ③KNO
4 2 4 3
A.②①③ B.③②① C.③①② D.①③②
【答案】C
【解析】在含大量BaSO 固体的浊液中加入0.01mol①BaSO 时,对BaSO 的沉淀溶解平衡不产生任何影响,
4 4 4
c(Ba2+)不变;加入0.01mol②NaSO 时,增大了溶液中的c( ),使BaSO 的沉淀溶解平衡逆向移动,
2 4 4
c(Ba2+)减小;加入0.01mol③KNO 时,发生盐效应,使BaSO 的溶解度增大,从而使c(Ba2+)增大。综合以
3 4
上分析,溶液中c(Ba2+)由大到小的排序③①②,故选C。
9.(2023·浙江杭州·校联考模拟预测)牙齿表面有一薄层釉质保护着,釉质层主要成分是难溶的羟基
磷灰石,存在如下平衡: ,已知
的 。下列说法不正确的是
A.在牙膏中添加适量的磷酸盐,能起到保护牙齿的作用
B.正常口腔的pH接近中性,牙齿不易被腐蚀C.使用添加 的含氟牙膏,可实现 与 的转化,该反应的平衡常数约为
D.口腔中的食物残渣能产生有机酸,容易导致龋齿,使 增大
【答案】D
【解析】A.在牙膏中添加适量的磷酸盐,增大了磷酸根离子的浓度,使得反应
化学平衡逆向移动,有利于生成羟基磷灰石,能起
到保护牙齿的作用,A正确;B.正常口腔中的pH接近中性,氢氧根离子浓度不变,化学平衡不移动,牙
齿不易被腐蚀,B正确;C.根据题干可知,Ca(PO)F的K =2.8×10-61,反应Ca(PO)OH(s)
5 4 3 sp 5 4 3
Ca(PO)F(s)的平衡常数K=(6.8×10-37)÷(2.8×10-61)=2.4×1024,因此使用添加NaF的含氟牙膏,可实现
5 4 3
与 的转化,C正确;D.K 只受温度的影响,温度不变,K 不变,D错误;
sp sp
故答案选D。
10.(2023·校联考二模)不同温度(T 和T)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡
1 2
在水中溶解时吸收热量。下列说法正确的是( )
A.T>T
1 2
B.加入BaCl 固体,可使a点变成c点
2
C.c点时,在T、T 两个温度下均有固体析出
1 2
D.a点和b点的K 相等
sp
【答案】D
【解析】A、难溶电解质的溶度积受温度的影响,T 的溶度积大于T 的,说明T 的温度大于T,故错误;
2 1 2 1
B、加入BaCl 固体,Ba2+的浓度增大,而a和c中c(Ba2+)相等,故错误;C、T 是c(Ba2+)×c(SO2
2 1 4
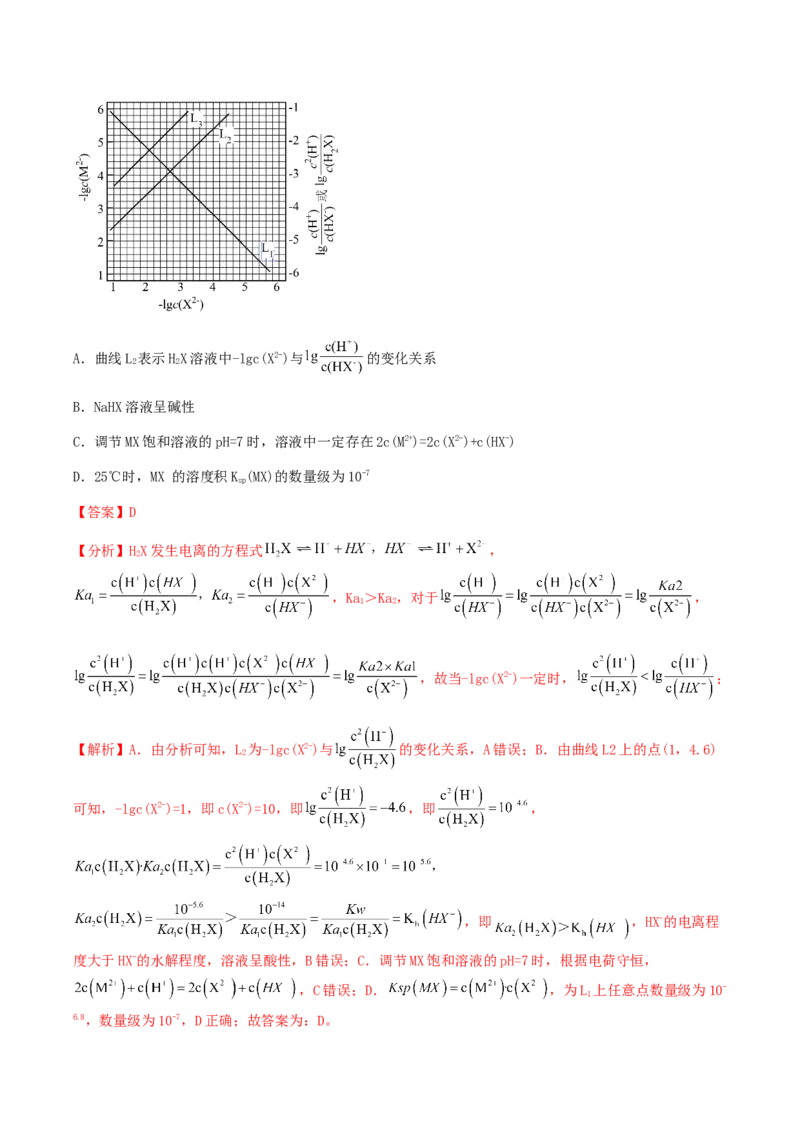
-)>K ,说明有沉淀析出,T 时,c(Ba2+)×c(SO2-)K (ZnCO),下列说法正确的是
sp 3 sp 3A.K (HCO)=10-6.4,K (ZnCO)=10-10.8
al 2 3 sp 3
B. ,平衡常数:
C.L 表示lgc(CO )-pH曲线
1
D.向a点溶液中加入ZnCl,可以达到b点溶液
2
【答案】A
【分析】分压固定的CO 气相中,使溶液中CO 浓度也相应固定,因此L 为HCO 的浓度,随着pH逐渐增大,
2 2 3 2 3
HCO 、CO 的浓度逐渐增大,且pH较小时HCO 的浓度大于CO 的浓度,所以L 表示HCO ,L 表示CO
1 2
;根据K (CaCO)>K (ZnCO)判断,L 为Ca2+的浓度,L 为Zn2+的浓度。
sp 3 sp 3 4 5
【解析】A.K (HCO)= ,pH=6.4时,HCO 和HCO 的浓度相等,此时K (HCO)=
al 2 3 2 3 al 2 3
=10-6.4,L 表示CO 、L 为Zn2+的浓度,两者交于lgc=-5.4,此时CO 、Zn2+的浓度均为10-5.4,
2 5
K (ZnCO)=c(Zn2+)·c(CO )=10-10.8,故A正确;B.通过b点数据可得K (CaCO)=c(Ca2+)·c(CO )=10-
sp 3 sp 3
3.2×10-5=10-8.2,选项中反应的平衡常数 ,故B错误;C.由上述分析可知L
1
表示HCO ,故C错误;D.向a点溶液中加入CaCl 可以达到b点溶液,故D错误;故选:A。
2
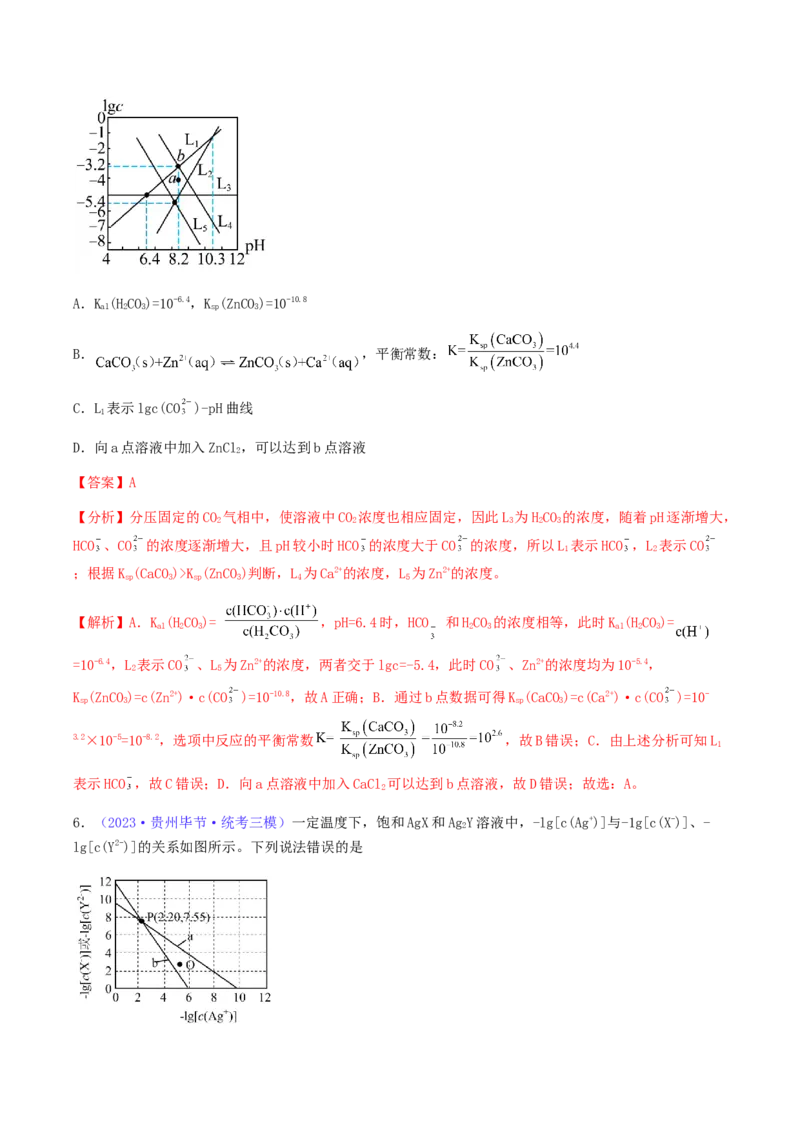
6.(2023·贵州毕节·统考三模)一定温度下,饱和AgX和AgY溶液中,-lg[c(Ag+)]与-1g[c(X-)]、-
2
lg[c(Y2-)]的关系如图所示。下列说法错误的是A.Ksp(AgY)=10-11.95
2
B.图中a代表AgX溶液
C.Q点溶液对应AgX生成沉淀,而AgY不产生沉淀
2
D.将AgNO 溶液加入NaX和NaY混合溶液中至产生两种沉淀,此时溶液中 =102.20
3 2
【答案】D
【分析】利用P点计算K [AgY]=c2(Ag+)c(Y2-)=10-7.55×(10-2.2)2=10-11.95。同理计算
sp 2
K [AgX]=c(Ag+)c(X-)=10-7.55×10-2.2=10-9.75。当X-和Y2-相同时为1mol/L时,AgY中的Ag+为10-5.95mol/L而
sp 2
AgX中Ag+为10-9.75mol/L,所以a为AgX,而b为AgY。
2
【解析】A.由上分析,A项正确;B.由上分析,a为AgX,B项正确;C.对于两条线的左下方均为其过饱
和溶液,Q点位于b的右上方为未饱和溶液无沉淀,而Q位于a的左下方为过饱和有沉淀,C项正确;D.
由于Ag+浓度未知,无法计算该值,D项错误;故选D。
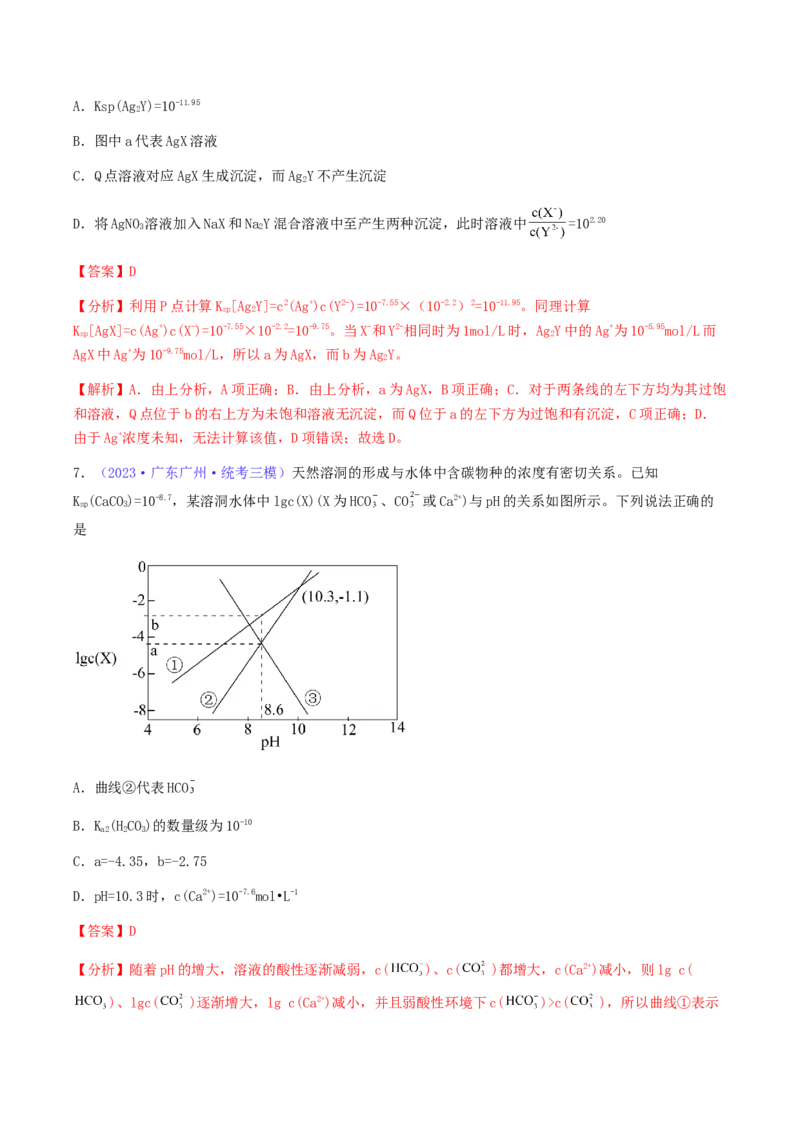
7.(2023·广东广州·统考三模)天然溶洞的形成与水体中含碳物种的浓度有密切关系。已知
K (CaCO)=10-8.7,某溶洞水体中lgc(X)(X为HCO 、CO 或Ca2+)与pH的关系如图所示。下列说法正确的
sp 3
是
A.曲线②代表HCO
B.K (HCO)的数量级为10-10
a2 2 3
C.a=-4.35,b=-2.75
D.pH=10.3时,c(Ca2+)=10-7.6mol•L-1
【答案】D
【分析】随着pH的增大,溶液的酸性逐渐减弱,c( )、c( )都增大,c(Ca2+)减小,则lg c(
)、lgc( )逐渐增大,lg c(Ca2+)减小,并且弱酸性环境下c( )>c( ),所以曲线①表示与pH的关系,曲线②表示与pH的关系,曲线③表示钙离子与的关系。(10.3,-1.1)点为c(
)=c( ),K = 。
a2
【解析】A.曲线①表示 与pH的关系,曲线②表示 与pH的关系,曲线③表示钙离子与的关系,
A错误;B.(10.3,-1.1)点为c( )=c( ),K = ,数量级为10-11,B错误;
a2
C.由上述分析可知,曲线②表示 与pH的关系,曲线③表示钙离子与的关系,两线交点时碳酸根离子
的浓度与钙离子浓度相等,c( )= ,即a=-4.35,K =10-10.3,则c(
a2
)= ,即b=-2.65,C错误;D.pH=10.3时,c( )=10-
1.1mol/L,根据溶度积常数计算c(Ca2+)= =10-7.6mol•L-1,D正确;故选D。
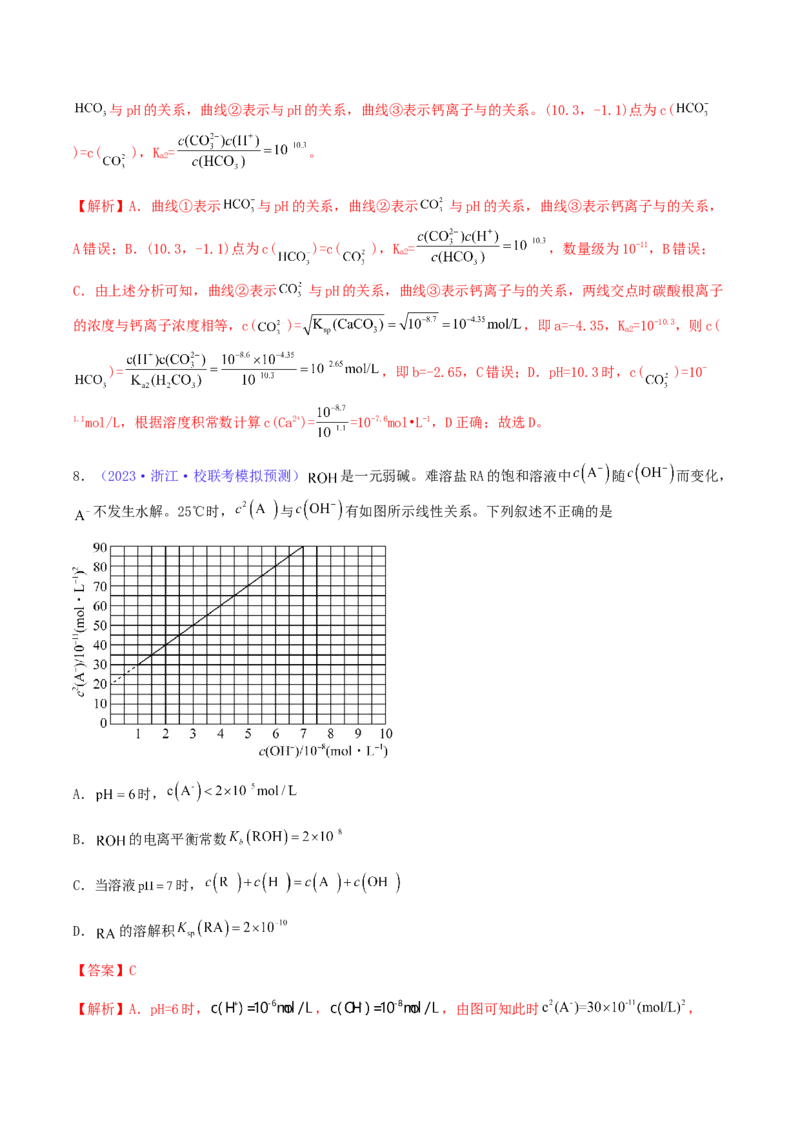
8.(2023·浙江·校联考模拟预测) 是一元弱碱。难溶盐RA的饱和溶液中 随 而变化,
不发生水解。25℃时, 与 有如图所示线性关系。下列叙述不正确的是
A. 时,
B. 的电离平衡常数
C.当溶液 时,
D. 的溶解积
【答案】C
【解析】A.pH=6时, , ,由图可知此时 ,,A正确;B.由图可知,当 =0时, ,
此时 ,则 ,选择曲线上 的点代入等
式可得, ,解得 ,B正确;C.难溶盐RA的饱
和溶液中因为阳离子的水解显酸性,所以当溶液显中性时,说明加入了碱,若加溶液 ,则
表示电荷守恒成立,若加其它碱则不成立,C错误;D.由图可知,当
=0时, ,此时 ,则 ,D
正确;故选C。
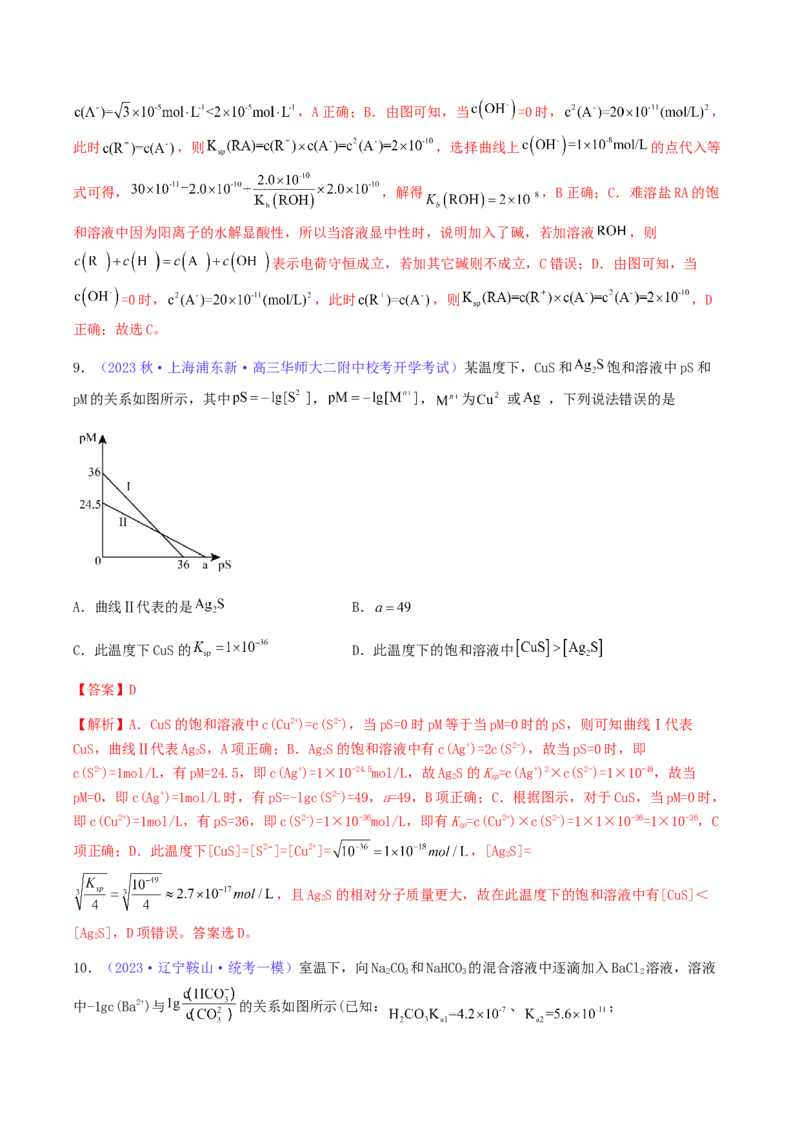
9.(2023秋·上海浦东新·高三华师大二附中校考开学考试)某温度下,CuS和 饱和溶液中pS和
pM的关系如图所示,其中 , , 为 或 ,下列说法错误的是
A.曲线Ⅱ代表的是 B.
C.此温度下CuS的 D.此温度下的饱和溶液中
【答案】D
【解析】A.CuS的饱和溶液中c(Cu2+)=c(S2-),当pS=0时pM等于当pM=0时的pS,则可知曲线Ⅰ代表
CuS,曲线Ⅱ代表AgS,A项正确;B.AgS的饱和溶液中有c(Ag+)=2c(S2-),故当pS=0时,即
2 2
c(S2-)=1mol/L,有pM=24.5,即c(Ag+)=1×10-24.5mol/L,故AgS的K=c(Ag+)2×c(S2-)=1×10-49,故当
2 sp
pM=0,即c(Ag+)=1mol/L时,有pS=-lgc(S2-)=49,a=49,B项正确;C.根据图示,对于CuS,当pM=0时,
即c(Cu2+)=1mol/L,有pS=36,即c(S2-)=1×10-36mol/L,即有K=c(Cu2+)×c(S2-)=1×1×10-36=1×10-36,C
sp
项正确;D.此温度下[CuS]=[S2−]=[Cu2+]= ,[AgS]=
2
,且AgS的相对分子质量更大,故在此温度下的饱和溶液中有[CuS]<
2
[AgS],D项错误。答案选D。
2
10.(2023·辽宁鞍山·统考一模)室温下,向NaCO 和NaHCO 的混合溶液中逐滴加入BaCl 溶液,溶液
2 3 3 2
中-1gc(Ba2+)与 的关系如图所示(已知: 、 ;)。下列说法正确的是
A.a对应溶液pH=6.5
B.b对应溶液的c(HCO )=0.05mol/L
C.a→b的过程中,溶液中 一直增大
D.a对应的溶液中一定存在:
【答案】B
【解析】A.a点对应溶液 ,则 ,由 得,
, ,故A错误;B.b对应溶液 ,则
,由 ,可得 ,由b点
,则 ,故B正确;C.
,a→b的过程中, 逐渐增大, 逐
渐减小, 不变,则 逐渐减小,故C错误;D.a点对应溶液中, ,则
,由A可知溶液pH约为10.25,溶液中 ,溶液中存在电荷守恒关系式
,则 ,故D错
误;答案选B。