文档内容
专题七 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39 Ca 40
Mn 55 Fe 56 Cu 64
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.从下列实验事实所引出的相应结论正确的是( )
选项 实验事实 结论
其他条件相同,NaSO 溶液浓度越大,析 当其他条件不变时,增大反应物浓度,化
2 2 3
A
出S沉淀所需时间越短 学反应速率加快
在化学反应前后,催化剂的质量和化学性
B 催化剂一定不参与化学反应
质都没有发生改变
物质的量浓度相同的盐酸和醋酸分别与等
C 反应开始时速率相同
质量的、形状相同的锌粒反应
在容积可变的密闭容器中发生反应H(g)+
2
D 正反应速率加快,逆反应速率不变
I(g)2HI(g),把容积缩小一倍
2
2.在一定温度下,氧化铁可以与一氧化碳在恒容密闭容器中发生下列反应:FeO(s)+3CO(g)2Fe(s)+
2 3
3CO(g),不可用上述反应中某种物理量来说明该反应已达到平衡状态的是( )
2
A.CO的生成速率与CO 的生成速率相等
2
B.气体密度不再变化
C.CO的质量不变
D.体系的压强不再发生变化
3.2021年中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二
氧化碳转化为甲烷的新型催化转化方法:CO+4H===CH+2HO,这是迄今最接近人造光合作用的方法,CO
2 2 4 2 2
加氢制CH 的一种催化机理如图。下列说法正确的是( )
4
A.反应中LaO 是中间产物
2 3
B.CO 转化为CH 利用了CO 的氧化性
2 4 2
C.H 经过Ni活性中心裂解产生带负电荷的H
2
D.使用催化剂可以降低反应的焓变,从而提高化学反应速率4.苯乙烯与溴苯在一定条件下发生Heck反应:
溴苯用量/mmol 100 100 100 100 100 100 100
催化剂用量/mmol 2 2 2 2 2 2 2
反应温度/℃ 100 100 100 100 120 140 160
反应时间/h 10 12 14 16 14 14 14
产率/% 81.2 84.4 86.6 86.2 93.5 96.6 89.0
根据上表数据,下列说法正确的是( )
A.最佳反应温度为100 ℃
B.最佳反应时间为16 h
C.温度过高时催化剂活性可能降低
D.反应产物是顺式结构
5.某小组探究实验条件对反应速率的影响,设计如下实验,并记录结果如下:
编号 ① ② ③ ④
温度/℃ 20 20 50 80
10 mL HSO 溶液浓度/(mol·L-1) 0.10 0.10 0.10 0.10
2 4
5 mL KI溶液浓度/(mol·L-1) 0.40 0.80 0.40 0.40
1%淀粉溶液体积/mL 1 1 1 1
出现蓝色时间/s 40 21 5 未见蓝色
下列说法正确的是( )
A.由实验①②可知,反应速率v与c(I-)成正比
B.实验①~④中,应将HSO 溶液与淀粉溶液先混合
2 4
C.在I-被O 氧化过程中,H+只是降低活化能
2
D.由实验③④可知,温度越高,反应速率越慢
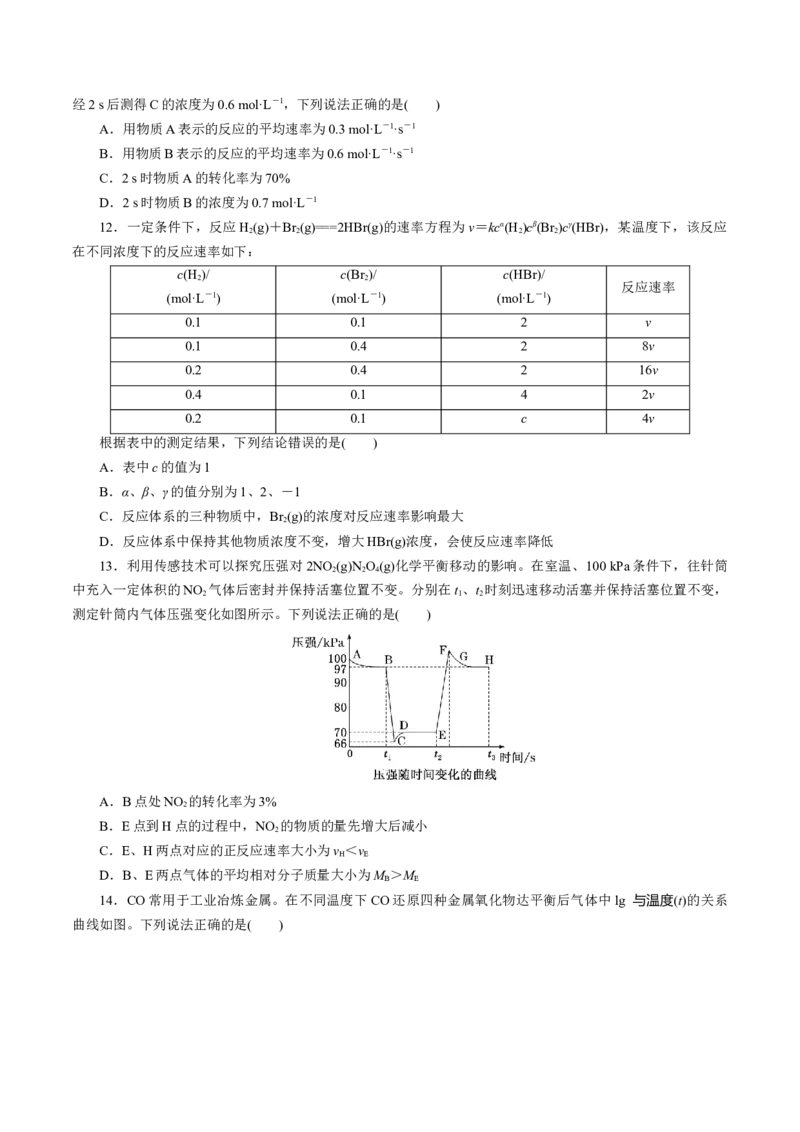
6.如图所示,三个烧瓶中分别充满NO 气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中加
2
入CaO,在(2)中不加其他任何物质,在(3)中加入NHCl晶体,发现(1)中红棕色变深,(3)中红棕色变浅。[已知
4
反应2NO(红棕色)NO(无色)]
2 2 4
下列叙述正确的是( )
A.2NONO 是放热反应
2 2 4
B.NHCl溶于水时放出热量
4
C.烧瓶(1)中平衡混合气体的相对分子质量增大
D.烧瓶(3)中气体的压强增大7.处于平衡状态的反应:2HS(g)2H(g)+S(g) ΔH>0,不改变其他条件的情况下合理的说法是( )
2 2 2
A.加入催化剂,反应途径将发生改变,ΔH也将随之改变
B.升高温度,正、逆反应速率都增大,HS分解率也增大
2
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注入一些H 后达新平衡,H 浓度将减小
2 2
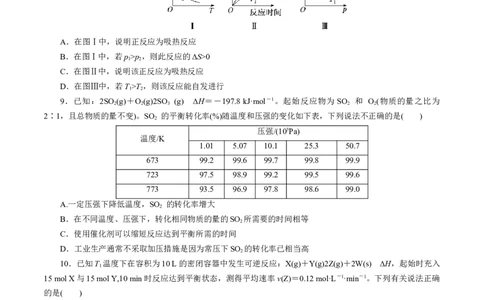
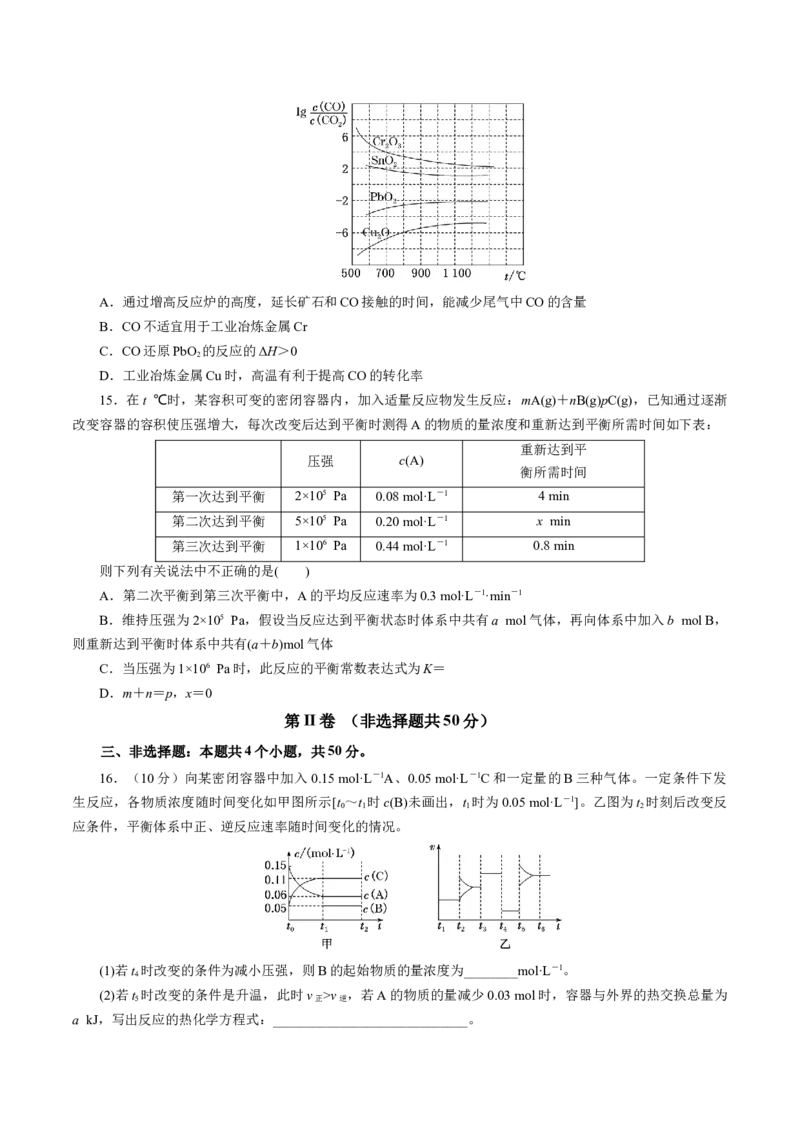
8.在其他条件不变时,只改变某一条件,化学反应aA(g)+B(g)cC(g)的平衡变化图像如下(图中p表示压强,
T表示温度,n表示物质的量,α表示平衡转化率),据此分析下列说法正确的是( )
A.在图Ⅰ中,说明正反应为吸热反应
B.在图Ⅰ中,若p>p,则此反应的ΔS>0
1 2
C.在图Ⅱ中,说明该正反应为吸热反应
D.在图Ⅲ中,若T>T,则该反应能自发进行
1 2
9.已知:2SO(g)+O(g)2SO (g) ΔH=-197.8 kJ·mol-1。起始反应物为SO 和 O(物质的量之比为
2 2 3 2 2
2∶1,且总物质的量不变)。SO 的平衡转化率(%)随温度和压强的变化如下表,下列说法不正确的是( )
2
压强/(105Pa)
温度/K
1.01 5.07 10.1 25.3 50.7
673 99.2 99.6 99.7 99.8 99.9
723 97.5 98.9 99.2 99.5 99.6
773 93.5 96.9 97.8 98.6 99.0
A.一定压强下降低温度,SO 的转化率增大
2
B.在不同温度、压强下,转化相同物质的量的SO 所需要的时间相等
2
C.使用催化剂可以缩短反应达到平衡所需的时间
D.工业生产通常不采取加压措施是因为常压下SO 的转化率已相当高
2
10.已知T 温度下在容积为10 L的密闭容器中发生可逆反应:X(g)+Y(g)2Z(g)+2W(s) ΔH,起始时充入
1
15 mol X与15 mol Y,10 min时反应达到平衡状态,测得平均速率v(Z)=0.12 mol·L-1·min-1。下列有关说法正确
的是( )
A.T 温度下该反应的平衡常数为2.56
1
B.平衡时再充入一定量的X,平衡正向移动,X的转化率增大
C.若T>T,T 时K=1.52,则该反应的ΔH>0
2 1 2
D.若其他条件不变,T 温度下,K=1.96,则Y的平衡转化率约为41.3%
3
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.将4 mol A气体和2 mol B气体在2 L的容器中混合,并在一定条件下发生反应:2A(g)+B(g)2C(g),若经2 s后测得C的浓度为0.6 mol·L-1,下列说法正确的是( )
A.用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
B.用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
C.2 s时物质A的转化率为70%
D.2 s时物质B的浓度为0.7 mol·L-1
12.一定条件下,反应H(g)+Br(g)===2HBr(g)的速率方程为v=kcα(H)cβ(Br)cγ(HBr),某温度下,该反应
2 2 2 2
在不同浓度下的反应速率如下:
c(H)/ c(Br)/ c(HBr)/
2 2
反应速率
(mol·L-1) (mol·L-1) (mol·L-1)
0.1 0.1 2 v
0.1 0.4 2 8v
0.2 0.4 2 16v
0.4 0.1 4 2v
0.2 0.1 c 4v
根据表中的测定结果,下列结论错误的是( )
A.表中c的值为1
B.α、β、γ的值分别为1、2、-1
C.反应体系的三种物质中,Br(g)的浓度对反应速率影响最大
2
D.反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低
13.利用传感技术可以探究压强对2NO(g)NO(g)化学平衡移动的影响。在室温、100 kPa条件下,往针筒
2 2 4
中充入一定体积的NO 气体后密封并保持活塞位置不变。分别在t、t 时刻迅速移动活塞并保持活塞位置不变,
2 1 2
测定针筒内气体压强变化如图所示。下列说法正确的是( )
A.B点处NO 的转化率为3%
2
B.E点到H点的过程中,NO 的物质的量先增大后减小
2
C.E、H两点对应的正反应速率大小为v <v
H E
D.B、E两点气体的平均相对分子质量大小为M >M
B E
14.CO常用于工业冶炼金属。在不同温度下CO还原四种金属氧化物达平衡后气体中lg 与温度(t)的关系
曲线如图。下列说法正确的是( )A.通过增高反应炉的高度,延长矿石和CO接触的时间,能减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属Cr
C.CO还原PbO 的反应的ΔH>0
2
D.工业冶炼金属Cu时,高温有利于提高CO的转化率
15.在t ℃时,某容积可变的密闭容器内,加入适量反应物发生反应:mA(g)+nB(g)pC(g),已知通过逐渐
改变容器的容积使压强增大,每次改变后达到平衡时测得A的物质的量浓度和重新达到平衡所需时间如下表:
重新达到平
压强 c(A)
衡所需时间
第一次达到平衡 2×105 Pa 0.08 mol·L-1 4 min
第二次达到平衡 5×105 Pa 0.20 mol·L-1 x min
第三次达到平衡 1×106 Pa 0.44 mol·L-1 0.8 min
则下列有关说法中不正确的是( )
A.第二次平衡到第三次平衡中,A的平均反应速率为0.3 mol·L-1·min-1
B.维持压强为2×105 Pa,假设当反应达到平衡状态时体系中共有a mol气体,再向体系中加入b mol B,
则重新达到平衡时体系中共有(a+b)mol气体
C.当压强为1×106 Pa时,此反应的平衡常数表达式为K=
D.m+n=p,x=0
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)向某密闭容器中加入0.15 mol·L-1A、0.05 mol·L-1C和一定量的B三种气体。一定条件下发
生反应,各物质浓度随时间变化如甲图所示[t ~t 时c(B)未画出,t 时为0.05 mol·L-1]。乙图为t 时刻后改变反
0 1 1 2
应条件,平衡体系中正、逆反应速率随时间变化的情况。
(1)若t 时改变的条件为减小压强,则B的起始物质的量浓度为________mol·L-1。
4
(2)若t 时改变的条件是升温,此时v >v ,若A的物质的量减少0.03 mol时,容器与外界的热交换总量为
5 正 逆
a kJ,写出反应的热化学方程式:_____________________________。(3)t 时改变的某一反应条件可能是________(填字母)。
3
a.使用催化剂 b.增大压强 c.增大反应物浓度
(4)在恒温恒压下通入惰性气体,v ____________v (填“>”“=”或“<”)。
正 逆
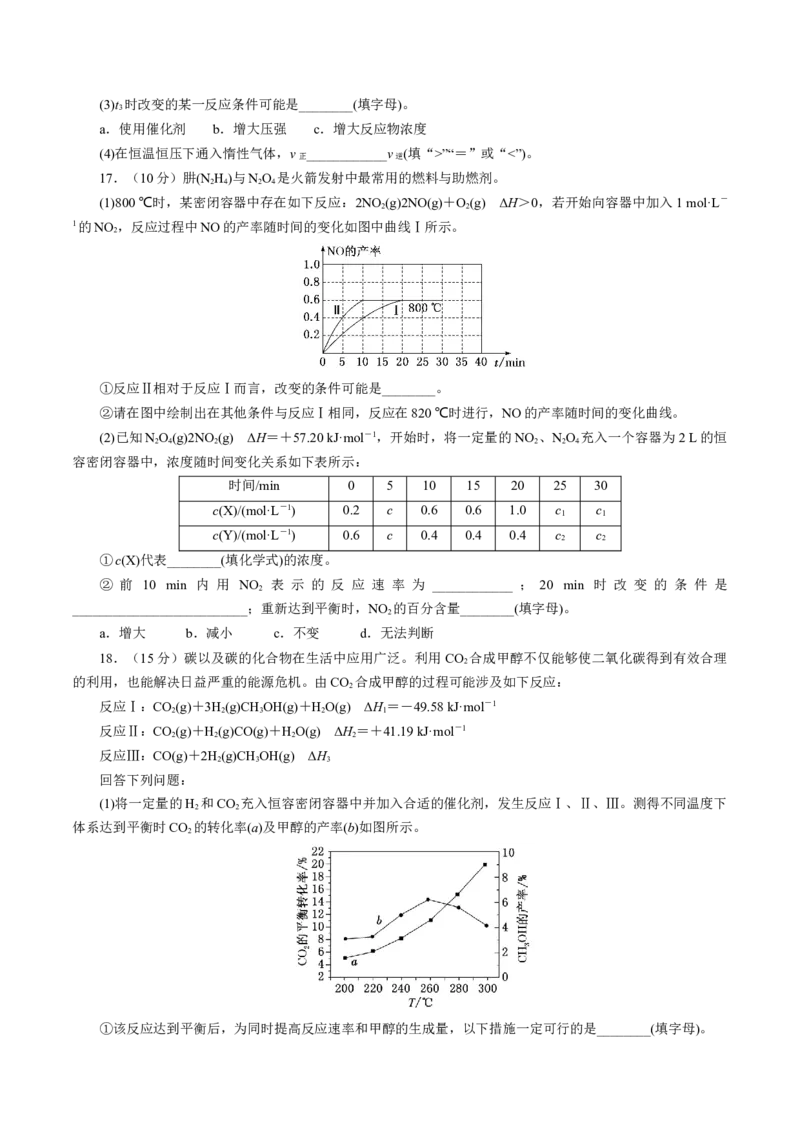
17.(10分)肼(NH)与NO 是火箭发射中最常用的燃料与助燃剂。
2 4 2 4
(1)800 ℃时,某密闭容器中存在如下反应:2NO(g)2NO(g)+O(g) ΔH>0,若开始向容器中加入1 mol·L-
2 2
1的NO,反应过程中NO的产率随时间的变化如图中曲线Ⅰ所示。
2
①反应Ⅱ相对于反应Ⅰ而言,改变的条件可能是________。
②请在图中绘制出在其他条件与反应Ⅰ相同,反应在820 ℃时进行,NO的产率随时间的变化曲线。
(2)已知NO(g)2NO(g) ΔH=+57.20 kJ·mol-1,开始时,将一定量的NO、NO 充入一个容器为2 L的恒
2 4 2 2 2 4
容密闭容器中,浓度随时间变化关系如下表所示:
时间/min 0 5 10 15 20 25 30
c(X)/(mol·L-1) 0.2 c 0.6 0.6 1.0 c c
1 1
c(Y)/(mol·L-1) 0.6 c 0.4 0.4 0.4 c c
2 2
①c(X)代表________(填化学式)的浓度。
② 前 10 min 内 用 NO 表 示 的 反 应 速 率 为 ____________ ; 20 min 时 改 变 的 条 件 是
2
__________________________;重新达到平衡时,NO 的百分含量________(填字母)。
2
a.增大 b.减小 c.不变 d.无法判断
18.(15分)碳以及碳的化合物在生活中应用广泛。利用CO 合成甲醇不仅能够使二氧化碳得到有效合理
2
的利用,也能解决日益严重的能源危机。由CO 合成甲醇的过程可能涉及如下反应:
2
反应Ⅰ:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-49.58 kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.19 kJ·mol-1
2 2 2 2
反应Ⅲ:CO(g)+2H(g)CHOH(g) ΔH
2 3 3
回答下列问题:
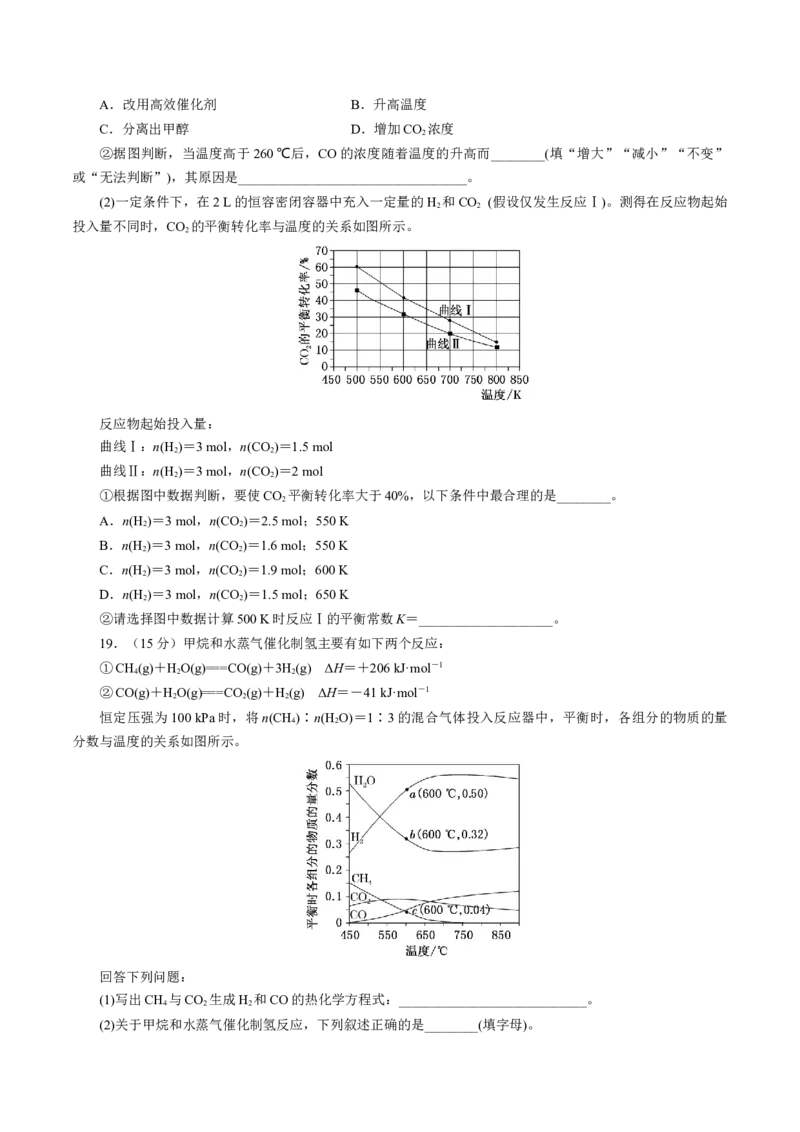
(1)将一定量的H 和CO 充入恒容密闭容器中并加入合适的催化剂,发生反应Ⅰ、Ⅱ、Ⅲ。测得不同温度下
2 2
体系达到平衡时CO 的转化率(a)及甲醇的产率(b)如图所示。
2
①该反应达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是________(填字母)。A.改用高效催化剂 B.升高温度
C.分离出甲醇 D.增加CO 浓度
2
②据图判断,当温度高于260 ℃后,CO的浓度随着温度的升高而________(填“增大”“减小”“不变”
或“无法判断”),其原因是__________________________________。
(2)一定条件下,在2 L的恒容密闭容器中充入一定量的H 和CO (假设仅发生反应Ⅰ)。测得在反应物起始
2 2
投入量不同时,CO 的平衡转化率与温度的关系如图所示。
2
反应物起始投入量:
曲线Ⅰ:n(H)=3 mol,n(CO)=1.5 mol
2 2
曲线Ⅱ:n(H)=3 mol,n(CO)=2 mol
2 2
①根据图中数据判断,要使CO 平衡转化率大于40%,以下条件中最合理的是________。
2
A.n(H)=3 mol,n(CO)=2.5 mol;550 K
2 2
B.n(H)=3 mol,n(CO)=1.6 mol;550 K
2 2
C.n(H)=3 mol,n(CO)=1.9 mol;600 K
2 2
D.n(H)=3 mol,n(CO)=1.5 mol;650 K
2 2
②请选择图中数据计算500 K时反应Ⅰ的平衡常数K=____________________。
19.(15分)甲烷和水蒸气催化制氢主要有如下两个反应:
①CH(g)+HO(g)===CO(g)+3H(g) ΔH=+206 kJ·mol-1
4 2 2
②CO(g)+HO(g)===CO(g)+H(g) ΔH=-41 kJ·mol-1
2 2 2
恒定压强为100 kPa时,将n(CH)∶n(HO)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量
4 2
分数与温度的关系如图所示。
回答下列问题:
(1)写出CH 与CO 生成H 和CO的热化学方程式:____________________________。
4 2 2
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是________(填字母)。A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现单位时间转化率不变
(3)系统中H 的含量在700 ℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
2
①低于700 ℃,____________________________________________________________;
②高于700 ℃,____________________________________________________________。
(4)已知投料比为n(CH)∶n(HO)=1∶3的混合气体,p=100 kPa。600 ℃时,CH 的平衡转化率为_____,
4 2 4
反应①的平衡常数的计算式为K=________(K 是以分压表示的平衡常数,分压=总压×物质的量分数)。
p p