文档内容
元素“位—构—性”关系的分析应用
1.“位—构—性”关系模型
2.原子结构与元素的性质
(1)物质的结构决定物质的性质,物质的性质反映物质的结构。原子越容易失去电子,元素的金属性就
越强;原子越容易得电子,元素的非金属性就越强。元素性质的比较如表所示:
同周期 同主族
性质
(自左而右) (自上而下)
电子层
层数相同 层数增大
结构
失电子
逐渐减弱 逐渐增强
能力
得电子
逐渐增强 逐渐减弱
能力
金属性 逐渐减弱 逐渐增强
非金属性 逐渐增强 逐渐减弱
主要
最高正价升高(O、F除外) 最高正价相同(O、F除外)
化合价
最高价氧 酸性增强:
酸性减弱:HNO >H PO
3 3 4
化物对应 H SiO Mg(OH) >Al(OH)
2 3非金属简
单氢化物 增强:SiH HCl>HBr>HI
4 3 2
的稳定性
原子
减小:Si>P>S>Cl 增大:FMg2+>Al3+ 增大:Li+S2->Cl- 增大:F-Y>W
B.简单氢化物键角:X>Y
C.反应过程中有蓝色沉淀产生
D.QZX Y W 是配合物,配位原子是Y
4 4 12
答案 D
解析 Q是ds区元素,焰色试验呈绿色,则Q为Cu元素;基态X原子的核外电子有5种空间运动状态,
则X可能为N(1s22s22p3)、O(1s22s22p4)、F(1s22s22p5);X、Y、Z原子序数依次增大,基态Y、Z原子有两个
未成对电子,若Y、Z为第2周期元素,可能为C(1s22s22p2)或O(1s22s22p4),C原子序数小于N,所以Y不
可能为C,若Y、Z为第3周期元素,可能为Si(1s22s22p63s23p2)或S(1s22s22p63s23p4),Y、Z可与Cu形成
CuZY ,所以Y、Z分别为O、S元素,则X只能为N元素;W原子序数小于N且能与X形成XW ,所以
4 3
W为H元素。S单质常温下呈固态,O 和H 均为分子晶体,O 的相对分子质量大于H ,所以沸点:
2 2 2 2
S>O >H ,故A正确;Y、X的简单氢化物分别为H O和NH ,H O的键角约为105°,NH 的键角为
2 2 2 3 2 3
107°,所以键角:X>Y,故B正确;硫酸铜溶液中滴加氨水,氨水不足时生成蓝色沉淀氢氧化铜,氨水过量时氢氧化铜溶解,生成[Cu(NH ) ]SO ,即反应过程中有蓝色沉淀产生,故C正确;[Cu(NH ) ]SO 中铜离
3 4 4 3 4 4
子提供空轨道、NH 的N原子提供孤电子对,两者形成配位键,配位原子为N,故D错误。
3
3.(2024·湖北,9)主族元素W、X、Y、Z原子序数依次增大,X、Y的价电子数相等,Z的价电子所在
能层有16个轨道,4种元素形成的化合物如图。下列说法正确的是( )
A.电负性:W>Y
B.酸性:W YX >W YX
2 3 2 4
C.基态原子的未成对电子数:W>X
D.氧化物溶于水所得溶液的pH:Z>Y
答案 D
解析 主族元素W、X、Y、Z原子序数依次增大,Z的价电子所在能层有16个轨道,则Z有4个能层,
且形成+1价离子,应为K;在此结构中W形成一个化学键,应为H;X、Y的价电子数相等,且X形成两
个化学键、Y形成六个化学键,可推知X、Y分别为O、S。W和Y可以形成H S,其中S显-2价,电负性:
2
S>H,A错误;H SO 是中强酸,而H SO 是强酸,在相同条件下后者的酸性较强,B错误;H只有1个电
2 3 2 4
子,O的2p轨道上有4个电子,有2个未成对电子,基态原子的未成对电子数:O>H,C错误;K的氧化
物溶于水且与水反应生成强碱KOH,S的氧化物溶于水且与水反应生成H SO 或H SO ,氧化物溶于水所
2 3 2 4
得溶液的pH的大小关系为K>S,D正确。
4.(2023·湖北,6)W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相邻,W的核
外电子数与X的价层电子数相等,Z 是氧化性最强的单质,4种元素可形成离子化合物(XY)+(WZ )-。
2 4
下列说法正确的是( )
A.分子的极性:WZ Y>Z>WB.原子半径:XX>Z>W,A错误;同一周期元素原子
半径从左到右依次减小,同一主族元素原子半径从上到下依次增大,故四种元素的原子半径大小为
YY>X
C.Q的氧化物是两性氧化物
D.该阴离子中含有配位键
答案 A
解析 由题干分析知,W为H,X为C,Y为O,Z为F,Q为Al。
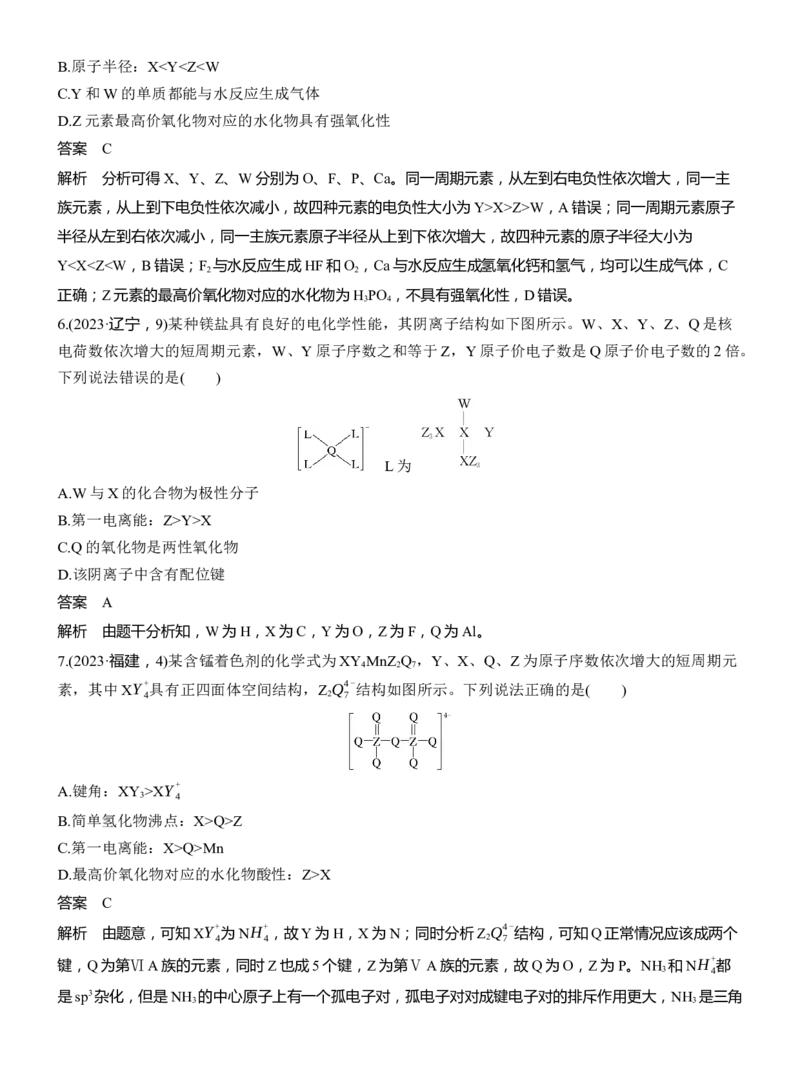
7.(2023·福建,4)某含锰着色剂的化学式为XY MnZ Q ,Y、X、Q、Z为原子序数依次增大的短周期元
4 2 7
素,其中XY+ 具有正四面体空间结构,Z Q4-结构如图所示。下列说法正确的是( )
4 2 7
A.键角:XY
>XY+
3 4
B.简单氢化物沸点:X>Q>Z
C.第一电离能:X>Q>Mn
D.最高价氧化物对应的水化物酸性:Z>X
答案 C
解析
由题意,可知XY+ 为NH+
,故Y为H,X为N;同时分析Z
Q4-
结构,可知Q正常情况应该成两个
4 4 2 7
键,Q为第ⅥA族的元素,同时Z也成5个键,Z为第ⅤA族的元素,故Q为O,Z为P。NH
和NH+
都
3 4
是sp3杂化,但是NH 的中心原子上有一个孤电子对,孤电子对对成键电子对的排斥作用更大,NH 是三角
3 3锥形结构,而NH+
是正四面体结构,故键角:NH
NH >PH ,即Q>X>Z,B错误;同主族元素从上到下第一电离能逐渐减小,同周期元素从左到右
2 3 3
第一电离能有增大的趋势,但第ⅡA、ⅤA族元素异常,故第一电离能:N>O>Mn,C正确;Z的最高价
氧化物对应的水化物为H PO ,X最高价氧化物对应的水化物为HNO ,前者为中强酸而后者为强酸,D错
3 4 3
误。
题型突破练 [分值:50 分]
(选择题1~10题,每小题3分,11~15题,每小题4分,共50分)
1.(2024·江西省部分高中学校高三下学期联考)X、Y、Z、W、Q是原子序数依次增大的前四周期元素且只
有Q为金属元素,基态X原子核外电子占据3个能级且每个能级上的电子数相等,Z是地壳中含量(质量分
数)最高的元素,基态W原子p轨道上的电子数比s轨道上的电子数多4,Q的原子序数为X、Y、W原子
序数的总和。下列说法正确的是( )
A.Q位于元素周期表的ds区
B.第一电离能:XZW
B.含W、R元素的化合物常用作生产农药
C.碱性溶液中:WY2-、XY-
、RY-能大量共存
3 3
·· ·· ··
D.共价化合物RXY的电子式为 ·R·X··Y
· · ··
·· ··
答案 C
解析 由题意可知,X、Y、Z、W、R分别为N、O、Mg、S、Cl。离子键的百分数是依据电负性的差值计
算的,电负性差值越大,离子键的百分数越大,O的电负性大于S,所以MgO离子键的百分数大于MgS,故A正确;碱性溶液中ClO-同样具有强氧化性,能将SO2- 氧化为SO2-
,不能大量共存,故C错误;共价
3 4
·· ·· ··
化合物RXY为ClNO,其电子式为
·Cl·N··O,D正确。
· · ··
·· ··
3.(2024·河北衡水部分高中高三下学期一模)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X与
Y相邻,X基态原子核外有2个未成对电子;Z是元素周期表中电负性最大的元素。W原子在同周期中原
子半径最大。下列说法不正确的是( )
A.第一电离能:I (Y)>I (Z)>I (X)
1 1 1
B.最高价氧化物对应水化物的酸性:Y>X
C.Z、W的简单离子的半径:r(Z)>r(W)
D.简单氢化物的热稳定性:Z>Y
答案 A
解析 由题意可知Z为F元素,W为Na元素,X为C元素,Y为N元素。同周期元素从左到右第一电离
能呈增大趋势,所以第一电离能:F>N>C,即I (Z)>I (Y)>I (X),A项错误;N元素的最高价氧化物对应的
1 1 1
水化物为硝酸,C元素的最高价氧化物对应的水化物为碳酸,硝酸酸性强于碳酸,B项正确;氟离子和钠
离子的核外电子排布相同,核电荷数大的离子半径小,氟离子的半径大于钠离子,C项正确;元素非金属
性越强,简单氢化物的热稳定性越强,所以简单氢化物的热稳定性:F>N,D项正确。
4.(2024·湖南衡阳高三下学期第二次联考)扬州大学俞磊教授团队利用萤石直接制备电池电解质材料甲
(XZY )的新方法如下:2ZM +5QY ===2ZY +5QM 、ZY +XY===XZY ,其中X、Y、Z、M、Q为原子序
6 5 2 5 2 5 6
数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基
态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是( )
A.基态X原子核外只有1个未成对电子
B.第一电离能:QM>Y
D.ZM 、ZY 均为三角锥形分子
3 3
答案 C
解析 由题意可知,Y是F元素,Z是P元素,M是Cl元素,X是Li元素,Q是Ca元素。基态Li原子核
外电子排布式为1s22s1,只有1个未成对电子,故A正确;同周期元素从左到右第一电离能呈增大趋势,
同主族元素从上到下第一电离能依次减小,第一电离能:CaCa2+>F-,故C错误;PCl 、PF 中P原子价层电
3 3
子对数均为4,均有1个孤电子对,空间结构均为三角锥形,故D正确。
5.W、X、Y、Z是电负性依次增大的前四周期主族元素。W为前四周期电负性最小的元素,X为地壳中含
量第二的元素,Y的基态原子中单电子和成对电子个数比为3∶4,Z的一种单质是极性分子且常用于消毒
杀菌。下列说法正确的是( )
A.第一电离能:YZC.1 mol XZ 晶体中有2 mol X—Z
2
D.元素X、Y、Z的最高正化合价依次升高
答案 B
解析 由题意可知,W为K元素,X为Si元素,Y为N元素,Z为O元素。Y为N元素,其2p能级处于
半充满的较稳定状态,第一电离能大于同周期相邻元素,即第一电离能:N>O,A错误;KH常温下为固
体,H O、H O 常温下为液体,氢化物的沸点:KH>H O(或H O ),B正确;1 mol SiO 中含4 mol Si—O,
2 2 2 2 2 2 2
C错误;Si元素最高正价为+4价,N元素最高正价为+5价,O元素无最高正价,D错误。
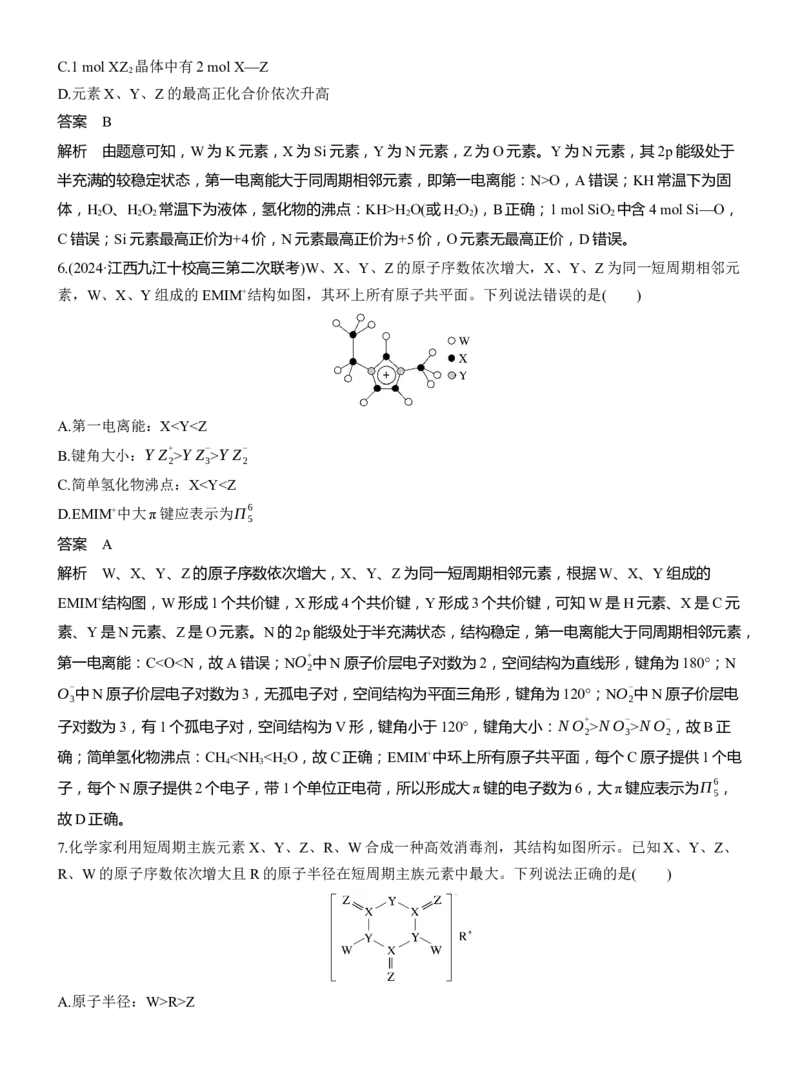
6.(2024·江西九江十校高三第二次联考)W、X、Y、Z的原子序数依次增大,X、Y、Z为同一短周期相邻元
素,W、X、Y组成的EMIM+结构如图,其环上所有原子共平面。下列说法错误的是( )
A.第一电离能:XY Z- >Y Z-
2 3 2
C.简单氢化物沸点:XNO- >NO-
,故B正
2 3 2
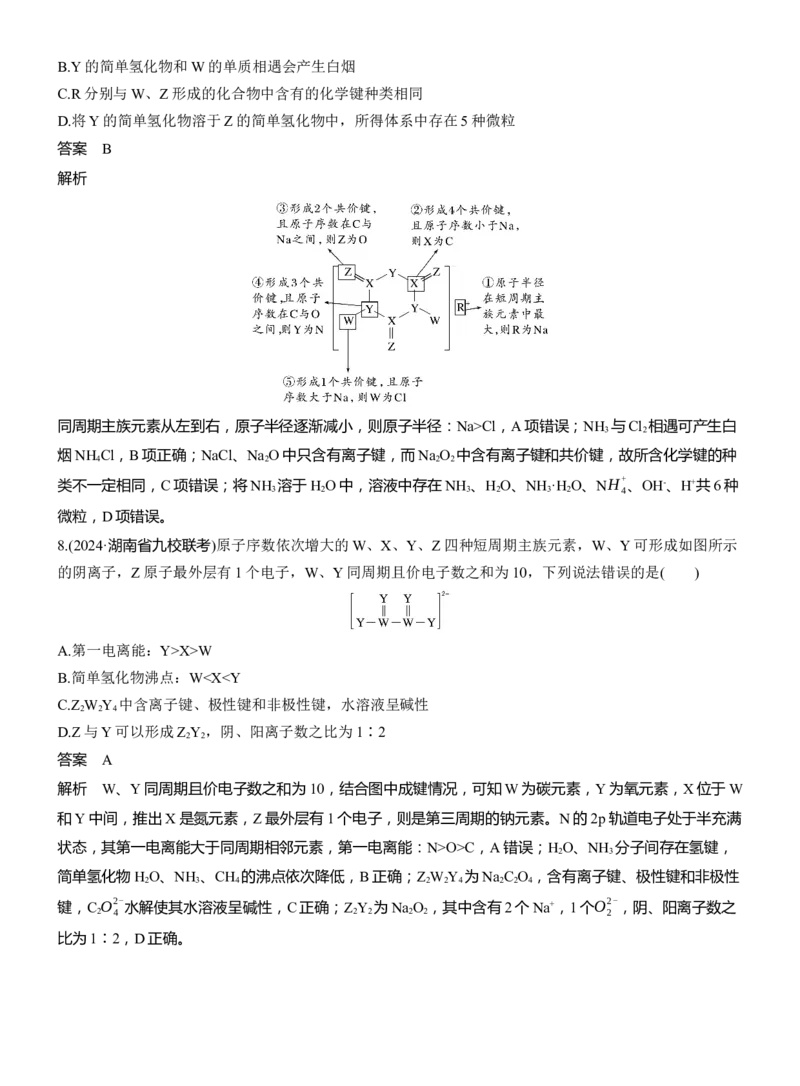
确;简单氢化物沸点:CH R>ZB.Y的简单氢化物和W的单质相遇会产生白烟
C.R分别与W、Z形成的化合物中含有的化学键种类相同
D.将Y的简单氢化物溶于Z的简单氢化物中,所得体系中存在5种微粒
答案 B
解析
同周期主族元素从左到右,原子半径逐渐减小,则原子半径:Na>Cl,A项错误;NH 与Cl 相遇可产生白
3 2
烟NH Cl,B项正确;NaCl、Na O中只含有离子键,而Na O 中含有离子键和共价键,故所含化学键的种
4 2 2 2
类不一定相同,C项错误;将NH 溶于H O中,溶液中存在NH 、H O、NH ·H
O、NH+
、OH-、H+共6种
3 2 3 2 3 2 4
微粒,D项错误。
8.(2024·湖南省九校联考)原子序数依次增大的W、X、Y、Z四种短周期主族元素,W、Y可形成如图所示
的阴离子,Z原子最外层有1个电子,W、Y同周期且价电子数之和为10,下列说法错误的是( )
A.第一电离能:Y>X>W
B.简单氢化物沸点:WO>C,A错误;H O、NH 分子间存在氢键,
2 3
简单氢化物H O、NH 、CH 的沸点依次降低,B正确;Z W Y 为Na C O ,含有离子键、极性键和非极性
2 3 4 2 2 4 2 2 4
键,C
O2-
水解使其水溶液呈碱性,C正确;Z Y 为Na O
,其中含有2个Na+,1个O2-
,阴、阳离子数之
2 4 2 2 2 2 2
比为1∶2,D正确。9.(2024·河南省五市高三下学期第一次联考)短周期主族元素W、X、Y、Z的原子序数依次增大,W原子的
最外层电子数等于Y原子最外层电子数的2倍,四种元素形成的一种化合物的结构如图所示,该化合物的
阴离子中每个原子的最外层均满足8电子稳定结构。下列说法正确的是( )
A.原子半径:XY>Z>W,故A错误;Y的单质与X的最高价氧化物对应的水化物氢氧化钠反应时,水中氢元素得到电
子,水是氧化剂,故B错误;与Z相邻的短周期同族元素为C,C的氢化物为烃,碳原子数较多的烃常温
下为固态,其熔、沸点大于H O,故C错误;W与X形成的二元化合物氧化钠或过氧化钠中阳离子和阴离
2
子个数比均为2∶1,故D正确。
10.(2024·辽宁省协作校高三下学期一模大联考)短周期元素W、X、Y、Z、Q的原子序数依次增大,已知
A、B、C、D是它们中的两种或三种形成的化合物,且A、B、C均含有Z元素。A的焰色试验呈黄色,水
溶液呈碱性;B是两性氢氧化物;D是由W与Q形成的化合物,常温下0.1 mol·L-1D溶液的pH为1,在一
定条件下它们之间的相互转化关系如图所示。下列说法正确的是( )
A.X元素的单质可能含有极性键,氢化物可能含有非极性键
B.X、Y、Z元素的简单离子半径大小是XY>Z,故B错误;Na与Cl和H与Cl元素形成的化合物分别为氯化钠和氯化
氢,均属于电解质,氯化钠中的化学键为离子键,而氯化氢中的化学键为共价键,故C错误;元素的非金
属性越强,其最高价含氧酸的酸性越强,但F元素无正价,所以氯元素的最高价含氧酸在同主族中最强,
但其他价态的含氧酸,如HClO为弱酸,在同族中酸性不是最强,故D错误。
11.(2024·长春高三下学期检测)已知X、Y、Z、W、R是原子序数依次增大的五种短周期元素,W和R组
成的一种化合物具有强氧化性,可用于自来水消毒,五种元素形成的某种化合物结构如图,下列说法正确
的是( )
A.原子半径:R>W>Z>Y>X
B.简单氢化物的沸点:R>W>Z>Y
C.W单质均为非极性分子
D.X和Z组成的化合物可能含有非极性键
答案 D
解析 X、Y、Z、W、R是原子序数依次增大的五种短周期元素,由结构可知,化合物中X、Y、Z、W、
R形成的共价键的数目分别为1、4、3、2、1,W和R组成的一种化合物具有强氧化性,可用于自来水消
毒,应为ClO ,则X为H元素、Y为C元素、Z为N元素、W为O元素、R为Cl元素。同周期元素,从
2
左到右原子半径依次减小,则O、N、C的原子半径依次增大,故A错误;水分子能形成分子间氢键,氯
化氢不能形成分子间氢键,所以水的沸点高于氯化氢,故B错误;O 为非极性分子,O 为极性分子,故C
2 3
错误;N H 是含有极性键和非极性键的极性分子,故D正确。
2 4
12.(2024·东北三省三校二模联考)某种双核钴配合物阳离子的结构如图。X的第一电离能在第二周期主族元
素中位居第二,Y的核外电子只有一种运动状态,Z单质的一种同素异形体是极性分子。下列说法错误的
是( )
A.简单氢化物的稳定性:Z>X
B.电负性:Z>X>Y
C.Co位于元素周期表ds区,在该阳离子中呈+2价
D.从结构推测该配合物阳离子不稳定,且具有一定的氧化性答案 C
解析 由题意可知,X为N,Y为H,Z为O。非金属性:Z(O)>X(N),因此简单氢化物的稳定性:Z>X,
故A正确;同周期元素,从左到右电负性逐渐增大,同族元素,从上到下电负性逐渐减小,即电负性:
Z(O)>X(N)>Y(H),故B正确;Co位于元素周期表d区,故C错误;该配合物阳离子存在过氧键,因此不
稳定,且具有一定的氧化性,故D正确。
13.(2024·河北雄安新区高三下学期一模)一种具有解热镇痛作用的合成药物结构如图所示,W、Y、X、Q
为原子半径依次递减的短周期非金属元素,Q的最高正价和最低负价代数和为0,且W与Y的价层电子排
布均为ns2np2,下列说法正确的是( )
A.氢化物的沸点:X>Y>W
B.最高价氧化物对应水化物的酸性:YZ>T
B.W元素位于元素周期表的d区
C.580 ℃热分解后得到的固体化合物是WZ
D.简单氢化物的稳定性:Z>Y
答案 C
解析 W为常见的金属元素,离子的价层电子排布式为3d6,则W为Fe元素;X、Y、Z、T分别位于三个
短周期,原子序数依次增加,则X为H元素;常温下YZ 为气体,其分子的总电子数为奇数,则YZ 为
2 2
NO ,则Y为N元素、Z为O元素;T与Z同主族,则T为S元素。同主族元素,从上到下第一电离能依
2
次减小,同周期元素,从左到右第一电离能呈增大趋势,N的第一电离能大于相邻元素,则第一电离能由
大到小的顺序为N>O>S,故A正确;铁元素的原子序数为26,基态铁原子的价层电子排布式为3d64s2,则
铁元素位于元素周期表的d区,故B正确;由题意可知,化合物的化学式为(NH ) Fe(SO ) ·6H O,相对分
4 2 4 2 2
子质量为392,取1 mol该物质进行热重分析,由热重曲线可知,580 ℃热分解后得到固体的质量为392
g×(100%-9.2%-9.2%-9.2%-52.0%)≈80 g,则固体化合物为0.5 mol氧化铁,故C错误;元素的非金属性:
O>N,则简单氢化物的稳定性:H O>NH ,故D正确。
2 3