文档内容
化工生产中物质的分离与提纯
1.(11分)(1)碘化亚铜(CuI)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水碘化亚铜
的流程。
①步骤a中Cu S被转化为Cu,同时有大气污染物A生成,相关反应的化学方程式为 。
2
熔渣B主要成分为黑色磁性物质,其化学式为 。
②步骤b中H O 的作用是 ;步骤c中加入过量NaI涉及的主要反应的离子方程式为
2 2
。
③步骤d用乙醇洗涤的优点是 ;检验沉淀是否洗涤干净的方法是 。
(2)下图是Na SO 和Na SO ·10H O的溶解度曲线,则由Na SO 溶液得到Na SO 固体的操作是 →
2 4 2 4 2 2 4 2 4
→用乙醇洗涤→干燥。用乙醇洗涤而不用水洗的原因是 。
2.(11分)(2023·厦门高三第二次质量检测)磷精矿主要成分为Ca F(PO ) ,含少量REPO 、FeO、Fe O 、
5 4 3 4 2 3
SiO ,其中RE代表稀土元素。从磷精矿分离稀土元素的工业流程如下。
2
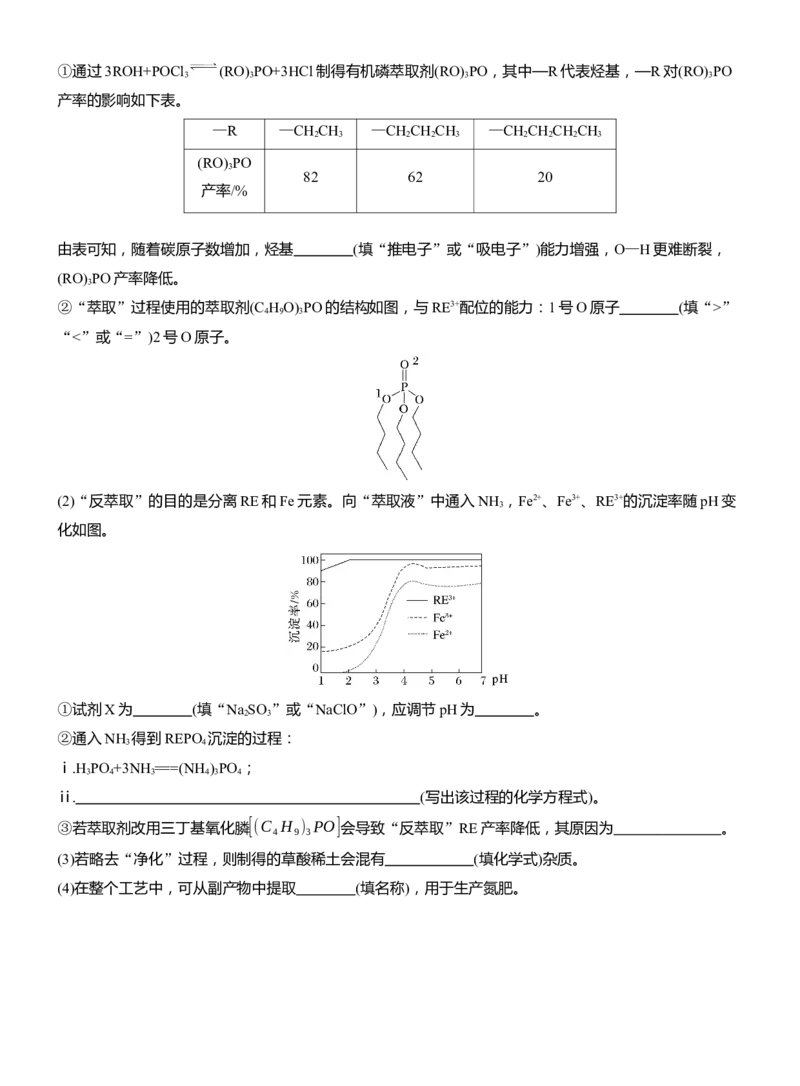
(1)“萃取”的目的是富集RE,但其他元素也会按一定比例进入萃取剂中。①通过3ROH+POCl (RO) PO+3HCl制得有机磷萃取剂(RO) PO,其中—R代表烃基,—R对(RO) PO
3 3 3 3
产率的影响如下表。
—R —CH CH —CH CH CH —CH CH CH CH
2 3 2 2 3 2 2 2 3
(RO) PO
3
82 62 20
产率/%
由表可知,随着碳原子数增加,烃基 (填“推电子”或“吸电子”)能力增强,O—H更难断裂,
(RO) PO产率降低。
3
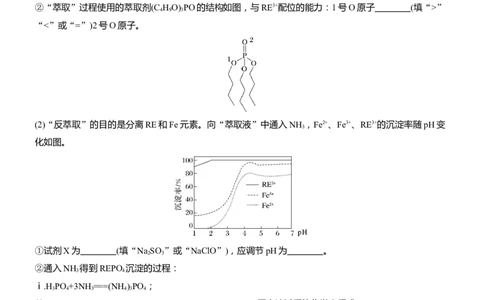
②“萃取”过程使用的萃取剂(C H O) PO的结构如图,与RE3+配位的能力:1号O原子 (填“>”
4 9 3
“<”或“=”)2号O原子。
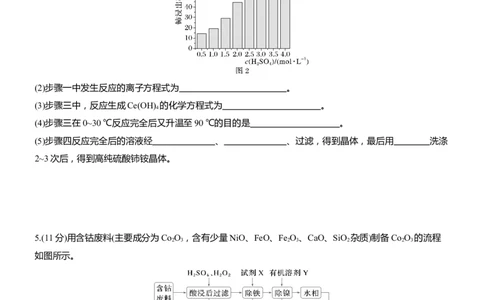
(2)“反萃取”的目的是分离RE和Fe元素。向“萃取液”中通入NH ,Fe2+、Fe3+、RE3+的沉淀率随pH变
3
化如图。
①试剂X为 (填“Na SO ”或“NaClO”),应调节pH为 。
2 3
②通入NH 得到REPO 沉淀的过程:
3 4
ⅰ.H PO +3NH ===(NH ) PO ;
3 4 3 4 3 4
ⅱ. (写出该过程的化学方程式)。
③若萃取剂改用三丁基氧化膦[(C H ) PO]会导致“反萃取”RE产率降低,其原因为 。
4 9 3
(3)若略去“净化”过程,则制得的草酸稀土会混有 (填化学式)杂质。
(4)在整个工艺中,可从副产物中提取 (填名称),用于生产氮肥。3.(6分)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为CuIn Ga Se 。某探究小组回收处
0.5 0.5 2
理流程如图:
(1)高温焙烧得到的烧渣主要成分是氧化物(如:Cu O、In O 、Ga O ),“酸浸氧化”得蓝色溶液,则该过
2 2 3 2 3
程发生的主要氧化还原反应的离子方程式为 。
(2)“滤渣”与SOCl 混合前需要洗涤、干燥,检验滤渣是否洗净的操作: 。
2
(3)SOCl 的作用: 。
2
4.(11分)硫酸铈铵[(N H ) Ce(SO ) ]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。某
4 2 4 3
工厂用含铈矿石[主要成分为Ce (CO ) ]制备硫酸铈铵的工艺流程如图所示:
2 3 3
已知:①K [Ce(OH) ]=2×10-48。
sp 4
②硫酸铈铵的熔点为130 ℃,沸点为330 ℃。
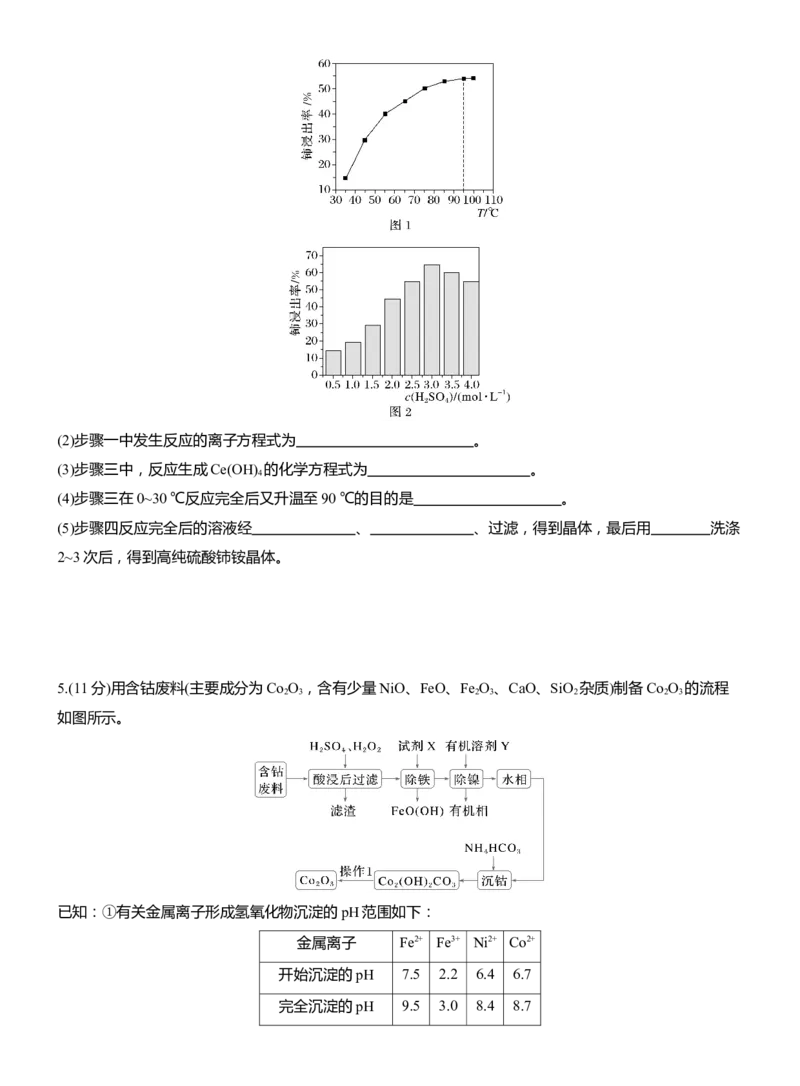
(1)含铈矿石进行的“一系列操作”包含用硫酸酸浸,其中铈浸出率与温度的关系如图1所示,铈浸出率与
硫酸浓度的关系如图2所示。工业生产应选择的适宜温度是 ℃,适宜的硫酸浓度是
mol·L-1。(2)步骤一中发生反应的离子方程式为 。
(3)步骤三中,反应生成Ce(OH) 的化学方程式为 。
4
(4)步骤三在0~30 ℃反应完全后又升温至90 ℃的目的是 。
(5)步骤四反应完全后的溶液经 、 、过滤,得到晶体,最后用 洗涤
2~3次后,得到高纯硫酸铈铵晶体。
5.(11分)用含钴废料(主要成分为Co O ,含有少量NiO、FeO、Fe O 、CaO、SiO 杂质)制备Co O 的流程
2 3 2 3 2 2 3
如图所示。
已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 Fe2+ Fe3+ Ni2+ Co2+
开始沉淀的pH 7.5 2.2 6.4 6.7
完全沉淀的pH 9.5 3.0 8.4 8.7②在pH为4~6时,Fe3+水解生成含Fe(OH)
·nFe3+·(n-x)SO2-
胶粒的胶体。
3 4
(1)“酸浸”步骤中可以有效提高废料利用率的方法有 (写出一种方法即可)。“过
滤”所得滤渣的成分是 (填化学式)。
(2)“酸浸”时Co O 与H O 发生反应的离子方程式为 。
2 3 2 2
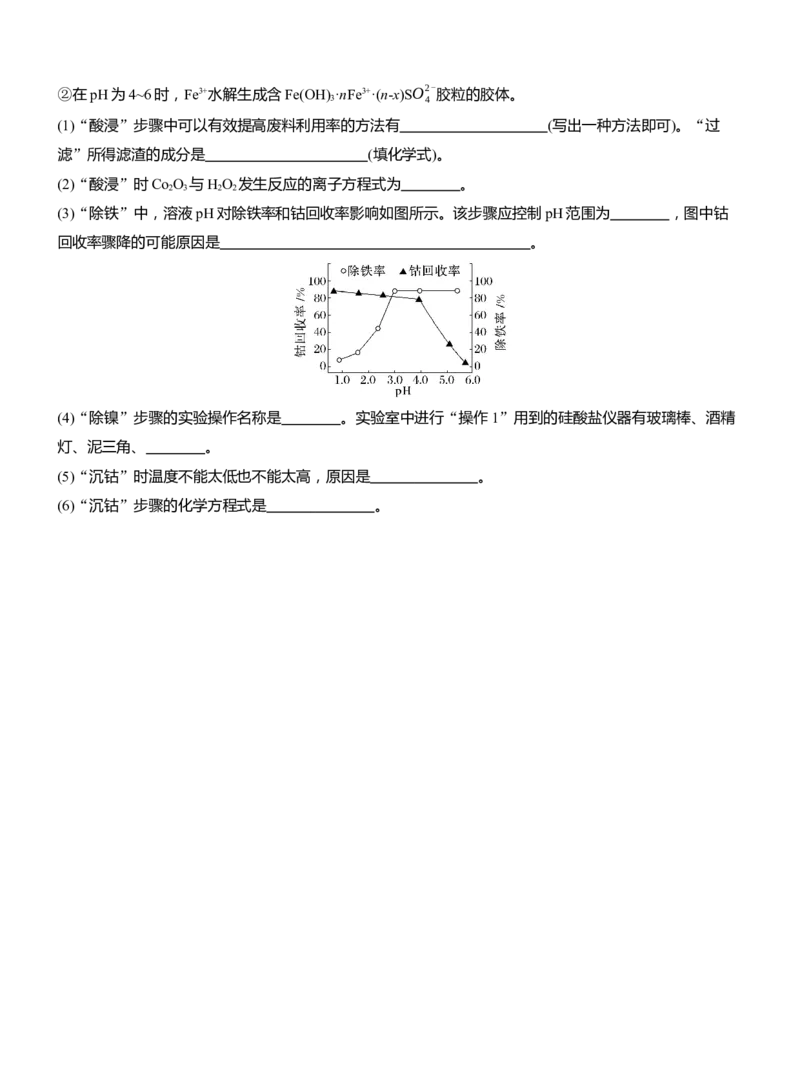
(3)“除铁”中,溶液pH对除铁率和钴回收率影响如图所示。该步骤应控制pH范围为 ,图中钴
回收率骤降的可能原因是 。
(4)“除镍”步骤的实验操作名称是 。实验室中进行“操作1”用到的硅酸盐仪器有玻璃棒、酒精
灯、泥三角、 。
(5)“沉钴”时温度不能太低也不能太高,原因是 。
(6)“沉钴”步骤的化学方程式是 。答案精析
1.(1)①Cu S+O 2Cu+SO Fe O
2 2 2 3 4
②作氧化剂,将Cu O和Cu氧化为Cu2+ 2Cu2++4I-===2CuI↓+I ③洗去残余水分且可快速晾干 蘸取最
2 2
后一次洗涤液进行焰色试验,如果火焰无黄色则已洗净(或其他合理答案) (2)蒸发结晶 趁热过滤 防止
Na SO 固体转化为Na SO ·10H O,并防止Na SO 因溶于水而损耗
2 4 2 4 2 2 4
2.(1)①推电子 ②< (2)①Na SO 2 ②(NH ) PO +RE(NO ) ===REPO ↓+3NH NO ③—C H 有较强的
2 3 4 3 4 3 3 4 4 3 4 9
推电子作用,导致稀土与萃取剂形成的配位键牢固,难以断裂实现反萃取 (3)CaC O (4)硝酸铵、硝酸
2 4
解析 磷精矿加入硝酸酸浸,二氧化硅不反应得到滤渣1,稀土元素、铁、钙元素进入滤液,加入萃取剂
萃取出稀土元素,然后加入亚硫酸钠将三价铁转化为二价铁,通入氨气,调节pH分离出含有稀土的固相,
再加入硝酸溶解,加入硫酸除去钙元素得到滤渣2硫酸钙,滤液加入草酸分离出草酸稀土。(1)②由随着碳
原子数增加,烃基推电子能力增强可知,烃基导致1号位氧更难与RE3+配位,故与RE3+配位的能力:1号
O原子<2号O原子。(2)①由图可知,亚铁离子与RE的分离效果更好,则试剂X为将铁离子转化为亚铁离
子的物质,故应选择Na SO ;结合图像可知,应调节pH为2,此时RE几乎完全沉淀,而亚铁离子几乎没
2 3
有沉淀,分离效果好。②总反应为通入NH 得到REPO 沉淀,反应ⅰ.H PO +3NH ===(NH ) PO ,则反应
3 4 3 4 3 4 3 4
ⅱ为(NH ) PO 和稀土的硝酸盐转化为REPO 沉淀的反应:(NH ) PO +RE(NO ) ===REPO ↓+3NH NO 。(4)
4 3 4 4 4 3 4 3 3 4 4 3
在整个工艺中,通入氨气生成的硝酸铵,以及酸溶加入的硝酸均含有氮元素,故可从副产物中提取硝酸铵、
硝酸用于生产氮肥。
3.(1)Cu O+H O +4H+===2Cu2++3H O (2)取最后一次洗涤液于试管中,加入盐酸酸化,无明显现象,再加
2 2 2 2
氯化钡溶液,若无白色沉淀生成,则证明洗涤干净;若有白色沉淀生成,则证明没有洗涤干净 (3)将氢氧
化物转化为氯化物;作溶剂
4.(1)95 3.0 (2)2Ce3++6 HCO 3 - ===Ce 2 (CO 3 ) 3 ↓+3CO 2 ↑+3H 2 O (3)Ce 2 (SO 4 ) 3 +H 2 O 2 +6NH 3 ·H 2 O
2Ce(OH) ↓+3(NH ) SO (4)0~30 ℃反应是防止H O 、氨水分解,后升温至90 ℃是除去过量的H O (合理
4 4 2 4 2 2 2 2
即可) (5)蒸发浓缩 冷却结晶 乙醇
解析 含铈矿石经过一系列操作,Ce3+进入溶液中,加入NH HCO 溶液得到Ce (CO ) ,加入0.5 mol·L-1
4 3 2 3 3
H SO 溶液得到Ce (SO ) 溶液,加入过氧化氢将Ce3+氧化为Ce4+,加入氨水控温在0~30 ℃,然后升温至
2 4 2 4 3
90 ℃得到Ce(OH) 悬浊液,加入硫酸、硫酸铵得到硫酸铈铵晶体。
4
5.(1)适当提高H SO 浓度、粉碎废料、充分搅拌、适当延长酸浸时间等(写出一种即可) SiO 、CaSO
2 4 2 4
(2)Co O +H O +4H+===2Co2++O ↑+3H O (3)3.0~4.0 Fe3+水解生成含Fe(OH) ·nFe3+·(n-x)SO2-胶粒的胶体,
2 3 2 2 2 2 3 4
吸附大量的Co2+,导致钴回收率下降 (4)萃取(或萃取分液) 坩埚 (5)温度过低,反应速率慢;温度过高,
NH HCO 不稳定受热易分解 (6)2CoSO +4NH HCO ===Co (OH) CO ↓+3CO ↑+H O+2(NH ) SO
4 3 4 4 3 2 2 3 2 2 4 2 4
解析 含钴废料主要成分为Co O ,含有少量NiO、FeO、Fe O 、CaO、SiO 杂质,用硫酸溶解,过氧化氢
2 3 2 3 2
把Co3+还原为Co2+,把Fe2+氧化为Fe3+得到含有Co2+、Fe3+、Ni2+的溶液,CaSO 微溶、SiO 难溶,过滤出
4 2沉淀;调节溶液的pH在3.0~4.0,除去Fe3+;滤液中加入萃取剂,萃取除去Ni2+,取水相加入NH HCO 生
4 3
成Co (OH) CO ,在空气中灼烧Co (OH) CO 生成Co O 。
2 2 3 2 2 3 2 3