文档内容
专题六 能力提升检测卷
1.下列关于ΔH的说法正确的是
A.反应过程中,消耗的反应物越多,ΔH越大
B.ΔH>0,吸热反应;ΔH<0,放热反应
C.ΔH越大,说明反应放出的热量越多
D.能量变化如图所示的化学反应为吸热反应,ΔH符号为“+”
【答案】B
【解析】ΔH与化学方程式中的化学计量数有关,与反应物的用量无关,A错误;
B.若反应物的能量低于生成物能量时,发生反应时反应物要吸收能量变为生成物,该反应为吸热反
应,ΔH>0;若反应物的能量高于生成物能量时,发生反应多余的能量就会释放出来,该反应为放热反
应,ΔH<0,B正确;
C.ΔH有正、负之分,反应放出的热量越多,则反应热ΔH越小;若反应发生时吸收的热量越多,则
反应热ΔH越大,C错误;
D.根据图示可知:反应物的总焓大于生成物的总焓,故发生反应时多余的能量要释放出来,该反应
为放热反应,ΔH<0,ΔH符号为“-”,D错误;故选B。
2.根据如图能量关系示意图,下列说法正确的是
A.1molC(s)与1molO (g)的能量之和为393.5kJ
2
B.反应2CO(g)+O(g)=2CO (g)中,生成物的总能量大于反应物的总能量
2 2
C.由C(s)→CO(g)的热化学方程式为:2C(s)+O(g)=2CO(g) ΔH=-221.2kJ·mol-1
2
D.热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1kJ·mol-1【答案】C
【解析】由图示可知,1molC(s)与1molO (g)的能量比1molCO (g)的能量高393.5 kJ,A错误;
2 2
B.由图示可知,2CO(g)+O(g)=2CO (g)为放热反应,生成物的总能量小于反应物的总能量,B错
2 2
误;
C.由图示可知,1molC(s)与O(g)反应生成1molCO(g)放出热量为393.5 kJ-282.9 kJ=110.6 kJ,且物质
2
的量与热量成正比,焓变为负,则热化学方程式为:2C(s)+O(g)=2CO(g) ΔH=-221.2 kJ·mol-1,C正确;
2
D.若热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO的热值为 ≈10.1 kJ·g-1,
D错误;答案选C。
3.室温下,将CuSO ·5H O(s)溶于水会使溶液温度降低,将 CuSO (s)溶于水会使溶液温度升
4 2 4
高。则下列能量转化关系不正确的是
A.ΔH>0 B.ΔH<ΔH C.ΔH<ΔH D.ΔH=ΔH +ΔH
1 2 3 3 1 2 1 3
【答案】B
【解析】CuSO ·5H O (s)受热分解生成CuSO (s),为吸热反应,△H>0,故A正确;
4 2 4 1
B.将CuSO ·5H O(s)溶于水会使溶液温度降低,所以ΔH>0;将 CuSO (s)溶于水会使溶液温
4 2 2 4
度升高,所以ΔH<0,所以ΔH>ΔH,故B错误;
3 2 3
C.CuSO ·5H O(s)受热分解生成CuSO (s),为吸热反应,△H>0;将 CuSO (s)溶于水会使溶液温
4 2 4 1 4
度升高,ΔH<0,所以ΔH<ΔH,故C正确;
3 3 1
D.根据盖斯定律可知:ΔH=ΔH +ΔH ,故D正确;故答案B。
2 1 3
4.晶格能(U)是气态离子形成1mol离子晶体释放的能量。 是离子晶体,其晶格能的实验值可通
过玻恩-哈伯热力学循环图计算得到。已知: ,
下列说法不正确的是
A. B.O—O键键能为
C. D.
【答案】D
【解析】根据题给晶格能的定义和题图可知,2mol气态锂离子和 结合成 (晶体)
释放的能量即 ,选项A正确;
B.O=O键键能为 ,选项B正确;
C. ,选项C正确;
D.根据盖斯定律求出 ,Li第一电离能为
,选项D错误;答案选D。
5.镁和氯气反应生成氯化镁的能量关系图如图所示。已知,气态的卤素原子得电子生成气态的卤离
素子是放热过程。下列说法正确的是
A.∆H=∆H +∆H +∆H +∆H +∆H
6 1 2 3 4 5
B.Ca(g)–2e-=Ca2+(g) ∆H ,则∆H>∆H
7 7 3
C.I(g)+e-=I-(g) ∆H ,则∆H>∆H
8 8 4
D.MgCl (s)=Mg2+(aq)+2Cl-(aq) ∆H,则∆H>∆H
2 9 9 5【答案】C
【解析】根据盖斯定律可知,∆H=∆H+∆H+∆H+∆H-∆H,故A错误;原子失去电子变为离子属于
6 1 2 3 4 5
吸热过程,Ca和Mg属于同主族,Ca的金属性强于Mg,Ca→Ca2+吸收热量小于Mg→Mg2+吸收热量,即
∆H<∆H,故B错误;原子得电子变为离子属于放热过程,Cl非金属性强于I,即Cl→Cl-放出热量比
7 3
I→I-放出热量多,即∆H>∆H,故C正确;MgCl (s)=Mg2+(g)+2Cl-(g)属于吸热反应,即∆H>0,Mg2+
8 4 2 5
(g)、2Cl-(g)转化成Mg2+(aq)、2Cl-(aq)要放出热量,发生MgCl (s)=Mg2+(aq)+2Cl-(aq)吸收热量比
2
MgCl (s)=Mg2+(g)+2Cl-(g)少,即∆H<∆H,故D错误;答案为C。
2 9 5
6.已知:
其他数据如下表:
化学键 C=O O=O C-H O-H C=C
x
键能/( ) 798 413 463 615
下列说法正确的是
A.乙烯的燃烧热为
B.
C.
D.当生成4molO-H键时,该反应放出热量一定为akJ
【答案】B
【解析】表示燃烧热时,水应为液态,A项错误;
B.根据 等于反应物键能总和减生成物键能总和: ,可得
出 ,B项正确;
C.生成 , ,C项错误;
D.生成4molO-H键,即生成 ,水的状态不能确定,D项错误;故选B。7.25℃、101 kPa下,1 mol 氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正
确的是
A.2H (g) + O (g) = 2H O(1) H = -285.8kJ/mol
2 2 2
B.2H (g) + O (g) = 2H O(1) △H = +571.6 kJ/mol
2 2 2
C.2H (g) + O (g) = 2H O(g) △ H = -571.6 kJ/mol
2 2 2
△
D.H (g) + O (g) = H O(1) H = -285.8kJ/mol
2 2 2
△
【答案】D
【解析】放出热量说明反应热△H<0,2g氢气燃烧生成液态水,放出285.8kJ热量,说明消耗
1molH ,放出285.8 kJ/mol;
2
A.2molH 生成2mol液体水,放出的热量为 ,A错误;
2
B.2molH 生成2mol液体水,为放热反应,B错误;
2
C.2molH 生成2mol气态水,放出的热量大于571.6kJ/mol,C错误;
2
D.1molH 生成1mol气态水,放出的热量285.8kJ/mol,D正确;故选D。
2
8.近日,科学家开发了基于碳布的首个“ ”电池,其装置如图所示,电池总反应为
。已知 在碳布上生成,下列叙述正确的是
A.原电池工作时, 通过玻璃纤维向X极迁移
B.原电池工作时,Y极发生还原反应.
C.原电池工作时, 通过玻璃纤维向X极移动
D. 参与反应时理论上转移0.6mol电子
【答案】B【分析】由题干装置图结合电池总反应: 可知,X电极为负极,电极反应为:Li-e-
=Li+,6Li++N +6e-=2Li N,据此分析解题。
2 3
【解析】A.观察图示,在碳布(Y极)表面生成氮化锂, 要留在玻璃纤维右边的溶液中与 形成
,说明 不能通过玻璃纤维,是 通过玻璃纤维由X极移向Y极,A错误;
B.放电时,Y极为正极,氮气发生还原反应生成氮化锂,B正确;
C.电池工作时,阳离子向正极迁移,即向Y极迁移,C错误;
D. 参与反应,理论上转移6mol电子,但是没有指明“标准状况”,不能用 计
算,D错误;故答案为B。
9.某原电池装置如图所示,电池总反应为 。下列说法不正确的是
A.充分放电后左侧溶液中的盐酸浓度基本不变
B.正极反应为
C.放电时,交换膜右侧溶液不会有大量白色沉淀生成
D.当电路中转移 时,经过交换膜的离子是
【答案】B
【分析】根据电池总反应为 可知,Ag失电子作负极失电子,氯气在正极上得电子生
成氯离子,以此解答。
【解析】A.电池总反应为 可知,放电后左侧溶液中的氯离子由右侧通过阴离子交换
膜补充,所以左侧溶液中的盐酸浓度基本不变,故A正确;B.正极上氯气得电子生成氯离子,其电极反应为: ,故B错误;
C.放电时,交换膜左侧银为负极失电子形成银离子与溶液中的氯离子结合成AgCl沉淀,所以左侧溶
液中有大量白色沉淀氯化银生成,故C正确;
D.放电时,当电路中转移 时,交换膜右则会有0.01mol氯离子通过阴离子交换膜向负极移
动,故D正确;故选B。
10.一种熔融碳酸盐燃料电池原理如图所示。下列说法正确的是
A.电子从电极A经熔融碳酸盐转移到电极B
B.熔融碳酸盐中CO 向电极B移动
C.CH 在电极A放电生成CO
4 2
D.反应过程熔融盐中CO 的物质的量不变
【答案】D
【分析】由图可知,CO、H 在A电极失电子生成CO、HO,电极A是负极,电极B是正极。
2 2 2
【解析】A.电极A是负极,电极B是正极,电子不能经过内电路,故A错误;
B.A是负极、B是正极,熔融碳酸盐中CO 向电极A移动,故B错误;
C.CO、H 在电极A放电生成CO、HO,故C错误;
2 2 2
D.电池总反应为 ,反应过程熔融盐中CO 的物质的量不变,故D正确;
选D。
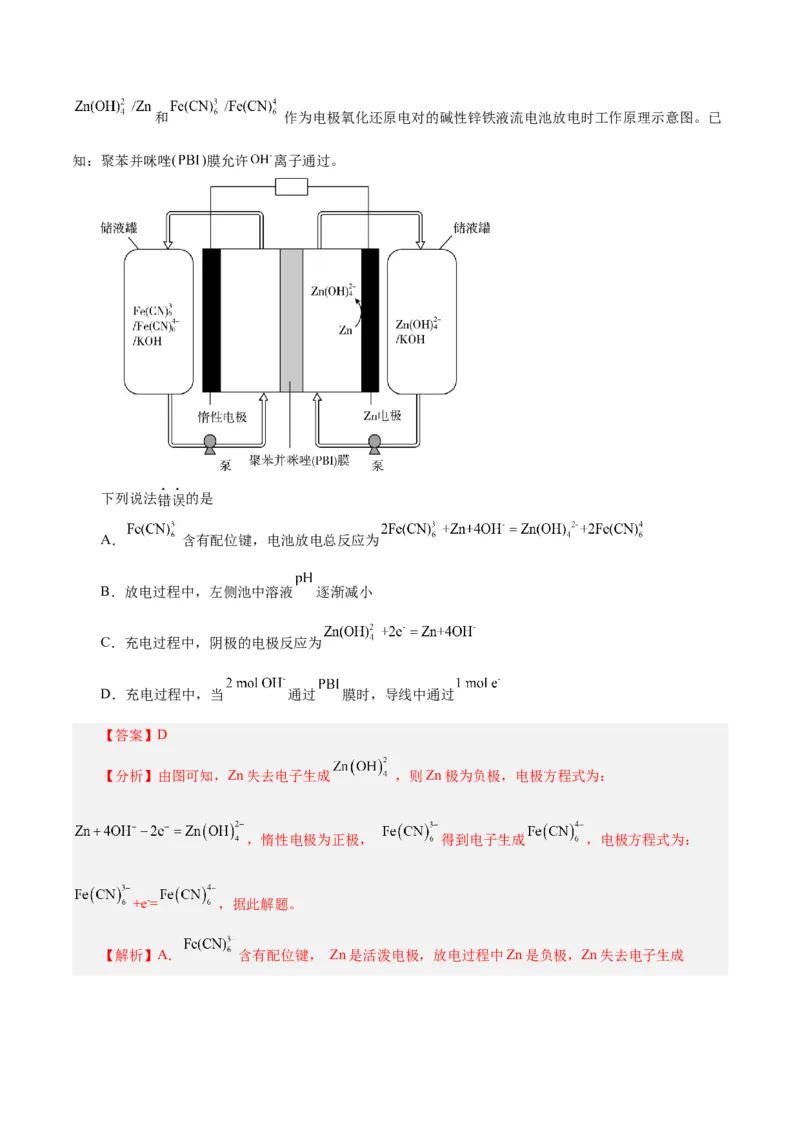
11.锌铁液流电池由于安全、稳定、电解液成本低等优点成为电化学储能热点技术之一、如图为以和 作为电极氧化还原电对的碱性锌铁液流电池放电时工作原理示意图。已
知:聚苯并咪唑( )膜允许 离子通过。
下列说法错误的是
A. 含有配位键,电池放电总反应为
B.放电过程中,左侧池中溶液 逐渐减小
C.充电过程中,阴极的电极反应为
D.充电过程中,当 通过 膜时,导线中通过
【答案】D
【分析】由图可知,Zn失去电子生成 ,则Zn极为负极,电极方程式为:
,惰性电极为正极, 得到电子生成 ,电极方程式为:
+e-= ,据此解题。
【解析】A. 含有配位键, Zn是活泼电极,放电过程中Zn是负极,Zn失去电子生成,电极方程式为:Zn-2e-+4OH-= ;惰性电极为正极, 得到电子生成 ,
电极方程式为: +e-= ;则放电过程中,总反应为
,故A正确;
B.放电过程中,左侧惰性电极为正极,右侧Zn是负极。负极电极方程式为:Zn-2e-+4OH-=
,该过程需要的OH-由左侧池经过聚苯并咪唑( )膜进入右侧池,左侧池中溶液 逐渐减小,故B正
确;
C.充电过程中,Zn是阴极,电极方程式为: +2e-= Zn+4OH-,故C正确;
D.充电过程中,Zn是阴极,电极方程式为: +2e-= Zn+4OH-,该过程生成的OH-一半进入
左侧池,当 通过 膜时,导线中通过 ,故D错误;
故选D。
12.一种可用于吸收 的电池,其工作时的原理如图所示。下列说法正确的是
A.电极a上发生的电极反应为
B.Ⅰ室出口处溶液的pH大于入口处
C.如果将Ⅰ室、Ⅱ室间改为阳离子交换膜,则电池工作时Ⅰ室可能有 沉淀生成D.该装置可以制取 和
【答案】D
【分析】由图可知氢气在电极a上失电子,结合I室中的氢氧根离子生成水,电极反应为:
。A极为负极,b极为正极,b电极上氢离子得电子生成氢气,据此解答。
【解析】A.由以上分析可知电极a上反应为: ,故A错误;
B.I室中氢氧根离子逐渐被消耗,溶液pH值逐渐减小,则出口处pH小于入口处,故B错误;
C.如果将Ⅰ室、Ⅱ室间改为阳离子交换膜,则I室中的钙离子通过交换膜向Ⅱ室移动,在Ⅱ室中结合
碳酸根可能生成 沉淀,故C错误;
D.该装置I室中有钙离子,从Ⅱ室迁移来的氯离子,故I室可以制取氯化钙;Ⅱ室中含钠离子和反应
生成的碳酸氢根离子,可得到碳酸氢钠,故D正确;
故选D。
13.一种水性电解液 离子选择双隔膜电池如图所示(已知在 溶液中, 以
存在)。关于电池放电时,下列叙述错误的是
A.MnO 为电池的正极
2
B.Ⅱ、Ⅲ区间的隔膜为阳离子交换膜
C.Zn电极反应:
D.当Ⅱ区质量增加17.4g时,电路中转移0.1mol电子
【答案】D【解析】A.此装置为原电池, 电极做正极,发生得到电子的还原反应,电极反应为
,A正确;
B.负极区(III区) 剩余,通过隔膜迁移到II区,因此它们之间的隔膜为阳离子交换膜,B正确;
C. 为负极,发生氧化反应,电极反应为 ,C正确;
D.正极区 过量,通过隔膜迁移到II区,故II区中 溶液的浓度增大,当II区增加
时,电路中转移 电子,现增加 ,则转移 电子,D错误。
答案选D。
14.燃料电池近几年发展迅速,如图是科学家利用页岩气设计的一种固态(熔盐)燃料电池工作示意
图。下列说法错误的是
A.电极材料采用石墨烯,吸附甲烷的电极为负极,发生氧化反应
B.通入氧气的电极上电极反应式为
C.电池工作时, 向通甲烷的电极一侧移动
D.该电池的优点是二氧化碳可循环利用,不会释放温室气体
【答案】D
【解析】A.依题意,甲烷发生氧化反应生成二氧化碳,吸附甲烷的电极为负极,A项正确;
B. 、 共同参与反应,电极反应式为 ,B项正确;
C.根据原电池工作原理,阴离子向负极移动,C项正确;
D.电池总反应为 ,会释放出二氧化碳,D项错误;故选D。
15.一种钠离子电池的工作原理如图所示,放电时电池反应可表示为
,下列说法正确的是
A.放电时,电能转化为化学能
B.放电时,Y极发生还原反应
C.充电时,X极电极反应式为
D.充电时,每转移1mol ,Y极质量减少23g
【答案】C
【分析】由图可知,放电时,X电极为原电池的正极,钠离子作用下Na FePO 在正极得到电子发生
1−x 4
还原反应生成NaFePO ,电极反应式为Na FePO +xe—+xNa+=NaFePO,Y电极为负极,NaC在负极失去
4 1−x 4 4 x
电子发生氧化反应生成钠离子和碳,电极反应式为NaC—xe—=xNa++C,充电时,X极与直流电源的正极
x
相连做阳极,Y电极做阴极。
【解析】A.由分析可知,放电时,该装置为化学能转化为电能的原电池,故A错误;
B.由分析可知,Y电极为负极,NaC在负极失去电子发生氧化反应生成钠离子和碳,故B错误;
x
C.由分析可知,充电时,X极与直流电源的正极相连做阳极,电极反应式为NaFePO —xe—
4
=Na FePO +xNa+,故C正确;
1−x 4
D.由分析可知,充电时,Y电极做阴极,电极反应式为xNa++C+xe—=Na C,则每转移1mol电子,Y
x
极质量增加23g,故D错误;
故选C。
16.用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定三颈烧瓶中压强随时间变化关系以及
溶解氧(DO)随时间变化关系的曲线如图。下列说法正确的是A.溶解氧随着溶液酸性减弱而增大
B.pH=2.0的溶液压强增大,主要是因为产生了氢气
C.整个过程中,负极电极反应式为:Fe-3e-=Fe3+
D.pH=4.0时,发生析氢腐蚀,不发生吸氧腐蚀
【答案】B
【解析】A.溶液酸性减弱,铁发生吸氧腐蚀,消耗氧气导致溶解氧减少,A错误;
B.pH=2时,溶液酸性较强,氢离子与铁反应生成氢气,导致烧瓶内压强增大,B正确;
C.整个过程中,锥形瓶中的Fe与C粉构成原电池,Fe为原电池负极,电极反应式为Fe-2e-=Fe2+,C
错误;
D.pH=4时,烧瓶内压强几乎不变,发生吸氧腐蚀消耗氧气导致压强减小,发生析氢腐蚀产生氢气导
致压强增大,故说明pH=4时,吸氧腐蚀和析氢腐蚀同时发生,D错误;
故答案选B。
17.镍离子( )和钴离子( )性质相似,可用如图所示装置实现二者分离。图中的双极膜中间层
中的 解离为 和 ,并在直流电场作用下分别向两极迁移; 与乙酰丙酮不反应。下列说法正
确的是A.石墨M电极上的电势低于石墨N电极上的电势
B.石墨M电极的电极反应式为 。
C.水解离出的 可以抑制Ⅱ室中的转化反应
D.导线中流过 ,Ⅰ室与Ⅲ室溶液质量变化之差约为130g
【答案】D
【解析】A.由图分析, 向石墨N电极方向移动,则石墨N电极为阴极、石墨M电极为阳极,石
墨M电极上的电势更高,A项错误;
B.石墨M电极上由 失电子,电极反应式为 ,B项错误;
C.由原子守恒和电荷守恒知,Ⅱ室中的转化反应生成 ,故水解离出的 可以促进Ⅱ室中的转化
反应,C项错误;
D.由原理可知,导线中流过 ,Ⅰ室移入Ⅱ室的 和 的总物质的量为1mol,同时有
生成 ,质量减少 ,Ⅲ室中阴极反应消耗的 由水解离出的 等量补充,溶液质量不变,
故两室溶液质量变化之差约为 ,D项正确;
故答案为D。
18.利用电化学原理控制反应条件能将 电催化还原为HCOOH,电解过程中还伴随着析氢反应,
反应过程原理的示意图如图。下列有关说法正确的是A.玻碳电极发生还原反应
B.铂电极发生的电极反应为
C.电池工作时,电流由玻碳电极经电解质溶液到铂电极
D.当电路中转移1mol 时,阳极室溶液的质量减少8g
【答案】C
【分析】分析该装置,HO转化为O,O失去电子发生氧化反应,则玻碳电极为阳极,铂电极为阴
2 2
极,据此解答。
【解析】A.玻碳电极为阳极,发生氧化反应,A错误;
B.铂电极发生的电极反应为CO+2H++2e-=HCOOH、 ,B错误;
2
C.玻碳电极为阳极,铂电极为阴极,电池工作时,电流由玻碳电极经电解质溶液到铂电极,C正
确;
D.当电路中转移1mol 时,同时有1mol氢离子通过质子交换膜进入左侧,阳极室溶液的质量减少
,D错误;
故选C。
19.目前工业废水处理备受关注。我国科研人员设计了一种通过内部物质循环处理含有机物C (H O)
m 2 n
的废水的实验装置,其工作原理如图所示,其中双极膜中间层中的HO解离为H+和OH-,并在直流电场作
2
用下分别向两极迁移。图中·OH 表示电中性的自由基。下列说法错误的是A.循环利用的气体X为O
2
B.工作时两极区HSO 溶液和NaOH溶液的浓度均逐渐减小
2 4
C.相同时间内,理论上生成CO 的物质的量小于生成O 的物质的量
2 2
D.工作时需向催化电极M区补充适量气体X
【答案】C
【分析】从图看,催化电极M为O 结合H+发生还原反应,该极为电解池的阴极。则电极N为电解池
2
的阳极,该极OH-优先放电得到O。
2
【解析】A.M极消耗O,而N极产生的O 可循环利用,所以X为O,A项正确;
2 2 2
B.M极H+与O 结合消耗导致酸的浓度下降,同时在N极OH-被电解消耗,所以HSO 溶液和NaOH
2 2 4
溶液的浓度均逐渐减小,B项正确;
C.由电子得失守恒mCO ~C (H O) ~mO ,即生成CO 的物质的量等于生成O 的物质的量,C项错
2 m 2 n 2 2 2
误;
D.M极其他还原物质可能消耗O,所以需要适量补充O,D项正确;
2 2
故选C。
20.双极电化学法装置如图所示,是在传统电解装置中放置了导电性电极BPE,通电时,BPE两端界
面产生电势差;生成梯度合金。
下列有关说法正确的是
A.n为电源负极B.在BPE中电子的移动方向由b到c
C.装置c端发生的反应为2HO+2e- =H ↑+ 2OH-
2 2
D.BPE的b端到中心的不同位置能形成组成不同的铜镍合金
【答案】D
【分析】由电解装置图可知,a电极上,水转化为氧气,发生氧化反应,a极阳极,电极反应为:
,则n为电源正极,m为电源负极,则溶液中靠着正极的b端电势高于靠近负极的c
端,则b端得到电子发生还原反应,电极反应为: ,c端失去电子发生氧化
反应,电极反应为: 。
【解析】A.由分析可知,n为电源正极,A项错误;
B.电子由电势低的地方流向电势高的地方,则在BPE中电子的移动方向由c到b,B项错误;
C.由分析可知,装置c端发生的反应为 ,C项错误;
D.BPE的b端到中心的不同位置,由于电势不同,电极反应: 中x不
同,能形成组成不同的铜镍合金由于电势不同,D项正确;答案选D
21.请运用反应热的知识填写下列空白:
(1)已知: (s,白磷)= (s,黑磷) ;
(s,白磷)= (s,红磷) ;
由此推知,其中最稳定的磷单质是 。
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl 气体和H,放出225 kJ热量,该反应的热化学方程
3 2
式为 。
②在 25℃ 和 101kPa时,4 g硫粉在O 中完全燃烧生成SO 气体,放出37 kJ的热量,写出表示S燃
2 2
烧热的热化学方程式: 。
(3)已知上述反应中相关的化学键键能数据如下:
化学键 C-H C=O H-H C O(CO)
键能/kJ·mol−1 413 745 436 1075则该反应的 ΔH = 。
(4)将 氢化为 有三种方法,对应的反应依次为:
①
②
③
反应③的 ΔH = (用ΔH,ΔH 表示)
3 1 2
(5)①2Cu O(s) + O (g) =4CuO(s) ΔH=-277kJ·mol-1
2 2 1
②8CuO(s) + CH (g)=4Cu O(s) + CO (g)+2HO(g) ΔH=-348kJ·mol-1
4 2 2 2 2
反应CH(g) +2O (g)=CO (g)+2HO(g) ΔH= kJ·mol-1
4 2 2 2
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该
反应的热化学方程式 。
【答案】(1)黑磷
(2) S(s) + O (g) = SO (g) ΔH =
2 2
-296 kJ·mol-1
(3)+120 kJ·mol-1
(4)
(5)-902
(6)
【解析】(1)根据热化学方程式可看出白磷转化为黑磷放出的热量更多,能量越低物质越稳定,因此黑磷的能量最低最稳定。
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl 气体和H,放出225 kJ热量,该反应的热化学方
3 2
程式为: ;
②4 g硫粉的物质的量为 =0.125mol,在 25℃ 和 101kPa时,0.125mol硫粉在O 中完全燃烧
2
生成SO 气体,放出37 kJ的热量,则1mol硫粉在O 中完全燃烧生成SO 气体,放出 的热
2 2 2
量,写出表示S燃烧热的热化学方程式为:S(s) + O (g) = SO (g) ΔH = -296 kJ·mol-1。
2 2
(3)ΔH =反应物的键能总和-生成物的键能总和,可得ΔH =(4 413 kJ·mol-1+2 745 kJ·mol-1)-(2 1075
kJ·mol-1+2436 kJ·mol-1) = +120kJ·mol-1。
(4)由盖斯定律可知,反应③=反应②-反应①,则反应③的 ΔH = 。
3
(5)由盖斯定律可知,反应②+2 反应①可得CH(g) +2O (g)=CO (g)+2HO(g) ΔH=ΔH+2 ΔH=-902
4 2 2 2 2 1
kJ·mol-1。
(6)ΔH =生成物的能量-反应物的能量=(b-a) kJ·mol-1,该反应的热化学方程式为:
。
22.原电池电源在生活、生产中的应用非常广泛,根据题意回答下列问题。
(1)某兴趣小组设计如图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极
材料是 (填“锌”或“铜”);溶液中硫酸根向 (填“正极”或“负极”),当正极质量增加
12.8g时,转移了 mol电子。
(2)如图所示,运用原电池原理可将SO 转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和
2
还原反应室,能阻止气体通过而允许H+通过。则电极a是该原电池的 极(填“正”或“负”),b电
极反应式为 ,生产过程中H+向 (填“a”或“b”)电极区域运动。(3)铅酸蓄电池是一种典型的可充电电池,其放电时的电池总反应为:
Pb+PbO+2H SO =2PbSO+2H O。放电时 (化学式)被还原,负极的电极反应式为 ,正极质
2 2 4 4 2
量 (填“增重”或“减轻”“不变”)。
(4)燃料电池应用前景更加广泛,常见的是燃料主要有氢气、可燃有机物等,则燃料在电池 (填
“正极”或“负极”)通入。在碱性溶液燃料电池中氧气参与反应的电极反应式为 ;若用C H 为燃
2 6
料时酸性电解质中负极反应式为 。
【答案】(1)锌 负极 0.4
(2) 负 O+4e-+4H+=2H O b
2 2
(3)PbO Pb-2e-+SO =PbSO 增重
2 4
(4)负极 O+4e-+2H O=4OH- C H-14e-+4H O=2CO+14H+
2 2 2 6 2 2
【解析】(1)该装置为原电池,锌为负极,失电子被氧化,铜为正极,铜离子得电子生成铜,被还
原。溶液中硫酸根移向负极,正极质量增加12.8g时,生成铜的物质的量为: =0.2mol,转移电子
的物质的量为0.4mol;
(2)运用原电池原理可将SO 转化成硫酸,故SO 在负极失电子反应生成硫酸,a极为负极;b极为
2 2
正极,氧气在正极得电子,与氢离子反应生成水,电极反应为:O+4e-+2H O=4OH-,氢离子由左侧移向右
2 2
侧,即向b极区移动。
(3)根据铅酸蓄电池的总反应可判断铅作负极和还原剂,硫酸根与铅离子结合为沉淀,则放电时
PbO 被还原,铅酸蓄电池的负极反应式为Pb-2e-+SO =PbSO,正极反应为PbO +2e-+4H++SO
2 4 2
=PbSO+2H O,则正极质量增加。
4 2
(4)燃料发生氧化反应,在电池负极通入。在碱性溶液燃料电池中氧气发生还原反应,参与反应的
电极反应式为O+4e-+2H O=4OH-;若用C H 为燃料时酸性电解质中负极反应式为C H-14e-
2 2 2 6 2 6+4H O=2CO+14H+。
2 2
23.电化学保护法
金属在发生电化学腐蚀时,总是作为原电池 (阳极)的金属被腐蚀,作为 (阴极)的金属不
被腐蚀,如果能使被保护的金属成为 ,就不易被腐蚀。
(1)牺牲阳极法
原理:原电池原理
要求:被保护的金属作 ,活泼性更强的金属作 。
应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
实例 实验1:
如图装置反应一段时间后,往Fe电极区滴入2滴 色K[Fe(CN) ](铁氰化钾)溶液,观察实验现
3 6
象。
已知Fe2+与[Fe(CN) ]3-反应生成带有特征蓝色的KFe[Fe(CN) ]沉淀。
6 6
实验装置 电流表 阳极(负极区) 阴极(正极区)
现象 指针 Zn溶解 有 产生, 蓝色沉淀生成
Zn-2e-=Zn2
有关反应 — 2H++2e-=H ↑
+ 2
结论 溶液中不含 ,铁作正极未被腐蚀
实例 实验2:
培养皿中放入含有NaCl的琼脂,并注入5~6滴酚酞和K[Fe(CN) ]溶液,取两个2~3 cm的铁钉,用
3 6
砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。实验装
置
现象 铁钉周围 铁钉周围生成 ,铜丝周围
结论 铁作为 时易腐蚀,作为 时未腐蚀
(2)外加电流法
原理:电解池原理
要求:被保护的金属作为 ,与电源的 相连。
应用:钢铁闸门,高压线铁架,地下管道连接直流电源的 。
【答案】负极 正极 阴极 正极 负极 黄 偏转 气泡 无 Fe2+
变红 蓝色沉淀 变红 负极 正极 阴极 负极 负极
【解析】金属在发生电化学腐蚀时,总是作为原电池负极(阳极)的金属被腐蚀,作为正极(阴极)的金属
不被腐蚀,如果能使被保护的金属成为阴极,就不易被腐蚀。
(1)牺牲阳极法,利用的是原电池原理,被保护的金属作正极,活泼性更强的金属作负极。在实验1
中,按如图装置反应一段时间后,往Fe电极区滴入2滴黄色K[Fe(CN) ](铁氰化钾)溶液,观察实验现象。
3 6
可以看到指针发生偏转,Zn溶解,有气泡产生,无蓝色沉淀生成,说明溶液中不含Fe2+,铁作正极未被腐
蚀。在实验2中,实验装置a中观察到铁钉周围变红,实验装置b中观察到铁钉周围生成蓝色沉淀,铜丝
周围变红,实验a和b说明铁作为负极时易腐蚀,作为正极时未腐蚀。
(2)外加电流法,利用的电解池原理,被保护的金属作为阴极,与电源的负极相连。利用该原理,可将
钢铁闸门,高压线铁架,地下管道连接直流电源的负极,将其保护起来防止腐蚀。
24.按照要求回答下列问题:
(1)用NaOH溶液吸收烟气中的SO ,将所得的NaSO 溶液进行电解,可循环再生NaOH,同时得到
2 2 3
HSO ,其原理如图所示(电极材料均为石墨)。
2 4①图中A口产生的气体为 ,B口流出的物质是 。
②b电极表面发生的电极反应式为 。
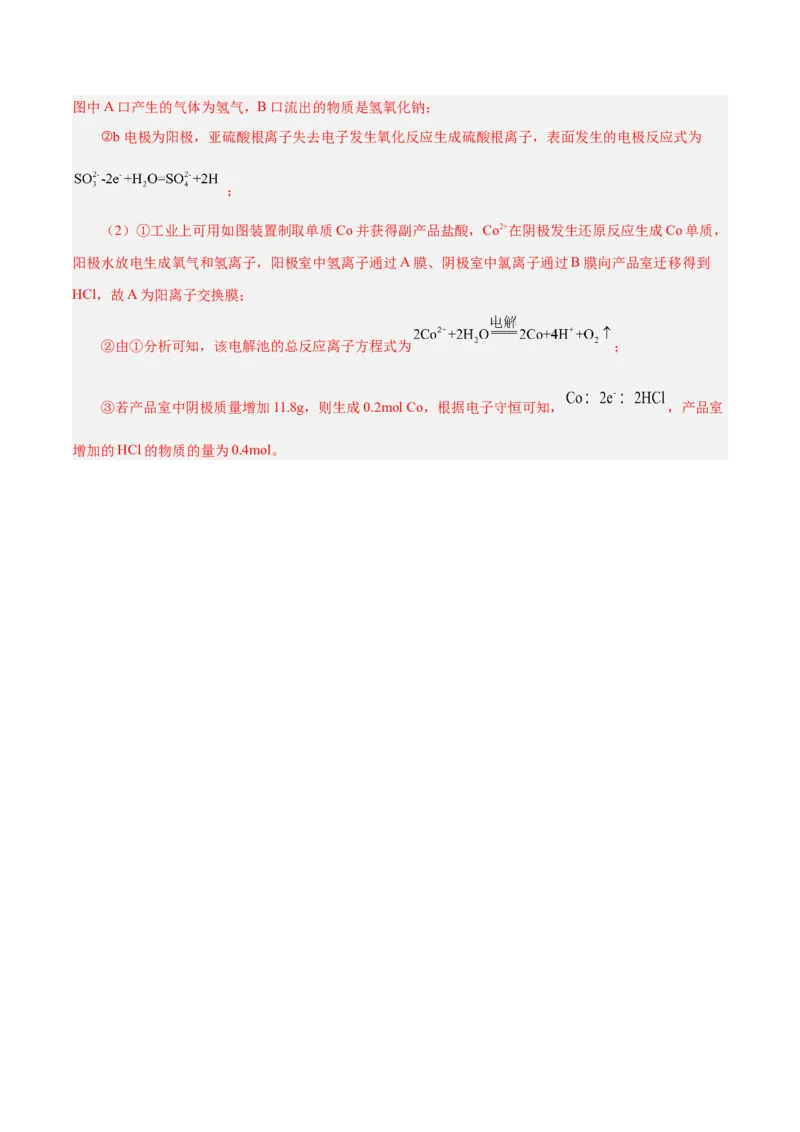
(2)Co是磁性合金的重要材料,也是维生素的重要组成元素。工业上可用如图装置制取单质Co并获得
副产品盐酸(A、B均为离子交换膜)。
①A为 (填“阳”或“阴”)离子交换膜。
②该电解池的总反应离子方程式为 。
③若产品室中阴极质量增加11.8g,则产品室增加的HCl的物质的量为 。
【答案】(1)氢气 氢氧化钠
(2) 阳 0.4mol
【分析】依据电解质溶液中阴阳离子的移动方向判断电极,阳离子移向阴极,a为阴极,b为阳极,
在阳极失去电子变成 ,可能伴有氢氧根离子放电生成氧气,所以C口流出的物质是HSO ,阴极
2 4
区放电离子为氢离子生成氢气;由图可知,Co为阴极,电极反应式为Co2++2e-=Co,石墨为阳极,电极反
应式为2HO-4e-=O ↑+4H+,据此作答。
2 2
【解析】(1)①电解池中阳离子向阴极移动,由图可知,a为阴极,水放电生成氢气和氢氧根离子,图中A口产生的气体为氢气,B口流出的物质是氢氧化钠;
②b电极为阳极,亚硫酸根离子失去电子发生氧化反应生成硫酸根离子,表面发生的电极反应式为
;
(2)①工业上可用如图装置制取单质Co并获得副产品盐酸,Co2+在阴极发生还原反应生成Co单质,
阳极水放电生成氧气和氢离子,阳极室中氢离子通过A膜、阴极室中氯离子通过B膜向产品室迁移得到
HCl,故A为阳离子交换膜;
②由①分析可知,该电解池的总反应离子方程式为 ;
③若产品室中阴极质量增加11.8g,则生成0.2mol Co,根据电子守恒可知, ,产品室
增加的HCl的物质的量为0.4mol。