文档内容
章末综合检测(四) 非金属及其化合物
一、选择题:本题包括10小题,每小题只有一个选项最符合题意。
1.(2021·安徽蚌埠质检)化学反应的原理应用在疫情防控中发挥着重要作用,下列说法
不正确的是( )
A.二氧化氯可用于自来水消毒
B.碘酒中的碘因有还原性而起到杀菌消毒作用
C.医用防护口罩的材料之一是聚丙烯,聚丙烯属于高分子材料
D.84消毒液和酒精混合消毒作用减弱,可能发生了复杂的化学反应
B [ClO 具有强氧化性,可使细菌体内蛋白质发生变性,可用于自来水消毒,A项正确;
2
碘酒中I 具有氧化性,起到杀菌消毒作用,B项错误;聚丙烯是丙烯发生加聚反应生成的高分
2
子材料,C项正确;84消毒液中NaClO具有强氧化性,乙醇具有还原性,混合使用发生复杂
反应,消毒作用减弱,D项正确。]
2.(2021·山西大同调研)下列所示的物质间转化在给定条件下均能实现的是( )
A.NaBr (aq)――→Br (aq)――→I(aq)
2 2
B.NaCl (aq)――→Cl(g)――→漂白粉(s)
2
C.FeS――→SO ――→HSO
2 2 2 4
D.SiO――→HSiO―——―→NaSiO
2 2 3 2 3
A [将Cl 通入石灰乳中制取漂白粉,不能使用石灰水,B项错误;SO 与水反应生成
2 2
HSO ,C项错误;SiO 不溶于水,也不能与水发生反应,D项错误。]
2 3 2
3.(2021·江西奉新一中检测)下列关于实验室制取Cl 的说法正确的是( )
2
A.将混有HCl杂质的Cl 通过盛有饱和NaHCO 溶液的洗气瓶除去杂质
2 3
B.实验室制取Cl,浓盐酸起到酸性和氧化剂作用
2
C.实验室用如图装置除去Cl 中的少量HCl
2
D.实验室制备Cl,可用排饱和食盐水集气法收集
2
D [HCl与饱和NaHCO 溶液反应生成CO ,应通过盛有饱和食盐水的洗气瓶除杂,A
3 2
项错误;利用MnO 和浓盐酸制取Cl,浓盐酸起到酸性和还原剂作用,B项错误;除去Cl 中
2 2 2
的少量HCl,应将混合气体从长管通过盛有饱和食盐水的洗气瓶,C项错误;Cl 不易溶于饱
2
和食盐水,故实验室可采用排饱和食盐水的方法收集Cl,D项正确。]
2
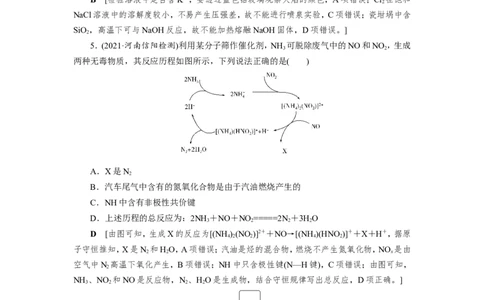
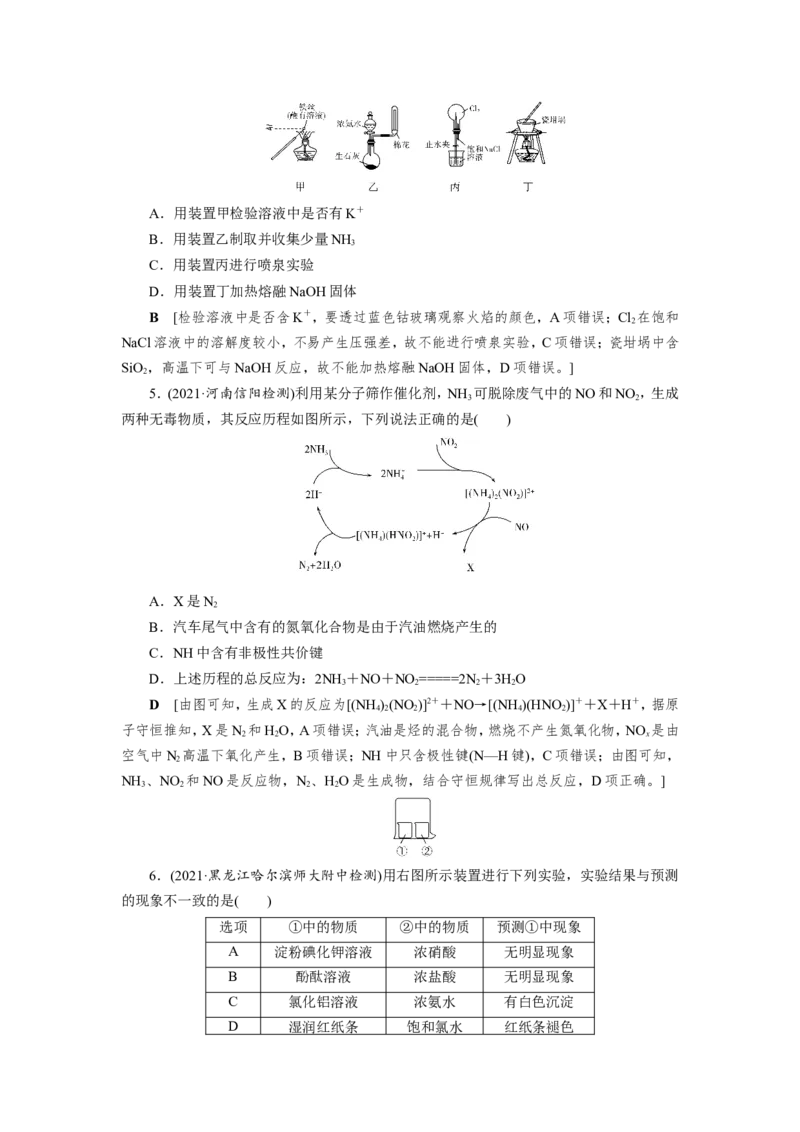
4.(2021·安徽师大附中检测)用下列实验装置进行相应实验,能达到实验目的的是(夹持
装置未画出)( )A.用装置甲检验溶液中是否有K+
B.用装置乙制取并收集少量NH
3
C.用装置丙进行喷泉实验
D.用装置丁加热熔融NaOH固体
B [检验溶液中是否含K+,要透过蓝色钴玻璃观察火焰的颜色,A项错误;Cl 在饱和
2
NaCl溶液中的溶解度较小,不易产生压强差,故不能进行喷泉实验,C项错误;瓷坩埚中含
SiO,高温下可与NaOH反应,故不能加热熔融NaOH固体,D项错误。]
2
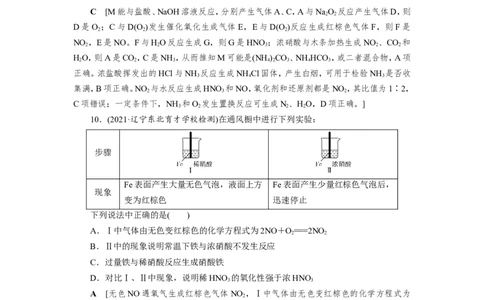
5.(2021·河南信阳检测)利用某分子筛作催化剂,NH 可脱除废气中的NO和NO ,生成
3 2
两种无毒物质,其反应历程如图所示,下列说法正确的是( )
A.X是N
2
B.汽车尾气中含有的氮氧化合物是由于汽油燃烧产生的
C.NH中含有非极性共价键
D.上述历程的总反应为:2NH +NO+NO =====2N+3HO
3 2 2 2
D [由图可知,生成X的反应为[(NH )(NO )]2++NO→[(NH )(HNO)]++X+H+,据原
4 2 2 4 2
子守恒推知,X是N 和HO,A项错误;汽油是烃的混合物,燃烧不产生氮氧化物,NO 是由
2 2 x
空气中N 高温下氧化产生,B项错误;NH中只含极性键(N—H键),C项错误;由图可知,
2
NH 、NO 和NO是反应物,N、HO是生成物,结合守恒规律写出总反应,D项正确。]
3 2 2 2
6.(2021·黑龙江哈尔滨师大附中检测)用右图所示装置进行下列实验,实验结果与预测
的现象不一致的是( )
选项 ①中的物质 ②中的物质 预测①中现象
A 淀粉碘化钾溶液 浓硝酸 无明显现象
B 酚酞溶液 浓盐酸 无明显现象
C 氯化铝溶液 浓氨水 有白色沉淀
D 湿润红纸条 饱和氯水 红纸条褪色A [浓硝酸挥发出的HNO 进入①中淀粉KI溶液,将I-氧化为I 而使溶液变蓝,A项错
3 2
误;浓盐酸挥发出HCl进入酚酞溶液,溶液不变色,B项正确;浓氨水挥发出NH 进入氯化铝
3
溶液,反应生成Al(OH) 白色沉淀,C项正确;饱和氯水挥发出Cl 溶于湿润红纸条中,并与水
3 2
反应生成HCl、HClO,HClO使红纸条漂白褪色,D项正确。]
7.(2020·山东枣庄二模)防治污染要坚决打好蓝天、碧水、净土三大保卫战。某工厂拟综
合处理含NH废水和工业废气(主要含N、CO、SO 、NO、CO,不考虑其他成分),设计了如下
2 2 2
流程:
下列说法正确的是( )
A.固体1的成分是CaCO 、CaSO
3 3
B.向气体1中通入的空气可以过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH废水时,发生的反应为NH+5NO+4H+===6NO↑+4HO
2
C [工业废气通过过量石灰乳,故固体1的成分是CaCO 、CaSO 及过量的Ca(OH) ,A
3 3 2
项错误;向气体1中通入空气不能过量,否则生成NO,B项错误;气体2是CO和N 混合气
2
体,N 是无污染气体,故捕获剂所捕获的是CO,C项正确;处理含NH废水时,NH与NO反
2
应生成N,D项错误。]
2
8.(2020·河南部分重点校联考)氮化铬(CrN)常用作薄膜涂层。实验室制备氮化铬的反应
原理为CrCl +NH =====CrN+3HCl,装置如图所示(注:没食子酸可以吸收少量氧气):
3 3
下列说法正确的是( )
A.装置①中的生石灰可以换成浓硫酸
B.装置⑤中产生的尾气冷却后有固体生成
C.装置④中的药品为无水氯化钙
D.装置③的作用是去除氧气,可将NaSO 固体换为没食子酸溶液
2 3
B [装置①用于产生NH ,浓氨水滴入浓硫酸中生成(NH )SO ,不能产生NH ,A项错
3 4 2 4 3
误;⑤的尾气中含有生成的HCl和未反应的NH ,冷却后可生成NH Cl固体,B项正确;无水
3 4
氯化钙可与NH 生成CaCl ·8NH ,不能用于干燥NH ,C项错误;装置③中盛有没食子酸溶
3 2 3 3
液,气体无法通过,D项错误。]
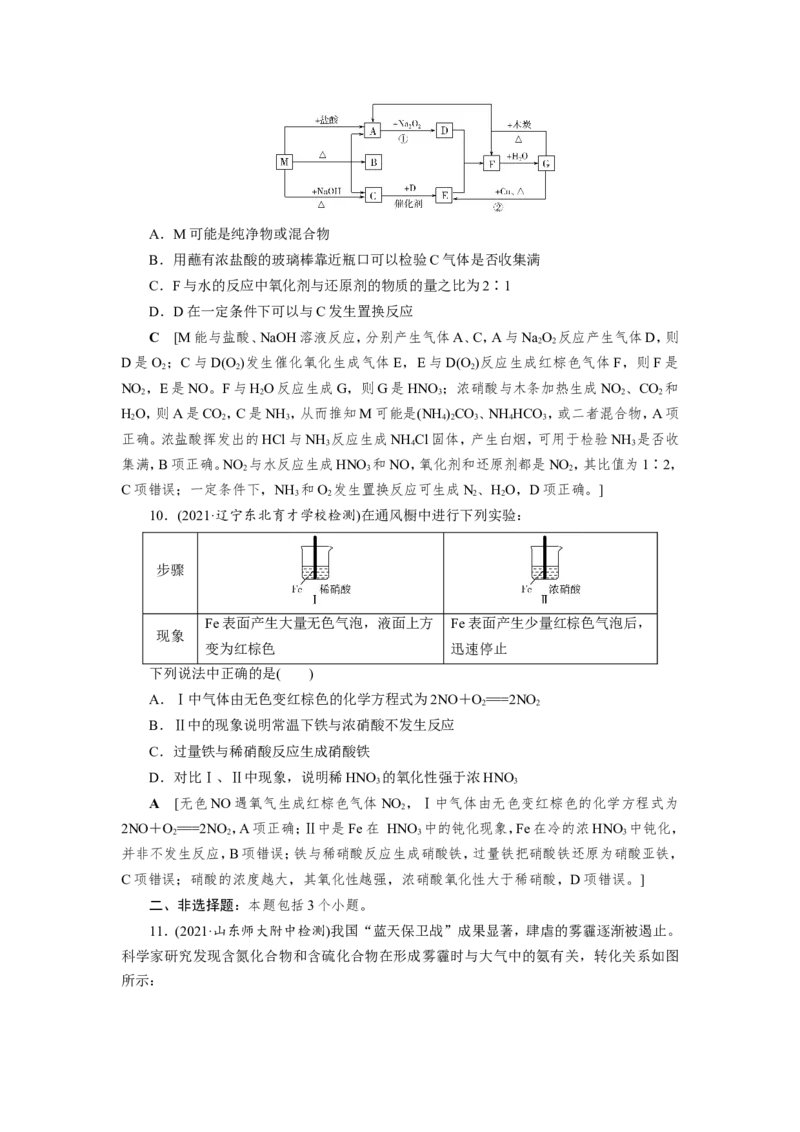
9.(2021·广西南宁二中检测)下图的每一方格中表示有关的一种反应物或生成物,其中
A、C、D、E为无色气体,F为红棕色气体。下列说法不正确的是( )A.M可能是纯净物或混合物
B.用蘸有浓盐酸的玻璃棒靠近瓶口可以检验C气体是否收集满
C.F与水的反应中氧化剂与还原剂的物质的量之比为2∶1
D.D在一定条件下可以与C发生置换反应
C [M能与盐酸、NaOH溶液反应,分别产生气体A、C,A与NaO 反应产生气体D,则
2 2
D是O ;C与D(O )发生催化氧化生成气体E,E与D(O )反应生成红棕色气体F,则F是
2 2 2
NO ,E是NO。F与HO反应生成G,则G是HNO;浓硝酸与木条加热生成NO 、CO 和
2 2 3 2 2
HO,则A是CO,C是NH ,从而推知M可能是(NH )CO、NH HCO ,或二者混合物,A项
2 2 3 4 2 3 4 3
正确。浓盐酸挥发出的HCl与NH 反应生成NH Cl固体,产生白烟,可用于检验NH 是否收
3 4 3
集满,B项正确。NO 与水反应生成HNO 和NO,氧化剂和还原剂都是NO ,其比值为1∶2,
2 3 2
C项错误;一定条件下,NH 和O 发生置换反应可生成N、HO,D项正确。]
3 2 2 2
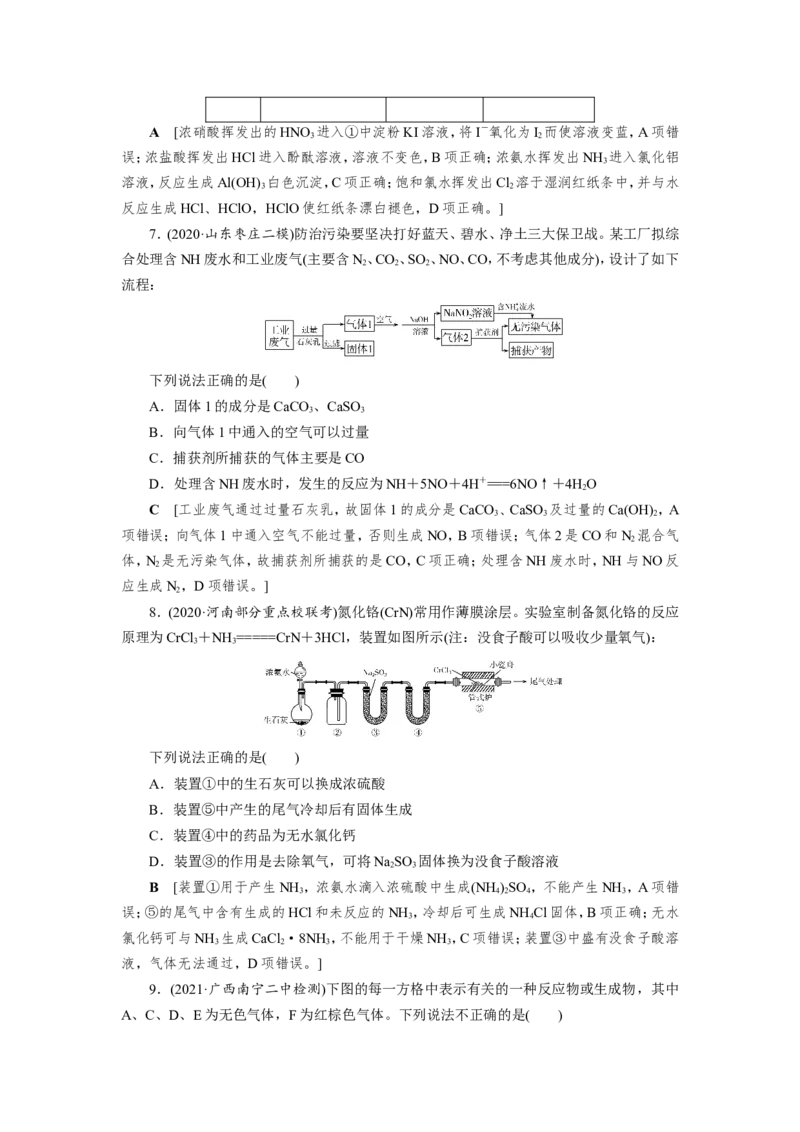
10.(2021·辽宁东北育才学校检测)在通风橱中进行下列实验:
步骤
Fe表面产生大量无色气泡,液面上方 Fe表面产生少量红棕色气泡后,
现象
变为红棕色 迅速停止
下列说法中正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式为2NO+O===2NO
2 2
B.Ⅱ中的现象说明常温下铁与浓硝酸不发生反应
C.过量铁与稀硝酸反应生成硝酸铁
D.对比Ⅰ、Ⅱ中现象,说明稀HNO 的氧化性强于浓HNO
3 3
A [无色NO遇氧气生成红棕色气体NO ,Ⅰ中气体由无色变红棕色的化学方程式为
2
2NO+O===2NO,A项正确;Ⅱ中是Fe 在 HNO 中的钝化现象,Fe在冷的浓HNO 中钝化,
2 2 3 3
并非不发生反应,B项错误;铁与稀硝酸反应生成硝酸铁,过量铁把硝酸铁还原为硝酸亚铁,
C项错误;硝酸的浓度越大,其氧化性越强,浓硝酸氧化性大于稀硝酸,D项错误。]
二、非选择题:本题包括3个小题。
11.(2021·山东师大附中检测)我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。
科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图
所示:回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有________________(写化学式)。
(2)图中物质溶于水溶液呈碱性的是________。
(3)写出SO 转化为SO 的化学方程式_________________________________________。
2 3
(4)工业上利用氨气制备一氧化氮,反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(5)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为
________________________________________________________________________
(用化学方程式表示)。
(6)氨气与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学
方程式为________________________________________________。
解析 (1)酸性氧化物是指与碱反应只生成一种盐和水的氧化物,SO 、SO 和NO 都是
2 3 2 5
酸性氧化物。
(4)NH 在催化剂作用下被O 氧化生成NO和HO,结合得失电子守恒和原子守恒写出
3 2 2
化学方程式。
(6)氨气与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,结合原子守恒
推知,产物为N 和HO,结合得失电子守恒和原子守恒写出化学方程式。
2 2
答案 (1)N O、SO 、SO
2 5 2 3
(2)NH
3
(3)2SO +O 2SO
2 2 3
(4)4NH +5O=====4NO+6HO
3 2 2
(5)4HNO=====4NO ↑+O↑+2HO
3 2 2 2
(6)4NH +6NO=====5N+6HO
3 2 2
12.(2021·天津滨海新区四校联考)利用元素的化合价推测物质的性质是化学研究的重
要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的________性。
(2) 从 硫 元 素 化 合 价 变 化 的 角 度 分 析 , 图 中 只 有 还 原 性 的 物 质 有
____________________(填化学式)。
(3)将HS与SO 混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之
2 2
比为________。
(4)配平下列反应:
NaS+____NaSO +____HSO ===____NaSO +____S↓+____HO
2 2 3 2 4 2 4 2
(5)如图是验证SO 性质的实验装置。
2
Ⅰ.二氧化硫具有:①漂白性、②酸性氧化物性质、③还原性、④氧化性,上述装置中对应
表现出的性质是:A中________(填序号,下同);B中________;C中________。
Ⅱ.D装置的作用是_________________________________________________________。
解析 (1)X是HSO ,浓硫酸与碳在加热时反应生成SO 、CO 和HO,浓硫酸体现其强
2 4 2 2 2
氧化性。
(2)S元素显-2价时,含硫物质只具有还原性,如HS、NaS等。
2 2
(4)Na S中-2价S被氧化为0价,NaSO 中+4价S被还原为0价,HSO 中S元素未变
2 2 3 2 4
价,根据得失电子守恒和原子守恒配平可得:2NaS+NaSO +3HSO ===3Na SO +3S↓+
2 2 3 2 4 2 4
3HO。
2
答案 (1)强氧化 (2)H S、NaS
2 2
(3)2∶1 (4)2 1 3 3 3 3
(5)Ⅰ.② ① ③ Ⅱ.吸收SO 尾气,防止污染空气
2
13.(2021·河北衡水中学调研)人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提
高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)将N 转化为含氮化合物的过程称为氮的固定。
2
①人工固氮,将N→NH N 发生________反应。
2 3, 2
②自然界固氮,可将少量N 转化为Ca(NO ) 等氮肥,转化途径如下(转化所需试剂及条
2 3 2件已略去):
N―→NO―→NO ―→HNO――→Ca(NO )
2 2 3 3 2
写出NO→NO →HNO 的化学方程式__________________________________________、
2 3
____________________________________________。
将 HNO 转 化 为 Ca(NO ) , 列 举 三 种 不 同 类 别 的 化 合 物
3 3 2
M________________________________________(写化学式)。
(2)科学合理地保存、施用氮肥
①NH HCO 需阴凉处保存,原因是__________________________(写化学方程式)。
4 3
②铵态氮肥不能与碱性肥料混合使用,以NH Cl为例写出发生反应的离子方程式
4
________________________________________________________________________。
(3)过度施用氮肥将导致大气中NH 含量增高,加剧雾霾的形成。(NH )SO 是雾霾的成
3 4 2 4
分之一,其形成过程如下图所示(转化所需试剂及条件已略去):
①X可能是________________。 Y是________。
②尿素CO(NH) 是一种常用化肥,缓慢与HO发生非氧化还原反应释放出NH 则尿素
2 2 2 3
中C元素化合价为
____________。
解析 (1)②NO被O 氧化为NO ,NO 与HO反应生成HNO ;HNO 与Ca、 CaO、
2 2 2 2 3 3
Ca(OH) 、CaCO 等反应生成Ca(NO )。
2 3 3 2
(2)② 铵态氮肥不能与碱性肥料混合使用,混合施用时,NH 与 OH-反应生成
NH ·HO,会释放出NH ,降低肥效。
3 2 3
(3)①燃料燃烧产生SO ,SO 与水反应生成HSO ,HSO 被氧化生成HSO ,HSO 与
2 2 2 3 2 3 2 4 2 4
NH 反应生成(NH )SO 。
3 4 2 4
② 尿素CO(NH) 是一种常用化肥,缓慢与HO发生非氧化还原反应释放出NH ,则尿
2 2 2 3
素中O、N和H元素的化合价分别为-2、-3和+1,根据各元素化合价代数和为0推知,尿
素中C元素的化合价为+4。
答案 (1)①还原
②2NO+O=== 2 NO 3NO +HO === 2HNO+NO Ca、CaO、Ca(OH) 、CaCO
2 2 2 2 3 2 3
(2)①NH HCO =====NH ↑ + CO↑ + HO ② NH + OH - ===NH↑ + HO( 或
4 3 3 2 2 3 2
NH ·H O)
3 2
(3)①SO 、HSO HSO ②+4
3 2 3 2 4