文档内容
专题讲座(三)
1.X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示。下列说法正确的是( )
A.Y、Z、X三种元素的原子半径依次增大
B.X、Z都是第二周期ⅥA族元素,单质的氧化性:X>Z
C.Y的气态氢化物的热稳定性比Z的强
D.R元素与W同族且相邻周期,则R元素最高价氧化物对应的水化物的酸性比Z的强
2.A、B、C、D、E五种短周期主族元素,原子序数依次增大。A元素的一种核素质子数与质量数在数
值上相等;B的单质分子中有三对共用电子;C、D同主族,且核电荷数之比为1∶2。下列有关说法不正确
的是( )
A.C、D、E的简单离子半径:D>E>C
B.A与B、C、D、E四种元素均可形成18电子分子
C.由A、B、C三种元素形成的化合物均能促进水的电离
D.分子DE 中原子均满足8电子稳定结构,则分子中存在非极性键
2 2
3.短周期主族元素X、Y、Z最外层电子数之和为11,它们在元素周期表中的相对位置如图所示,
下列关于X、Y、Z元素的说法正确的是( )
X
Y Z
A.X、Z的最高价氧化物的性质相同
B.原子半径的大小顺序为X<Y<Z
C.元素X的最高价氧化物对应水化物的酸性比Z的弱
D.Y单质与氢氧化钠溶液或盐酸反应都能产生气体
4.已知W、X、Y、Z为原子序数依次增大的四种短周期元素。W、Z同主族,X、Y、Z同周期,其中
只有X为金属元素,Z元素原子的最外层电子数是其电子层数的2倍。下列说法不正确的是( )
A.原子半径:X>Y>Z>W
B.X与W形成化合物与稀盐酸反应不可能产生氧气
C.Y与W形成化合物能与NaOH溶液反应D.简单氢化物的稳定性:W>Z>Y
5.几种短周期元素的原子半径及主要化合价见下表:
元素代号 K L M Q R T N
原子半径/nm 0.186 0.160 0.143 0.106 0.111 0.066 0.152
主要化合价 +1 +2 +3 +6、-2 +2 -2 +1
下列叙述正确的是( )
A.K、L、M三种元素的金属性逐渐增强
B.在RCl 分子中,各原子均满足8电子稳定结构
2
C.Q元素的最高价氧化物为电解质,其水溶液能够导电
D.K在T单质中燃烧所生成的化合物是淡黄色的NaO 固体
2 2
6.短周期主族元素W、X、Y、Z的原子序数依次增大。X和Z形成的化合物的水溶液呈中性,W和 X
的最外层电子数之和等于Z的最外层电子数,Y的原子序数是W的2倍。YWZ 滴入水中,可观察剧烈反
2
应,液面上有雾生成,并有带刺激性气味的气体逸出。下列说法正确的是( )
A.原子半径:W<X<Y<Z
B.W分别与X、Z均只能形成一种二元化合物
C.W、Y、Z的最简单氢化物中,Z的氢化物沸点最高
D.YWZ 滴入水时,逸出的气体能使品红褪色
2
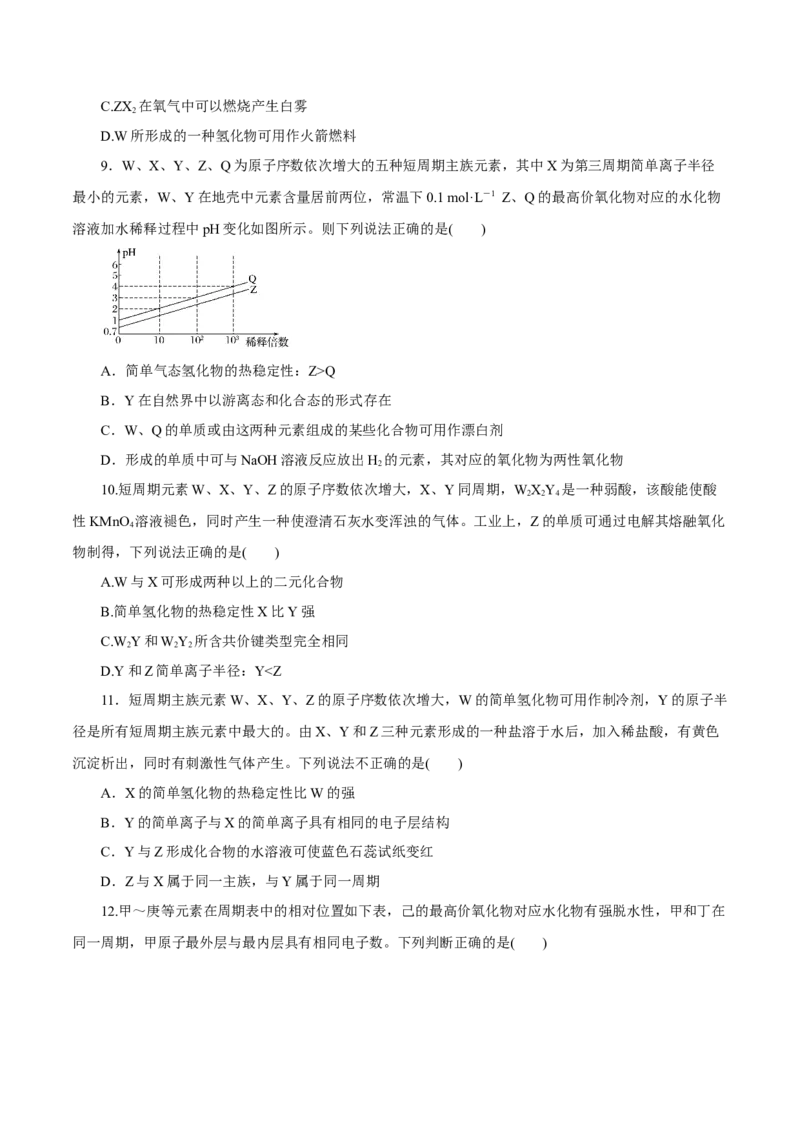
7.X、Y、Z、M、R、Q为六种短周期元素,其原子半径和最外层电子数之间的关系如图所示,下列
说法正确的是( )
A.R离子的半径大于M离子的半径
B.Q的单质与Y的氧化物之间可能发生置换反应
C.X与M可形成XM 型离子化合物
2 2
D.X与Y形成化合物的沸点一定低于X与Z所形成的化合物
8.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可与其最高价氧化物的水化物
反应生成盐,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的某一种盐加入
稀盐酸后,有黄色沉淀析出,同时有刺激性气味气体产生。下列说法正确的是( )
A.W、X、Y、Z的简单离子的半径依次增大
B.简单氢化物的热稳定性:X<WC.ZX 在氧气中可以燃烧产生白雾
2
D.W所形成的一种氢化物可用作火箭燃料
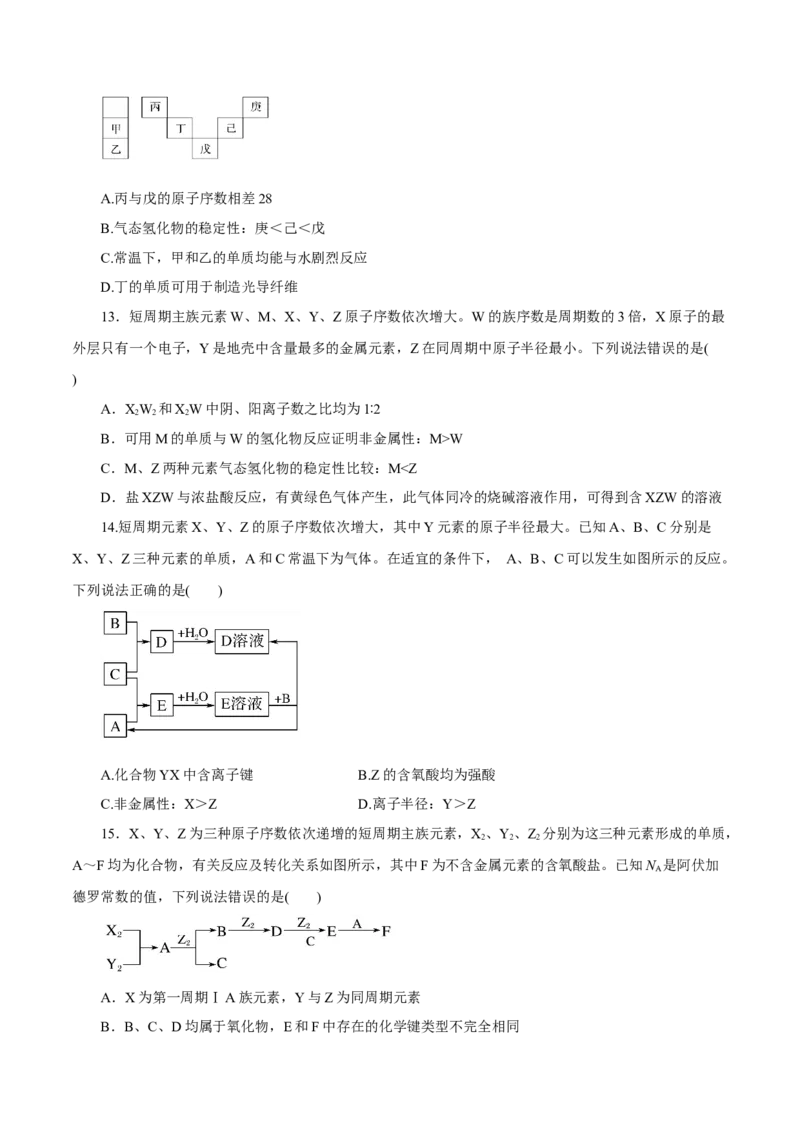
9.W、X、Y、Z、Q为原子序数依次增大的五种短周期主族元素,其中X为第三周期简单离子半径
最小的元素,W、Y在地壳中元素含量居前两位,常温下0.1 mol·L-1 Z、Q的最高价氧化物对应的水化物
溶液加水稀释过程中pH变化如图所示。则下列说法正确的是( )
A.简单气态氢化物的热稳定性:Z>Q
B.Y在自然界中以游离态和化合态的形式存在
C.W、Q的单质或由这两种元素组成的某些化合物可用作漂白剂
D.形成的单质中可与NaOH溶液反应放出H 的元素,其对应的氧化物为两性氧化物
2
10.短周期元素W、X、Y、Z的原子序数依次增大,X、Y同周期,WXY 是一种弱酸,该酸能使酸
2 2 4
性KMnO 溶液褪色,同时产生一种使澄清石灰水变浑浊的气体。工业上,Z的单质可通过电解其熔融氧化
4
物制得,下列说法正确的是( )
A.W与X可形成两种以上的二元化合物
B.简单氢化物的热稳定性X比Y强
C.W Y和WY 所含共价键类型完全相同
2 2 2
D.Y和Z简单离子半径:YW
C.M、Z两种元素气态氢化物的稳定性比较:MX>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
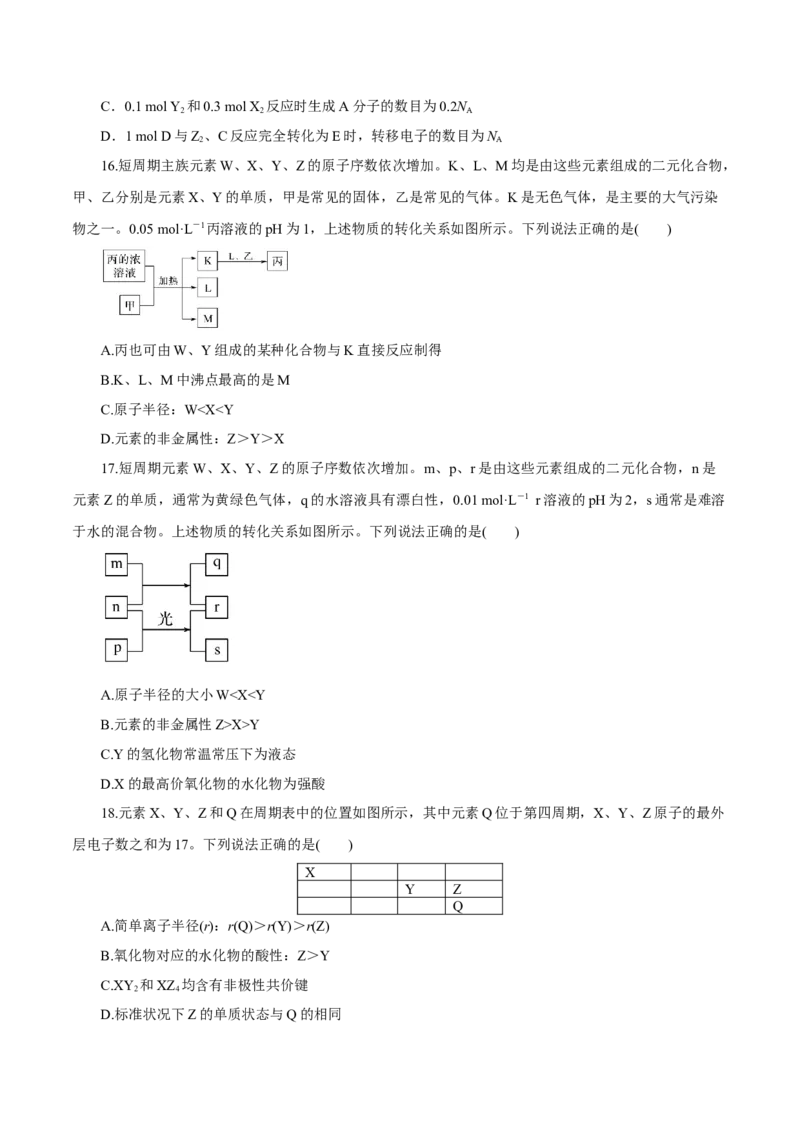
18.元素X、Y、Z和Q在周期表中的位置如图所示,其中元素Q位于第四周期,X、Y、Z原子的最外
层电子数之和为17。下列说法正确的是( )
X
Y Z
Q
A.简单离子半径(r):r(Q)>r(Y)>r(Z)
B.氧化物对应的水化物的酸性:Z>Y
C.XY 和XZ 均含有非极性共价键
2 4
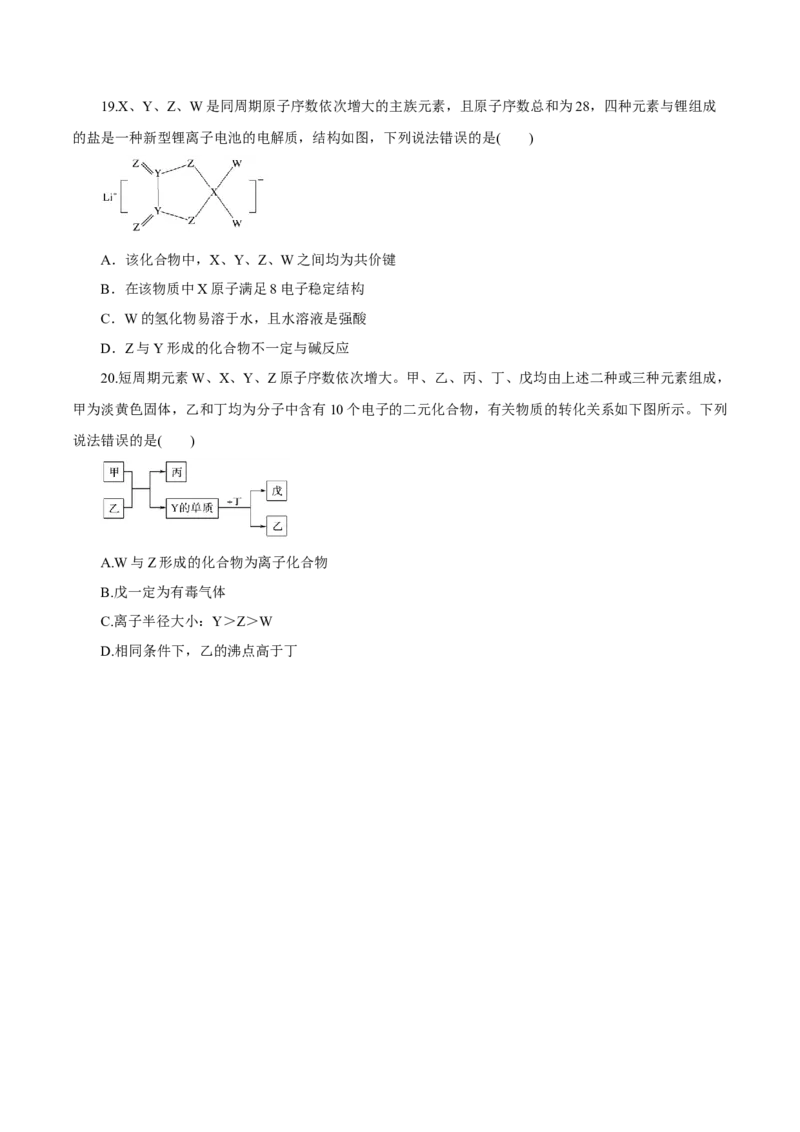
D.标准状况下Z的单质状态与Q的相同19.X、Y、Z、W是同周期原子序数依次增大的主族元素,且原子序数总和为28,四种元素与锂组成
的盐是一种新型锂离子电池的电解质,结构如图,下列说法错误的是( )
A.该化合物中,X、Y、Z、W之间均为共价键
B.在该物质中X原子满足8电子稳定结构
C.W的氢化物易溶于水,且水溶液是强酸
D.Z与Y形成的化合物不一定与碱反应
20.短周期元素W、X、Y、Z原子序数依次增大。甲、乙、丙、丁、戊均由上述二种或三种元素组成,
甲为淡黄色固体,乙和丁均为分子中含有10个电子的二元化合物,有关物质的转化关系如下图所示。下列
说法错误的是( )
A.W与Z形成的化合物为离子化合物
B.戊一定为有毒气体
C.离子半径大小:Y>Z>W
D.相同条件下,乙的沸点高于丁