文档内容
专题讲座(二)阿伏加德罗常数的突破
【化学学科素养】
1.宏观辨识与微观探析:认识阿伏加德罗常数是联系宏观物质和微观粒子的重要工具,能从宏观和微
观相结合的视角分析与解决实际问题。
2.证据推理与模型认知:在有关物质的最计算过程中,通过分析、推理等理解计算的方法,建立阿伏
加德罗常数、气体摩尔体积等题目解答的模型。
【必备知识解读】
一、阿伏加德罗常数的综合应用
1.气体摩尔体积的适用条件:考查气体时经常给定非标准状况下,如25℃、1.01×105 Pa气体体积,
让考生用22.4 L·mol-1进行换算,误入陷阱。
2.物质的聚集状态:22.4 L·mol-1适用对象是气体(包括混合气体)。命题者常用在标准状况下呈非气
态的物质来迷惑考生,如HO、CCl 、SO 、苯、己烷、CS、乙醇、单质硫、石墨等。
2 4 3 2
3.物质的组成、结构:气体单质的组成除常见的双原子分子外,还有单原子分子(如He、Ne等)、三
原子分子(如O)等。NO 和NO,的最简式相同,根据质量计算它们的混合物中元素的原子个数时,可将
3 2 2 4
最简式看作是混合物的分子式来计算。NaO 由Na+和O构成,而不是Na+和O2-,苯中不含碳碳单键和碳
2 2
碳双键等。
4.物质中的化学键数目:如白磷(31 g白磷含1.5 mol P—P键)、金刚石(12 g金刚石含2 mol C—C键)、
晶体硅及晶体SiO(60 g二氧化硅晶体含4 mol Si—O键)等。
2
5.混淆某些氧化还原反应中电子转移的数目:命题者常用一些反应中转移电子的数目来迷惑考生,
如NaO 与HO、CO 的反应(1 mol Na O 反应转移1 mol电子);Cl 与HO、NaOH的反应(1 mol Cl 反应转
2 2 2 2 2 2 2 2 2
移1 mol电子);Cu与硫的反应(1 mol Cu反应转移1 mol电子或1 mol S反应转移2 mol电子)等。
6.特殊物质的摩尔质量及微粒数目:如DO、18O、H37Cl等。
2 2
7.电解质溶液中因微粒的电离或水解造成微粒数目的变化:如强电解质HCl、HNO 等完全电离,不
3
存在电解质分子;弱电解质CHCOOH、HClO等部分电离,而使溶液中CHCOOH、HClO浓度减小;Fe3
3 3
+、Al3+、CO、CHOO-等因发生水解使该种粒子数目减少;Fe3+、Al3+、CO等因发生水解而使溶液中阳
3
离子或阴离子总数增多等。
8.胶体粒子的组成:如1 mol Fe3+形成Fe(OH) 胶体时,由于Fe(OH) 胶粒是小分子聚集体,胶粒数
3 3
目小于N 。
A
9.忽视可逆反应不能进行到底:如2NO NO、2SO +O 2SO 、合成氨反应等。
2 2 4 2 2 3
10.不仔细审题:如只给出物质的量浓度即要求计算微粒数目,考生往往按1 L溶液进行计算,从而落入圈套。
二、阿伏加德罗常数的易错分析
1.辨“两状”,突破气体与状况陷阱
2. 排“干扰”,突破质量(或物质的量)与状况无关陷阱
给出非标准状况下气体的物质的量或质量,干扰正确判断,误以为无法求解物质所含的粒子数,实际
上此时物质所含的粒子数与温度、压强等外界条件无关。
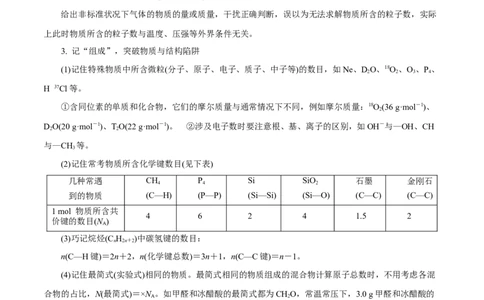
3. 记“组成”,突破物质与结构陷阱
(1)记住特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O、O、P、
2 2 3 4
H 37Cl等。
①含同位素的单质和化合物,它们的摩尔质量与通常情况下不同,例如摩尔质量:18O(36 g·mol-1)、
2
DO(20 g·mol-1)、TO(22 g·mol-1)。 ②涉及电子数时要注意根、基、离子的区别,如OH-与—OH、CH
2 2
与—CH 等。
3
(2)记住常考物质所含化学键数目(见下表)
几种常遇 CH P Si SiO 石墨 金刚石
4 4 2
到的物质 (C—H) (P—P) (Si—Si) (Si—O) (C—C) (C—C)
1 mol 物质所含共
4 6 2 4 1.5 2
价键的数目(N )
A
(3)巧记烷烃(C H )中碳氢键的数目:
n 2n+2
n(C—H键)=2n+2,n(化学键总数)=3n+1,n(C—C键)=n-1。
(4)记住最简式(实验式)相同的物质。最简式相同的物质组成的混合物计算原子总数时,不用考虑各混
合物的占比,N(最简式)=×N 。如甲醛和冰醋酸的最简式都为CHO,常温常压下,3.0 g甲醛和冰醋酸的
A 2
混合物中含有的N(CHO)为0.1N ,则含有的原子总数为0.4N 。
2 A A
(5)记住摩尔质量相同的物质,如N、CO和C H,其摩尔质量均为28 g·mol-1,其它的还有KCl与
2 2 4
NaClO、NaO 与NaS、CaCO 与MgN 等。
2 2 2 3 3 2
4.审“组成”“体积”因素,突破电解质溶液中粒子数目陷阱
(1)是否有弱电解质电离。
(2)是否有离子水解。
(3)是否指明了溶液的体积。(4)不要忽略溶剂水中H、O原子数目。
(5)Fe(OH) 胶体粒子数目小于形成胶体的Fe3+数目。
3
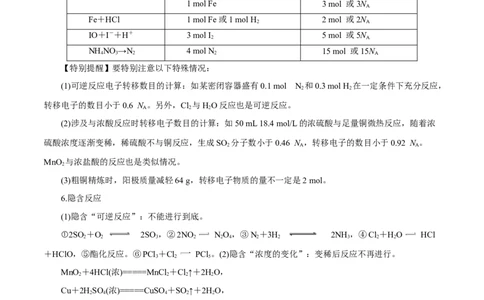
5.突破氧化还原反应中电子转移数目的判断
反应 参加反应的物质或生成的物质 转移电子的物质的量或数目
1 mol Na O 1 mol 或N
2 2 A
NaO+CO(或HO)
2 2 2 2
1 mol O 2 mol 或2N
2 A
Cl+NaOH 1 mol Cl 1 mol 或N
2 2 A
1 mol Cl 2 mol 或2N
2 A
Cl+Fe
2
1 mol Fe 3 mol 或3N
A
Fe+HCl 1 mol Fe或1 mol H 2 mol 或2N
2 A
IO+I-+H+ 3 mol I 5 mol 或5N
2 A
NH NO →N 4 mol N 15 mol 或15N
4 3 2 2 A
【特别提醒】要特别注意以下特殊情况:
(1)可逆反应电子转移数目的计算:如某密闭容器盛有0.1 mol N 和0.3 mol H 在一定条件下充分反应,
2 2
转移电子的数目小于0.6 N 。另外,Cl 与HO反应也是可逆反应。
A 2 2
(2)涉及与浓酸反应时转移电子数目的计算:如50 mL 18.4 mol/L的浓硫酸与足量铜微热反应,随着浓
硫酸浓度逐渐变稀,稀硫酸不与铜反应,生成SO 分子数小于0.46 N ,转移电子的数目小于0.92 N 。
2 A A
MnO 与浓盐酸的反应也是类似情况。
2
(3)粗铜精炼时,阳极质量减轻64 g,转移电子物质的量不一定是2 mol。
6.隐含反应
(1)隐含“可逆反应”:不能进行到底。
①2SO +O 2SO ,②2NO NO,③N+3H 2NH ,④Cl+HO HCl
2 2 3 2 2 4 2 2 3 2 2
+HClO,⑤酯化反应。⑥PCl +Cl PCl 。(2)隐含“浓度的变化”:变稀后反应不再进行。
3 2 5
MnO +4HCl(浓)=====MnCl +Cl↑+2HO,
2 2 2 2
Cu+2HSO (浓)=====CuSO +SO ↑+2HO,
2 4 4 2 2
C+4HNO(浓)=====CO↑+4NO ↑+2HO。
3 2 2 2
(3)隐含“钝化”。
常温下,铁、铝遇浓硫酸、浓硝酸发生“钝化”。
(4)隐含“副反应”。
甲烷在光照条件下与氯气反应,可生成多种卤代烃。
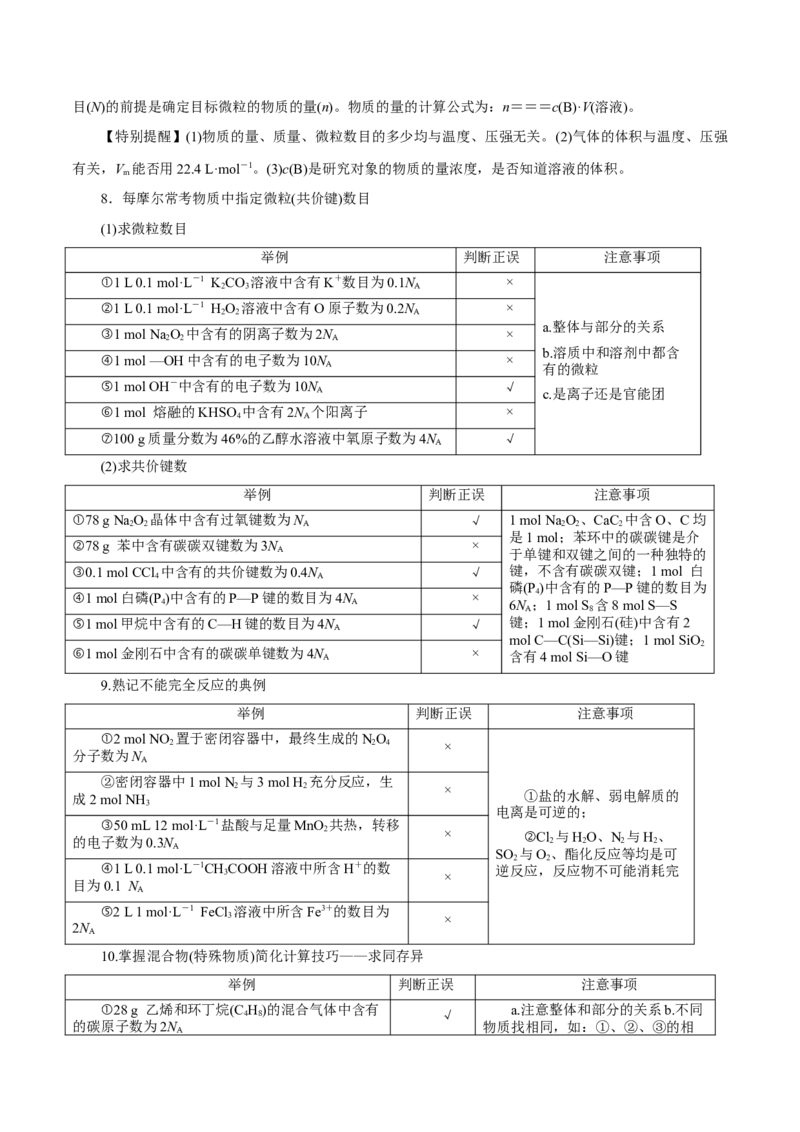
7.宏观量(m、V)与微粒数的换算公式
物质所含微粒(分子、原子、离子、质子、中子和电子等)数目的计算公式为N=n·N ,因此确定微粒数
A目(N)的前提是确定目标微粒的物质的量(n)。物质的量的计算公式为:n===c(B)·V(溶液)。
【特别提醒】(1)物质的量、质量、微粒数目的多少均与温度、压强无关。(2)气体的体积与温度、压强
有关,V 能否用22.4 L·mol-1。(3)c(B)是研究对象的物质的量浓度,是否知道溶液的体积。
m
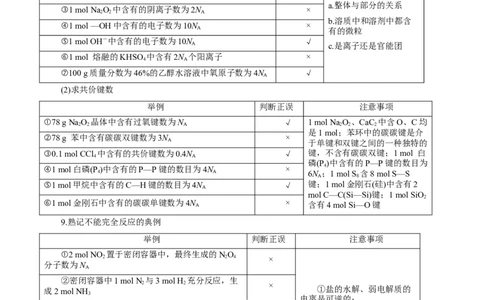
8.每摩尔常考物质中指定微粒(共价键)数目
(1)求微粒数目
举例 判断正误 注意事项
①1 L 0.1 mol·L-1 KCO 溶液中含有K+数目为0.1N ×
2 3 A
②1 L 0.1 mol·L-1 HO 溶液中含有O原子数为0.2N ×
2 2 A
a.整体与部分的关系
③1 mol Na O 中含有的阴离子数为2N ×
2 2 A
b.溶质中和溶剂中都含
④1 mol —OH中含有的电子数为10N ×
A 有的微粒
⑤1 mol OH-中含有的电子数为10N √
A c.是离子还是官能团
⑥1 mol 熔融的KHSO 中含有2N 个阳离子 ×
4 A
⑦100 g质量分数为46%的乙醇水溶液中氧原子数为4N √
A
(2)求共价键数
举例 判断正误 注意事项
①78 g Na O 晶体中含有过氧键数为N √ 1 mol Na O、CaC 中含O、C均
2 2 A 2 2 2
是1 mol;苯环中的碳碳键是介
②78 g 苯中含有碳碳双键数为3N ×
A 于单键和双键之间的一种独特的
③0.1 mol CCl 中含有的共价键数为0.4N √ 键,不含有碳碳双键;1 mol 白
4 A
磷(P )中含有的P—P键的数目为
④1 mol白磷(P )中含有的P—P键的数目为4N × 4
4 A 6N ;1 mol S 含8 mol S—S
A 8
⑤1 mol甲烷中含有的C—H键的数目为4N √ 键;1 mol金刚石(硅)中含有2
A
mol C—C(Si—Si)键;1 mol SiO
2
⑥1 mol金刚石中含有的碳碳单键数为4N A × 含有4 mol Si—O键
9.熟记不能完全反应的典例
举例 判断正误 注意事项
①2 mol NO 置于密闭容器中,最终生成的NO
2 2 4 ×
分子数为N
A
②密闭容器中1 mol N 与3 mol H 充分反应,生
2 2 ×
成2 mol NH ①盐的水解、弱电解质的
3
电离是可逆的;
③50 mL 12 mol·L-1盐酸与足量MnO 共热,转移
的电子数为0.3N
2 × ②Cl
2
与H
2
O、N
2
与H
2
、
A
SO 与O、酯化反应等均是可
2 2
④1 L 0.1 mol·L-1CHCOOH溶液中所含H+的数 逆反应,反应物不可能消耗完
3 ×
目为0.1 N
A
⑤2 L 1 mol·L-1 FeCl 溶液中所含Fe3+的数目为
3 ×
2N
A
10.掌握混合物(特殊物质)简化计算技巧——求同存异
举例 判断正误 注意事项
①28 g 乙烯和环丁烷(C
4
H
8
)的混合气体中含有
√
a.注意整体和部分的关系b.不同
的碳原子数为2N 物质找相同,如:①、②、③的相
A②常温常压下,92 g NO 和NO 的混合气体
2 2 4 √
中含有的原子数为6N
A
③16 g O 和O 的混合气体中含有的O原子数 同部分分别是最简式为
2 3 √
为N “CH”“NO”“O”;④中前者的相对
A 2 2
原子质量为后者的2倍,铜原子数也
④8.0 g Cu S和CuO的混合物中含有铜原子数
2 √ 为后者的2倍;⑤每摩尔物质中都含
为0.1N
A 两摩尔“O”;⑥虽然都是水,但二
⑤1 mol CO 和SO 的混合气体中含有的氧原 者的相对分子质量不同,每个分子
2 2 √
子数为2N 中所含中子数也不相同
A
⑥18 g H O、DO组成的物质中含有的质子数
2 2 ×
为10N
A
【关键能力拓展】
陷阱一、抓“两看”,突破气体与状况陷阱
一看“气体”是否处在“标准状况”。
二看“标准状况”下,物质是否为“气体”[如CCl 、CHCl 、CHCl(注:CHCl为气体)、HO、溴、
4 3 2 2 3 2
SO 、己烷、苯、HF等在标准状况下均不为气体]。
3
陷阱二、排“干扰”,突破质量(或物质的量)与状况无关陷阱
给出非标准状况下气体的物质的量或质量,干扰正确判断,误以为无法求解物质所含的粒子数,实际
上,此时物质所含的粒子数与温度、压强等外界条件无关。
陷阱三、记“组成和结构”,突破陷阱
1.记特殊物质中所含微粒(分子、原子、电子、质子、中子等)的数目,如Ne、DO、18O 、—OH、
2 2
OH-等。
2.记最简式相同的物质,如NO 和NO、乙烯(C H)和丙烯(C H)等。
2 2 4 2 4 3 6
3.记摩尔质量相同的物质,如N、CO、C H 等。
2 2 4
4.记物质中所含化学键的数目,如1分子HO、C H 中化学键的数目分别为3、3n+1。1 mol SiO
2 2 n 2n+2 2
中含4 N 个Si—O键,1 mol Si中含Si—Si键数目为2N ,1 mol P (白磷)中含P—P键数目为6N 。
A A 4 A
陷阱四、理解反应原理,突破“隐含”陷阱
1.可逆反应不能进行到底,反应物不能全部转化为产物。常见的可逆反应:① 2NO NO ;②Cl
2 2 4 2
+HO HCl+HClO;③NH +HO NH ·H O NH+OH-;④2SO +O 2SO ;⑤N+
2 3 2 3 2 2 2 3 2
3H 2NH 。
2 3
2.常温下,不能共存的气体间的反应
(1)HCl+NH ===NHCl;
3 4
(2)2NO+O===2NO;
2 2
(3)2H S+SO ===3S↓+2HO。
2 2 23.“隐含”浓度变化
(1)在MnO 与浓盐酸的反应中,随着反应的进行,浓盐酸逐渐变为稀盐酸,MnO 与稀盐酸不反应。
2 2
(2)在Cu与浓硫酸的反应中,随着反应的进行,浓硫酸逐渐变为稀硫酸,Cu与稀硫酸不反应。
(3)常温下,Fe在浓硝酸、浓硫酸中钝化,反应不具有持续性。
4.常在难电离、易水解的粒子数目上设题
判断电解质溶液中粒子数目时注意“三看”:一看是否有弱电解质的电离;二看是否有弱离子的水解;
三看是否指明了溶液的体积。弱电解质在水溶液中部分电离,可水解盐溶液中离子发生微弱水解,都会导
致相关粒子数目减少。
陷阱五、突破氧化还原反应中电子转移的陷阱
1.同一种物质在不同反应中做氧化剂、还原剂的判断,如(1)Cl 和Fe、Cu等反应,Cl 只做氧化剂,
2 2
而Cl 和NaOH反应,Cl 既做氧化剂又做还原剂;(2)Na O 与CO 或HO反应,NaO 既做氧化剂又做还原
2 2 2 2 2 2 2 2
剂,而NaO 与SO 反应,NaO 只做氧化剂;(3)NO 和HO反应,NO 既做氧化剂又做还原剂。
2 2 2 2 2 2 2 2
2.反应物量不同,生成物所表现的化合价不同,如Fe和HNO 反应,Fe不足时生成Fe3+,Fe过量时
3
生成Fe2+。
3.氧化剂或还原剂不同,生成物所表现的化合价不同,如 Cu和Cl 反应生成CuCl ,而Cu和S反应
2 2
生成Cu S。
2
4.注意氧化还原反应的顺序,如向FeI 溶液中通入Cl,Cl 先氧化I-,再氧化Fe2+。
2 2 2
陷阱六、突破电解质溶液中微粒数目上的陷阱
1.是否存在弱电解质的电离或盐类水解。
2.已知浓度,是否指明体积,是否能用公式“n=cV ”计算。
3.在判断溶液中微粒总数时,是否忽视溶剂水。
4.胶粒是大量难溶分子、离子的聚集体。
【核心题型例解】
高频考点一 考查粒子微粒数目
例1. (2022·辽宁卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C. 标准状况下, 气体中 数目为D. 的 溶液中 数目为
【答案】A
【解析】1个 原子中含有10个中子, 的物质的量为 ,故
中含有中子的物质的量为 ,中子数为 ,故A正确;乙烯分子的结构式为 ,1个乙
烯分子中含有5个 键, 的物质的量为 ,所以 分子中含有的 键数目为
,B错误; 是共价化合物, 分子中不存在 ,故C错误;没有给出 溶液的体积,无法
计算 的 溶液中 的数目,故D错误;故选A。
【变式探究】(2021·全国甲卷)N 为阿伏加德罗常数的值。下列叙述正确的是 ( )
A
A.8g 重水(DO)中含有质子数为 10N
2 A
B.3mol 的 NO 与 HO 完全反应转移的电子数为 4N
2 2 A
C.2g 环状 S( )分子中含有 S-S 键数为 1N
8 A
D.1L pH 值等于 4 的 0.1mol/L 的 K 2 Cr 2 O 7 溶液中含 2- 有 Cr 2 O 7 数为 0.1N A
【答案】C
【解析】D0的质子数为10,18gD0的物质的量为0.9mol,则所含质子数为9N ,A错误;NO 与
2 2 A 2
HO反应的方程式为:3NO +H O=2HNO +NO,该反应转移的电子数为2e-,若有3mol的NO 参与反应,
2 2 2 3 2
则转移的电子数为2N ,B错误;S 分子中含有的S-S键数为8,32gS 含有的S-S键数为1N ,C正确;D
A 8 8 A
选项:酸性KCr O 中存在:Cr O2-+H O=2CrO2-+2H+,含Cr元素物种有Cr O2-和CrO2-,则溶液中Cr O2-
2 2 7 2 7 2 4 2 7 4 2 7
离子数小于0.1N ,D错误。
A
【举一反三】火箭发射时可用 作燃料, 作氧化剂,其反应为 。
为阿伏加德罗常数的值,下列说法正确的是A.1 mol 中含有的π键数为
B.9.2 g 中含有的质子数为
C.1.8 g 中氧的价层电子对数为
D.当生成6.72 L 时转移电子数为
【答案】C
【解析】 中存在4个N-H单键和一个N-N单键,单键形成 键, 中不含π键,A错误;9.2
g 物质的量为0.1mol,1个 含有46个质子,则9.2g含有的质子数为 ,B错误;1.8 g
物质的量为0.1mol,氧的价层电子对数为4,则1.8 g 中氧的价层电子对数为 ,C正确;气体温
度压强未知,无法计算,D错误;故选C。
高频考点二 考查氧化还原反应转移电子数目
例2.(2023·辽宁卷第5题)我国古代四大发明之一黑火药的爆炸反应为:
。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 含 键数目为N
A
B. 每生成 转移电子数目为N
A
C. 晶体中含离子数目为0.2N
A
D. 溶液中含 数目为0.1N
A
【答案】C
【解析】题中没有说是标况条件下,气体摩尔体积未知,无法计算,A项错误;2.8gN 的物质的量
2
,1molN 生成转移的电子数为12N ,则0.1molN 转移的电子数为1.2N ,B项
2 A 2 A错误;0.1molKNO 晶体含有离子为K+、NO -,含有离子数目为0.2N ,C项正确;因为S2-水解使溶液中S2-
3 3 A
的数目小于0.1N ,D项错误;故选C。
A
【变式探究】(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗
A
常数的值,下列说法正确的是
A. 反应转移电子为0.1mol B. HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D. 反应生成标准状况下气体3.36L
A
【答案】A
【解析】2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为0.3mol,两者
发生反应后,Fe完全溶解,而盐酸过量。Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;HCl溶
液中Cl-的物质的量为0.3mol,因此,Cl-数为0.3N ,B不正确;56Fe 的质子数为26、中子数为30,
A
2.8g56Fe的物质的量为0.05mol,因此,2.8g56Fe含有的中子数为1.5N ,C不正确;反应生成H 的物质的量
A 2
为0.05mol,在标准状况下的体积为1.12L ,D不正确;综上所述,本题A。
【举一反三】 是阿伏加德罗常数的值。下列说法正确的是
A.1mol 中含有Si-O键的数目为2
B.25℃、101kPa下,4g 中含有的原子数为2
C.标准状况下,6.72L 与水充分反应转移的电子数目为0.1
D.25℃时,1.0L 的 溶液中含有 的数目为0.2
【答案】B
【解析】SiO 中1个Si原子结合4个O原子,即1mol SiO 晶体中含有硅氧键的数目为4N ,A错误;
2 2 A
4g 的物质的量为n= ,所含原子个数为2N ,B正确;标况下二氧化氮不是气体,无
A
法计算,C错误;25℃时, pH=13的Ba(OH) 溶液中OH-浓度为 ,故1.0L溶液中含有OH-的数
2
目为0.1mol,个数为0.1N ,D错误;故选B。
A
高频考点三 考查反应限度例3.(2022·浙江卷)N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
【答案】C
【解析】 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物质的
量为0.1mol,因此,其中只含有 个阳离子,A说法不正确;没有指明气体的温度和压强,无法确定
乙烷和丙烯的混合气体的物质的量是多少,因此,无法确定其中所含碳氢键的数目,B说法不正
确; 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为 ,C说
法正确; 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此,
和 于密闭容器中充分反应后, 分子总数小于 ,D说法不正确。综上所述,
故选C。
【变式探究】(2021·河北卷)N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A. 22.4L(标准状况)氟气所含的质子数为18N
A
B. 1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C. 电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D. 1L1mol•L-1溴化铵水溶液中NH 与H+离子数之和大于N
A
【答案】C
【解析】在标准状况下22.4L氟气的物质的量为1mol,其质子数为18N ,A正确;碘蒸气与氢气发生
A
的反应为: ,反应为可逆反应,有一定的限度,所以充分反应,生成的碘化氢分子数小于2N ,B正确;电解饱和食盐水时电极总反应为:2NaCl+2H O 2NaOH+H ↑+Cl↑,若阴阳两极产生
A 2 2 2
气体分别是氢气与氯气,且物质的量之比为1:1,若气体的总质量为73g,则说明反应生成的氢气与氯气的
物质的量各自为1mol,根据关系式H 2e-可知,转移的电子数为2N ,C错误; 1L1mol•L-1溴化铵水溶
2 A
液存在电荷守恒,即c(NH +)+c(H+)=c(Br-)+c(OH-),则物质的量也满足n(NH +)+n(H+)=n(Br-)+n(OH-),因为
4 4
n(Br-)=1mol,所以该溶液中NH +与H+离子数之和大于N ,D正确;故选C。
4 A
【举一反三】设 为阿伏加德罗常数,下列说法正确的是
A.将 和 于密闭容器中充分反应后,容器内的分子数等于
B.常温下,任意比例混合的环丙烷和丙烯中,含氢原子的数目为 个
C. 分子中有 个 键
D.标况下, 溶于水得到的溶液中, 和 的总数小于
【答案】D
【解析】氮气与氢气合成氨气的反应为可逆反应,反应物不能完全转化为生成物,所以将1mol N 与
2
3mol H 充入一密闭容器内充分应后,容器内气体分子数大于2N , 故A错误;物质的物质的量不确定,
2 A
无法计算氢原子个数,故B错误; 的物质的量为1mol,含有7N 个 键,故C错误;标况
A
下, 的物质的量为0.2mol,根据原子守恒可知NH 、 和 的总物质的量为0.2mol,
3
故 和 的总数小于 ,故D正确;故选D。
高频考点四 考查电解质溶液中离子数目
例4.(2023·浙江卷6月第7题)N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B. 1.7gH O 中含有氧原子数为0.2N
2 2 A
C. 向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D. 标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
【答案】A【解析】1个C HO中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4gC HO的物质的量为
2 4 2 4
0.1mol,则含有σ键数目最多为0.7N ,A正确;1.7gH O 的物质的量为 =0.05mol,则含有氧原子
A 2 2
数为0.1N ,B不正确;向1L0.1mol/LCHCOOH溶液通氨气至中性,溶液中存在电荷守恒关系:
A 3
c(CHCOO-)+c(OH-)=
3
c(NH +)+c(H+),中性溶液c(OH-)=c(H+),则c(CHCOO-)=c(NH+),再根据物料守恒:n(CHCOO-)+
4 3 4 3
n(CHCOOH)=0.1mol,得出铵根离子数小于0.1N ,C不正确;标准状况下,11.2LCl 的物质的量为
3 A 2
0.5mol,通入水中后只有一部分Cl 与水反应生成H+、Cl-和HClO,所以溶液中氯离子数小于0.5N ,D不
2 A
正确;故选A。
【变式探究】(2022·全国甲卷) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
【答案】C
【解析】25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A错
误;Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故B
3 3 A
错误;苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生成7molCO ,则
2
0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;电解熔融CuCl 时,阳极反应为
2 A 2
,阴极反应为 ,阴极增加的重量为Cu的质量,6.4gCu的物质的量为0.1mol,
根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为0.2N ,故D错误;故选C。
A
【举一反三】 代表阿伏加德罗常数的值。下列说法正确的是
A.标准状况下, 乙醇的分子数约为B. 中所含电子数为
C. 与足量稀硝酸反应转移电子数目为
D. 的 水溶液中阴离子的数目为
【答案】C
【解析】标准状况下,乙醇为液体,摩尔体积不是 ,不能计算分子数,A错误; 的电
子式为: , 中所含电子数为 ,B错误;稀硝酸具有强氧化性,将Fe氧化成为 ,
与足量稀硝酸反应转移电子数目为 ,C正确; 溶液中, 发生水解:
,根据电荷守恒: ,
, ,阴离子的数目大于 ,D错误;故选C。
高频考点五 考查共价键的数目
例5.(2023·全国甲卷第10题)N 为阿伏加德罗常数的值。下列叙述正确的是
A
A. 异丁烷分子中共价键的数目为
B. 标准状况下, 中电子的数目为
C. 的 溶液中 的数目为
的
D. 溶液中 的数目为
【答案】A
【解析】异丁烷的结构式为 ,1mol异丁烷分子含有13N 共价键,所以0.50mol异丁烷分
A
子中共价键的数目为6.5N ,A正确;在标准状况下,SO 状态为固态,不能计算出2.24L SO 物质的量,
A 3 3
故无法求出其电子数目,B错误;pH=2的硫酸溶液中氢离子浓度为c(H+)=0.01mol/L,则1.0L pH=2的硫酸
溶液中氢离子数目为0.01N ,C错误;NaCO 属于强碱弱酸盐,在水溶液中CO2-会发生水解,所以1.0L
A 2 3 31.0 mol/L的NaCO 溶液中CO2-的数目小于1.0N ,D错误;故选A。
2 3 3 A
【变式探究】(2022·浙江卷)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
【答案】A
【解析】1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量
2
0.01mol/L×1L=0.01mol,OH-的数目为0.01N ,A正确;1.8g重水(D O)的物质的量为:0.09mol,所含质子
A 2
数为0.9N ,B错误;足量的浓盐酸与8.7gMnO(0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数目
A 2
为0.2N ,C错误;甲醇的结构简式为:CHOH,32g(1mol)的分子中含有C—H键的数目为3N ,D错误;
A 3 A
故选A。
【举一反三】汽车尾气中的碳氢化物与臭氧反应是造成城市光化学污染的主要原因,其中常见的反应
为 ,已知 为阿伏加德罗常数的值,下列有关说法正确的是
A.标准状况下, 中所含极性共价键数目为
B. 和 均为只含非极性键的非极性分子
C. 和 分子中C原子采取 杂化和 杂化
D.若有 参与反应,则反应中转移的电子数目为
【答案】C
【解析】标准状况下, 是气体,2.24L 是0.1mol,一个
中所含极性共价键数目为8个,即0.1mol 中所含极性共价键数目为11
个,A错误;含有非极性键不一定是非极性分子,要看其正负电荷重心是否重合,O 分子结构重心不对
3
称,正负电荷重心不重合,故O 不是非极性分子,B错误;饱和碳原子采取 杂化,碳氧双键和碳碳双
3键的碳原子采取 杂化,所以CHCHO和CHCH=CHCH 分子中C原子采取 杂化和 杂,C正确;
3 3 3
在该常见反应中,2-丁烯转变为乙醛,碳元素化合价平均从-2升高到-1,氧元素化合价从0降低到-2,若
2molO 反应,电子转移4mol,D错误;故选C。
3
高频考点六 考查气体摩尔体积
例6. (2021·广东卷)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 1molCHCl 含有C-Cl键的数目为3N
3 A
B. 1.0mol·L-1的盐酸含有阴离子总数为2N
A
C.11.2LNO与11.2LO 混合后的分子数目为N
2 A
D. 23gNa与足量HO反应生成的H 分子数目为N
2 2 A
【答案】A
【解析】1个CHCl 分子中含有3个C-Cl键,微粒个数与物质的量成正比,故1molCHCl 含有3molC-
3 3
Cl键,C-Cl键的数目为3N ,A正确;盐酸为氯化氢的水溶液,氯化氢会全部电离出阴离子Cl-,水会部分
A
电离出阴离子OH-,水的质量及电离程度未知,故无法计算1L1.0mol·L-1的盐酸含有阴离子总数,B错误;
未提到具体的温度、压强(如标况下),故无法计算11.2LNO与11.2LO 混合后的分子数目,C错误;
2
23gNa为1mol,钠与足量的水反应生成氢气的关系式为: ,故1mol Na应对应生成0.5mol H ,H
2 2
分子数目应为0.5N ,D错误;故选A。
A
【变式探究】(2021·浙江卷)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 1 mol NH F晶体中含有的共价键数目为3N
4 A
B. CH 和C H 混合气体2.24L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A
C. 向100mL 0.10mol·L-1FeCl 溶液中加入足量Cu粉充分反应,转移电子数目为0.01N
3 A
D. 0.1 mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目为0.1N
3 3 2 3 2 3 A
【答案】C
【解析】NH F结构中只有铵根中含有4个共价键,则l mol NH F晶体中含有的共价键数目为4N ,A
4 4 A
错误;CH 和C H 混合气体2.24L(标准状况)的物质的量是0.1mol,由于1mol CH 和C H 分别完全燃烧消
4 2 4 4 2 4
耗氧气的物质的量分别是2mol、3mol,则0.1mol混合气体完全燃烧消耗氧气的分子数目应该介于0.2N 和
A
0.3N 之间,B错误;l00 mL0.10 mol/L FeCl 溶液中铁离子的物质的量是0.01mol,加入足量Cu粉充分反
A 3
应,铁离子被还原为亚铁离子,则转移电子数目为0.01N ,C正确;乙酸和乙醇的酯化反应是可逆反应,
A
则0.1 mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目小于0.1N ,D错误;故
3 3 2 3 2 3 A
选C 。【举一反三】设 表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下, 溶液含离子总数为
B.常温常压下, 中含有的电子数总数为
C.标准状况下, 中含有的分子数目为
D. 溶液中含有的 数目为
【答案】B
【解析】没有说明溶液的体积,无法计算溶液中离子的数目,故A错误; 水的物质的量为 ,
水中含有 电子,含有的电子数总数为 ,故B正确;标况下,乙醇不是气体,题中条件无
法计算乙醇的物质的量,故C错误; 2 溶液中含有溶质碳酸钠 碳酸钠中含有
碳酸根离子,由于碳酸根离子部分水解,溶液中含有的碳酸根离子的数目小于 ,故D错误;故
选B。