文档内容
专题讲座(八) 无机化工流程题的解题策略
第一部分:高考真题感悟
1.(2021·福建·高考真题)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如
下:
下列说法错误的是
A.FeSO 的分解产物X为FeO B.本流程涉及复分解反应
4
C.HNO 的沸点比HSO 的低 D.制备使用的铁锅易损坏
3 2 4
【答案】A
【解析】A.据图可知FeSO 分解时生成SO 和SO ,部分S元素被还原,则Fe元素应被氧化,X为
4 2 3
Fe O,A错误;B.HSO 与KNO 在蒸馏条件下生成HNO 和KSO ,为复分解反应,B正确;C.HSO
2 3 2 4 3 3 2 4 2 4
与KNO 混合后,蒸馏过程中生成HNO,说明HNO 的沸点比HSO 的低,C正确;D.硫酸、硝酸均可
3 3 3 2 4
以和铁反应,所以制备使用的铁锅易损坏,D正确;综上所述答案为A。
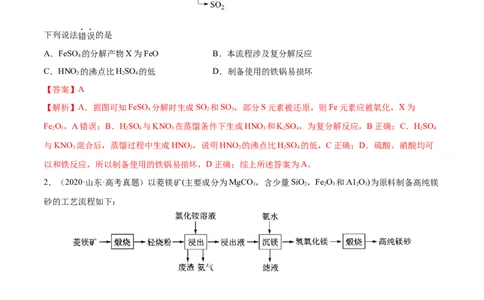
2.(2020·山东·高考真题)以菱镁矿(主要成分为MgCO ,含少量SiO,Fe O 和A1 O)为原料制备高纯镁
3 2 2 3 2 3
砂的工艺流程如下:
已知浸出时产生的废渣中有SiO,Fe(OH) 和Al(OH) 。下列说法错误的是
2 3 3
A.浸出镁的反应为
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
【答案】B
【解析】菱镁矿煅烧后得到轻烧粉,MgCO 转化为MgO,加入氯化铵溶液浸取,浸出的废渣有SiO、
3 2Fe(OH) 、Al(OH) ,同时产生氨气,则此时浸出液中主要含有Mg2+,加入氨水得到Mg(OH) 沉淀,煅烧得
3 3 2
到高纯镁砂。A.高温煅烧后Mg元素主要以MgO的形式存在,MgO可以与铵根水解产生的氢离子反应,
促进铵根的水解,所以得到氯化镁、氨气和水,化学方程式为MgO+2NH Cl=MgCl +2NH↑+H O,故A正
4 2 3 2
确;B.一水合氨受热易分解,沉镁时在较高温度下进行会造成一水合氨大量分解,挥发出氨气,降低利
用率,故B错误;C.浸出过程产生的氨气可以回收制备氨水,沉镁时氯化镁与氨水反应生成的氯化铵又
可以利用到浸出过程中,故C正确;D.Fe(OH) 、Al(OH) 的K 远小于Mg(OH) 的K ,所以当pH达到一
3 3 sp 2 sp
定值时Fe3+、Al3+产生沉淀,而Mg2+不沉淀,从而将其分离,故D正确;故答案为B。
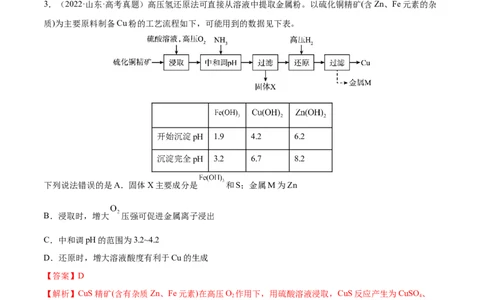
3.(2022·山东·高考真题)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂
质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
【答案】D
【解析】CuS精矿(含有杂质Zn、Fe元素)在高压O 作用下,用硫酸溶液浸取,CuS反应产生为CuSO 、
2 4
S、HO,Fe2+被氧化为Fe3+,然后加入NH 调节溶液pH,使Fe3+形成Fe(OH) 沉淀,而Cu2+、Zn2+仍以离子
2 3 3
形式存在于溶液中,过滤得到的滤渣中含有S、Fe(OH) ;滤液中含有Cu2+、Zn2+;然后向滤液中通入高压
3
H,根据元素活动性:Zn>H>Cu,Cu2+被还原为Cu单质,通过过滤分离出来;而Zn2+仍然以离子形式存
2
在于溶液中,再经一系列处理可得到Zn单质。A.经过上述分析可知固体X主要成分是S、Fe(OH) ,金
3
属M为Zn,A正确;B.CuS难溶于硫酸,在溶液中存在沉淀溶解平衡CuS(s) Cu2+(aq)+S2-(aq),增大O
2
的浓度,可以反应消耗S2-,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进金属离子的浸取,
B正确;C.根据流程图可知:用NH 调节溶液pH时,要使Fe3+转化为沉淀,而Cu2+、Zn2+仍以离子形式
3存在于溶液中,结合离子沉淀的pH范围,可知中和时应该调节溶液pH范围为3.2~4.2,C正确;D.在
用H 还原Cu2+变为Cu单质时,H 失去电子被氧化为H+,与溶液中OH-结合形成HO,若还原时增大溶液
2 2 2
的酸度,c(H+)增大,不利于H 失去电子还原Cu单质,因此不利于Cu的生成,D错误;故合理选项是D。
2
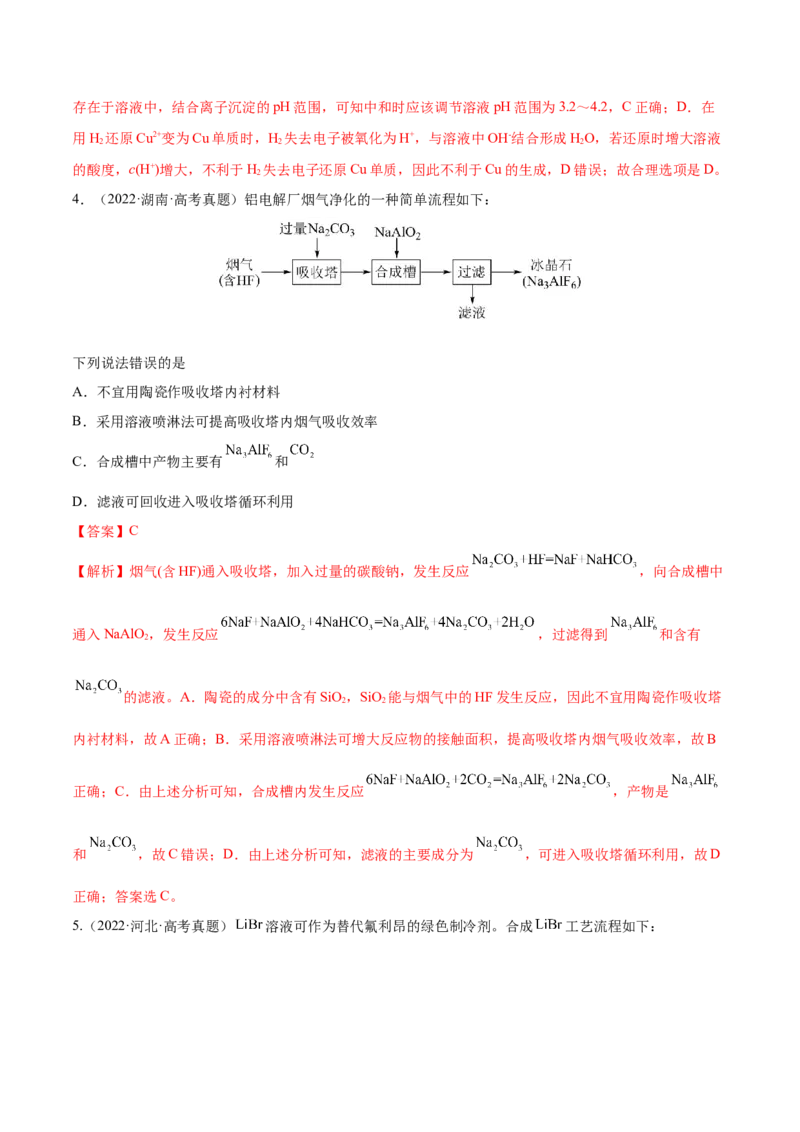
4.(2022·湖南·高考真题)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用
【答案】C
【解析】烟气(含HF)通入吸收塔,加入过量的碳酸钠,发生反应 ,向合成槽中
通入NaAlO ,发生反应 ,过滤得到 和含有
2
的滤液。A.陶瓷的成分中含有SiO,SiO 能与烟气中的HF发生反应,因此不宜用陶瓷作吸收塔
2 2
内衬材料,故A正确;B.采用溶液喷淋法可增大反应物的接触面积,提高吸收塔内烟气吸收效率,故B
正确;C.由上述分析可知,合成槽内发生反应 ,产物是
和 ,故C错误;D.由上述分析可知,滤液的主要成分为 ,可进入吸收塔循环利用,故D
正确;答案选C。
5.(2022·河北·高考真题) 溶液可作为替代氟利昂的绿色制冷剂。合成 工艺流程如下:下列说法错误的是
A.还原工序逸出的 用 溶液吸收,吸收液直接返回还原工序
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为
D.参与反应的 为1∶1∶1
【答案】A
【解析】由流程可知,氢溴酸中含有少量的溴,加入硫化钡将溴还原生成溴化钡和硫,再加入硫酸除杂,
得到的滤渣为硫酸钡和硫;加入碳酸锂进行中和,得到的溴化锂溶液经浓缩等操作后得到产品溴化锂。
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液中含有溴化钠和次溴酸钠等物质,若直接返回还原工序,
2
则产品中会有一定量的溴化钠,导致产品的纯度降低,A说法错误;B.除杂工序中产生的滤渣为硫酸钡
和硫,硫属于非极性分子形成的分子晶体,而硫酸钡属于离子晶体,根据相似相溶原理可知,硫可溶于煤
油,而硫酸钡不溶于煤油,因此可用煤油进行组分分离,B说法正确;C.中和工序中,碳酸锂和氢溴酸
发生反应生成溴化锂、二氧化碳和水,该反应的化学方程式为 LiCO+2HBr=CO ↑ +2LiBr +H O,C说法
2 3 2 2
正确;D.根据电子转化守恒可知,溴和硫化钡反应时物质的量之比为1:1;根据硫酸钡的化学组成及钡元
素守恒可知,n(BaS):n(HSO )为1:1,因此,参与反应的n(Br): n(BaS):n(H SO )为1:1:1,D说法正确;综
2 4 2 2 4
上所述,本题选A。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·湖南·湘阴县第一中学高三期中)以镁铝复合氧化物(MgO-Al O)为载体的负载型镍铜双金属催
2 3
化剂(Ni-Cu/MgO-Al O)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
2 3已知加热时尿素[CO(NH)]在水中发生水解反应,放出两种气体。下列说法错误的是
2 2
A.“洗涤”过程中,可用氯化钡溶液检验滤饼是否洗净
B.“晶化”过程中,需保持恒温60℃,可采用直接加热
C.“焙烧”过程中,可使用蒸发皿或坩埚
D.“还原”过程中,以M代表Ni或Cu,所发生的反应为MO+H M+HO
2 2
【答案】BC
【解析】A.洗涤”过程中,洗涤液中含有阴离子硫酸根,可以用氯化钡溶液检验,操作方法为:取少量
最后一次洗涤液,加入盐酸酸化的氯化钡溶液,若产生白色沉淀,则滤饼未洗涤干净,反之,洗涤干净,
A项正确;B.“晶化”过程中,恒温60℃可以用水浴加热来稳定温度,不可以直接加热,B项错误;C.
“焙烧”过程中,温度较高,不能使用蒸发皿,应选用坩埚,C项错误;D.“还原”过程中,NiO+H
2
Ni+H O;CuO+H Cu+H O,D项正确;答案选BC。
2 2 2
2.(2022·天津河北·二模)硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质
(见下图)。下列说法正确的是
A.漂白粉的有效成分是CaCl 和Ca(ClO)
2 2
B.可用饱和NaHCO 溶液或KMnO 溶液除去CO 中的SO 气体
3 4 2 2
C.SO 氧化为SO 是可逆反应,提高O 浓度和使用适合的催化剂均可提高SO 的转化率
2 3 2 2
D.用CO合成CHOH进而合成HCHO的两步反应,原子利用率均为100%
3
【答案】B【解析】CaSO 与焦炭、空气在高温下反应产生CaO、CO、SO ,SO 与O 在催化剂存在的条件下加热发
4 2 2 2
生氧化还原反应产生SO ,SO 被水吸收得到HSO ;CO与H 在催化剂存在条件下加热,发生反应产生
3 3 2 4 2
CHOH;CaO与HO反应产生Ca(OH) ,Ca(OH) 与Cl 发生歧化反应制取漂白粉。A.漂白粉的成分是
3 2 2 2 2
CaCl 和Ca(ClO) ,有效成分是Ca(ClO) ,A错误;B.KMnO 溶液具有强氧化性,会在溶液中将SO 氧化
2 2 2 4 2
为硫酸,硫酸能够与NaHCO 溶液反应产生CO 气体,而CO 不能溶解在饱和NaHCO 溶液中,因此可以
3 2 2 3
达到除杂净化的目的,B正确;C.SO 氧化为SO 是可逆反应,提高O 浓度可提高SO 的转化率;但使用
2 3 2 2
适合的催化剂只能加快反应速率,缩短达到平衡所需时间,而化学平衡不移动,因此不能提高SO 的转化
2
率,C错误;D.工业上一般采用下列两种反应合成甲醇:反应Ⅰ:CO(g)+2H(g) CHOH(g);反应Ⅱ:
2 3
CO(g)+3H(g) CHOH(g)+H O(g),反应Ⅱ中不是所有原子进入期望产物,原子利用率不为100%,D错
2 2 3 2
误;故合理选项是B。
3.(2022·河南·模拟预测)一种利用绿矾(FeSO ·7H O) 和磷酸制备电池正极材料LiFePO 的工艺流程如图
4 2 4
所示:
下列说法错误的是
A.“溶解”时,HPO 的用量不宜过多
3 4
B.反应1时,参与反应的氧化剂与还原剂物质的量之比为2:1
C.可用硝酸酸化的硝酸银溶液检验FePO 是否洗涤干净
4
D.LiFePO 电池放电时装置如图,则电极a为负极,电极b为正极
4
【答案】B
【解析】由题给流程可知,将绿矾溶于磷酸溶液得到磷酸酸化的硫酸亚铁溶液,向溶液中加入次氯酸钠溶
液,将亚铁离子氧化为铁离子,向氧化后的溶液中加入氢氧化钠溶液调节溶液pH,将铁离子转化为磷酸铁
沉淀,过滤得到磷酸铁;向磷酸铁中加入草酸和氢氧化锂溶液得到磷酸亚铁锂沉淀,过滤、洗涤得到磷酸
亚铁锂。A.溶解时若磷酸溶液的用量过多会导致反应1消耗较多的氢氧化钠溶液,造成浪费,所以溶解时磷酸溶液的的用量不宜过多,故A正确;B.由分析可知,反应1时,向溶液中加入次氯酸钠溶液的目
的是将亚铁离子氧化为铁离子,由得失电子数目守恒可知,参与反应的氧化剂次氯酸钠与还原剂亚铁离子
物质的量之比为1:2,故B错误;C.由分析可知,磷酸铁沉淀的表面附有可溶性的氯化钠,所以可用硝
酸酸化的硝酸银溶液检验磷酸铁是否洗涤干净,故C正确;D.由锂离子的移动方向可知,放电时,电极a
为负极,电极b为正极,故D正确;故选B。
4.(2022·湖南娄底·模拟预测)某小组回收锌锰电池废料(主要含MnO 、MnOOH等)制备高锰酸钾,简易
2
流程如图所示。
下列说法错误的是
A.“碱熔”可选择铁坩埚,不能用瓷坩埚或铝坩埚
B.“碱熔”中副产物是Cl
2
C.“氧化”操作是利用Cl 氧化KMnO 制备KMnO ,可推知在碱性条件下Cl 氧化性大于KMnO
2 2 4 4 2 4
D.“系列操作”中,高温下干燥KMnO
4
【答案】BD
【解析】锌锰电池废料主要含MnO 、MnOOH等,因二氧化硅与碱高温下反应,可选铁坩埚碱熔,Mn元
2
素的化合价升高,氯酸钾中Cl元素的化合价降低,生成KMnO 溶液,碱熔时氯酸钾可能分解生成氧气,
2 4
氧化时氯气可氧化生成KMnO ,加热结晶分离出固体KMnO A.“碱熔”中有KOH,不能用瓷坩埚、铝
4 4。
坩埚,可以选择铁坩埚,A项正确;B.在KOH存在条件下不能生成氯气,B项错误;C.“氧化”中氯
气是氧化剂,高锰酸钾是氧化产物,氧化剂的氧化性大于氧化产物的氧化性,C项正确;D.高温下高锰
酸钾会分解,D项错误;故选BD。
5.(2022·江苏·南京市第十三中学模拟预测)用高分子吸附树脂提取卤水中的确(主要以 形式存在)的工
艺流程如下
下列说法不正确的是
A.流程中①和④所得溶液中,后者c( )大B.流程中②中 不宜过量,防止 进一步氧化
C.制备 ,理论上需 的质量约为408g
D.流程中④的作用是将吸附的碘氧化而脱离高分子树脂
【答案】D
【解析】由题给流程可知,向卤水中加入稀硫酸酸化后,通入氯气将溶液中的碘离子氧化为单质碘,用高
分子吸附树脂吸附溶液中的碘,向树脂中加入亚硫酸钠溶液,将碘还原为碘化钠而脱离高分子树脂,向所
得的溶液中加入氯酸钾溶液,将碘化钠氧化为单质碘,单质碘经分离提纯得到碘产品。A.由分析可知,
流程中①和④为碘元素的富集过程,则流程中①和④所得溶液中碘离子的物质的量相同,但④所得溶液碘
离子浓度大于①,故A正确;B.由分析可知,流程②为通入氯气将溶液中的碘离子氧化为单质碘,为防
止过量的氯气将碘氧化,通入的氯气不宜过量,故B正确;C.由分析可知,加入氯酸钾溶液的目的是将
碘化钠氧化为单质碘,由得失电子数目守恒可知,制备10mol碘,理论上需要氯酸钾的质量为10mol×
×122.5g/mol=408g,故C正确;D.由分析可知,流程中④为向树脂中加入亚硫酸钠溶液,将碘还原为碘
化钠而脱离高分子树脂,故D错误;故选D。
6.(2022·山东临沂·二模)一种以硼镁矿(含2MgO·B O·H O、SiO 及少量FeO、Fe O、Al O 等)为原料
2 3 2 2 2 3 2 3
生产硼酸(H BO)的工艺流程如下。
3 3
已知: 与足量NaOH溶液反应生成 。
下列说法错误的是
A. 的电离方程式为
B.“热过滤”的目的是防止 从溶液中结晶析出
C.“除杂”过程中加入的试剂X依次为MgO、
D.“母液”经蒸发浓缩、冷却结晶、过滤洗涤、干燥可得到硫酸镁晶体
【答案】C【解析】由流程可知,加硫酸溶解只有SiO 不溶,趁热过滤,防止HBO 从溶液中析出,浸出渣为
2 3 3
SiO,“除杂”需加入试剂X应该先加HO 溶液,将亚铁离子转化为铁离子,再加入MgO调节溶液的pH
2 2 2
约为5,使铁离子、铝离子均转化为沉淀,则滤渣为氢氧化铝、氢氧化铁,然后对滤液蒸发浓缩、降温结
晶、过滤分离出HBO,母液中主要含有硫酸镁和硼酸。A. 由题干信息可知, 与足量NaOH溶液
3 3
反应生成 , 的电离方程式为 ,A正确;B. 由分析可知,
“热过滤”的目的是防止 从溶液中结晶析出,B正确;C. 由分析可知,“除杂”过程中加入的试剂
X应该先加HO 溶液,将亚铁离子转化为铁离子,再加入MgO调节溶液的pH约为5,使铁离子、铝离子
2 2
均转化为沉淀,C错误;D. 由分析可知,“母液”中主要含有硫酸镁和硼酸,则经蒸发浓缩、冷却结晶、
过滤洗涤、干燥可得到硫酸镁晶体,D正确;故答案为:C。
7.(2022·全国·模拟预测)一种以烟气中 制取轻质 的流程如下:
已知 且 时视为沉淀完全。下列说法错误的是
A.“反应I”中增大氨水浓度能提高烟气中 去除率
B.“反应II”中溶液的导电能力随石灰乳的加入快速上升
C.若测得“滤液”中 ,则 沉淀完全
D.所得“滤液”可转移到“反应I”中循环利用
【答案】B
【解析】将烟气通入氨水中发生反应Ⅰ生成碳酸铵,再加入石灰乳发生反应Ⅱ生成碳酸钙和氨水,过滤得
到的滤液中含有氨水,可循环使用;所得碳酸钙沉淀进行洗涤干燥,得到轻质 。A.“反应I”中增
大氨水浓度,可以充分吸收二氧化碳,能提高烟气中 去除率,选项A正确;B.加入石灰乳时生成碳酸钙沉淀和氨水,故初始时溶液中的铵根离子、碳酸根离子因反应而快速降低导致导电能力快速降低,后
加入过量的氢氧化钙,由于生成氨水的电离及过量氢氧化钙的电离导致离子浓度增大,导电能力逐渐上升,
选项B错误;C.若测得“滤液”中 ,则
, ,故
沉淀完全,选项C正确;D.所得“滤液”中含有氨水,可转移到“反应I”中循环利用,选项D正确;
答案选B。
8.(2022·江苏扬州·一模)烟气脱硫能有效减少 的排放。实验室用粉煤灰(主要含 等)制备
碱式硫酸铝[ ]溶液,并用于烟气脱硫。下列说法正确的是
A.“酸浸”时 不宜过量太多,目的是防止 溶解
B. 约为3.6时,溶液中存在大量的
C.调节 时的离子方程式:
D.碱式硫酸铝溶液多次循环使用后 增大的原因是部分 发生氧化反应
【答案】D
【解析】由题给流程可知,粉煤灰用硫酸溶液酸浸时,氧化铝与硫酸溶液反应生成硫酸铝,二氧化硅与硫
酸溶液不反应,过滤得到二氧化硅滤渣1和硫酸铝溶液;向硫酸铝溶液中加入碳酸钙粉末调节溶液pH为
3.6,碳酸钙与过量的硫酸转化为硫酸钙,铝离子部分水解得到碱式硫酸铝,过滤得到硫酸钙滤渣2和碱式
硫酸铝溶液;碱式硫酸铝溶液循环吸收二氧化硫,溶于水的二氧化硫与水反应生成亚硫酸,加热时,部分
亚硫酸受热分解,部分被氧化为硫酸,使溶液中硫酸根离子浓度增大,促进碱式硫酸铝的生成。
A.二氧化硅与硫酸溶液不反应,所以酸浸时硫酸溶液不能过量太多是因为溶液pH过小,加入碳酸钙粉末调节溶液pH时,不利于铝离子水解转化为碱式硫酸铝,故A错误;B.铝离子和碳酸氢根离子在溶液中发
生双水解反应,不能大量共存,所以pH为3.6的溶液中不可能存在碳酸氢根离子,故B错误;C.调节溶
液pH为3.6时发生的反应为碳酸钙与硫酸溶液反应生成硫酸钙、二氧化碳和水,反应的离子方程式为
CaCO +SO +2H+=CaSO +CO +H O,故C错误;D.由分析可知,碱式硫酸铝溶液循环吸收二氧化硫,溶
3 4 2 2
于水的二氧化硫与水反应生成亚硫酸,加热时,部分亚硫酸受热分解,部分被氧化为硫酸,使溶液中硫酸
根离子浓度增大,促进碱式硫酸铝的生成,故D正确;故选D。
9.(2022·全国·模拟预测)高温焙烧碳粉与重晶石混合物,发生的主反应为 。
工业上以重晶石矿(含 、 杂质)为原料制取 的流程如图所示。下列说法错误的是
A.“焙烧”过程需要在隔绝空气条件下进行
B.“滤渣1“中最多含有两种单质
C.“滤液1”加CuO反生的反应:
D.“滤液2”经蒸发浓缩、冷却结晶、过滤得 晶体
【答案】B
【解析】由题给流程可知,高温焙烧碳粉与重晶石混合物时,硫酸钡与碳高温反应得到硫化钡,氧化铁、
二氧化硅与碳高温反应得到铁和硅,焙烧后的固体经热水浸取、过滤得到含有过量碳粉、铁、硅的滤渣1
和含有硫化钡的滤液1;向滤液1中加入氧化铜,硫化钡溶液与氧化铜反应生成氢氧化钡和硫化铜沉淀,
过滤得到含有硫化铜的滤渣2和含有氢氧化钡的滤液2;滤液2经蒸发浓缩、冷却结晶、过滤得八水氢氧
化钡晶体。A.若焙烧过程在空气中进行,碳粉高温下会与空气中的氧气反应,无法与重晶石反应,所以
需要在隔绝空气条件下进行,故A正确;B.由分析可知,滤渣1中含有过量碳粉、铁、硅共3种单质,
故B错误;C.由分析可知,滤液1中加入氧化铜发生的反应为硫化钡溶液与氧化铜反应生成氢氧化钡和
硫化铜沉淀,反应的化学方程式为 ,故C正确;D.由分析可知,滤液2经蒸发浓缩、冷却结晶、过滤得八水氢氧化钡晶体,故D正确;故选B。
10.(2022·北京通州·一模)稀土永磁材料——高性能钕铁硼合金为新能源汽车提供核心原材料。从制钕
铁硼的废料中提取氧化钕(Nd O)的工艺流程如图1所示,草酸钕晶体的热重曲线如图2所示。
2 3
已知:ⅰ. 与酸反应生成 离子,草酸钕晶体[ ]的摩尔质量是 ;ⅱ.
生成 ,开始沉淀时 ,完全沉淀时
生成 ,开始沉淀时 ,完全沉淀时
下列说法不正确的是
A.气体1的主要成分是 ,滤渣1是硼和其他不溶性杂质
B.“氧化”时会发生反应:
C.若“调 ”与“氧化”顺序颠倒, 的利用率无影响
D.由图2可知, 时剩余固体的主要成分是
【答案】C
【解析】钕铁硼废料中主要含Nd、Fe、B,由信息及流程可知,加入稀盐酸,硼不与酸反应,则滤渣是硼,
Fe与盐酸反应生成气体为氢气,Nd能与酸发生置换反应,反应为Fe+2HCl=FeCl +H ↑、
2 2
2Nd+6HCl=2NdCl +3H ↑,然后加过氧化氢可氧化亚铁离子,加NaOH调节pH使铁离子转化为氢氧化铁沉
3 2
淀,滤液2中加草酸生成Nd (C O)•10H O在氧气下焙烧得到Nd O。A.Fe与盐酸反应生成气体为氢气,
2 2 4 3 2 2 3硼不与酸反应,则气体的主要成分是H,滤渣是硼和其他不溶性杂质,A正确;B.往滤液1中加入HO
2 2 2
的目的是将Fe2+氧化为Fe3+,pH=4时Fe3+已经完全沉淀,则反应方程式为,
,B正确;C.若“调 ”与“氧化”顺序颠倒,即先氧化此
时溶液显酸性,反应为2Fe2++H O+2H+=2Fe3++2H O,此时生成Fe3+并未完全沉淀,且Fe3+能够催化HO 的
2 2 2 2 2
分解,从而减小了HO 的利用率,C错误;D.由图可知,设质量为100g,含结晶水为100g×
2 2
≈24.6g,则110℃时完全失去结晶水,然后Nd (C O) 在氧气中加热导致固体质量减少,此时剩余固体的摩
2 2 4 3
尔质量为732g/mol×51.9%=379.91g/mol,Nd OCO 的摩尔质量为380g/mol,则500℃时剩余固体的主要成
2 2 3
分是Nd OCO,D正确;故答案为:C。
2 2 3
11.(2022·山东泰安·三模)高铁酸钾(K FeO)是种环保、高效、多功能饮用水处理剂,制备流程如图所示:
2 4
下列叙述错误的是
A.若通过电解法以铁为原料制高铁酸钾,铁棒应做阳极
B.“尾气”可用碱溶液吸收也可用FeCl 等具有还原性的物质溶液吸收
2
C.反应Ⅱ中生成1molNa FeO 时转移的电子数为3N
2 4 A
D.最后一步能制取KFeO 的原因是相同温度下KFeO 的溶解度大于NaFeO
2 4 2 4 2 4
【答案】D
【解析】由题给流程可知,铁屑与氯气燃烧生成氯化铁,氯化铁与次氯酸钠、氢氧化钠混合溶液反应生成
氯化钠、高铁酸钠和水,向高铁酸钠溶液中加入饱和氢氧化钾溶液将溶解度大的高铁酸钠转化为溶解度小
高铁酸钾,过滤得到粗高铁酸钾晶体。A.通过电解法以铁为原料制高铁酸钾时铁元素的化合价升高被氧
化,则铁棒应做阳极失去电子发生氧化反应生成高铁酸钠,故A正确;B.铁屑与氯气在燃烧生成氯化铁
时,氯气过量会产生含有氯气的尾气,尾气中的氯气能用氯化亚铁等具有还原性的溶液吸收,防止污染空
气,故B正确;C.由分析可知,反应Ⅱ中发生的反应为氯化铁与次氯酸钠、氢氧化钠混合溶液反应生成
氯化钠、高铁酸钠和水,反应中生成1mol高铁酸钠时转移电子的物质的量为3mol,则转移的电子数为
1mol×3×N mol—1=3N ,故C正确;D.由分析可知,向高铁酸钠溶液中加入饱和氢氧化钾溶液的目的是将
A A
溶解度大的高铁酸钠转化为溶解度小高铁酸钾,故D错误;故选D。12.(2022·湖南·株洲市第一中学高三期中)以高杂质碳酸锂 含Ca、Mg杂质 为原料制备电池级碳酸锂
的工艺流程如图。已知EDTA对 杂质离子有很好的络合效果; 的溶解度随温度升高而降
低,且在乙醇中溶解度小。下列说法错误的是
A.氢化过程需通入过量的 ,发生的主要反应方程式为:
B.操作1为分液,实验室进行该操作时使用的玻璃仪器为漏斗、玻璃棒、烧杯
C.氢化阶段应控制反应温度为高温,利于反应进行,加快反应速率
D.操作2中,提高碳酸锂回收率的方法有升高温度和加入乙醇溶剂
【答案】BC
【解析】由流程可知,碳酸锂经氢化反应生成碳酸氢锂,过滤除去滤渣,加入EDTA除去Ca2+、Mg2+等杂
质离子,在经过加热分解得到碳酸锂,操作2为过滤,分离出碳酸锂,在乙醇中洗涤、烘干后得到电池级
碳酸锂。A.氢化过程通入过量的 将碳酸锂转化为碳酸氢锂,发生的主要反应方程式为:
,A项正确;B.操作1为过滤,除去滤渣,使用的玻璃仪器为漏斗、玻璃棒、
烧杯,B项错误;C. 的溶解度随温度升高而降低,高温不利于反应进行,反应速率变慢,C项错
误;D. 的溶解度随温度升高而降低,且在乙醇中溶解度小,所以升高温度和加入乙醇溶剂可提高
操作2中碳酸锂回收率,D项正确;故答案选BC。
二、主观题(共3小题,共40分)
13.(2022·青海·海东市第一中学二模)(15分)钌(Ru)是一种极其昂贵的稀有贵金属,广泛应用于电子、
航空航天、石油化工、有机合成等领域。钌的矿产资源很少,因此从含钌废液中回收钌尤为重要。某含钌
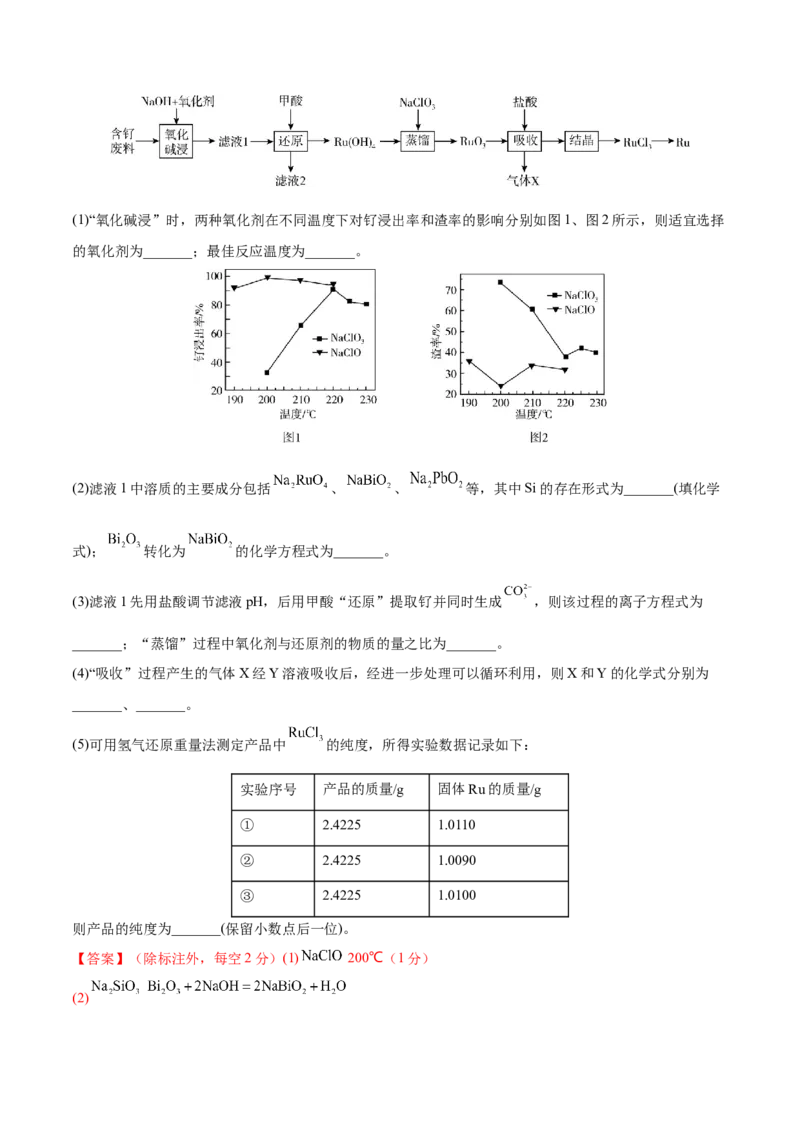
的废渣主要成分为Ru、 、 、 ,回收钌的工艺流程如下:(1)“氧化碱浸”时,两种氧化剂在不同温度下对钌浸出率和渣率的影响分别如图1、图2所示,则适宜选择
的氧化剂为_______;最佳反应温度为_______。
(2)滤液1中溶质的主要成分包括 、 、 等,其中Si的存在形式为_______(填化学
式); 转化为 的化学方程式为_______。
(3)滤液1先用盐酸调节滤液pH,后用甲酸“还原”提取钌并同时生成 ,则该过程的离子方程式为
_______;“蒸馏”过程中氧化剂与还原剂的物质的量之比为_______。
(4)“吸收”过程产生的气体X经Y溶液吸收后,经进一步处理可以循环利用,则X和Y的化学式分别为
_______、_______。
(5)可用氢气还原重量法测定产品中 的纯度,所得实验数据记录如下:
实验序号 产品的质量/g 固体Ru的质量/g
① 2.4225 1.0110
② 2.4225 1.0090
③ 2.4225 1.0100
则产品的纯度为_______(保留小数点后一位)。
【答案】(除标注外,每空2分)(1) 200℃(1分)
(2)(3)
(4)
(5)85.7%
【解析】含钌废料在碱性溶液中被氧化,Ru、 Pb 、 SiO 、 BiO 分别转化为NaRuO 、 NaPbO 、
2 2 3 2 4 2 2
NaSiO、 NaBiO,加甲酸还原,NaRuO 被还原为Ru(OH) ,然后在氧化条件下蒸馏得到RuO,再加盐
2 3 2 2 4 4 3
酸吸收,生成氯气和RuCl ,最后还原得到钌。
3
(1)从图中可以看出,用NaClO钌浸出率更高,且渣率低,最佳温度控制在200℃,此时钌的浸出率接近
100%,且渣率最低。
(2)SiO 能和NaOH溶液反应生成NaSiO,所以在滤液1中Si的存在形式为NaSiO,BiO 也能和
2 2 3 2 3 2 3
NaOH溶液反应转化为NaBiO,化学方程式为BiO+2NaOH=2NaBiO +H O。
2 2 3 2 2
(3)滤液1中含有NaRuO ,用甲酸“还原”提取钌,钌被还原为Ru(OH) ,甲酸被氧化为 ,根据
2 4 4
电子守恒、电荷守恒和质量守恒写出该反应的离子方程式为HCOOH+ +H O=Ru(OH) ↓+ 。“蒸
2 4
馏”阶段是NaClO 将Ru(OH) 转化为RuO,该反应中钌的化合价从+4价升高到+6价,做还原剂,NaClO
3 4 3 3
中氯的化合价从+5价降低到-1价,NaClO 做氧化剂,根据电子守恒,氧化剂与还原剂的物质的量之比为
3
1:3。
(4)“吸收”过程是RuO 和盐酸反应生成RuCl ,钌的化合价降低,则盐酸做还原剂,氯的化合价升高,
3 3
则生成的气体为Cl,氯气可以被NaOH溶液吸收生成NaClO,可以用在“氧化酸浸”步骤中。
2
(5)三次实验得到固体钌的质量平均值为1.0100g,即0.0100mol,可计算出RuCl 的质量为
3
0.01mol×207.5g/mol=2.0750g,则产品纯度为 85.7%。
14.(2022·广西·模拟预测)(15分)以含锂电解铝废渣(主要含AlF、NaF、LiF、CaO)和浓硫酸为原料,
3
制备电池级碳酸锂,同时得副产品冰晶石,其工艺流程如下:已知:LiOH易溶于水,LiCO 微溶于水。
2 3
回答下列问题:
(1)电解铝废渣与浓硫酸的反应能否在玻璃仪器中进行:_______ ( 填“能”或“否”)。滤渣1的主要成分
是_______(写化学式)。
(2)碱解反应中,同时得到气体和沉淀反应的离子方程式为_______。
(3)一般地说K>105时,该反应进行得就基本完全了。苛化反应中存在如下平衡:LiCO(s)+Ca2+ (aq)
2 3
2Li+ (aq) +CaCO (s) ,通过计算说明该反应是否进行完全:_______。[已知K (Li CO)=8.64×10-4、
3 sp 2 3
K (CaCO)=2.5×10-9]。
sp 3
(4)从碳化反应后的溶液得到LiCO 固体的具体实验操作中,第一步应在_______中(填一种主要仪器的名
2 3
称)进行,该流程中可以循环使用的物质是_______。
(5)上述流程得到副产品冰晶石的化学方程式为_______。
【答案】(除标注外,每空2分)(1)否 CaSO
4
(2)2Al3++3 +3H O═2Al(OH) ↓+3CO ↑
2 3 2
(3)Li CO(s)+Ca2+(aq) 2Li+(aq)+ CaCO (s)的K= = = =
2 3 3
=3.5×105>105,可以认为该反应进行完全
(4)蒸发皿 二氧化碳(1分)
(5)6HF+NaSO +NaAlO =Na AlF+HSO +2HO
2 4 2 3 6 2 4 2
【解析】含锂电解铝废渣主要含AlF、NaF、LiF、CaO等,加入浓硫酸生成的气体为HF,水浸后过滤分
3
离出滤渣1为CaSO,滤液中加碳酸钠发生2Al3++3 +3H O═2Al(OH) ↓+3CO ↑、2Li++ ═Li CO,
4 2 3 2 2 3
气体为CO,过滤分离出滤液含硫酸钠,分离出Al(OH) 、LiCO,加水调浆再加CaO、苛化反应将不溶性
2 3 2 3
的碳酸锂转化成氢氧化锂溶液,过滤分离出滤渣2含CaCO 和Al(OH) ,碳化时LiOH与二氧化碳反应所得
3 3
的溶液为LiHCO ,提取晶体后再分解生成LiCO 固体,二氧化碳在流程中可循环使用。
3 2 3
(1)电解铝废渣与浓硫酸的反应生成HF、HF能与二氧化硅反应,故不能在玻璃仪器中进行:答案为
“否”。滤渣1的主要成分是CaSO。
4
(2)碱解反应中,同时得到气体和沉淀反应是铝离子和碳酸根离子的双水解反应,离子方程式为2Al3++3
+3H O═2Al(OH) ↓+3CO ↑。
2 3 2(3)LiCO(s)+Ca2+(aq) 2Li+(aq)+ CaCO (s)的K= = = =
2 3 3
=3.5×105>105,可以认为该反应进行完全。
(4)从碳化反应后的溶液得到LiCO 固体的具体实验操作中,第一步应为提取LiHCO 晶体,需要进行加
2 3 3
热浓缩、冷却结晶、过滤、洗涤、干燥,故第一步主要在蒸发皿进行,该流程中可以循环使用的物质是二
氧化碳。
(5)上述流程得到副产品冰晶石,根据流程图知,反应物为HF、NaSO 、NaAlO ,生成物为NaAlF,
2 4 2 3 6
根据原子守恒及反应原理书写方程式为:6HF+NaSO +NaAlO =Na AlF+HSO +2HO。
2 4 2 3 6 2 4 2
15.(2022·广东·珠海市第一中学模拟预测)(10分)五氟化锑( )是非常强的路易斯酸其酸性是纯硫
酸的1500万倍。以某矿(主要成分为 ,含有少量CuO、PbO、 等杂质)为原料制备 的工艺
流程如图。
已知:Ⅰ.CuS、PbS的 分别为 、 ;
Ⅱ. 微溶于水、 难溶于水,它们均为两性氧化物,SbOCl难溶于水。
回答下列问题:
(1)为提高锑矿浸出率可采取的措施有_______。(填一种)
(2)“滤渣Ⅰ”中存在少量的SbOCl,可加入氨水对其“除氯”转化为 回收,不宜用NaOH溶液代替氨
水的原因为_______。
(3)已知:浸出液中: , ,在“沉淀”过程中,缓慢滴加极稀的
硫化钠溶液,先产生的沉淀1是_______(填化学式);当CuS、PbS共沉时,“沉淀1”是否已沉淀完全(离子
浓度小于 即可)_______。(填“是”或“否”)(4)“除砷”时, 转化为 ,该反应的氧化剂是_______。
(5)“电解”时,以情性材料为电极,锑的产率与电压大小关系如图所示,阴极的电极反应式为_______;当
电压超过 时,锑的产率降低的原因可能是发生了副反应_______。(填电极反应式)
(6) 与 反应,首次实现用非电解法制取 ,同时生成 和 ,若生成 (标准状况),
则转移电子的数目为_______(设 为阿伏加德罗常数)
【答案】(除标注外,每空2分)(1)粉碎或加热或增大盐酸浓度等
(2) 为两性氧化物,能溶于过量的NaOH溶液
(3)CuS 是(1分)
(4) 或 (1分)
(5) (1分) (1分)
(6)
【解析】由题给流程可知,锑矿用盐酸浸出时,矿中的氧化物均转化为可溶的氯化物,过滤得到滤渣和含
有可溶的氯化物的滤液;向滤液中加入硫化钠溶液,将铜离子、铅离子转化为硫化铜、硫化铅沉淀,过滤
得到除去铜离子、铅离子的滤液;向滤液中加入NaH PO 溶液,将溶液中的砷离子转化为砷,过滤得到砷
2 2
和含有氯化锑的滤液;电解滤液,在阴极得到锑,锑与氯气反应生成五氯化锑,五氯化锑与通入的氟化氢
反应生成五氟化锑。
(1)粉碎、加热、增大盐酸浓度等措施能提高锑矿浸出率,故答案为:粉碎或加热或增大盐酸浓度等;
(2)由题给信息可知,三氧化二锑为两性氧化物,若用氢氧化钠溶液代替氨水,三氧化二锑会与过量的
氢氧化钠溶液反应,导致回收产率降低,所以不能用氢氧化钠溶液代替氨水,故答案为: 为两性氧化物,能溶于过量的NaOH溶液;
(3)由溶度积可知,铜离子、铅离子开始沉淀时硫离子浓度分别为 =6.0×10−34mol/L、
=9.0×10−27mol/L,则铜离子转化为硫化铜沉淀所需硫离子浓度小于铅离子,先产生的沉淀1是硫
化铜,当硫化铜、硫化铅共沉时,溶液中铜离子浓度为 <1.0×10−5mol/L,则铜离子已经完
全沉淀,故答案为:CuS;是;
(4)由除砷时, 转化为 可知,反应中砷元素的化合价降低被还原,砷离子为反应的氧化剂,
故答案为: 或 ;
(5)由分析可知,以情性材料为电极电解三氯化锑时,锑离子在阴极得到电子发生还原反应生成锑,电
极反应式为 ,当电压超过UV时,锑的产率降低的原因可能是溶液中的氢离子在阴极得到
0
电子发生还原反应生成了氢气,电极反应式为 ,故答案为: ;
;
(6)由化合价的变化可知,标准状况下生成3.36L氟气时,反应转移电子数目为 ×2×N mol—
A
1=0.3N ,故答案为:0.3N 。
A A