文档内容
化学基本理论误区突破
(一)关于元素周期律(表)的6大误区
常见误区 出错原因
误认为最高正价和最低负价绝对值相 忽视了第ⅠA族的H的最高正价为+1,
等的元素只有第ⅣA族的元素 最低负价为-1
误认为主族元素的最高正价一定等于 忽视了氧元素无最高正价,氟元素无正
其族序数 价
误认为元素的非金属性越强,其氧化
忽视了关键词“最高价”
物对应水化物的酸性就越强
误认为失电子难的原子得电子的能力 忽视了稀有气体元素原子失电子难,得
一定强 电子也难
误认为同周期相邻两主族元素原子序
忽视了长周期也有相差11或25的情况
数之差都等于1
忽视了元素原子得失电子数目的多少与
误认为得(失)电子数的数目越多,元
元素的非金属性、金属性强弱没有必然
素的非金属性(金属性)越强
的联系
(二)热化学中的5个易错点
致误原因 特别提醒
ΔH表示反应进行到底时的能量变化。对于可逆反
忽视反应热的意义
应,改变条件平衡可能发生移动,但ΔH不变
1
A(g)+ B(g) C(g) ΔH ,平衡常数为K ;
2 1 1
忽视反应热和平衡常数的 1
C(g)+ B(g) D(g) ΔH ,平衡常数为K 。
2 2 2
计算的不同
则反应A(g)+B(g) D(g) ΔH=ΔH +ΔH ,平衡常
1 2
数K=K ·K
1 2
忽视用键能或用能量计算 ΔH=反应物总键能-生成物总键能
反应热时公式的不同 ΔH=生成物总能量-反应物总能量
忽视催化剂对活化能与反 催化剂能改变正、逆反应的活化能,但不能改变反
应热的影响不同 应的反应热忽视反应热的符号 比较反应热的大小时,需带上正、负号进行比较
(三)规避化学反应速率与平衡的失分点与误区
致误原因 应对策略 解释或举例
混淆化学反应速率 不能认为化学平衡向正反应方
若正反应是吸热反应,升高温度,平
与化学平衡移动的 向移动,则v 一定增大,v
正 逆
衡正向移动,v 、v 都增大
正 逆
影响因素 一定减小
不能认为化学平衡向正反应方 2HI(g) H (g)+I (g),反应达到平
2 2
混淆平衡移动与转
向移动,则反应物的转化率一 衡状态后再充入一定量的HI(g),平
化率的关系
定增大 衡正向移动,但HI(g)的转化率不变
不能认为增大反应物浓度时,
2SO (g)+O (g) 2SO (g),
化学平衡向正反应方向移动, 2 2 3
混淆“减弱”与
达到平衡后增大SO (g)的浓度,平衡
则反应物浓度一定减小。要正 2
“消除”的概念
正向移动,再次达到平衡时,SO (g)
确理解化学平衡原理中的“减 2
的浓度比原平衡时的大
弱”二字
混淆化学平衡移动 不能认为化学平衡向正反应方 平衡常数只与温度有关,温度不变,
与平衡常数的关系 向移动,则平衡常数一定变大 平衡常数不变
(四)规避有关“电解质溶液”的失分点
1.弱电解质电离平衡移动的3个易失分点
(1)误认为电离平衡正向移动,弱电解质的电离程度一定增大。如向CH COOH溶液中加入少量冰醋酸,
3
平衡向电离方向移动,但CH COOH的电离程度减小。
3
(2)误认为当对酸、碱溶液稀释时,溶液中所有离子的浓度都减小。如对于电离平衡CH COOH
3
CH COO-+H+,当加水稀释时,由于K 是定值,故c(H+)减小,c(OH-)增大;当对碱溶液稀释时,c(OH-)
3 w
减小,c(H+)增大。
(3)误认为电离平衡右移,电离平衡常数一定增大。对于同一反应,电离平衡常数只与温度有关,只有
因为温度升高而导致平衡右移时,电离平衡常数才会增大。
2.有关溶液酸碱性的4个易失分点
(1)误认为由水电离出的c(H+)=10-13 mol·L-1的溶液一定呈碱性。如25 ℃,0.1 mol·L-1的盐酸或氢氧化钠
溶液中由水电离出的c(H+)都为10-13 mol·L-1。(2)误认为溶液的酸碱性取决于pH。如pH=7的溶液在温度不同时,可能显酸性也可能显碱性,还可能
显中性。
(3)误认为酸碱恰好中和时溶液一定显中性。如强酸和弱碱恰好中和时溶液显酸性,强碱和弱酸恰好中
和时溶液显碱性,强酸和强碱恰好中和时溶液才显中性。
(4)不能正确理解酸、碱的无限稀释规律。常温下任何酸(碱)溶液无限稀释时,溶液的pH都不可能大于
7(小于7),只能无限接近7。
3.盐类水解的5个易失分点
(1)误认为酸式盐一定呈酸性。如NaHSO 、NaHSO 、NaH PO 溶液均呈酸性,但NaHCO 、NaHS溶液
4 3 2 4 3
均呈碱性。
(2)误认为能够发生水解的盐溶液一定呈酸性或碱性,但其实是与弱离子的水解程度有关。如
CH COONH 为弱酸弱碱盐,发生水解,但溶液呈中性。
3 4
(3)误认为水解平衡正向移动,离子的水解程度一定增大。如向FeCl 溶液中加入少量FeCl 固体,平衡
3 3
向水解方向移动,但Fe3+的水解程度减小。
(4)误认为弱酸强碱盐都因水解而显碱性。如NaHSO
因HSO-
的电离能力大于其水解能力,所以
3 3
NaHSO 溶液显酸性。
3
(5)由于加热可促进盐类水解,错误地认为可水解的盐溶液在蒸干后都得不到原溶质。对于水解程度不
是很大、水解产物不能脱离平衡体系的情况[如Al (SO ) 、Na CO 溶液]来说,溶液蒸干仍得原溶质。
2 4 3 2 3
4.沉淀溶解平衡的4个易失分点
(1)误认为沉淀溶解平衡右移,K 一定增大。K 与其他化学平衡常数一样,只与难溶电解质的性质和温
sp sp
度有关,而与沉淀的量和溶液中离子浓度的变化无关。
(2)误认为沉淀溶解平衡右移,溶解度一定变大。溶解度表示的是100 g溶剂中所能溶解溶质的质量,
溶解度受温度和同离子效应的影响,若是加水使沉淀溶解平衡右移,溶解度不变。
(3)误认为只要K 越大,其溶解度就会越大。K 还与难溶电解质类型有关,只有同类型的难溶物的K
sp sp sp
大小可用于比较其溶解度大小。
(4)误认为K 小的难溶电解质不能转化为K 大的难溶电解质,只能实现K 大的难溶电解质向K 小的
sp sp sp sp
难溶电解质转化。实际上当两种难溶电解质的K 相差不是很大时,通过调节某种离子的浓度,可实现
sp
由K 小的难溶电解质向K 大的难溶电解质转化。
sp sp
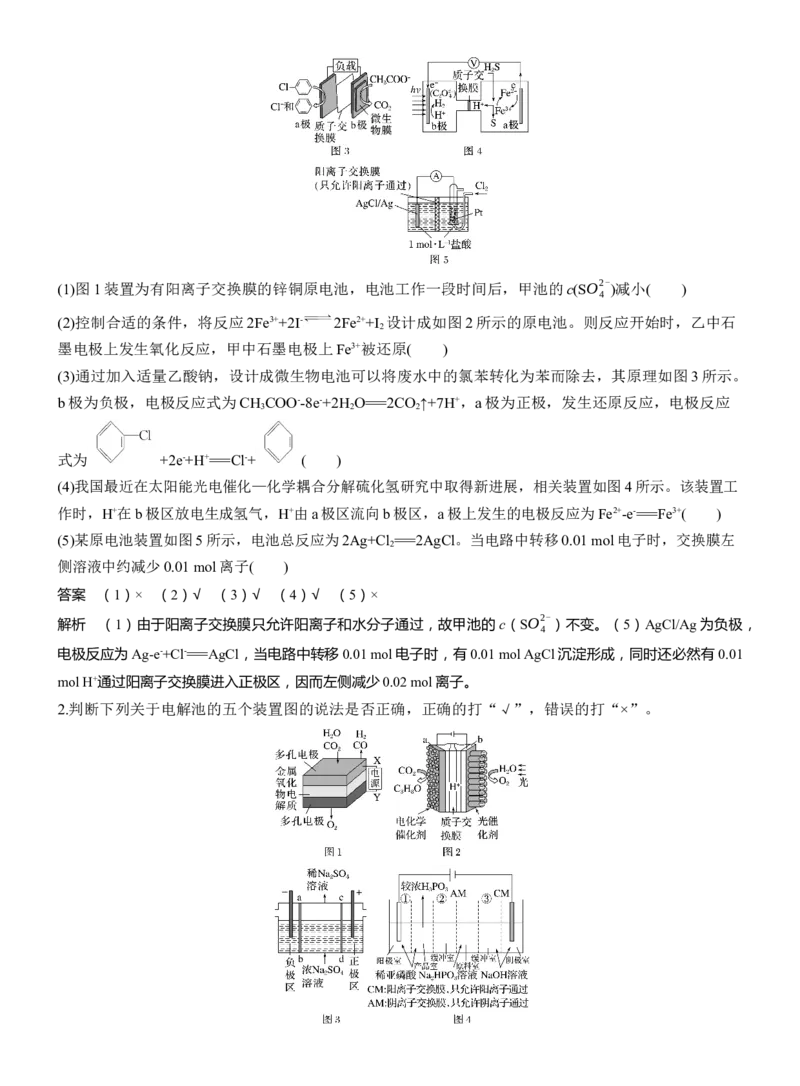
(五)电化学装置分析举例
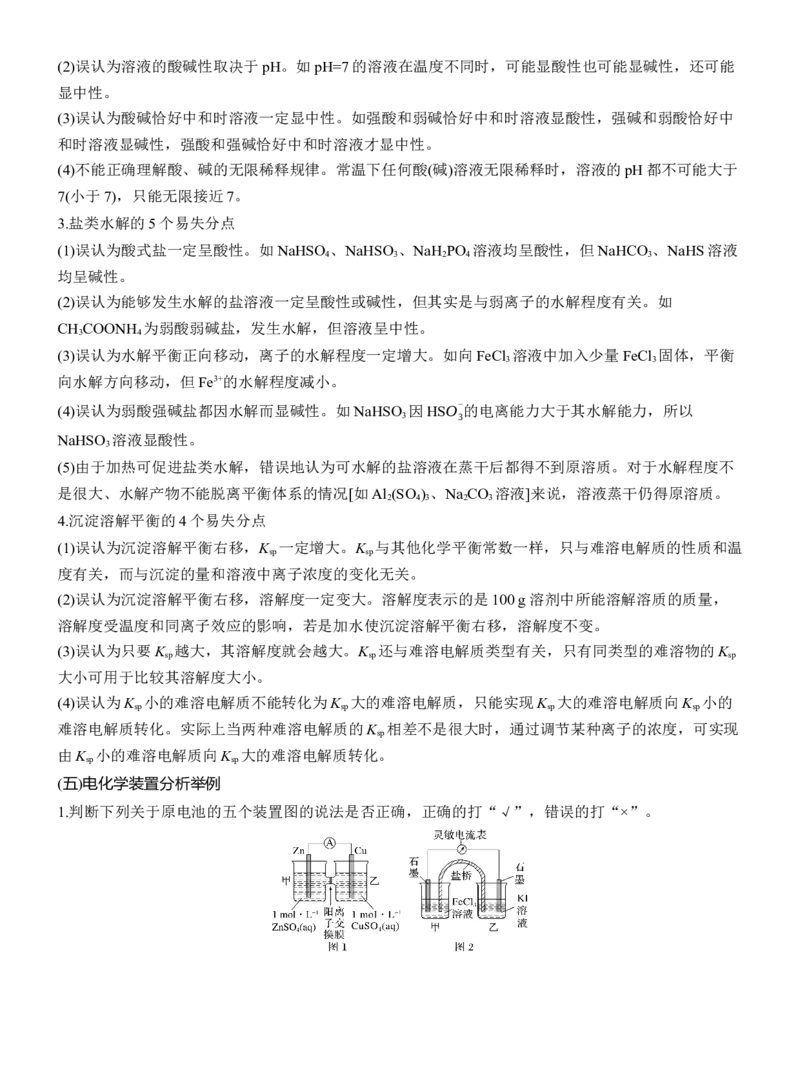
1.判断下列关于原电池的五个装置图的说法是否正确,正确的打“√”,错误的打“×”。(1)图1装置为有阳离子交换膜的锌铜原电池,电池工作一段时间后,甲池的c(SO2- )减小( )
4
(2)控制合适的条件,将反应2Fe3++2I- 2Fe2++I 设计成如图2所示的原电池。则反应开始时,乙中石
2
墨电极上发生氧化反应,甲中石墨电极上Fe3+被还原( )
(3)通过加入适量乙酸钠,设计成微生物电池可以将废水中的氯苯转化为苯而除去,其原理如图3所示。
b极为负极,电极反应式为CH COO--8e-+2H O===2CO ↑+7H+,a极为正极,发生还原反应,电极反应
3 2 2
式为 +2e-+H+===Cl-+ ( )
(4)我国最近在太阳能光电催化—化学耦合分解硫化氢研究中取得新进展,相关装置如图4所示。该装置工
作时,H+在b极区放电生成氢气,H+由a极区流向b极区,a极上发生的电极反应为Fe2+-e-===Fe3+( )
(5)某原电池装置如图5所示,电池总反应为2Ag+Cl ===2AgCl。当电路中转移0.01 mol电子时,交换膜左
2
侧溶液中约减少0.01 mol离子( )
答案 (1)× (2)√ (3)√ (4)√ (5)×
解析
(1)由于阳离子交换膜只允许阳离子和水分子通过,故甲池的c(SO2-
)不变。(5)AgCl/Ag为负极,
4
电极反应为Ag-e-+Cl-===AgCl,当电路中转移0.01 mol电子时,有0.01 mol AgCl沉淀形成,同时还必然有0.01
mol H+通过阳离子交换膜进入正极区,因而左侧减少0.02 mol离子。
2.判断下列关于电解池的五个装置图的说法是否正确,正确的打“√”,错误的打“×”。(1)在固态金属氧化物电解池中,高温条件下电解H
2
O⁃CO
2
混合气体制备H
2
和CO是一种新的能源利用
方式,基本原理如图1所示。X是电源的负极,电池总反应是H O+CO H +CO+O ( )
2 2 2 2
(2)某模拟“人工树叶”电化学实验装置如图2所示。该装置能将H O和CO 转化为O 和燃料(C H O)。
2 2 2 3 8
a电极的电极反应式为3CO +18H+-18e-===C H O+5H O( )
2 3 8 2
(3)三室式电渗析法处理含Na SO 废水的原理如图3所示,采用惰性电极,ab、cd均为离子交换膜,在
2 4
直流电场的作用下,两膜中间的Na+和SO2-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中
4
间隔室。该法在处理含Na SO 废水时可以得到NaOH和H SO 产品( )
2 4 2 4
(4)亚磷酸钠(Na HPO )溶液电渗析法制备H PO (亚磷酸)的原理如图4所示,膜①③均为CM,阳极的电
2 3 3 3
极反应式为2H O-4e-===4H++O ↑( )
2 2
(5)高压直流电线路的瓷绝缘子可能出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,如图
5所示,该装置为牺牲阳极法,瓷绝缘子表面产生的OH-向阴极移动( )
答案 (1)√ (2)× (3)√ (4)√ (5)×
解析 (2)a极为阴极,应为得电子的还原反应。(5)该装置为外加电流法,OH-向阳极移动。