文档内容
专项训练 化学条件的优化和选择(解析版)
一、单选题
1.硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关反应
的说法中不正确的是
A.实际生产中, 、 再循环使用提高原料利用率
B.实际生产中,为了提高反应速率,压强越高越好
C.在生产中,通入过量空气的目的是提高 的转化率
D.实际生产中,选定400~500℃作为操作温度的主要原因是催化剂的活性最高
【答案】B
【详解】A.二氧化硫和氧气的反应为可逆反应,SO 和O 不能反应完,因此SO 和
2 2 2
O 需再循环利用以提高原料利用率,A正确;
2
B.压强过大,设备可能无法承受太大的压强,适当增大压强可提高反应速率和转化率,
B错误;
C.通入过量的空气,则反应平衡正向移动,SO 的转化率提高,C正确;
2
D.实际生产中,温度为400-500℃时,催化剂的活性最高,因此400-500℃作为操作
温度,D正确;
故答案选B。
2.2007年诺贝尔化学奖颁给了德国化学家格哈德•埃特尔(GerhardErtl),以表彰他在固
体表面化学研究中取得的开拓性成就。他的成就之一是证实了氢气与氮气在固体催化
剂表面合成氨气的反应过程,模拟示意图如图。关于合成氨工艺,下列说法正确的是
A.图①到图③的活化能减去图⑤到图③的活化能就是合成氨反应的反应热
试卷第1页,共20页
学科网(北京)股份有限公司B.反应中有极性键的断裂与形成
C.当温度、体积一定时,在原料气中添加少量惰性气体,有利于提高平衡转化率
D.合成氨反应使用的条件高温、高压是为了提高反应物的平衡转化率
【答案】A
【详解】A.图①到图③为氮气和氢气中的化学键断裂的过程,图⑤到图③为氨气中
化学键的断裂的过程,故图①到图③的活化能减去图⑤到图③的活化能就是合成氨反
应的反应热,A正确;
B.该反应过程为氮气和氢气反应生成氨气,反应过程中只有非极性键的断裂和极性键
的形成,B错误;
C.当温度、体积一定时,在原料气中添加少量惰性气体不影响各组分的浓度,因此不
影响平衡,不能提高平衡转化率,C错误;
D.合成氨的反应是气体总体积减小的放热反应,故高压是为了提高反应物的平衡转
化率,但高温不是为了提高转化率,D错误;
故选A。
3.一种生产环氧乙烷的反应为:
下列说法正确的是
A.该反应
B.使用 是为了提高乙烯的平衡转化率
C.该反应中每消耗 乙烯,转移电子的数目为
D.实际生产投料时, 值越大,平衡体系中环氧乙烷物质的量分数越
大
【答案】C
【详解】A.根据反应式可知该反应 ,根据反应自发的条件, ,A错误;
B.任何催化剂不会影响平衡转化率,B错误;
C.根据方程式,反应中消耗 乙烯时,消耗 物质的量为 ,转移电子 ,
C正确;
资料收集整理【淘宝店铺:向阳百分百】 第2页,共20页D. 值增大,可理解为 用量一定、增加 用量; 用量增加,
可提高 转化率,增加平衡体系中环氧乙烷物质的量,但因为 用
量一定,平衡体系中环氧乙烷物质的量的增加是有限的,而混合体系物质的量总量增
加是无限的,当 用量超过一定程度时,虽然环氧乙烷物质的量仍然增加,但其物质
的量分数(在体系中所占物质的量百分比)却减小,D错误;
故答案为:C。
4.焦炉煤气(主要成分:CH、CO、H、CO)在炭催化下,使CH 与CO 重整生成H
4 2 2 4 2 2
和CO。其主要反应为
反应I:
反应II:
反应III:
反应IV:
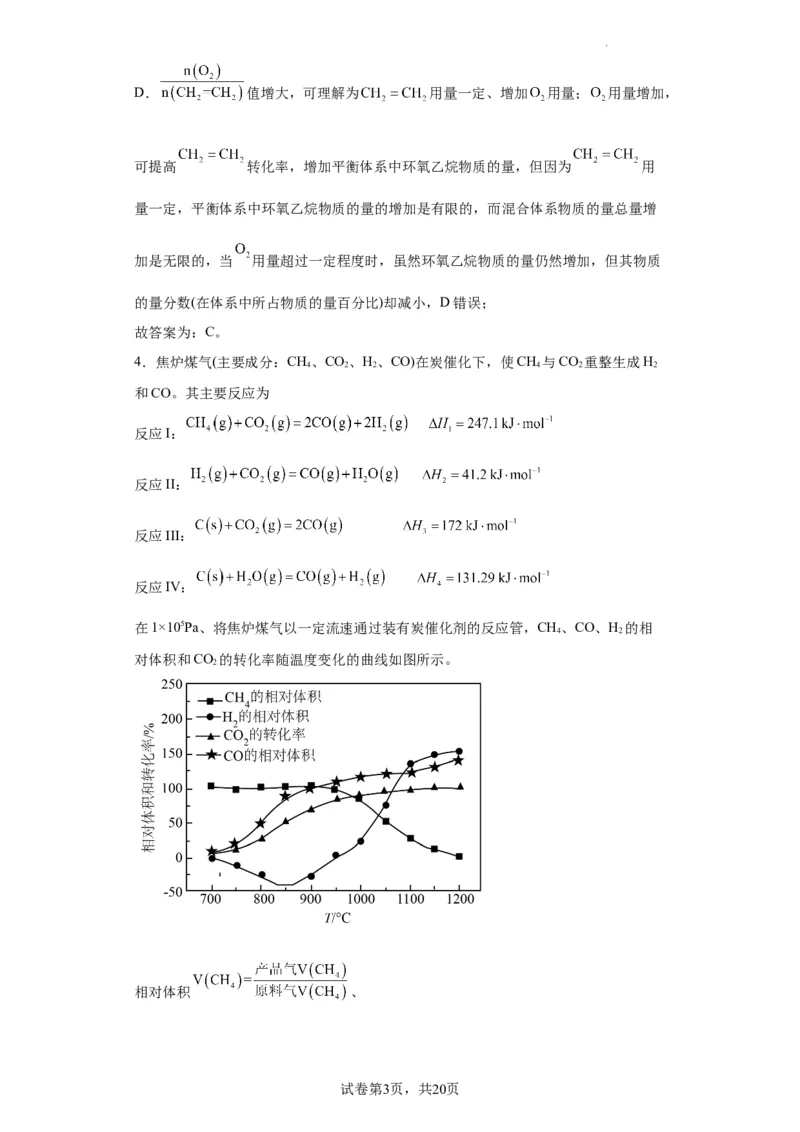
在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH、CO、H 的相
4 2
对体积和CO 的转化率随温度变化的曲线如图所示。
2
相对体积 、
试卷第3页,共20页
学科网(北京)股份有限公司相对体积
下列说法不正确的是
A.温度低于900℃,反应I基本不发生
B.850℃~900℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积
D.工业生产上需要研发低温下CH 转化率高的催化剂
4
【答案】C
【详解】A.从图中可以看出,温度低于900℃时,CH 的相对体积基本上是100%,
4
所以反应I基本不发生,A正确;
B.850℃~900℃时,H、CO的体积分数都增大,且增大的幅度相近,而CH 的相对
2 4
体积略有减小,可能是CO 转化率增大的原因,所以反应I进行的幅度很小,反应Ⅱ、
2
Ⅲ基本不发生,主要发生反应Ⅳ,B正确;
C.从图中可以看出,4个反应均为生成CO的反应,且都为吸热反应,所以若想提高
CO的相对体积,应选择升高温度,与增大焦炉煤气的流速无关,C不正确;
D.图中信息显示,温度低于900℃,CH 的相对体积基本上是100%,则反应I基本不
4
发生,所以工业生产上需要研发低温下CH 转化率高的催化剂,D正确;
4
故选C。
5.以 、 为原料合成 涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
在5MPa下,按照 投料,平衡时,CO和 在含碳产物中物质
的量分数及 的转化率随温度的变化如图。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】 第4页,共20页A.反应Ⅲ中反应物的总键能大于生成物的总键能
B.曲线 代表CO在含碳产物中物质的量分数
C.该条件下温度越低,越有利于工业生产
D.图示270℃时,平衡体系中 的体积分数约为66.6%
【答案】D
【详解】A.根据盖斯定律I-Ⅱ可得反应ⅢCO(g)+2H(g) CHOH(g) ΔH=-49kJ·mol-1-
2 3 3
41kJ·mol-1=-90kJ·mol-1;ΔH=反应物的总键能-生成物的总键⇌能,故反应Ⅲ中反应物的总
键能小于生成物的总键能,A错误;
B.反应Ⅱ的正反应是吸热反应,生成物中有CO,温度升高,反应Ⅱ的平衡正向移动,
CO的物质的量分数增大;反应Ⅲ的正反应是放热反应,反应物中有CO,温度升高,
反应Ⅲ的平衡逆向移动,CO的物质的量分数也会增大,也就是说,温度升高,CO的
产量变大,则CO在含碳产物的物质的量分数增大,故符合这个规律的是曲线n,B错
误;
C.由图可知,温度在150℃时有利于反应Ⅰ进行,CHOH的含量高,有利于提高
3
CHOH的产率,但并不是温度越低越好,因为温度太低反应速率太慢,C错误;
3
D.根据题意设起始量n(CO)=1mol,n(H )=3mol,平衡时甲醇和CO的物质的量相等,
2 2
设CHOH物质的量为 xmol,则CO 的物质的量也为xmol,270℃时CO 的转化率为
3 2
25%,则平衡时CO 的物质的量为0.75mol,根据碳守恒:0.75+2x=1,解得x=0.125,
2
根据氧守恒,水的物质的量为:2mol-0.75mol×2-0.125mol-0.125mol=0.25mol,根据氢
守恒,氢气的物质的量为 =2.5mol,则反应后总的物质的量
0.75mol+0.125mol+0.125mol+2.5mol+0.25mol=3.75mol,则平衡体系中H 的体积分数为
2
=66.7%,D正确;
答案选D。
试卷第5页,共20页
学科网(北京)股份有限公司6.恒压条件下,密闭容器中将CO、H 按照体积比为1:3合成CHOH,其中涉及的
2 2 3
主要反应:
Ⅰ.CO(g)+3H(g) CHOH(g)+H O(g) ΔH -49kJ·moI-1
2 2 3 2 1=
Ⅱ.CO(g)+H(g) CO(g)+HO(g) ΔH=41kJ·moI-1
2 2 2 2
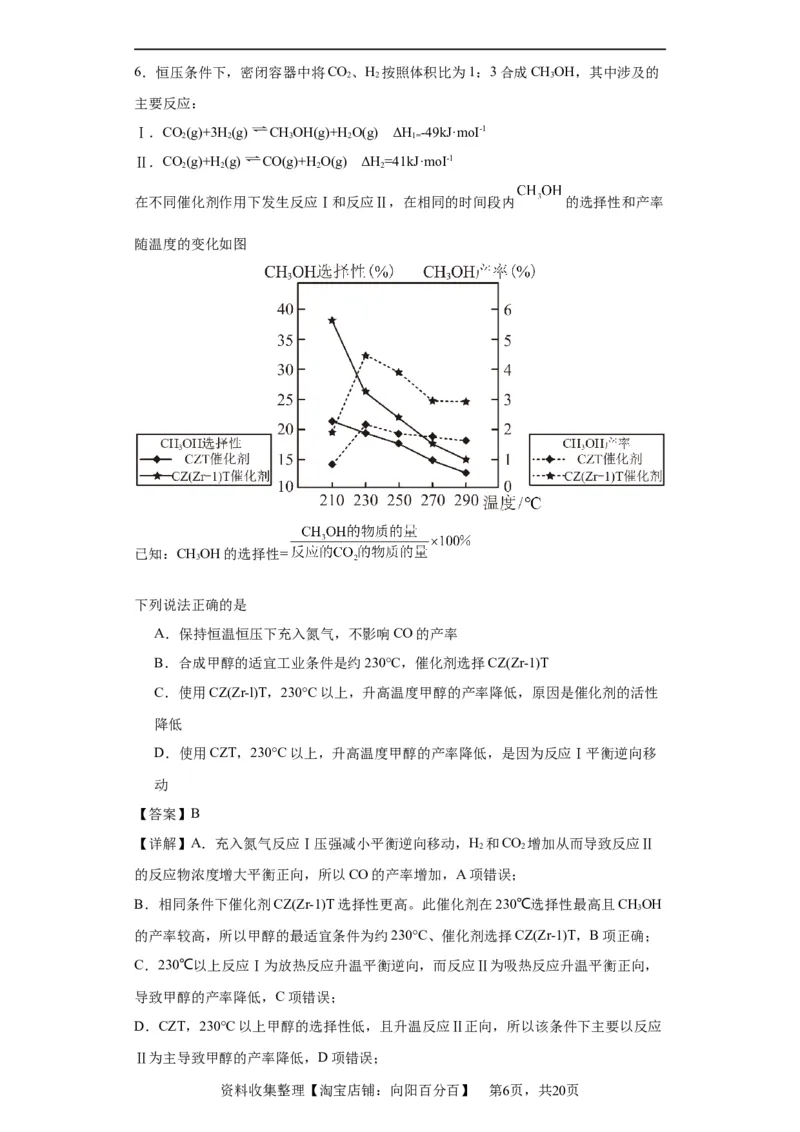
在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率
随温度的变化如图
已知:CHOH的选择性=
3
下列说法正确的是
A.保持恒温恒压下充入氮气,不影响CO的产率
B.合成甲醇的适宜工业条件是约230°C,催化剂选择CZ(Zr-1)T
C.使用CZ(Zr-l)T,230°C以上,升高温度甲醇的产率降低,原因是催化剂的活性
降低
D.使用CZT,230°C以上,升高温度甲醇的产率降低,是因为反应Ⅰ平衡逆向移
动
【答案】B
【详解】A.充入氮气反应Ⅰ压强减小平衡逆向移动,H 和CO 增加从而导致反应Ⅱ
2 2
的反应物浓度增大平衡正向,所以CO的产率增加,A项错误;
B.相同条件下催化剂CZ(Zr-1)T选择性更高。此催化剂在230℃选择性最高且CHOH
3
的产率较高,所以甲醇的最适宜条件为约230°C、催化剂选择CZ(Zr-1)T,B项正确;
C.230℃以上反应Ⅰ为放热反应升温平衡逆向,而反应Ⅱ为吸热反应升温平衡正向,
导致甲醇的产率降低,C项错误;
D.CZT,230°C以上甲醇的选择性低,且升温反应Ⅱ正向,所以该条件下主要以反应
Ⅱ为主导致甲醇的产率降低,D项错误;
资料收集整理【淘宝店铺:向阳百分百】 第6页,共20页故选B。
7.空气中的氮气可通过人工固氮获得氨气,氨气是重要的化工原料,通过氨氧化法可
制得硝酸,反应过程如图:
硝酸是一种强氧化性酸,制硝酸工业产生的尾气中含有氮氧化物,应处理后才能排放。
下列说法不正确的是
A.常温下,浓硝酸可盛放在铝制或铁制容器中
B.BaSO 固体能溶于稀硝酸,生成Ba(NO ),放出SO 气体
3 3 2 2
C.工业上,当转化①的反应达到平衡时,需不断地从混合气体中分离出NH ,将
3
未反应的原料气送回合成塔以提高原料的利用率
D.转化④中,当V(NO)∶V(O)=4∶1时,理论上NO 全部转化为HNO
2 2 2 3
【答案】B
【详解】A.常温下,铁、铝的表面被浓硝酸氧化,生成了一层致密的氧化物薄膜,
这层薄膜阻止了酸与内层金属的进一步反应,故常温下,浓硝酸可盛放在铝制或铁制
容器中,A正确;
B.硝酸是氧化性酸,BaSO 固体能溶于稀硝酸,被氧化生成硫酸钡,硝酸被还原生成
3
NO,B错误;
C.工业上,当转化①的反应达到平衡时,根据勒夏特列原理知需不断地从混合气体中
分离出NH ,将未反应的原料气送回合成塔以提高原料的利用率,C正确;
3
D.转化④中,当V(NO)∶V(O)=4∶1时,理论上NO 全部转化为HNO:
2 2 2 3
4NO +O +H O=4HNO ,D正确;
2 2 2 3
故选B。
8.1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大太满足了当时
日益增长的人口对粮食的需求。下图是合成氨生产流程示意图,下列说法不正确的是
试卷第7页,共20页
学科网(北京)股份有限公司A.“干燥净化”可以防止催化剂中毒
B.“压缩机加压”既提高了原料的转化率又加快了反应速率
C.“冷却”提高了原料的平衡转化率和利用率
D.“铁触媒”在生产过程中需使用外加热源持续加热
【答案】D
【详解】A.合成氨反应的原料中含有能使催化剂中毒的杂质,所以“干燥净化”可
以防止催化剂中毒,故A正确;
B.合成氨反应是气体体积减小的反应,增大压强,化学反应速率加快,平衡向正反应
方向移动,原料的转化率增大,所以“压缩机加压”既提高了原料的转化率又加快了
反应速率,故B正确;
C.氨气易液化,冷却时氨气转化为液氨,生成物的浓度减小,平衡向正反应方向移动,
原料的转化率增大,所以“冷却”提高了原料的平衡转化率和利用率,故C正确;
D.合成氨反应为放热反应,“铁触媒”在生产过程中可以通过反应放出的热量和热
交换达到反应所需的温度,不需使用外加热源持续加热,故D错误;
故选D。
9.下列有关工业生产的叙述正确的是
A.合成氨工业中增大压强既可加快反应速率,又可提高原料转化率,所以压强越
高越好
B.合成氨工业中将NH 液化分离,可加快正反应速率,提高N、H 的转化率
3 2 2
C.硫酸工业中,催化氧化SO 时常通入稍过量氧气,目的是提高SO 的转化率
2 2
D.自来水厂用液氯进行自来水的消毒时会加入少量液氨,发生以下反应,生成比
HClO稳定的NH Cl: ,目的是降低HClO的毒性
2
【答案】C
【详解】A.合成氨反应正向气体分子数减小,增大压强既能提高速率也能使平衡正
资料收集整理【淘宝店铺:向阳百分百】 第8页,共20页向移动提高原料转化率,但压强太高对设备要求提高,增加了生成成本,因此压强不
是越高越好,故A错误;
B.分离产物可使平衡正向移动,从而提高反应物的转化率,但降低浓度使速率降低,
故B错误;
C.硫酸工业中,适当增大反应物氧气的浓度,可使平衡正向移动,提高二氧化硫的转
化率,故C正确;
D.该处理方式的目的是防止HClO分解,并能缓慢释放HClO,让消毒更持久,故D
错误;
故选:C。
二、填空题
10.合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前常用醋
2 2 3
酸二氨合铜(I)溶液来吸收原料气中的CO,其反应是
。
(1)必须除去原料气中CO的原因为 。
(2)醋酸二氨合铜(I)溶液吸收CO的生产适宜条件应为_____。
A.低温高压 B.低温低压 C.高温高压 D.高温低压
(3)吸收CO后的醋酸二氨合铜溶液经过适当处理又可再生,恢复其吸收CO的能力以
供循环使用。醋酸二氨合铜溶液再生的生产适宜条件应是_____。
A.低温高压 B.低温低压 C.高温高压 D.高温低压
【答案】(1)防止合成塔中的催化剂中毒
(2)A
(3)D
【详解】(1)合成氨的流程中的除杂,是为了除去能使催化剂中毒的物质,题干中指
出:在合成氨的过程中必须除去 CO,因此 CO是属于使催化剂中毒的物质;
(2)吸收 CO 的反应是正反应为气体体积缩小的放热反应,因此为了使 CO尽最大
可能地被吸收,应采取高压、低温的办法使平衡正向移动;
(3)要使醋酸二氨合铜(I)溶液再生,即使平衡逆向移动,故必须采取低压、高温的办
法。
11.二氧化碳催化加氢制甲醇,能助力“碳达峰”。涉及反应有:
反应I.
试卷第9页,共20页
学科网(北京)股份有限公司反应II.
反应III.
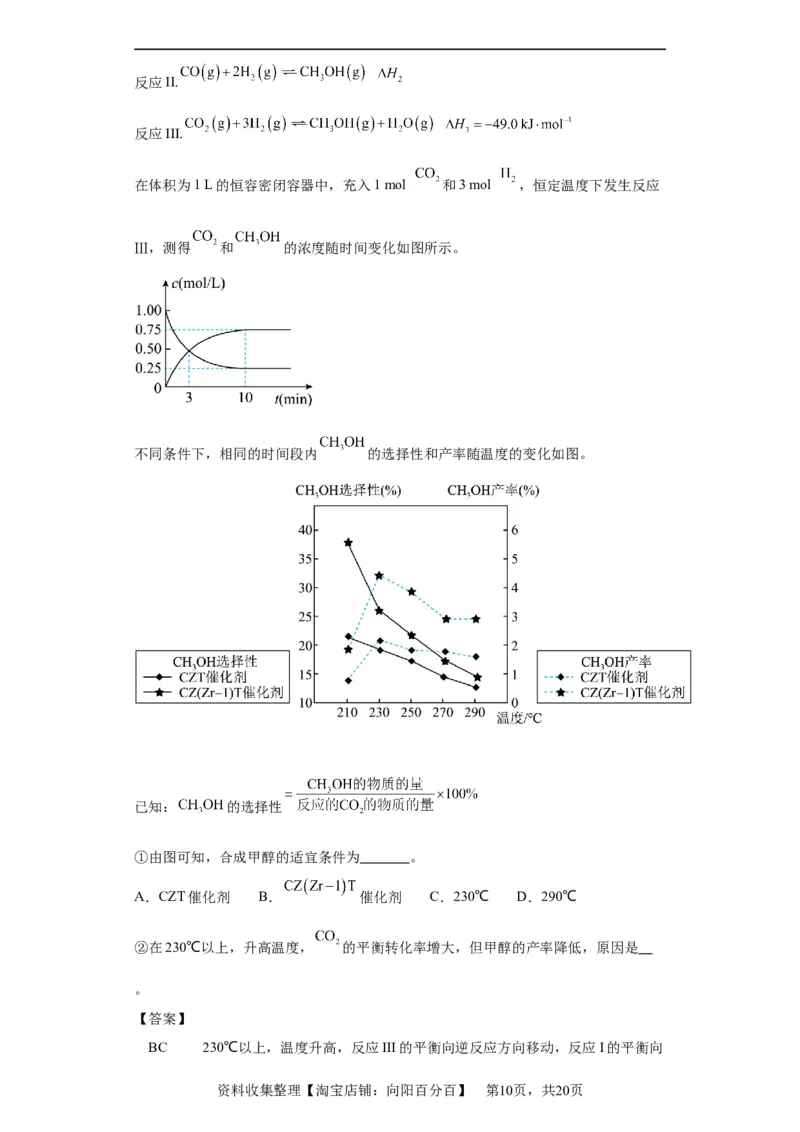
在体积为1 L的恒容密闭容器中,充入1 mol 和3 mol ,恒定温度下发生反应
Ⅲ,测得 和 的浓度随时间变化如图所示。
不同条件下,相同的时间段内 的选择性和产率随温度的变化如图。
已知: 的选择性
①由图可知,合成甲醇的适宜条件为 。
A.CZT催化剂 B. 催化剂 C.230℃ D.290℃
②在230℃以上,升高温度, 的平衡转化率增大,但甲醇的产率降低,原因是
。
【答案】
BC 230℃以上,温度升高,反应III的平衡向逆反应方向移动,反应I的平衡向
资料收集整理【淘宝店铺:向阳百分百】 第10页,共20页正反应方向移动
【详解】
①由图可知,使用CZ(Zr-1)T催化剂时CHOH的选择性和产率都比使用CZT催化剂时
3
大,故适宜的催化剂为CZ(Zr-1)T催化剂;在230℃时CHOH的选择性较高,CHOH
3 3
的产率最大,故适宜的温度为230℃;答案选BC。
②230℃以上,温度升高,反应III的平衡向逆反应方向移动,反应I的平衡向正反应方
向移动,则升高温度,CO 的平衡转化率增大,但甲醇的产率降低;答案为:230℃以
2
上,温度升高,反应III的平衡向逆反应方向移动,反应I的平衡向正反应方向移动。
12. CO可用于合成甲醇,反应方程式为CO(g)+2H(g) CHOH(g)。CO在不同温度
2 3
下的平衡转化率与压强的关系如图所示。该反应ΔH ⇌ 0(填“>”或“<”),实际生
产条件控制在250℃、1.3×104kPa左右,选择此压强而不选择更高压强的理由是
。
【答案】
< 在1.3×104kPa下,CO转化率已较高,再增大压强CO转化率提高不大,而生
产成本增加,得不偿失
【解析】
同一压强下,升高温度,CO的平衡转化率降低,平衡逆向移动,则该反应是放热反应,
ΔH<0;实际生产条件控制在250℃、1.3×104kPa左右,选择此压强而不选择更高压强
的理由是在1.3×104kPa下,CO转化率已较高,再增大压强CO转化率提高不大,而生
产成本增加,得不偿失。
13.脱除烟气中的氮氧化物(主要是指NO和NO )可以净化空气、改善环境,是环境保
2
护的主要课题。
(1)次氯酸盐氧化法。次氯酸盐脱除NO的主要过程如下:
i.NO+HClO=NO +HCl ii. NO+NO+H O 2HNO iii. HClO+HNO =HNO +HCl
2 2 2 2 2 3
①下列叙述正确的是 (填序号)。 ⇌
A.烟气中含有的少量O 能提高NO的脱除率
2
B.NO 单独存在时不能被脱除
2
试卷第11页,共20页
学科网(北京)股份有限公司C.脱除过程中,次氯酸盐溶液的pH下降
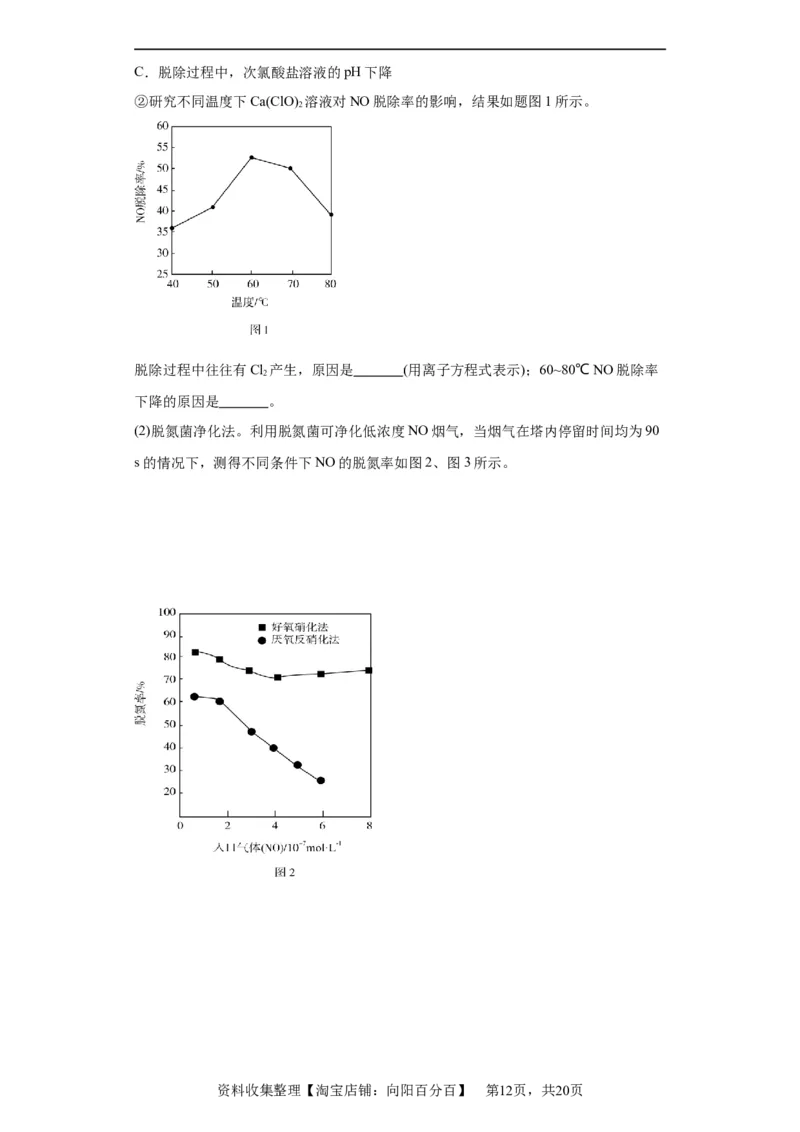
②研究不同温度下Ca(ClO) 溶液对NO脱除率的影响,结果如题图1所示。
2
脱除过程中往往有Cl 产生,原因是 (用离子方程式表示);60~80℃ NO脱除率
2
下降的原因是 。
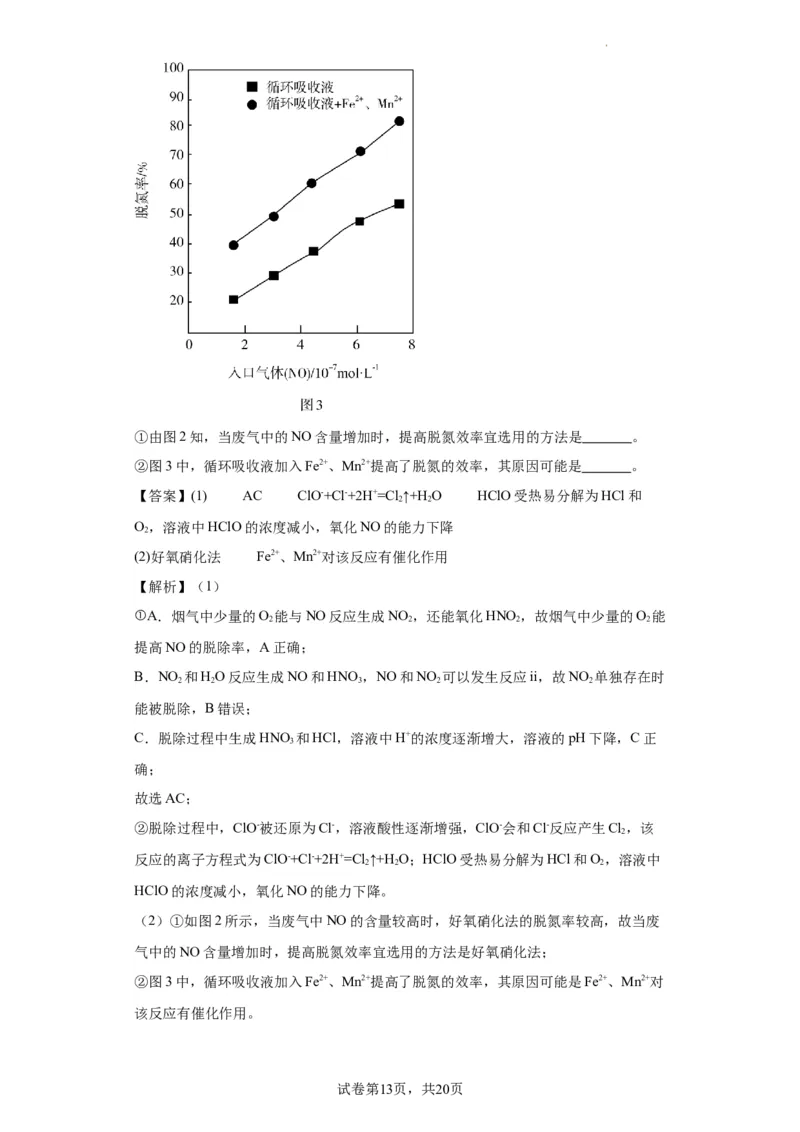
(2)脱氮菌净化法。利用脱氮菌可净化低浓度NO烟气,当烟气在塔内停留时间均为90
s的情况下,测得不同条件下NO的脱氮率如图2、图3所示。
资料收集整理【淘宝店铺:向阳百分百】 第12页,共20页①由图2知,当废气中的NO含量增加时,提高脱氮效率宜选用的方法是 。
②图3中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其原因可能是 。
【答案】(1) AC ClO-+Cl-+2H+=Cl↑+H O HClO受热易分解为HCl和
2 2
O,溶液中HClO的浓度减小,氧化NO的能力下降
2
(2)好氧硝化法 Fe2+、Mn2+对该反应有催化作用
【解析】(1)
①A.烟气中少量的O 能与NO反应生成NO ,还能氧化HNO,故烟气中少量的O 能
2 2 2 2
提高NO的脱除率,A正确;
B.NO 和HO反应生成NO和HNO,NO和NO 可以发生反应ii,故NO 单独存在时
2 2 3 2 2
能被脱除,B错误;
C.脱除过程中生成HNO 和HCl,溶液中H+的浓度逐渐增大,溶液的pH下降,C正
3
确;
故选AC;
②脱除过程中,ClO-被还原为Cl-,溶液酸性逐渐增强,ClO-会和Cl-反应产生Cl,该
2
反应的离子方程式为ClO-+Cl-+2H+=Cl↑+H O;HClO受热易分解为HCl和O,溶液中
2 2 2
HClO的浓度减小,氧化NO的能力下降。
(2)①如图2所示,当废气中NO的含量较高时,好氧硝化法的脱氮率较高,故当废
气中的NO含量增加时,提高脱氮效率宜选用的方法是好氧硝化法;
②图3中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其原因可能是Fe2+、Mn2+对
该反应有催化作用。
试卷第13页,共20页
学科网(北京)股份有限公司14.高效利用能源并且减少 的排放,对完成“碳中和”的目标有重要意义。
利用 与 合成甲醇涉及的主要反应如下:
a.
b.
试回答下列问题:
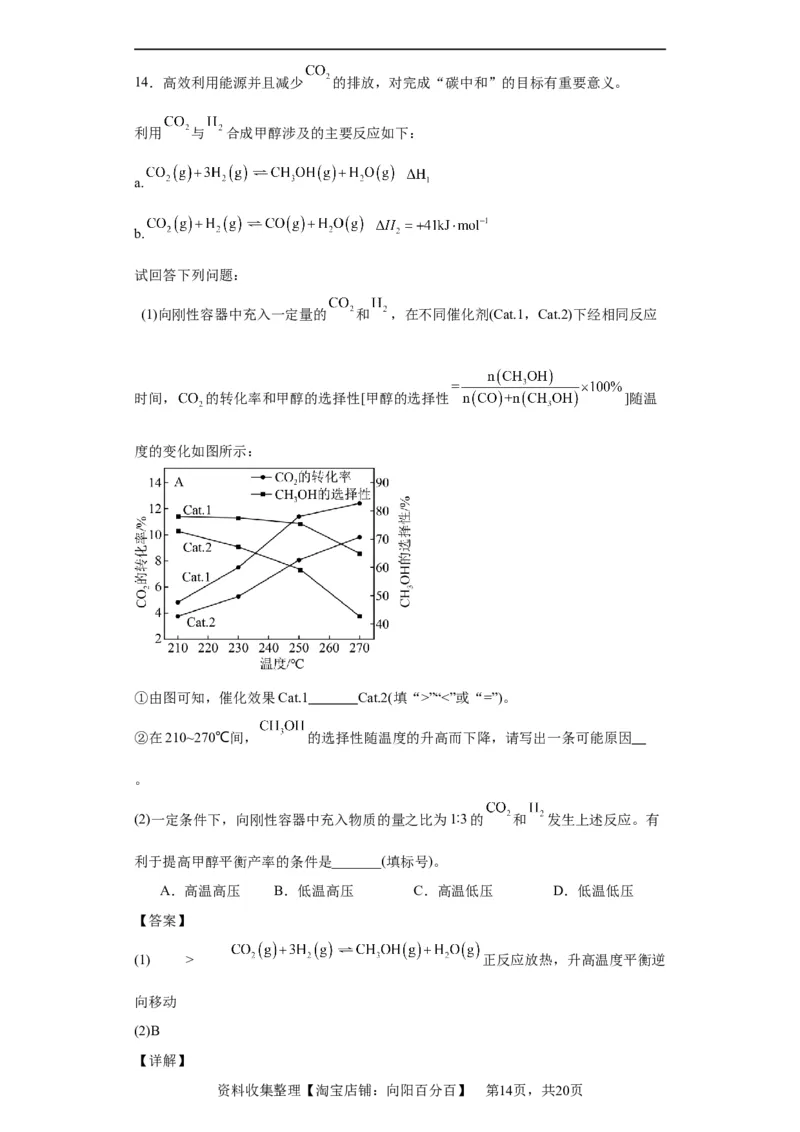
(1)向刚性容器中充入一定量的 和 ,在不同催化剂(Cat.1,Cat.2)下经相同反应
时间, 的转化率和甲醇的选择性[甲醇的选择性 ]随温
度的变化如图所示:
①由图可知,催化效果Cat.1 Cat.2(填“>”“<”或“=”)。
②在210~270℃间, 的选择性随温度的升高而下降,请写出一条可能原因
。
(2)一定条件下,向刚性容器中充入物质的量之比为1∶3的 和 发生上述反应。有
利于提高甲醇平衡产率的条件是_______(填标号)。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
【答案】
(1) > 正反应放热,升高温度平衡逆
向移动
(2)B
【详解】
资料收集整理【淘宝店铺:向阳百分百】 第14页,共20页(1)①根据图示,其它条件相同,Cat.1作催化剂时 的转化率和甲醇的选择性高,
所以催化效果Cat.1>Cat.2。
② 正反应放热,升高温度平衡逆向移动,所
以在210~270℃间, 的选择性随温度的升高而下降。
(2) 正反应放热,降低温度,平衡正向移动;
正反应气体物质的量减少,增大压强,平衡正向移动,所以有利于提高甲醇平衡产率
的条件是低温高压,选B;
15.金属钛具有密度小、强度高、耐腐蚀、无毒等优点,已广泛应用于航空航天工业,
并逐步进入了化工、船舶、汽车、体育器材、医疗等民用领域,并显示出了巨大的发
展潜力。还原法是工业上冶炼钛常用方法之一,该方法是以金红石(主要含 )为原
料来制取,其主要工艺流程如下:
试回答下列问题:
(1)已知反应①通常在800~900℃的条件下进行,产物中有一种可燃性无色气体,写出
反应①的化学方程式 。
(2)反应②通常在800℃的条件下进行,通入氩气的目的是 ;
(3)②中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为
℃。
试卷第15页,共20页
学科网(北京)股份有限公司【答案】(1)
(2)防止镁和钛在高温条件下被氧化
(3) 1000
【分析】金红石(主要含 )中加入焦炭,通入氯气发生反应生成TiCl ,同时生成
4
CO,在TiCl 中通入氩气、Mg得到Ti、MgCl ,电解氯化镁可得镁,海绵状钛经熔融
4 2
可得钛锭。
【详解】(1)反应①的反应物为 、 、 ,结合流程图知有 生成,利用
原子守恒及题给信息可知另一气体产物是 ,所以反应的化学方程式为
,答案为:
;
(2)反应②中反应物Mg以及产物Ti在高温下都易被空气中的氧气等氧化,所以通入
氩气的目的是防止镁和钛在高温条件下被氧化,答案为:防止镁和钛在高温条件下被
氧化;
(3)由图像可知应该选择1000℃,答案为:1000。
16.钌(Ru)是一种极其昂贵的稀有贵金属,广泛应用于电子、航空航天、石油化工、
有机合成等领域。钌的矿产资源很少,因此从含钌废渣中回收钌尤为重要。某含钌的
废渣主要成分为Ru、Pb、SiO、BiO(一种两性氧化物) ,回收钌的工艺流程如下:
2 2 3
(1)“氧化碱浸”时,两种氧化剂在不同温度下对钌浸出率和渣率的影响分别如图1、图
2所示,则适宜选择的氧化剂为 (填化学式);最佳反应温度为 。
资料收集整理【淘宝店铺:向阳百分百】 第16页,共20页【答案】(1) NaClO 200℃
【分析】含钌废料在碱性溶液中被氧化,Ru、 Pb 、 SiO 、 BiO 分别转化为
2 2 3
NaRuO 、 NaPbO 、NaSiO、 NaBiO,加甲酸还原,NaRuO 被还原为Ru(OH) ,
2 4 2 2 2 3 2 2 4 4
然后在氧化条件下蒸馏得到RuO,再加盐酸吸收,生成氯气和RuCl ,最后还原得到
3 3
钌。
【详解】(1)从图中可以看出,用NaClO钌浸出率更高,且渣率低,最佳温度控制
在200℃,此时钌的浸出率接近100%,且渣率最低。故答案为:NaClO;200℃;
17.钌 粉主要用于生产钌靶材,而钌靶材是生产计算机硬盘不可替代的材料。以
钌废料(废料中钌主要以单质的形式存在,还含有Al、Cr、Cr、CO、Ti、Fe等杂质)制
备高纯钌粉的流程如下:
已知:i.钌在碱性条件下被氯气氧化为 , 是有毒的挥发性物质,用盐酸吸
收得到红色 溶液,其中还含有少量 ;
ii. 易溶于水,微溶于酒精。
回答下列问题:
(1)钌废料在碱性条件下被氯气氧化的离子方程式为 ;钌废料氧化时,随着温度
的升高,钌的回收率变化如图所示。综合考虑,确定氧化时的温度以 ℃为宜。
试卷第17页,共20页
学科网(北京)股份有限公司【答案】(1) 80
【分析】钌废料被氯气氧化成 ,杂质被氧化成为氯化物,蒸馏出 ,
与盐酸反应生成 , 溶液浓缩后,加双氧水和氯化铵反应得到
沉淀, 煅烧得到 , 经氢气高温还原得到高纯度
钌粉,据此分析解答。
【详解】(1)钌废料在碱性条件下被氯气氧化为 ,根据得失电子守恒及元素守
恒得反应方程式: ,钌废料氧化时,随着温度
的升高,钌的回收率逐渐升高,在80℃左右回收率已经很高,再升高温度回收率增幅
不明显,且会增加能量消耗,因此温度80℃为宜,故答案为:
;80;
18.金属钪可用作宇航材料、火箭和飞机的制造材料;氧化钪可提高计算机记忆元件
性能。赤泥是铝土矿加工过程中产生的废料,含有丰富的钪元素,另含有 、 、
等氧化物。一种从赤泥中提取氧化钪的工艺流程如图所示( 是一种磷酸酯萃
取剂)
资料收集整理【淘宝店铺:向阳百分百】 第18页,共20页回答下列问题:
(1)为了提高酸浸时的浸出率可采取的措施是 (写2条)。
(2)写出赤泥经盐酸处理后所得“浸渣”与强碱溶液反应的离子方程式 。
(3)赤泥“酸浸”时温度过高,酸浸速率反而下降,其原因是 。
(4) 萃取浸出液,其浓度、料液温度对萃取率的影响如表所示,萃取时 最佳浓
度及料液温度分别为 、 。
浓度对萃取率的影响如表:
试验编 分相情
浓度/% 钪萃取率/% 铁萃取率/%
号 况
1-1 1 分相快 90.76 15.82
分相容
1-2 2 91.53 19.23
易
分相容
1-3 3 92.98 13.56
易
有第三
1-4 4 90.69 30.12
相
轻微乳
1-5 5 91.74 39.79
化
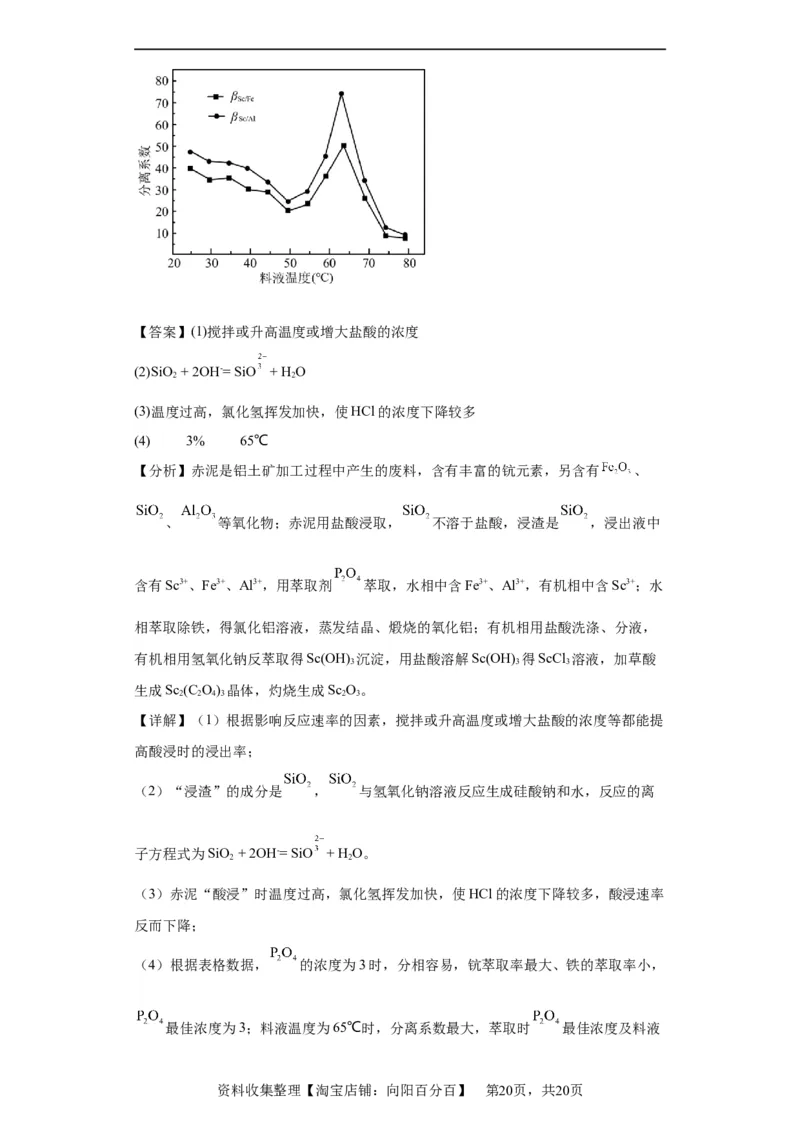
料液温度对分离系数的影响如图:
试卷第19页,共20页
学科网(北京)股份有限公司【答案】(1)搅拌或升高温度或增大盐酸的浓度
(2)SiO + 2OH-= SiO + H O
2 2
(3)温度过高,氯化氢挥发加快,使HCl的浓度下降较多
(4) 3% 65℃
【分析】赤泥是铝土矿加工过程中产生的废料,含有丰富的钪元素,另含有 、
、 等氧化物;赤泥用盐酸浸取, 不溶于盐酸,浸渣是 ,浸出液中
含有Sc3+、Fe3+、Al3+,用萃取剂 萃取,水相中含Fe3+、Al3+,有机相中含Sc3+;水
相萃取除铁,得氯化铝溶液,蒸发结晶、煅烧的氧化铝;有机相用盐酸洗涤、分液,
有机相用氢氧化钠反萃取得Sc(OH) 沉淀,用盐酸溶解Sc(OH) 得ScCl 溶液,加草酸
3 3 3
生成Sc (C O) 晶体,灼烧生成Sc O。
2 2 4 3 2 3
【详解】(1)根据影响反应速率的因素,搅拌或升高温度或增大盐酸的浓度等都能提
高酸浸时的浸出率;
(2)“浸渣”的成分是 , 与氢氧化钠溶液反应生成硅酸钠和水,反应的离
子方程式为SiO + 2OH-= SiO + H O。
2 2
(3)赤泥“酸浸”时温度过高,氯化氢挥发加快,使HCl的浓度下降较多,酸浸速率
反而下降;
(4)根据表格数据, 的浓度为3时,分相容易,钪萃取率最大、铁的萃取率小,
最佳浓度为3;料液温度为65℃时,分离系数最大,萃取时 最佳浓度及料液
资料收集整理【淘宝店铺:向阳百分百】 第20页,共20页温度分别为3、65℃。
19.Br 是一种重要的工业原料,沸点为59℃,微溶于水,有很强的挥发性和腐蚀性。
2
海水苦卤含溴(Br-)高达60mg•L-1,是非常宝贵的化工资源。从苦卤中提溴的一种工艺
流程如图1,回答下列问题:
(1)①不同pH下,Cl 的用量即配氯率(实际通入Cl 和理论需要Cl 的体积比)与所得溶
2 2 2
液中Br 的含量关系如图2所示。综合考虑,选择配氯率为和酸化的pH分别为 。
2
a.1.1,1 b.1.1,3 c.1.1,5 d.1,7
【答案】(1) a
【分析】氯气的氧化性强于Br ,海水苦卤中通入氯气,发生Cl+2Br-=Br +2Cl-,利用
2 2 2
液溴易溶于有机溶剂,然后分液,向有机相中通入碳酸钠,根据问题(2),液溴与碳酸
钠发生5Br +3Na CO=5NaBr+NaBrO +3CO ↑,然后分液,向水相2中通入硫酸,发生
2 2 3 3 2
5Br-+BrO +6H+=3Br +3H O,利用液溴易挥发,采用蒸馏方法得到液溴,据此分析;
2 2
【详解】(1)①由图可知,选择配氯率为1.1、酸化的pH为1.0时,所得溶液中溴的
含量最高,故答案为:a;
20.铈(Ce)是一种应用广泛的稀土元素,从氟碳铈矿(主要含CeFCO、Fe O、SiO)和
3 2 3 2
天青石(主要含SrSO 、并含有少量Ba、Ca等杂质)伴生矿中回收铈,同时生产高纯碳
4
酸锶(SrCO )的一种生产工艺流程如图:
3
试卷第21页,共20页
学科网(北京)股份有限公司已知:①铈的常见价态是+3和+4价;
②碳酸氢铵受热易分解
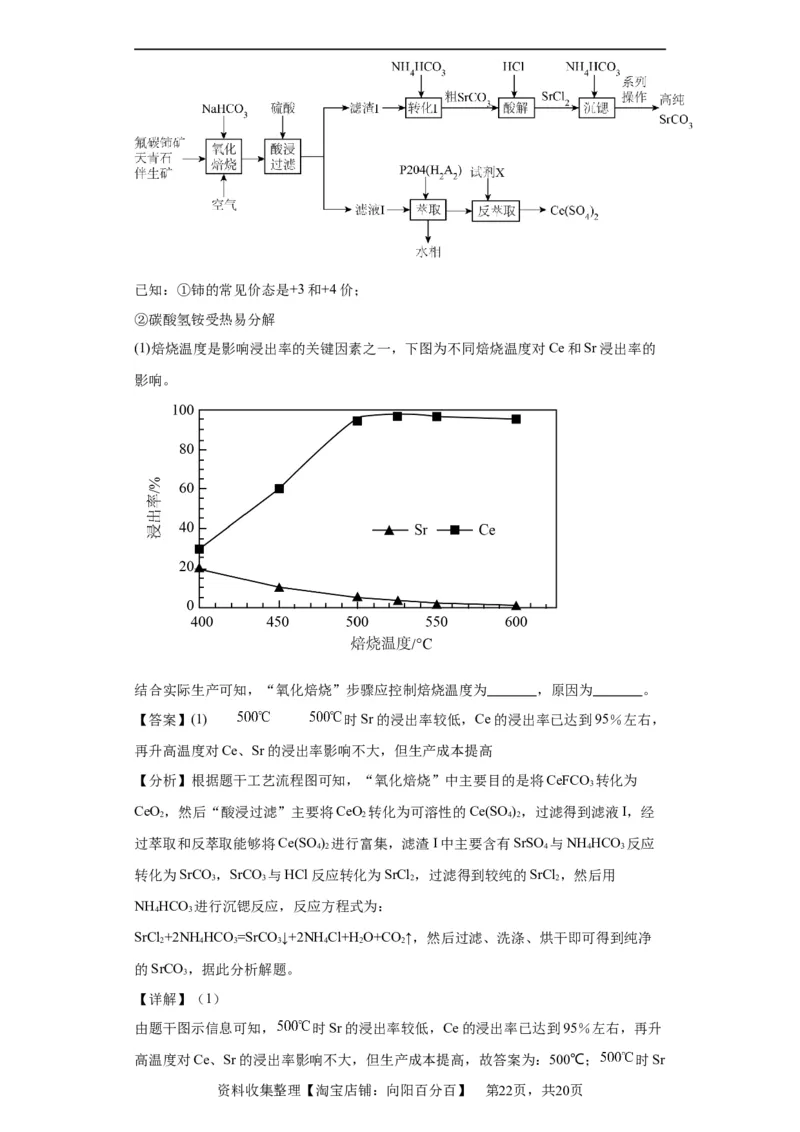
(1)焙烧温度是影响浸出率的关键因素之一,下图为不同焙烧温度对Ce和Sr浸出率的
影响。
结合实际生产可知,“氧化焙烧”步骤应控制焙烧温度为 ,原因为 。
【答案】(1) 时Sr的浸出率较低,Ce的浸出率已达到95%左右,
再升高温度对Ce、Sr的浸出率影响不大,但生产成本提高
【分析】根据题干工艺流程图可知,“氧化焙烧”中主要目的是将CeFCO 转化为
3
CeO,然后“酸浸过滤”主要将CeO 转化为可溶性的Ce(SO),过滤得到滤液I,经
2 2 4 2
过萃取和反萃取能够将Ce(SO) 进行富集,滤渣I中主要含有SrSO 与NH HCO 反应
4 2 4 4 3
转化为SrCO ,SrCO 与HCl反应转化为SrCl ,过滤得到较纯的SrCl ,然后用
3 3 2 2
NH HCO 进行沉锶反应,反应方程式为:
4 3
SrCl +2NHHCO =SrCO↓+2NHCl+H O+CO↑,然后过滤、洗涤、烘干即可得到纯净
2 4 3 3 4 2 2
的SrCO ,据此分析解题。
3
【详解】(1)
由题干图示信息可知, 时Sr的浸出率较低,Ce的浸出率已达到95%左右,再升
高温度对Ce、Sr的浸出率影响不大,但生产成本提高,故答案为:500℃; 时Sr
资料收集整理【淘宝店铺:向阳百分百】 第22页,共20页的浸出率较低,Ce的浸出率已达到95%左右,再升高温度对Ce、Sr的浸出率影响不
大,但生产成本提高。
试卷第23页,共20页
学科网(北京)股份有限公司