文档内容
微专题 06 “四型”和“四法”破解
与量有关离子方程式书写
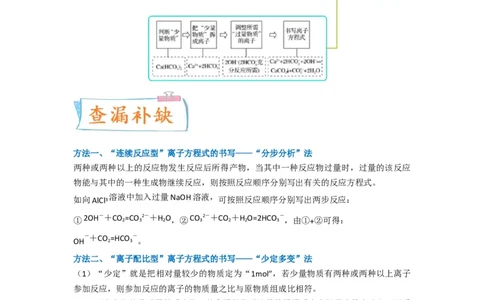
1.(2022·浙江·统考高考真题)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH ·H O= +2H O
3 2 2
【答案】C
【解析】A. 将碳酸氢钙溶液与过量的澄清石灰水混合,反应生成碳酸钙和水,反应的离子
方程式为: +Ca2++OH-=CaCO ↓+H O,选项A正确;
3 2
B. 将少量NO 通入NaOH溶液,反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:
2
2NO +2OH-= + +H O,选项B正确;
2 2
C. 将少量SO 通入NaClO溶液,反应生成硫酸钠和盐酸,反应的离子方程式为:
2
SO +H O+3ClO-= +2HClO+Cl-,选项C不正确;
2 2
D. 向氨水中滴入少量硝酸银溶液,反应生成氢氧化二氨合银,反应的离子方程式为:Ag+
+2NH ·H O= +2H O,选项D正确;
3 2 2
资料收集整理【淘宝店铺:向阳百分百】 1
学科网(北京)股份有限公司答案选C。
2.(2022·全国·高考真题)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH +2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
2 4 4
=BaSO ↓+2H O
4 2
【答案】D
【解析】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO
或NO ,反应的离子方程式为4H++2NO +S2-=S↓+2NO ↑+2H O(浓)或8H++2NO +3S2-
2 2 2
=3S↓+2NO↑+4H O(稀),A错误;
2
B.明矾在水中可以电离出Al3+,可以与氨水电离出的OH-发生反应生成Al(OH) ,但由于氨
3
水的碱性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3+
3
+3NH ·H O=Al(OH) ↓+3NH ,B错误;
3 2 3
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根
据其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO
+H O+CO =H SiO ↓+CO (CO 少量)或SiO +2H O+2CO =H SiO ↓+2HCO (CO 过量),C错误;
2 2 2 3 2 2 2 2 3 2
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的OH-
2 4 4 2
与NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO 反应生
4 4 2 4 4
成BaSO 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO =BaSO ↓+2H O,D正确;
4 4 2
故答案选D。
资料收集整理【淘宝店铺:向阳百分百】 2
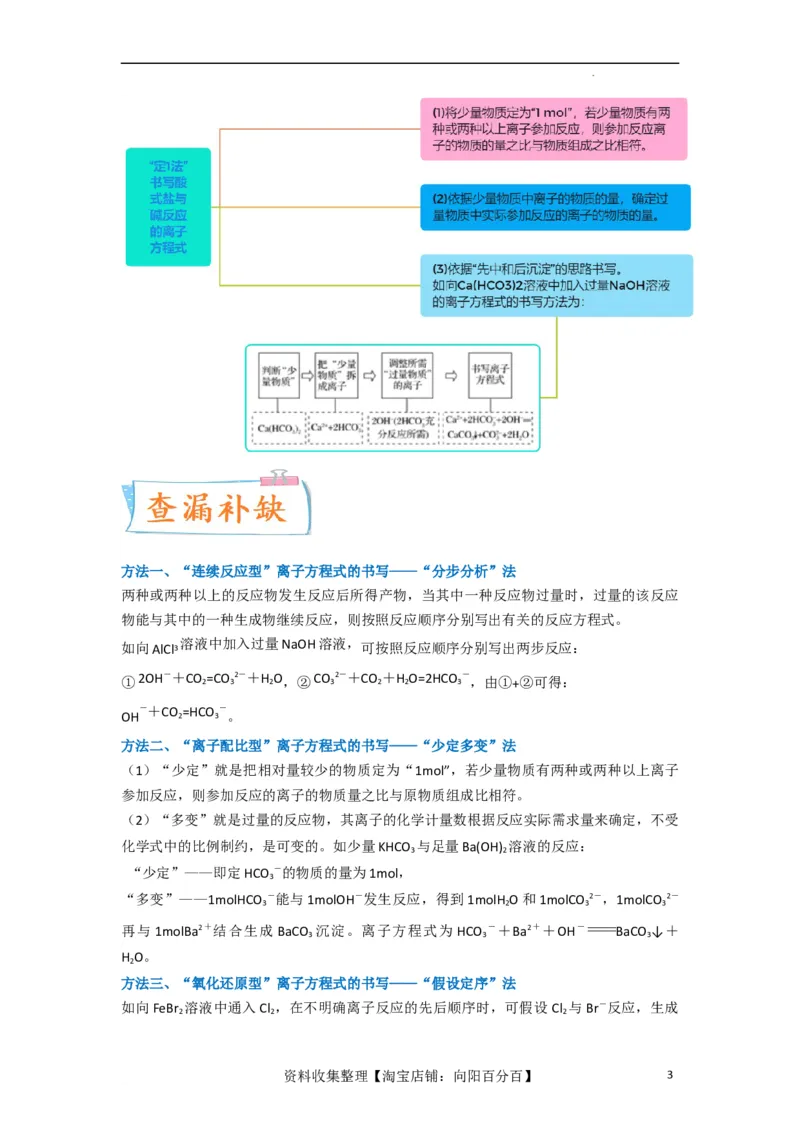
学科网(北京)股份有限公司方法一、“连续反应型”离子方程式的书写——“分步分析”法
两种或两种以上的反应物发生反应后所得产物,当其中一种反应物过量时,过量的该反应
物能与其中的一种生成物继续反应,则按照反应顺序分别写出有关的反应方程式。
如向AlCl3
溶液中加入过量NaOH溶液,
可按照反应顺序分别写出两步反应:
①2OH-+CO 2 =CO 3 2-+H 2 O,②CO 3 2-+CO 2 +H 2 O=2HCO 3 - ,由①+②可得:
OH -+CO 2 =HCO 3 - 。
方法二、“离子配比型”离子方程式的书写——“少定多变”法
(1)“少定”就是把相对量较少的物质定为“1mol”,若少量物质有两种或两种以上离子
参加反应,则参加反应的离子的物质量之比与原物质组成比相符。
(2)“多变”就是过量的反应物,其离子的化学计量数根据反应实际需求量来确定,不受
化学式中的比例制约,是可变的。如少量KHCO 与足量Ba(OH) 溶液的反应:
3 2
“少定”——即定HCO -的物质的量为1mol,
3
“多变”——1molHCO -能与1molOH-发生反应,得到1molH O和1molCO 2-,1molCO 2-
3 2 3 3
再与 1molBa2+结合生成 BaCO 沉淀。离子方程式为 HCO -+Ba2++OH- BaCO ↓+
3 3 3
H O。
2
方法三、“氧化还原型”离子方程式的书写——“假设定序”法
如向FeBr 溶液中通入Cl ,在不明确离子反应的先后顺序时,可假设 Cl 与Br-反应,生成
2 2 2
资料收集整理【淘宝店铺:向阳百分百】 3
学科网(北京)股份有限公司的溴单质还要氧化Fe2+生成Fe3+,这样即可确定Cl 先与Fe2+后与Br-反应,然后再根据量
2
的关系书写。
(1)①FeBr 溶液中通入少量Cl 2Fe2+ + Cl == 2Fe3+ + 2Cl-
2 2 2
②FeBr 溶液中通入与其等物质的量的氯气 2Fe2+ + 2Br- + 2Cl == 2Fe3+ + Br + 4Cl-
2 2 2
③FeBr 溶液中通入足量的氯气 2Fe2+ + 4Br- + 3Cl == 2Fe3+ + 2Br + 6Cl-
2 2 2
方法四、“反应先后型”离子方程式的书写——“强先弱后”法
一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因为
反应次序不同而跟用量有关,又可称为竞争型。依据“竞争反应,强者优先”的规律,解
决离子反应的先后顺序问题,先确定出反应先后的离子,再分步书写出离子方程式。
如:向含有H+、Al3+、NH +的溶液中,逐滴加入NaOH溶液至过量,反应的离子方程式依
4
次为
①H+ + OH- =H O
2
②Al3++3OH-= Al(OH) ↓
3
③NH + + OH- =NH .H O
4 3 2
④Al(OH)3+OH-=AlO2-+2H2O,
1.(2021·全国·高考真题)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:
B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
【答案】A
【解析】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方
程式为:C +CaSO =CaCO +S ,故A正确;
4 3
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H+
+2N =3Fe2++2NO↑+4H O,故B错误;
2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:
Al3++3OH-=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2+
+H S=CuS↓+2H+,故D错误;
2
答案选A。
资料收集整理【淘宝店铺:向阳百分百】 4
学科网(北京)股份有限公司2.(2019·浙江·高考真题)能正确表示下列离子方程式是
A.KI溶液久置空气中变黄色:4I-+O +2 H O = 2 I +4 OHˉ
2 2 2
B.少量三氧化硫与氨水反应:SO +NH ·H O = NH ++HSO -
3 3 2 4 4
C.Na与CuSO 水溶液反应:2Na+Cu2+ =Cu +2Na+
4
D.(NH ) SO 和FeSO 混合溶液与足量NaOH反应:Fe2++2 OHˉ= Fe(OH) ↓
4 2 4 4 2
【答案】A
【解析】A、碘离子会被空气中的氧气氧化为碘单质,选项A正确;B、硫酸氢根离子无法
在碱性条件下大量存在,选项B不正确;C、金属钠投入到硫酸铜水溶液中会先和水反应生
成氢氧化钠和氢气,接着氢氧化钠会和硫酸铜反应生成蓝色的氢氧化铜沉淀,选项C不正
确;D、氢氧化钠会和硫酸铵生成弱电解质一水合氨,要以化学式写在方程式中,选项D
不正确。答案选A。
1.(2023·全国·高三专题练习)指反应生成的离子因又能跟剩余(过量)的反应物继续反应
而跟用量有关。
(1) 通入 溶液中:
碱过量:_______;
碱不足:_______。
(2) 溶液与稀盐酸反应:
稀盐酸不足:_______;
稀盐酸过量:_______。
(3)铝盐溶液与强碱溶液反应:
铝盐过量:_______;
强碱过量:_______。
(4) 溶液与强酸溶液反应:
过量:_______;
强酸过量:_______。
(5) 通入 溶液中:
过量:_______;
不足:_______。
【答案】(1)
(2)
资料收集整理【淘宝店铺:向阳百分百】 5
学科网(北京)股份有限公司(3)
(4)
(5)
【解析】(1) 通入 溶液中,当NaOH过量时生成碳酸钠,离子方程式为:
;当 过量时生成碳酸氢钠,离子方程式为:
。
(2) 溶液与稀盐酸反应,当盐酸不足时生成碳酸氢钠,离子方程式为:
;当盐酸足量时生成二氧化碳和水,离子方程式为:
。
(3)铝盐溶液与强碱溶液反应,当铝盐过量时生成氢氧化铝,离子方程式为:
;当强碱过量时生成偏铝酸钠,离子方程式为:
。
(4) 溶液与强酸溶液反应,当 过量时生成氢氧化铝,离子方程式为:
;当强酸过量时生成铝离子,离子方程式为:
。
(5) 通入 溶液中,当 过量时生成氢氧化铝和碳酸钠,离子方程式为:
;当 过量时生成氢氧化铝和碳酸氢钠,离子
方程式为: 。
2.向含有OH-,CO 2-,AlO -的溶液中,逐滴加入稀盐酸至过量,因为结合质子的能力:
3 2
OH->AlO - > CO 2-,故反应的离子方程式依次为
2 3
(1)
(2)
(3)
(4)
【答案】(1)OH-+H++ H O
2
(2)AlO -+H++H O Al(OH) ↓
2 2 3
(3)CO 2-+2H+ H O+CO ↑
3 2 2
(4)Al(OH) +3H+ Al3++3H O
3 2
3.按用量要求书写下列离子方程式
资料收集整理【淘宝店铺:向阳百分百】 6
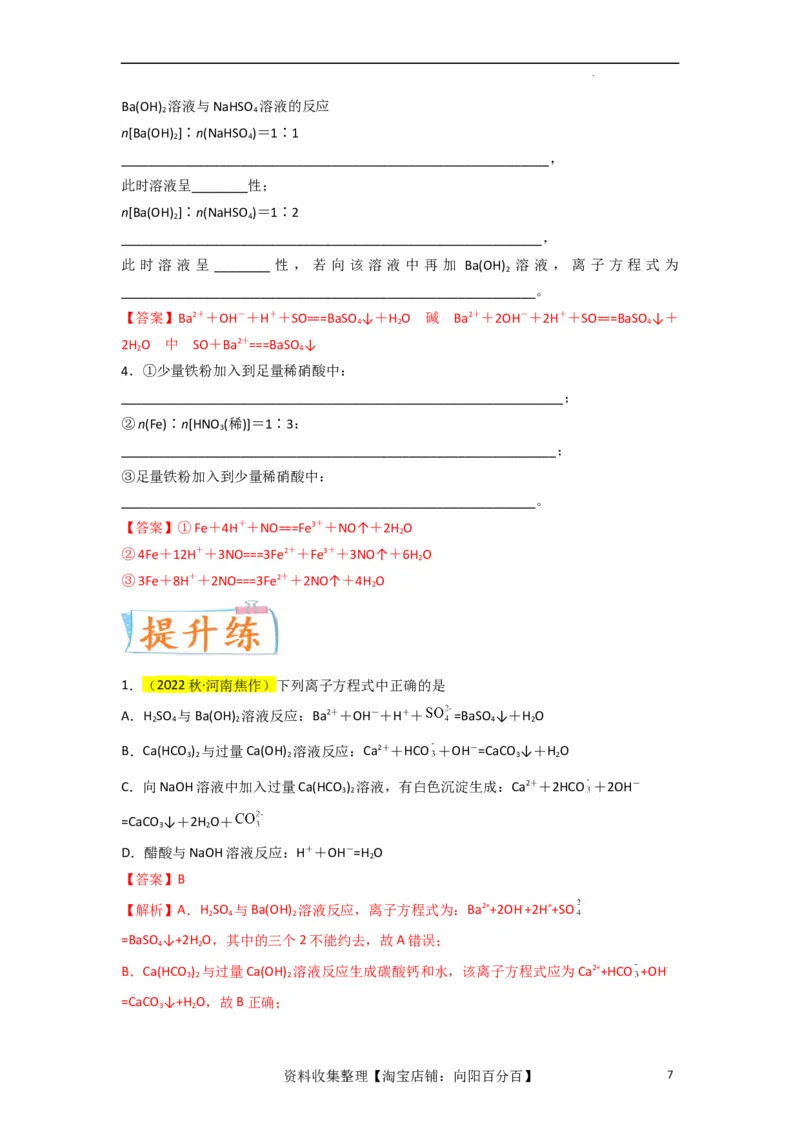
学科网(北京)股份有限公司Ba(OH) 溶液与NaHSO 溶液的反应
2 4
n[Ba(OH) ]∶n(NaHSO )=1∶1
2 4
_____________________________________________________________,
此时溶液呈________性;
n[Ba(OH) ]∶n(NaHSO )=1∶2
2 4
____________________________________________________________,
此 时 溶 液 呈 ________ 性 , 若 向 该 溶 液 中 再 加 Ba(OH) 溶 液 , 离 子 方 程 式 为
2
___________________________________________________________。
【答案】Ba2++OH-+H++SO===BaSO ↓+H O 碱 Ba2++2OH-+2H++SO===BaSO ↓+
4 2 4
2H O 中 SO+Ba2+===BaSO ↓
2 4
4.①少量铁粉加入到足量稀硝酸中:
_______________________________________________________________;
②n(Fe)∶n[HNO (稀)]=1∶3:
3
______________________________________________________________;
③足量铁粉加入到少量稀硝酸中:
___________________________________________________________。
【答案】①Fe+4H++NO===Fe3++NO↑+2H O
2
②4Fe+12H++3NO===3Fe2++Fe3++3NO↑+6H O
2
③3Fe+8H++2NO===3Fe2++2NO↑+4H O
2
1.(2022秋·河南焦作)下列离子方程式中正确的是
A.H SO 与Ba(OH) 溶液反应:Ba2++OH-+H++ =BaSO ↓+H O
2 4 2 4 2
B.Ca(HCO ) 与过量Ca(OH) 溶液反应:Ca2++HCO +OH-=CaCO ↓+H O
3 2 2 3 2
C.向NaOH溶液中加入过量Ca(HCO ) 溶液,有白色沉淀生成:Ca2++2HCO +2OH-
3 2
=CaCO ↓+2H O+
3 2
D.醋酸与NaOH溶液反应:H++OH-=H O
2
【答案】B
【解析】A.H SO 与Ba(OH) 溶液反应,离子方程式为:Ba2++2OH-+2H++SO
2 4 2
=BaSO ↓+2H O,其中的三个2不能约去,故A错误;
4 2
B.Ca(HCO ) 与过量Ca(OH) 溶液反应生成碳酸钙和水,该离子方程式应为Ca2++HCO +OH-
3 2 2
=CaCO ↓+H O,故B正确;
3 2
资料收集整理【淘宝店铺:向阳百分百】 7
学科网(北京)股份有限公司C.向NaOH溶液中加入过量Ca(HCO ) 溶液,有白色沉淀生成,发生反应的离子方程式为
3 2
Ca2++HCO +OH-=CaCO ↓+H O,故C错误;
3 2
D.CH COOH是弱电解质,不能拆,正确的离子方程式为:CH COOH+OH-═H O+CH COO-,
3 3 2 3
故D错误;
故答案为B。
2.(2023·安徽宣城·统考一模)下列离子方程式表示正确的是
A.向KOH溶液中通入少量、过量H S的离子方程式均为:H S+2OH-=S2-+2H O
2 2 2
B.向FeBr 溶液中通少量、过量Cl 的离子方程式均为:2Fe2++2Br-+2Cl =2Fe3++Br +4Cl-
2 2 2 2
C.向NaHCO 溶液中加入少量、过量Ba(OH) 溶液的离子方程式均为:Ba2++OH-+HCO
3 2
=BaCO ↓+H O
3 2
D.向C H ONa溶液中通入少量、过量CO 的离子方程式均为:H O+CO +C H O-→HCO
6 5 2 2 2 6 5
+C H OH
6 5
【答案】D
【解析】A.向KOH溶液中通入少量H S反应生成硫化钾和水:H S+2OH-=S2-+2H O;通入过
2 2 2
量H S生成硫氢化钾,H S+OH-=HS-+H O,A错误;
2 2 2
B.亚铁离子的还原性大于溴离子,向FeBr 溶液中通少量Cl ,反应生成铁离子和氯离子:
2 2
2Fe2++Cl =2Fe3++2Cl-;通入过量Cl 生成铁离子和溴单质:2Fe2++4Br-+3Cl =2Fe3++2Br +6Cl-,B
2 2 2 2
错误;
C.向NaHCO 溶液中加入少量Ba(OH) 溶液,钡离子、氢氧根离子完全反应生成碳酸钡沉
3 2
淀和碳酸根离子:Ba2++2OH-+2HCO =BaCO ↓+2H O+CO ;通入过量Ba(OH) 溶液,碳酸氢
3 2 2
根离子完全反应生成碳酸钡沉淀和水:Ba2++OH-+HCO =BaCO ↓+H O,C错误;
3 2
D.向C H ONa溶液中通入少量、过量CO 均生成苯酚和碳酸氢根离子:H O+CO +C H O-
6 5 2 2 2 6 5
→HCO +C H OH,D正确;
6 5
故选D。
3.(2023春·江苏南京)向含等物质的量浓度的FeI 、FeBr 混合溶液中通入一定量的氯气
2 2
后,再滴加少量的KSCN溶液,溶液变红。则下列离子方程式书写不合理的是
A.2I-+2Fe2++2Cl =2Fe3++I +4Cl-
2 2
B.2Br-+2I-+2Fe2++3Cl =I +Br +2Fe3++6Cl-
2 2 2
C.2Br-+4I-+2Fe2++4Cl =2I +Br +2Fe3++8Cl-
2 2 2
D.2Fe2++4I-+3Cl =2Fe3++2I +6Cl-
2 2
【答案】C
【解析】离子还原性: ,通入氯气后溶液中离子按照还原性强弱顺序依次反应,
由题意可知三种离子的物质的量量之比为:1:1:1,滴加KSCN溶液,溶液变红说明存在
三价铁离子,则可知碘离子完全反应。
资料收集整理【淘宝店铺:向阳百分百】 8
学科网(北京)股份有限公司A.通入氯气先于碘离子反应,然后再与 反应,两者可恰好按照1:1完全反应,离子
方程式合理,故A不选;
B.通入氯气足量时, 可按照1:1:1的比例完全反应,离子方程式合理,故
B不选;
C.若溴离子开始反应,则 应先于溴离子完全反应,且两者比例应保持1:1,因此
该离子方程式不合理,故C选;
D.通入氯气的量若使碘离子完全反应, 一半反应,则可得该离子方程式,反应合理,
故D不选;
故选:C。
4.(2023·全国·模拟预测)下列离子方程式正确的是
A.足量的CO 通入饱和碳酸钠溶液中:CO +CO +H O=2HCO
2 2 2
B.酸性条件下KIO 溶液与KI溶液反应生成I :5I-+IO +3H O=3I +6OH-
3 2 2 2
C.向NH Al(SO ) 溶液中滴入Ba(OH) 使SO 恰好完全反应:2Ba2++4OH-+Al3++2SO
4 4 2 2
=BaSO ↓+AlO +2H O
4 2
D.NH HSO 溶液中逐滴加入足量的Ba(OH) 溶液:NH +HSO +Ba2++2OH-
4 3 2
=BaSO ↓+NH ·H O+H O
3 3 2 2
【答案】D
【解析】A.由于碳酸氢钠的溶解度较小,足量的CO 通入饱和碳酸钠溶液中会析出碳酸氢
2
钠晶体,离子方程式应为2Na++CO +CO +H O=2NaHCO ,A错误;
2 2 3
B.酸性条件不会有氢氧根生成,正确离子方程式为5I-+IO +6H+=3I +3H O,B错误;
2 2
C.铵根也可以和氢氧根反应,SO 恰好完全反应时应生成氢氧化铝沉淀,正确离子方程
式为2Ba2++4OH-+Al3++NH 2SO =2BaSO ↓+Al(OH) ↓+NH ·H O,C错误;
4 3 3 2
D.NH HSO 溶液中逐滴加入足量的Ba(OH) 溶液生成亚硫酸钡沉淀和一水合氨,D正确;
4 3 2
综上所述答案为D。
5.(2023·上海·模拟预测)下列化学反应,相应的离子方程式一定正确的是
A.向 溶液中加入少量 溶液:
B. 溶液与一定量氯气反应,转移电子数为6.02×1023时:
C.将2.24L(标准状况)CO 通入500mL 0.3 mol·L-1 溶液中:
2
D.向 溶液通入少量SO :
2
资料收集整理【淘宝店铺:向阳百分百】 9
学科网(北京)股份有限公司【答案】C
【解析】A.Fe3+结合OH-能力更强,先产生Fe(OH) ,A项错误;
3
B.计算得FeBr 物质的量为1mol。还原性强弱:Fe2+>Br-,转移6.02×1023电子时只有Fe2+被
2
氧化即2Fe2++Cl =2Cl-+2Fe3+,B项错误;
2
C.CO 和NaOH物质的量之比为0.1:0.15=2:3,反应同时产生 和 ,该离子方程
2
式正确,C项正确;
D.HClO为强氧化性能将SO 氧化为 ,该反应表达错误,D项错误;
2
故选C。
6.(2023春·浙江杭州)下列指定反应的方程式不正确的是
A.向含有 和 的混合溶液中通入少量 :
B.同体积同浓度的 溶液与 溶液混合:
C.铜与浓硝酸溶液反应:
D.保存 溶液的试剂瓶用橡胶塞不用玻璃塞的原因是:
【答案】A
【解析】A.由于钙离子和碳酸根离子结合生成CaCO 沉淀,故向含有NaOH和Ca(OH) 的
3 2
混合溶液中通入少量CO 的离子方程式为:Ca2++CO +2OH-=CaCO ↓+H O,A符合题意;
2 2 3 2
B.已知NH HSO = +H++ ,H+结合OH-的能力比 强,则同体积同浓度的NH HSO
4 4 4 4
溶液与NaOH溶液混合:H++OH-=H O,B不合题意;
2
C.铜与浓硝酸溶液反应方程式为:Cu+4HNO (浓)=Cu(NO ) +2NO ↑+2H O,则其离子方程式
3 3 2 2 2
为: ,C不合题意;
D.保存NaOH溶液的试剂瓶用橡胶塞不用玻璃塞的原因是由于玻璃中的SiO 能与NaOH溶
2
液反应,其离子方程式为: ,D不合题意;
故答案为:A。
7.(2023·安徽马鞍山·统考二模)能正确表示下列反应的离子方程式为
A.新制氯水中加入少量CaCO : 2Cl +H O+CaCO =Ca2++2Cl-+CO ↑+2HClO
3 2 2 3 2
B.硫酸铜溶液中滴入几滴氨水: Cu2++4NH ·H O = [Cu(NH ) ]2++4H O
3 2 3 4 2
C.久置的H S溶液变浑浊: 2S2-+ O +4H+ = 2S↓+2H O
2 2 2
D.用铜电极电解硫酸铜溶液: 2Cu2+ +2H O 2Cu+O ↑+4H+
2 2
【答案】A
【解析】A.Cl 与水反应生成HCl与HClO,CaCO 与HCl反应生成CaCl 和CO 和H O,故A
2 3 2 2 2
正确;
资料收集整理【淘宝店铺:向阳百分百】 10
学科网(北京)股份有限公司B.硫酸铜溶液与浓氨水反应生成络合物,几滴氨水生成Cu(OH) 沉淀,不生成配合物
2
[Cu(NH ) ]2+,故B错误;
3 4
C.H S是弱电解质,不能拆成离子,故C错误;
2
D.电解反应为,阳极: ,阴极: ,总反应为:
,故D错误;
故答案选A。
8.(2023春·浙江杭州)下列离子方程式的书写及评价均合理的是
选
离子方程式 评价
项
将 通入含 的溶液中: 正确; 过量,可
A
将 、 全部氧化
溶液与足量的 溶液反应: 正确;酸式盐与碱反
B
应生成正盐和水
将过量 通入饱和 溶液中: 正确;生成
C
溶液
正确; 与
溶液和 溶液等体积混合:
D 消耗的 的
物质的量之比为2:3
A.A B.B C.C D.D
【答案】D
【解析】A.由于还原性:I->Fe2+,将2mol Cl 通入到含1 mol FeI 溶液中,Cl 将还原性强
2 2 2
的I-氧化完全,同时能将Fe2+氧化完全,Fe2+和I-按照化学式配比发生反应,反应离子方程式
为: ,A错误;
B.Mg(HCO ) 溶液与足量的NaOH溶液反应生成Mg(OH) 沉淀、碳酸钠和水,反应离子方
3 2 2
程式为Mg2++2HCO +4OH-═Mg(OH) ↓+2CO +2H O,B错误;
2 2
C.将过量 通入饱和 溶液中反应生成碳酸氢钠晶体,离子方程式为:
,C错误;
D.AlO −2与H+以1:1反应生成Al(OH) 沉淀,以1:4反应生成Al3+,等体积1 mol·L-1的
3
资料收集整理【淘宝店铺:向阳百分百】 11
学科网(北京)股份有限公司NaAlO 溶液和2.5 mol·L-1的HCl溶液中AlO 与H+的物质的量比为2:5,则AlO 与Al(OH)
2 3
消耗的H+的物质的量之比为2∶3,反应离子方程式为 ,
D正确;
故选:D。
9.(2023·全国·模拟预测)下列反应的离子方程式不正确的是
A.向MgSO 溶液中加入(NH ) CO 溶液生成Mg(OH) •MgCO :2Mg2++3CO
4 4 2 3 2 3
+2H O=Mg(OH) •MgCO ↓+2HCO
2 2 3
B.向CuSO 溶液中滴加过量的氨水:Cu2++2NH •H O=Cu(OH) ↓+2NH
4 3 2 2
C.向NaHSO 溶液中加入过量NaHSO 溶液:HSO +H+=H O+SO ↑
3 4 2 2
D.将等物质的量浓度的NH Al(SO ) 与Ba(OH) 溶液按体积比为1:2混合:NH +Al3++2SO
4 4 2 2
+2Ba2++4OH-=NH •H O+Al(OH) ↓+2BaSO ↓
3 2 3 4
【答案】B
【解析】A. 在溶液中会发生水解 ,水解生成的 和
未水解的 结合 生成 ,离子方程式为
,故A正确;
B.向CuSO₄溶液中滴加过量的氨水,先生成沉淀后沉淀溶解,最终生成硫酸四氨合铜,离
子方程式为 ,故B错误;
C.向NaHSO 溶液中加入过量NaHSO 溶液生成硫酸钠、二氧化硫、水,反应的离子方程式
3 4
为 ,故C正确;
D.将等物质的量浓度的NH Al(SO ) 与Ba(OH) 溶液按体积比为1:2混合,恰好完全反应生
4 4 2 2
成一水合氨、氢氧化铝沉淀、硫酸钡,离子方程式为
,故D正确;
选B。
10.(2023春·重庆沙坪坝·高三重庆八中校考阶段练习)下列表示对应化学反应的离子方
程式正确的是
A.将足量铁加入一定量稀硝酸中:3Fe+2NO +8H+=3Fe2++2NO↑+4H O
2
B.泡沫灭火器原理:2Al3++3CO +3H O=2Al(OH) ↓+3CO2↑
2 3
C.向Ca(ClO) 溶液中通入少量的SO :Ca2++ClO-+H O+SO =Cl-+CaSO ↓+2H+
2 2 2 2 4
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶1混合:Ba2++OH-+H++SO
2 4 4
=H O+BaSO ↓
2 4
资料收集整理【淘宝店铺:向阳百分百】 12
学科网(北京)股份有限公司【答案】A
【解析】A.将足量铁加入一定量稀硝酸中,最终得到Fe2+,生成的气体为NO,A项正确;
B.泡沫灭火器中物质为Al(OH) 和NaHCO , 和Al3+发生双水解反应,对应的离子方
3 3
程式为Al3++3HCO =Al(OH) ↓+3CO ↑,B项错误;
3 2
C.Ca(ClO) 具有强氧化性,可以氧化通入的少量SO ,生成的H+会和过量的ClO-结合生成
2 2
弱电解质HClO,对应的离子方程式为Ca2++3ClO-+SO +H O=CaSO ↓+Cl-+2HClO,C项错误;
2 2 4
D.NH HSO 与Ba(OH) 物质的量之比为1∶1, 会和OH-生成弱电解质NH H O,对应的
4 4 2 3 2
离子方程式为Ba2++2OH-+ +H++ =BaSO ↓+NH H O+H O,D项错误。∙
4 3 2 2
答案选A。 ∙
11.(2023秋·上海杨浦)下列能用离子方程式:Ca2++2 +2OH-=CaCO ↓+ +2H O
3 2
表示的反应是
A.Ca(OH) 与少量的NH HCO B.Ca(OH) 与足量的NaHCO
2 4 3 2 3
C.Ca(HCO ) 与少量的KOH D.Ca(HCO ) 与足量的Ca(OH)
3 2 3 2 2
【答案】B
【解析】A.Ca(OH) 与少量的NH HCO ,按照“少定多变”思想即碳酸氢铵定为1mol,则
2 4 3
Ca2++ +2OH-+ =CaCO ↓+NH ↑+2H O,故A不符合题意;
3 3 2
B.Ca(OH) 与足量的NaHCO ,按照“少定多变”思想即Ca(OH) 定为1mol,则Ca2++2
2 3 2
+2OH-=CaCO ↓+ +2H O,故B符合题意;
3 2
C.Ca(HCO ) 与少量的KOH,按照“少定多变”思想即KOH定为1mol,则Ca2++ +OH
3 2
-=CaCO ↓+H O,故C不符合题意;
3 2
D.Ca(HCO ) 与足量的Ca(OH) ,按照“少定多变”思想即Ca(OH) 定为1mol,则Ca2++
3 2 2 2
+OH-=CaCO ↓+H O,故D不符合题意。
3 2
综上所述,答案为B。
12.(2023秋·辽宁葫芦岛·高三统考期末)下列过程对应的离子反应方程式书写正确的是
A. 溶液与过量澄清石灰水混合:
B.明矾溶液与过量氨水混合:
C.用 溶液吸收少量 :
D.向水垢中滴加足量醋酸:
【答案】C
【解析】A.根据“以少定多”原则,NaHCO 溶液与过量的澄清石灰水反应的离子方程式
3
为: ,故A错误;
资料收集整理【淘宝店铺:向阳百分百】 13
学科网(北京)股份有限公司B.向明矾溶液加入过量氨水的离子反应为Al3++3 =Al(OH) ↓+3 ,故B错误;
3
C.用 溶液吸收少量 ,离子方程式为: ,故
C正确;
D.醋酸是弱酸,在离子方程式中不能拆,故D错误;
故选C。
13.(2023·全国·高三专题练习)一种反应物的两种或两种以上的组成离子,都能跟另一种
反应物的组成离子反应,但因反应次序不同而跟用量有关,又可称为竞争型。
(1) 溶液与 溶液的反应:
不足:_______;
过量:_______。
(2)向含有 的溶液中,逐滴加入 溶液至过量,反应依次为:
_______;
_______;
_______;
_______。
(3)向 溶液中通 :
少量:_______;
过量:_______。
【答案】(1)
(2)
(3)
【解析】(1)硫酸氢铵溶液与不足量氢氧化钠溶液反应生成硫酸铵、硫酸钠和水,反应的
离子方程式为 ,硫酸氢铵溶液与足量氢氧化钠溶液反应生成硫酸钠、一水
合氨和水,反应的离子方程式为 ,故答案为:
; ;
(2)向含有氢离子、铝离子和铵根离子的溶液中,逐滴加入氢氧化钠溶液至过量依次发生
的反应为,氢离子与氢氧根离子反应生成水,反应的离子方程式为 ,铝离
子与氢氧根离子反应生成氢氧化铝沉淀,反应的离子方程式为 ,
铵根离子与氢氧根离子反应生成一水合氨,反应的离子方程式为 ,
资料收集整理【淘宝店铺:向阳百分百】 14
学科网(北京)股份有限公司反应生成的氢氧化铝与氢氧根离子反应生成偏铝酸根离子和水,反应的离子方程式为
,故答案为: ; ;
; ;
(3)溴化亚铁溶液与少量氯气反应生成氯化铁和溴化铁,反应的离子方程式为
,溴化亚铁溶液与足量氯气反应生成氯化铁和溴,反应的离子方
程式为 ,故答案为: ;
。
资料收集整理【淘宝店铺:向阳百分百】 15
学科网(北京)股份有限公司