文档内容
微专题15 铜及其化合物的性质、制备与实验探究
1.(2023·全国·统考高考真题)一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变
化的是
A 硫酸亚铁溶液出现棕黄色沉淀
B 硫化钠溶液出现浑浊颜色变深
C 溴水颜色逐渐褪去
D 胆矾表面出现白色粉末
A.A B.B C.C D.D
2.(2020·海南·高考真题)向CuSO 溶液中滴加氨水至过量,下列叙述正确的是
4
A.先出现沉淀,后沉淀溶解变为无色溶液
B.离子方程式为Cu2+ + 4NH ·H O = [Cu(NH ) ]2+ + 4H O
3 2 3 4 2
C.Cu2+与 NH 中的氮原子以π键结合
3
D.NH 分子中∠HNH为109º28ˊ
3
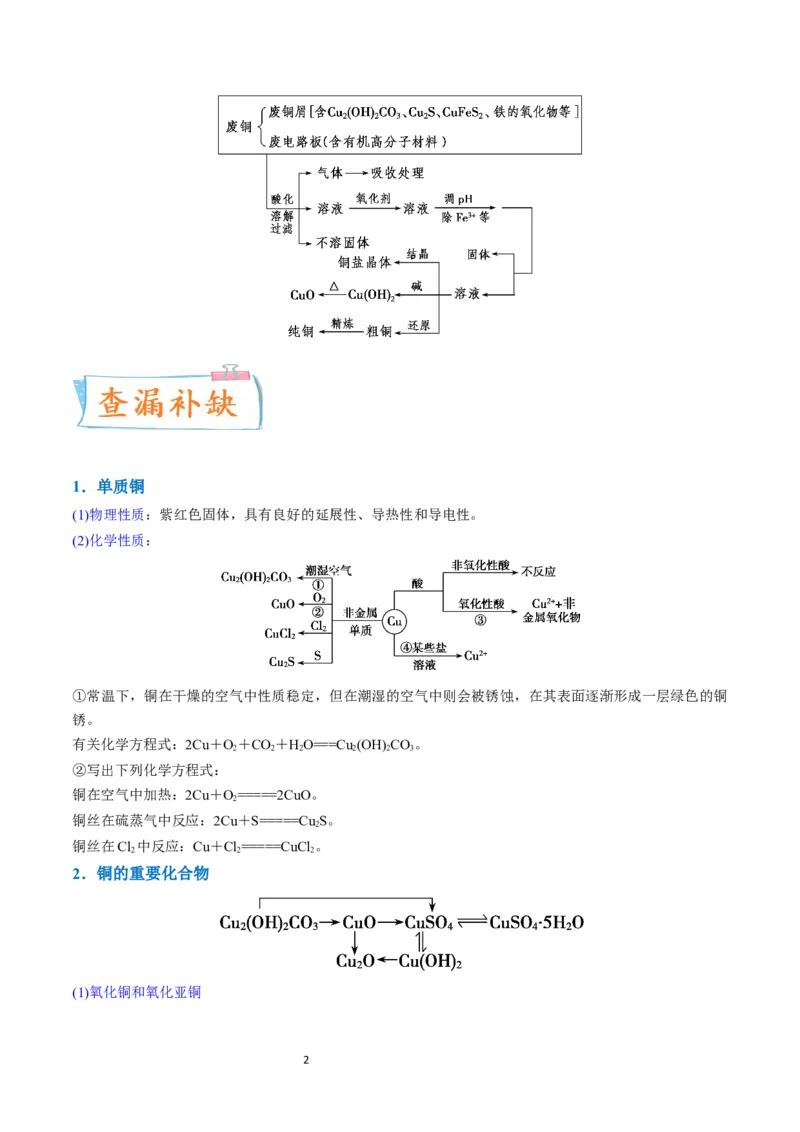
废铜综合利用的常见流程框图模式
11.单质铜
(1)物理性质:紫红色固体,具有良好的延展性、导热性和导电性。
(2)化学性质:
①常温下,铜在干燥的空气中性质稳定,但在潮湿的空气中则会被锈蚀,在其表面逐渐形成一层绿色的铜
锈。
有关化学方程式:2Cu+O+CO+HO===Cu (OH) CO。
2 2 2 2 2 3
②写出下列化学方程式:
铜在空气中加热:2Cu+O=====2CuO。
2
铜丝在硫蒸气中反应:2Cu+S=====Cu S。
2
铜丝在Cl 中反应:Cu+Cl=====CuCl 。
2 2 2
2.铜的重要化合物
(1)氧化铜和氧化亚铜
2名称 氧化铜 氧化亚铜
颜色 黑色 砖红色
与酸反应 CuO+2H+=== Cu O+2H+===
2
(H+) Cu2++HO Cu2++Cu+HO
2 2
(2)氢氧化铜
①物理性质:蓝色不溶于水的固体。
②化学性质及应用:
(3)铜盐
①Cu (OH) CO 的名称为碱式碳酸铜,是铜绿、孔雀石的主要成分,受热分解可生成黑色的氧化铜,化学
2 2 3
方程式:Cu (OH) CO 2CuO+CO↑+HO。
2 2 3 2 2
②CuSO ·5H O为蓝色晶体,俗称蓝矾、胆矾,其受热分解的化学方程式为 CuSO ·5H O CuSO +
4 2 4 2 4
5HO,蓝色晶体受热转化为白色粉末。无水CuSO 遇水变蓝色(生成CuSO ·5H O),据此可用来检验水的存
2 4 4 2
在。
(4)铜盐的毒性
铜盐溶液有毒,主要是因为铜离子能与蛋白质作用,使蛋白质变性失去生理活性,因此人们利用这一性质
用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。
3.铜及其化合物的制备
(1)工业上由黄铜矿(主要成分CuFeS )冶炼铜的主要流程如下:
2
(2)Cu S是火法炼铜的重要原料之一,下面是由Cu S冶炼铜及制取CuSO ·5H O的流程图:
2 2 4 2
Cu S――→Cu――→Cu O、CuO―――――→A――→B――――――――→胆矾
2 2
31.(2020·全国·高考真题)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿
色来自孔雀石颜料(主要成分为Cu(OH) ·CuCO ),青色来自蓝铜矿颜料(主要成分为Cu(OH) ·2CuCO )。下列说
2 3 2 3
法错误的是
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱
D.Cu(OH) ·CuCO 中铜的质量分数高于Cu(OH) ·2CuCO
2 3 2 3
2.(2020·全国·高考真题)北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则
成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是
A.胆矾的化学式为CuSO
4
B.胆矾可作为湿法冶铜的原料
C.“熬之则成胆矾”是浓缩结晶过程
D.“熬胆矾铁釜,久之亦化为铜”是发生了置换反应
1.(2023·湖北·统考二模)湖北随州出土的曾侯乙编钟属于青铜制品,先秦《考工记》记载:“金有六齐,
六分其金而锡居其一,谓之钟鼎之齐,……”。下列有关说法错误的是
A.青铜是一种铜锡合金
B.青铜硬度大但熔点比纯铜低
C.用硝酸处理青铜表面的铜锈[主要成分 ]
D.现代工艺采用电解精炼提纯铜,用粗铜作阳极
2.(2023·河北·高三专题练习)中国古代涉及的“铜”文化丰富多彩。下列说法错误的是
A.“青铜器时期”早于“铁器时期”的原因之一是铜比铁稳定
B.诗句“庐山山南刷铜绿”中的“铜绿”借指的是 的颜色
C.铸造“铜钱儿”用的材料黄铜是单质铜
D.“石胆化铁为铜”中涉及金属键的断裂
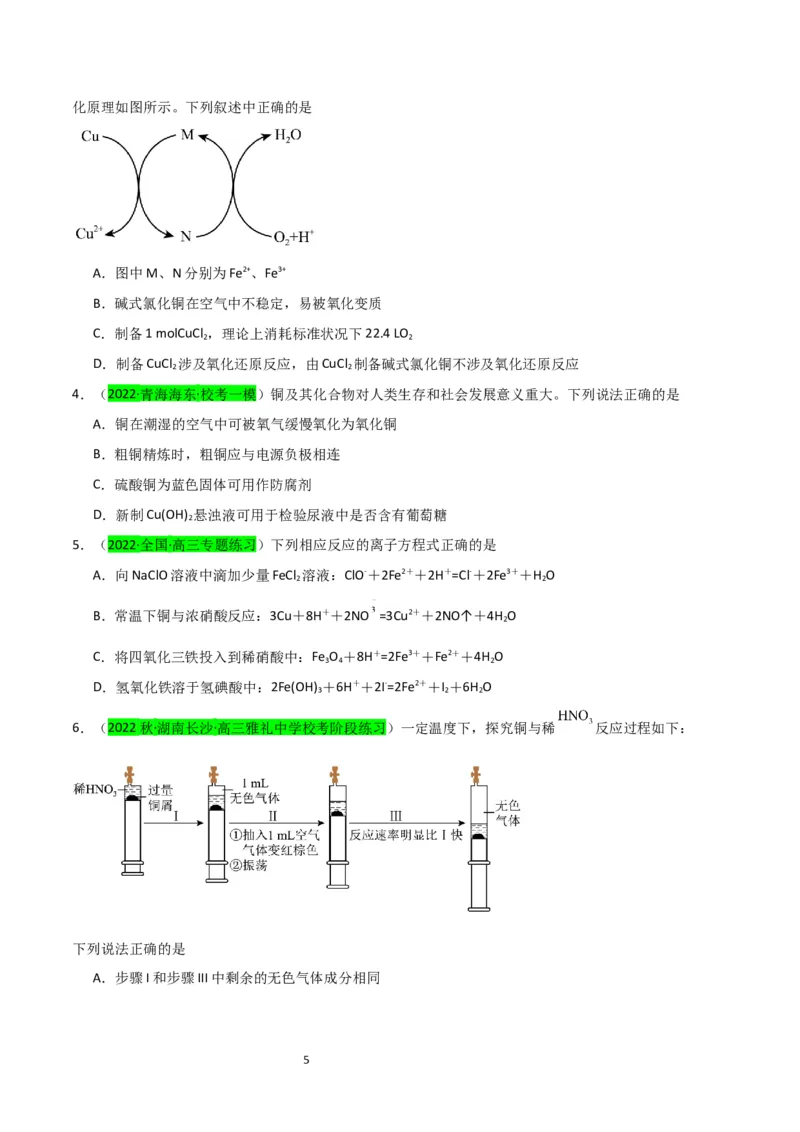
3.(2022秋·湖北宜昌·高三当阳一中校考期中)碱式氯化铜[CuCl(OH)·nH O]是一种农药。制备时先将
x y z 2
铜粉加入稀盐酸中,并持续通空气反应生成CuCl ,继而制得碱式氯化铜。Fe3+对该反应有催化作用,其催
2
4化原理如图所示。下列叙述中正确的是
A.图中M、N分别为Fe2+、Fe3+
B.碱式氯化铜在空气中不稳定,易被氧化变质
C.制备1 molCuCl ,理论上消耗标准状况下22.4 LO
2 2
D.制备CuCl 涉及氧化还原反应,由CuCl 制备碱式氯化铜不涉及氧化还原反应
2 2
4.(2022·青海海东·校考一模)铜及其化合物对人类生存和社会发展意义重大。下列说法正确的是
A.铜在潮湿的空气中可被氧气缓慢氧化为氧化铜
B.粗铜精炼时,粗铜应与电源负极相连
C.硫酸铜为蓝色固体可用作防腐剂
D.新制Cu(OH) 悬浊液可用于检验尿液中是否含有葡萄糖
2
5.(2022·全国·高三专题练习)下列相应反应的离子方程式正确的是
A.向NaClO溶液中滴加少量FeCl 溶液:ClO-+2Fe2++2H+=Cl-+2Fe3++H O
2 2
B.常温下铜与浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H O
2
C.将四氧化三铁投入到稀硝酸中:Fe O +8H+=2Fe3++Fe2++4H O
3 4 2
D.氢氧化铁溶于氢碘酸中:2Fe(OH) +6H++2I-=2Fe2++I +6H O
3 2 2
6.(2022秋·湖南长沙·高三雅礼中学校考阶段练习)一定温度下,探究铜与稀 反应过程如下:
下列说法正确的是
A.步骤I和步骤III中剩余的无色气体成分相同
5B.由实验可知, 可能对该反应具有催化作用
C.步骤III反应速率比I快的原因是 溶于水,使 增大
D.当活塞不再移动时,再抽入空气,铜不再溶解
7.(2022秋·黑龙江绥化·高三绥化市第一中学校考期中)一同学设计了两种由CuO→Cu的实验方案:
方案一:Zn H Cu;
2
方案二:CuO CuSO Cu。
4
大家认为方案二优于方案一,理由是:①节约能源;②Cu产率高;③产品纯净;④操作安全。其中,评
价正确的是
A.①②④ B.①②③ C.①③④ D.①②③④
8.(2022秋·河北衡水·高三河北深州市中学校考阶段练习)通过如图流程制备硝酸铜晶体,下列说法不正
确的是
A.将废铜片粉碎,可提高反应速率
B.若将废铜片直接用硝酸“溶解”,既产生污染又降低硝酸的利用率
C.用无水乙醇代替水“洗涤”的目的之一是减少晶体的溶解损失
D.为了使硝酸铜尽可能析出,“结晶”应将溶液蒸干
1.(2023·北京朝阳·统考二模)小组同学探究 和物质A的反应,实验如下。
序
装置 物质A 实验现象
号
铜粉溶解,溶液变为深棕色[经检验含
溶液(调
①
) ]
② 溶液 铜粉溶解,溶液变为蓝绿色
6③ 溶液(调 ) 无明显变化
下列分析不正确的是
A.②中铜粉溶解的原因:
B.①中产生 的原因: 时直接将 还原为
C.若向③中加入 固体,推测铜粉会溶解
D.①②③现象的差异不仅与物质氧化性(或还原性)强弱有关,也与反应速率有关
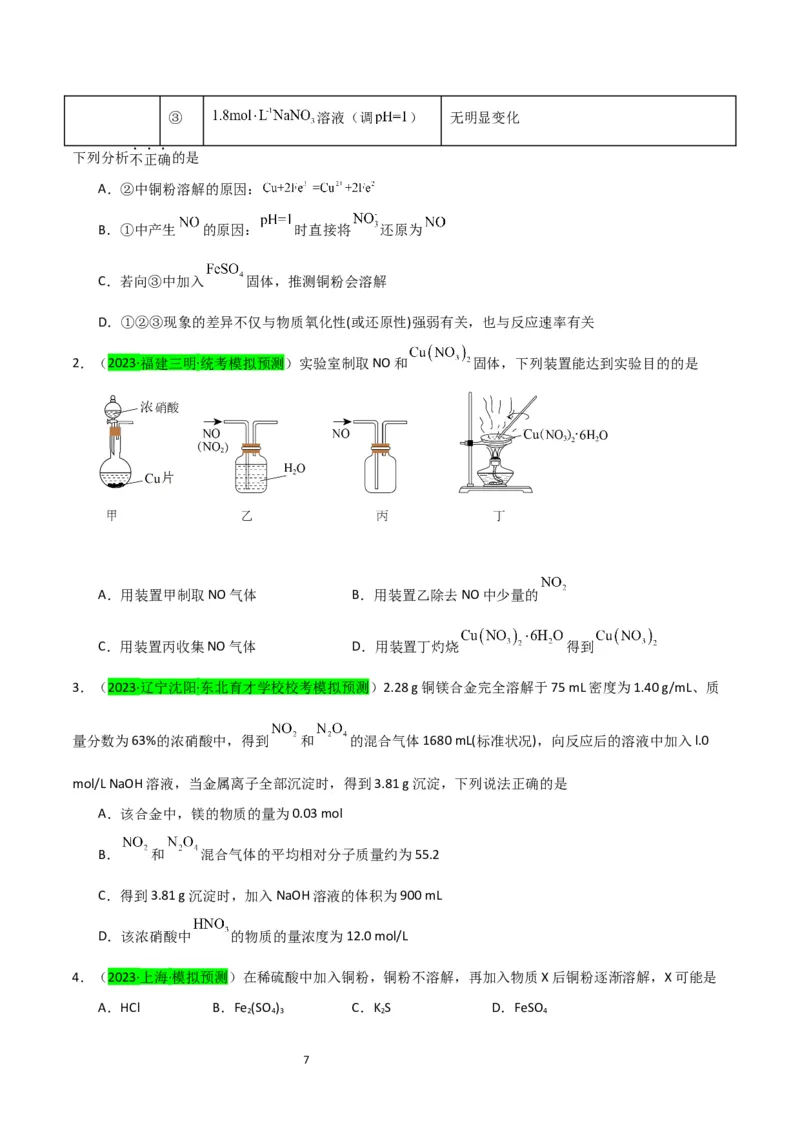
2.(2023·福建三明·统考模拟预测)实验室制取NO和 固体,下列装置能达到实验目的的是
A.用装置甲制取NO气体 B.用装置乙除去NO中少量的
C.用装置丙收集NO气体 D.用装置丁灼烧 得到
3.(2023·辽宁沈阳·东北育才学校校考模拟预测)2.28 g铜镁合金完全溶解于75 mL密度为1.40 g/mL、质
量分数为63%的浓硝酸中,得到 和 的混合气体1680 mL(标准状况),向反应后的溶液中加入l.0
mol/L NaOH溶液,当金属离子全部沉淀时,得到3.81 g沉淀,下列说法正确的是
A.该合金中,镁的物质的量为0.03 mol
B. 和 混合气体的平均相对分子质量约为55.2
C.得到3.81 g沉淀时,加入NaOH溶液的体积为900 mL
D.该浓硝酸中 的物质的量浓度为12.0 mol/L
4.(2023·上海·模拟预测)在稀硫酸中加入铜粉,铜粉不溶解,再加入物质X后铜粉逐渐溶解,X可能是
A.HCl B.Fe (SO ) C.K S D.FeSO
2 4 3 2 4
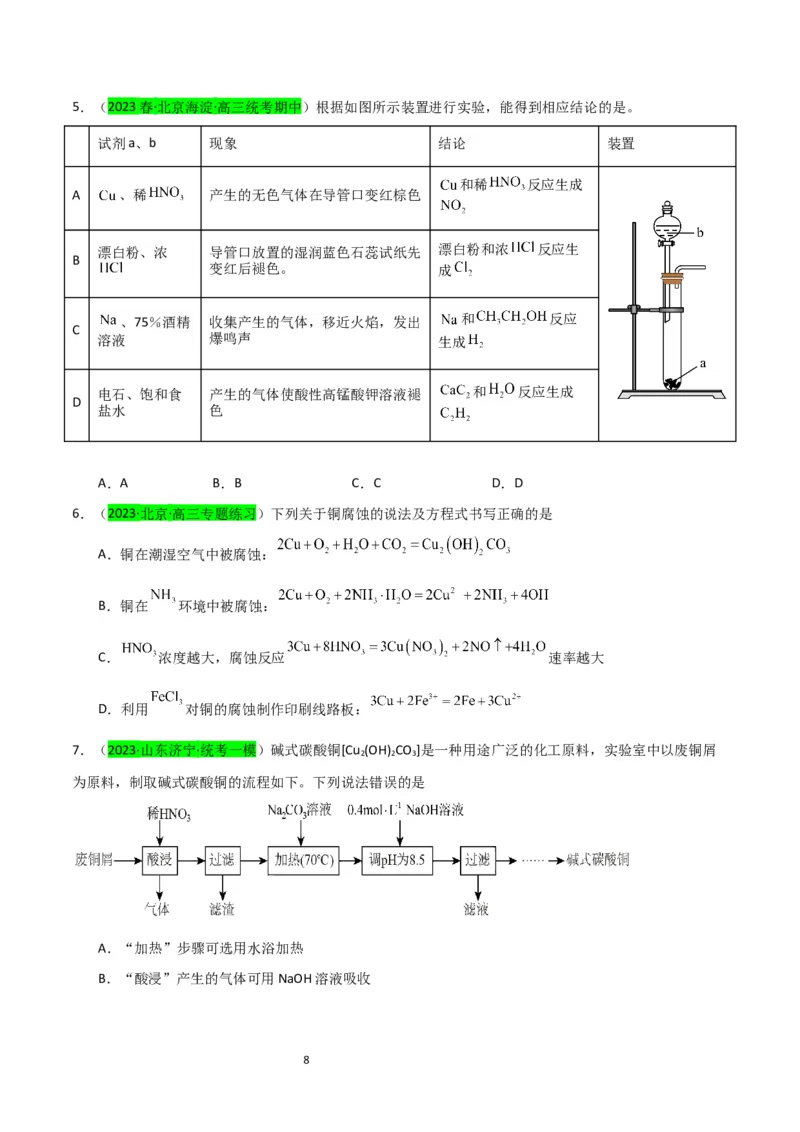
75.(2023春·北京海淀·高三统考期中)根据如图所示装置进行实验,能得到相应结论的是。
试剂a、b 现象 结论 装置
和稀 反应生成
A 、稀 产生的无色气体在导管口变红棕色
漂白粉、浓 导管口放置的湿润蓝色石蕊试纸先 漂白粉和浓 反应生
B
变红后褪色。 成
、75%酒精 收集产生的气体,移近火焰,发出 和 反应
C
溶液 爆鸣声 生成
电石、饱和食 产生的气体使酸性高锰酸钾溶液褪 和 反应生成
D
盐水 色
A.A B.B C.C D.D
6.(2023·北京·高三专题练习)下列关于铜腐蚀的说法及方程式书写正确的是
A.铜在潮湿空气中被腐蚀:
B.铜在 环境中被腐蚀:
C. 浓度越大,腐蚀反应 速率越大
D.利用 对铜的腐蚀制作印刷线路板:
7.(2023·山东济宁·统考一模)碱式碳酸铜[Cu (OH) CO ]是一种用途广泛的化工原料,实验室中以废铜屑
2 2 3
为原料,制取碱式碳酸铜的流程如下。下列说法错误的是
A.“加热”步骤可选用水浴加热
B.“酸浸”产生的气体可用NaOH溶液吸收
8C.“滤液”中溶质的主要成分为
D.可用盐酸和 溶液检验“滤液”中是否有
8.(2023·北京东城·北京五十五中校考模拟预测)氯化亚铜( )广泛应用于冶金工业,也用作催化剂和
杀菌剂。以硫化铜精矿为原料生产 的工艺如下:
已知: 难溶于醇和水,溶于 较大的体系 ,潮湿空气中易水解氧化。
(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是 。
(2)步骤2是溶解过程,溶解时反应的离子方程式 。
(3)步骤3为主反应, 的沉淀率与加入的 的量关系如图所示。
①反应的氧化产物是 ;
②比较 相对大小:A点 C点(填“>”、“<”或“=”);
③提高C点状态混合物中 沉淀率的措施是 ;
(4)步骤4进行的实验操作是 ;
(5)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是 。用乙醇洗涤的目的是 。
(6)产品纯度测定:称取 产品a g于锥形瓶中,加入足量的酸性 溶液使其充分溶解,然后用
标准溶液滴定 ,消耗 溶液b mL。(本实验中 的被还原为 ,不与
9产品中杂质和 反应)。
① 溶于 溶液的离子方程式是 。
②产品中 (摩尔质量为99g/mol)的质量分数为 。
9.(2023·海南海口·海南中学校考二模)纳米氧化亚铜(Cu O)是一种用途广泛的光电材料,以主要成分为
2
CuFeS 的黄铜矿(含有杂质SiO )为原料制取纳米Cu O的一种工艺流程如图所示:
2 2 2
请回答下列问题:
(1)“滤渣1”中含有硫单质及 。
(2)“调pH”的过程中也能用 (写出一种物质即可)来代替CuO,要使Fe3+完全沉淀,则溶液的pH
至少为 (已知该工艺条件下K [Fe(OH) ]≈8×10-38,Kw≈1×10-14,lg2≈0.3,化学上认为当离子浓度
sp 3
小于1×10-5mol·L-1时沉淀完全)。
(3)现代工业也可用铜作电极,电解食盐水制备Cu O,写出:a.阴极的电极反应式为 ;b.制
2
备氧化亚铜的化学方程式为 ;c.电解过程中Cl-的浓度 。(填“变小”“变大”
“不变”)
10.(2023·北京·高三专题练习)工业上可用过氧化氢为氧化剂浸取废旧线路板中的铜,某兴趣小组采取
不同方案进行实验并研究可行性。
方案1
实验装置 加入液体试剂 反应现象
10mL 30% 溶液 开始无明显现象,静置10小时后,溶液变为浅蓝色,铜片上有少
(pH约为4) 量蓝色沉淀,之后不再有明显变化
(1)实验结果表明,双氧水与铜可以缓慢的反应,其电极反应式可表示为
i.还原反应
10ii.氧化反应
(2)根据电极反应式,有同学设想可以通过以下方式加快反应。
i.增大 ,增强 的氧化性
ii.降低 ,增强Cu的还原性
(3)以此为依据设计了方案2与方案3
编
加入液体试剂 反应现象
号
开始产生少量气泡,溶液变为蓝色,片刻后,反应越来越剧烈,甚至形
方 10mL30% 溶液和
成大量泡沫涌出(经检测,生成气体可使带火星木条复燃),反应后剩余
案2
2mL 5mol/L 溶液 铜片表面光亮
方 10mL 30% 溶液和 生成较多气泡,溶液变为深蓝色。一段时间后,反应逐渐变慢,此时铜
案3
2mL 5mol/L 氨水
片上覆盖少量蓝色沉淀物。
方案2与方案3均在一定程度上加快了反应。
①方案2中,生成气体明显更剧烈的原因是 。
②方案3中发生主要反应的离子方程式为 。
③试评价方案2在回收铜过程的优缺点 。
(4)方案3中生成沉淀会降低铜的回收率并会阻碍反应进行,进一步改进方案获得了良好效果。
编号 加入液体试剂 反应现象
10mL 30% 溶液
方案4 2mL 5mol/L氨水 生成较多气泡,溶液变为深蓝色。反应后铜片变薄且表面光亮。
同时加入少量固体
试分析 的作用 。
(5)小组同学通过进一步探究发现,含有 和氨水的混合溶液能继续浸取单质铜。资料: 在
水溶液中不稳定,Cu(I)在溶液中能以 等形式稳定存在。
①用离子方程式表示上述反应原理 。
②通常条件下,含 的溶液不能与Cu发生反应,请从氧化还原角度分析此反应能够发生的原因 。
11