文档内容
(新高考)小题必练11:金属的腐蚀与防护
主要是在新高考中逐渐出现相关的题型,往常常与化学电源,电解原理等结合考查金属
的腐蚀与防护,特别是金属的防护中的几种重要的方法。常见的有铁的吸氧腐蚀和析氢腐蚀
为主。
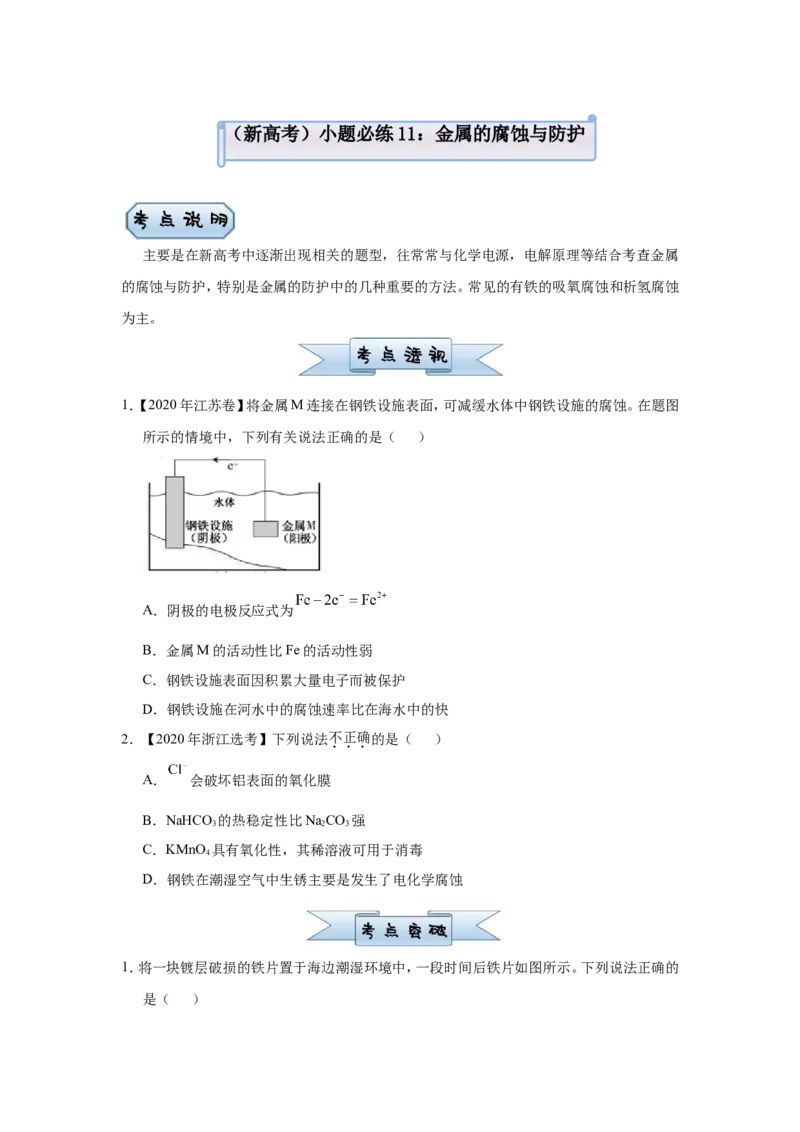
1.【2020年江苏卷】将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图
所示的情境中,下列有关说法正确的是( )
A.阴极的电极反应式为
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
2.【2020年浙江选考】下列说法不正确的是( )
A. 会破坏铝表面的氧化膜
B.NaHCO 的热稳定性比NaCO 强
3 2 3
C.KMnO 具有氧化性,其稀溶液可用于消毒
4
D.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
1.将一块镀层破损的铁片置于海边潮湿环境中,一段时间后铁片如图所示。下列说法正确的
是( )A.电子由镀层流向铁 B.铁片凹陷深处产生了较多OH−
C.镀层的金属性比铁弱 D.对铁进行了牺牲阳极的阴极保护
2.钢铁在潮湿的空气中会形成原电池而被腐蚀,下列说法正确的是( )
A.原电池的正极反应为:O+2H O+4e−=4OH−
2 2
B.原电池的负极反应为:Fe=Fe3++3e−
C.钢铁设备上连接铜块可以防止腐蚀
D.钢铁与外加直流电源的正极相连可以防止腐蚀
3.下列生产、生活中的事实不能用金属活动性顺序表解释的是( )
A.铝制器皿不宜盛放酸性食物
B.金属钠和熔融氯化钾反应置换出金属钾
C.电解饱和食盐水时,阴极区产生的是氢气
D.镀锌铁桶镀层破损后铁仍不易被腐蚀
4.(双选)考古中出土的锡青铜(铜锡合金)文物常有Cu (OH) Cl覆盖在其表面。下列说法正
2 3
确的是( )
A.锡青铜的熔点比纯铜低
B.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
C.锡青铜中的锡加速了铜的腐蚀速度
D.生成Cu (OH) Cl覆盖物是电化学腐蚀过程,但不是化学反应过程
2 3
5.下列事实不能用电化学理论解释的是( )
A.轮船船尾连接锌块
B.铝片不用特殊方法保护
C.纯锌与稀硫酸反应时,滴入少量的CuSO 溶液后速率加快
4
D.白口铁(镀锌的铁)比马口铁(镀锡的铁)耐用
6.某小组同学研究84消毒液(主要成分为NaClO)对铁的腐蚀作用:将等量的铁钉(铁碳合金)
和纯铁粉分别浸没于10mL 84消毒液中,记录现象如下:
1小时 2小时 5小时铁钉表面“生长”
铁钉表面出现少
铁钉 无明显现象 出
量红褐色物质
大量红褐色物质
纯铁粉 无明显现象 无明显现象 无明显现象
下列说法正确的是( )
A.铁钉主要发生的是化学腐蚀
B.铁钉腐蚀后的溶液中c(Cl−)增大
C.铁粉的腐蚀速率慢主要是由于其表面积大
D.84消毒液有强氧化性,因此Fe被腐蚀时发生:Fe-3e−=Fe3+
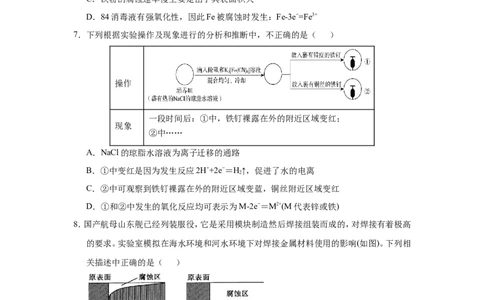
7.下列根据实验操作及现象进行的分析和推断中,不正确的是( )
操作
一段时间后:①中,铁钉裸露在外的附近区域变红;
现象
②中……
A.NaCl的琼脂水溶液为离子迁移的通路
B.①中变红是因为发生反应2H++2e−=H↑,促进了水的电离
2
C.②中可观察到铁钉裸露在外的附近区域变蓝,铜丝附近区域变红
D.①和②中发生的氧化反应均可表示为M-2e−=M2+(M代表锌或铁)
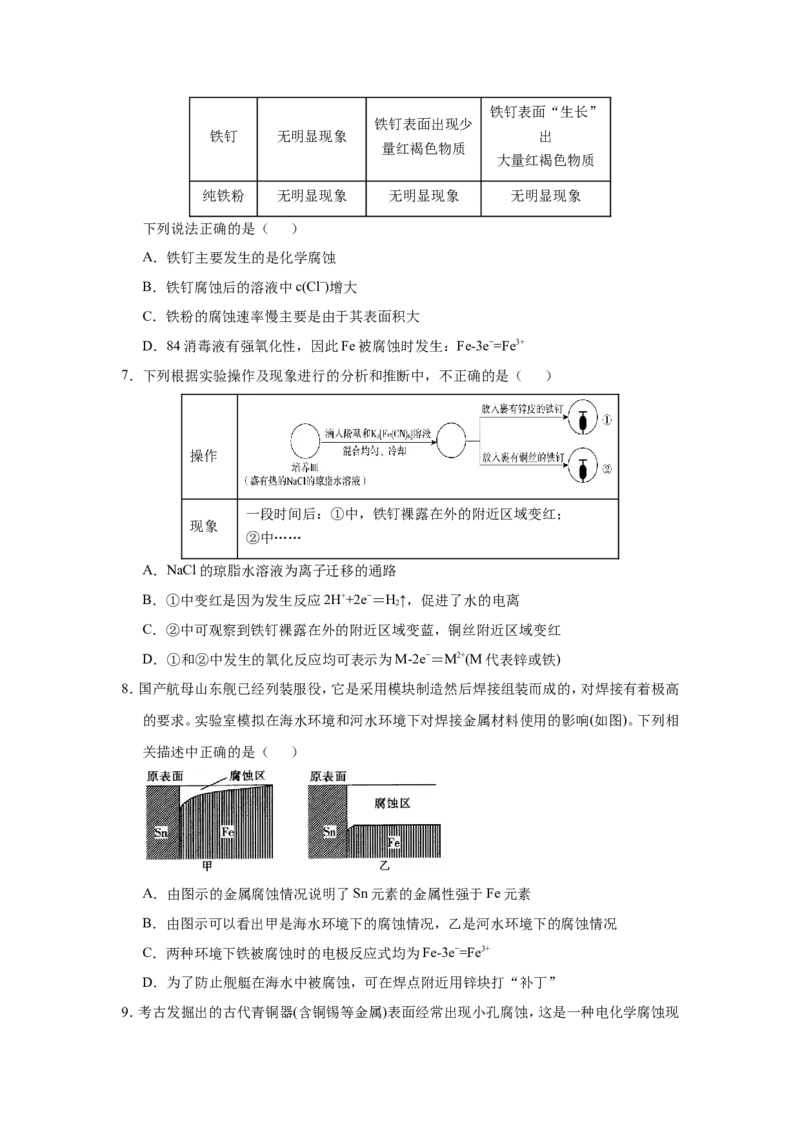
8.国产航母山东舰已经列装服役,它是采用模块制造然后焊接组装而成的,对焊接有着极高
的要求。实验室模拟在海水环境和河水环境下对焊接金属材料使用的影响(如图)。下列相
关描述中正确的是( )
A.由图示的金属腐蚀情况说明了Sn元素的金属性强于Fe元素
B.由图示可以看出甲是海水环境下的腐蚀情况,乙是河水环境下的腐蚀情况
C.两种环境下铁被腐蚀时的电极反应式均为Fe-3e−=Fe3+
D.为了防止舰艇在海水中被腐蚀,可在焊点附近用锌块打“补丁”
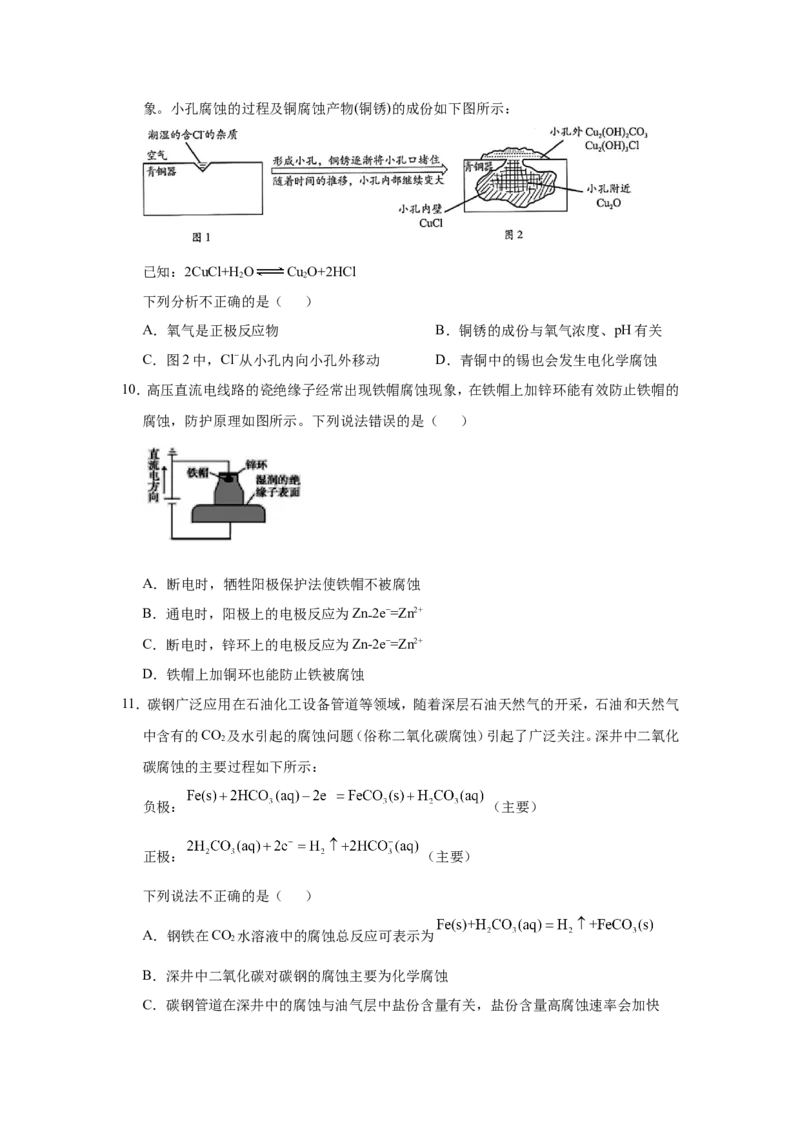
9.考古发掘出的古代青铜器(含铜锡等金属)表面经常出现小孔腐蚀,这是一种电化学腐蚀现象。小孔腐蚀的过程及铜腐蚀产物(铜锈)的成份如下图所示:
已知:2CuCl+H O Cu O+2HCl
2 2
下列分析不正确的是( )
A.氧气是正极反应物 B.铜锈的成份与氧气浓度、pH有关
C.图2中,Cl−从小孔内向小孔外移动 D.青铜中的锡也会发生电化学腐蚀
10.高压直流电线路的瓷绝缘子经常出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的
腐蚀,防护原理如图所示。下列说法错误的是( )
A.断电时,牺牲阳极保护法使铁帽不被腐蚀
B.通电时,阳极上的电极反应为Zn-2e−=Zn2+
C.断电时,锌环上的电极反应为Zn-2e−=Zn2+
D.铁帽上加铜环也能防止铁被腐蚀
11.碳钢广泛应用在石油化工设备管道等领域,随着深层石油天然气的开采,石油和天然气
中含有的CO 及水引起的腐蚀问题(俗称二氧化碳腐蚀)引起了广泛关注。深井中二氧化
2
碳腐蚀的主要过程如下所示:
负极: (主要)
正极: (主要)
下列说法不正确的是( )
A.钢铁在CO 水溶液中的腐蚀总反应可表示为
2
B.深井中二氧化碳对碳钢的腐蚀主要为化学腐蚀
C.碳钢管道在深井中的腐蚀与油气层中盐份含量有关,盐份含量高腐蚀速率会加快D.腐蚀过程表明含有CO 的溶液其腐蚀性比相同pH值的HCl溶液腐蚀性更强
2
12.如图为我国圆明园兽首铜像—兔首和鼠首,看上去仍熠熠生辉。下列对其原因的分析最
可能的是( )
A.它们表面的铜绿已用酸性溶液洗去
B.利用电镀原理在其表面镀了一层耐腐蚀的黄金
C.铜的活动性很弱,与空气成分不反应
D.它们是含一定比例金、银、锡、锌的铜合金
13.埋在地下的钢管常用如图所示方法加以保护,使其免受腐蚀,下列说法正确的是( )
A.金属棒X的材料可能为钠
B.金属棒X的材料可能为铜
C.钢管附近土壤的pH增大
D.这种方法称为外加电流的阴极保护法
参考答案考点透视
1.【答案】C
【解析】阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;阳极
金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性
比Fe的活动性强,故B错误;金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表
面积累大量电子,自身金属不再失电子从而被保护,故C正确;海水中的离子浓度大于河水
中的离子浓度,离子浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在
河水中快,故D错误;故选:C。
【点睛】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属M作负极,
钢铁设备作正极。
2.【答案】B
【解析】Cl−很容易被吸附在铝表面的氧化膜上,将氧化膜中的氧离子取代出来,从而破坏
氧化膜,A选项正确;B.碳酸氢钠受热分解可产生碳酸钠、水和二氧化碳,则稳定性:
NaHCO <NaCO,B选项错误;C.KMnO 具有强氧化性,可使病毒表面的蛋白质外壳变形,
3 2 3 4
其稀溶液可用于消毒,C选项正确;D.钢铁在潮湿的空气中,铁和碳、水膜形成原电池,发生
电化学腐蚀,腐蚀速率更快,D选项正确;答案选B。
【点睛】金属的腐蚀与电解质溶液有关。
考点突破
1.【答案】C
【解析】A.由图可知,铁片被腐蚀,说明铁做负极,电子由铁流向镀层金属,故A不选;B.
铁皮作负极,失电子产生较多的Fe2+,即铁皮凹陷处产生较多的Fe2+,故B不选;C.构成原电
池的条件之一就是由两活性不同的电极,由图可知,铁片被腐蚀,说明铁做负极,所以镀层金
属的金属性比铁弱,故选C;D.如果镀层金属的金属性别铁强,则铁为正极,镀层为负极,则
为栖牲阳极保护阴极,但本题中镀层金属的金属性比铁弱,不属于牺牲阳极阴极保护法,故
D不选;答案选C。
2.【答案】A
【解析】A.钢铁在潮湿的空气中形成原电池,发生的主要是吸氧腐蚀,铁作负极,碳作正
极,正极上氧气得电子发生还原反应,电极反应式为:O+2H O+4e−=4OH−,A正确;B.原电池
2 2
的负极反应为:Fe-2e−=Fe2+,B错误;C.铁、铜相连和合适的电解质溶液能构成原电池,由于金属活动性Fe>Cu,所以铁作负极,负极上铁更易失电子而被腐蚀,C错误;D.钢铁与外加直
流电源的正极连接时,Fe作阳极,阳极上铁失电子生成亚铁离子而被腐蚀,D错误;故合理选
项是A。
【点睛】金属的防腐蚀措施常常利用外加电源的阴极保护法,将需保护的金属与电源的负
极相连和牺牲阳极的阴极保护法,选用比被保护的金属性强的金属与之相连。
3.【答案】B
【解析】A.金属活动顺序表中,铝排在氢的前面,铝能置换出氢,所以铝制器皿不宜盛放
酸性食物,A不合题意;B.在金属活动顺序表中,金属钠排在钾的后面,但钠能与熔融氯化钾
反应置换出金属钾,B符合题意;C.电解饱和食盐水时,阴极区H+得电子产生氢气,而没有
得到Na,表明H+的得电子能力比Na+强,C不合题意;D.因为锌的金属活动性大于铁,所以
镀锌铁桶镀层破损后,锌强于铁失电子,铁仍不易被腐蚀,D不合题意;故选B。
4.【答案】AB
【解析】A.锡青铜是合金,合金的熔点比纯金属的熔点都低,故A符合题意;B.在潮湿环
境中,锡青铜易形成原电池而发生电化学腐蚀,所以在潮湿环境中的腐蚀比干燥环境中快,
故B符合题意;C.锡青铜中的锡比铜活泼,所以形成原电池时,锡作负极,则铜被保护,故C
不符合题意;D.生成Cu (OH) Cl覆盖物是电化学腐蚀过程,但属于化学反应,故D不符合题
2 3
意;答案选AB。
5.【答案】B
【解析】A.Zn比Fe活泼,构成原电池时Zn作负极,Fe受保护,是牺牲阳极的阴极保护法,
故A不选;B.由于在金属铝的表面有一层致密的氧化膜,能够阻止内部金属的腐蚀,和电化
学原理无关,故B选;C.Zn置换出Cu,与稀硫酸构成原电池,加快反应速率,故C不选;D.
Zn比Fe活泼,构成原电池时Fe受保护,Fe比Sn活泼,构成原电池时,Fe受腐蚀,故D不选;
答案选B。
6.【答案】B
【解析】A.铁钉为铁碳合金,主要发生的是电化学腐蚀,A说法错误;B.铁钉腐蚀后,次氯
酸根离子生成为氯离子,溶液中c(Cl−)增大,B说法正确;C.铁粉的腐蚀速率慢主要是铁粉与
次氯酸钠不发生化学腐蚀,C说法错误;D.84消毒液有强氧化性,铁钉发生电化学腐蚀,Fe
失电子生成亚铁离子,电极反应式为Fe-2e−=Fe2+,D说法错误;答案为B。
7.【答案】B
【解析】①中,锌的金属活动性大于铁,则锌作原电池的负极,发生反应Zn-2e−=Zn2+,铁钉作正极,发生反应O+4e−+2H O=4OH−;②中,铁的金属活动性大于铜,则铁作原电池的负极,
2 2
发生反应Fe-2e−=Fe2+,铜作正极,发生反应O+4e−+2H O=4OH−。A.NaCl的琼脂水溶液能够
2 2
让离子自由运动,所以其为离子迁移的通路,A正确;B.①中变红是因为发生反应O+4e−
2
+2H O=4OH−,OH−使酚酞变红,B不正确;C.反应生成的Fe2+与[Fe(CN) ]3−反应生成蓝色沉
2 6
淀,使②中铁钉裸露在外的附近区域变蓝,因生成OH−使酚酞变红,而使铜丝附近区域变红,
C正确;D.①中发生的氧化反应为Zn-2e−=Zn2+,②中发生的氧化反应为Fe-2e−=Fe2+,均可表
示为M-2e−=M2+(M代表锌或铁),D正确;故选B。
8.【答案】D
【解析】A.两图中被腐蚀的都是Fe,说明Fe是负极,Sn为正极,说明金属性Fe>Sn,A错
误;B.从腐蚀程度来讲,乙明显比较严重,因海水中含有较多的盐分,腐蚀速率比河水快,故
乙是海水环境下的腐蚀情况,甲是河水环境下的腐蚀情况,B错误;C.铁被腐蚀时电极反应
式应为Fe-2e−=Fe2+,C错误;D.金属性 ,用 锌做补丁,Zn做负极被腐蚀,可
以保护 ,D正确;答案选D。
9.【答案】C
【解析】A.青铜器中含铜锡等金属,也含有其它金属及非金属杂质,由于物质活动性不同,
周围有电解质溶液,形成了原电池,Cu为原电池的负极,失去电子发生氧化反应,由于电解
质溶液为中性,发生吸氧腐蚀,正极上氧气得到电子,变为OH−,因此氧气是正极反应物,A
正确;B.根据图2可知:在锈蚀小孔外物质成分为Cu (OH) CO、Cu (OH) Cl,Cu元素化合价
2 2 3 2 3
为+2价;在小孔附近物质是Cu O,小孔内壁物质成分是CuCl,Cu元素化合价为+1价,小孔
2
外氧气浓度大,Cu元素价态高,小孔内氧气浓度小,Cu元素价态低,物质成分与氧气浓度有
关;在溶液酸性较强时可逆反应2CuCl+H O Cu O+2HCl的平衡逆向移动,物质成分主
2 2
要是CuCl,若溶液酸性弱,平衡正向移动,物质成分主要是Cu O,可见物质成分也与溶液的
2
pH有关,B正确;C.溶液中微粒Cl-总是向低洼处流动,因此会从小孔外向小孔内移动,与氧
气浓度较小时的+1价Cu形成难溶性固体CuCl,C错误;D.由于Sn是比较活泼的金属,因此
也会与活动性比Sn弱的金属构成原电池,Sn为负极,被氧化而引起电化学腐蚀,D正确;故
合理选项是C。
10.【答案】D
【解析】由题干中的防护原理图分析可知,该装置为电化学防腐,加有外接电源,通电时,加锌环的铁帽作阳极,湿润的绝缘子作阴极,断电时,锌环作负极,铁作正极。A.断电时,锌
环作负极失去电子作负极,利用的原电池原理,是牺牲阳极保护法使铁帽不被腐蚀,A选项
正确;B.通电时,加锌环的铁帽作阳极,锌失去电子发生氧化反应,电极反应为Zn-2e−=Zn2+,
B选项正确;C.断电时发生原电池反应,锌环作负极失去电子,电极反应为Zn-2e−=Zn2+,C选
项正确;D.Fe比Cu更活泼,若将锌环换成铜环,通电时,加铜环的铁帽作阳极,铁失去电子,
不能防止铁被腐蚀,D选项错误;答案选D。
【点睛】掌握金属的防腐措施为解答本题的关键,牺牲阳极的阴极保护法利用原电池原理,
连接一个更活泼的金属做原电池负极,外加电流的阴极保护法是指将被保护金属与电源的
负极相连,作电解池的阴极。
11.【答案】B
【解析】A.将正极反应式和负极反应式相加得到钢铁在CO 水溶液中的腐蚀总反应为
2
,故A正确;B.深井中二氧化碳对碳钢的腐蚀主要为电
化学腐蚀,不是化学腐蚀,故B错误;C.盐份含量高,溶液的导电性越好,腐蚀速率越快,故C
正确;D.腐蚀过程表明含有CO 的溶液主要腐蚀电化学腐蚀,腐蚀性比相同pH值的HCl溶
2
液腐蚀性更强,故D正确;故选B。
12.【答案】D
【解析】A.铜锈是可以被酸性溶液所除去,但是它们之所以“熠熠生辉”,不是因为铜锈
被酸性溶液洗去,否则是“坑坑洼洼”的,A错误;B.圆明园铜首是在我国清朝制作的,那个
时期还未掌握电的运用,B错误;C.铜的金属活动性很弱,但是在空气中,与O、CO、HO反
2 2 2
应生成铜锈,C错误;D.它们的金属材料是合金,相对来说它们的化学稳定性比纯铜要好,类
似于牺牲阳极的阴极保护法来保护金属,使其不易被腐蚀,D正确;故选D。
13.【答案】C
【解析】A.金属钠性质很活泼,极易和空气、水反应,不能作电极材料,故A错误;B.构成
的原电池中,金属棒X作原电池负极,所以金属棒X材料的活泼性应该大于铁,不可能是Cu
电极,故B错误;C.该装置发生吸氧腐蚀,正极钢管上氧气得电子生成氢氧根离子,导致钢
管附近土壤的pH可能会增大,故C正确;D.该装置没有外接电源,不属于外加电流的阴极
保护法,而是牺牲阳极的阴极保护法,故D错误;故答案为C。
【点睛】考查金属的腐蚀与防护,明确金属腐蚀与防护的原理、金属发生析氢腐蚀和吸氧
腐蚀的条件即可解答,根据图片知,该金属防护措施采用的是牺牲阳极的阴极保护法,即把金属和钢管、及电解质溶液构成原电池,金属棒X作负极,钢铁作正极,从而钢管得到保护。