文档内容
大题优练 4 物质制备类工艺流程
优 选 例 题
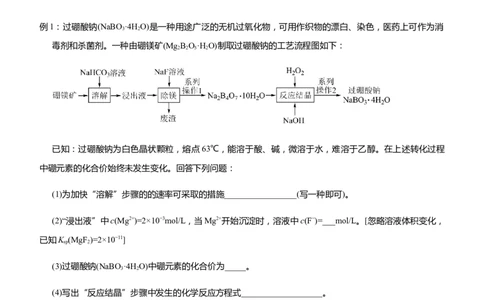
例1:过硼酸钠(NaBO ·4HO)是一种用途广泛的无机过氧化物,可用作织物的漂白、染色,医药上可作为消
3 2
毒剂和杀菌剂。一种由硼镁矿(Mg B O·HO)制取过硼酸钠的工艺流程图如下:
2 2 5 2
已知:过硼酸钠为白色晶状颗粒,熔点63℃,能溶于酸、碱,微溶于水,难溶于乙醇。在上述转化过程
中硼元素的化合价始终未发生变化。回答下列问题:
(1)为加快“溶解”步骤的的速率可采取的措施_________________(写一种即可)。
(2)“浸出液”中c(Mg2+)=2×10−3mol/L,当Mg2+开始沉淀时,溶液中c(F−)=___mol/L。[忽略溶液体积变化,
已知K (MgF )=2×10−11]
sp 2
(3)过硼酸钠(NaBO ·4HO)中硼元素的化合价为_____。
3 2
(4)写出“反应结晶”步骤中发生的化学反应方程式___________________。
(5)“反应结晶”步骤在冰水浴中进行的原因_____________________________。
(6)过硼酸钠的水溶液不稳定,极易生成偏硼酸钠(NaBO )并放出氧气,写出该反应的化学反应方程式
2
__________________________。
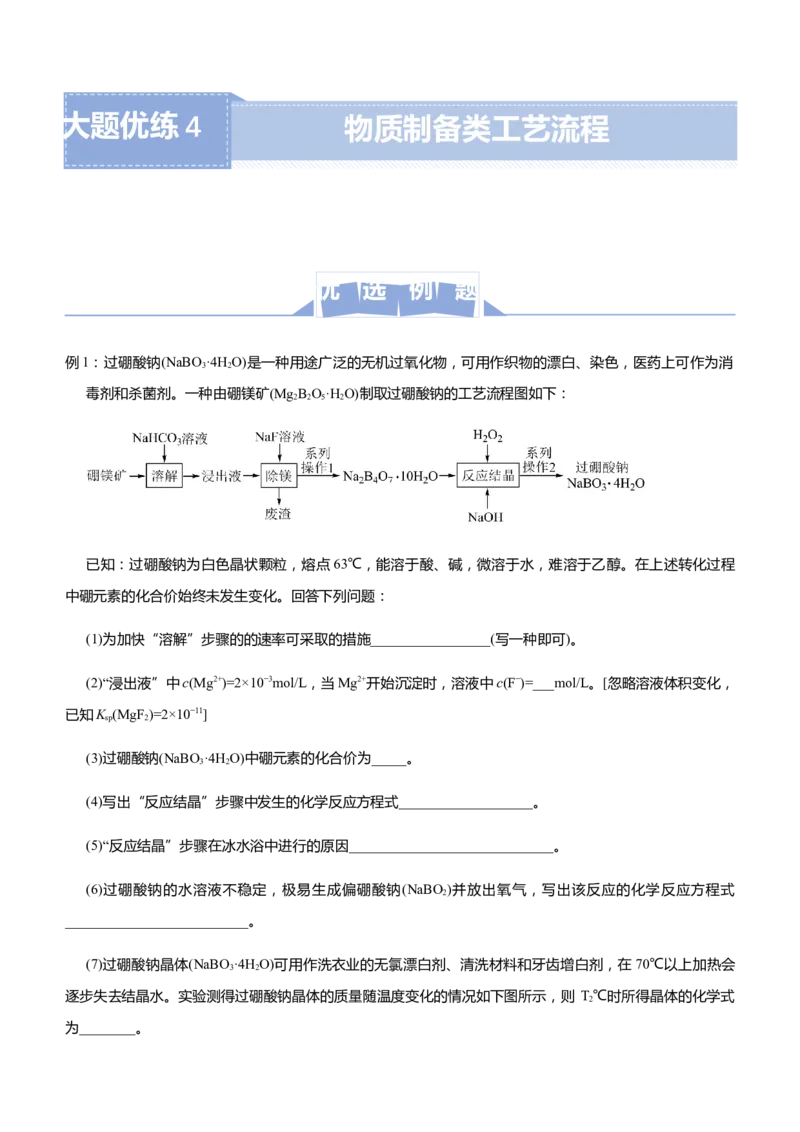
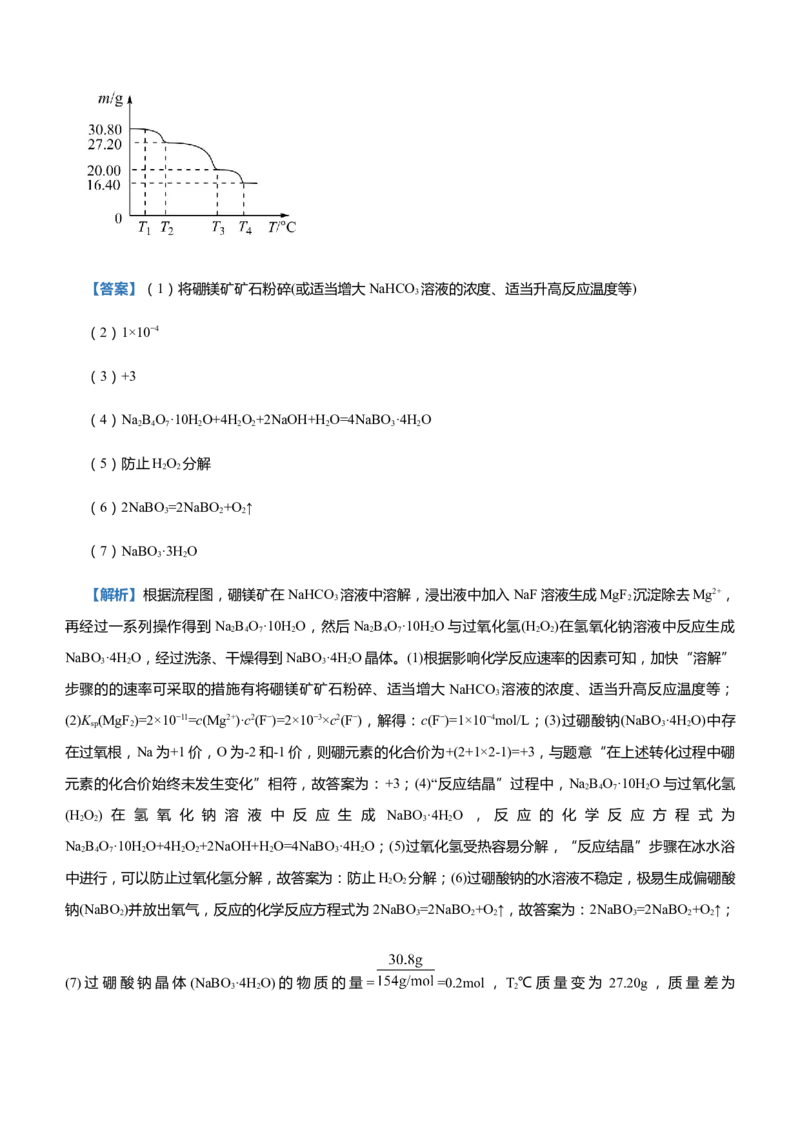
(7)过硼酸钠晶体(NaBO ·4HO)可用作洗衣业的无氯漂白剂、清洗材料和牙齿增白剂,在70℃以上加热会
3 2
逐步失去结晶水。实验测得过硼酸钠晶体的质量随温度变化的情况如下图所示,则 T℃时所得晶体的化学式
2
为________。【答案】(1)将硼镁矿矿石粉碎(或适当增大NaHCO 溶液的浓度、适当升高反应温度等)
3
(2)1×10−4
(3)+3
(4)NaB O·10HO+4HO+2NaOH+HO=4NaBO·4HO
2 4 7 2 2 2 2 3 2
(5)防止HO 分解
2 2
(6)2NaBO =2NaBO +O ↑
3 2 2
(7)NaBO ·3HO
3 2
【解析】根据流程图,硼镁矿在NaHCO 溶液中溶解,浸出液中加入NaF溶液生成MgF 沉淀除去Mg2+,
3 2
再经过一系列操作得到NaB O·10HO,然后NaB O·10HO与过氧化氢(H O)在氢氧化钠溶液中反应生成
2 4 7 2 2 4 7 2 2 2
NaBO ·4HO,经过洗涤、干燥得到NaBO ·4HO晶体。(1)根据影响化学反应速率的因素可知,加快“溶解”
3 2 3 2
步骤的的速率可采取的措施有将硼镁矿矿石粉碎、适当增大 NaHCO 溶液的浓度、适当升高反应温度等;
3
(2)K (MgF )=2×10−11=c(Mg2+)·c2(F−)=2×10−3×c2(F−),解得:c(F−)=1×10−4mol/L;(3)过硼酸钠(NaBO ·4HO)中存
sp 2 3 2
在过氧根,Na为+1价,O为-2和-1价,则硼元素的化合价为+(2+1×2-1)=+3,与题意“在上述转化过程中硼
元素的化合价始终未发生变化”相符,故答案为:+3;(4)“反应结晶”过程中,NaB O·10HO与过氧化氢
2 4 7 2
(H O) 在 氢 氧 化 钠 溶 液 中 反 应 生 成 NaBO ·4HO , 反 应 的 化 学 反 应 方 程 式 为
2 2 3 2
NaB O·10HO+4HO+2NaOH+HO=4NaBO·4HO;(5)过氧化氢受热容易分解,“反应结晶”步骤在冰水浴
2 4 7 2 2 2 2 3 2
中进行,可以防止过氧化氢分解,故答案为:防止HO 分解;(6)过硼酸钠的水溶液不稳定,极易生成偏硼酸
2 2
钠(NaBO )并放出氧气,反应的化学反应方程式为2NaBO =2NaBO +O ↑,故答案为:2NaBO =2NaBO +O ↑;
2 3 2 2 3 2 2
(7)过硼酸钠晶体(NaBO ·4HO)的物质的量= =0.2mol,T℃质量变为 27.20g,质量差为
3 2 230.8g-27.20g=3.6g,减少水的物质的量= =0.2mol,则1mol NaBO ·4HO失去水1mol,则T℃时所得
3 2 2
晶体的化学式为NaBO ·3HO,故答案为:NaBO ·3HO。
3 2 3 2
模 拟 优 练
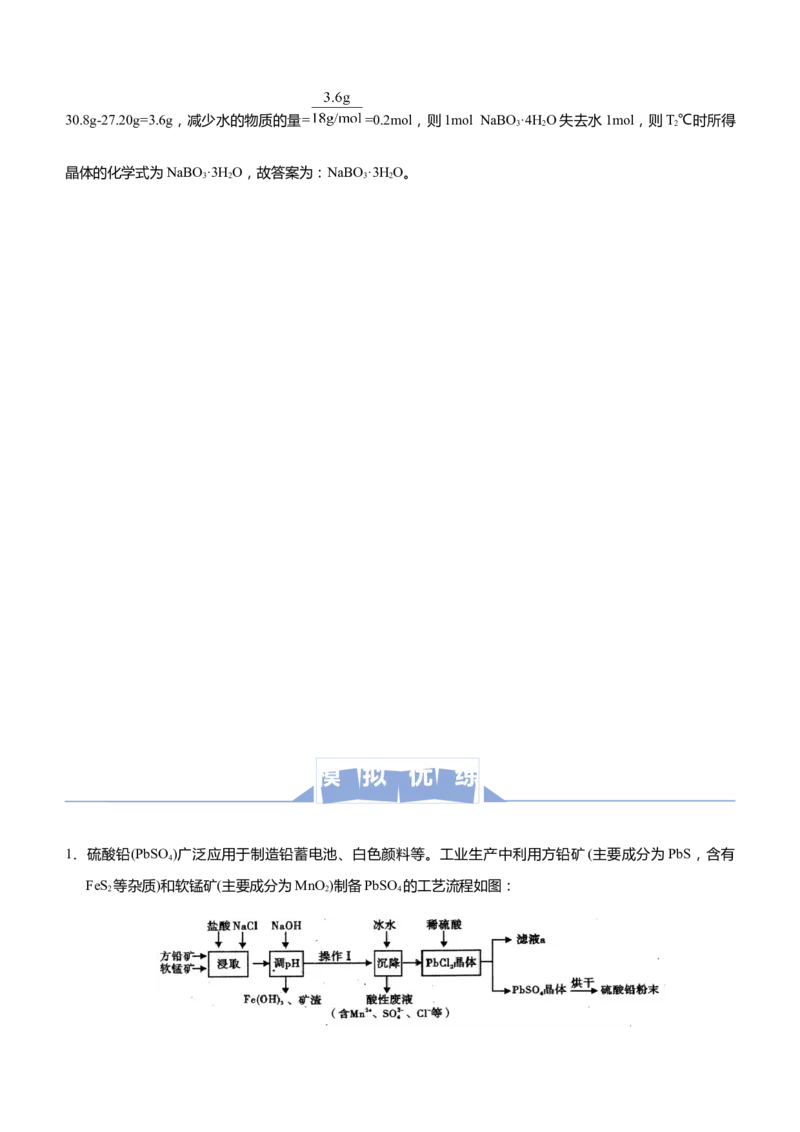
1.硫酸铅(PbSO )广泛应用于制造铅蓄电池、白色颜料等。工业生产中利用方铅矿(主要成分为PbS,含有
4
FeS 等杂质)和软锰矿(主要成分为MnO )制备PbSO 的工艺流程如图:
2 2 4已知:i.PbCl 难溶于冷水,易溶于热水
2
ii.PbCl (s)+2Cl−(aq) PbCl(aq) ΔH>0
2
iii.K (PbSO )=1.08×10−8,K (PbCl )=1.6×10−5
sp 4 sp 2
(1)“浸取”过程中盐酸与MnO 、PbS发生反应生成PbCl 和S的化学方程式为_____________,加入NaCl
2 2
的目的是_________________。
(2)沉降操作时加入冰水的作用是_______________________。
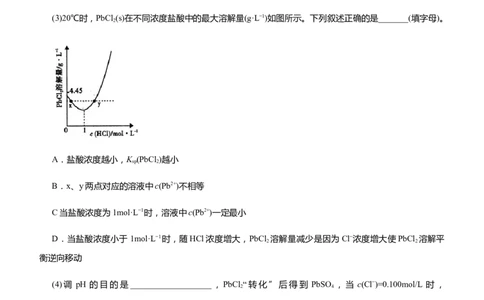
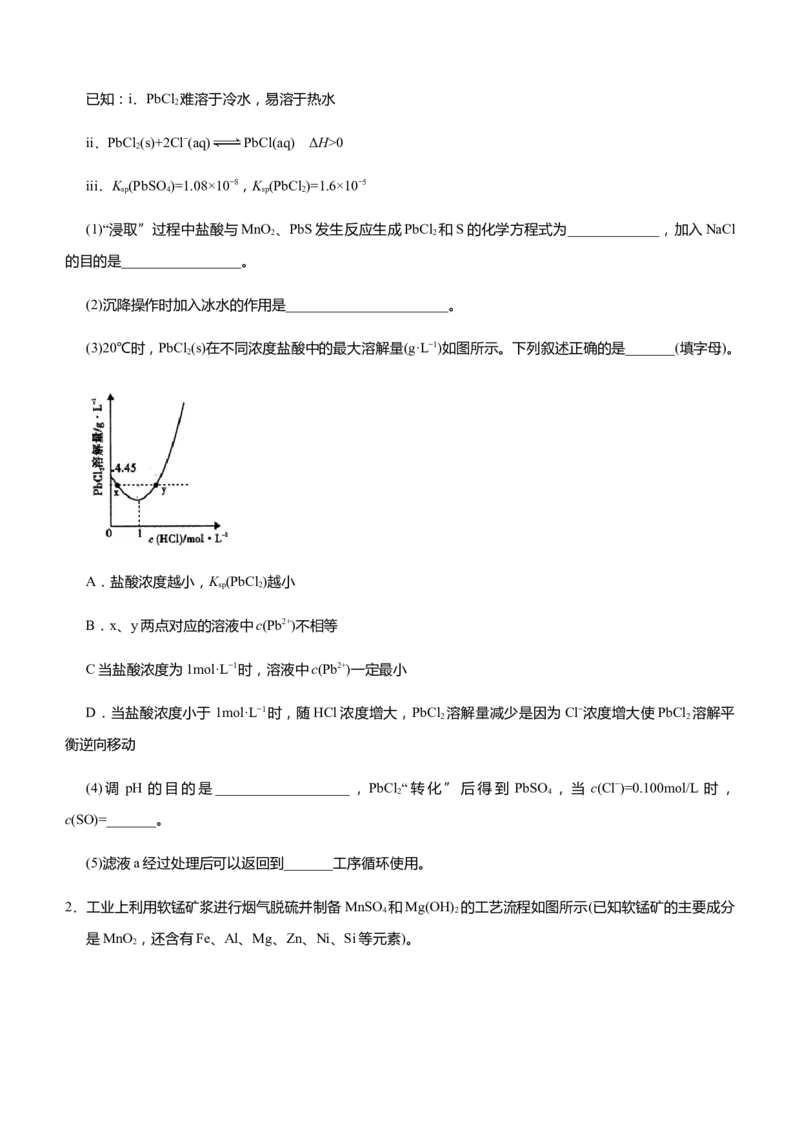
(3)20℃时,PbCl (s)在不同浓度盐酸中的最大溶解量(g·L−1)如图所示。下列叙述正确的是_______(填字母)。
2
A.盐酸浓度越小,K (PbCl )越小
sp 2
B.x、y两点对应的溶液中c(Pb2+)不相等
C当盐酸浓度为1mol·L−1时,溶液中c(Pb2+)一定最小
D.当盐酸浓度小于1mol·L−1时,随HCl浓度增大,PbCl 溶解量减少是因为Cl−浓度增大使PbCl 溶解平
2 2
衡逆向移动
(4)调 pH 的目的是___________________,PbCl “转化”后得到 PbSO ,当 c(Cl−)=0.100mol/L 时,
2 4
c(SO)=_______。
(5)滤液a经过处理后可以返回到_______工序循环使用。
2.工业上利用软锰矿浆进行烟气脱硫并制备MnSO 和Mg(OH) 的工艺流程如图所示(已知软锰矿的主要成分
4 2
是MnO ,还含有Fe、Al、Mg、Zn、Ni、Si等元素)。
2已知:K [Mg(OH) ]=4.9×10−12,K (NH ·H O)=1.8×10−5。
sp 2 b 3 2
(1)“脱硫浸锰”中软锰矿浆吸收SO 的化学方程式为______________________。
2
(2)向浸出液中添加适量MnO 的作用是_____________;滤渣2的主要成分是__________。
2
(3)“沉锰”的离子方程式为____________________________。
(4)“沉锰”过程中pH和温度对Mn2+和Mg2+沉淀率的影响如图所示。
①由图可知,“沉锰”的合适条件是________________________。
②当温度高于45℃时,Mn2+和Mg2+沉淀率变化的原因是___________________________。
(5)将NH 通入0.015mol·L−1 MgSO 溶液中,使Mg2+恰好完全沉淀即溶液中c(Mg2+)=1.0×10−5mol·L−1,
3 4
此时溶液中NH ·H O的物质的量浓度为____________(忽略反应前后溶液体积的变化,计算结果保留2位小
3 2
数)。
3.电池级 CoSO 可用于制备 CoCO 和 CoC O 等钴盐。一种以粗 Co(OH) 渣(含有 Fe O 、CuO、CaO、
4 3 2 4 3 2 3
MgO、ZnO、SiO 等杂质)为原料制备电池级CoSO ·7H O的工艺流程如图:
2 4 2
已知:黄钠铁矾NaFe (SO )(OH) 为淡黄色难溶物。
3 4 2 6回答下列问题:
(1)为了提高钴元素的浸出率,可以采取的措施有_______________(写两点)。
(2)滤渣1的主要成分为_______。
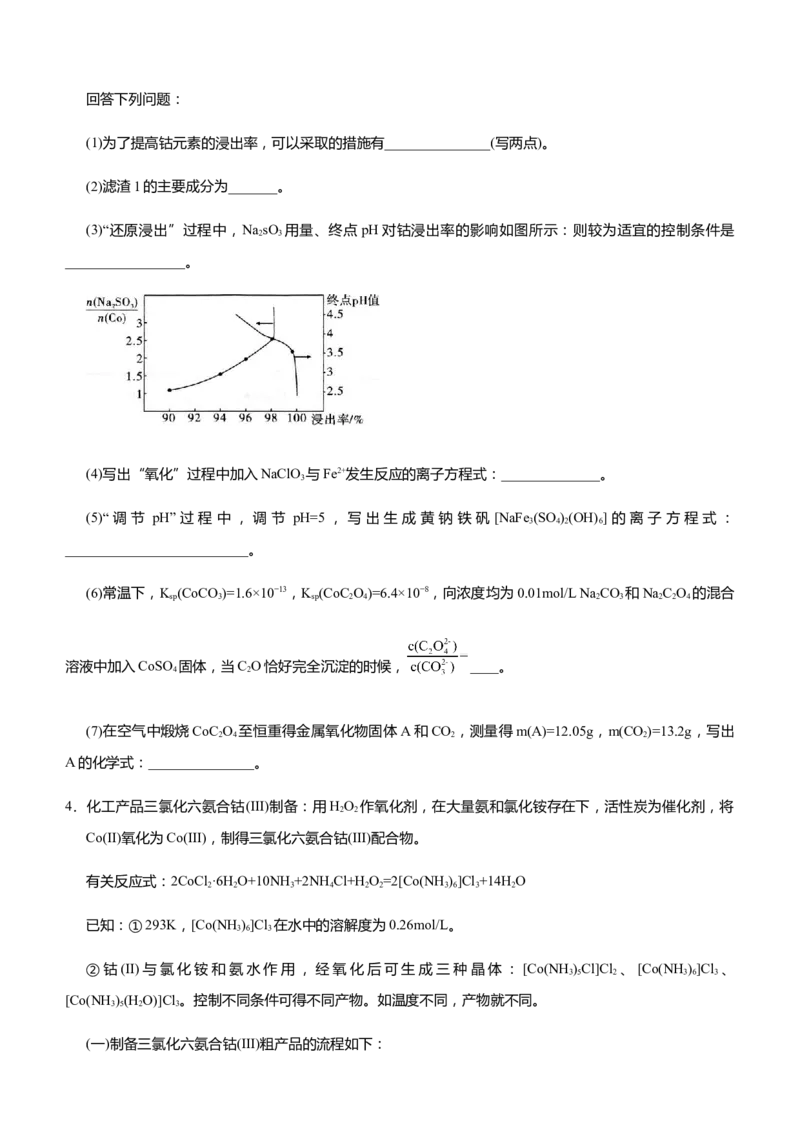
(3)“还原浸出”过程中,NasO 用量、终点pH对钴浸出率的影响如图所示:则较为适宜的控制条件是
2 3
_________________。
(4)写出“氧化”过程中加入NaClO 与Fe2+发生反应的离子方程式:______________。
3
(5)“ 调 节 pH” 过 程 中 , 调 节 pH=5 , 写 出 生 成 黄 钠 铁 矾 [NaFe (SO )(OH) ] 的 离 子 方 程 式 :
3 4 2 6
__________________________。
(6)常温下,K (CoCO)=1.6×10−13,K (CoC O)=6.4×10−8,向浓度均为0.01mol/L Na CO 和NaC O 的混合
sp 3 sp 2 4 2 3 2 2 4
溶液中加入CoSO 固体,当C O恰好完全沉淀的时候, ____。
4 2
(7)在空气中煅烧CoC O 至恒重得金属氧化物固体A和CO ,测量得m(A)=12.05g,m(CO )=13.2g,写出
2 4 2 2
A的化学式:_______________。
4.化工产品三氯化六氨合钴(III)制备:用HO 作氧化剂,在大量氨和氯化铵存在下,活性炭为催化剂,将
2 2
Co(II)氧化为Co(III),制得三氯化六氨合钴(III)配合物。
有关反应式:2CoCl ·6H O+10NH +2NHCl+H O=2[Co(NH)]Cl +14H O
2 2 3 4 2 2 3 6 3 2
已知:①293K,[Co(NH )]Cl 在水中的溶解度为0.26mol/L。
3 6 3
②钴(II)与氯化铵和氨水作用,经氧化后可生成三种晶体:[Co(NH )Cl]Cl 、[Co(NH )]Cl 、
3 5 2 3 6 3
[Co(NH )(H O)]Cl 。控制不同条件可得不同产物。如温度不同,产物就不同。
3 5 2 3
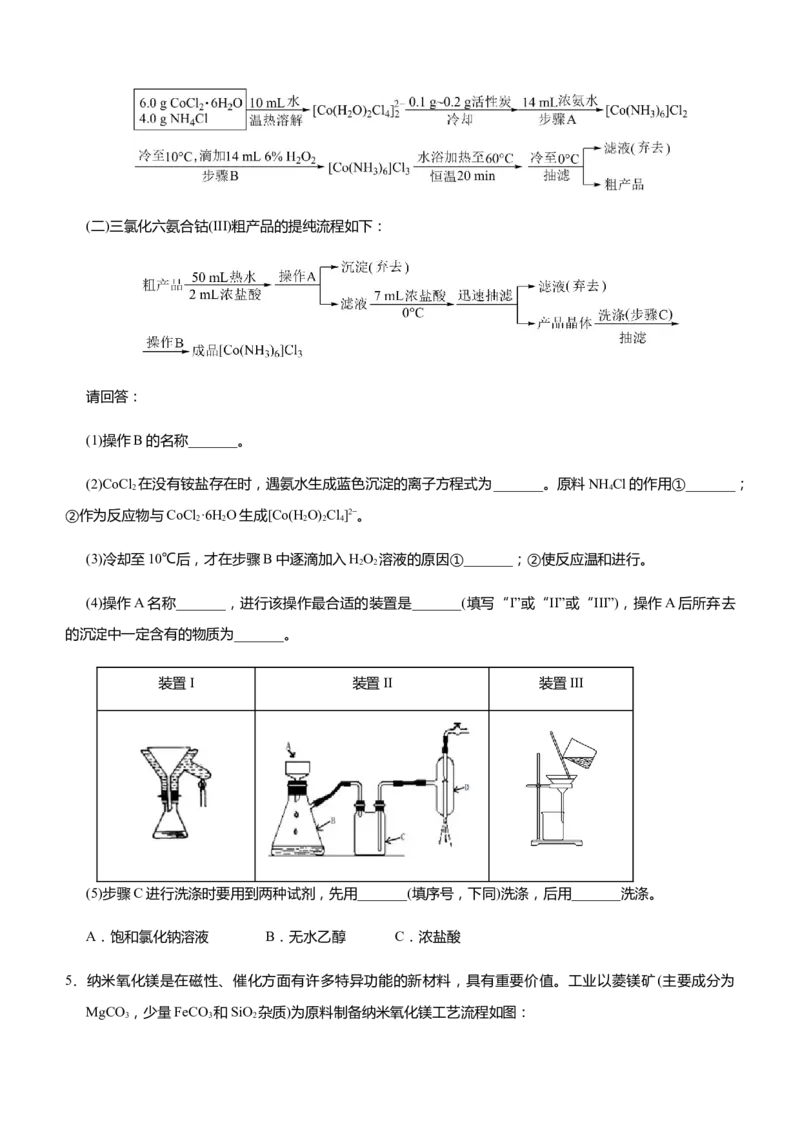
(一)制备三氯化六氨合钴(III)粗产品的流程如下:(二)三氯化六氨合钴(III)粗产品的提纯流程如下:
请回答:
(1)操作B的名称_______。
(2)CoCl 在没有铵盐存在时,遇氨水生成蓝色沉淀的离子方程式为_______。原料NH Cl的作用①_______;
2 4
②作为反应物与CoCl ·6H O生成[Co(H O) Cl]2−。
2 2 2 2 4
(3)冷却至10℃后,才在步骤B中逐滴加入HO 溶液的原因①_______;②使反应温和进行。
2 2
(4)操作A名称_______,进行该操作最合适的装置是_______(填写“I”或“II”或“III”),操作A后所弃去
的沉淀中一定含有的物质为_______。
装置I 装置II 装置III
(5)步骤C进行洗涤时要用到两种试剂,先用_______(填序号,下同)洗涤,后用_______洗涤。
A.饱和氯化钠溶液 B.无水乙醇 C.浓盐酸
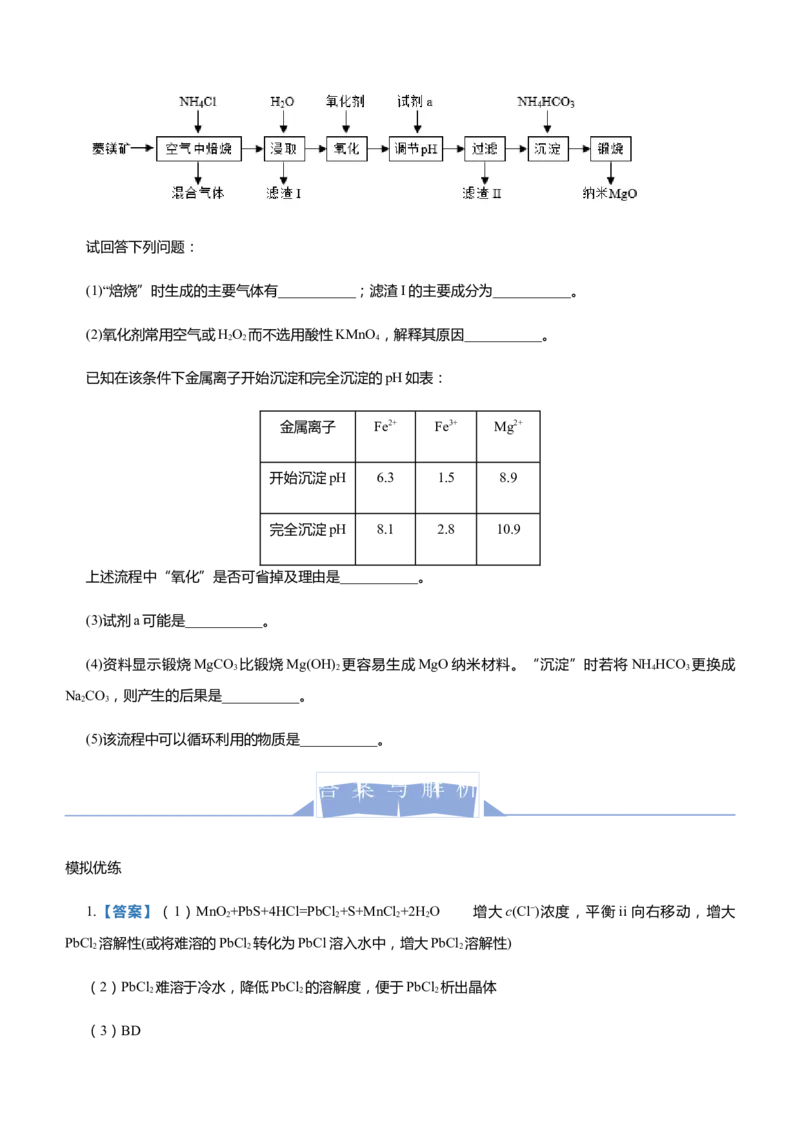
5.纳米氧化镁是在磁性、催化方面有许多特异功能的新材料,具有重要价值。工业以菱镁矿(主要成分为
MgCO ,少量FeCO 和SiO 杂质)为原料制备纳米氧化镁工艺流程如图:
3 3 2试回答下列问题:
(1)“焙烧”时生成的主要气体有___________;滤渣I的主要成分为___________。
(2)氧化剂常用空气或HO 而不选用酸性KMnO ,解释其原因___________。
2 2 4
已知在该条件下金属离子开始沉淀和完全沉淀的pH如表:
金属离子 Fe2+ Fe3+ Mg2+
开始沉淀pH 6.3 1.5 8.9
完全沉淀pH 8.1 2.8 10.9
上述流程中“氧化”是否可省掉及理由是___________。
(3)试剂a可能是___________。
(4)资料显示锻烧MgCO 比锻烧Mg(OH) 更容易生成MgO纳米材料。“沉淀”时若将NH HCO 更换成
3 2 4 3
NaCO,则产生的后果是___________。
2 3
(5)该流程中可以循环利用的物质是___________。
答 案 与 解 析
模拟优练
1.【答案】(1)MnO +PbS+4HCl=PbCl +S+MnCl +2H O 增大c(Cl−)浓度,平衡ii向右移动,增大
2 2 2 2
PbCl 溶解性(或将难溶的PbCl 转化为PbCl溶入水中,增大PbCl 溶解性)
2 2 2
(2)PbCl 难溶于冷水,降低PbCl 的溶解度,便于PbCl 析出晶体
2 2 2
(3)BD(4)使Fe3+沉淀而除去 6.75×10−6
(5)浸取
【解析】方铅矿精矿(主要成分为PbS,含有FeS 等杂质)和软锰矿(主要成分为MnO )中加入稀盐酸,根据
2 2
酸性废液中的成分可知该过程中PbS中部分S元素被氧化成硫酸根离子,MnO 被还原成Mn2+,加入的NaCl
2
可促进反应PbCl (s)+2Cl−(aq) PbCl(aq)平衡正向移动使更多的Pb元素存在于溶液中,加入NaOH溶液调
2
节溶液pH,使铁离子转化成氢氧化铁沉淀,过滤得到氢氧化铁、矿渣和滤液;PbCl 难溶于冷水,将滤液冷
2
水沉降过滤得到PbCl 晶体,之后加入稀硫酸发生沉淀转化,生成硫酸铅晶体,过滤得到晶体烘干得到硫酸
2
铅粉末,滤液a中主要成分为HCl。(1)根据题意可知该过程中MnO 将PbS 中的S元素氧化成S单质,锰元
2 2
素被还原成Mn2+,根据电子守恒和元素守恒可得方程式为 MnO +PbS+4HCl=PbCl +S+MnCl +2H O;加入
2 2 2 2
NaCl的目的是增大c(Cl−)浓度,平衡ii向右移动,增大PbCl 溶解性(或将难溶的PbCl 转化为PbCl溶入水中,
2 2
增大PbCl 溶解性);(2)根据题目信息可知氯化铅难溶于冷水,加入冰水可降低PbCl 的溶解度,便于析出
2 2
PbCl 晶体;(3)PbCl 是微溶化合物,溶于水存在下列平衡:PbCl (s) Pb2+(aq)+2Cl−(aq),由图象可知在浓
2 2 2
度为1mol/L时溶解量最小,小于1mol/L时,主要是电离出的氯离子抑制氯化铅的溶解,大于1mol/L时,可
发生络合反应:PbCl (s)+2Cl−(aq) PbCl(aq),而促进溶解。A.K (PbCl )只受温度的影响,温度不变,则
2 sp 2
K (PbCl )不变,故A错误;B.根据分析可知x、y两点对应的溶液中的溶质不同,所以c(Pb2+)不相等,故B
sp 2
正确;C.根据分析可知当盐酸浓度大于1mol/L时,可发生反应:PbCl (s)+2Cl−(aq) PbCl(aq),所以此时
2
c(Pb2+)不一定最小,故C错误;D.根据分析可知盐酸浓度小于1mol·L−1时,主要存在平衡PbCl (s) Pb2+
2
(aq)+2Cl−(aq),氯离子的增多使平衡逆向移动,故D正确;综上所述选BD;(4)溶液中有杂质铁离子,调pH
值可使Fe3+沉淀而除去;分离固体和液体的操作为过滤;沉淀转化的方程式为PbCl (s)+SO(aq) PbSO (s)
2 4
+2Cl−(aq),该反应的平衡常数K= ,所以当c(Cl−)=0.100mol/L
时,c(SO)= mol·L−1=6.75×10−6mol/L;(5)由分析可知,滤液a中的主要溶质为HCl,所以经
处理后可以返回到浸取工序循环使用。
2.【答案】(1)MnO +SO=MnSO
2 2 4
(2)将Fe2+氧化为Fe3 NiS和ZnS
(3)Mn2++HCO+NH ·H O=MnCO ↓+NH+HO
3 2 3 2(4)45℃、pH=7.5 当温度高于45℃时,随着温度升高,NH HCO 分解,c(CO)下降,所以Mn2+沉淀
4 3
率下降;同时随着温度升高,Mg2+水解生成Mg(OH) 程度增大,所以Mg2+沉淀率增大
2
(5)1.17mol·L−1
【解析】软锰矿的主要成分是MnO ,还含有Fe、Al、Mg、Zn、Ni、Si等元素,应均以金属氧化物的形
2
式存在,SiO 、MnO 与硫酸不反应,硫酸酸化的软锰矿浆中含有 Fe2+、Al3+、Mg2+、Zn2+、Ni2+和SiO 、
2 2 2
MnO ,通入含有SO 的烟气将二氧化硫吸收,二氧化硫与软锰矿浆中的MnO 作用生成生成Mn2+和SO,过
2 2 2
滤后形成含有Mn2+、Fe2+、Al3+、Mg2+、Zn2+、Ni2+、SO等的浸出液,二氧化硅不反应经过滤成为滤渣1,向
浸出液中加入MnO ,将浸出液中的Fe2+氧化为Fe3+,加入氨水,调节pH值,使Fe3+、Al3+形成Fe(OH) 、
2 3
Al(OH) 沉淀除去,再向浸出液中加入硫化铵把Zn2+、Ni2+转化为NiS和ZnS沉淀除去,过滤后得到的滤渣2
3
为NiS和ZnS,向过滤后的滤液中加入氨水和碳酸氢铵,得到碳酸锰和含有Mg2+的溶液,向碳酸锰中加入硫
酸得到硫酸锰,向含有Mg2+的溶液通入氨气,得到氢氧化镁。(1)“脱硫浸锰”中软锰矿浆中,MnO 与SO 反
2 2
应生硫酸锰,化学方程式为MnO +SO=MnSO ;(2)根据分析,向浸出液中添加适量MnO 的作用是将浸出液
2 2 4 2
中的Fe2+氧化为Fe3+;滤渣2的主要成分是NiS和ZnS;(3)根据分析,向过滤后的滤液中加入氨水和碳酸氢铵,
得到碳酸锰和含有Mg2+的溶液,“沉锰”的离子方程式为Mn2++HCO+NH ∙H O=MnCO ↓+NH+HO;(4)①由
3 2 3 2
图可知,“沉锰”的合适条件是:温度控制在45℃左右,pH=7.5左右锰离子的沉淀率最高;②当温度高于
45℃时,Mn2+和Mg2+沉淀率变化的原因是:沉锰是要加入碳酸氢铵,铵盐受热易分解,当温度高于 45℃时,
随着温度升高,NH HCO 分解,c(CO)下降,所以Mn2+沉淀率下降;同时随着温度升高,Mg2+水解生成
4 3
Mg(OH) 程 度 增 大 , 所 以 Mg2+ 沉 淀 率 增 大 ; (5)K [Mg(OH) ]=c(Mg2+)×c2(OH−)=4.9×10−12 , c2(OH−)=
2 sp 2
=
4.9×10−7,c(OH−)=7×10−4mol·L−1,NH 通入0.015mol·L−1 MgSO 溶液中,Mg2+恰好完全沉淀时生成硫酸铵,
3 4
c(NH)=2c(SO)=2×0.015mol/L=0.03mol/L,一水合氨是弱电解质,电离方程式为:NH ·H O NH+OH−,
3 2
K (NH ·H O)= =1.8×10−5,则NH ·H O的物质的量浓度为 =1.17
b 3 2 3 2
mol/L。
3.【答案】(1)将粗Co(OH) 渣研细、适当地升温、适当增大硫酸的浓度(任意答两点)
3
(2)SiO 和CaSO
2 4(3) 且终点pH=3.5
(4) =
(5) =3CO ↑+NaFe (SO )(OH) ↓
2 3 4 2 6
(6)4×105
(7)Co O
3 4
【解析】粗Co(OH) 渣(含有Fe O 、CuO、CaO、MgO、ZnO、SiO 等杂质)加入硫酸酸浸后,SiO 不溶于
3 2 3 2 2
酸出现在滤渣1中,硫酸钙微溶液出现下滤渣1中,溶液中存在Fe3+、Cu2+、Ca2+、Mg2+、Zn2+,加入NaClO
3
把亚硫酸根氧化为硫酸根,加入NaCO 调pH使Fe3+转化为黄钠铁矾[NaFe (SO )(OH) ],得到含Co2+的溶液
2 3 3 4 2 6
再加入NaF沉淀Ca2+、Mg2+,加入PO 沉淀Cu2+、Zn2+,最终得到CoSO ·7H O。(1)通过搅拌、适当升高温
2 4 4 2
度、研磨矿石、适当增大酸的浓度等,可以提高溶浸工序中原料的浸出率,故答案为:将粗Co(OH) 渣研细、
3
适当地升温、适当增大硫酸的浓度(任意答两点);(2)由分析可知,滤渣1的成分是SiO 和CaSO ;(3)由图可
2 4
知,当 且终点pH=3.5时,钴浸出率最高,故答案为: 且终点pH=3.5;(4)“氧
化”过程中NaClO 把过量的亚硝酸钠氧化为硫酸钠,离子方程式为: = ;
3
(5) 加 入 NaCO 调 pH 使 Fe3+ 转 化 为 黄 钠 铁 矾 [NaFe (SO )(OH) ] , 离 子 方 程 式 为 :
2 3 3 4 2 6
=3CO ↑+ NaFe (SO )(OH) ↓;(6)等浓度的C O和CO,CO先沉淀,当C O恰
2 3 4 2 6 2 2
好完全沉淀的时候, ,故答案为:4×105;(7)在空气中煅烧CoC O 得到氧化
2 4
物和二氧化碳,根据元素守恒可知, , , ,则固体A中
,故化学式为Co O,故答案为:Co O。
3 4 3 44.【答案】(1)烘干
(2) 抑制NH ·H O的电离
3 2
(3)避免HO 的分解
2 2
(4)趁热过滤 Ⅰ 活性炭 C
(5)B
【解析】将六水合氯化钴和氯化铵固体溶解于水中,得到[Co(H O) Cl]2−,加入活性炭冷却后加入浓氨水
2 2 4
得到[Co(NH )]Cl 溶液,冷却后滴加双氧水得到[Co(NH )]Cl 溶液,水浴加热后冷却抽滤,得到[Co(NH )]Cl
3 6 2 3 6 3 3 6 3
粗产品,将粗产品溶于水中,加入2mL浓盐酸,得到沉淀,由于粗产品中含有不溶于水的活性炭,所以沉淀
中一定含有活性炭,过滤后,向滤液中加入7mL浓盐酸,由于同离子效应,[Co(NH )]Cl 从溶液中析出,抽
3 6 3
滤后得到[Co(NH )]Cl 晶体,洗涤后抽滤、干燥得到纯净的[Co(NH )]Cl 。(1)抽滤后得到的产品中含有水分,
3 6 3 3 6 3
需要烘干,因此操作B的名称是烘干;(2)CoCl 在没有铵盐存在的情况下,遇氨水生成蓝色沉淀,该蓝色沉
2
淀是氢氧化钴,该反应的离子方程式为 ;在碱性条件下容易生成氢
氧化钴沉淀,因此原料NH Cl的主要作用除了提供NH 以外,还有抑制NH ·H O的电离,降低溶液的碱性;
4 3 3 2
(3)由于双氧水不稳定,受热易分解,因此冷却至10℃后,步骤B中逐滴加入HO 溶液的目的是避免HO 的
2 2 2 2
分解,另外使反应温和进行;故答案为:避免HO 的分解;(4)由于温度不同,产物也不同,因此操作A应
2 2
该是趁热过滤;由于需要保持一定温度,所以选择装置I;粗产品中含有活性炭,不溶于水,沉淀中一定含
有活性炭;(5)增大氯离子浓度可以防止产品溶解而损失,因此三氯化六氨合钴首先应该用浓盐酸洗涤,最后
再用有机溶剂乙醇洗涤;故答案为:C;B。
5.【答案】(1)NH 、CO SiO
3 2 2
(2)引入新杂质Mn2+,产品不纯;将Cl−氧化为Cl 造成污染 否,不先将Fe2+氧化为Fe3+,调pH分步
2
沉淀中产生的Fe(OH) 为絮状沉淀,不易通过过滤分离除去
2
(3)MgO(或MgCO 、Mg(OH) 、Mg(OH) CO 等)
3 2 2 2 3
(4)NaCO 碱性更强,反应中易生成更多Mg(OH) 而不利于MgO纳米材料的生成,纳米MgO纯度降低
2 3 2
(5)NH Cl
4
【解析】菱镁矿主要成分为MgCO (含少量FeCO 和SiO 杂质),加入NH Cl在空气中焙烧,主要反应
3 3 2 4为MgCO +2NHCl=====MgCl +2NH↑+CO ↑+H O,杂质FeCO 也发生类似的反应生成 FeCl ,加水溶解,
3 4 2 3 2 2 3 2
SiO 不溶于水,进入滤渣I中,加入氧化剂,将Fe2+氧化为Fe3+,加入试剂a调pH,但不能引入新物质,故
2
试剂a可以选择Mg的化合物MgO、MgCO 、Mg(OH) 、Mg(OH) CO 等,此时Fe3+完全水解为Fe(OH) ,过
3 2 2 2 3 3
滤除去Fe(OH) (滤渣II),加入NH HCO ,Mg2+转化为MgCO 沉淀并得到NH Cl溶液,经过煅烧得到纳米
3 4 3 3 4
MgO。(1)根据分析,“焙烧”时生成的主要气体有NH 、CO ;滤渣I的主要成分为SiO ;(2)H O 的还原产
3 2 2 2 2
物为HO,不会引入新杂质,而MnO的还原产物为Mn2+,引入新杂质Mn2+,产品不纯,另外,MnO氧化性
2
很强,可将溶液中的Cl−氧化为Cl ,造成污染;根据表格数据可知,Fe2+的沉淀不会影响Mg2+,但调pH时
2
Fe2+会转化为Fe(OH) 絮状沉淀,不易通过过滤分离除去,故需将 Fe2+氧化为Fe3+,得到的Fe(OH) 容易过滤
2 3
除去;(3)根据分析,试剂 a 可能是 MgO(或 MgCO 、Mg(OH) 、Mg(OH) CO 等);(4)Na CO 碱性比
3 2 2 2 3 2 3
NH HCO 更强,碱性强的溶液中易生成更多Mg(OH) ,而锻烧MgCO 比锻烧Mg(OH) 更容易生成MgO纳米
4 3 2 3 2
材料,故使用NaCO 不利于MgO纳米材料的生成,纳米MgO纯度降低;(5)根据分析,沉淀步骤中可得
2 3
NH Cl溶液,故可以循环的物质是NH Cl。
4 4