文档内容
(新高考)2021 届高考考前冲刺卷 选项 A B C D
化 学(十四)
实验操作
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴
在答题卡上的指定位置。
制取氨气将其溶 用碳酸钠与稀硫 过滤获得碳酸 蒸发浓缩氯化铵
实验目的
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写 于饱和食盐水 酸制二氧化碳 钠晶体 溶液
在试题卷、草稿纸和答题卡上的非答题区域均无效。 5.下列事实与电化学无关的是
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和
答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Sc 45
A.暖宝宝(含铁粉、 B.海沙比河沙混凝
C.家用铁锅生锈 D.铁罐运输浓硫酸
碳、氯化钠等)发热 土更易使钢筋生锈
一、选择题:每小题3分,共45分。每小题给出的四个选项中,只有一项是符合题目要求的。
6.枸橼酸是一种天然的防腐剂,其结构简式如图所示。下列有关枸橼酸的说法正确的是
1.化学与生产、生活、社会密切相关,下列有关说法正确的是
A.新型冠状病毒有可能在空气中以气溶胶的形式传播,气溶胶不属于胶体
B.河水中有许多杂质和有害细菌,加入明矾消毒杀菌后可以直接饮用
C.面粉中禁止添加CaO、过氧化苯甲酰等增白剂,CaO 属于碱性氧化物,也属于离子化合物,其
2 2
A.不可能存在分子中含有苯环的同分异构体
阴阳离子个数比为2∶1,过氧化苯甲酰属于有机物
B.1mol枸橼酸最多能与3mol H 发生加成反应
2
D.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量
C.一定条件下发生消去反应可得两种产物(不包括立体异构)
2.N 表示阿伏加德罗常数的值,下列说法中正确的是
A
D.通过分子内酯化反应可形成五元环状化合物
A.0.1mol NaHSO 固体所含的离子总数为0.3N
4 A
7.X、Y、Z、W为原子序数依次增大的4种短周期主族元素,Z元素的气态氢化物和最高价氧化物对
B.12g石墨所含的C-C键的数目约为2.408×1024
应的水化物可以形成离子化合物。这4种元素形成某有机物的结构简式如图。下列说法正确的是
C.常温下,1L pH=5的CuCl 溶液中由水电离出的H+数为10−5N
2 A
D.标准状况下将22.4L NH 溶于水配成1mol/L的溶液,则c(NH)+c(NH ·HO)=1mol/L
3 3 2
3.“中国芯”的主要原材料是高纯单晶硅,反应SiCl (g)+2H(g)=====Si(s)+4HCl(g)可用于纯硅的制
4 2
备。下列有关说法正确的是
A.SiCl 为极性分子 B.HCl的电子式为
4
A.含氧酸的酸性:Z>Y
B.原子半径:XZ>Y
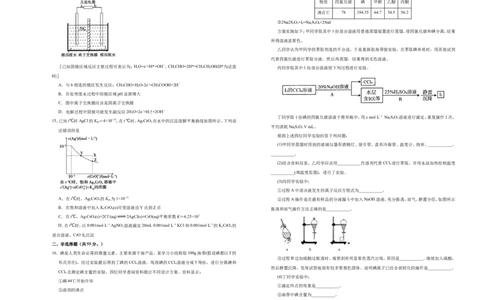
4.实验室模拟侯氏制碱法制取纯碱和氯化铵溶液,下列选项有关操作错误的是 D.这4种元素组成的一种化合物M可与盐酸反应,也可与氢氧化钠溶液反应
封密不订装只卷此
号位座
号场考
号证考准
名姓
级班8.工业上常用纳米级零价铁(ZVI)处理废水[含C HCl (三氯乙烯)和NO]。处理后C HCl 转化为C H 下列说法中错误的是
2 3 2 3 2 4
和Cl−、NO转化为NH。下列说法正确的是
A.配合物中Co2+价电子排布式为3d7
A.水体中含NO越多,三氯乙烯脱Cl的效果越好
B.钴的配位数为6
B.当产生3mol Fe2+时有1mol三氯乙烯完全脱Cl
C.用纳米级零价铁处理被三氯乙烯污染的水体可加快脱氯速率
C.C点的原子坐标参数为( )
D.NO发生的电极反应为NO+7H O+8e−=NH+10OH−
2
9.根据下列实验操作和现象所得到的结论正确的是 D.该物质的化学式为TiCoO
2
选项 实验操作和现象 实验结论 12.常温下,对于pH=9的CH 3 COONa溶液,下列说法错误的是
A.该溶液中:c(OH−)>c(CHCOOH)+c(H+)
将植物油加入溴的苯溶液中,振荡、静置后溴 3
A 植物油中可能含有碳碳双键
的苯溶液褪色
B.往该溶液中滴加醋酸,可能出现c(Na+)<c(CHCOO−)
3
将NH HSO 加热分解,产生的气体通入
B 4 3 SO 能与BaCl 溶液反应
BaCl 2 溶液中,产生白色沉淀 2 2 C.往该溶液中通入HCl气体, 保持不变
向Fe(NO ) 溶液中加入过量HI溶液充分反
C 3 3 氧化性:Fe3+>HNO >I
应后,再滴加KSCN溶液溶液未变红 3 2 D.相同温度下,该CHCOONa溶液的浓度大于pH=9的NaOH溶液的浓度
3
13.在恒容密闭容器中发生反应2SiHCl (g) SiHCl(g)+SiCl (g)。在323K和343K时SiHCl 的转
从装有过氧化钠的试剂瓶中取一定量固体于 3 2 2 4 3
D 过氧化钠变质产生碳酸钠
试管中然后加入MgCl 溶液,产生白色沉淀
2 化率随时间变化的结果如图所示。下列说法正确的是
10.某废催化剂含SiO、ZnS、CuS及少量的Fe O。某实验小组以废催化剂为原料,进行回收利用。设
2 3 4
计实验流程如图:
A.323K时,缩小容器体积可提高SiHCl 的转化率
3
B.a、b点对应的反应速率大小关系:v(a)H CO,但没有说明是最高价含氧酸,如酸性HNOZ>W>X,故B错误;C.最简单氢化物的沸点:
3 2 3 3 2
3. 【答案】B HO>NH >CH ,但不一定是简单氢化物,另外如果W是S,也不符合,故C错误;D.这4种元素组成
2 3 4
【解析】A.SiCl 和CH 的空间构型一样,都是正四面体构型,结构对称,为非极性分子,A错误;
4 4 的一种化合物M是碳酸氢铵,既可与盐酸反应,也可与氢氧化钠溶液反应,故D正确;故选D。
8. 【答案】C
B.HCl的电子式为 ,B正确;C.单晶硅与金刚石的晶体结构相似,为空间网状结构,为原子晶
【解析】根据图示,铁转化为亚铁离子,发生氧化反应,三氯乙烯C HCl 中C原子化合价为+1价,
2 3
乙烯中C原子化合价为-2价,C HCl 转化为C H 和Cl−,C HCl 发生还原反应;NO转化为NH,NO也
2 3 2 4 2 3
是发生还原反应。A.三氯乙烯C HCl 中C原子化合价为+1价,乙烯中C原子化合价为-2价,处理后
体,C错误;D.Si原子的结构示意图为 ,D错误;故选B。 2 3
C HCl 转化为C H 和Cl−,C HCl 发生还原反应;NO转化为NH,NO也是发生还原反应,根据得失电
2 3 2 4 2 3
4. 【答案】C 子守恒,水体中含NO越多,三氯乙烯脱Cl的效果越差,故A错误;B.三氯乙烯C HCl 中C原子化合
2 3
【解析】A.加热氯化铵和消石灰混合固体制取氨气,为了防止水倒流引起试管底部炸裂,试管口应
价为+1价,乙烯中C原子化合价为-2价,1mol C HCl 脱去3mol氯原子转化为1mol C H 时,得到
2 3 2 4
向下倾斜,且氨气极易溶于水,倒置的漏斗可防止倒吸,故A正确;B.装置图中的稀硫酸从分液漏斗
6mol电子,再加上NO转化为NH,发生反应得到的电子,则得失电子总量大于6mol,所以产生的
中滴入锥形瓶,和固体碳酸钠发生反应生成二氧化碳气体,故B正确;C.侯氏制碱法是向氨化的饱和
Fe2+的总量大于3mol,故B错误;C.用纳米级零价铁处理被三氯乙烯污染的水体,增大了单位体积水
氯化钠溶液中通入二氧化碳,发生反应生成碳酸氢钠晶体和氯化铵溶液,过滤得到的晶体是碳酸氢钠,
体中小微粒ZVI的投入量,可以增大ZVI和正极的接触面积,加快ZVI释放电子的速率,可加快水体
故C错误;D.蒸发皿中蒸发浓缩氯化铵溶液,用玻璃棒不断搅拌,装置操作正确,故D正确;故选C。修复速率,故C正确;D.由示意图及N元素的化合价变化,NO发生反应的电极反应式为NO+10H+ 12. 【答案】A
+8e−=NH+3H O,故D错误;故选C。 【解析】A.CHCOONa溶液中存在质子守恒:c(OH−)=c(CHCOOH)+c(H+),A错误;B.往该溶液中
2 3 3
9. 【答案】A 滴加醋酸,可能使溶液呈酸性,c(OH−)<c(H+),溶液中存在电荷守恒:c(OH−)+c(CHCOO−)
3
【解析】A.植物油含碳碳双键能使溴的苯溶液褪色,故A正确;B.将NH HSO 加热分解,产生气
4 3
=c(Na+)+c(H+),则可能出现c(Na+)<c(CHCOO−),B正确;C. ,水解常
3
体SO 和NH ,盐酸的酸性大于亚硫酸的酸性,则SO 与BaCl 溶液不会反应产生白色沉淀,但将产生
2 3 2 2
的SO 和NH 通入BaCl 溶液中,SO 和NH 反应生成亚硫酸铵,亚硫酸铵可与氯化钡反应生成亚硫
2 3 2 2 3
酸 钡 白 色 沉 淀 , 故 B 错 误 ; C . 向 Fe(NO ) 溶 液 中 加 入 过 量 HI 溶 液 发 生 反 应
3 3
数K 只与温度有关,温度不变,其值不变,则往该溶液中通入HCl气体, 保持
h
Fe(NO )+4HI=2H O+2I +Fe(NO)+NO↑,生成了二价铁,再滴加KSCN溶液溶液不会变红,而氧化性:
3 3 2 2 3 2
HNO>Fe3+>I ,故C错误;D.从装有过氧化钠的试剂瓶中取一定量固体于试管中然后加入MgCl 溶
3 2 2
不变,C正确;D.CHCOONa水解使溶液呈碱性,而水解是微弱的,NaOH是强碱,则相同温度下,该
3
液,产生白色沉淀,因过氧化钠可与水反应生成氢氧化钠,此白色沉淀可能是碳酸镁也可能是氢氧化
CHCOONa溶液的浓度大于pH=9的NaOH溶液的浓度,D正确;故选A。
3
镁,过氧化钠可能未变质,故D错误;答案为A。
13.【答案】C
10. 【答案】B
【解析】A.缩小容器体积,增大压强,平衡不移动,不能提高SiHCl 的转化率,故A错误;B.温度
3
【解析】由题给流程可知,向废催化剂中加入稀硫酸,硫化锌和四氧化三铁与稀硫酸反应得到硫酸
越高,反应速率越快,a对应温度为343K、b对应温度为323K,所以a、b点对应的反应速率大小关系:
锌、硫酸铁和硫酸亚铁的混合溶液,二氧化硅和硫化铜不与稀硫酸反应,过滤得到含有硫酸锌、硫酸
v(a)>v(b),故B错误;C.343K时,SiHCl 的平衡转化率为22%,
3
铁和硫酸亚铁的滤液1和含有二氧化硅和硫化铜的滤渣1;滤液1经蒸发浓缩、冷却结晶、过滤得到
含有杂质的粗皓矾;向滤渣中加入稀硫酸和过氧化氢的混合溶液,酸性条件下,硫化铜与过氧化氢反
应生成硫酸铜、硫沉淀和水,过滤得到含有硫酸铜的滤液2和含有硫和二氧化硅的滤渣2;滤液2经
蒸发浓缩、冷却结晶、过滤得到粗胆矾。A.由分析可知,滤液1中含有铁离子,若选用硫氰化钾溶液和
新制的氯水检验亚铁离子,铁离子会干扰亚铁离子检验,故A错误;B.步骤①操作中,硫化锌与稀硫
,故C正确;D.如图示可知,a点所在的曲线反应速率快,对应温度高,
酸反应生成硫酸锌和硫化氢气体,硫化氢气体能与碱反应,可用碱液吸收,故B正确;C.由分析可知,
滤渣1含有与稀硫酸不反应的二氧化硅和硫化铜,滤渣2为硫和二氧化硅,故C错误;D.硫酸是高沸
SiHCl (g)平衡转化率大,说明升高温度平衡正向移动,所以2SiHCl (g) SiHCl(g)+SiCl (g)的正
3 3 2 2 4
点酸,则滤液2经蒸发浓缩、冷却结晶、过滤得到粗胆矾时,不需要滴加稀硫酸防止硫酸铜水解,故D
反应为吸热反应,故D错误;选C。
错误;故选B。
14.【答案】D
11. 【答案】D
【解析】根据钠离子的流向可知b为电源负极,右侧为阴极区,a为电源正极,左侧为阳极区。A.与
【解析】A.配合物中Co2+价电子个数为7,价电子排布式为3d7,故A正确;B.由晶胞结构图可知,
b相连的极区为阴极区,根据题目所给信息可知该区域乙醛被还原为乙醇,A错误;B.阳极区乙醛被
氧化为乙酸,电极反应为:CHCHO+H O-2e−=CH COOH+2H+,产生氢离子,pH逐渐减小,B错误;C.
3 2 3
钴周围有6个O2−,配位数为6,故B正确;C.C点的原子处于体心,坐标参数为( ),故C正确; 根据B选项可知电解过程中会生成醋酸,根据题意可知阴极区会产生氢氧根,为防止氢氧根中和醋
酸,离子交换膜应为阳离子交换膜,C错误;D.电解过程中阴极上,水电离出的氢离子可能放电生成
氢气,发生反应2HO+2e−=H ↑+2OH−,D正确;综上所述答案为D。
2 2
15.【答案】D
D.此晶胞中O原子为6× =3,Ti原子为8× =1,Co原子为1,该物质的化学式为TiCoO ,故D错
3
【解析】A.在t℃时,Ag CrO 的K 为K (Ag CrO)=c2(Ag+)·c(CrO)=(1×10−3)2×10−5=1×10−11,A正确;
2 4 sp sp 2 4
误;故选D。 B.在饱和溶液中加入KCrO(s),c(CrO)增大,可使溶液由Y点到Z点,故B正确;C.在t ℃,
2 4Ag CrO(s)+2Cl−(aq) 2AgCl(s)+CrO(aq)的平衡常数K= × = 0.5cV×10−3mol,所以碘的含量为 ×100%=
2 4
0.635cV%。
=6.25×107,故C正确;D.在t℃时,开始产生AgCl沉淀时,c(Ag+)= =4×10−7mol/L,开始产
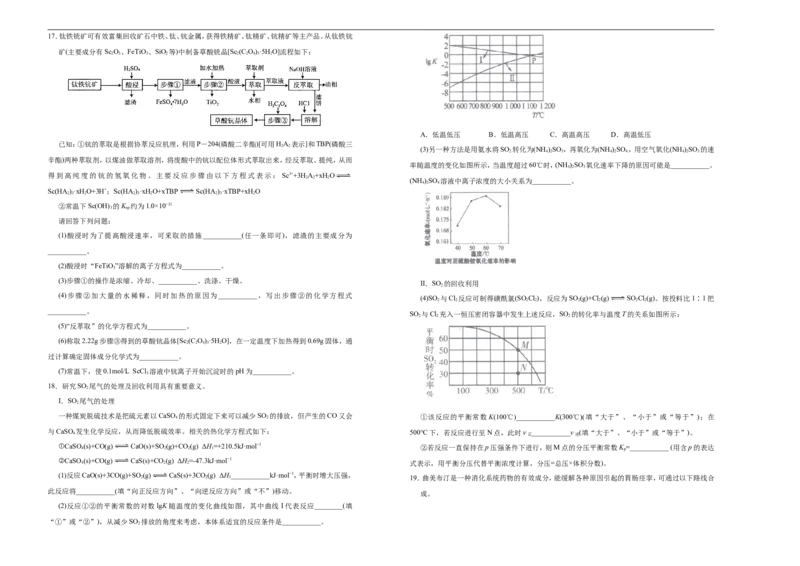
17.【答案】(1)升温(粉碎矿石、搅拌、增大硫酸浓度等) SiO
2
(2)FeTiO +6H+=Fe2++Ti4++3H O
3 2
(3)过滤
生Ag 2 CrO 4 沉淀时,[ =1×10−4mol/L,所以Cl−沉淀需要的c(Ag+)较小而先沉淀,故 (4)促进Ti4+水解趋于完全,得到更多的TiO 2 沉淀 Ti(SO 4 ) 2 +2H 2 O=TiO 2 ↓+2H 2 SO 4
(5)Sc(HA )·xTBP+3NaOH Sc(OH) ↓+3NaHA +xTBP(或Sc(HA )·xTBP+6NaOH
D错误;故选D。 2 3 3 2 2 3
16.【答案】(1)蒸馏烧瓶 锥形瓶 Sc(OH) ↓+3Na A+xTBP+3HO)
3 2 2 2
(2)乙醚 34.5~44℃ (6)Sc O
2 3
(3)3I+6OH−=5I−+IO+3H O a 酸碱中和反应放热,使碘升华 取上层清液滴加稀硫酸,若 (7)4
2 2
没有紫黑色固体出现,则碘离子已经完全转化(或滴加AgNO 溶液,无黄色沉淀出现) 【解析】钛铁钪矿(主要成分有Sc O、FeTiO 、SiO 等)加入硫酸酸浸,根据后续流程可知过滤得到
3 2 3 3 2
(4)当滴入最后一滴NaSO 时,CCl 层由紫红色变为无色 0.635cV% 含有Fe2+、Sc3+、Ti4+等阳离子的溶液,SiO 难溶于硫酸,成为滤渣;滤液经蒸发浓缩、冷却结晶、过滤、
2 2 3 4 2
【解析】本实验的目的是分离碘和CCl 4 及测定碘含量,由于四氯化碳的沸点高于碘的升华温度,所 洗涤、干燥得到FeSO 4 ·7H 2 O晶体,此时滤液中还有Sc3+、Ti4+等阳离子,加水加热促进Ti4+的水解形成
以直接蒸馏时得到四氯化碳中会有升华出来的碘,造成浪费,所以应选用沸点低于碘升华温度的萃取 TiO 沉淀,剩余酸液加入萃取剂萃取,将废酸中的钪以配位体形式萃取出来,加入NaOH溶液反萃取
2
剂如乙醚,然后再蒸馏;测定碘含量时,丙同学先用NaOH溶液进行反萃取,使碘在碱性环境中发生 过滤得到高纯度的钪的氢氧化物,加盐酸溶解,在加入草酸得到草酸钪晶体。(1)升温、粉碎矿石增大
歧化反应,得到含有I−和IO的水溶液,然后加入硫酸酸化使I−和IO反应得到碘的悬浊液,静置沉降 接触面积、搅拌、增大硫酸浓度等措施都可以提高酸浸速率;滤渣主要成分为难溶于硫酸的SiO;(2)
2
过滤得到碘单质;丁同学是利用Na 2 S 2 O 3 标准液来滴定碘单质的含量,Na 2 S 2 O 3 会将碘还原为易溶于水 根据后续流程可知酸浸时FeTiO 3 转化为Fe2+、Ti4+,根据元素守恒和电荷守恒可得离子方程式为
的碘离子,所以滴定终点时四氯化碳溶液会变无色。(1)蒸馏时一般需要酒精灯加热,蒸馏烧瓶盛放待 FeTiO +6H+=Fe2++Ti4++3H O;(3)从溶液中获取晶体一般经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等
3 2
蒸馏液体,温度计测定馏分温度,直形冷凝管进行冷凝,接引管导流,锥形瓶承接蒸馏出来的液体,所 操作;(4)溶液中存在Ti4++2H O TiO +4H+,加水稀释降低氢离子的浓度,同时加热促进水解,使
2 2
以还需要的仪器为蒸馏烧瓶、锥形瓶;(2)为避免蒸馏时碘升华,所用萃取剂的沸点应低于碘的升华温 Ti4+水解趋于完全,得到更多的TiO 沉淀,化学方程式为Ti(SO )+2H O=
2 4 2 2
度,所以选用沸点为 34.5℃的乙醚作溶剂代替四氯化碳进行萃取,并用水浴加热控制温度在 TiO ↓+2H SO ;(5)根据题目所给信息可知萃取液中 Sc元素以Sc(HA )·xTBP的形式存在,加入
2 2 4 2 3
34.5~44℃之间;(3)①碘在NaOH溶液中发生歧化反应生成碘酸钠和碘化钠,根据电子守恒和元素守 NaOH溶液降低pH值,得到Sc(OH) 沉淀,结合元素守恒可知当NaOH少量时,化学方程式为
3
恒可得离子方程式为3I+6OH−=5I−+IO+3H O;②使用分液漏斗进行萃取,振荡和放气时应使分液的
2 2
Sc(HA )·xTBP+3NaOH Sc(OH) ↓+3NaHA +xTBP,当NaOH过量时为Sc(HA )·xTBP+6NaOH
下口漏斗朝斜上方,通过下口进行放气,故选a;③滴加硫酸时有碘单质生成,而硫酸和过量的NaOH 2 3 3 2 2 3
发生中和反应时会放出热量,使生成的碘单质升华,所以紫色蒸气出现;只要确定上层清液中没有碘
Sc(OH) ↓+3Na A+xTBP+3HO;(6)2.22g草酸钪晶体的物质的量为 =0.05mol,含有
离子则说其完全转化,所以可以取上层清液滴加稀硫酸,若没有紫黑色固体出现,则碘离子已经完全 3 2 2 2
转化;也可以利用硝酸银检验碘离子,具体操作为滴加AgNO 溶液,无黄色沉淀出现,则碘离子已经 0.1mol Sc,则0.69g固体中其他元素的质量为0.69g-0.1mol×45g/mol=0.24g,根据草酸钪晶体的组成
3
完全转化;(4)①到达滴定终点时碘单质被全部还原,四氯化碳中不再有碘单质,所以现象为:当滴入 可知加热过程中C元素会转化为CO,H元素转为为水蒸气,所以残留固体中应还有O元素,物质的
2
最后一滴NaSO 时,CCl 层由紫红色变为无色;②滴定时发生反应:2Na2S O+I =Na SO+2NaI,消
2 2 3 4 2 3 2 2 4 6
量为 =0.15mol,n(Sc)∶n(O)=0.1mol∶0.15mol=2∶3,所以固体成分化学式为 Sc O ;
2 3
耗的 NaSO 的物质的量为 cV×10−3mol,则从 =20g 海带中提取的碘单质的物质的量为
2 2 3
(7)0.1mol/L ScCl 溶液中 c(Sc3+)=0.1mol/L,Sc(OH) 的K 约为 1.0×10−31,则开始沉淀时 c(OH−)=
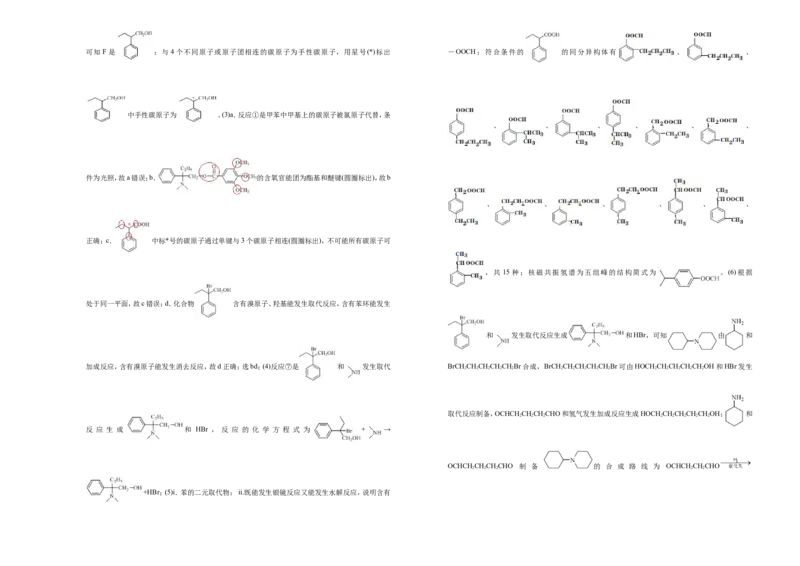
3 3 sp19.【答案】(1)甲苯 还原反应
mol/L=10−10mol/L,则此时c(H+)=10−4mol/L,pH=4。
(2)
18.【答案】(1)-399.7 向正反应方向
(2)② B
(3)bd
(3)温度过高,(NH )SO 分解,浓度减小或温度升高,氧气在溶液中的溶解度降低
4 2 3
(4) + → +HBr
(4)大于 大于
(5)15
【解析】I.(1)根据盖斯定律可知,由②×4-①可得反应CaO(s)+3CO(g)+SO (g) CaS(s)+3CO
2 2
(g),故ΔH 3 =-47.3kJ·mol−1×4-(+210.5kJ·mol−1)=-399.7kJ·mol−1;该反应是气体物质的量减小的反应,则 (6)OCHCH 2 CH 2 CH 2 CHO HOCH 2 CH 2 CH 2 CH 2 OH BrCH 2 CH 2 CH 2 CH 2 Br
平衡时,增大压强,此反应将向正反应方向移动;(2)由曲线I知,随着温度的升高,lgK减小,即K值减
小,则升温平衡逆向移动,则该反应的正反应为放热反应,故曲线I代表反应②;反应①生成SO ,则
2
为减少SO 排放,应使反应①逆向移动,降低温度,增大压强,均可以使反应①平衡逆向移动,故本体
2
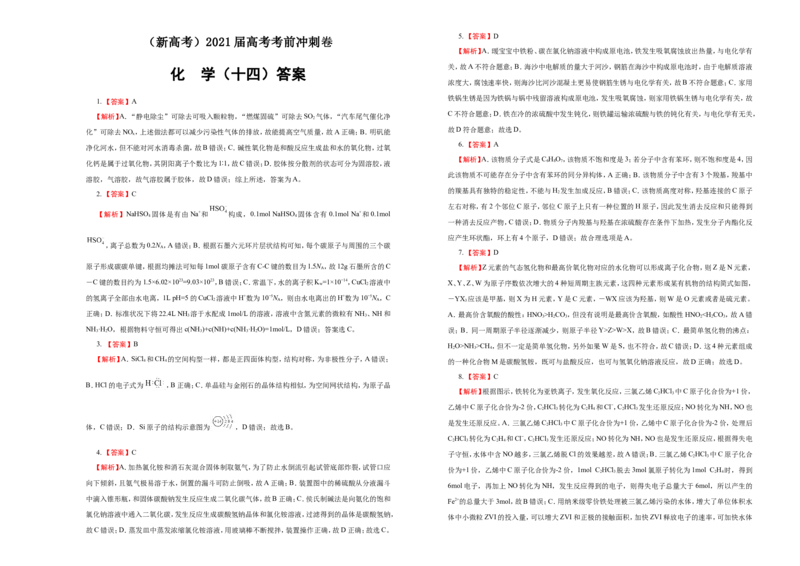
系适宜的反应条件是B;(3)当温度超过60℃时,(NH
4
)
2
SO
3
氧化速率下降的原因可能是温度过高,
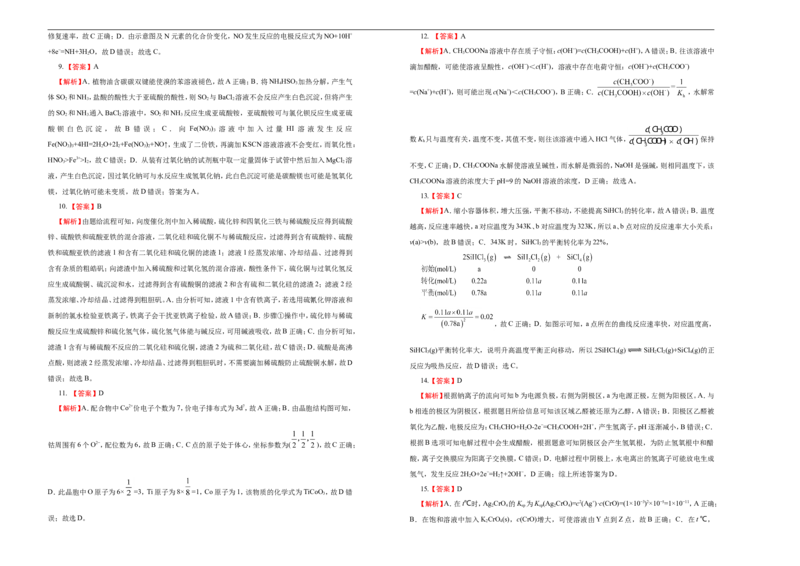
(NH )SO 分解,浓度减小或温度升高,氧气在溶液中的溶解度降低;(NH )SO 溶液中NH离子水解
4 2 3 4 2 4
使溶液显酸性,且水解是微弱的,则离子浓度的大小关系为 ;II.
【解析】A的分子式是C H,由C的结构简式逆推,可知A是 ;F的分子式是C H O,由G
7 8 10 14
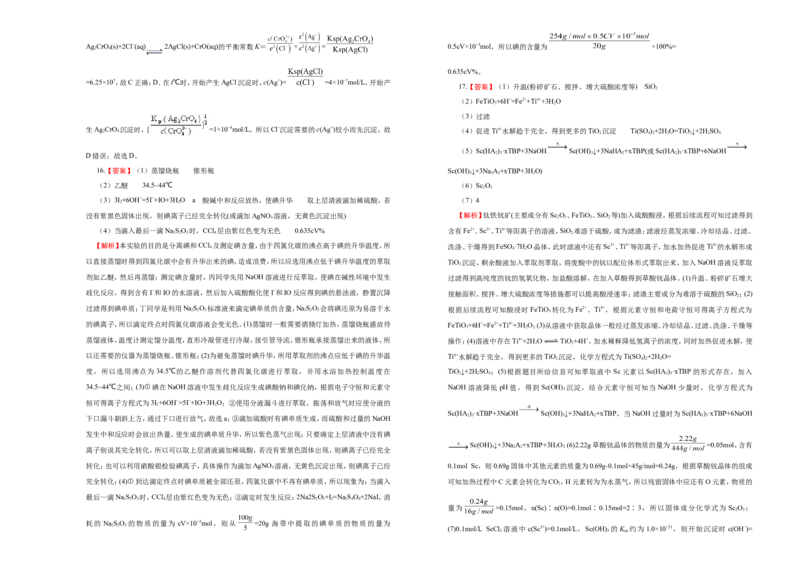
(4)①由图可知,升高温度,平衡时SO 的转化率减小,说明升温平衡逆向移动,该反应为放热反应,则
2
该反应的平衡常数K(100℃)大于K(300℃);在500℃下,若反应进行至N点,此时,SO 的转化率比该
2
温度下平衡时SO 的转化率小,则反应正向进行,v 大于v ;②若反应一直保持在p压强条件下进行,
2 正 逆
的 结 构 简 式 逆 推 , 可 知 F 是 ; H 和 反 应 生 成
M点时,平衡时SO 的转化率为50%,假设起始加入SO 、Cl 均为1mol,则可列出三段式(单位:mol):
2 2 2
,逆推可知H是 。(1)A的分子式是C H,由C的
7 8
则 M 点 SO (g) 、 Cl(g) 、 SO Cl(g) 的 分 压 均 为 , 则 M 点 的 分 压 平 衡 常 数
2 2 2 2
结构简式逆推,可知A是 ,名称是甲苯;反应⑤是 生成 ,分子中氢原子
。
数增多、氧原子数减少,所以反应类型是还原反应;(2)F的分子式是C H O,由G的结构简式逆推,
10 14可知F是 ;与4个不同原子或原子团相连的碳原子为手性碳原子,用星号(*)标出 -OOCH;符合条件的 的同分异构体有 、 、
中手性碳原子为 。(3)a.反应①是甲苯中甲基上的碳原子被氯原子代替,条
、 、 、 、 、 、
件为光照,故a错误;b. 的含氧官能团为酯基和醚键(圆圈标出),故b
、 、 、 、 、 、
正确;c. 中标*号的碳原子通过单键与3个碳原子相连(圆圈标出),不可能所有碳原子可
,共 15 种;核磁共振氢谱为五组峰的结构简式为 。(6)根据
处于同一平面,故c错误;d.化合物 含有溴原子、羟基能发生取代反应,含有苯环能发生
和 发生取代反应生成 和HBr,可知 由 和
加成反应,含有溴原子能发生消去反应,故d正确;选bd;(4)反应⑦是 和 发生取代 BrCHCHCHCHCHBr合成,BrCHCHCHCHCHBr可由HOCH CHCHCHCHOH和HBr发生
2 2 2 2 2 2 2 2 2 2 2 2 2 2 2
取代反应制备,OCHCH CHCHCHO和氢气发生加成反应生成HOCH CHCHCHCHOH; 和
2 2 2 2 2 2 2 2
反 应 生 成 和 HBr , 反 应 的 化 学 方 程 式 为 + →
OCHCH CHCHCHO 制 备 的 合 成 路 线 为 OCHCH CHCHO
2 2 2 2 2
+HBr;(5)i.苯的二元取代物; ii.既能发生银镜反应又能发生水解反应,说明含有HOCH CHCHCHOH BrCHCHCHCHBr 。
2 2 2 2 2 2 2 2