文档内容
培优训练12:定量分析类综合实验
1.PCl 是磷的常见氯化物,可用于半导体生产的外延、扩散工序。有关物质的部分
3
性质如下:
熔点/℃ 沸点/℃ 密度/ g·mL-1 其他
2P+3Cl (少量)=====2PCl ;
黄磷 44.1 280.5 1.82 2 3
2P+5Cl (过量)=====2PCl
2 5
遇水生成H PO 和HCl,遇O
PCl -112 75.5 1.574 3 3 2
3 生成POCl
3
(一)制备
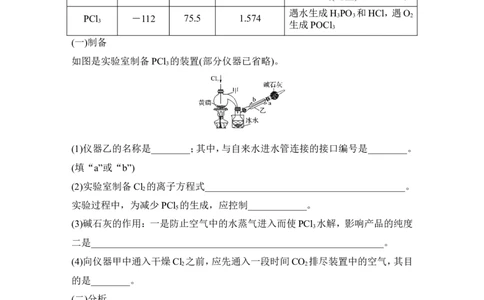
如图是实验室制备PCl 的装置(部分仪器已省略)。
3
(1)仪器乙的名称是________;其中,与自来水进水管连接的接口编号是________。
(填“a”或“b”)
(2)实验室制备Cl 的离子方程式_________________________________________。
2
实验过程中,为减少PCl 的生成,应控制____________。
5
(3)碱石灰的作用:一是防止空气中的水蒸气进入而使PCl 水解,影响产品的纯度
3
二是____________________________________________________________。
(4)向仪器甲中通入干燥Cl 之前,应先通入一段时间CO 排尽装置中的空气,其目
2 2
的是________。
(二)分析
测定产品中PCl 纯度的方法如下:迅速称取 4.100 g产品,水解完全后配成 500
3
mL溶液,取出25.00 mL加入过量的0.100 0 mol·L-1 20.00 mL碘溶液,充分反应
后再用0.100 0 mol·L-1 Na S O 溶液滴定过量的碘,终点时消耗12.00 mL Na S O
2 2 3 2 2 3
溶液。
已知:H PO +H O+I ===H PO +2HI;I +2Na S O ===2NaI+Na S O ;假设测定
3 3 2 2 3 4 2 2 2 3 2 4 6
过程中没有其他反应。(5)根据上述数据,该产品中PCl (相对分子质量为137.5)的质量分数为________。
3
若滴定终点时俯视读数,则 PCl 的质量分数________(填“偏大”“偏小”或
3
“无影响”)。
(三)探究
(6)设计实验证明PCl 具有还原性:____________________________________
3
_____________________________________________________________________
。
(限选试剂有:蒸馏水、稀盐酸、碘水、淀粉)
解析 (1)仪器乙为冷凝管,用于冷凝蒸馏产物,为了使冷凝效果最好,进水口为
b,故答案为:冷凝管;b;
(2)实验室用二氧化锰和浓盐酸加热或高锰酸钾和浓盐酸制备氯气,方程式为:
MnO +4H++2Cl-=====Mn2++Cl ↑+2H O(或2MnO+16H++10Cl-===2Mn2
2 2 2
++5Cl ↑+8H O);实验过程中,为减少PCl 的生成,应控制氯气的通入速率;故
2 2 5
答案为:MnO +4H++2Cl-=====Mn2++Cl ↑+2H O(或2MnO+16 H++10Cl-
2 2 2
===2Mn2++5Cl ↑+8H O);氯气的通入速率;
2 2
(3)氯气有毒,污染空气,碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气
进入影响产品纯度,故答案为:碱石灰吸收多余氯气,防止污染空气;
(4)由于PCl 遇O 会生成POCl ,遇水生成H PO 和HCl,通入一段时间的CO 可
3 2 3 3 3 2
以排尽装置中的空气,防止生成的PCl 与空气中的O 和水反应;通入二氧化碳赶
3 2
净空气,避免水和氧气与三氯化磷发生反应,故答案为:排净装置中的空气,防止
空气中的水分和氧气与PCl 反应;
3
(5)0.100 0 mol·L-1碘溶液20.00 mL中含有碘单质的物质的量为:0.100 0 mol·L-
1×0.020 L=0.002 mol,根据反应I +2Na S O ===2NaI+Na S O 可知,与磷酸反
2 2 2 3 2 4 6
应消耗的碘单质的物质的量为:0.002 mol-0.100 0 mol·L-1×0.012 L×1/2=0.001
4 mol,再由H PO +H O+I ===H PO +2HI可知,25 mL三氯化磷水解后的溶液
3 3 2 2 3 4
中含有的H PO 的物质的量为:n(H PO )=n(I )=0.001 4 mol,500 mL该溶液中含
3 3 3 3 2
有H PO 的物质的量为:0.001 4 mol×500 mL/25 mL=0.028 mol,所以4.100 g产
3 3
品中含有的三氯化磷的物质的量为 0.028 mol,该产品中 PCl 的质量分数为:
3
×100%≈93.9%;若滴定终点时俯视读数,读出的标准液硫代硫酸钠溶液体积偏
小,计算出的H PO 消耗的碘单质的物质的量偏大,三氯化磷的物质的量偏大,三
3 3氯化磷的质量分数偏大,故答案为:93.9%;偏大;
(6)设计实验证明PCl 具有还原性的方案为:向碘水中加入PCl ,碘水褪色;故答案
3 3
为:向碘水中加入PCl ,碘水褪色。
3
答案 (1)冷凝管(或冷凝器) b
(2)MnO +4H++2Cl-=====Mn2++Cl ↑+2H O(或 2MnO+16H++10Cl-
2 2 2
===2Mn2++5Cl ↑+8H O) 氯气通入的速率(或流量)
2 2
(3)吸收多余的Cl ,防止污染环境
2
(4)排净装置中的空气,防止O 和水与PCl 反应
2 3
(5)93.9% 偏大
(6)向碘水中加入PCl ,碘水褪色
3
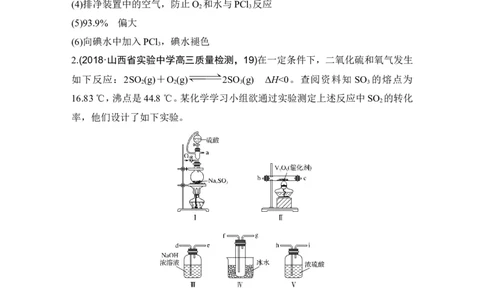
2.(2018·山西省实验中学高三质量检测,19)在一定条件下,二氧化硫和氧气发生
如下反应:2SO (g)+O (g) 2SO (g) ΔH<0。查阅资料知 SO 的熔点为
2 2 3 3
16.83 ℃,沸点是44.8 ℃。某化学学习小组欲通过实验测定上述反应中SO 的转化
2
率,他们设计了如下实验。
请根据要求回答问题:
(1)各装置接口的连接顺序是a→________________________________________。
(2)装置Ⅳ烧杯中盛放冰水的作用是_____________________________________。
(3) 装 置 Ⅰ 所 用 硫 酸 , 一 般 选 用 浓 度 为 70% ~ 80% 的 硫 酸 , 原 因 是
____________________________________________________________________。
(4)当装置Ⅰ中反应结束时,要打开止水夹继续通入O 一段时间,继续通入O 的目
2 2
的是__________________________________________________________________________________________________________________________________。
(5)称量a g Na SO 粉末与足量硫酸反应,实验结束后称得装置Ⅳ增重b g,列式表
2 3
示该实验中SO 的转化率_________________________________________。
2
解析 (1)Ⅰ是制备二氧化硫,Ⅱ是氧化二氧化硫,Ⅳ是收集三氧化硫,Ⅲ是吸收
尾 气 , 为 测 定 SO 转 化 为 SO 的 转 化 率 , 仪 器 的 连 接 顺 序 是
2 3
a→h→i→b→c→f→g→d→e。(2)由于SO 的熔点为16.83 ℃,沸点是44.8 ℃,所以
3
装置Ⅳ烧杯中盛放冰水的作用是使SO 冷凝以便从气相中分离出来;(3)由于硫酸
3
浓度过大时主要以分子形式存在,反应较慢;硫酸浓度过小时生成的 SO 会部分
2
溶解在稀硫酸中,故制备二氧化硫气体时一般选用浓度为70%~80%的硫酸与亚
硫酸钠固体加热反应; (4)当装置Ⅰ中反应结束时,继续通入O 一段时间,目的是
2
将装置中的SO 全部转移到装置Ⅱ中发生反应,将SO 全部转移到装置Ⅳ中冷凝
2 3
为固体,提高测量SO 转化率的准确性;(5)称量a g Na SO 粉末与足量硫酸反应,
2 2 3
实验结束后称得装置Ⅳ增重b g,由硫元素守恒可知,SO 的转化率=b g÷
2
80 g/mol÷(a g÷126 g/mol)=×100%。
答案 (1)h→i→b→c→f→g→d→e
(2)使SO 冷凝以便从气相中分离出来
3
(3)硫酸浓度过大时主要以分子形式存在,反应较慢;硫酸浓度过小时生成的 SO
2
会部分溶解在稀硫酸中
(4)将装置中的SO 全部赶入装置Ⅱ中发生反应,将SO 全部赶入装置Ⅳ中冷凝为
2 3
固体,提高测量SO 转化率的准确性
2
(5)×100%
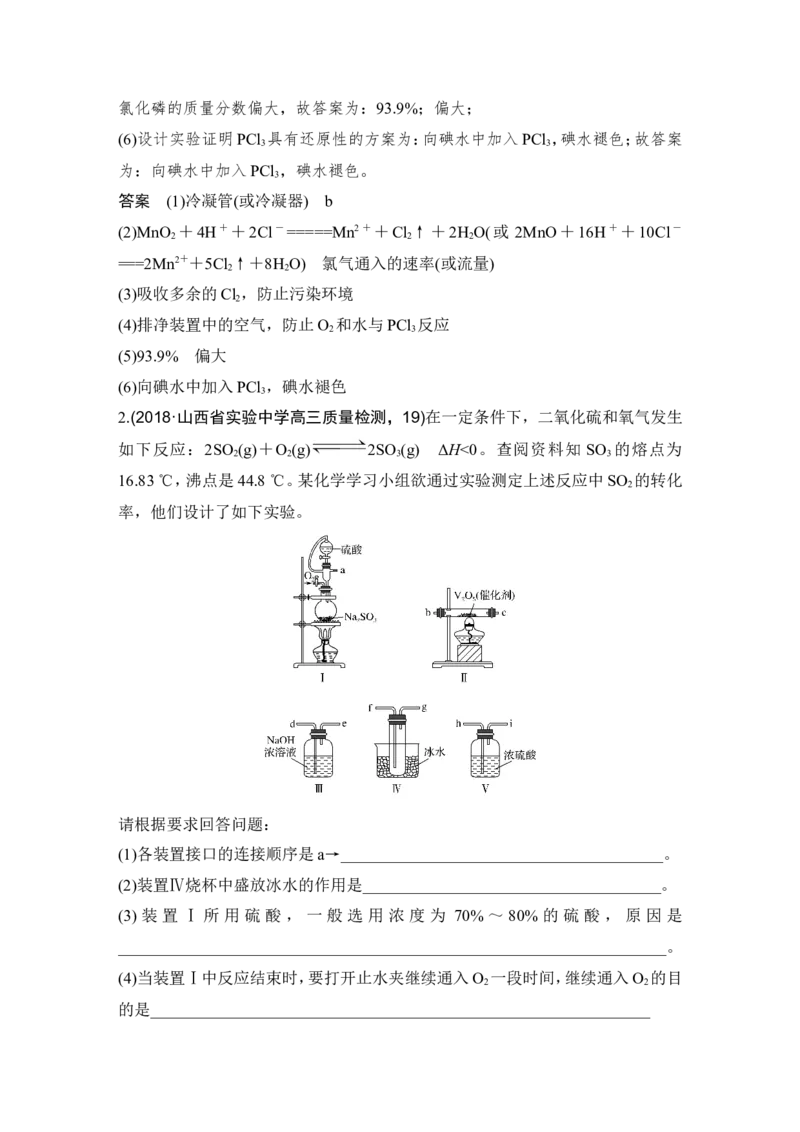
3.(2018·河南洛阳二模,26)为测定某氟化稀土样品中氟元素的质量分数,某化学
兴趣小组进行了如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化
氢(低沸点酸)蒸出,再滴定测量。实验装置如图所示。(1)a 的 作 用 是 ________ , 仪 器 d 的 名 称 是
____________________________________________________________________。
(2)检查装置气密性:________(填操作),关闭k,微热c,导管e末端有气泡冒出;停
止加热,导管e内有一段稳定的水柱,说明装置气密性良好。
(3)c中加入一定体积高氯酸和m g氟化稀土样品,f中盛有滴加酚酞的NaOH溶液
加热b、c,使b中产生的水蒸气进入c。
①下列物质可代替高氯酸的是________(填序号)。
A.硝酸 B.盐酸
C.硫酸 D.磷酸
②实验中除有HF气体外,可能还有少量SiF (易水解)气体生成。若有SiF 生成,实
4 4
验结果将________(填“偏高”“偏低”或“不受影响”)。
③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结
果偏低,原因是____________________________________________________
___________________________________________________________________。
(4)向馏出液中加入V mL c mol·L-1La(NO ) 溶液,得到LaF 沉淀,再用c mol·L-
1 1 3 3 3 2
1 EDTA标准溶液滴定剩余 La3+(La3+与EDTA按1∶1配合),消耗EDTA标准溶
液V mL,则氟化稀土样品中氟的质量分数为________。
2
(5)用样品进行实验前,需要用0.084 g氟化钠代替样品进行实验,改变条件(高氯
酸用量、反应温度、蒸馏时间),测量并计算出氟元素质量,重复多次。该操作的目
的是________________________。
解析 (1)a的作用是平衡压强,防止圆底烧瓶中压强过大,引起爆炸。仪器d的名
称是直形冷凝管。
(2)检查装置气密性时在b和f中加水,使水浸没a和e的末端,从而形成密闭体系。
(3)①此实验是利用高氯酸(高沸点酸)将样品中的氟元素转化为HF(低沸点酸)蒸
出。硝酸和盐酸易挥发,A、B项错误;硫酸和磷酸沸点高,难挥发,C、D项正确。
②实验中除有HF气体外,可能还有少量SiF (易水解)气体生成,若有SiF 生成,
4 4
SiF 易水解,与NaOH溶液反应也生成NaF,不影响实验结果。
4
③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结
果偏低,原因是充分吸收HF气体,防止其挥发损失。
(5)用样品进行实验前,需要用0.084 g氟化钠代替样品进行实验,改变条件(高氯酸的用量、反应温度、蒸馏时间),测量并计算出氟元素质量,重复多次,该操作的
目的是通过做对比实验,寻找最佳的实验条件。
答案 (1)平衡压强 直形冷凝管
(2)在b和f中加水,水浸没导管a和e末端
(3)①CD ②不受影响
③充分吸收HF气体,防止其挥发损失
(4)%
(5)寻找最佳实验条件
4.(2019·平度一中高三阶段性质量检测,28)Cu SO ·CuSO ·2H O是一种深红色固
2 3 3 2
体(以下用M表示)。某学习小组拟测定胆矾样品的纯度,并以其为原料制备M。
已知:①M不溶于水和乙醇,100℃时发生分解反应;
②M 可 由 胆 矾 和 SO 为 原 料 制 备 , 反 应 原 理 为 3Cu2 + + 6H O +
2 2
3SO =====Cu SO ·CuSO ·2H O↓+8H++SO。
2 2 3 3 2
Ⅰ.测定胆矾样品的纯度。
(1)取 g胆矾样品溶于蒸馏水配制成250 mL溶液,从中取25.00 mL于锥形瓶中
w
加入指示剂,用c mol·L-1EDTA(简写成Na Y)标准溶液滴定至终点(滴定原理:
4
Cu2++Y4-===CuY2-),测得消耗了V mL EDTA标准溶液。则该胆矾样品的纯度为
________%(用含c、V、 的代数式表示)。如果滴定管装液前没有用EDTA标准溶
w
液润洗,测得的结果会__________ (填“偏高”“偏低”或“无影响”)。
Ⅱ.制备M实验装置如下图所示:
(2)实验室用70%硫酸与亚硫酸钠粉末在常温下制备SO 。上图A处的气体发生装
2
置可从下图装置中选择,最合适的是________(填字母)。(3)装置D中的试剂是________。装置B中水浴加热的优点是__________。
(4)实验完毕冷却至室温后,从锥形瓶中分离产品的操作包括:________、水洗、乙
醇洗、常温干燥,得产品 Cu SO ·CuSO ·2H O。检验产品已水洗完全的操作是
2 3 3 2
______________________________________________________________________
_____________________________________________________________________
。
解析 (1)Cu2+~Y4-,故胆矾样品的纯度=×100%=%。如果滴定管装液前没有
用EDTA标准溶液润洗,EDTA标准溶液在滴定管中会被稀释,使滴定消耗的
EDTA标准溶液体积偏大,结果偏高。
(2)70%硫酸与亚硫酸钠粉末在常温下反应生成SO ,应选择固液不加热制气装置,
2
即装置a。
(3)装置D用于吸收未反应的SO ,其中盛装的试剂可以是NaOH溶液、Na CO 溶
2 2 3
液、NaHCO 溶液或Na SO 溶液等。装置B中水浴加热的优点是受热均匀,容易控
3 2 3
制温度范围,可防止温度过高导致产品分解。
(4)用过滤的方法分离固体和溶液。水洗的目的是除去产品表面的可溶性杂质,通
过检验洗涤液中是否存在SO或H+来判断水洗是否完全。
答案 (1) 偏高 (2)a
(3)NaOH溶液(其他合理答案也可) 受热均匀,容易控制温度范围,可防止温度过
高导致产品分解
(4)过滤 取最后一次洗涤液少许于试管中,加入盐酸酸化的BaCl 溶液,若无沉淀
2
生成,则产品已水洗完全(也可检验最后一次洗涤液中的H+)
5.黄铜矿是工业炼铜的主要原料,主要成分为CuFeS ,含少量脉石。为测定该黄铜
2
矿的纯度,某同学设计了如下实验:现用电子天平称取研细的黄铜矿样品1.150 g,在空气存在下进行煅烧,生成Cu、
Fe O 和SO 气体,实验后取d中溶液的置于锥形瓶中,用0.05 mol·L-1标准碘溶
3 4 2
液进行滴定,消耗标准碘溶液20.00 mL。请回答下列问题:
(1) 将 样 品 研 细 后 再 进 行 反 应 , 其 目 的 是
______________________________________________________________________
_____________________________________________________________________
,
标准碘溶液应盛放在________(填“碱式”或“酸式”)滴定管中。
(2)装置a的作用是________。
A.除去空气中的二氧化碳
B.除去空气中的水蒸气
C.有利于气体混合
D.有利于观察、控制空气流速
(3)若去掉c装置,会使测定结果________(填“偏低”“偏高”或“无影响”),写
出 影 响 测 定 结 果 的 化 学 方 程 式
_____________________________________________________________________
_____________________________________________________________________
。
(4)上述反应结束后,仍需通一段时间的空气,其目的是
_____________________________________________________________________
。
(5)通过计算可知,该黄铜矿的纯度为________。
(6)假设实验操作均正确,测得的黄铜矿纯度仍然偏低,可能的原因主要有
______________________________________________________________________
_____________________________________________________________________
。解析 (1)将样品研细的目的是与O 充分接触,使之燃烧充分,加快燃烧速率。因
2
碘溶液腐蚀橡胶,故应放入酸式滴定管中。
(2)a中浓H SO 能吸水,且可通过a装置观察气泡,控制空气流速。
2 4
(3)铜网的作用是除去过量的O ,防止O 将SO 氧化。同时O 也有可能将I-氧化
2 2 2 2
成I ,I 继续氧化SO ,故去掉c消耗碘溶液会小于20.00 mL,使测定结果偏低。
2 2 2
(4)空气能将反应生成的SO 全部赶入d中,使测定结果准确。
2
(5)令黄铜矿的纯度为x,由SO +I +2H O===H SO +2HI和硫元素守恒得:
2 2 2 2 4
CuFeS ~ 2SO ~2I
2 2 2
184 g 2 mol
1.150x g 0.05 mol·L-1×20.00×10-3 L×10
=
x=80%。
(6)若滴定时消耗的I 少,则滴定的SO 少,测得纯度较低,原因可能是反应速率快
2 2
SO 未被水完全吸收,或H SO 被过量O 氧化等。
2 2 3 2
答案 (1)增大与空气的接触面积,加快反应速率,且充分燃烧 酸式
(2)BD
(3)偏低 2SO +O +2H O===2H SO 、O +4I-+4H+===2I +2H O
2 2 2 2 4 2 2 2
(4)使反应生成的SO 全部进入d中,使测定结果准确
2
(5)80%
(6)反应速率快,用水吸收SO 不充分,H SO 被过量的O 氧化
2 2 3 2
6.(2018·南昌NCS项目三模,26)磷化铝(AlP)通常可作为一种广谱性熏蒸杀虫剂,
吸水后会立即产生高毒性PH 气体(沸点为-87.7 ℃,还原性强)。某化学兴趣小组
3
的同学用下述方法测定粮食中残留的磷化物的含量,实验装置如图所示。
在 C 中加入 100 g 原粮,E 中加入 20.00 mL 1.50×10-3 mol·L-1 KMnO 溶液
4
(H SO 酸化),往C中加入足量的水,充分反应后,用亚硫酸钠标准溶液滴定E中
2 4过量的KMnO 溶液。
4
回答下列问题:
(1)仪器D的名称是________。
(2)AlP与水反应的化学方程式为____________________________________。
(3)装置A中盛装酸性KMnO 溶液的作用是除去空气中的还原性气体,装置 B中
4
盛有焦性没食子酸的碱性溶液,其作用是_________________________________。
(4)通入空气的作用是__________________________________________________。
(5)装置E中PH 被氧化成磷酸,则装置E中发生反应的氧化剂和还原剂的物质的
3
量之比为_____________________________________________________________。
(6)收集装置E中的吸收液,加水稀释至250 mL,取25.00 mL于锥形瓶中,用
4.0×10-4 mol·L-1的Na SO 标准溶液滴定剩余的KMnO 溶液,消耗Na SO 标准
2 3 4 2 3
溶 液 15.00 mL , Na SO 与 KMnO 溶 液 反 应 的 离 子 方 程 式 为
2 3 4
_____________________________________________________________________,
则 该 原 粮 中 磷 化 物 ( 以 PH 计 ) 的 含 量 为
3
_____________________________________
mg·kg-1(写计算表达式和计算结果)。
解析 (1)仪器D为直形冷凝管。(2)AlP与H O反应生成PH 和Al(OH) 。(3)装置B
2 3 3
中焦性没食子酸的碱性溶液的作用是吸收空气中的 O ,避免O 进入装置C中将
2 2
PH 氧化。(4)要准确测定PH 的含量,需要用酸化的KMnO 溶液将其全部吸收,通
3 3 4
入空气的作用是保证生成的 PH 全部被酸性 KMnO 溶液吸收。(5)PH 被酸性
3 4 3
KMnO 溶液氧化成磷酸,KMnO 在酸性条件下被还原为Mn2+,根据反应前后元
4 4
素化合价的变化可写出并配平该反应的离子方程式为 5PH +8MnO+24H+
3
===5H PO +8Mn2++12H O,其中MnO为氧化剂,PH 为还原剂,二者物质的量
3 4 2 3
之比为8∶5。(6)与酸性KMnO 溶液反应时,Na SO 被氧化成Na SO ,KMnO 在
4 2 3 2 4 4
酸性条件下被还原为Mn2+,根据元素化合价变化可写出并配平该反应的离子方
程式为5SO+2MnO+6H+===5SO+2Mn2++3H O。滴定时消耗Na SO 的物质的
2 2 3
量为 15.00×10-3×4.0×10-4mol,对应消耗 KMnO 的物质的量为(15.00×10-
4
3×4.0×10-4×)mol,则与 PH 反应的 KMnO 的物质的量为 (20.00×10-
3 4
3×1.50×10-3-15.00×10-3×4.0×10-4××)mol=6×
10-6mol,结合关系式5PH ~8MnO可求出该原粮中磷化物(以PH 计)的含量为
3 3mg·kg-1=1.275 mg·kg-1。
答案 (1)直形冷凝管(或冷凝管) (2)AlP+3H O===PH ↑+Al(OH) (3)吸收空
2 3 3
气中的O (4)保证生成的PH 全部被酸性KMnO 溶液吸收 (5)8∶5
2 3 4
(6)5SO+2MnO+6H+===5SO+2Mn2++3H O
2
[(20.00×10-3×1.50×10-3-15.00×10-3×4.0×10-4×)××34×103]÷(100×10-
3)mg·kg-1=1.275