文档内容
第 21 讲 硫及其化合物的相互转化
[复习目标] 1.通过完成不同价态、类别含硫物质的转化关系,进一步提升从价、类不同视
角探究物质性质的学科素养。2.进一步巩固硫及其典型代表物的性质及应用。
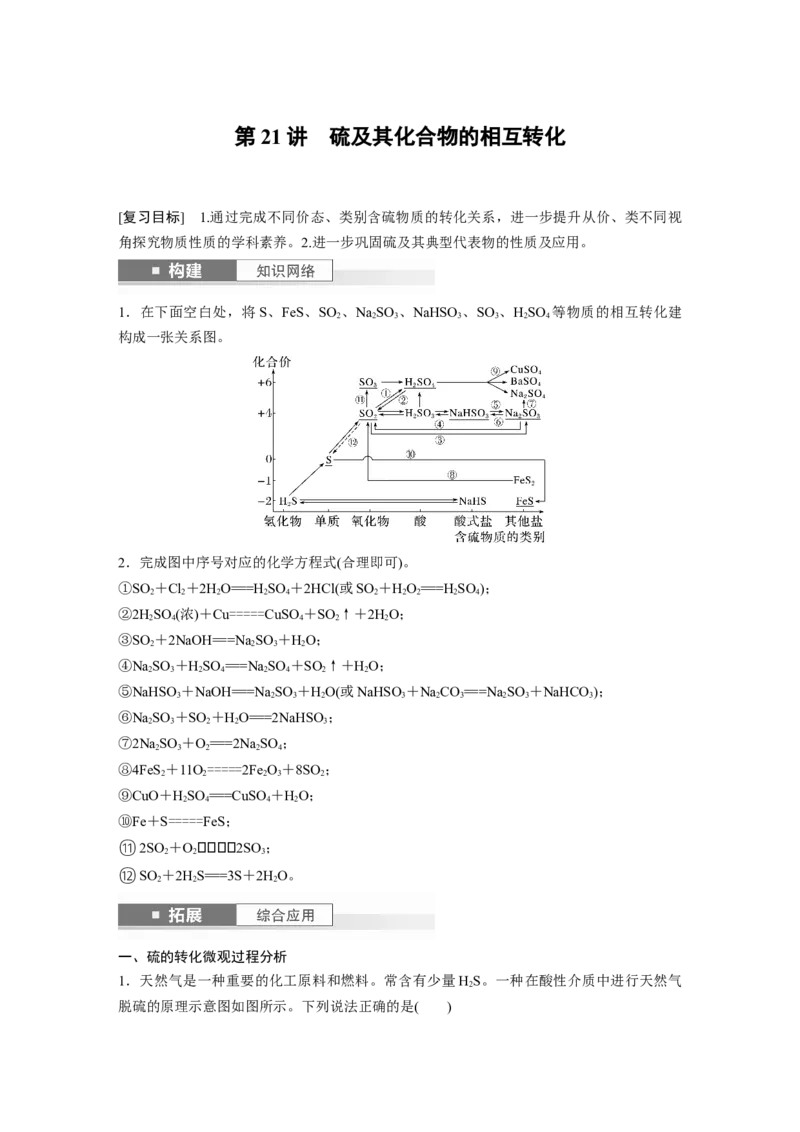
1.在下面空白处,将S、FeS、SO 、NaSO 、NaHSO 、SO 、HSO 等物质的相互转化建
2 2 3 3 3 2 4
构成一张关系图。
2.完成图中序号对应的化学方程式(合理即可)。
①SO +Cl+2HO===HSO +2HCl(或SO +HO===HSO );
2 2 2 2 4 2 2 2 2 4
②2HSO (浓)+Cu=====CuSO +SO ↑+2HO;
2 4 4 2 2
③SO +2NaOH===NaSO +HO;
2 2 3 2
④NaSO +HSO ===NaSO +SO ↑+HO;
2 3 2 4 2 4 2 2
⑤NaHSO+NaOH===NaSO +HO(或NaHSO+NaCO===NaSO +NaHCO );
3 2 3 2 3 2 3 2 3 3
⑥NaSO +SO +HO===2NaHSO;
2 3 2 2 3
⑦2NaSO +O===2NaSO ;
2 3 2 2 4
⑧4FeS+11O=====2Fe O+8SO ;
2 2 2 3 2
⑨CuO+HSO ===CuSO +HO;
2 4 4 2
⑩Fe+S=====FeS;
⑪2SO +O2SO ;
2 2 3
⑫SO +2HS===3S+2HO。
2 2 2
一、硫的转化微观过程分析
1.天然气是一种重要的化工原料和燃料。常含有少量HS。一种在酸性介质中进行天然气
2
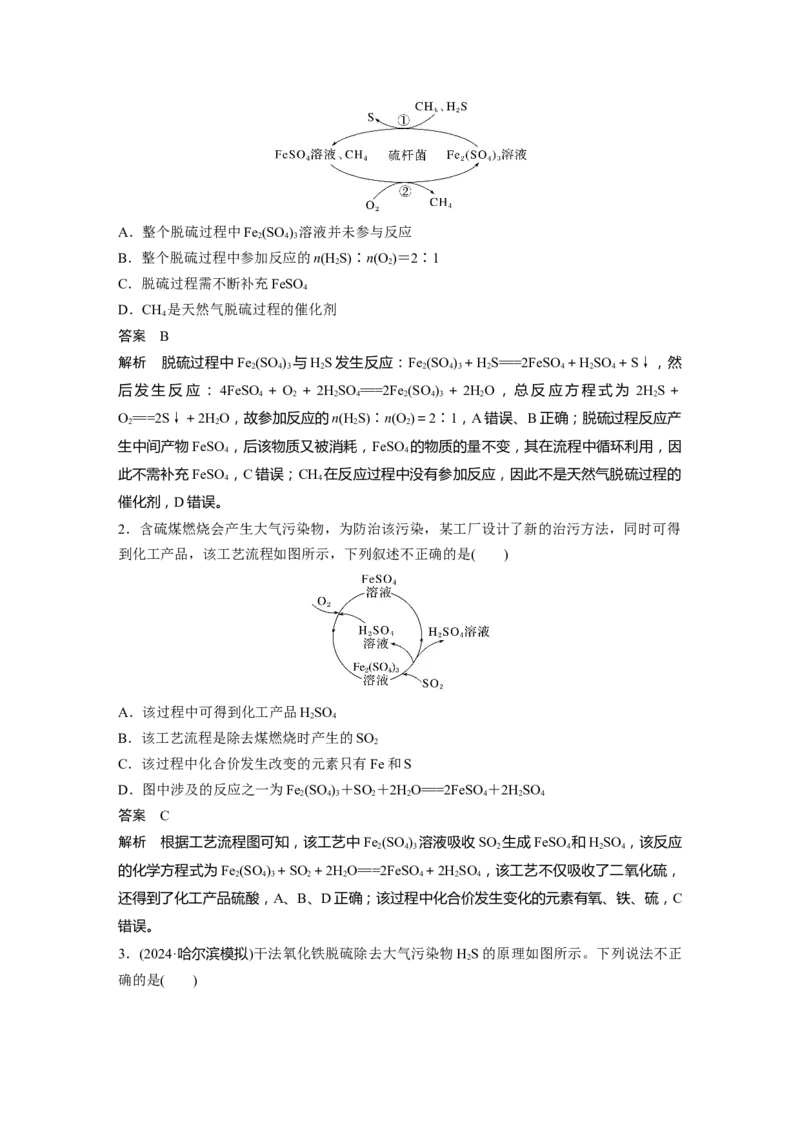
脱硫的原理示意图如图所示。下列说法正确的是( )A.整个脱硫过程中Fe (SO ) 溶液并未参与反应
2 4 3
B.整个脱硫过程中参加反应的n(H S)∶n(O )=2∶1
2 2
C.脱硫过程需不断补充FeSO
4
D.CH 是天然气脱硫过程的催化剂
4
答案 B
解析 脱硫过程中Fe (SO ) 与HS发生反应:Fe (SO ) +HS===2FeSO +HSO +S↓,然
2 4 3 2 2 4 3 2 4 2 4
后发生反应:4FeSO +O +2HSO ===2Fe (SO ) +2HO,总反应方程式为 2HS+
4 2 2 4 2 4 3 2 2
O===2S↓+2HO,故参加反应的n(H S)∶n(O )=2∶1,A错误、B正确;脱硫过程反应产
2 2 2 2
生中间产物FeSO ,后该物质又被消耗,FeSO 的物质的量不变,其在流程中循环利用,因
4 4
此不需补充FeSO ,C错误;CH 在反应过程中没有参加反应,因此不是天然气脱硫过程的
4 4
催化剂,D错误。
2.含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得
到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
A.该过程中可得到化工产品HSO
2 4
B.该工艺流程是除去煤燃烧时产生的SO
2
C.该过程中化合价发生改变的元素只有Fe和S
D.图中涉及的反应之一为Fe (SO )+SO +2HO===2FeSO +2HSO
2 4 3 2 2 4 2 4
答案 C
解析 根据工艺流程图可知,该工艺中Fe (SO ) 溶液吸收SO 生成FeSO 和HSO ,该反应
2 4 3 2 4 2 4
的化学方程式为Fe (SO ) +SO +2HO===2FeSO +2HSO ,该工艺不仅吸收了二氧化硫,
2 4 3 2 2 4 2 4
还得到了化工产品硫酸,A、B、D正确;该过程中化合价发生变化的元素有氧、铁、硫,C
错误。
3.(2024·哈尔滨模拟)干法氧化铁脱硫除去大气污染物HS的原理如图所示。下列说法不正
2
确的是( )A.Fe O·H O为该反应的催化剂
2 3 2
B.脱硫反应为3HS+Fe O·H O===Fe S·H O+3HO
2 2 3 2 2 3 2 2
C.再生过程中,硫元素被还原
D.总反应为2HS+O=====2S↓+2HO
2 2 2
答案 C
解析 根据题图可知,Fe O·H O先参与反应后又生成,为该反应的催化剂,A正确;根据
2 3 2
题图可知,脱硫过程中HS和Fe O·H O反应生成Fe S·H O和HO,B正确;再生过程中,
2 2 3 2 2 3 2 2
Fe S·H O转化为S单质,硫元素的化合价升高,被氧化,C错误;根据转化关系可知,总
2 3 2
反应为2HS+O=====2S↓+2HO,D正确。
2 2 2
二、实验室中实现硫及其化合物的转化
4.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①NaSO 溶液 ②浓硫酸 ③NaS溶液 ④稀硫酸 ⑤酸性
2 3 2
KMnO 溶液 ⑥品红溶液 ⑦铜片
4
实验序号 预期转化 选择试剂(填序号) 证明实现转化的现象
ⅰ S―→S
ⅱ ①③④ 淡黄色沉淀
ⅲ S―→S ②⑥⑦
(1)实验ⅰ选择的试剂是①和________(填序号),证明实现转化的现象是_________________,
该转化利用了NaSO 的________性。
2 3
(2)实验ⅱ实现了________价S向________价S的转化。
(3)实验ⅲ中发生反应的化学方程式是____________________________________________,
证 明 实 现 转 化 的 现 象 是
_____________________________________________________________。
答案 (1)⑤ 酸性KMnO 溶液褪色 还原
4
(2)+4(或-2) 0 (3)Cu+2HSO (浓)=====CuSO +SO ↑+2HO 将产生的气体通入品红
2 4 4 2 2
溶液,品红溶液褪色
三、工艺流程中硫的转化
5.硫代硫酸钠是一种常用的滴定剂,利用硫化亚铜制取硫代硫酸钠晶体的步骤如图所示。
试回答下列问题。(1)反应釜中发生反应的化学方程式为_______________________________________________
_______________________________________________________________________________
。
(2)当=________时,固体 A和气体 B的利用率最高。若高于该比值,则产品中会混有
________杂质。
(3)Na SO 的应用——测定KBrO 的纯度(杂质不参与反应)
2 2 3 3
取m g KBrO 样品溶于适量水中,加入稀硫酸酸化,加入过量KI溶液,将反应后溶液稀释
3
为250 mL。取25 mL置于锥形瓶中,加入指示剂,用c mol·L-1的NaSO 溶液滴定,重复
2 2 3
实验3次,平均消耗NaSO 溶液的体积为V mL(已知:I+2SO===2I-+SO)。
2 2 3 2 2 4
①向KBrO 溶液中加入过量KI溶液,发生反应的离子方程式为_______________________。
3
②滴定过程中所用的指示剂为__________,KBrO 样品的纯度为__________%。
3
答案 (1)S+SO +2NaHCO ===NaSO+HO+2CO
2 3 2 2 3 2 2
(2) 亚硫酸钠
(3)①BrO+6I- +6H+===3I↓+Br-+3HO ②淀粉溶液
2 2
解析 (1)Cu S在空气中煅烧可以发生两种反应,①Cu S+O=====2CuO+S,②Cu S+
2 2 2 2
2O=====SO +2CuO;则可推断产生的黄色固体为S,反应釜中S和SO 与过量NaHCO 反
2 2 2 3
应,化学方程式为 S+SO +2NaHCO ===NaSO +HO+2CO 。(2)由 S+SO +
2 3 2 2 3 2 2 2
2NaHCO ===NaSO+HO+2CO 可知,n(S)∶n(SO )为1∶1时,固体A与气体B的利用率
3 2 2 3 2 2 2
最高,①+②可得:2Cu S+3O=====4CuO+S+SO ,当=时,利用率最高,若高于此值,
2 2 2
二氧化硫会与碳酸氢钠反应生成亚硫酸钠。(3)②滴定过程中所用指示剂为淀粉溶液,因为
淀粉遇碘变蓝,消耗NaSO 的物质的量为c mol·L-1×V×10-3 L=cV×10-3 mol,根据关
2 2 3
系式:KBrO ~3I ~6SO,25 mL溶液中KBrO 的物质的量为×cV×10-3 mol,则250 mL
3 2 2 3
溶液中KBrO 的物质的量为×cV×10-2 mol,纯度为×100%=%。
3
1.(2021·辽宁,8)含S元素的某钠盐a能发生如图转化。下列说法错误的是( )
A.a可能为正盐,也可能为酸式盐B.c为不溶于盐酸的白色沉淀
C.d为含极性键的非极性分子
D.反应②中还可能生成淡黄色沉淀
答案 C
解析 由题干信息可知,盐 a溶液与足量的稀盐酸反应产生刺激性气味气体 d,d能使
KMnO 溶液褪色,故d为SO ,则盐a为NaSO 或者NaHSO ,也可能是NaSO ,盐a溶
4 2 2 3 3 2 2 3
液与足量Cl 反应后生成SO,与BaCl 溶液反应得到沉淀c,故c为BaSO ,据此分析解题。
2 2 4
由分析可知,a可能为正盐,也可能为酸式盐,A正确;c为BaSO,故c为不溶于盐酸的白
4
色沉淀,B 正确;d 为 SO ,是含有极性键的极性分子,C 错误;盐 a 为 NaSO 或者
2 2 3
NaHSO ,也可能是NaSO ,NaSO 与稀盐酸可发生反应:NaSO +2HCl===2NaCl+S↓
3 2 2 3 2 2 3 2 2 3
+SO ↑+HO,故反应②中还可能生成淡黄色沉淀,D正确。
2 2
2.(2021·山东,8)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法
2 3
错误的是( )
A.吸收过程中有气体生成
B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高
D.中和后溶液中含NaSO 和NaHCO
2 3 3
答案 B
解析 根据流程图分析可知,吸收过程中有二氧化碳生成,A正确;结晶后母液中含饱和
NaHSO 和过量的二氧化硫形成的亚硫酸,没有NaHCO ,B错误;NaHSO 高温时易分解变
3 3 3
质,所以气流干燥过程中温度不宜过高,C正确;结合上述分析可知,中和后溶液中含
NaSO 和NaHCO ,D正确。
2 3 3
3.(2018·浙江11月选考,28)某同学用下列装置完成了浓硫酸和SO 性质实验(夹持装置已
2
省略)。请回答:
(1)下列说法正确的是________(填字母)。
A.反应后,将试管Ⅰ中的白色固体加入水中,溶液呈蓝色B.取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO
4
C.试管Ⅳ中KMnO 溶液褪色,说明SO 具有氧化性
4 2
D.试管Ⅴ中的NaOH溶液可用NaCO 溶液代替
2 3
(2) 取下试管Ⅱ,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜
色再次变浅。解释“无色→红色→颜色变浅”变化的原因:____________________________
________________________________________________________________________________
_______________________________________________________________________________
。
答案 (1)ABD
(2)SO 遇品红溶液生成不稳定无色物质,受热释放SO ,溶液恢复红色;温度降低,SO 在
2 2 2
品红溶液中溶解度增大,溶液颜色变浅
解析 根据装置图可以判断,Ⅰ生成SO ,Ⅱ验证SO ,Ⅲ验证SO 是否和BaCl 反应,Ⅳ
2 2 2 2
验证SO 的还原性,Ⅴ吸收剩余的SO ,防止污染。(1)A项,白色固体应为CuSO ,加水,
2 2 4
溶液呈蓝色;B项,由于在Ⅲ中生成了HSO ,HSO 很容易被O 氧化生成HSO ,所以生
2 3 2 3 2 2 4
成BaSO 沉淀;D项,由于NaCO 水解呈碱性,所以也可以吸收SO 气体。
4 2 3 2
课时精练
1.用下列两种途径制取HSO ,某些反应条件和产物已省略,下列有关说法不正确的是(
2 4
)
途径① S――→HSO ;
2 4
途径② S――→SO ――→SO ――→HSO
2 3 2 4
A.途径①反应中体现了浓硝酸的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O 的浓度来降低成本
2
C.由途径①和②分别制取1 mol H SO ,理论上各消耗1 mol S,各转移6 mol电子
2 4
D.途径②与途径①相比更能体现“绿色化学”的理念
答案 A
解析 途径①反应的化学方程式为S+6HNO(浓)===HSO +6NO ↑+2HO,浓硝酸只体现
3 2 4 2 2
了强氧化性,没有体现酸性,故 A错误;氧气来源于空气,价格较低,增大氧气的浓度可
提高二氧化硫的转化率,从而降低成本,故B正确;途径①和②中硫元素的价态都是从0价
升高到+6价,故C正确;途径①中会产生NO 有毒气体,故D正确。
2
2.硫在空气中燃烧生成气体A,把A溶于水得溶液B,向B中滴加溴水,溴水褪色,B变
成C,向C中加NaS产生气体D,把D通入B溶液得浅黄色沉淀E。A、B、C、D、E都含
2
同一种元素。下列各物质按A、B、C、D、E顺序排列的是( )
A.SO 、HSO 、HSO 、HS、S
2 2 4 2 3 2B.SO 、HSO 、HSO 、HS、S
2 2 3 2 4 2
C.SO 、HSO 、HSO 、SO 、NaSO
2 2 3 2 4 3 2 2 3
D.SO 、HSO 、HSO 、SO 、NaSO
3 2 4 2 3 2 2 2 3
答案 B
解析 硫在空气中燃烧生成SO ,SO 溶于水得HSO ,向HSO 中滴加溴水生成HSO 和
2 2 2 3 2 3 2 4
HBr,向HSO 溶液中加NaS产生气体HS,HS与HSO 反应产生浅黄色沉淀S,故B项
2 4 2 2 2 2 3
正确。
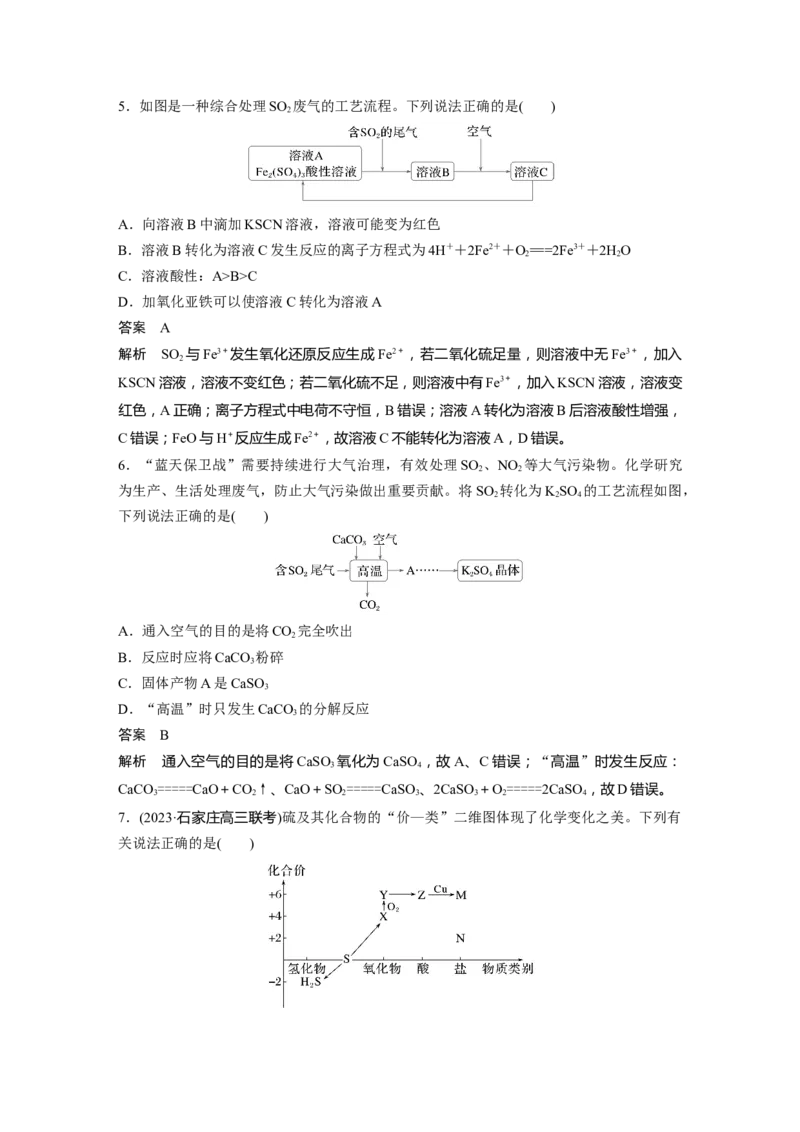
3.(2023·长春模拟)在“价—类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及
其定量关系。图中的字母分别代表硫及其常见化合物,下列相关推断不合理的是( )
A.b、d、f既具有氧化性又具有还原性
B.硫酸型酸雨的形成过程涉及b到c的转化
C.a溶液与b溶液反应过程中有淡黄色沉淀生成
D.d在加热条件下与强碱溶液反应生成e和f,且n(e)∶n(f)=1∶2
答案 D
解析 根据图中信息,b为HSO ,d为S,f为亚硫酸盐,其中S元素都处于中间价态,既
2 3
有氧化性,又有还原性,A正确;硫酸型酸雨的形成涉及HSO 被氧气氧化转化为HSO ,
2 3 2 4
B正确;a为HS,b为HSO ,a溶液与b溶液反应过程中有淡黄色沉淀生成,C正确;d为
2 2 3
S,e 为 S2-形成的盐,f 为 SO 形成的盐,由 3S+6OH-=====2S2-+SO+3HO 可得,
2
n(e)∶n(f)=2∶1,D错误。
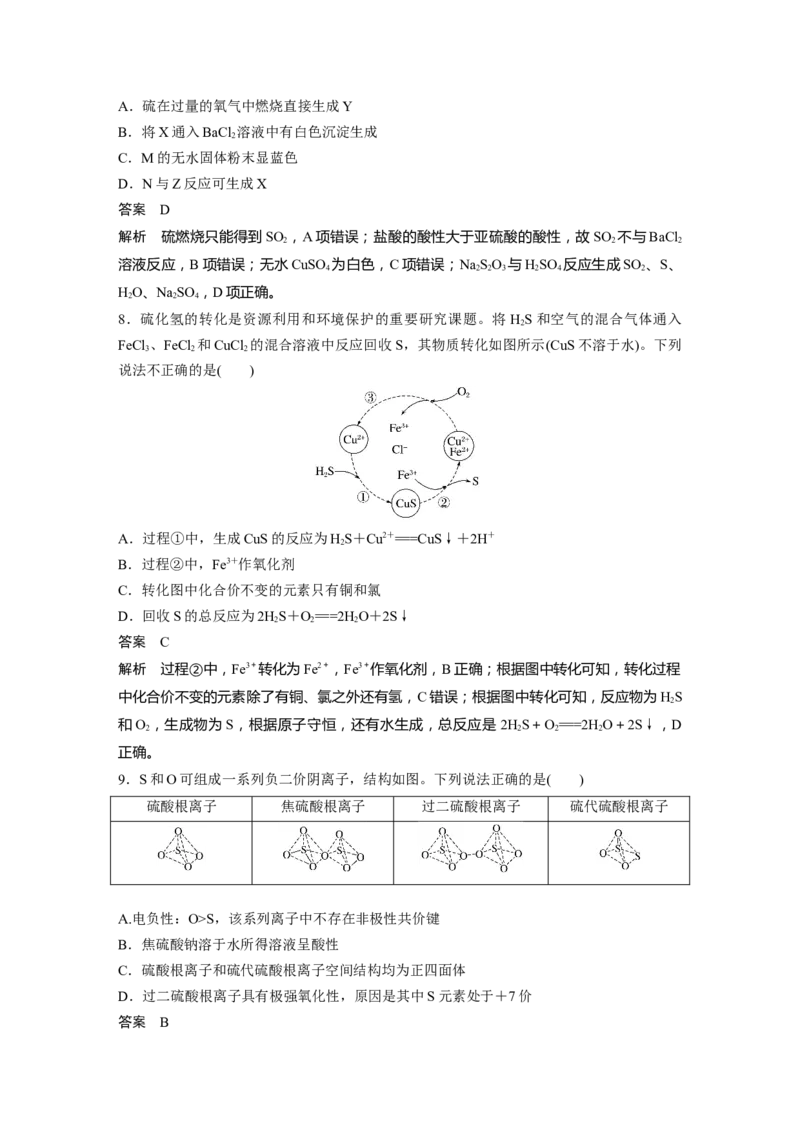
4.如图是硫元素在自然界中的循环示意图,下列说法不正确的是( )
A.海水中的硫元素主要以S2-形式存在
B.煤中含有硫元素,燃煤中加入生石灰可脱硫
C.硫具有弱氧化性,和变价金属反应,通常将金属氧化成低价态
D.硫化氢溶于水得到氢硫酸,氢硫酸是弱酸,能与碱、碱性氧化物反应
答案 A5.如图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
答案 A
解析 SO 与Fe3+发生氧化还原反应生成Fe2+,若二氧化硫足量,则溶液中无Fe3+,加入
2
KSCN溶液,溶液不变红色;若二氧化硫不足,则溶液中有Fe3+,加入KSCN溶液,溶液变
红色,A正确;离子方程式中电荷不守恒,B错误;溶液A转化为溶液B后溶液酸性增强,
C错误;FeO与H+反应生成Fe2+,故溶液C不能转化为溶液A,D错误。
6.“蓝天保卫战”需要持续进行大气治理,有效处理SO 、NO 等大气污染物。化学研究
2 2
为生产、生活处理废气,防止大气污染做出重要贡献。将SO 转化为KSO 的工艺流程如图,
2 2 4
下列说法正确的是( )
A.通入空气的目的是将CO 完全吹出
2
B.反应时应将CaCO 粉碎
3
C.固体产物A是CaSO
3
D.“高温”时只发生CaCO 的分解反应
3
答案 B
解析 通入空气的目的是将CaSO 氧化为CaSO ,故A、C错误;“高温”时发生反应:
3 4
CaCO =====CaO+CO↑、CaO+SO =====CaSO、2CaSO+O=====2CaSO,故D错误。
3 2 2 3 3 2 4
7.(2023·石家庄高三联考)硫及其化合物的“价—类”二维图体现了化学变化之美。下列有
关说法正确的是( )A.硫在过量的氧气中燃烧直接生成Y
B.将X通入BaCl 溶液中有白色沉淀生成
2
C.M的无水固体粉末显蓝色
D.N与Z反应可生成X
答案 D
解析 硫燃烧只能得到SO ,A项错误;盐酸的酸性大于亚硫酸的酸性,故SO 不与BaCl
2 2 2
溶液反应,B项错误;无水CuSO 为白色,C项错误;NaSO 与HSO 反应生成SO 、S、
4 2 2 3 2 4 2
HO、NaSO ,D项正确。
2 2 4
8.硫化氢的转化是资源利用和环境保护的重要研究课题。将 HS和空气的混合气体通入
2
FeCl 、FeCl 和CuCl 的混合溶液中反应回收S,其物质转化如图所示(CuS不溶于水)。下列
3 2 2
说法不正确的是( )
A.过程①中,生成CuS的反应为HS+Cu2+===CuS↓+2H+
2
B.过程②中,Fe3+作氧化剂
C.转化图中化合价不变的元素只有铜和氯
D.回收S的总反应为2HS+O===2HO+2S↓
2 2 2
答案 C
解析 过程②中,Fe3+转化为Fe2+,Fe3+作氧化剂,B正确;根据图中转化可知,转化过程
中化合价不变的元素除了有铜、氯之外还有氢,C错误;根据图中转化可知,反应物为HS
2
和O ,生成物为S,根据原子守恒,还有水生成,总反应是 2HS+O===2HO+2S↓,D
2 2 2 2
正确。
9.S和O可组成一系列负二价阴离子,结构如图。下列说法正确的是( )
硫酸根离子 焦硫酸根离子 过二硫酸根离子 硫代硫酸根离子
A.电负性:O>S,该系列离子中不存在非极性共价键
B.焦硫酸钠溶于水所得溶液呈酸性
C.硫酸根离子和硫代硫酸根离子空间结构均为正四面体
D.过二硫酸根离子具有极强氧化性,原因是其中S元素处于+7价
答案 B解析 焦硫酸钠溶于水生成NaHSO ,为强酸的酸式盐,溶液呈酸性,故B正确;由图可知,
4
硫酸根离子空间结构为正四面体,其中1个O原子被S取代,导致硫代硫酸根离子中空间结
构为四面体,但不是正四面体,故C错误;过二硫酸根离子中含有过氧键,S为+6价,其
具有较强的氧化性是因为其中含有过氧键,故D错误。
10.(2023·河北唐山二模)连二亚硫酸钠(Na SO)俗称保险粉,是一种强还原剂,广泛用于纺
2 2 4
织工业。某种NaSO 的生产工艺流程如图所示,若在实验室模拟该工艺流程,下列说法正
2 2 4
确的是( )
A.可用银氨溶液鉴别甲酸中是否含有甲醛
B.NaCl溶解度大于NaSO·2H O的溶解度
2 2 4 2
C.过滤操作中需要用的玻璃仪器只有漏斗、烧杯
D.由溶液A制备NaSO 溶液过程中,氧化剂与还原剂物质的量之比为1∶2
2 2 4
答案 B
解析 甲酸和甲醛都含有醛基,A错误;NaSO 溶液加入NaCl晶体冷却,过滤可以得到
2 2 4
NaSO·2H O,B正确;过滤操作中需要用的玻璃仪器有漏斗、烧杯、玻璃棒,C错误。
2 2 4 2
11.利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的S2-,制取石膏(CaSO·2H O)的
4 2
过程如下:
下列说法错误的是( )
A.CaSO·2H O属于盐类和纯净物
4 2
B.过程Ⅱ中,反应的离子方程式为4MnO+2S2-+9HO===SO+4Mn(OH) ↓+10OH-
2 2 2
C.过程Ⅰ后溶液碱性增强
D.将10 L上清液中的S2-(S2-浓度为480 mg·L-1)转化为SO,理论上共需要0.3 mol O
2
答案 C
解析 根据转化关系图,过程Ⅱ中S2-与MnO生成SO和Mn(OH) ,根据氧化还原反应得
2 2
失电子守恒和元素守恒,反应的离子方程式为4MnO+2S2-+9HO===SO+4Mn(OH) ↓+
2 2 2
10OH-,故 B 正确;分析可知过程Ⅰ中发生反应:2Mn(OH) +O +4OH-===2MnO+
2 2
4HO,溶液的pH减小,溶液碱性减弱,故C错误;10 L上清液中的S2-的物质的量为=
20.15 mol,根据物质转化过程可知,S2-转化为SO过程中需要消耗氧气,SO转化为SO也
2 2
需要消耗氧气,在转化过程中,硫元素的化合价由-2价变成+6价,S2-共失去 0.15
mol×8=1.2 mol电子,1 mol O 在反应中得到4 mol电子,所以将10 L上清液中的S2-转化
2
为SO,理论上共需要O 的物质的量为=0.3 mol,故D正确。
2
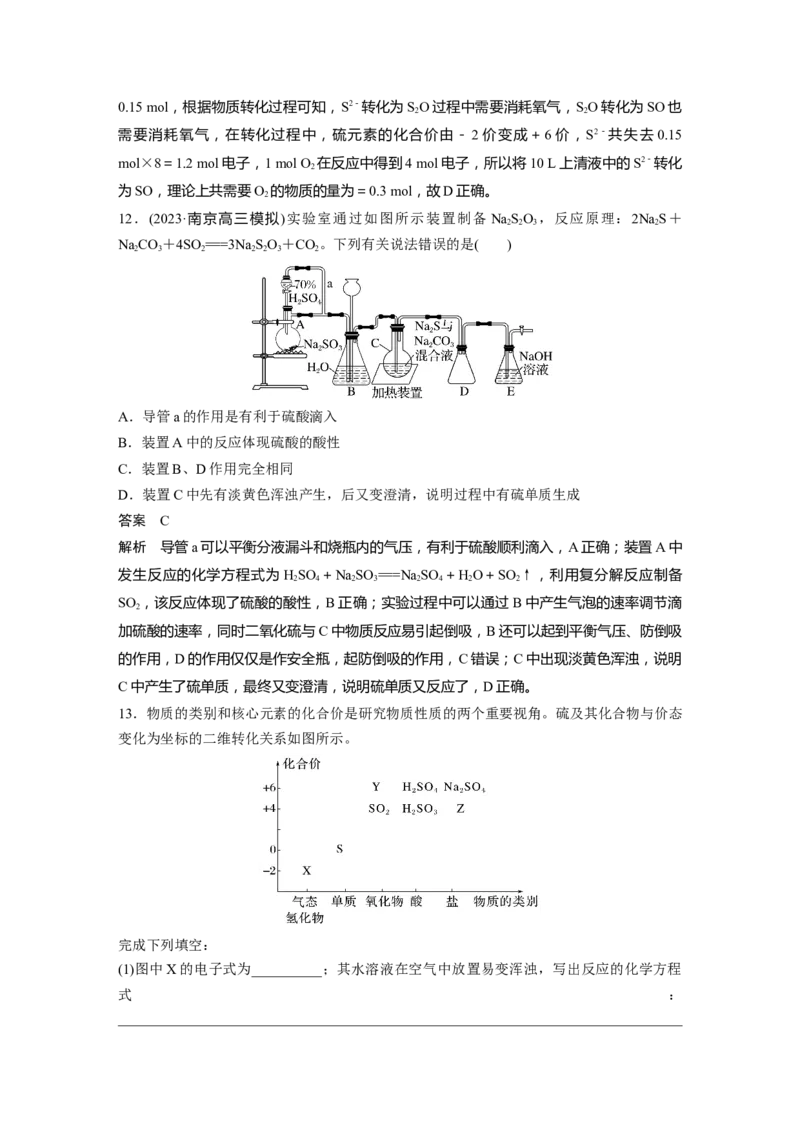
12.(2023·南京高三模拟)实验室通过如图所示装置制备 NaSO ,反应原理:2NaS+
2 2 3 2
NaCO+4SO ===3NaSO+CO。下列有关说法错误的是( )
2 3 2 2 2 3 2
A.导管a的作用是有利于硫酸滴入
B.装置A中的反应体现硫酸的酸性
C.装置B、D作用完全相同
D.装置C中先有淡黄色浑浊产生,后又变澄清,说明过程中有硫单质生成
答案 C
解析 导管a可以平衡分液漏斗和烧瓶内的气压,有利于硫酸顺利滴入,A正确;装置A中
发生反应的化学方程式为HSO +NaSO ===NaSO +HO+SO ↑,利用复分解反应制备
2 4 2 3 2 4 2 2
SO ,该反应体现了硫酸的酸性,B正确;实验过程中可以通过B中产生气泡的速率调节滴
2
加硫酸的速率,同时二氧化硫与C中物质反应易引起倒吸,B还可以起到平衡气压、防倒吸
的作用,D的作用仅仅是作安全瓶,起防倒吸的作用,C错误;C中出现淡黄色浑浊,说明
C中产生了硫单质,最终又变澄清,说明硫单质又反应了,D正确。
13.物质的类别和核心元素的化合价是研究物质性质的两个重要视角。硫及其化合物与价态
变化为坐标的二维转化关系如图所示。
完成下列填空:
(1)图中X的电子式为__________;其水溶液在空气中放置易变浑浊,写出反应的化学方程
式 :
_______________________________________________________________________________________________________________________________________________________________
;
该变化说明S的非金属性比O__________(填“强”或“弱”)。
(2)下列物质用于NaSO 制备,从氧化还原反应的角度,理论上有可能的是________(填字
2 2 3
母)。
a.NaS+S b.Z+S
2
c.NaSO +Y d.NaHS+NaHSO
2 3 3
(3)治理含CO、SO 的烟道气,以Fe O 作催化剂,将CO、SO 在380 ℃时转化为S和一种
2 2 3 2
无毒气体,写出该治理烟道气反应的化学方程式:____________________________________
_______________________________________________________________________________
。
答案 (1) 2HS+O===2S↓+2HO 弱 (2)bd (3)2CO+SO =====S+2CO
2 2 2 2 2
解析 (1)H S水溶液在空气中放置易变浑浊是因为HS被氧气氧化为S,反应的化学方程式
2 2
为2HS+O===2S↓+2HO,所以S的非金属性比O弱。(2)Na SO 中S为+2价,从氧化
2 2 2 2 2 3
还原的角度分析,反应物中S的化合价必须分别大于2和小于2,b、d符合题意。
14.(2023·辽宁鞍山模拟)硫代硫酸钠(Na SO)可用作分析试剂及还原剂,受热、遇酸均易分
2 2 3
解。某学习小组用如图装置利用绿矾受热分解生成的SO 气体制备硫代硫酸钠。
2
已知:①绿矾受热分解反应为2FeSO ·7H O=====Fe O+SO ↑+SO ↑+14HO↑;
4 2 2 3 3 2 2
②SO 的沸点为44.8 ℃。
3
回答下列问题:
(1)完成实验操作过程:连接装置,______________,加入药品(Na S和NaCO 混合溶液用
2 2 3
煮沸过的蒸馏水配制),使所有活塞处于关闭状态。开始制备,打开某些活塞,通入一段时
间N ;关闭活塞__________,打开活塞__________,加热绿矾;使用pH传感器始终观测C
2
处溶液的pH,pH为7~8之间时停止加热,同时关闭活塞K ;……将锥形瓶用热水浴浓缩
3
至水层表面出现结晶为止,经过__________、过滤、洗涤、干燥得到NaSO 晶体。
2 2 3
(2) 写 出 锥 形 瓶 中 发 生 反 应 的 离 子 方 程 式 :
____________________________________________
_______________________________________________________________________________
。
(3)装置B的作用为______________________________________________________________。
(4)将锥形瓶中的反应停止在pH传感器的读数为7~8时的原因是_______________________。(5)该装置存在一个明显的缺点,请提出改进方法:
_______________________________________________________________________________
。
答案 (1)检查装置气密性 K、K K 冷却结晶
1 2 3
(2)2CO+4SO +2S2-+HO===3SO+2HCO
2 2 2
(3)除去SO ,使SO 与SO 分离
3 3 2
(4)pH小于7时,会造成生成的硫代硫酸根离子在酸性条件下分解;pH大于8时,原料反应
不充分,二者都会影响硫代硫酸钠的产率和纯度
(5)m处接一个尾气处理装置
解析 (1)由题给信息可知,制备硫代硫酸钠的实验操作过程:连接装置,检查装置的气密
性,向锥形瓶中加入用煮沸过的蒸馏水配制的硫化钠和碳酸钠的混合溶液,为防止装置内空
气中的氧气氧化硫化钠,加热前打开活塞K 、K ,关闭活塞K ,通入一段时间氮气,排尽
1 2 3
装置中的空气后,关闭活塞K 、K ,打开活塞K ,加热绿矾,为防止酸性条件下硫代硫酸
1 2 3
钠分解,实验时使用pH传感器始终观测C处溶液的pH,在溶液pH在7~8之间时停止加
热,同时关闭活塞K ,制得硫代硫酸钠溶液;将锥形瓶用热水浴浓缩至水层表面出现结晶
3
为止,经过冷却结晶、过滤、洗涤、干燥得到硫代硫酸钠晶体。