文档内容
第 13 讲 铁盐、亚铁盐 铁及其化合物的转化
[复习目标] 1.掌握Fe2+和Fe3+的性质和检验方法。2.能从物质类别和元素价态变化的角度
理解铁及其化合物的转化路径。
考点一 Fe2+、Fe3+的性质与检验
1.铁盐
(1)常见的铁盐有Fe (SO )、FeCl 等。
2 4 3 3
(2)含Fe3+的溶液,呈黄色,Fe3+具有较强的氧化性。Fe3+与Cu、HS反应的离子方程式分
2
别为 2Fe 3 + + Cu == = 2Fe 2 + + Cu 2 + 、 2Fe 3 + + H S == = 2Fe 2 + + S ↓ + 2H + 。
2
(3)Fe3+易水解,只能存在于酸性较强的溶液中。
①用FeCl 固体配制FeCl 溶液的方法:将氯化铁固体先溶于较浓的盐酸中,然后再稀释至
3 3
所需浓度。
②工业上常用调节pH的方法除去溶液中的Fe3+。
③FeCl 溶液加热蒸干并灼烧,所得固体主要成分为Fe O。
3 2 3
④Fe3+与HCO、AlO混合时都会得到Fe(OH) 沉淀。
3
2.亚铁盐
(1)FeSO ·7H O呈绿色,俗称绿矾。
4 2
(2)含有Fe2+的溶液,呈浅绿色,Fe2+既有氧化性,又有还原性。
①氧化性:Fe2+与Zn反应的离子方程式为 Fe 2 + + Zn == = Zn 2 + + Fe 。
②还原性:Fe2+与Cl 反应的离子方程式为 2Fe 2 + + Cl == = 2Fe 3 + + 2Cl - 。
2 2
(3)Fe2+在酸性介质中比较稳定,因而保存亚铁盐溶液时,应加入一定量的酸,同时放入少
量 铁屑 ( 钉 )来防止氧化。
3.高铁酸钾(K FeO)
2 4
暗紫色晶体,其中Fe为 + 6 价,具有强氧化性,可用作水体的杀菌、消毒剂或高容量电池
材料。
4.Fe2+和Fe3+的检验
(1)(2)
(3)含Fe2+、Fe3+的混合溶液中Fe2+、Fe3+的检验
―――――→溶液变红色,说明含有 Fe 3 + 。
――――→酸性KMnO 溶液紫红色褪去,说明含有 Fe 2 + 。
4
1.硫酸亚铁片和维生素C同时服用能增强治疗缺铁性贫血的效果( )
2.中性溶液中可能大量存在Fe3+、Cl-、K+、SO( )
3.Fe (SO ) 和KI溶液反应的离子方程式:2Fe3++2I-===2Fe2++I( )
2 4 3 2
4.将Fe(NO ) 样品溶于稀HSO 后,滴加KSCN溶液,溶液变红,则Fe(NO ) 晶体已氧化
3 2 2 4 3 2
变质( )
5.向FeCl 溶液中滴加酸性KMnO 溶液,若酸性KMnO 溶液褪色,证明含有Fe2+( )
2 4 4
答案 1.√ 2.× 3.√ 4.× 5.×
一、铁盐、亚铁盐的性质
1.铁及其化合物是中学化学中一类重要的物质。下列关于铁元素的叙述正确的是( )
A.采用将FeCl 溶液直接蒸干的方法制备FeCl 固体
3 3
B.保存FeCl 溶液常常加一些铁粉,其目的是抑制Fe2+水解
2
C.25 ℃时,pH=0的溶液中,Al3+、NH、NO、Fe2+可以大量共存
D.FeSO 溶液中加入HO 溶液时,Fe2+表现还原性
4 2 2
答案 D
解析 加热促进Fe3+的水解,且生成HCl易挥发,采用将FeCl 溶液直接蒸干的方法不能制
3
备FeCl 固体,故A错误;亚铁离子易被氧化为铁离子,保存 FeCl 溶液常常加一些铁粉,
3 2
其目的是防止Fe2+被氧化,故B错误;pH=0的溶液显酸性,H+、NO、Fe2+发生氧化还原
反应不能共存,故C错误;亚铁离子可被过氧化氢氧化,发生反应:2Fe2++HO +2H+
2 2
===2Fe3++2HO,Fe2+表现还原性,故D正确。
2
2.(2023·厦门模拟)用黄色的FeCl 溶液分别进行下列实验,解释或结论不正确的是( )
3
选项 实验 现象 解释或结论
A 加入FeCl 固体 溶液变成红褐色 FeCl 的水解程度变大
3 3
B 加入等体积水 溶液颜色变浅 c(Fe3+)变小
C 加入足量Fe粉 溶液颜色变浅绿色 2Fe3++Fe===3Fe2+
D 将FeCl 溶液微热 溶液变成红褐色 水解反应ΔH>0
3答案 A
解析 FeCl 溶液中存在Fe3+的水解平衡,水解的离子方程式为Fe3++3HOFe(OH) +3H
3 2 3
+。A项,加入FeCl 固体,平衡右移,c(Fe3+)增大,但水解程度减小,错误;B项,加入等
3
体积的水,平衡右移,c(Fe3+)减小,溶液颜色变浅,正确;C项,加入Fe粉,发生反应:
2Fe3++Fe===3Fe2+,Fe2+呈浅绿色,正确;D项,加热,促进水解,说明水解是吸热反应,
正确。
二、应用Fe3+、Fe2+的性质除杂
3.除去括号中的杂质,并写出反应的离子方程式。
(1)FeCl (FeCl ) , 除 杂 方 法 : ______________ , 离 子 方 程 式 :
2 3
_____________________________。
(2)FeCl (FeCl ) , 除 杂 方 法 : ______________ , 离 子 方 程 式 :
3 2
______________________________。
(3)Fe (SO )(FeSO ) , 除 杂 方 法 : __________ , 离 子 方 程 式 :
2 4 3 4
____________________________。
(4)FeCl (Cu2 + ) , 除 杂 方 法 : ______________ , 离 子 方 程 式 :
2
_____________________________。
(5)CuCl 溶液(FeCl ),除杂方法:__________________________________________________。
2 2
答案 (1)加入过量铁粉 2Fe3++Fe===3Fe2+
(2)加入氯水(或通入Cl) 2Fe2++Cl===2Fe3++2Cl-
2 2
(3)滴加HO 2Fe2++HO+2H+===2HO+2Fe3+
2 2 2 2 2
(4)加入过量铁粉,过滤 Fe+Cu2+===Cu+Fe2+
(5)先向溶液中加入氧化剂(如HO 、氯水),然后向混合液中加入CuO或Cu(OH) ,调pH,
2 2 2
促进Fe3+水解生成Fe(OH) 沉淀,静置过滤
3
三、Fe2+和Fe3+的检验实验方案设计
4.下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中通入Cl,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
2
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中
只含有Fe2+,不含有Mg2+
答案 C
解析 A项中只能说明含有Fe3+,不能说明不含Fe2+;B项原溶液中也可能只有Fe3+而没有
Fe2+;D项中氧化后生成的红褐色沉淀Fe(OH) 也可能掩盖了生成的白色沉淀Mg(OH) 。
3 2
5.设计简单实验,证明Fe O 中含有+2、+3两种价态的铁元素(提供的试剂有Fe O 粉末、
3 4 3 4浓、稀硫酸、硝酸、盐酸、KSCN溶液、酸性KMnO 溶液)。
4
答案 取固体粉末溶于适量稀硫酸,将溶液分成两份,一份滴加 KSCN溶液,溶液变红,
证明含有Fe3+,另一份滴加酸性KMnO 溶液,KMnO 溶液紫红色褪去,证明含Fe2+。
4 4
Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,有干
4 4
扰)。
考点二 铁及其重要化合物的转化关系
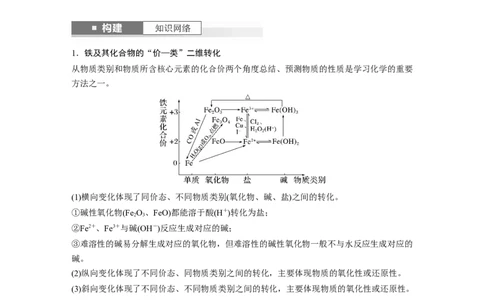
1.铁及其化合物的“价—类”二维转化
从物质类别和物质所含核心元素的化合价两个角度总结、预测物质的性质是学习化学的重要
方法之一。
(1)横向变化体现了同价态、不同物质类别(氧化物、碱、盐)之间的转化。
①碱性氧化物(Fe O、FeO)都能溶于酸(H+)转化为盐;
2 3
②Fe2+、Fe3+与碱(OH-)反应生成对应的碱;
③难溶性的碱易分解生成对应的氧化物,但难溶性的碱性氧化物一般不与水反应生成对应的
碱。
(2)纵向变化体现了不同价态、同物质类别之间的转化,主要体现物质的氧化性或还原性。
(3)斜向变化体现了不同价态、不同物质类别之间的转化,主要体现物质的氧化性或还原性。
2.用离子方程式实现Fe3+与Fe2+的相互转化
Fe2+Fe3+
①2Fe2++Cl===2Fe3++2Cl-;
2
②3Fe2++4H++NO===3Fe3++2HO+NO↑;
2
③2Fe2++HO+2H+===2Fe3++2HO;
2 2 2
④5Fe2++MnO+8H+===5Fe3++Mn2++4HO;
2
⑤2Fe3++Fe===3Fe2+;
⑥Cu+2Fe3+===Cu2++2Fe2+;⑦2Fe3++HS===2Fe2++S↓+2H+。
2
一、过量铁对氧化产物的影响
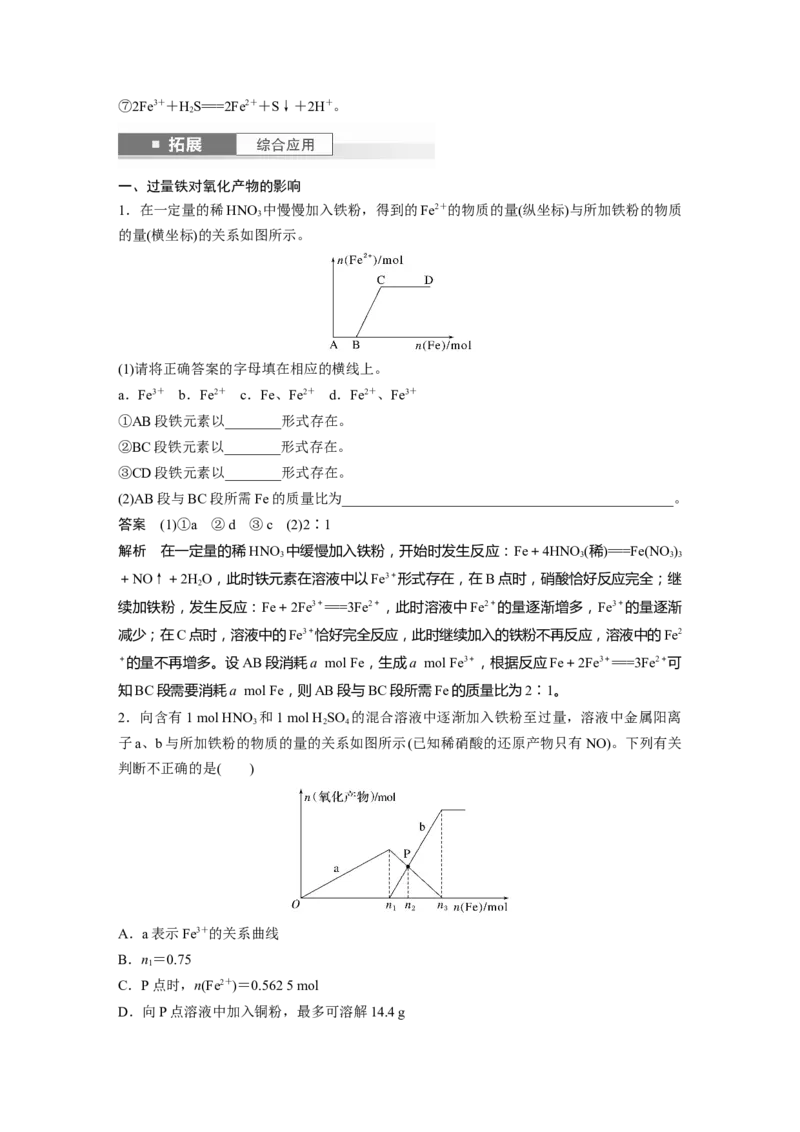
1.在一定量的稀HNO 中慢慢加入铁粉,得到的Fe2+的物质的量(纵坐标)与所加铁粉的物质
3
的量(横坐标)的关系如图所示。
(1)请将正确答案的字母填在相应的横线上。
a.Fe3+ b.Fe2+ c.Fe、Fe2+ d.Fe2+、Fe3+
①AB段铁元素以________形式存在。
②BC段铁元素以________形式存在。
③CD段铁元素以________形式存在。
(2)AB段与BC段所需Fe的质量比为_______________________________________________。
答案 (1)①a ②d ③c (2)2∶1
解析 在一定量的稀HNO 中缓慢加入铁粉,开始时发生反应:Fe+4HNO(稀)===Fe(NO )
3 3 3 3
+NO↑+2HO,此时铁元素在溶液中以Fe3+形式存在,在B点时,硝酸恰好反应完全;继
2
续加铁粉,发生反应:Fe+2Fe3+===3Fe2+,此时溶液中Fe2+的量逐渐增多,Fe3+的量逐渐
减少;在C点时,溶液中的Fe3+恰好完全反应,此时继续加入的铁粉不再反应,溶液中的Fe2
+的量不再增多。设AB段消耗a mol Fe,生成a mol Fe3+,根据反应Fe+2Fe3+===3Fe2+可
知BC段需要消耗a mol Fe,则AB段与BC段所需Fe的质量比为2∶1。
2.向含有1 mol HNO 和1 mol H SO 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离
3 2 4
子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关
判断不正确的是( )
A.a表示Fe3+的关系曲线
B.n=0.75
1
C.P点时,n(Fe2+)=0.562 5 mol
D.向P点溶液中加入铜粉,最多可溶解14.4 g答案 C
解析 该反应可以看作两步:①Fe+4H++NO===Fe3++NO↑+2HO,硝酸根离子过量,
2
氢离子不足;②2Fe3++Fe===3Fe2+。a表示Fe3+的关系曲线,A正确;溶液中共有3 mol H
+参加反应,消耗0.75 mol铁,B正确;P点n(Fe2+)=n(Fe3+),两者均为0.45 mol,C不正
确;P点剩余0.45 mol Fe3+,消耗0.225 mol铜,质量为14.4 g,D正确。
二、铁盐、亚铁盐的制备
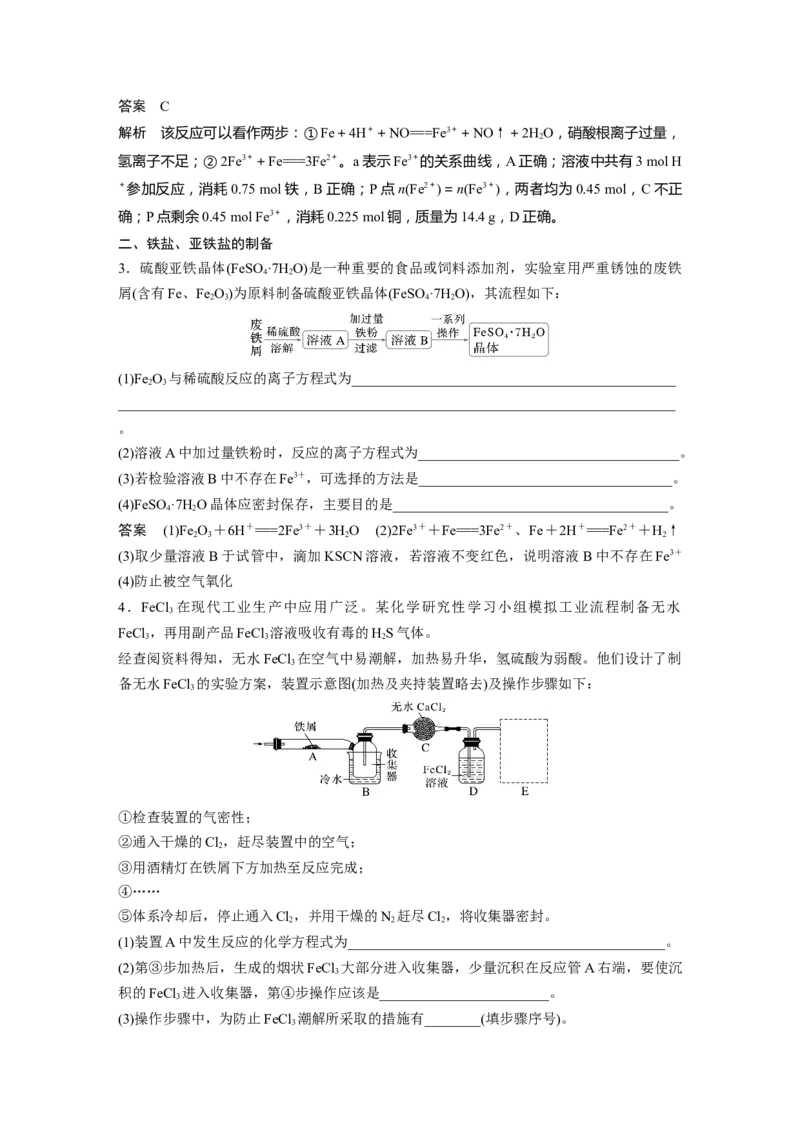
3.硫酸亚铁晶体(FeSO ·7H O)是一种重要的食品或饲料添加剂,实验室用严重锈蚀的废铁
4 2
屑(含有Fe、Fe O)为原料制备硫酸亚铁晶体(FeSO ·7H O),其流程如下:
2 3 4 2
(1)Fe O 与稀硫酸反应的离子方程式为______________________________________________
2 3
_______________________________________________________________________________
。
(2)溶液A中加过量铁粉时,反应的离子方程式为_____________________________________。
(3)若检验溶液B中不存在Fe3+,可选择的方法是____________________________________。
(4)FeSO ·7H O晶体应密封保存,主要目的是_______________________________________。
4 2
答案 (1)Fe O +6H+===2Fe3++3HO (2)2Fe3++Fe===3Fe2+、Fe+2H+===Fe2++H↑
2 3 2 2
(3)取少量溶液B于试管中,滴加KSCN溶液,若溶液不变红色,说明溶液B中不存在Fe3+
(4)防止被空气氧化
4.FeCl 在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水
3
FeCl ,再用副产品FeCl 溶液吸收有毒的HS气体。
3 3 2
经查阅资料得知,无水FeCl 在空气中易潮解,加热易升华,氢硫酸为弱酸。他们设计了制
3
备无水FeCl 的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
3
①检查装置的气密性;
②通入干燥的Cl,赶尽装置中的空气;
2
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl,并用干燥的N 赶尽Cl,将收集器密封。
2 2 2
(1)装置A中发生反应的化学方程式为_____________________________________________。
(2)第③步加热后,生成的烟状FeCl 大部分进入收集器,少量沉积在反应管A右端,要使沉
3
积的FeCl 进入收集器,第④步操作应该是________________________。
3
(3)操作步骤中,为防止FeCl 潮解所采取的措施有________(填步骤序号)。
3(4)装置B中冷水浴的作用为________;装置D中FeCl 全部反应后,因失去吸收Cl 的作用
2 2
而失效,检验此时溶液中存在的金属阳离子,写出离子方程式:________________。
(5)在虚线框中画出尾气吸收装置E并注明试剂。
(6)FeCl 溶液与HS气体反应的离子方程式为_______________________________________。
3 2
答案 (1)2Fe+3Cl=====2FeCl
2 3
(2)在沉积的FeCl 固体下方加热 (3)②⑤
3
(4)冷凝、收集氯化铁 Fe3++3SCN-Fe(SCN)
3
(5)
(6)2Fe3++HS===2Fe2++S↓+2H+
2
三、陌生含铁物质的制备
5.以高硫铝土矿(主要成分为Fe O、Al O、SiO,少量FeS 和硫酸盐)为原料制备聚合硫酸
2 3 2 3 2 2
铁{[Fe (OH)(SO )]}和明矾的部分工艺流程如下,下列说法错误的是( )
2 x 4 y n
已知:赤泥液的主要成分为NaCO。
2 3
A.赤泥液的作用是吸收“焙烧”阶段中产生的SO
2
B.聚合硫酸铁可用于净化自来水,与其组成中的Fe3+具有氧化性有关
C.在“聚合”阶段,若增加Fe O 的用量,会使[Fe (OH)(SO )] 中x变大
2 3 2 x 4 y n
D.从“滤液”到“明矾”的过程中还应有“除硅”步骤
答案 B
解析 高硫铝土矿(主要成分为Fe O 、Al O 、SiO ,少量FeS 和硫酸盐)焙烧时,FeS 与O
2 3 2 3 2 2 2 2
反应生成Fe O 和SO ,并用赤泥液吸收生成的SO ;焙烧后,Al O 、Fe O 、SiO 、硫酸盐
2 3 2 2 2 3 2 3 2
进入“碱浸”步骤,Al O 、SiO 溶于KOH溶液,硫酸盐溶于水,过滤,滤液经一系列处理
2 3 2
获得明矾,滤渣主要是Fe O ,酸浸后加入双氧水氧化可能存在的亚铁离子,此时溶液中主
2 3
要有Fe (SO ),加入氧化铁进行聚合,经浓缩、干燥,获得聚合硫酸铁,据此解答。聚合硫
2 4 3
酸铁可用于净化自来水,与其组成中的 Fe3+可水解产生胶体的性质有关,与 Fe3+具有氧化
性无关,故B错误;在“聚合”阶段,若增加Fe O 的用量,碱性增强,x变大,故C正确;
2 3
由上述分析可知,从“滤液”到“明矾”的过程中,由于碱浸造成二氧化硅溶于氢氧化钾,
滤液中含硅酸盐,需要进行“除硅”步骤,故D正确。
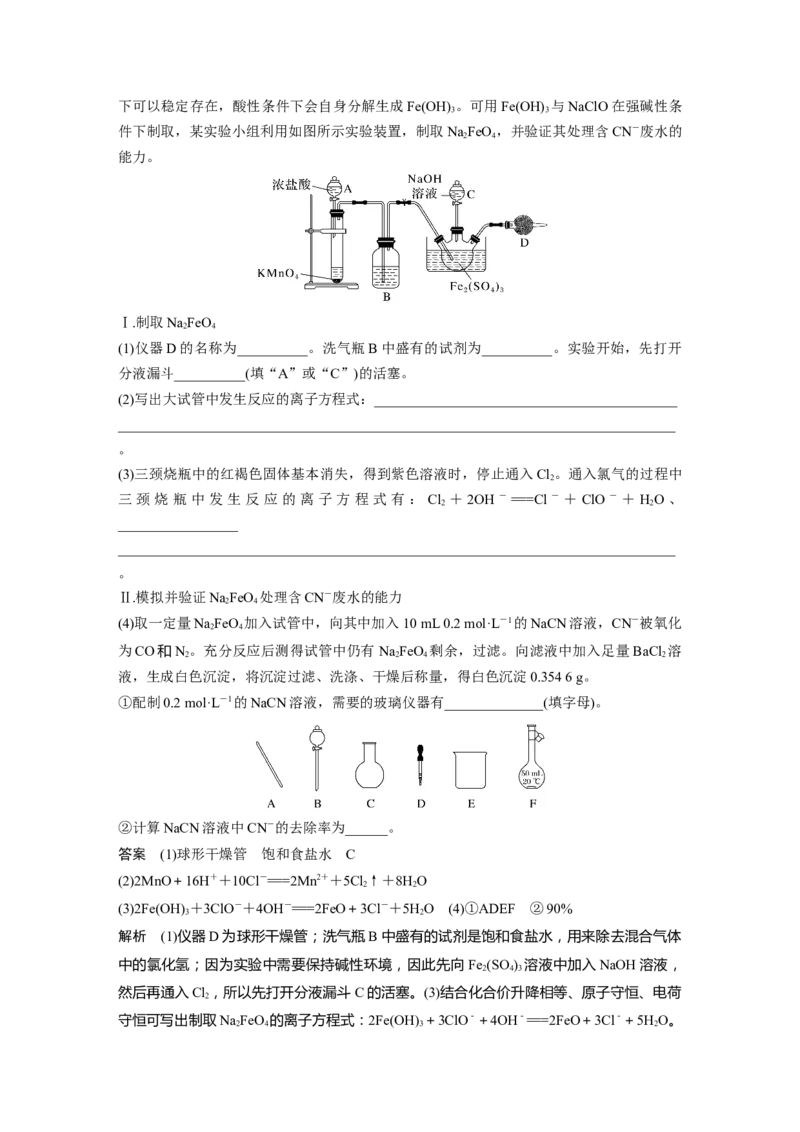
6.(2023·天津模拟)NaFeO 具有强氧化性,是一种新型的绿色非氯净水消毒剂,碱性条件
2 4下可以稳定存在,酸性条件下会自身分解生成Fe(OH) 。可用Fe(OH) 与NaClO在强碱性条
3 3
件下制取,某实验小组利用如图所示实验装置,制取NaFeO ,并验证其处理含CN-废水的
2 4
能力。
Ⅰ.制取NaFeO
2 4
(1)仪器D的名称为__________。洗气瓶B中盛有的试剂为__________。实验开始,先打开
分液漏斗__________(填“A”或“C”)的活塞。
(2)写出大试管中发生反应的离子方程式:___________________________________________
_______________________________________________________________________________
。
(3)三颈烧瓶中的红褐色固体基本消失,得到紫色溶液时,停止通入Cl 。通入氯气的过程中
2
三 颈 烧 瓶 中 发 生 反 应 的 离 子 方 程 式 有 : Cl + 2OH -===Cl -+ ClO -+ HO 、
2 2
_________________
_______________________________________________________________________________
。
Ⅱ.模拟并验证NaFeO 处理含CN-废水的能力
2 4
(4)取一定量NaFeO 加入试管中,向其中加入10 mL 0.2 mol·L-1的NaCN溶液,CN-被氧化
2 4
为CO和N 。充分反应后测得试管中仍有NaFeO 剩余,过滤。向滤液中加入足量BaCl 溶
2 2 4 2
液,生成白色沉淀,将沉淀过滤、洗涤、干燥后称量,得白色沉淀0.354 6 g。
①配制0.2 mol·L-1的NaCN溶液,需要的玻璃仪器有______________(填字母)。
②计算NaCN溶液中CN-的去除率为______。
答案 (1)球形干燥管 饱和食盐水 C
(2)2MnO+16H++10Cl-===2Mn2++5Cl↑+8HO
2 2
(3)2Fe(OH) +3ClO-+4OH-===2FeO+3Cl-+5HO (4)①ADEF ②90%
3 2
解析 (1)仪器D为球形干燥管;洗气瓶B中盛有的试剂是饱和食盐水,用来除去混合气体
中的氯化氢;因为实验中需要保持碱性环境,因此先向 Fe (SO ) 溶液中加入NaOH溶液,
2 4 3
然后再通入Cl ,所以先打开分液漏斗C的活塞。(3)结合化合价升降相等、原子守恒、电荷
2
守恒可写出制取NaFeO 的离子方程式:2Fe(OH) +3ClO-+4OH-===2FeO+3Cl-+5HO。
2 4 3 2(4)①溶液配制需要胶头滴管、烧杯、50 mL 容量瓶、玻璃棒。②n(BaCO)==0.001 8
3
mol,所以CN-的去除率为×100%=90%。
1.(2023·浙江6月选考,3)氯化铁是一种重要的盐,下列说法不正确的是( )
A.氯化铁属于弱电解质
B.氯化铁溶液可腐蚀覆铜板
C.氯化铁可由铁与氯气反应制得
D.氯化铁溶液可制备氢氧化铁胶体
答案 A
解析 氯化铁能完全电离出铁离子和氯离子,属于强电解质,A错误;氯化铁溶液与铜反应
生成氯化铜和氯化亚铁,可用来蚀刻覆铜板,B正确;氯气具有强氧化性,氯气与铁单质加
热生成氯化铁,C正确。
2.下列有关判断错误的是________(填字母)。
A.铁与碘反应易生成碘化铁(2022·浙江1月选考,9A)
B.FeCl 溶液中滴加KSCN溶液,将观察到溶液变红色(2022·海南,6C)
2
C.已知金属性:Fe>Cu,可推理出氧化性:Fe3+