文档内容
第 49 讲 化学反应的方向与调控
[复习目标] 1.知道化学反应是有方向的,知道化学反应的方向与反应的焓变和熵变有关。
2.认识化学反应速率和化学平衡的综合调控在生产、生活和科学研究中的重要作用。
考点一 化学反应的方向
1.自发反应
在一定条件下,无需外界帮助就能自发进行的反应称为自发反应。
2.熵和熵变的含义
(1)熵的含义
度量体系混乱程度的物理量,符号为____。熵值越大,体系混乱度越大。同一条件下,不同
物 质 有 不 同 的 熵 值 ; 同 一 种 物 质 在 不 同 状 态 下 熵 值 也 不 同 , 一 般 规 律 是
S(g)____S(l)____S(s)。
(2)熵变的含义
ΔS=S(生成物)-S(反应物)。化学反应的ΔS越大,越有利于反应____________。
3.判断化学反应方向的判据
ΔG=ΔH-TΔS
ΔG<0时,反应____自发进行;
ΔG=0时,反应处于______状态;
ΔG>0时,反应______自发进行。
1.同一物质的固、液、气三种状态的熵值相同( )
2.非自发反应,一定条件下也能使其反应发生( )
3.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向( )
4.需要加热才能够进行的反应,肯定不是自发反应( )
5.ΔH<0,ΔS>0的反应在温度低时不能自发进行( )
6.一定温度下,反应MgCl (l)Mg(l)+Cl(g)的ΔH>0、ΔS>0( )
2 2
7.反应NH (g)+HCl(g)===NH Cl(s)在室温下可自发进行,则该反应的ΔH<0( )
3 4综合判断化学反应的自发性
1.(2022·浙江1月选考,20)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为
AB(s)===An+(aq)+Bn-(aq),其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解
质,下列说法正确的是( )
A.ΔH和ΔS均大于零
B.ΔH和ΔS均小于零
C.ΔH可能大于零或小于零,ΔS大于零
D.ΔH和ΔS均可能大于零或小于零
2.(1)汽车燃油不完全燃烧时产生 CO,有人设想按下列反应除去 CO:2CO(g)===2C(s)+
O(g) 。 已 知 该 反 应 的 ΔH > 0 , 简 述 该 设 想 能 否 实 现 的 依 据 :
2
________________________________
______________________________________________________________________________。
(2)超音速飞机在平流层飞行时,尾气中的 NO会破坏臭氧层。科学家正在研究利用催化技
术将尾气中的NO和CO转变成CO 和N ,化学方程式为2NO+2CO2CO +N 。反应能
2 2 2 2
够自发进行,则反应的ΔH________0(填“>”“<”或“=”),理由是________________
______________________________________________________________________________。
(3)已知CaSO(s)+CO(g)CaO(s)+SO (g)+CO(g) ΔH=+218 kJ·mol-1,该反应能够自
4 2 2
发进行的反应条件是________。
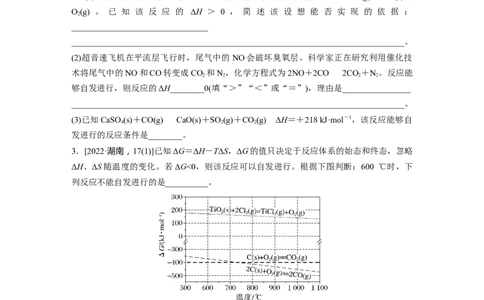
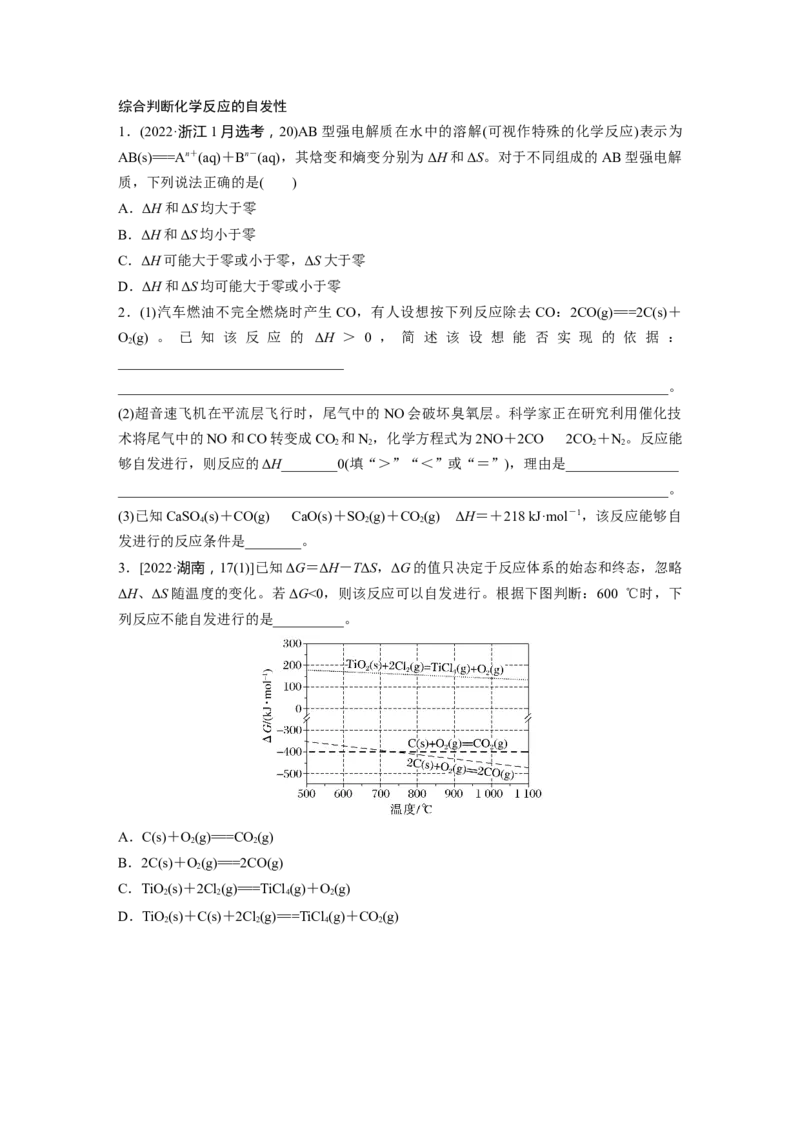
3.[2022·湖南,17(1)]已知ΔG=ΔH-TΔS,ΔG的值只决定于反应体系的始态和终态,忽略
ΔH、ΔS随温度的变化。若ΔG<0,则该反应可以自发进行。根据下图判断:600 ℃时,下
列反应不能自发进行的是__________。
A.C(s)+O(g)===CO(g)
2 2
B.2C(s)+O(g)===2CO(g)
2
C.TiO(s)+2Cl(g)===TiCl (g)+O(g)
2 2 4 2
D.TiO(s)+C(s)+2Cl(g)===TiCl (g)+CO(g)
2 2 4 2考点二 化学反应的调控——工业合成氨
1.化工生产适宜条件选择的一般原则
条件 原则
从化学反应速率分析 既不能过快,又不能太慢
既要注意外界条件对速率和平衡影响的一致性,又要注意
从化学平衡移动分析
对二者影响的矛盾性
增加易得廉价原料,提高难得高价原料的利用率,从而降
从原料的利用率分析
低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意催化剂的活性受温度的限制
2.控制反应条件的基本措施
(1)控制化学反应速率的措施
通过改变反应体系的温度、溶液的浓度、气体的压强(或浓度)、固体的表面积以及使用催化
剂等途径调控反应速率。
(2)提高转化率的措施
通过改变可逆反应体系的温度、溶液的浓度、气体的压强(或浓度)等改变可逆反应的限度,
从而提高转化率。
一、工业合成氨适宜条件选择
1.如图是工业合成氨的工艺,根据流程解答下列问题:
(1)工业合成氨是人类科学技术的一项重大突破,其热化学方程式为 N(g)+
2
3H(g)2NH (g) ΔH=-92.4 kJ·mol-1,结合反应的化学方程式分析哪些措施可以提高合
2 3
成氨的反应速率?哪些措施可以提高氮气或氢气的转化率?
_______________________________________________________________________________
_______________________________________________________________________________(2)工业合成氨中,使用铁触媒作催化剂。
①铁触媒加快化学反应速率的原因是什么?
_______________________________________________________________________________
_______________________________________________________________________________
②铁触媒能提高氢气的平衡转化率吗? 简述理由。
_______________________________________________________________________________
③铁触媒能提高反应混合物中氨的体积分数吗?
_______________________________________________________________________________
(3)合成氨时选择500 ℃而不采用常温主要考虑什么因素?
_______________________________________________________________________________
(4)合成氨时一般采用的压强为10 MPa~30 MPa的原因是什么?
_______________________________________________________________________________
_______________________________________________________________________________
(5)合成氨工业中,为提高反应物的转化率,还采取哪些措施?
_______________________________________________________________________________
外部条件 工业合成氨的适宜条件
压强 根据反应器可使用钢材的质量及综合指标来选择压强
温度 适宜温度,700 K左右
催化剂 使用铁触媒做催化剂(为防止催化剂中毒,原料气要净化处理)
N 和H 的物质的量之比为1∶2.8的投料比,将氨及时地从混合气中分离
2 2
浓度
出来
二、综合分析其他工业生产的适宜条件
2.钾是一种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为Na(l)
+KCl(l)NaCl(l)+K(g) ΔH>0。
该反应的平衡常数可表示为K=c(K),各物质的沸点与压强的关系见下表:
压强/kPa 13.33 53.32 101.3
K的沸点/℃ 590 710 770
Na的沸点/℃ 700 830 890
NaCl的沸点/℃ - - 1 437
KCl的沸点/℃ - - 1 465
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为________,而反应的最
高温度应低于________。
(2)制取钾的过程中,为了提高原料的转化率可以采取的措施是________________________________________________________________________________________________________
。
(3) 常 压 下 , 当 反 应 温 度 升 高 到 900 ℃ 时 , 该 反 应 的 平 衡 常 数 可 表 示 为
_____________________
_______________________________________________________________________________
。
3.(2023·河南新乡模拟)甲烷化反应即为氢气和碳氧化物反应生成甲烷,有利于实现碳循环
利用。已知涉及的反应如下:
反应 Ⅰ:CO(g)+3H(g)CH(g)+HO(g) ΔH=-206.2 kJ·mol-1
2 4 2 1
反应 Ⅱ:CO(g)+HO(g)CO(g)+H(g) ΔH
2 2 2 2
反应 Ⅲ:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-165.0 kJ ·mol-1
2 2 4 2 3
积碳反应(CO的歧化反应和CH 的裂解反应是催化剂积碳的主要成因):2CO(g)CO(g)+
4 2
C(s)(反应 Ⅳ);CH(g)C(s) +2H(g)(反应Ⅴ)。
4 2
回答下列问题:
(1)ΔH=________kJ·mol-1。
2
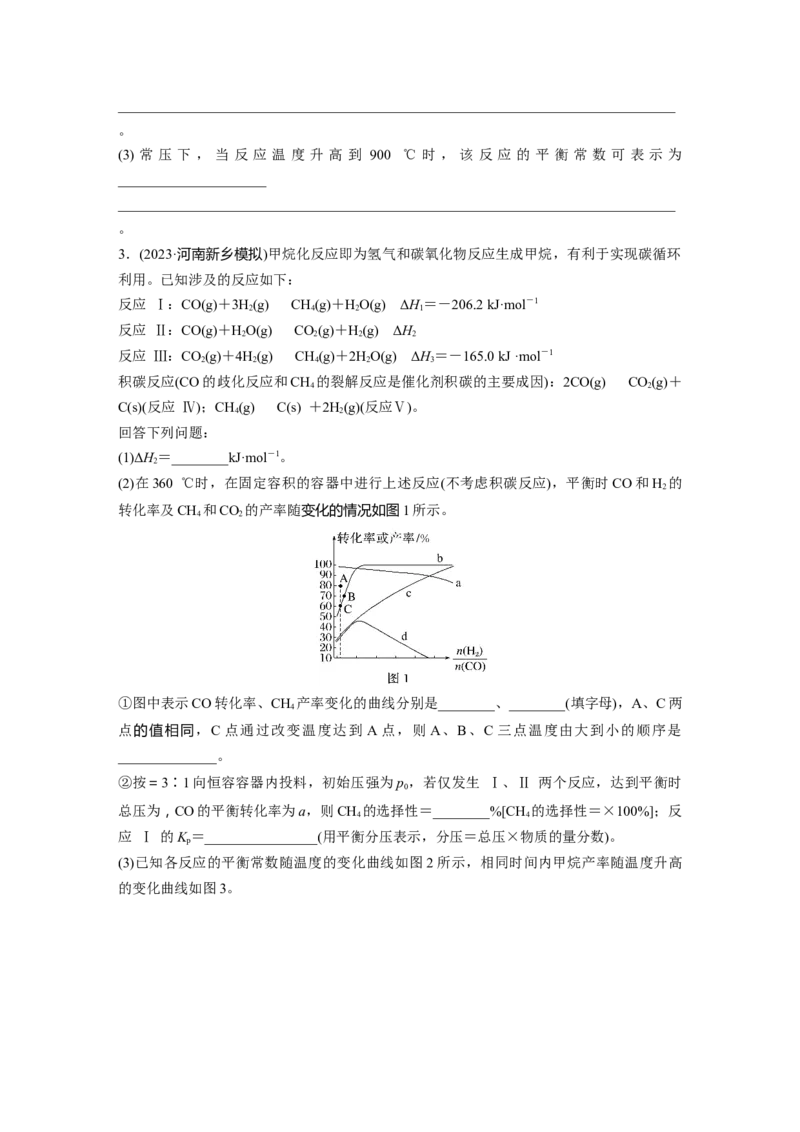
(2)在360 ℃时,在固定容积的容器中进行上述反应(不考虑积碳反应),平衡时CO和H 的
2
转化率及CH 和CO 的产率随变化的情况如图1所示。
4 2
①图中表示CO转化率、CH 产率变化的曲线分别是________、________(填字母),A、C两
4
点的值相同,C 点通过改变温度达到 A 点,则 A、B、C 三点温度由大到小的顺序是
______________。
②按=3∶1向恒容容器内投料,初始压强为p ,若仅发生 Ⅰ、Ⅱ 两个反应,达到平衡时
0
总压为,CO的平衡转化率为a,则CH 的选择性=________%[CH 的选择性=×100%];反
4 4
应 Ⅰ 的K =________________(用平衡分压表示,分压=总压×物质的量分数)。
p
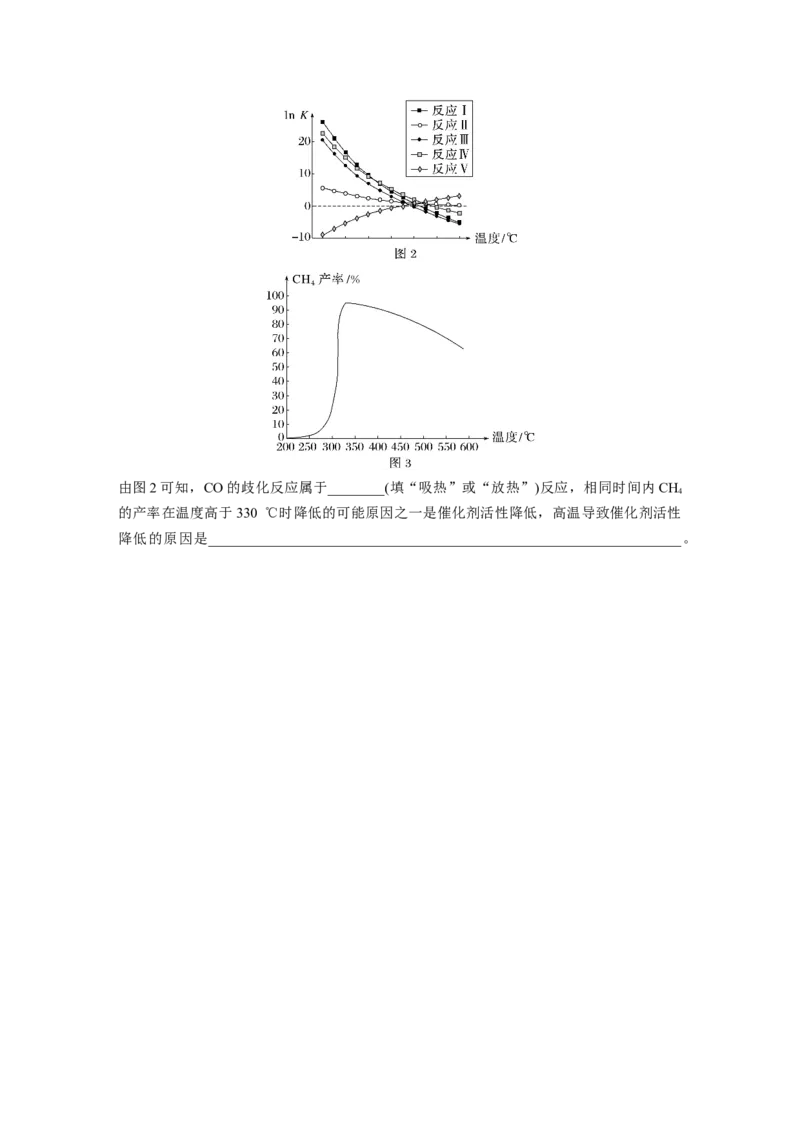
(3)已知各反应的平衡常数随温度的变化曲线如图2所示,相同时间内甲烷产率随温度升高
的变化曲线如图3。由图2可知,CO的歧化反应属于________(填“吸热”或“放热”)反应,相同时间内CH
4
的产率在温度高于330 ℃时降低的可能原因之一是催化剂活性降低,高温导致催化剂活性
降低的原因是___________________________________________________________________。