文档内容
第 48 讲 影响化学平衡的因素
[复习目标] 1.掌握外界条件改变对化学平衡的影响。2.掌握并会运用勒夏特列原理分析平
衡的移动。3.掌握平衡移动与转化率的关系。
考点一 化学平衡的移动
1.化学平衡移动的根本原因
(1)平衡移动的过程
(2)平衡移动与速率的关系
①v正 >v逆 ,化学平衡向正反应方向移动;
②v正 <v逆 ,化学平衡向逆反应方向移动;
③v正 =v逆 ,化学平衡不发生移动。
2.化学平衡移动的重要实验再现
(1)探究浓度对化学平衡的影响
实验一:Fe3++3SCN-Fe(SCN) (红色),加入较浓的FeCl 溶液或KSCN溶液、少量铁
3 3
粉、KCl固体,通过观察溶液红色的变化,分析平衡移动。
提示 ①加入较浓的FeCl 溶液或KSCN溶液,红色加深,平衡正向移动。②加入少量Fe
3
粉,红色变浅,平衡逆向移动。③加入少量KCl固体,红色几乎不变,平衡不移动。
实验二:Cr O(橙色)+HO2CrO (黄色)+2H+,滴加NaOH溶液或硫酸溶液,通过观察
2 2
溶液颜色的变化,分析平衡移动。
提示 ①滴加NaOH溶液,溶液由橙色变为黄色,平衡正向移动。②滴加HSO 溶液,溶液
2 4
橙色加深,平衡逆向移动。
(2)探究压强对化学平衡的影响
实验三:2NO (红棕色)NO(无色)
2 2 4
通过压缩体积观察颜色变化,分析平衡移动。
提示 气体的颜色先变深后变浅,最终还是比最初的颜色深。增大压强,平衡向生成 NO
2 4
的方向(气体体积减小的方向)移动。(3)探究温度对化学平衡的影响
实验四:[Cu(H O) ]2+(蓝色)+4Cl-[CuCl ]2-(黄色)+4HO ΔH>0。
2 4 4 2
将分别盛有2 mL 0.5 mol·L-1 CuCl 溶液的两支试管,一支试管先加热,然后置于冷水中,
2
与另一支试管进行对比。
实验步骤 实验现象 结论
在其他条件不变时,升高温度,平
加热试管 溶液由蓝色变为绿色
衡向正反应 ( 吸热 ) 方向移动
在其他条件不变时,降低温度,平
将上述试管置于冷水中 溶液恢复蓝色
衡向逆反应 ( 放热 ) 方向移动
思考 在对CuCl 溶液加热时,为何未看到溶液变为黄色?
2
答案 因为加热时,平衡正向移动,[Cu(H O) ]2+有部分转化为[CuCl ]2-,[Cu(H O) ]2+显蓝
2 4 4 2 4
色,[CuCl ]2-显黄色,而二者的混合色为绿色,故看不到黄色。
4
3.化学平衡移动原理——勒夏特列原理
如果改变影响平衡的一个因素(如浓度、压强或温度),平衡就向着能够减弱这种改变的方向
移动,这就是勒夏特列原理,也称化学平衡移动原理。
一、外因对正逆反应速率与化学平衡移动的影响
1.外界条件对化学平衡的影响是通过改变正、逆反应速率来实现的,其移动方向取决于改
变条件的瞬间v正 和v逆 的相对大小。试完成下表(说明:表中的压强的变化是指通过改变气
体的体积实现的)。
改变条件的瞬间反应速率的变化
条件的改变(假设其他条件不变) 化学平衡的移动
v正 v逆
①增大反应物浓度
②减小反应物浓度
(1)浓度
③增大生成物浓度
④减小生成物浓度
①增大压强
(2)压强
②减小压强
①升高温度
(3)温度
②降低温度
(4)催化剂 使用催化剂
答案 (1)①增大 不变 正向移动 ②减小 不变 逆向移动 ③不变 增大 逆向移动
④不变 减小 正向移动 (2)①增大 增大 向气体体积减小的方向移动 ②减小 减小
向气体体积增大的方向移动 (3)①增大 增大 向吸热反应方向移动 ②减小 减小 向放热反应方向移动 (4)增大 增大 不移动
2.将NO 装入带活塞的密闭容器中,当反应2NO (g)NO(g)达到平衡后,改变下列一个
2 2 2 4
条件,其中叙述正确的是( )
A.升高温度,气体颜色加深,则此反应为吸热反应
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D.恒温恒压时,充入惰性气体,平衡向左移动,混合气体的颜色变深
答案 C
解析 升高温度,气体颜色加深,则平衡向左移动,该反应为放热反应,A错误;体积减小
一半,根据勒夏特列原理,混合气体的颜色比原平衡深,压强小于原平衡的两倍,B错误,
C正确;恒温恒压,充入惰性气体,容器体积扩大,平衡向气体分子数增大的方向(即生成
NO 的方向)移动,但NO 气体的浓度最终变小,混合气体的颜色变浅,D错误。
2 2
惰性气体对化学平衡的影响
二、通过图像理解化学平衡移动
3.一定条件下,在密闭容器中发生如下反应:2SO (g)+O(g)2SO (g) ΔH=-198 kJ·mol
2 2 3
-1。
(1)若在t
0
时刻只增大压强(缩小容器的体积),请在图1中作出v正 、v逆 的变化图像。
答案
(2)请在图2中作出不同温度下(T>T)SO 的转化率随时间变化的示意图。
2 1 2答案
4.(2021·湖南,11改编)已知:A(g)+2B(g)3C(g) ΔH<0,向一恒温恒容的密闭容器中
充入________发生反应,t 时达到平衡状态Ⅰ,在t 时改变某一条件,t 时重新达到平衡状
1 2 3
态Ⅱ,正反应速率随时间的变化如图所示。t 时改变的条件:____________。
2
答案 一定量的A和B 向容器中加入C
解析 反应从正反应开始,所以为充入一定量的A和B。t 时v 瞬间不变,后不断增大,
2 正
v 是突变后不断减小,故改变的条件是加入C。
逆
考点二 平衡移动与平衡转化率的关系
一、新旧平衡转化率的比较
1.对于以下反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答下列
问题。
(1)PCl (g)PCl (g)+Cl(g)
5 3 2
再充入 PCl (g),平衡向________方向移动,达到平衡后,PCl (g)的转化率________,
5 5
PCl (g)的百分含量______。
5
(2)2HI(g)I(g)+H(g)
2 2
再充入HI(g),平衡向________方向移动,达到平衡后,HI(g)的分解率__________,HI(g)的
百分含量________。
(3)2NO (g)NO(g)
2 2 4
再充入NO (g),平衡向________方向移动,达到平衡后,NO (g)的转化率________,NO (g)
2 2 2
的百分含量________。(4)mA(g)+nB(g)pC(g)
同等倍数的加入A(g)和B(g),平衡________移动,达到平衡后,①m+n>p,A、B的转化
率都________,体积分数都________;②m+n=p,A、B的转化率、体积分数都________;
③m+n丁
3答案 D
解析 甲和乙若都是恒温恒压,则两者等效,但乙为绝热恒压,该反应正反应为放热反应,
则温度:甲<乙,温度升高平衡向逆反应方向移动,c(SO ):甲<乙,平衡常数K:甲>乙,
2
A、B项错误;丙和丁若都是恒温恒容,则两者等效,但丁为绝热恒容,则温度:丙<丁,
温度越高,反应速率越快,达到平衡的时间越短,所用的时间:丙>丁,C项错误;温度升
高平衡向逆反应方向移动,体积分数φ(SO ):丙>丁,D项正确。
3
(1)构建恒温恒容平衡思维模式
新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。
(2)构建恒温恒压平衡思维模式(以气体物质的量增加的反应为例,见图示)
新平衡状态可认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。
二、外因对多重平衡的影响
4.[2022·河北,16(2)①]工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.CH (g)+HO(g)CO(g)+3H(g)
4 2 2
Ⅱ.CO(g)+HO(g)CO(g)+H(g)
2 2 2
下列操作中,能提高CH(g)平衡转化率的是__________(填字母)。
4
A.增加CH(g)用量
4
B.恒温恒压下通入惰性气体
C.移除CO(g)
D.加入催化剂
答案 BC
解析 增加CH(g)用量可以提高HO(g)的转化率,但是CH(g)平衡转化率减小,A不符合
4 2 4
题意;恒温恒压下通入惰性气体,相当于减小体系压强,反应混合物中各组分的浓度减小,
反应Ⅰ的化学平衡正向移动,能提高CH(g)平衡转化率,B符合题意;移除CO(g),减小了
4
反应混合物中CO(g)的浓度,反应Ⅰ的化学平衡正向移动,能提高CH(g)平衡转化率,C符
4
合题意;加入催化剂不能改变平衡状态,故不能提高CH(g)平衡转化率,D不符合题意。
4
5.[2022·湖南,16(1)①]在一定温度下,向体积固定的密闭容器中加入足量的 C(s)和1 mol
HO(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
2
Ⅰ.C(s)+HO(g)CO(g)+H(g) ΔH=+131.4 kJ·mol-1
2 2 1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41.1 kJ·mol-1
2 2 2 2下列说法正确的是__________。
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时H 的体积分数可能大于
2
D.将炭块粉碎,可加快反应速率
答案 BD
解析 在恒温恒容条件下,平衡时向容器中充入惰性气体不能改变各组分的浓度,因此反应
Ⅰ的平衡不移动,A说法不正确;在反应中固体C转化为气体,气体的质量增加,而容器的
体积不变,因此气体的密度在反应过程中不断增大,当混合气体的密度保持不变时,说明反
应体系已达到平衡,B说法正确;若C(s)和HO(g)完全反应全部转化为CO(g)和H(g),由
2 2 2
C(s)+2HO(g)CO(g)+2H(g)可知,H 的体积分数的极值为,由于可逆反应有一定的限
2 2 2 2
度,因此,平衡时H 的体积分数不可能大于,C说法不正确;将炭块粉碎可以增大其与
2
HO(g)的接触面积,因此可加快反应速率,D说法正确。
2
1.(2023·北京,4)下列事实能用平衡移动原理解释的是( )
A.HO 溶液中加入少量MnO 固体,促进HO 分解
2 2 2 2 2
B.密闭烧瓶内的NO 和NO 的混合气体,受热后颜色加深
2 2 4
C.铁钢放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D.锌片与稀HSO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 2
答案 B
解析 MnO 会催化 HO 分解,与平衡移动无关,A项不符合题意;NO 转化为NO 是放
2 2 2 2 2 4
热的可逆反应,升温平衡逆向移动,NO 浓度增大,混合气体颜色加深,B项符合题意;常
2
温下铁在浓硝酸中钝化,加热会使表面的氧化膜溶解,铁与浓硝酸反应生成大量红棕色气体,
与平衡移动无关,C项不符合题意;加入少量硫酸铜后,锌置换出铜,构成原电池,从而使
反应速率加快,与平衡移动无关,D项不符合题意。
2.(2022·海南,8)某温度下,反应CH==CH(g)+HO(g)CHCHOH(g)在密闭容器中达
2 2 2 3 2
到平衡,下列说法正确的是( )
A.增大压强,v正 >v逆 ,平衡常数增大
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒容下,充入一定量的HO(g),平衡向正反应方向移动
2
D.恒容下,充入一定量的CH==CH(g),CH==CH(g)的平衡转化率增大
2 2 2 2
答案 C
解析 该反应是一个气体分子数减小的反应,增大压强可以加快化学反应速率,正反应速率
增大的幅度大于逆反应,故v >v ,平衡向正反应方向移动,但是因为温度不变,故平衡
正 逆常数不变,A不正确;催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时
CHCHOH(g)的浓度,B不正确;恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡
3 2 2 2
向正反应方向移动,C正确;恒容下,充入一定量的CH==CH(g),平衡向正反应方向移动,
2 2
但是CH==CH(g)的平衡转化率减小,D不正确。
2 2
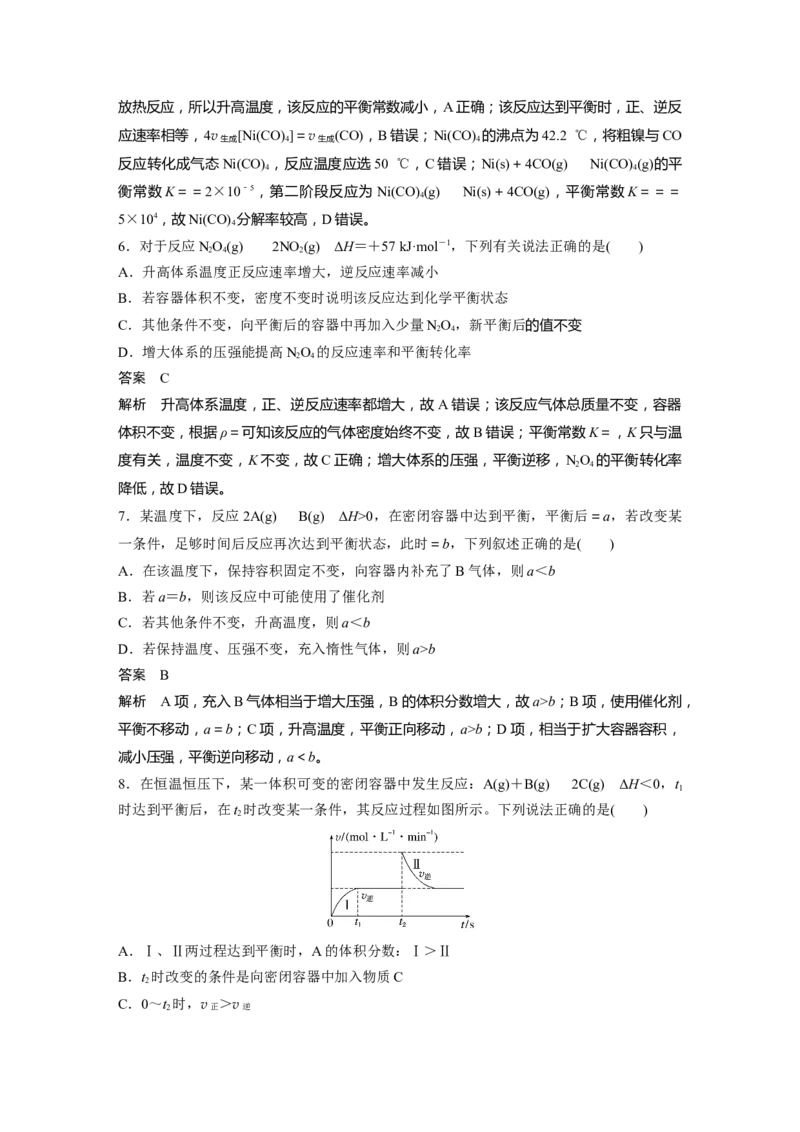
3.[2023·新课标卷,29(4)]在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分
数与温度的计算结果如图所示。其中一种进料组成为 =0.75、 =0.25,另一种为
=0.675、 =0.225、x =0.10。(物质i的摩尔分数:x=)
Ar i
①图中压强由小到大的顺序为________________,判断的依据是________________。
②进料组成中含有惰性气体Ar的图是________________。
③图1中,当p=20 MPa、 =0.20时,氮气的转化率α=________________。该温度时,
2
反应N(g)+H(g)NH (g)的平衡常数K =________________(MPa)-1(化为最简式)。
2 2 3 p
答案 ①p <p <p 合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分
1 2 3
数越大 ②图2 ③33.33%
解析 ①合成氨的反应中,压强越大平衡时氨的摩尔分数越大。由图中信息可知,在相同温
度下,反应达平衡时氨的摩尔分数:p <p <p ,因此,图中压强由小到大的顺序为p <p
1 2 3 1 2
<p 。②该反应为气体分子数减小的反应,在相同温度和相同压强下,惰性气体Ar不利于
3
合成氨,进料组成中含有惰性气体Ar的图是图2。③图1中,进料组成为 =0.75、
=0.25,两者物质的量之比为 3∶1。假设进料中氢气和氮气的物质的量分别为 3 mol和1mol,达到平衡时氮气的变化量为x mol,则有:
N(g)+3H(g)2NH (g)
2 2 3
始/mol 1 3 0
变/mol x 3x 2x
平/mol 1-x 3-3x 2x
当p =20 MPa、 =0.20时, ==0.20,解得x=,则氮气的转化率α=≈33.33%,
2
平衡时N 、H 、NH 的物质的量分别为 mol、2 mol、 mol,其物质的量分数分别为、、,
2 2 3
则该温度下K′ ==(MPa)-2,因此,该温度时反应N(g)+H(g)NH (g)的平衡常数K ==
p 2 2 3 p
(MPa)-1。
课时精练
1.下列不能用勒夏特列原理解释的事实是( )
A.红棕色的NO 加压后颜色先变深后变浅
2
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C.黄绿色的氯水光照后颜色变浅
D.向含有[Fe(SCN)]2+的红色溶液中加铁粉,振荡,溶液红色变浅或褪去
答案 B
解析 A项,涉及二氧化氮与四氧化二氮的平衡转化,故可以用勒夏特列原理解释;C项,
光照后,次氯酸见光分解,使氯气与水反应的平衡向右移动,故可以用勒夏特列原理解释;
D项,在该溶液中存在平衡:Fe3++SCN-[Fe(SCN)]2+,向溶液中加入铁粉,Fe3+会和Fe
发生反应生成Fe2+,导致Fe3+浓度降低,平衡向逆反应方向移动,使[Fe(SCN)]2+(红色)的浓
度降低,故可以用勒夏特列原理解释。
2.反应NH HS(s)NH (g)+HS(g)在某温度下达到平衡,下列各种情况不会使平衡发生移
4 3 2
动的是( )
A.温度、容积不变时,通入SO 气体
2
B.移走一部分NH HS固体
4
C.容器体积不变,充入HCl气体
D.保持压强不变,充入氮气
答案 B
解析 A项,2HS+SO ===3S+2HO,通入SO 气体使平衡正向移动;C项,NH (g)+
2 2 2 2 3
HCl(g)===NH Cl(s),充入HCl气体使平衡正向移动;D项,保持压强不变,充入氮气,平
4
衡向正反应方向移动。3.(2020·浙江7月选考,20)一定条件下:2NO (g)NO(g) ΔH<0。在测定NO 的相对
2 2 4 2
分子质量时,下列条件中,测定结果误差最小的是( )
A.温度0 ℃、压强50 kPa
B.温度130 ℃、压强300 kPa
C.温度25 ℃、压强100 kPa
D.温度130 ℃、压强50 kPa
答案 D
解析 测定NO 的相对分子质量时,要使平衡逆向移动,且逆向移动的程度越大,测定结
2
果的误差越小。该反应的正反应是气体分子数减少的放热反应,因此温度越高、压强越小时,
平衡逆向移动的程度越大,故选D。
4.在水溶液中,CrO呈黄色,Cr O呈橙色,重铬酸钾(K Cr O)在水溶液中存在以下平衡:
2 2 2 7
Cr O+HO2CrO+2H+,下列说法正确的是( )
2 2
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙色
B.该反应是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度
比原溶液大
D.向体系中加入少量水,平衡逆向移动
答案 C
解析 向该溶液中加入过量浓NaOH溶液后,消耗氢离子,氢离子浓度减小,平衡正向移
动,溶液呈黄色,A错误;反应前后元素的化合价均不发生变化,该反应不是氧化还原反应,
B错误;向该溶液中滴加适量的浓硫酸,氢离子浓度增大,平衡向逆反应方向移动,由于只
能是减弱这种改变,所以再次达到平衡后,氢离子浓度比原溶液大,C正确;向体系中加入
少量水,相当于稀释,平衡正向移动,D错误。
5.(2023·广州实验中学模拟)常压下羰基化法精炼镍的原理为Ni(s)+4CO(g)Ni(CO) (g)。
4
230 ℃时,该反应的平衡常数K=2×10-5。已知:Ni(CO) 的沸点为42.2 ℃,固体杂质不
4
参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO) ;第二阶段:将第一阶段反应后的气体分
4
离出来,加热至230 ℃制得高纯镍。
下列判断正确的是( )
A.升高温度,该反应的平衡常数减小
B.该反应达到平衡时,v生成 [Ni(CO)
4
]=4v生成 (CO)
C.第一阶段,在30 ℃和50 ℃两者之间选择反应温度应选30 ℃
D.第二阶段,Ni(CO) 分解率较低
4
答案 A
解析 反应Ni(s)+4CO(g)Ni(CO) (g)正反应是一个熵减的自发反应,故可判断该反应是
4放热反应,所以升高温度,该反应的平衡常数减小,A正确;该反应达到平衡时,正、逆反
应速率相等,4v [Ni(CO) ]=v (CO),B错误;Ni(CO) 的沸点为42.2 ℃,将粗镍与CO
生成 4 生成 4
反应转化成气态Ni(CO) ,反应温度应选50 ℃,C错误;Ni(s)+4CO(g)Ni(CO) (g)的平
4 4
衡常数K==2×10-5,第二阶段反应为Ni(CO) (g)Ni(s)+4CO(g),平衡常数K===
4
5×104,故Ni(CO) 分解率较高,D错误。
4
6.对于反应NO(g) 2NO (g) ΔH=+57 kJ·mol-1,下列有关说法正确的是( )
2 4 2
A.升高体系温度正反应速率增大,逆反应速率减小
B.若容器体积不变,密度不变时说明该反应达到化学平衡状态
C.其他条件不变,向平衡后的容器中再加入少量NO,新平衡后的值不变
2 4
D.增大体系的压强能提高NO 的反应速率和平衡转化率
2 4
答案 C
解析 升高体系温度,正、逆反应速率都增大,故 A错误;该反应气体总质量不变,容器
体积不变,根据ρ=可知该反应的气体密度始终不变,故B错误;平衡常数K=,K只与温
度有关,温度不变,K不变,故C正确;增大体系的压强,平衡逆移,NO 的平衡转化率
2 4
降低,故D错误。
7.某温度下,反应2A(g)B(g) ΔH>0,在密闭容器中达到平衡,平衡后=a,若改变某
一条件,足够时间后反应再次达到平衡状态,此时=b,下列叙述正确的是( )
A.在该温度下,保持容积固定不变,向容器内补充了B气体,则a<b
B.若a=b,则该反应中可能使用了催化剂
C.若其他条件不变,升高温度,则a<b
D.若保持温度、压强不变,充入惰性气体,则a>b
答案 B
解析 A项,充入B气体相当于增大压强,B的体积分数增大,故a>b;B项,使用催化剂,
平衡不移动,a=b;C项,升高温度,平衡正向移动,a>b;D项,相当于扩大容器容积,
减小压强,平衡逆向移动,a<b。
8.在恒温恒压下,某一体积可变的密闭容器中发生反应:A(g)+B(g)2C(g) ΔH<0,t
1
时达到平衡后,在t 时改变某一条件,其反应过程如图所示。下列说法正确的是( )
2
A.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数:Ⅰ>Ⅱ
B.t 时改变的条件是向密闭容器中加入物质C
2
C.0~t
2
时,v正 >v逆D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数:K(Ⅰ)<K(Ⅱ)
答案 B
解析 反应速率与其物质的量浓度成正比,Ⅰ、Ⅱ达到平衡状态时逆反应速率相等,说明Ⅰ、
Ⅱ达到平衡状态时各物质的物质的量浓度不变,则A的体积分数:Ⅰ=Ⅱ,故A错误;向
密闭容器中加物质C,逆反应速率瞬间增大,再次建立的平衡和原平衡相同,符合图像,故
B正确;由题图可知,0~t 时,逆反应速率增大,说明平衡正向移动,即 v >v ,t ~t
1 正 逆 1 2
时,逆反应速率不变,说明处于平衡状态,即 v =v ,故C错误;化学平衡常数只与温度
正 逆
有关,Ⅰ、Ⅱ温度相同,则其平衡常数相同,故D错误。
9.(2023·河北沧州高三联考)T ℃下,在恒压密闭容器中发生反应:SCl(l,浅黄色)+
2 2
Cl(g)2SCl (l,红棕色) ΔH<0。已知SCl 分子中各原子均满足8电子稳定结构,下列
2 2 2 2
说法正确的是( )
A.当单位时间内断裂n mol S—S,同时有n mol Cl 被还原时,说明反应达到平衡状态
2
B.平衡后,升高温度,容器体积减小
C.平衡后,压缩容器体积,容器中黄绿色先变深后变浅,最终气体颜色和原来一样
D.平衡后,增加SCl (l)的物质的量,平衡向正反应方向移动
2 2
答案 C
解析 单位时间内断裂n mol S—S和n mol Cl 被还原都在描述正反应速率,不能作为平衡
2
判据,A项错误;因该反应在恒压密闭容器中进行且ΔH<0,平衡后,升高温度,平衡逆向
移动,生成Cl ,容器体积增大,B项错误;平衡常数K=,温度不变,平衡常数不变,即
2
c(Cl )不变,增大压强后c(Cl )先增大后减小,最终与原来一样,C项正确;增加SCl (l)的
2 2 2 2
物质的量,平衡不移动,D项错误。
10.Deacon 催化氧化法将 HCl 转化为 Cl 的反应为 4HCl(g)+O(g)2Cl(g)+2HO(g)
2 2 2 2
ΔH,研究发现CuCl (s)催化反应的过程如下:
2
反应ⅰ:2CuCl (s)2CuCl(s)+Cl(g)
2 2
反应ⅱ:2CuCl(s)+O(g)2CuO(s)+Cl(g)
2 2
反应ⅲ:……
下列关于Deacon催化氧化法制Cl 的说法正确的是( )
2
A.反应ⅰ增大压强,达到新平衡后Cl 浓度减小
2
B.反应4HCl(g)+O(g)2Cl(g)+2HO(g)的ΔH>0
2 2 2
C.由反应过程可知催化剂参与反应,通过改变反应路径提高平衡转化率
D.推断反应ⅲ应为CuO(s)+2HCl(g)CuCl (s)+HO(g)
2 2
答案 D
解析 温度不变,平衡常数不变,K=c(Cl ),因此反应ⅰ增大压强,达到新平衡后Cl 浓度
2 2
不变,A错误;反应4HCl(g)+O(g)2Cl(g)+2HO(g)是放热反应,B错误;依据盖斯定
2 2 2
律,用[总反应-(反应ⅰ+反应ⅱ)]×得反应ⅲ:CuO(s)+2HCl(g)CuCl (s)+HO(g),D
2 2正确;由反应ⅰ、ⅱ、ⅲ知,催化剂CuCl 参加反应,通过改变反应历程,从而提高反应速
2
率,但不影响平衡,改变不了平衡转化率,C错误。
11.如图所示,左室容积为右室的两倍,温度相同,现分别按照如图所示的量充入气体,同
时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反应再次达到平衡。
下列说法不正确的是( )
A.第一次平衡时,SO 的物质的量左室更多
2
B.气体未反应前,左室压强和右室一样大
C.第一次平衡时,左室内压强一定小于右室
D.第二次平衡时,SO 的总物质的量比第一次平衡时左室SO 的物质的量的2倍多
2 2
答案 D
解析 两室中发生反应2SO (g)+O(g)2SO (g),若右室的容积与左室相等,左室和右
2 2 3
室在相同条件下达到的平衡状态相同,含有的SO 物质的量相等,右室在此平衡状态时将体
2
积缩小为原来的,压强增大,平衡向生成SO 的方向移动,SO 物质的量减少,则第一次平
3 2
衡时,SO 的物质的量左室更多,A项正确;通入气体未反应前,左室气体总物质的量为 4
2
mol,右室气体总物质的量为2 mol,左室容积为右室的两倍,温度相同,则左室压强和右
室一样大,B项正确;左室从正反应开始建立平衡,左室平衡时压强小于左室起始压强,右
室从逆反应开始建立平衡,右室平衡时压强大于右室起始压强,左室与右室起始压强相等,
则第一次平衡时左室内压强一定小于右室,C项正确;若在容积为2倍左室容积的容器中起
始充4 mol SO 、2 mol O ,相同条件下达到平衡时SO 的物质的量为左室SO 物质的量的2
2 2 2 2
倍,打开活塞相当于在容积为1.5倍左室容积的容器中起始充入2 mol SO 、1 mol O 、2 mol
2 2
SO (g)、1 mol Ar,相当于在容积为1.5倍左室容积的容器中起始充入4 mol SO 、2 mol O 、
3 2 2
1 mol Ar,相对于2倍左室容积的容器缩小了体积,压强增大,平衡向正反应方向移动,
SO 物质的量减小,即第二次平衡时,SO 的总物质的量比第一次平衡时左室SO 物质的量
2 2 2
的2倍要少,D项错误。
12.(2023·安徽蚌埠统考模拟)能源的合理开发和利用、低碳减排是人类正在努力解决的大问
题。
(1)在固相催化剂作用下CO 加氢合成甲烷过程中发生以下两个反应:
2
主反应:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-156.9 kJ·mol-1
2 2 4 2 1
副反应:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.1 kJ·mol-1
2 2 2 2
工业合成甲烷通常控制温度为500 ℃左右,其主要原因为_____________________
________________________________________________________________________。
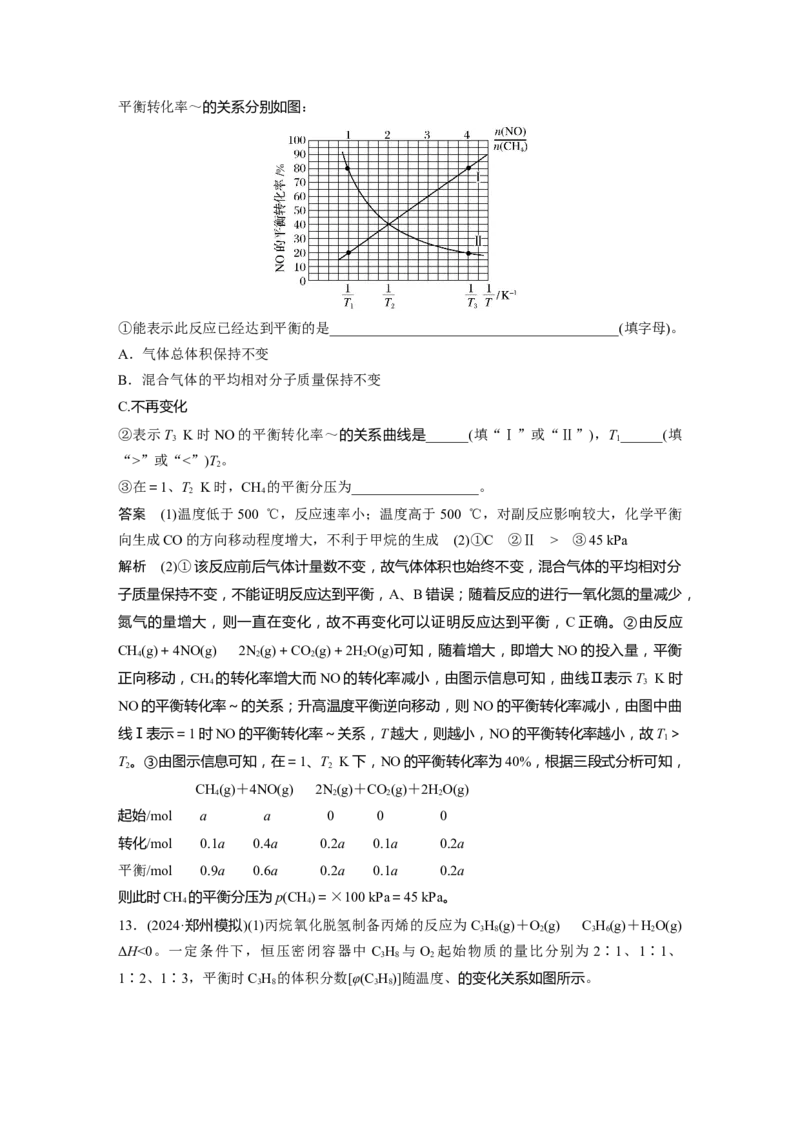
(2)向密闭容器中充入一定量的 CH(g)和NO(g),保持总压为100 kPa发生反应:CH(g)+
4 4
4NO(g)2N(g)+CO(g)+2HO(g) ΔH<0。当=1时NO的平衡转化率~、T K下NO的
2 2 2 3平衡转化率~的关系分别如图:
①能表示此反应已经达到平衡的是_________________________________________(填字母)。
A.气体总体积保持不变
B.混合气体的平均相对分子质量保持不变
C.不再变化
②表示T K时NO的平衡转化率~的关系曲线是______(填“Ⅰ”或“Ⅱ”),T______(填
3 1
“>”或“<”)T。
2
③在=1、T K时,CH 的平衡分压为__________________。
2 4
答案 (1)温度低于500 ℃,反应速率小;温度高于500 ℃,对副反应影响较大,化学平衡
向生成CO的方向移动程度增大,不利于甲烷的生成 (2)①C ②Ⅱ > ③45 kPa
解析 (2)①该反应前后气体计量数不变,故气体体积也始终不变,混合气体的平均相对分
子质量保持不变,不能证明反应达到平衡,A、B错误;随着反应的进行一氧化氮的量减少,
氮气的量增大,则一直在变化,故不再变化可以证明反应达到平衡,C正确。②由反应
CH(g)+4NO(g)2N(g)+CO(g)+2HO(g)可知,随着增大,即增大NO的投入量,平衡
4 2 2 2
正向移动,CH 的转化率增大而NO的转化率减小,由图示信息可知,曲线Ⅱ表示T K时
4 3
NO的平衡转化率~的关系;升高温度平衡逆向移动,则 NO的平衡转化率减小,由图中曲
线Ⅰ表示=1时NO的平衡转化率~关系,T越大,则越小,NO的平衡转化率越小,故T>
1
T。③由图示信息可知,在=1、T K下,NO的平衡转化率为40%,根据三段式分析可知,
2 2
CH(g)+4NO(g)2N(g)+CO(g)+2HO(g)
4 2 2 2
起始/mol a a 0 0 0
转化/mol 0.1a 0.4a 0.2a 0.1a 0.2a
平衡/mol 0.9a 0.6a 0.2a 0.1a 0.2a
则此时CH 的平衡分压为p(CH)=×100 kPa=45 kPa。
4 4
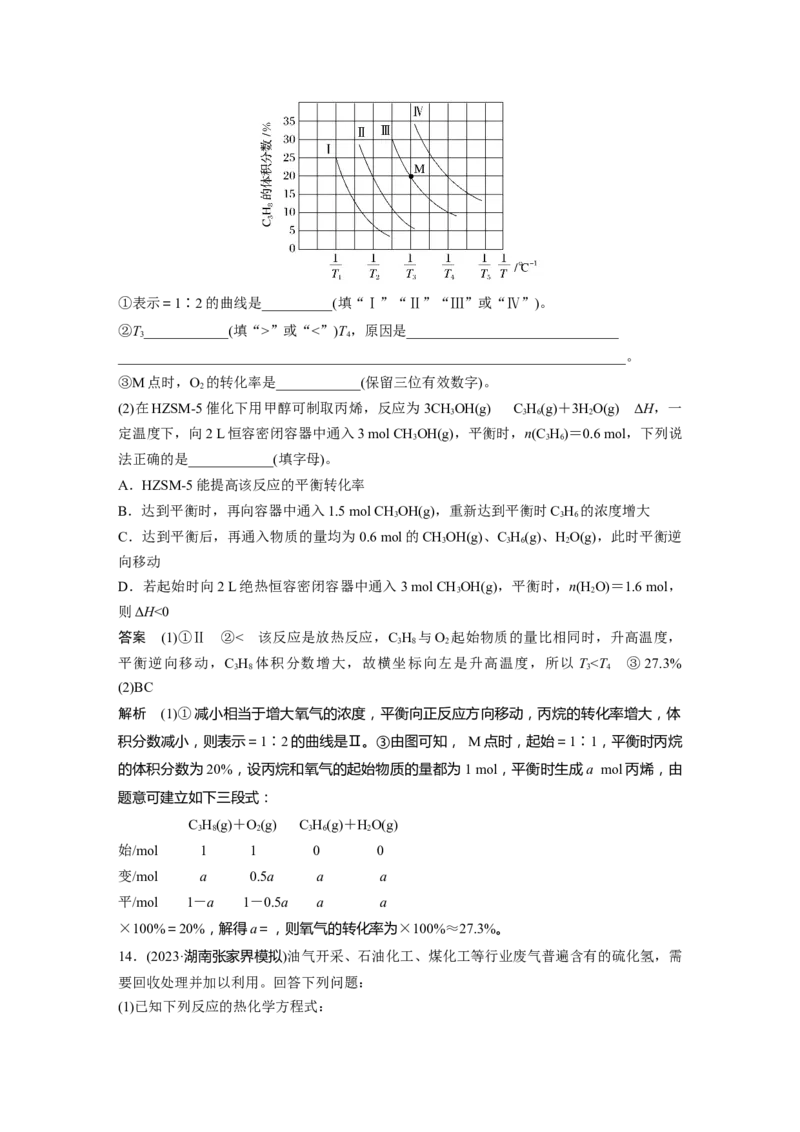
13.(2024·郑州模拟)(1)丙烷氧化脱氢制备丙烯的反应为C H(g)+O(g)C H(g)+HO(g)
3 8 2 3 6 2
ΔH<0。一定条件下,恒压密闭容器中 C H 与O 起始物质的量比分别为 2∶1、1∶1、
3 8 2
1∶2、1∶3,平衡时C H 的体积分数[φ(C H)]随温度、的变化关系如图所示。
3 8 3 8①表示=1∶2的曲线是__________(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
②T____________(填“>”或“<”)T,原因是______________________________
3 4
________________________________________________________________________。
③M点时,O 的转化率是____________(保留三位有效数字)。
2
(2)在HZSM-5催化下用甲醇可制取丙烯,反应为3CHOH(g)C H(g)+3HO(g) ΔH,一
3 3 6 2
定温度下,向2 L恒容密闭容器中通入3 mol CH OH(g),平衡时,n(C H)=0.6 mol,下列说
3 3 6
法正确的是____________(填字母)。
A.HZSM-5能提高该反应的平衡转化率
B.达到平衡时,再向容器中通入1.5 mol CH OH(g),重新达到平衡时C H 的浓度增大
3 3 6
C.达到平衡后,再通入物质的量均为0.6 mol的CHOH(g)、C H(g)、HO(g),此时平衡逆
3 3 6 2
向移动
D.若起始时向2 L绝热恒容密闭容器中通入3 mol CH OH(g),平衡时,n(H O)=1.6 mol,
3 2
则ΔH<0
答案 (1)①Ⅱ ②< 该反应是放热反应,C H 与O 起始物质的量比相同时,升高温度,
3 8 2
平衡逆向移动,C H 体积分数增大,故横坐标向左是升高温度,所以 TT>T 恒压条件下,HS的摩尔分数增大,平衡正向移动,最
1 2 3 2
终HS的转化率降低 (3)< 在1 000 K,反应①ΔG>0,反应趋势小,反应③ΔG<0,反应
2
趋势大,占主导 (4)1.28×104解析 (1)反应③等于反应①减去反应②,ΔH =+180 kJ·mol-1-(-81 kJ·mol-1)=+261
3
kJ·mol-1;A项中都表示正反应,故A不符合题意;该反应是气体分子数变化的反应,恒容
条件下压强不变即达到平衡,故B符合题意;恒容条件又都是气体参与反应,故密度始终
保持不变,故C不符合题意。(2)反应①是吸热反应,温度升高,平衡正向移动,则 HS的
2
转化率增大,故T>T>T 。(3)在1 000 K,反应①ΔG>0,不易自发,反应③ΔG<0,容易自
1 2 3
发,故反应自发趋势①<③。(4)设n(H S)=3 mol,列三段式
2
CH(g)+2HS(g)CS(g)+4H(g)
4 2 2 2
初始/mol 3 3 0 0
转化/mol x 2x x 4x
平衡/mol 3-x 3-2x x 4x
达到平衡时,CS 分压与HS的分压相同即有3-2x=x,解得x=1,平衡后气体的总物质的
2 2
量为2 mol+1 mol+1 mol+4 mol+2 mol=10 mol,则K ==1.28×104。
p