文档内容
第 48 讲 影响化学平衡的因素
[复习目标] 1.掌握外界条件改变对化学平衡的影响。2.掌握并会运用勒夏特列原理分析平
衡的移动。3.掌握平衡移动与转化率的关系。
考点一 化学平衡的移动
1.化学平衡移动的根本原因
(1)平衡移动的过程
(2)平衡移动与速率的关系
①v正 ____v逆 ,化学平衡向正反应方向移动;
②v正 ____v逆 ,化学平衡向逆反应方向移动;
③v正 ____v逆 ,化学平衡不发生移动。
2.化学平衡移动的重要实验再现
(1)探究浓度对化学平衡的影响
实验一:Fe3++3SCN-Fe(SCN) (红色),加入较浓的FeCl 溶液或KSCN溶液、少量铁
3 3
粉、KCl固体,通过观察溶液红色的变化,分析平衡移动。
_______________________________________________________________________________
_______________________________________________________________________________
实验二:Cr O(橙色)+HO2CrO (黄色)+2H+,滴加NaOH溶液或硫酸溶液,通过观察
2 2
溶液颜色的变化,分析平衡移动。
_______________________________________________________________________________
_______________________________________________________________________________
(2)探究压强对化学平衡的影响
实验三:2NO (红棕色)NO(无色)
2 2 4
通过压缩体积观察颜色变化,分析平衡移动。
_______________________________________________________________________________
_______________________________________________________________________________
(3)探究温度对化学平衡的影响实验四:[Cu(H O) ]2+(蓝色)+4Cl-[CuCl ]2-(黄色)+4HO ΔH>0。
2 4 4 2
将分别盛有2 mL 0.5 mol·L-1 CuCl 溶液的两支试管,一支试管先加热,然后置于冷水中,
2
与另一支试管进行对比。
实验步骤 实验现象 结论
加热试管
将上述试管置于冷水中
思考 在对CuCl 溶液加热时,为何未看到溶液变为黄色?
2
_______________________________________________________________________________
_______________________________________________________________________________
3.化学平衡移动原理——勒夏特列原理
如果改变影响平衡的一个因素(如浓度、压强或温度),平衡就向着能够________这种改变的
方向移动,这就是勒夏特列原理,也称化学平衡移动原理。
一、外因对正逆反应速率与化学平衡移动的影响
1.外界条件对化学平衡的影响是通过改变正、逆反应速率来实现的,其移动方向取决于改
变条件的瞬间v正 和v逆 的相对大小。试完成下表(说明:表中的压强的变化是指通过改变气
体的体积实现的)。
改变条件的瞬间反应速率的变化
条件的改变(假设其他条件不变) 化学平衡的移动
v正 v逆
①增大反应物浓度
②减小反应物浓度
(1)浓度
③增大生成物浓度
④减小生成物浓度
①增大压强
(2)压强
②减小压强
①升高温度
(3)温度
②降低温度
(4)催化剂 使用催化剂
2.将NO 装入带活塞的密闭容器中,当反应2NO (g)NO(g)达到平衡后,改变下列一个
2 2 2 4
条件,其中叙述正确的是( )
A.升高温度,气体颜色加深,则此反应为吸热反应
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D.恒温恒压时,充入惰性气体,平衡向左移动,混合气体的颜色变深惰性气体对化学平衡的影响
二、通过图像理解化学平衡移动
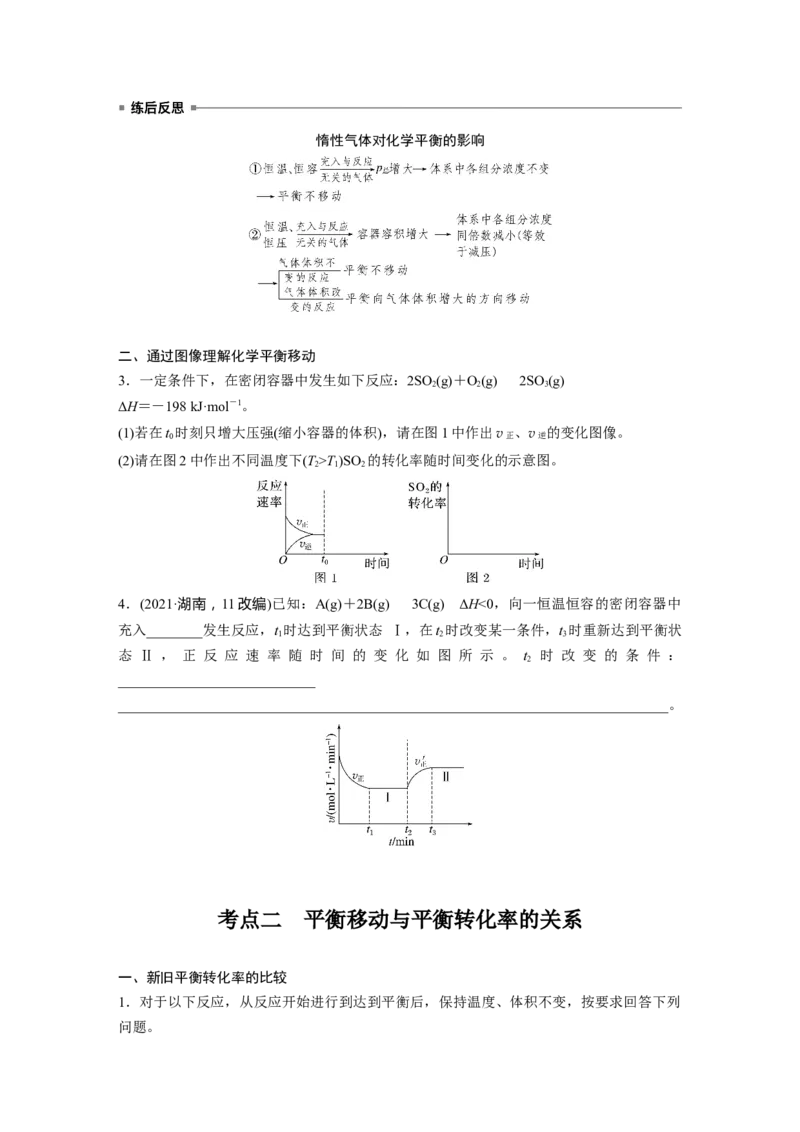
3.一定条件下,在密闭容器中发生如下反应:2SO (g)+O(g)2SO (g)
2 2 3
ΔH=-198 kJ·mol-1。
(1)若在t
0
时刻只增大压强(缩小容器的体积),请在图1中作出v正 、v逆 的变化图像。
(2)请在图2中作出不同温度下(T>T)SO 的转化率随时间变化的示意图。
2 1 2
4.(2021·湖南,11改编)已知:A(g)+2B(g)3C(g) ΔH<0,向一恒温恒容的密闭容器中
充入________发生反应,t 时达到平衡状态 Ⅰ,在t 时改变某一条件,t 时重新达到平衡状
1 2 3
态 Ⅱ , 正 反 应 速 率 随 时 间 的 变 化 如 图 所 示 。 t 时 改 变 的 条 件 :
2
____________________________
______________________________________________________________________________。
考点二 平衡移动与平衡转化率的关系
一、新旧平衡转化率的比较
1.对于以下反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答下列
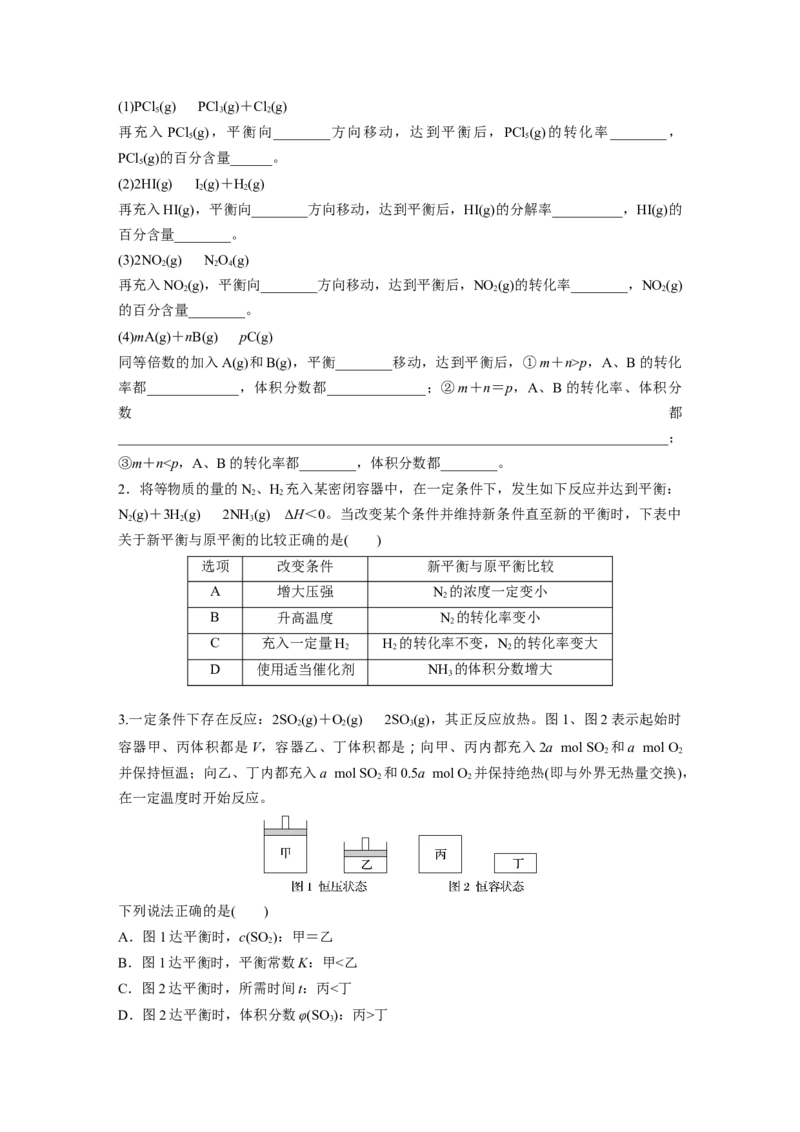
问题。(1)PCl (g)PCl (g)+Cl(g)
5 3 2
再充入 PCl (g),平衡向________方向移动,达到平衡后,PCl (g)的转化率________,
5 5
PCl (g)的百分含量______。
5
(2)2HI(g)I(g)+H(g)
2 2
再充入HI(g),平衡向________方向移动,达到平衡后,HI(g)的分解率__________,HI(g)的
百分含量________。
(3)2NO (g)NO(g)
2 2 4
再充入NO (g),平衡向________方向移动,达到平衡后,NO (g)的转化率________,NO (g)
2 2 2
的百分含量________。
(4)mA(g)+nB(g)pC(g)
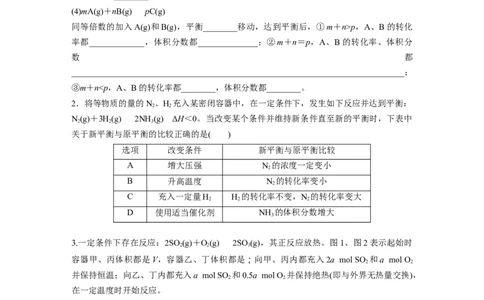
同等倍数的加入A(g)和B(g),平衡________移动,达到平衡后,①m+n>p,A、B的转化
率都_____________,体积分数都______________;②m+n=p,A、B的转化率、体积分
数 都
______________________________________________________________________________;
③m+n丁
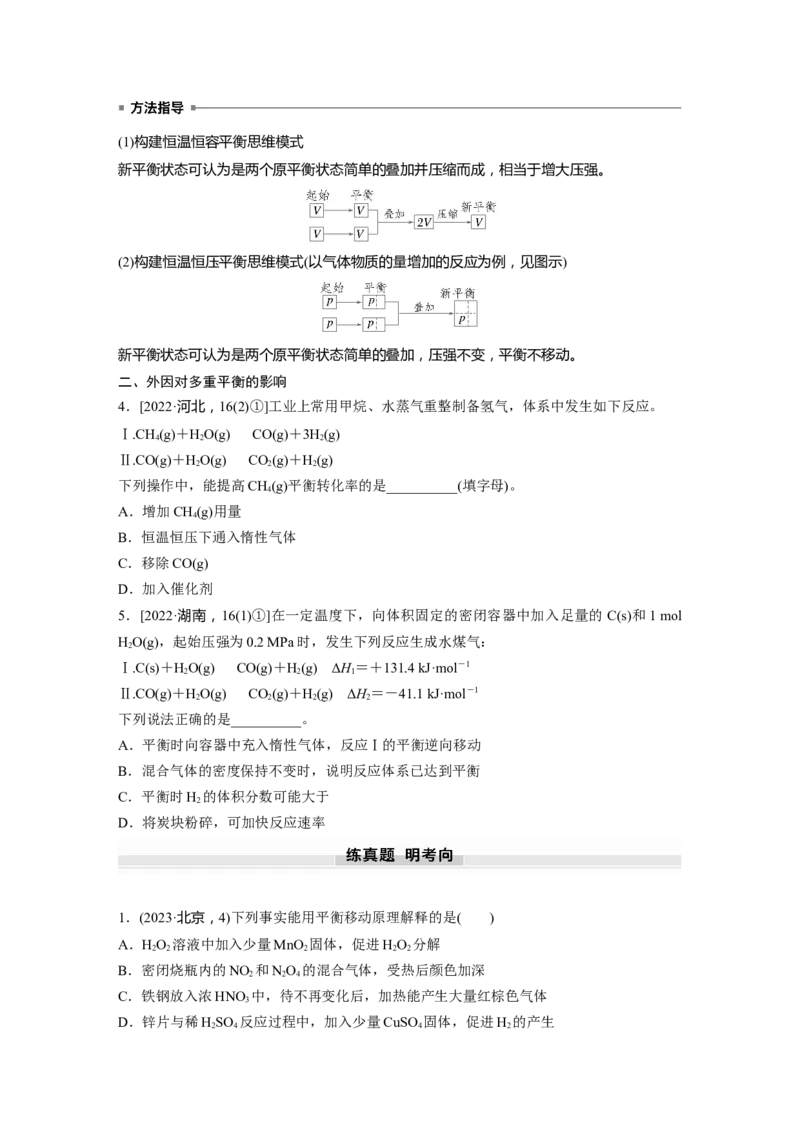
3(1)构建恒温恒容平衡思维模式
新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大压强。
(2)构建恒温恒压平衡思维模式(以气体物质的量增加的反应为例,见图示)
新平衡状态可认为是两个原平衡状态简单的叠加,压强不变,平衡不移动。
二、外因对多重平衡的影响
4.[2022·河北,16(2)①]工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.CH (g)+HO(g)CO(g)+3H(g)
4 2 2
Ⅱ.CO(g)+HO(g)CO(g)+H(g)
2 2 2
下列操作中,能提高CH(g)平衡转化率的是__________(填字母)。
4
A.增加CH(g)用量
4
B.恒温恒压下通入惰性气体
C.移除CO(g)
D.加入催化剂
5.[2022·湖南,16(1)①]在一定温度下,向体积固定的密闭容器中加入足量的 C(s)和1 mol
HO(g),起始压强为0.2 MPa时,发生下列反应生成水煤气:
2
Ⅰ.C(s)+HO(g)CO(g)+H(g) ΔH=+131.4 kJ·mol-1
2 2 1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41.1 kJ·mol-1
2 2 2 2
下列说法正确的是__________。
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时H 的体积分数可能大于
2
D.将炭块粉碎,可加快反应速率
1.(2023·北京,4)下列事实能用平衡移动原理解释的是( )
A.HO 溶液中加入少量MnO 固体,促进HO 分解
2 2 2 2 2
B.密闭烧瓶内的NO 和NO 的混合气体,受热后颜色加深
2 2 4
C.铁钢放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D.锌片与稀HSO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 22.(2022·海南,8)某温度下,反应CH===CH(g)+HO(g)CHCHOH(g)在密闭容器中达
2 2 2 3 2
到平衡,下列说法正确的是( )
A.增大压强,v正 >v逆 ,平衡常数增大
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒容下,充入一定量的HO(g),平衡向正反应方向移动
2
D.恒容下,充入一定量的CH===CH(g),CH===CH(g)的平衡转化率增大
2 2 2 2
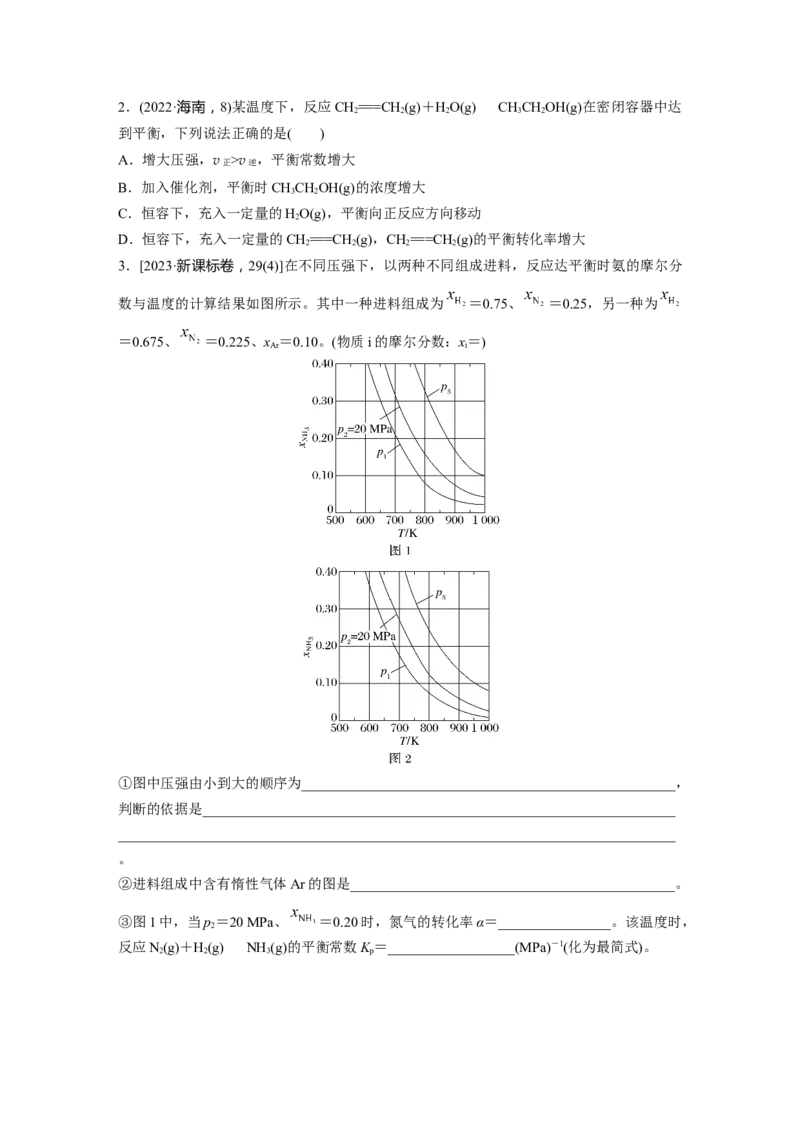
3.[2023·新课标卷,29(4)]在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分
数与温度的计算结果如图所示。其中一种进料组成为 =0.75、 =0.25,另一种为
=0.675、 =0.225、x =0.10。(物质i的摩尔分数:x=)
Ar i
①图中压强由小到大的顺序为_____________________________________________________,
判断的依据是___________________________________________________________________
_______________________________________________________________________________
。
②进料组成中含有惰性气体Ar的图是______________________________________________。
③图1中,当p=20 MPa、 =0.20时,氮气的转化率α=________________。该温度时,
2
反应N(g)+H(g)NH (g)的平衡常数K =__________________(MPa)-1(化为最简式)。
2 2 3 p