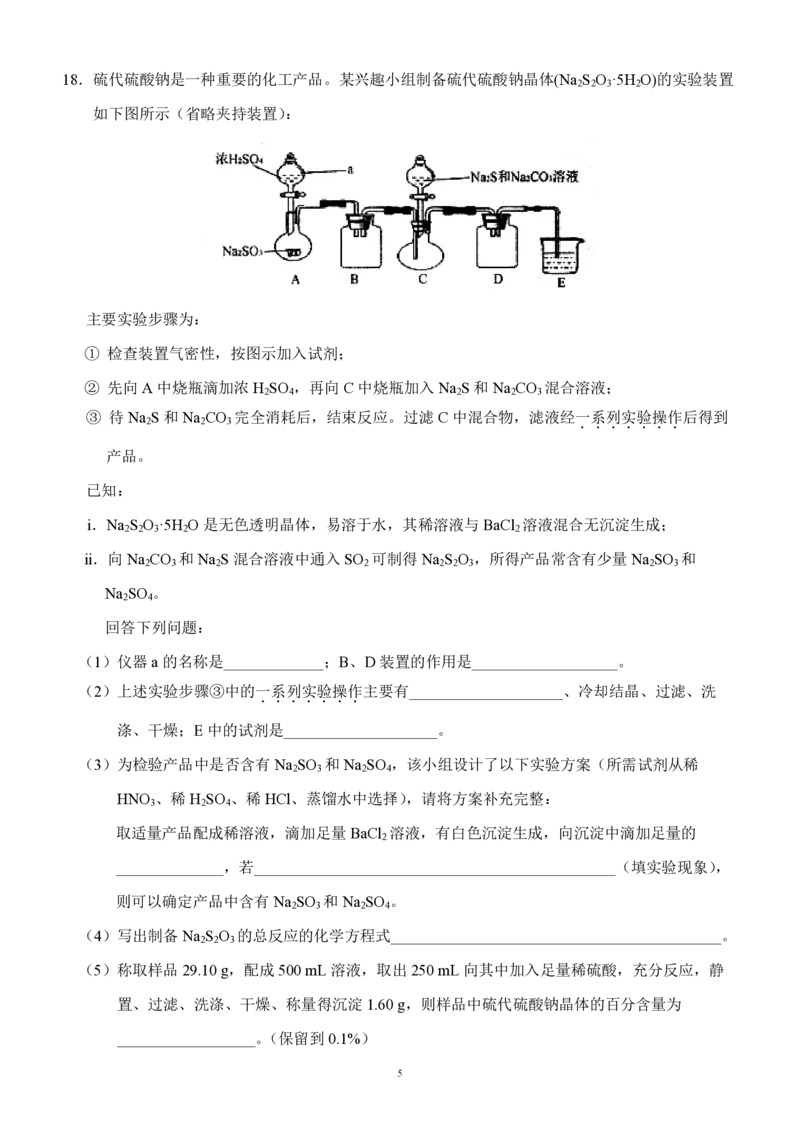
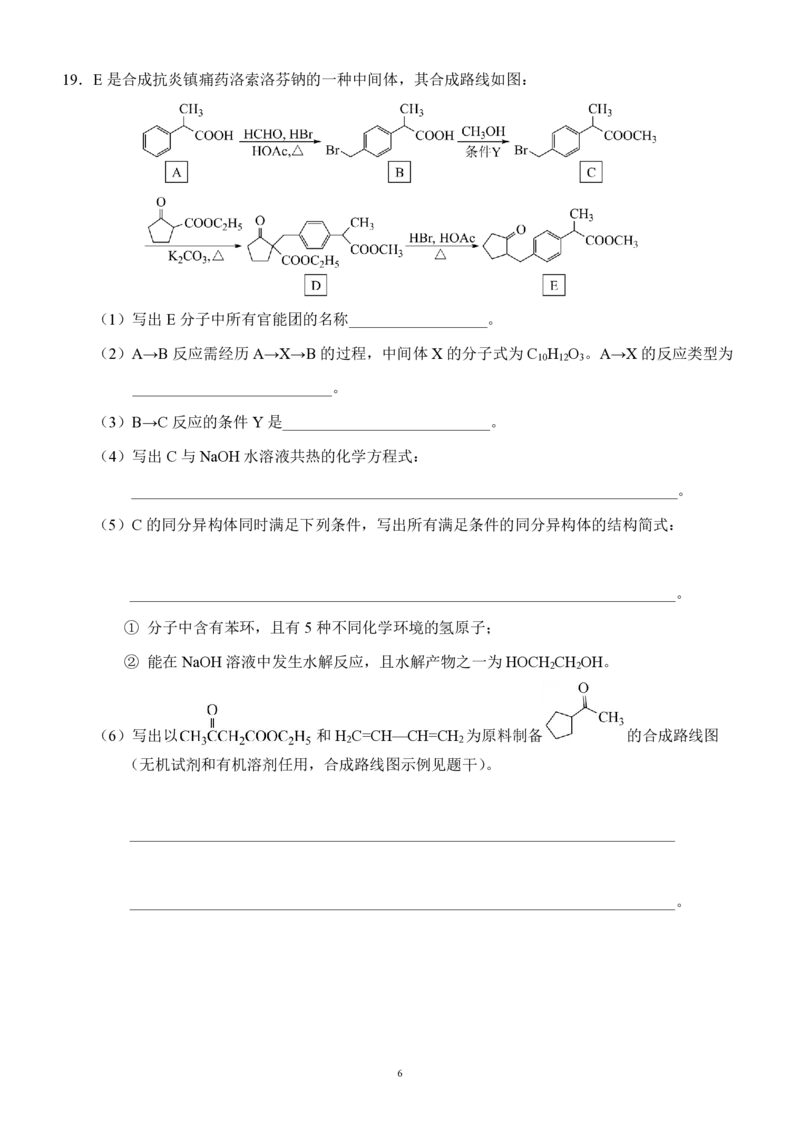
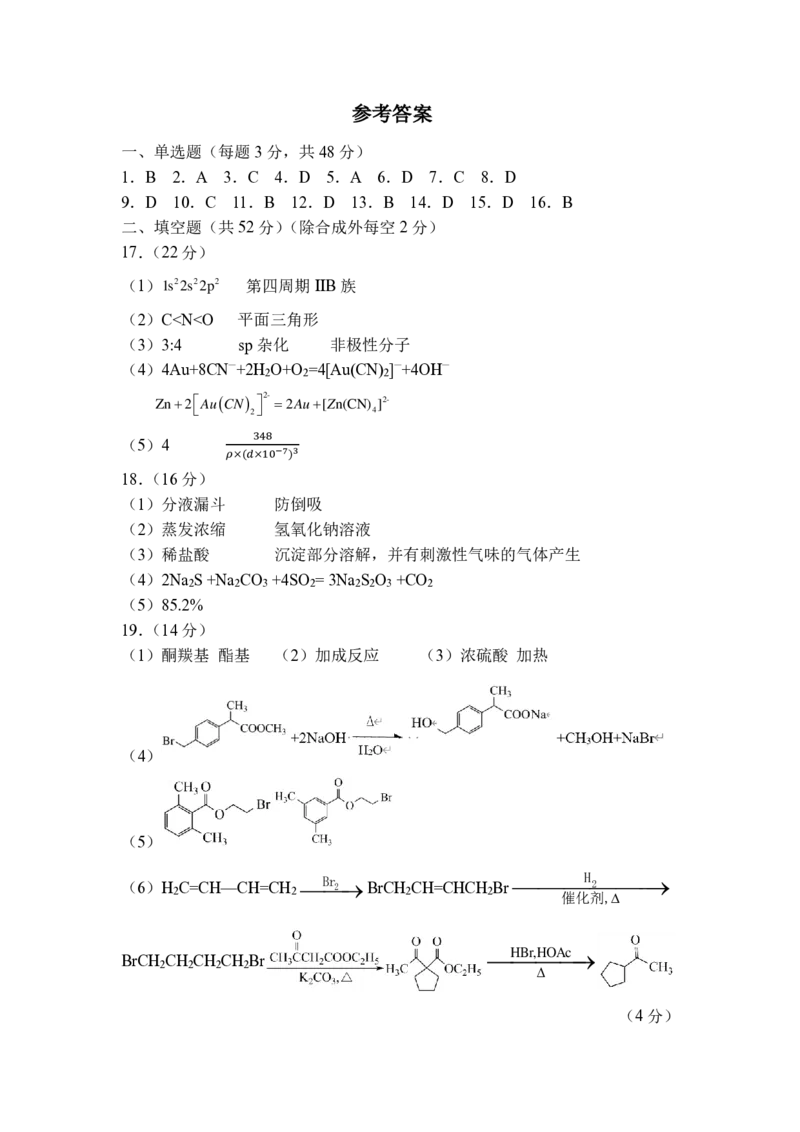
文档内容
天津市新华中学 2022—2023 学年度第一学期高三级部第二次月考
化学 学科(共 6 页) 2022年 12月
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 Mg-24 P-31 S-32 Cl-35.5 Mn-55 Fe-56 Cu-64
Ⅰ卷
一、选择题(每题 3 分,共 48 分)
1.化学与生活密切相关。下列叙述错误的是
A.中国古代利用明矾溶液清除铜镜表面的铜锈
B.二氧化硅是将太阳能转变为电能的常用材料
C.使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力差
D.与铜相比,青铜具有熔点低、硬度大等特点
2.下列说法正确的是
A.电负性:Se>As B.离子半径:Na+>Cl−
C.第一电离能:Al>Mg D.键长:Cl−Cl>Br−Br
3.下列化学用语正确的是
A.二氧化碳的电子式:
B.HBr 的形成过程:
C.基态Mn2+的价电子轨道表示式:
D.乙酸的结构式:
4.设 N 为阿伏加德罗常数的值,下列说法正确的是
A
A.7.8gNa O 和Na S混合物中所含的阴离子总数为 0.15N
2 2 2 A
B.1 L 0.1 mol/L K Cr O 溶液中 Cr O 2—离子数为 0.1N
2 2 7 2 7 A
C.常温常压下,124 g P 中所含 P-P 键的数目为 4N
4 A
D.向密闭容器中充入 2 mol NO 与 1 mol O 充分反应后容器内的分子数小于 2N
2 A
5.在指定溶液中下列离子可能大量共存的是
A.透明澄清的溶液:NH +、Fe3+、SO 2-、NO —
4 4 3
B.能使酚酞变红的溶液:Na+、Ca2+、AlO —、HCO —-
2 3
C.c(ClO—)=0.1 mol/L 的溶液:K+、Na+、CO 2-、S2-
3
D.加入 Al 能放出 H 的溶液:Mg2+、NH +、Cl—、NO —
2 4 3
6.下列有关热化学方程式的叙述正确的是
A.已知 C(石墨,S) ⇌ C(金刚石,S) ΔH>0,则金刚石比石墨稳定
B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
C.甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为
CH (g)+2O (g)=CO (g)+2H O(g) ΔH=-890.3kJmol-1
4 2 2 2
D.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l) ΔH=-57.3kJmol-1,则含40.0g NaOH的稀溶液
2
与稀醋酸完全中和,放出小于57.3kJ的热量
17.在配制一定物质的量浓度的溶液的实验中,下列操作及误差分析正确的是
A.将 NaOH 固体放在托盘天平左盘称量纸上,称量后放入烧杯中溶解,待冷却后注入容量瓶
B.将量取的18.4molL−1浓硫酸 10 mL,注入已盛有 30 mL 水的 100 mL 容量瓶中,待冷却后再定
容至刻度线即可配得1.8molL−1的稀硫酸
C.定容时仰视容量瓶刻度线,会导致所配溶液浓度偏低
D.往容量瓶转移溶液时,不小心有洒落,适当补充即可
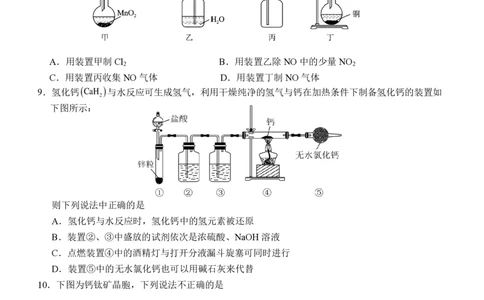
8.下列装置能达到实验目的的是
A.用装置甲制 Cl B.用装置乙除 NO 中的少量 NO
2 2
C.用装置丙收集 NO 气体 D.用装置丁制 NO 气体
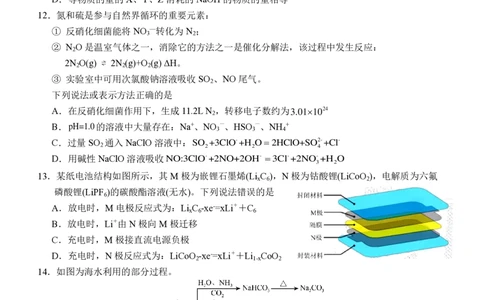
9.氢化钙
(CaH )
与水反应可生成氢气,利用干燥纯净的氢气与钙在加热条件下制备氢化钙的装置如
2
下图所示:
则下列说法中正确的是
A.氢化钙与水反应时,氢化钙中的氢元素被还原
B.装置②、③中盛放的试剂依次是浓硫酸、NaOH 溶液
C.点燃装置④中的酒精灯与打开分液漏斗旋塞可同时进行
D.装置⑤中的无水氯化钙也可以用碱石灰来代替
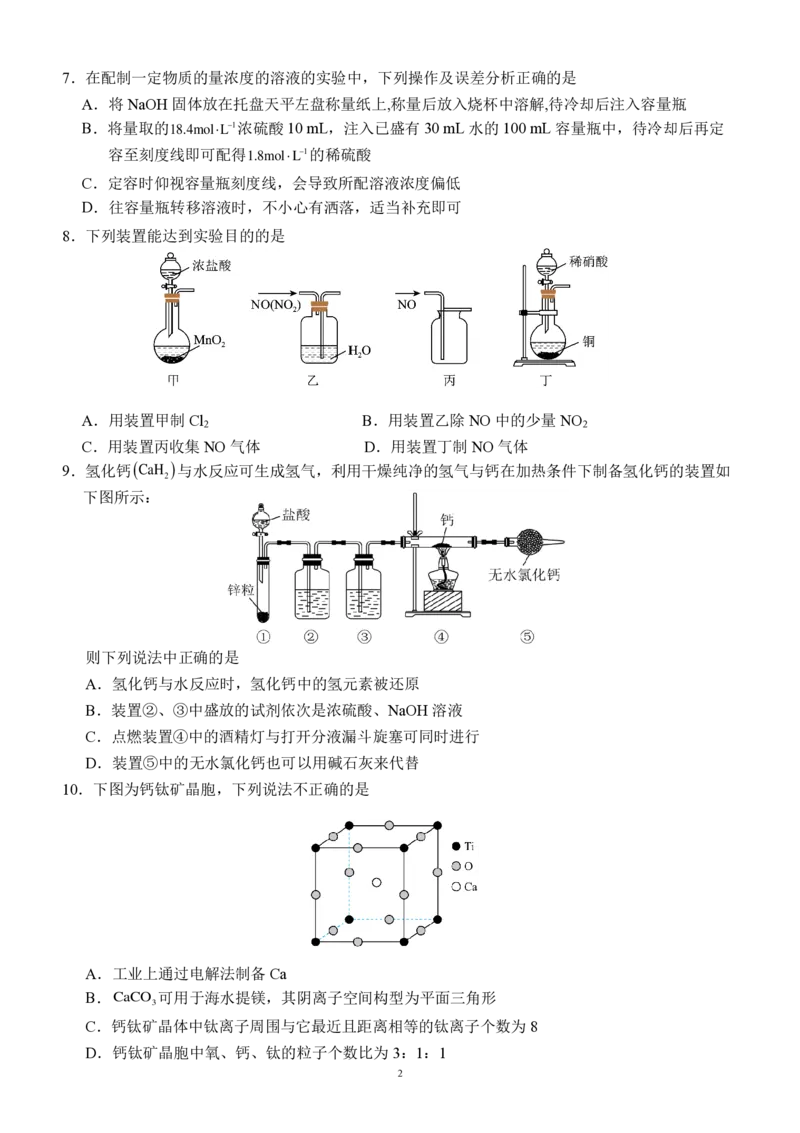
10.下图为钙钛矿晶胞,下列说法不正确的是
A.工业上通过电解法制备 Ca
B.CaCO 可用于海水提镁,其阴离子空间构型为平面三角形
3
C.钙钛矿晶体中钛离子周围与它最近且距离相等的钛离子个数为 8
D.钙钛矿晶胞中氧、钙、钛的粒子个数比为 3:1:1
211.药物异博定能有效控制血压升高、促进血液循环,其合成路线中有如下转化过程。
下列说法正确的是
A.X 的沸点高于其同分异构体
B.一定条件下,X 可与 HCHO 发生缩聚反应
C.Z 分子不存在顺反异构体
D.等物质的量的 X、Y、Z 消耗的 NaOH 的物质的量相等
12.氮和硫是参与自然界循环的重要元素:
① 反硝化细菌能将 NO —转化为 N ;
3 2
② N O 是温室气体之一,消除它的方法之一是催化分解法,该过程中发生反应:
2
2N O(g) ⇌ 2N (g)+O (g) ΔH。
2 2 2
③ 实验室中可用次氯酸钠溶液吸收 SO 、NO 尾气。
2
下列说法或表示方法正确的是
A.在反硝化细菌作用下,生成 11.2L N ,转移电子数约为3.011024
2
B.pH=1.0的溶液中大量存在:Na+、NO —、HSO —、NH +
3 3 4
C.过量 SO 通入 NaClO 溶液中:SO +3ClO-+H O = 2HClO+SO2-+Cl-
2 2 2 4
D.用碱性 NaClO 溶液吸收NO:3ClO-+2NO+2OH- =3Cl-+2NO-+H O
3 2
13.某纸电池结构如图所示,其 M 极为嵌锂石墨烯(Li C ),N 极为钴酸锂(LiCoO ),电解质为六氟
x 6 2
磷酸锂(LiPF )的碳酸酯溶液(无水)。下列说法错误的是
6
A.放电时,M 电极反应式为:Li C -xe-=xLi++C
x 6 6
B.放电时,Li+由 N 极向 M 极迁移
C.充电时,M 极接直流电源负极
D.充电时,N 极反应式为:LiCoO -xe-=xLi++Li CoO
2 1-x 2
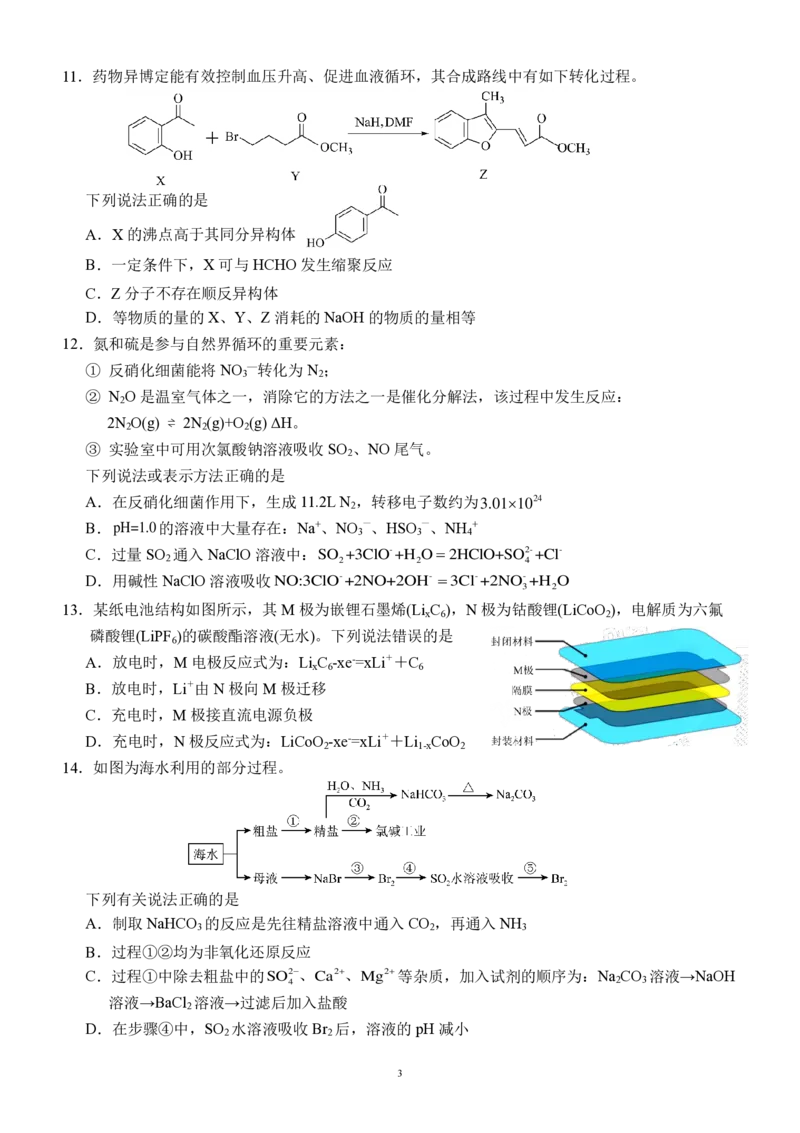
14.如图为海水利用的部分过程。
下列有关说法正确的是
A.制取 NaHCO 的反应是先往精盐溶液中通入 CO ,再通入 NH
3 2 3
B.过程①②均为非氧化还原反应
C.过程①中除去粗盐中的SO2−、Ca2+、Mg2+等杂质,加入试剂的顺序为:Na CO 溶液→NaOH
4 2 3
溶液→BaCl 溶液→过滤后加入盐酸
2
D.在步骤④中,SO 水溶液吸收 Br 后,溶液的 pH 减小
2 2
315.某实验小组测定铁的氧化物 Fe O 的化学式,已知该氧化物中铁元素只有+2 和+3 两种价态,实
x y
验步骤如图,下列说法正确的是
A.步骤①和步骤②都发生了氧化还原反应
B.溶液 a 中阳离子只有 Fe3+和 Fe2+
C.溶液 b 中 n(Fe3+):n(Cl—)=1:3
D.计算可得该氧化物的化学式为:Fe O
4 5
16.将 m g 铜镁合金完全溶解于 50 ml、密度为1.40g/cm3、质量分数为 63%的浓硝酸中,得到 1792
mL (标准状况)NO 气体,向反应后的溶液中加入一定量 2.0 mol/L NaOH(aq),使溶液中的金属离
2
子恰好全部沉淀。下列说法不正确的是
A.该浓硝酸物质的量浓度是 14.0 mol/L
B.加入 NaOH(aq)的体积是 350 ml
C.0.96