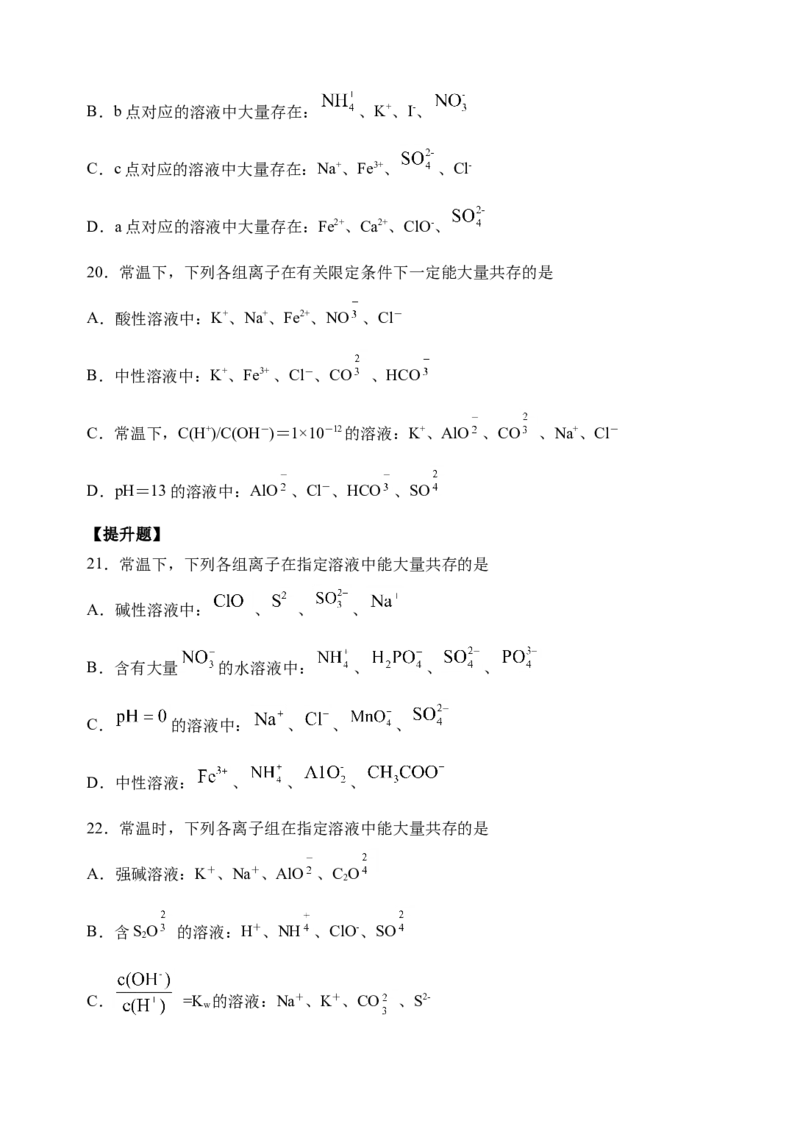文档内容
微专题 06 “四点”破解离子共存
一、离子共存
1.“四点”突破离子能否大量共存
(1)一色——溶液颜色
几种常见离子的颜色
Fe3+:棕黄色, Fe2+ :浅绿色, MnO -:紫红色,Cu2+ :蓝色
4
(2)二性——溶液的酸碱性
①在强酸性溶液中,OH-及弱酸根(如 、 、S2-、CHCOO-等)均不能大量共存。
3
②在强碱性溶液中,H+及弱碱阳离子(如NH +、Al3+、Fe3+等)均不能大量存在。
4
③酸式弱酸根离子(如HCO -、HSO -、HS-等)在强酸性或强碱性溶液中均不能大量存
3 3
在。
(3)三特殊——三种特殊情况
①Al3+与HCO -不能大量共存;
3
Al3++HCO -+HO=Al(OH) ↓+CO2-
3 2 3 3
②“NO -+H+” 组合具有强氧化性,能与S2-、Fe2+、I-、SO 2-等还原性的离子因发生
3 3
氧化还原反应而不能大量共存。
③NH+与CHCOO-、CO2-,Mg2+与HCO -等组合中,虽然两种离子都能水解且水解相
3 3 3
互促进,但总的水解程度仍很小,它们在溶液中能大量存在。
(4) 四反应——四种反应类型
指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
①复分解反应:如Ba2+与SO 2-,NH +与OH-,H+与CHCOO-等。
4 4 3
②氧化还原反应:如Fe3+与I-、S2-,NO (H+)与Fe2+,MnO (H+)与Br-等。
③相互促进和水解反应:如Al3+与HCO -,Al3+与AlO-等。
3 2
④配合反应:如Fe3+与SCN-等。
2.离子共存判断的思考路径
第一步:细审题,抓关键
(1) 注意“一定大量共存”“可能大量共存”还是“不能大量共存”等关键词。(2) 注意“透明溶液”或“澄清溶液”意味着无难溶物或微溶物,但并不意味着溶液无
色。
第二步:分析限制条件
注意题中的限制条件,如溶液颜色、溶液的酸碱性、发生某些反应等。
第三步:抓住反应发生的条件
(1)生成气体、沉淀、弱电解质的复分解反应。
(2)特别注意氧化还原反应。
(3)熟记互促水解反应。
(4)注意几个常见的配合反应。
二、典型精析
1.在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.无色溶液:Ca2+、H+、Cl-、HSO
B.能使pH试纸呈红色的溶液:Na+、NH、I-、NO
C.FeCl 溶液:K+、Na+、SO、AlO
2
D.=0.1 mol·L-1的溶液:Na+、K+、SiO、NO
2.下列各组物质混合后,能使溶液里同时体现NH、Fe3+、Cu2+、Cl-和SO几种离子,且
溶液不发生浑浊的一组是( )
A.CuCl 、NH Cl、Fe (SO )、NaNO
2 4 2 4 3 3
B.(NH )SO 、CuSO 、NaCO、FeCl
4 2 4 4 2 3 3
C.Cu(NO )、NH NO 、FeCl 、HS
3 2 4 3 3 2
D.BaCl 、Cu(NO )、(NH )SO 、Fe(NO )
2 3 2 4 2 4 3 3
3.下列各组离子一定能大量共存的是( )
A.在含有大量AlO的溶液中:NH、Na+、Cl+、H+
B.在强碱溶液中:Na+、K+、CO、NO
C.在pH=12的溶液中:NH、Na+、SO、Cl-
D.在c(H+)=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO
三、对点训练
1.下列关于电解质溶液的正确判断是( )
A.在pH=12的溶液中,K+、Cl-、HCO、Na+可以常量共存
B.在pH=0的溶液中,Na+、NO、SO、K+可以常量共存
C.由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH===B++OH-
D.由0.1 mol·L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+HO HA+
2
OH-
2.能在溶液中大量共存的一组离子是( )
A.NH、Ag+、PO、Cl-
B.Fe3+、H+、I-、HCO
C.K+、Na+、NO、MnO
D.Al3+、Mg2+、SO、CO
3.下列离子组一定能大量共存的是( )
A.甲基橙呈黄色的溶液中:I-、Cl-、NO、Na+
B.石蕊呈蓝色的溶液中:Na+、AlO、NO、HCO
C.含大量Al3+的溶液中:K+、NO、Na+、ClO-
D.含大量OH-的溶液中:CO、Cl-、F-、K+
4.常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Fe2+、NO、SO、Na+
B.由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO
C.c(H+)/c(OH-)=1012的溶液中:NH、Al3+、NO、Cl-
D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO、SCN-
4.下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀
生成的一组是( )
A.Ba2+、NO、NH、Cl-
B.Ca2+、HCO、NH、AlO
C.K+、Ba2+、Cl-、HSO
D.Mg2+、NH、SO、K+
5.在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+ 、Al3+、Cl-、SO
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO
C.含有0.1 mol·L-1 Ca2+溶液中:Na+、K+、CO、 Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、NO、SO
6.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是( )
A.滴加石蕊试液显红色的溶液:Fe3+、NH、Cl-、SCN-B.pH为1的溶液:Cu2+、Na+、Mg2+、NO
C.pH为13的溶液:K+、HCO、Br-、Ba2+
D.所含溶质为NaSO 的溶液:K+、AlO、NO、Al3+
2 4
7.在甲、乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO、OH- 6种离子
中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )
A.Cu2+、H+、Cl- B.CO、OH-、Cl-
C.K+、H+、Cl- D.K+、OH-、CO
8.下列各组离子在溶液中可以大量共存,当溶液呈强酸性时,有气体产生;而当溶液呈
强碱性时,又能生成沉淀。该组离子可能是( )
A.Na+、Cu2+、NO、CO
B.NH、K+、SO、HCO
C.Mg2+、NH、SO、Cl-
D.Fe2+、Na+、SO、NO
9.下列各组离子在指定溶液中一定能大量共存的是( )
A.使甲基橙变红的溶液中:Al3+、NO、Na+、SO
B.由水电离的H+浓度为10-12 mol·L-1的溶液中:Cl-、CO、NH、SO
2
C.加入Al能放出H 的溶液中:Mg2+、Cl-、K+、NO
2
D.无色溶液中:Cl-、Na+、Fe3+、SO
【实战演练】
【基础题】
1.下列各组中的离子,能在溶液中大量共存的是
A.Na+、Cu2+、NO 、SO B.K+、HCO 、Cl-、OH-
C.H+、Mg2+、NO 、Fe2+ D.Ba2+、K+、NO 、SO
2.在某无色透明的溶液中,能大量共存的离子组是
A.Ca2+、 、Cl- B.Cu2+、 、
C.Na+、 、Cl- D. 、Fe3+、Cl-3.下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A. K+、Ba2+、OH−、 B.Ag+、 、Cl-、K+
C.H+、 、Fe2+、Na+ D.Cu2+、 、Br-、OH-
4.下列各组离子,在指定条件下能大量共存的是
A.新制氯水中:Fe3+、K+、Br-、S2-
B.使pH试纸变红的溶液中:Na+、Mg2+、Cl-、SO
C.某无色透明的酸性溶液中:Na+、Cl-、MnO 、NO
D.使紫色石蕊溶液变蓝的溶液中:NH 、Ba2+、CO 、Cl-
5.某混合溶液中含 种离子,物质的量浓度如下表,则 的物质的量浓度以及离子符号
可能为(已知 具有强氧化性)
所含离子
物质的量浓度 ?
A. B. C. D.
6.常温下,下列各组离子在指定溶液中-定能大量共存的是
A. =1012的溶液中:Fe2+、Mg2+、NO 、Cl-
B.澄清透明的溶液中:H+、K+、SO 、NO
C.0.1mol/L的NaHCO 溶液中:Fe3+、K+、Cl-、SO
3D.由水电离产生的c(H+)=1×10-12mol/L的溶液中:K+、A13+、Cl-、SO
7.下列各组离子,能在指定溶液中大量共存的是
A.无色溶液中:Na+、 、 、Cl-
B.能使紫色石蕊试剂变红的溶液中:OH-、K+、Ba2+、Na+
C.透明的酸性溶液中:Fe3+、Mg2+、Cl-、
D.pH=1的溶液中: 、Fe2+、Cl-、
8.某无色溶液能与铝反应生成氢气,则溶液中可能大量共存的离子组为
A.H+、Ba2+、Mg2+、NO B.Cl-、Cu2+、Mg2+、SO
C.OH-、NO 、Ba2+、Cl- D.H+、Fe3+、Cl-、MnO
9.下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol•L-1NaCO 溶液中: K+、Na+、NO 、Cl-
2 3
B.0.1 mol•L-1FeCl 溶液中: Fe2+、I-、SCN-、SO
3
C.使酚酞变红色的溶液中: Na+、Cu2+、HCO 、NO
D.0.1 mol•L-1NaSO 溶液: H+、Ca2+、Cl-、SO
2 3
10.常温下,下列各组离子一定能在指定溶液中大量共存的是
A.强酸性溶液中: 、 、 、
B.使酚酞变红色的溶液中: 、 、 、
C.水溶液中: 、 、 、D.无色透明的溶液中: 、 、 、
【能力题】
11.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中: 、 、 、
B. 的溶液中: 、 、 、
C.滴入酚酞呈红色的溶液中: 、 、 、
D.水电离出的 的溶液中: 、 、 、
12.下列关于离子共存或离子方程式书写正确的是
A.某无色溶液中可能大量存在:H+、NH 、Cl-、Cr O
2
B.常温下,c(NH )=c(Cl-)的NH Cl和NH •H O的混合溶液中能大量存在:Fe3+、Cl-、
4 3 2
NO 、Al3+
C.向酸性KMnO 溶液中滴加HO:2MnO +5H O+6H+=2Mn2++5O ↑+8H O
4 2 2 2 2 2 2
D.用惰性电极电解MgCl 水溶液:2Cl-+2H O 2OH-+Cl↑+H ↑
2 2 2 2
13.下列各组离子在给定条件下,因发生配合反应而不能大量共存的一组是
A. 的溶液中: 、 、 、
B.含大量 的溶液: 、 、 、
C.含有大量 的溶液: 、 、 、D.溶解少量 气体的溶液: 、 、 、
14.常温下,下列各组离子在指定溶液中能大量共存的是
A. 的溶液中:Na+、K+、 、
B.c(Fe2+)=0.5mol·L-1的溶液中:H+、Mg2+、 、ClO—
C.无色溶液中:Na+、Fe3+、 、
D.能使酚酞变红的溶液中:Al3+、 、Cl—、
15.某溶液由Na+、Ba2+、Al3+、AlO 、CrO 、CO 、SO 中的若干种组成。取适量该
溶液进行如下实验:①加入过量盐酸有气体生成并得到无色溶液;②在①所得溶液中再
加入过量NH HCO 溶液,有气体生成并析出白色沉淀甲;③在②所得溶液中加入过量
4 3
Ba(OH) 溶液也有气体生成并产生白色沉淀乙,则原溶液中一定存在的离子是
2
A.Na+、AlO 、CrO 、CO B.Na+、AlO 、CO
C.Na+、AlO 、CO 、SO D.Na+、Ba2+、AlO 、CO
16.向 、 的混合溶液中逐滴加入稀盐酸,生成气体的量随 的量的
变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
A. 点对应的溶液中: 、 、 、B. 点对应的溶液中: 、 、 、
C. 点对应的溶液中: 、 、 、
D. 点对应的溶液中: 、 、 、
17.常温下,下列各组离子在指定溶液中可能大量共存的是
A. 的溶液中: 、 、 、
B. 的溶液中: 、 、 、
C.使酚酞变红色的溶液: 、 、 、
D.由水电离的 的溶液中: 、 、 、
18.常温下,关于离子反应,下列说法正确的是
A.在c(H)∶c(OH)=10-10的溶液中,Al3、 Ba2 、Cl不能大量共存,
B.在1 mol·L-1NaNO 溶液中能大量共存H 、Fe2 、SCN
3
C.向NH HCO 溶液中加入过量NaOH溶液,并加热:NH +OH =NH+HO
4 3 3 2
D.向1L0.5 mol·L-1FeBr 溶液中通入0.1molCl :2Fe2+4Br+3Cl = 2Fe3+2Br +6Cl
2 2 2 2
19.在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存的说法
中正确的是
A.d点对应的溶液中大量存在:Na+、K+、S2-、B.b点对应的溶液中大量存在: 、K+、I-、
C.c点对应的溶液中大量存在:Na+、Fe3+、 、Cl-
D.a点对应的溶液中大量存在:Fe2+、Ca2+、ClO-、
20.常温下,下列各组离子在有关限定条件下一定能大量共存的是
A.酸性溶液中:K+、Na+、Fe2+、NO 、Cl-
B.中性溶液中:K+、Fe3+ 、Cl-、CO 、HCO
C.常温下,C(H+)/C(OH-)=1×10-12的溶液:K+、AlO 、CO 、Na+、Cl-
D.pH=13的溶液中:AlO 、Cl-、HCO 、SO
【提升题】
21.常温下,下列各组离子在指定溶液中能大量共存的是
A.碱性溶液中: 、 、 、
B.含有大量 的水溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.中性溶液: 、 、 、
22.常温时,下列各离子组在指定溶液中能大量共存的是
A.强碱溶液:K+、Na+、AlO 、C O
2
B.含SO 的溶液:H+、NH 、ClO-、SO
2
C. =K 的溶液:Na+、K+、CO 、S2-
wD.能与Al反应放出H 的溶液:Na+、Cu2+、NO 、Cl-
2
23.在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是
①K+、ClO-、NO -、S2-
3
②K+、Fe2+、I-、SO 2-
4
③Na+、Cl-、NO -、SO 2-
3 4
④Na+、Ca2+、Cl-、HCO -
3
⑤K+、Ba2+、Cl-、NO -
3
A.①③ B.③⑤ C.③④ D.②⑤
24.某溶液中有S0 2-、CO2-、NH +、M,且SO 2-、CO2-、NH +的物质的量之比为1:
4 3 4 4 3 4
2:4,则离子M可能是
A.H+ B.K+ C.CI- D.Ba2+
25.下列说法正确的是
A.标准状况下,将1.12 L Cl 溶于水,反应中转移0.05 mol电子
2
B.向NH Al(SO ) 稀溶液中逐滴加入过量Ba(OH) 溶液,发生反应的离子方程NH ++Al3+
4 4 2 2 4
+2SO2—+2Ba2++5OH—=2BaSO↓+AlO —+2H O+NH ·H O
4 4 2 2 3 2
C.常温下,水电离的c(H+)为1.0×10-13 mol·L-1的溶液中,Fe2+、Cl—、Na+、NO —可能大
3
量共存
D.麦芽糖溶液中:SO 2—、MnO —、K+、H+可以大量共存
4 4
26.常温下,取铝土矿(含有A1 O、FeO、Fe O、SiO 等物质) 用硫酸浸出后的溶液,分
2 3 2 3 2
别向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是
A.加入过量NaOH 溶液: Na+、A1O -、OH-、SO 2-
2 4
B.加入过量氨水: NH +、A13+、OH-、SO 2-
4 4
C.通入过量SO : Fe2+、H+、SO 2-、SO 2-
2 3 4
D.加入过量NaClO溶液: Fe2+、Na+、C1O-、SO 2-
4
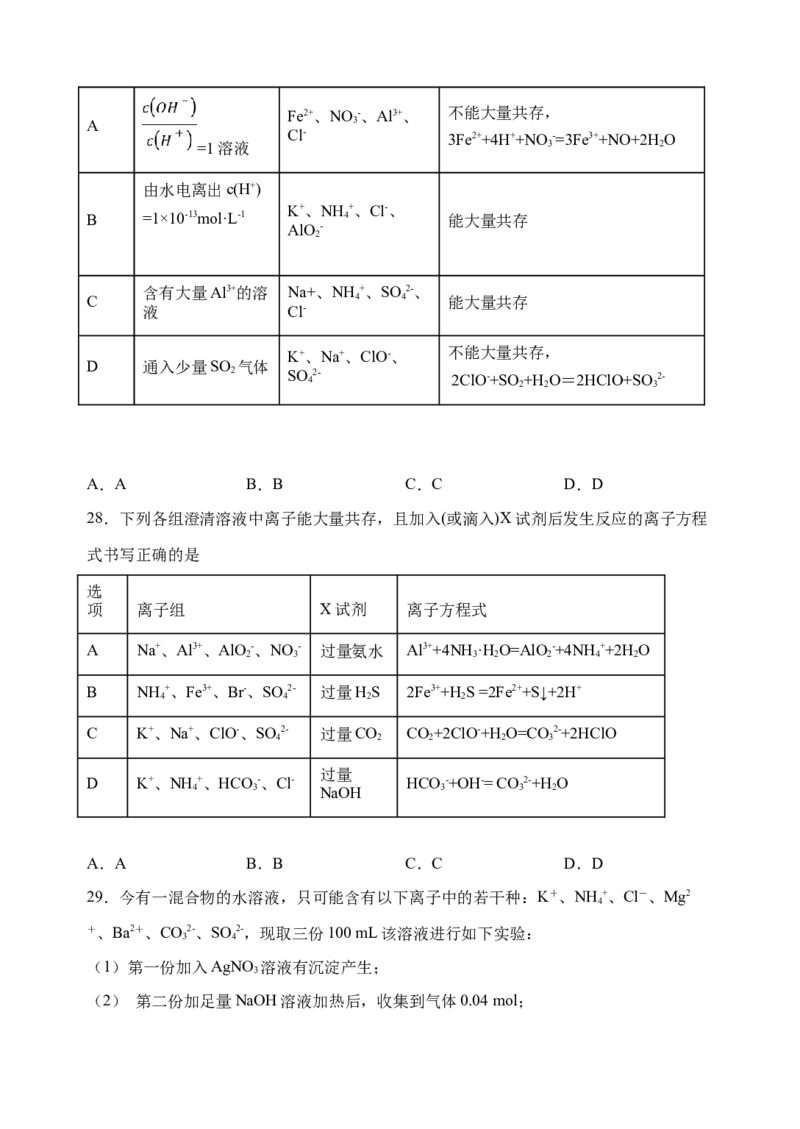
27.在给定条件下,下列离子组的离子共存判断及反应的离子方程式均正确的是
选项 条件 离子组 离子共存判断及的离子方程式Fe2+、NO -、Al3+、 不能大量共存,
A 3
Cl- 3Fe2++4H++NO-=3Fe3++NO+2HO
=1溶液 3 2
由水电离出c(H+)
K+、NH +、Cl-、
B =1×10-13mol·L-1 4 能大量共存
AlO-
2
含有大量Al3+的溶 Na+、NH +、SO 2-、
C 4 4 能大量共存
液 Cl-
K+、Na+、ClO-、 不能大量共存,
D 通入少量SO 气体
2 SO 4 2- 2ClO-+SO 2 +H 2 O=2HClO+SO 3 2-
A.A B.B C.C D.D
28.下列各组澄清溶液中离子能大量共存,且加入(或滴入)X试剂后发生反应的离子方程
式书写正确的是
选
项 离子组 X试剂 离子方程式
A Na+、Al3+、AlO-、NO - 过量氨水 Al3++4NH·H O=AlO-+4NH++2H O
2 3 3 2 2 4 2
B NH +、Fe3+、Br-、SO 2- 过量HS 2Fe3++H S =2Fe2++S↓+2H+
4 4 2 2
C K+、Na+、ClO-、SO 2- 过量CO CO+2ClO-+H O=CO2-+2HClO
4 2 2 2 3
过量
D K+、NH +、HCO -、Cl- HCO -+OH-= CO2-+H O
4 3 NaOH 3 3 2
A.A B.B C.C D.D
29.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH +、Cl-、Mg2
4
+、Ba2+、CO2-、SO 2-,现取三份100 mL该溶液进行如下实验:
3 4
(1)第一份加入AgNO 溶液有沉淀产生;
3
(2) 第二份加足量NaOH溶液加热后,收集到气体0.04 mol;(3)第三份加足量BaCl 溶液后,干燥后得沉淀6.27 g,经足量盐酸洗涤、干燥后,沉
2
淀质量为2.33 g。根据上述实验,以下推测正确的是( )
①K+一定存在; ②100 mL溶液中含0.01 molCO 2-; ③Cl-可能存在;④Ba2+一定不
3
存 在;⑤M g2+可能存在
A.③④ B.③④⑤
C.①② D.①③④
30.向HCl、AlCl 混合溶液中逐滴加入NaOH溶液,生成沉淀的量随NaOH溶液加入量
3
的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
A.M点对应的溶液中:K+、Fe2+、SO 2-、NO -
4 3
B.N点对应的溶液中:K+、NH +、Cl-、CO2-
4 3
C.S点对应的溶液中:Na+、SO 2-、HCO -、NO -
4 3 3
D.R点对应的溶液中:Na+、SO 2-、Cl-、NO -
4 3