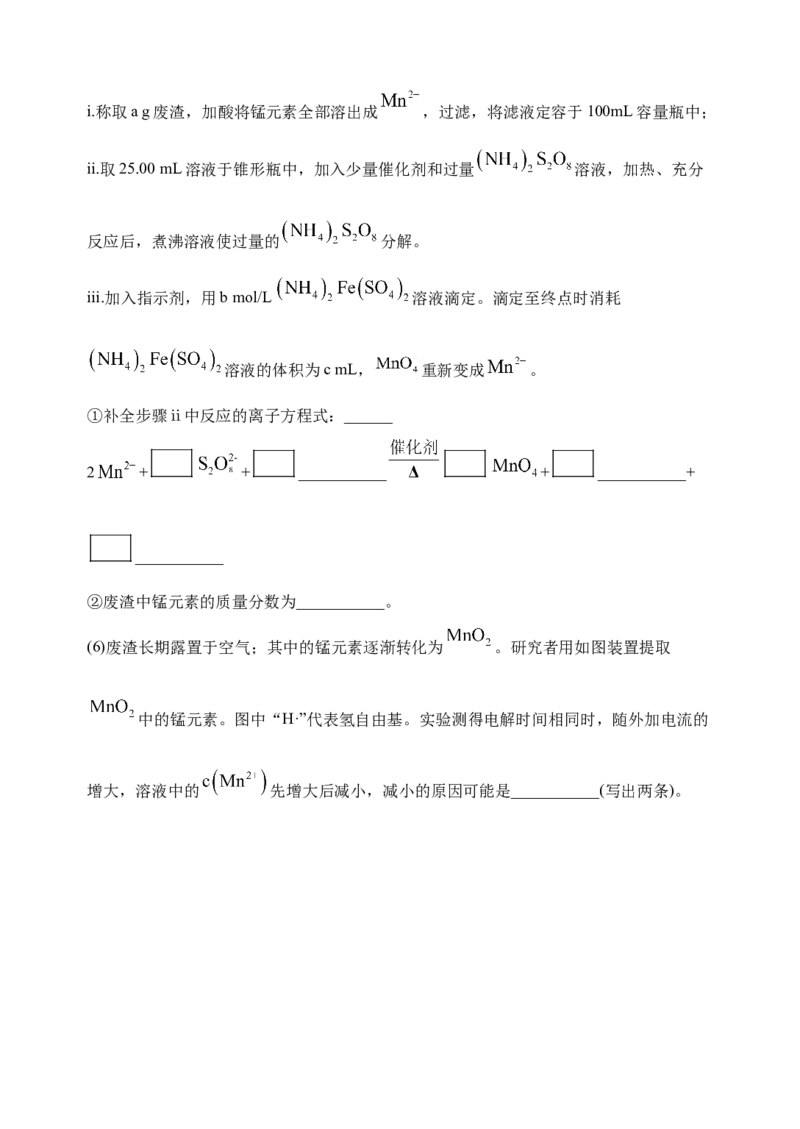文档内容
微专题18 金属及其化合物制备流程(Mn)
锰:元素符号Mn,原子序数25,原子量54.94,外围电子排布3d54s2,位于第四周期ⅦB
族。主要化合价+2、+4、+6、+7。
一、物理性质:
银白色金属,硬而脆,密度7.20克/厘米3,熔点1244.3℃,沸点1962℃。固态时有四种
同素异形体,常温下为α锰。
二、化学性质:
在空气中易氧化生成褐色氧化物覆盖层。燃烧时生成四氧化三锰。红热时与水反应生成
四氧化三锰和氢。溶于稀盐酸、稀硫酸生成二价锰盐。高温时跟卤素、硫、磷、碳、氮
直接化合。用于制合金,少量锰能改善钢的抗冲击性能,锰铁用作炼钢过程的脱氧、脱
硫添加剂。
三、用途:
还用于冶炼铝合金、镁合金。1774年瑞典人甘恩用木炭跟软锰矿共热得到锰。主要矿物
有软锰矿MnO ·xH O、黑锰矿MnO,最近发现大洋底部有大量锰结核矿。在地壳中丰
2 2 3 4
度
为0.1%。用铝还原软锰矿制得。
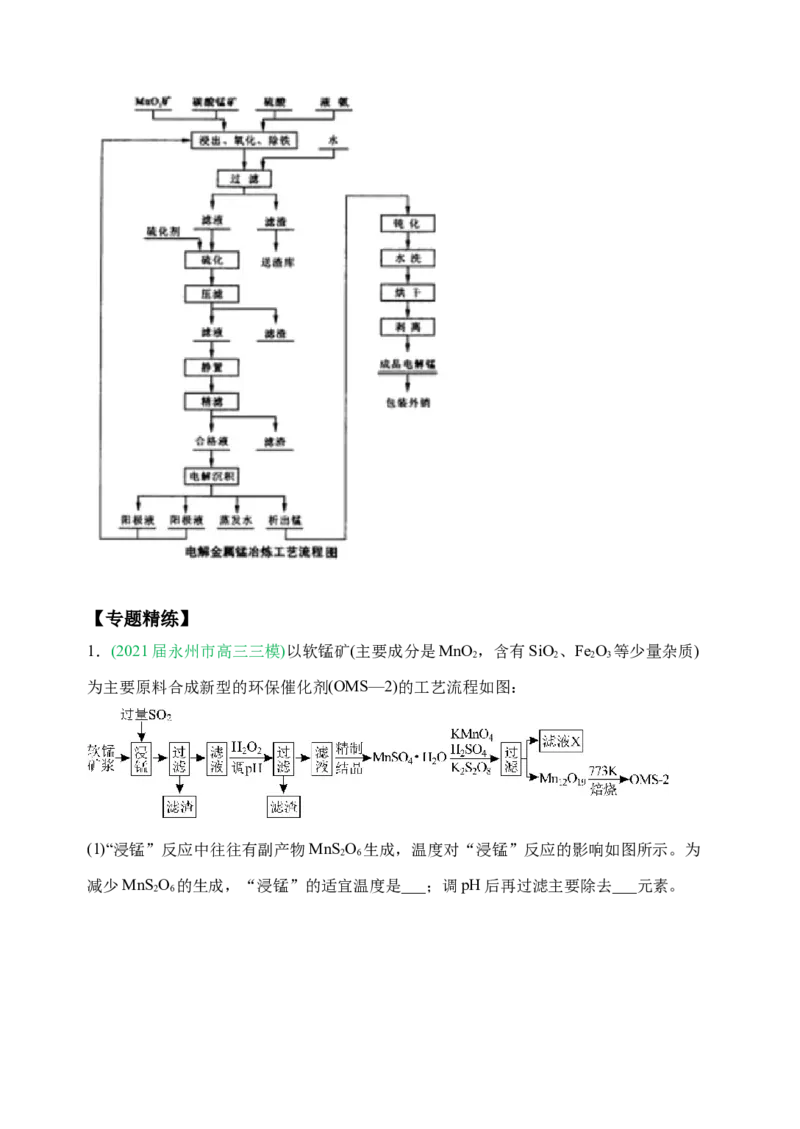
四、锰的提炼工艺
金属锰的提炼方式主要有热法(火法)和电解法(湿法)两种。热法生产的金属锰纯度不超过
95~98%,并且耗能高,污染严重,已经逐渐被淘汰了,而电解法生产的金属锰纯度可
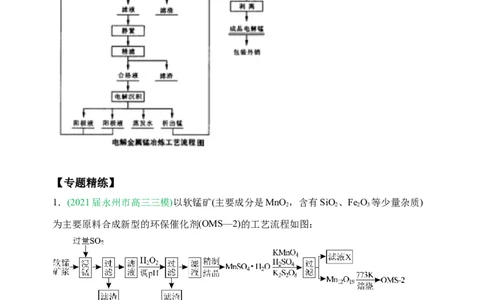
达99.7~99.9%以上,污染也相对较小,现在已成为了金属锰生产的主要方式。【专题精练】
1.(2021届永州市高三三模)以软锰矿(主要成分是MnO ,含有SiO、Fe O 等少量杂质)
2 2 2 3
为主要原料合成新型的环保催化剂(OMS—2)的工艺流程如图:
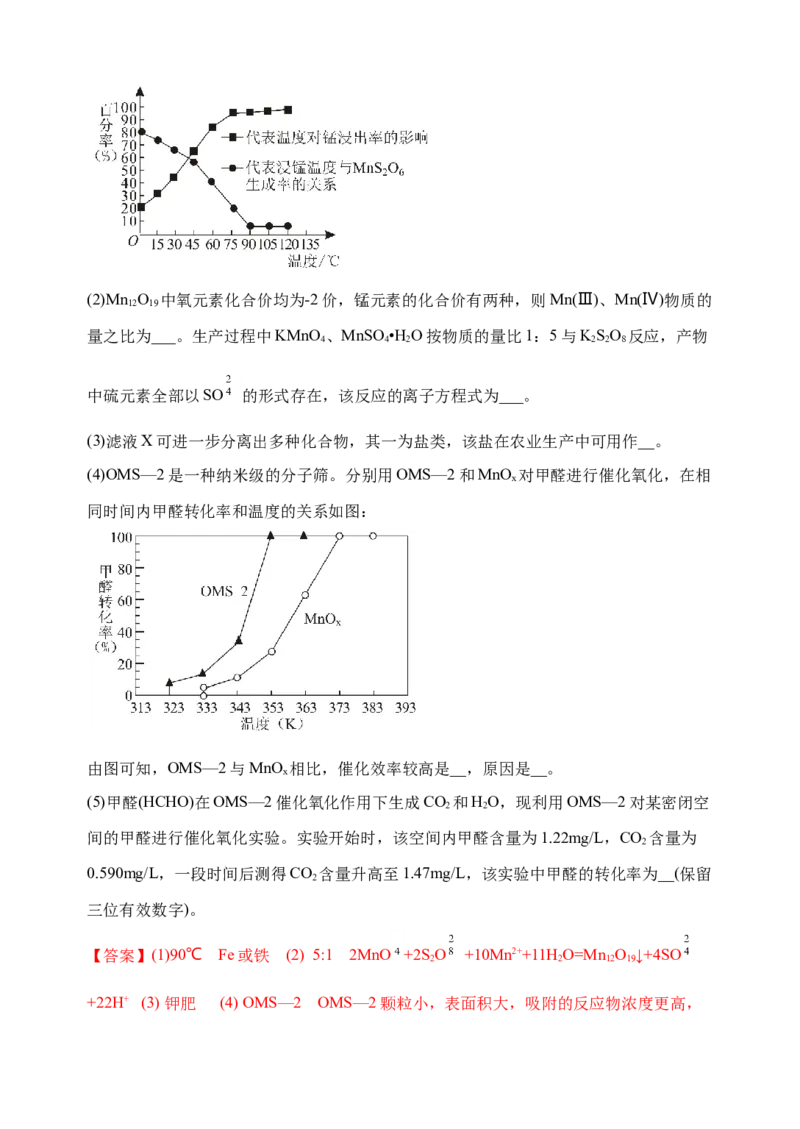
(1)“浸锰”反应中往往有副产物MnS O 生成,温度对“浸锰”反应的影响如图所示。为
2 6
减少MnS O 的生成,“浸锰”的适宜温度是___;调pH后再过滤主要除去___元素。
2 6(2)Mn O 中氧元素化合价均为-2价,锰元素的化合价有两种,则Mn(Ⅲ)、Mn(Ⅳ)物质的
12 19
量之比为___。生产过程中KMnO 、MnSO •H O按物质的量比1:5与KSO 反应,产物
4 4 2 2 2 8
中硫元素全部以SO 的形式存在,该反应的离子方程式为___。
(3)滤液X可进一步分离出多种化合物,其一为盐类,该盐在农业生产中可用作__。
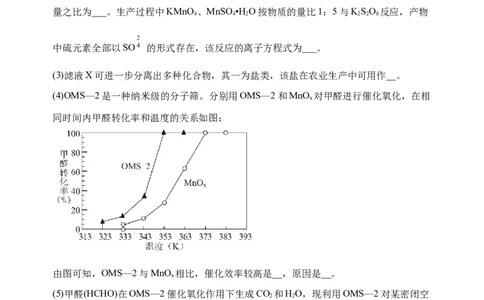
(4)OMS—2是一种纳米级的分子筛。分别用OMS—2和MnO 对甲醛进行催化氧化,在相
x
同时间内甲醛转化率和温度的关系如图:
由图可知,OMS—2与MnO 相比,催化效率较高是__,原因是__。
x
(5)甲醛(HCHO)在OMS—2催化氧化作用下生成CO 和HO,现利用OMS—2对某密闭空
2 2
间的甲醛进行催化氧化实验。实验开始时,该空间内甲醛含量为1.22mg/L,CO 含量为
2
0.590mg/L,一段时间后测得CO 含量升高至1.47mg/L,该实验中甲醛的转化率为__(保留
2
三位有效数字)。
【答案】(1)90℃ Fe或铁 (2) 5:1 2MnO +2S O +10Mn2++11H O=Mn O ↓+4SO
2 2 12 19
+22H+ (3) 钾肥 (4) OMS—2 OMS—2颗粒小,表面积大,吸附的反应物浓度更高,反应速率更快 49.2%
【解析】
(1)“浸锰”反应中往往有副产物MnS O 生成,温度越高MnS O 的生成率越低,“浸锰”
2 6 2 6
的适宜温度是90℃;软锰矿和黄铁矿加硫酸浸出,滤液A中含有Fe2+,加入HO 将
2 2
Fe2+氧化为Fe3+,调节pH将铁元素除去得到MnSO ·H O;
4 2
(2)Mn O 中氧元素化合价均为-2价,设Mn (Ⅲ)为x个,则Mn (Ⅳ)为12-x,根据化合物
12 19
中元素化合价代数和为0,即得3x+4(12-x)=2×19,x为10,Mn (Ⅳ)为2,Mn (Ⅲ)、Mn
(Ⅳ) 物质的量之比为5:1;根据题意生产过程中的原料KMnO 、KSO、MnSO ·H O按物
4 2 2 8 4 2
质的量比1:1:5反应,产物中硫元素全部以SO 2-的形式存在,该反应的离子方程式为
4
2MnO +2S O +10Mn2++11H O=Mn O ↓+4SO +22H+;
2 2 12 19
(3)根据反应方程式可知,溶液B中含有的KSO 、HSO ,该工艺中循环使用的物质化学
2 4 2 4
式是HSO ,KSO 在农业生产中可用作钾肥;
2 4 2 4
(4)由图像可以看出,相同温度下,OMS-2作催化剂时,因纳米级OMS-2 比MnO 表面积
x
大,吸附的反应物浓度更高,反应速率更快,故OMS-2与MnO 相比,催化效率较高是
x
OMS-2;
(5)设体积为VL,CO 含量由0.590mg/L升高至1.47mg/L,CO 含量增多0.88mg/L,反应
2 2
生成的CO 的物质的量为 ,根据原子个数守恒,参与反
2
应的甲醛的物质的量为 ,故该实验中甲醛的转化率为
=49.2%。2.(2021届江苏省高三调研)工业上常利用软锰矿浆(主要成分是MnO ,还含有硅、铁和
2
少量重金属镍的化合物等杂质)制备MnSO 溶液,并以MnSO 溶液为原料制取单质锰和四
4 4
氧化三锰。
(1)MnSO 溶液的制备:
4
①还原:以稀硫酸作介质,纤维素[(C H O)]还原MnO 时,发生反应的化学方程式为
6 10 5 n 2
______。
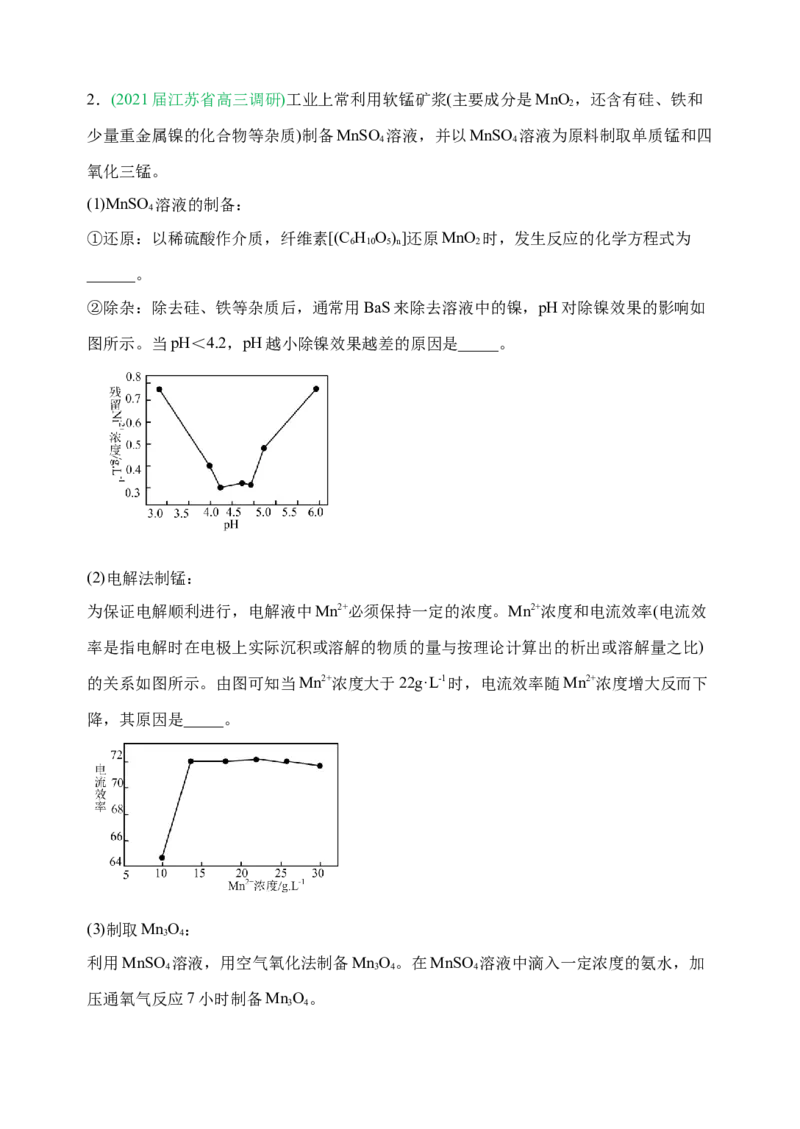
②除杂:除去硅、铁等杂质后,通常用BaS来除去溶液中的镍,pH对除镍效果的影响如
图所示。当pH<4.2,pH越小除镍效果越差的原因是_____。
(2)电解法制锰:
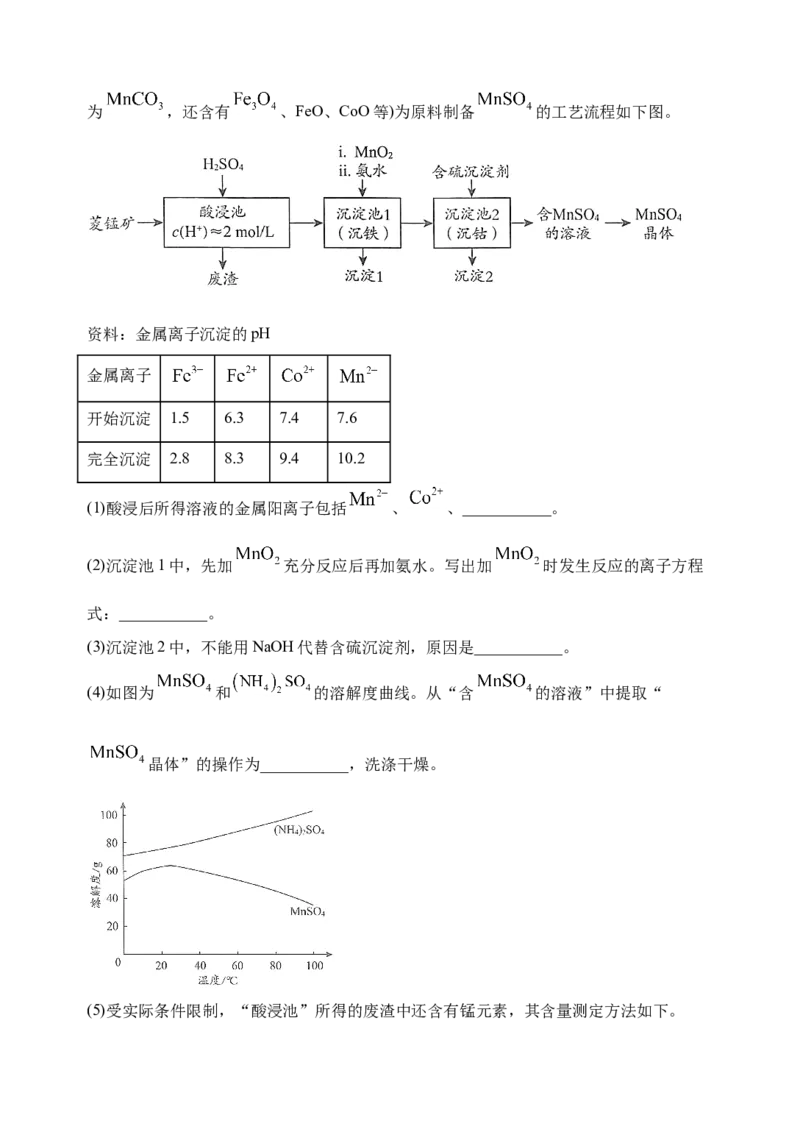
为保证电解顺利进行,电解液中Mn2+必须保持一定的浓度。Mn2+浓度和电流效率(电流效
率是指电解时在电极上实际沉积或溶解的物质的量与按理论计算出的析出或溶解量之比)
的关系如图所示。由图可知当Mn2+浓度大于22g·L-1时,电流效率随Mn2+浓度增大反而下
降,其原因是_____。
(3)制取MnO:
3 4
利用MnSO 溶液,用空气氧化法制备MnO。在MnSO 溶液中滴入一定浓度的氨水,加
4 3 4 4
压通氧气反应7小时制备MnO。
3 4①写出上述反应的离子方程式:_____。
②MnO 的含量与反应温度的关系如图所示。随着反应温度的升高,产物中MnO 的含
3 4 3 4
量的上升趋势呈现先快后慢的原因是_____。
【答案】(1) ①12nMnO +(C H O)+12nH SO =12nMnSO +6nCO ↑+17nH O ② pH越小,
2 6 10 5 n 2 4 4 2 2
c(H+)增大,硫化钡会与H+反应产生硫化氢气体 (2) Mn2+浓度增大,Mn2+扩散至阳极失
电子放电 (3) ①6Mn2++12NH∙HO+O=2Mn O↓+12NH +6H O ② 温度不太高的情况
3 2 2 3 4 2
下(反应主要受动力学影响),温度升高反应速率加快,MnO 的含量增大;温度较高的情
3 4
况下(反应受热力学影响),此氧化反应为放热反应,温度升高反应逆向移动
【解析】
(1)①纤维素[(C H O)]具有还原性,MnO 具有氧化性,二者发生氧化还原反应,反应的
6 10 5 n 2
化学方程式为12nMnO +(C H O)+12nH SO =12nMnSO +6nCO ↑+17nH O,故答案为:
2 6 10 5 n 2 4 4 2 2
12nMnO +(C H O)+12nH SO =12nMnSO +6nCO ↑+17nH O;
2 6 10 5 n 2 4 4 2 2
②pH过低,H+会与硫化钡反应产生硫化氢气体,根据图中的数据知道,当pH<4.2的时
候,镍离子随pH的减小而残留率增加,故答案为:pH越小,c(H+)增大,硫化钡会与
H+反应产生硫化氢气体;
(2)电解时,用惰性电极电解,阳极发生氧化反应,应该是水电离出的氢氧根离子放电,
当Mn2+浓度大于22g·L-1时,Mn2+扩散至阳极失电子放电,电流效率随Mn2+浓度增大反而
下降,故答案为:Mn2+浓度增大,Mn2+扩散至阳极失电子放电;
(3)①Mn2+在氨水存在下被氧气氧化生成MnO,反应的离子方程式为:6Mn2+
3 4+12NH∙HO+O=2Mn O↓+12NH +6H O,故答案为:6Mn2+
3 2 2 3 4 2
+12NH∙HO+O=2Mn O↓+12NH +6H O;
3 2 2 3 4 2
②由图可知,曲线斜率逐渐减小,即随着反应温度的升高,产物中MnO 的含量的上升
3 4
趋势呈现先快后慢,原因是:温度不太高的情况下(反应主要受动力学影响),温度升高反
应速率加快,MnO 的含量增大;温度较高的情况下(反应受热力学影响),此氧化反应为
3 4
放热反应,温度升高反应逆向移动。
3.(2021届毕节市高三4月第二次诊断)某化工厂利用软锰矿(主要成分为MnO ,另含有
2
少量Fe O、CaO、CuO、SiO 等杂质)脱除燃煤尾气中的SO ,同时制得电池材料MnO
2 3 2 2 2.
工艺流程如下:
(1)滤渣1的成分是___________(填化学式),提高软锰矿酸浸速率的措施有
___________(任答一条)。
(2)写出脱硫过程中二氧化锰转化为硫酸锰的化学反应方程式___________。
(3)加入碳酸锰的作用___________。
(4)写出高锰酸钾与硫酸锰发生反应的离子方程式___________。
(5)实验室检验钾离子的操作方法是_____
(6)已知25℃时K [Fe(OH) ]=4.0×10-38,欲使铁离子沉淀完全,应调节溶液pH不低于
sp 3
___________。(设 =a,结果用含a的代数式表示)。
【答案】(1)SiO 将矿石粉碎(或适当升高温度、适当增大硫酸的浓度、搅拌等) (2)
2MnO +SO=MnSO (3) 调节溶液的pH,除去溶液中Fe3+ (4) 2 +3 Mn2++2H O=
2 2 4 2
5MnO +4 H+ (5) 用洁净的铂丝蘸取待测液在酒精灯火焰上灼烧,透过蓝色的钴玻璃观察
2
到紫色火焰,证明含有钾离子 (6) 3- lga
【解析】
(1)根据上述分析,滤渣1的成分是二氧化硅,提高软锰矿酸浸速率的措施有将矿石粉碎、
适当升高温度、适当增大硫酸的浓度、搅拌等,故答案为:SiO;将矿石粉碎(或适当升
2
高温度、适当增大硫酸的浓度、搅拌等);
(2)脱硫过程中二氧化锰与二氧化硫发生氧化还原反应转化为硫酸锰,反应的化学反应方
程式为MnO +SO=MnSO ,故答案为:MnO +SO=MnSO ;
2 2 4 2 2 4
(3)根据流程图,加入碳酸锰的目的是调节溶液的pH,除去溶液中Fe3+,形成氢氧化铁沉
淀,故答案为:调节溶液的pH,除去溶液中Fe3+;
(4)高锰酸钾与硫酸锰发生氧化还原反应生成硫酸钾和二氧化锰,反应的离子方程式为2
+3 Mn2++2H O= 5MnO+4 H+,故答案为:2 +3 Mn2++2H O= 5MnO+4 H+;
2 2 2 2
(5)实验室常用焰色反应检验钾离子,操作方法是:用洁净的铂丝蘸取待测液在酒精灯火
焰上灼烧,透过蓝色的钴玻璃观察到紫色火焰,证明含有钾离子,故答案为:用洁净的
铂丝蘸取待测液在酒精灯火焰上灼烧,透过蓝色的钴玻璃观察到紫色火焰,证明含有钾
离子;
(6)K [Fe(OH) ]=c(Fe3+)•c3(OH-)=4.0×10-38,当c(Fe3+)=1×10-5mol/L,铁离子沉淀完全,此时
sp 3
c(OH-)= = ×10-11mol/L,则c(H+)= mol/L = mol/L,
pH=-lg =3- lg =3- lga,故答案为:3- lga。
4.(2021届北京市海淀区高三一模) 是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有 、FeO、CoO等)为原料制备 的工艺流程如下图。
资料:金属离子沉淀的pH
金属离子
开始沉淀 1.5 6.3 7.4 7.6
完全沉淀 2.8 8.3 9.4 10.2
(1)酸浸后所得溶液的金属阳离子包括 、 、___________。
(2)沉淀池1中,先加 充分反应后再加氨水。写出加 时发生反应的离子方程
式:___________。
(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是___________。
(4)如图为 和 的溶解度曲线。从“含 的溶液”中提取“
晶体”的操作为___________,洗涤干燥。
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。i.称取a g废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于100mL容量瓶中;
ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分
反应后,煮沸溶液使过量的 分解。
iii.加入指示剂,用b mol/L 溶液滴定。滴定至终点时消耗
溶液的体积为c mL, 重新变成 。
①补全步骤ⅱ中反应的离子方程式:______
2 + + ___________ + ___________+
___________
②废渣中锰元素的质量分数为___________。
(6)废渣长期露置于空气;其中的锰元素逐渐转化为 。研究者用如图装置提取
中的锰元素。图中“H·”代表氢自由基。实验测得电解时间相同时,随外加电流的
增大,溶液中的 先增大后减小,减小的原因可能是___________(写出两条)。【答案】(1) (2) (3) 因为NaOH
能与锰离子反应生成氢氧化锰沉淀而使锰元素损失 (4) 蒸发浓缩、趁热过滤 (5) ①
② (6) 锰离子浓度增加,
在阴极放电、锰离子水解生成氢氧化锰沉淀
【解析】
(1)酸浸后的溶液中含有的金属离子除了锰离子、钴离子外还含有 ,故填
;
(2)加入二氧化锰的目的是将亚铁离子氧化,其反应为
,故填
;
(3)不能用NaOH代替含硫沉淀剂,因为NaOH能与锰离子反应生成氢氧化锰沉淀而使锰
元素损失,故填因为NaOH能与锰离子反应生成氢氧化锰沉淀而使锰元素损失;
(4)从溶解度曲线中可以看出,硫酸锰的溶解度随温度升高而降低,可以采用蒸发浓缩,
趁热过滤的方法分离,故填蒸发浓缩、趁热过滤;(5)①可以通过氧化还原反应的规律进行配平,其反应为
,故填
;
②滴定时发生反应 , 设25.00ml溶液中所含
锰离子物质的量为n,
,
则n= mol,则100ml溶液中所含锰离子为: 4n= mol,
,即锰元素的质量分数为
,故填 ;
(6)图中阳极反应为 ,阴极反应为 ,
,随着外加电流的增大,溶液中 浓度增加,开始
在阴极放电,浓度降低,另一原因可能为氢离子浓度降低锰离子水解,故填锰离子浓度
增加,在阴极放电、锰离子水解生成氢氧化锰沉淀。
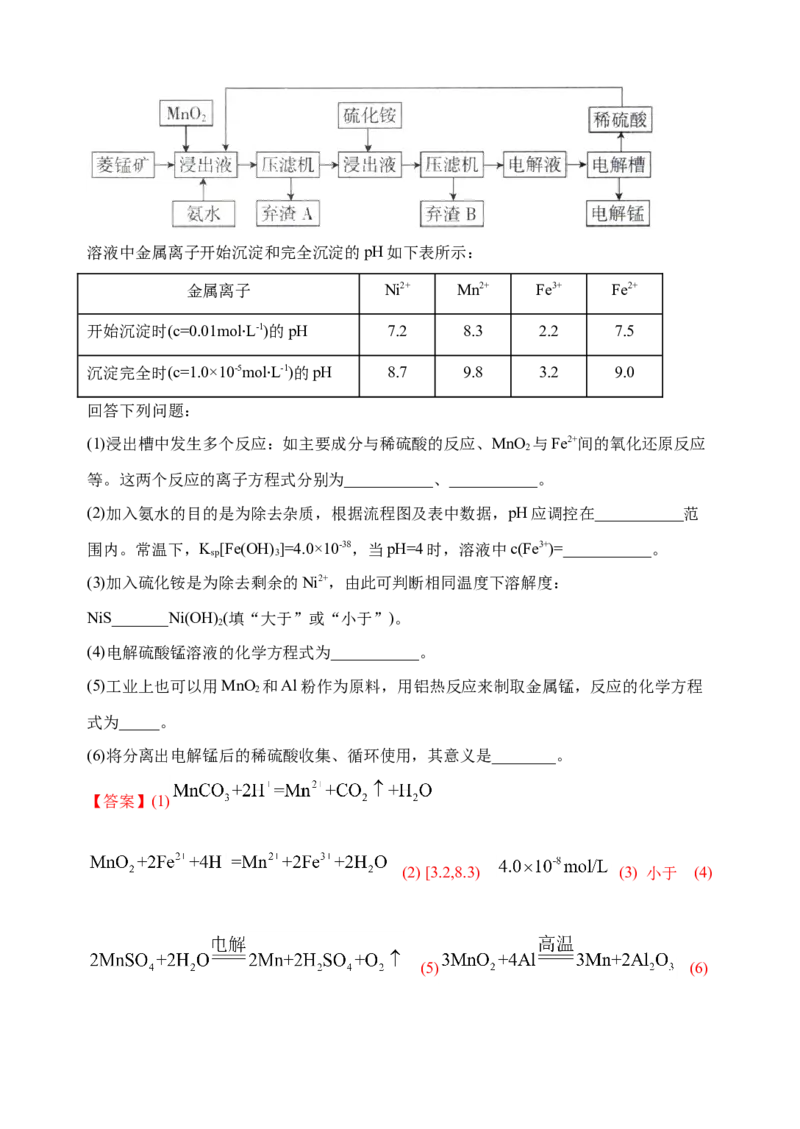
5.(2021届桂林市高三调研)工业上以菱锰矿(主要成分是MnCO ,还含有Fe2+、Ni2+等)为
3
原料制备电解锰的工艺流程如图所示。溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Mn2+ Fe3+ Fe2+
开始沉淀时(c=0.01mol‧L-1)的pH 7.2 8.3 2.2 7.5
沉淀完全时(c=1.0×10-5mol‧L-1)的pH 8.7 9.8 3.2 9.0
回答下列问题:
(1)浸出槽中发生多个反应:如主要成分与稀硫酸的反应、MnO 与Fe2+间的氧化还原反应
2
等。这两个反应的离子方程式分别为___________、___________。
(2)加入氨水的目的是为除去杂质,根据流程图及表中数据,pH应调控在___________范
围内。常温下,K [Fe(OH) ]=4.0×10-38,当pH=4时,溶液中c(Fe3+)=___________。
sp 3
(3)加入硫化铵是为除去剩余的Ni2+,由此可判断相同温度下溶解度:
NiS_______Ni(OH)(填“大于”或“小于”)。
2
(4)电解硫酸锰溶液的化学方程式为___________。
(5)工业上也可以用MnO 和Al粉作为原料,用铝热反应来制取金属锰,反应的化学方程
2
式为_____。
(6)将分离出电解锰后的稀硫酸收集、循环使用,其意义是________。
【答案】(1)
(2) [3.2,8.3) (3) 小于 (4)
(5) (6)节约成本,提高原料的利用率
【解析】
(1)主要成分 与硫酸的反应为复分解反应; 、 在酸性条件下的反应为
氧化还原反应,其反应分别为 、
,故填 、
;
(2)加入氨水的目的是为了除去 ,根据表中数据, 完全沉淀时的pH为3.2,
开始沉淀的pH分别为8.3,在不影响Mn元素的情况下,除去 的最佳pH控制
在3.2≤pH<8.3;pH=4时, ,根据 ,可
知 = = ,故填[3.2,8.3)、
;
(3)加入氨水时没能除去 ,加入硫化钠除去了剩余的 ,说明 比 更
难溶,即相同温度下, 的溶解度小于 ,故填小于;
(4)电解硫酸锰生成锰单质和硫酸,其反应为 ,故填 ;
(5) 与Al反应属于置换反应,其反应为 ,故填
;
(6)将电解锰后的硫酸收集循环使用的意义在于节约成本,提高原料的利用率,故填节约
成本,提高原料的利用率。
化学式MnO2,式量86.94。钢灰色块状固体或黑色粉末。天然产的称软锰矿。密度5.026
克/厘米3。不溶于水。溶于浓盐酸生成MnCl2和Cl2。在浓硫酸中放出氧气并生成硫酸锰。
与氯酸钾、氢氧化钾共熔生成锰酸钾。在酸性介质中呈强氧化性。用作催化剂,氧化剂,
制干电池,还用于炼钢、制玻璃、陶瓷、热敏电阻。将硝酸亚锰加热到200℃制得。也可
从天然软锰矿制取。
【硫酸锰】化学式MnSO4·4H2O,式量223.08。微红色细小晶体。密度2.107克/厘米3。
在干燥空气中风化。280℃失去结晶水成白色无水物。溶于水。用于制锰肥、电解锰、油
漆催干剂。由二氧化锰跟硫酸反应制得。