文档内容
微专题33 化学工艺流程题-----物质的分离与提纯
化学工艺流程题是将化工生产中的生产流程用框图形式表示出来,并根据生产流程中有
关的化学知识步步设问,是无机框图的创新。它以现代工业生产为基础,与化工生产成
本、产品提纯、环境保护等相融合,考查物质的制备、检验、分离提纯等基本实验原理
在化工生产中的实际应用,要求考生依据流程图分析原理,紧扣信息,抓住关键、准确
答题。这类试题具有较强的实用性和综合性,是高考化学命题的常考题型。
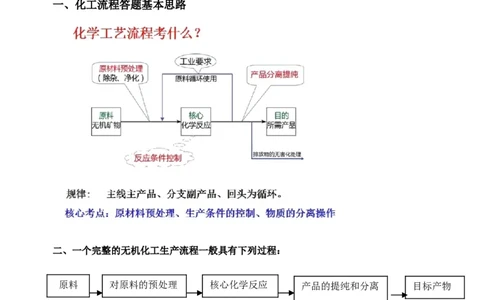
一、化工流程答题基本思路
二、一个完整的无机化工生产流程一般具有下列过程:
原料 对原料的预处理 核心化学反应 产品的提纯和分离 目标产物
分离提纯的方法:
过滤:一贴二低三靠四洗; 四洗--为什么要洗--用什么洗----怎么洗涤----洗干净没?
为什么洗:去除晶体表面的杂质;把目标产物尽可能洗出来,提升产率;
用什么洗:蒸馏水、冷水、有机溶剂(醇、酮、醚)等;如酒精洗硫酸亚铁铵晶体可降
低晶体因溶解造成损失,可以出去表面的水,酒精易挥发,易干燥。
怎么洗涤:沿着玻璃棒向过滤器中加入蒸馏水(其他溶剂)至浸没沉淀,待其自然流下
后,重复2~3次。洗干净没:(离子检验)取最后一次洗涤液少许于试管中,滴加某某试剂(其他操作),
产生什么现象?则是否洗干净。
减压过滤(吸滤、抽滤):减压过滤装置由真空泵、布氏漏斗、吸滤瓶组成。
结晶(重结晶):溶液单一溶质时,所得晶体不带结晶水,如氯化钠溶液结晶过程
为----蒸发结晶;所得晶体带有结晶水,如硫酸铜溶液得到CuSO5HO晶体过程为:
4 2
蒸发浓缩,冷却结晶,过滤。
溶液为两种以上溶质时,要得到溶解度受温度影响小得溶质----蒸发结晶,趁热过滤,
如除去NaCl中少量的KCl;要得到溶解度受温度影响大得溶质----蒸发浓缩,冷却结晶,
过滤, 如除KCl去中少量的NaCl。
晶体干燥:自然晾干、滤纸吸干、在干燥器中干燥、烘干(热稳定性较好)。
萃取(分液):当向混合物加入有机试剂(苯、四氯化碳等)后分离的,且题目信息有
涉及溶解度不同时考虑萃取。常见液—液萃取(如用苯或CCl4萃取水中的溴),固--液
萃取(如用酒精浸取黄豆中的豆油以提高油产量)。一般萃取分液后的混合溶液采取蒸
馏的方式分离。海带中提取碘(灼烧---溶解---过滤—氧化---萃取—蒸馏)。
蒸馏(分馏):题目信息有涉及沸点不同时,考虑蒸馏,常见混合液体或液-固体系
【典例精析】
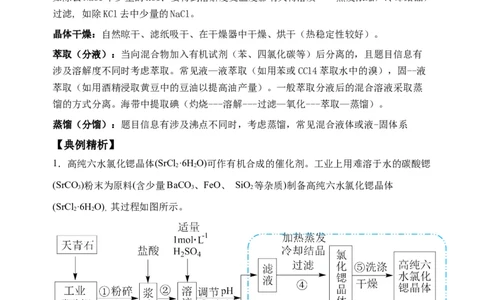
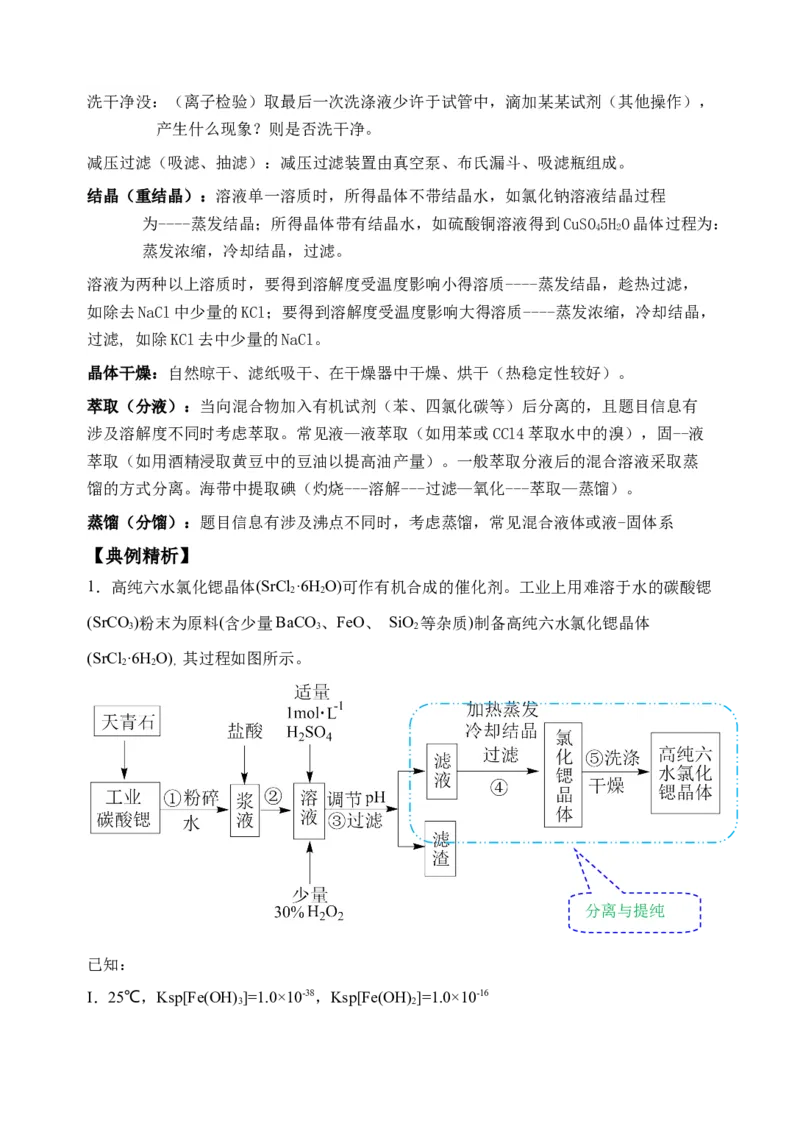
1.高纯六水氯化锶晶体(SrCl ·6H O)可作有机合成的催化剂。工业上用难溶于水的碳酸锶
2 2
(SrCO )粉末为原料(含少量BaCO 、FeO、 SiO 等杂质)制备高纯六水氯化锶晶体
3 3 2
(SrCl ·6H O) 其过程如图所示。
2 2 ,
分离与提纯
已知:
I.25℃,Ksp[Fe(OH) ]=1.0×10-38,Ksp[Fe(OH) ]=1.0×10-16
3 2II.SrCl ·6H O 晶体在61 ℃时开始失去结晶水。
2 2
请回答:
(1)天青石(主要成分SrSO )经过多步反应后可制得工业碳酸锶。其中第一步是与过量焦炭
4
隔绝空气微波加热还原为硫化锶,该过程的化学方程式为___________。
(2)步骤①中将工业碳酸锶粉碎制成浆液能加快反应速率的原因是___________。
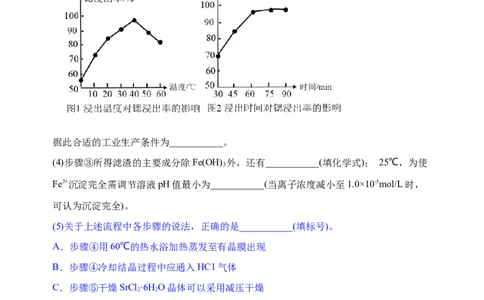
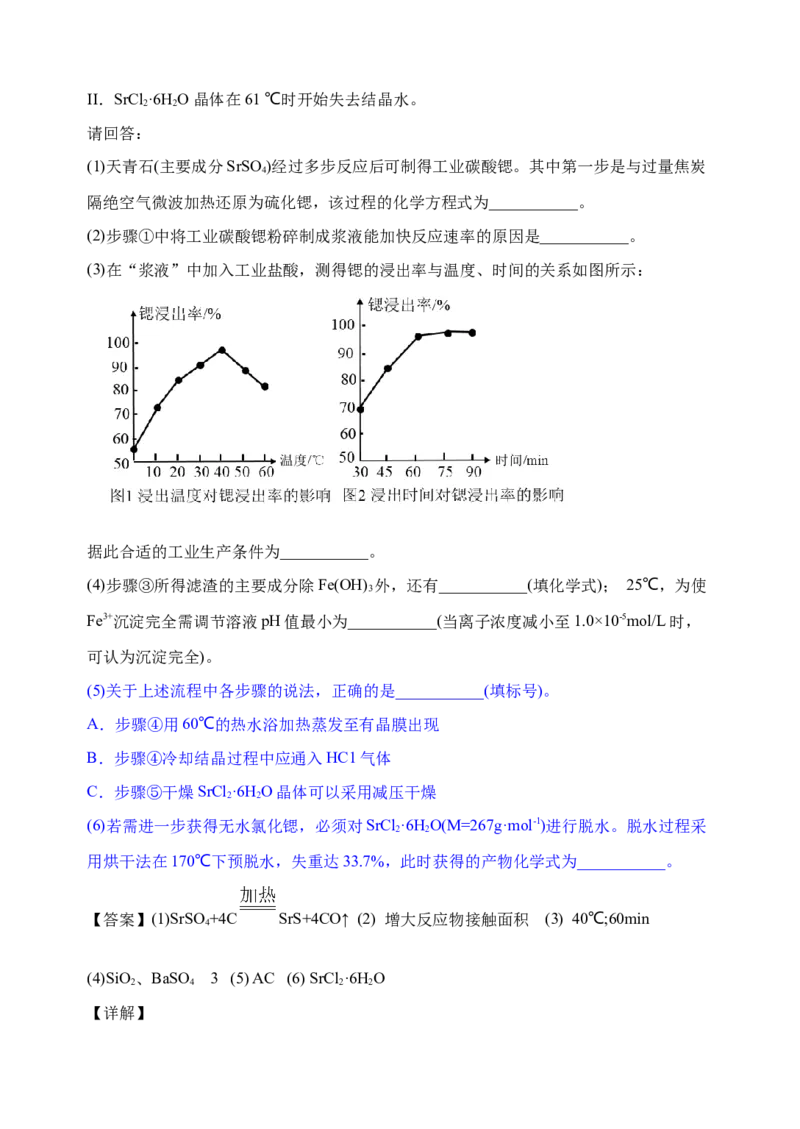
(3)在“浆液”中加入工业盐酸,测得锶的浸出率与温度、时间的关系如图所示:
据此合适的工业生产条件为___________。
(4)步骤③所得滤渣的主要成分除Fe(OH) 外,还有___________(填化学式); 25℃,为使
3
Fe3+沉淀完全需调节溶液pH值最小为___________(当离子浓度减小至1.0×10-5mol/L时,
可认为沉淀完全)。
(5)关于上述流程中各步骤的说法,正确的是___________(填标号)。
A.步骤④用60℃的热水浴加热蒸发至有晶膜出现
B.步骤④冷却结晶过程中应通入HC1气体
C.步骤⑤干燥SrCl ·6H O晶体可以采用减压干燥
2 2
(6)若需进一步获得无水氯化锶,必须对SrCl ·6H O(M=267g·mol-1)进行脱水。脱水过程采
2 2
用烘干法在170℃下预脱水,失重达33.7%,此时获得的产物化学式为___________。
【答案】(1)SrSO +4C SrS+4CO↑ (2) 增大反应物接触面积 (3) 40℃;60min
4
(4)SiO、BaSO 3 (5) AC (6) SrCl ·6H O
2 4 2 2
【详解】(1)此过程中硫酸锶与碳在高温下反应生成确化锶和一氧化碳,反应方程式为:SrSO +4C
4
SrS+4CO↑;
(2)根据影响化学反应速率的因素,增大接触面积、或升高温度、或增大盐酸浓度、或充
分搅拌等都能加快反应速率。步骤①中将矿石制成浆液,增大反应物接触面积,能加快
反应速率 答案:增大反应物接触面积。
;
(3)在“浆液”中加入工业盐酸,根据锶的没出率与温度、时间的关系图分析:由图1可
知: 40℃时锶的浸出率最高,由图2可知60min锶的浸出率最高,所以工业生产合适的
条件为40℃; 60min 答案: 40℃; 60min。
;
(4)步骤③所得滤液的主要成分除Fe(OH)) 外,还有不溶于水和酸的SiO 固体,还会有过
3 2
程中生成的BaSO 沉淀; 25℃,Ksp[Fe(OH) ]=1.0×10-38,Ksp[Fe(OH) ]=1.0×10-16,要使
4 3 2
Fe3+完全沉淀,c3(OH-)= Kp[Fe(OH) ]÷1.0×10-5=1.0×10-38÷1.0×10-5=1.0×10-33所以
3
c(OH-)=1.0×10-11mol/L,c(H+)=1.0×10-3即pH=3 要使Fe3+沉淀完全需调节溶液pH值最小为
,
3.答案: SiO、 BaSO; 3。
2 4
(5)SrCl ·6H O晶体在61℃时开始失去结品水,100℃时失去全部结品水。A.步骤③用
2 2
60℃的热水浴加热蒸发至有晶膜出现,不会造成SrCl ·6H O失去结晶水,又能加快速率,
2 2
故A正确: B. 因为Sr的金属性很强,Sr2+在溶液中不会发生水解,所以步骤④冷却结
晶过程中不用通入HC1气体,故B错误: C.步骤⑤干燥SrCl ·6H O晶体采用减压干燥
2 2
可以减少SrCl ·6H O晶体失水,故C正确:答案: AC。
2 2
(6)脱水过程采用烘干法在170℃下预脱水,失重达3.7% 设烘干法在170C下脱去x个结
,
晶水,则18x÷267×100%=33.7%, x=5, 即SrCl ·6H O脱水失去5个结晶水,故此时获
2 2
得的产物化学式为:SrCl ·H O。
2 2
【专题精练】
2.NaClO·3H O具有强氧化性,在消毒和果蔬保鲜等方面有广泛应用。
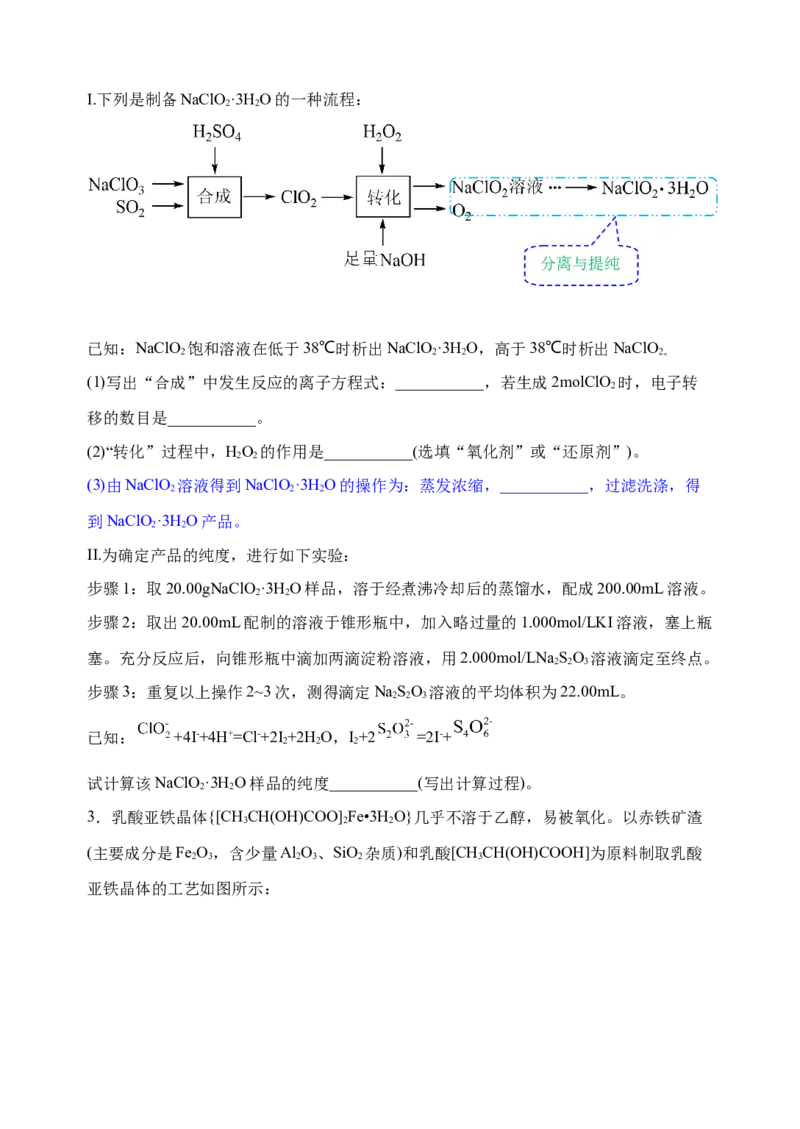
2 2I.下列是制备NaClO·3H O的一种流程:
2 2
分离与提纯
已知:NaClO 饱和溶液在低于38℃时析出NaClO·3H O,高于38℃时析出NaClO
2 2 2 2。
(1)写出“合成”中发生反应的离子方程式:___________,若生成2molClO 时,电子转
2
移的数目是___________。
(2)“转化”过程中,HO 的作用是___________(选填“氧化剂”或“还原剂”)。
2 2
(3)由NaClO 溶液得到NaClO·3H O的操作为:蒸发浓缩,___________,过滤洗涤,得
2 2 2
到NaClO·3H O产品。
2 2
II.为确定产品的纯度,进行如下实验:
步骤1:取20.00gNaClO ·3H O样品,溶于经煮沸冷却后的蒸馏水,配成200.00mL溶液。
2 2
步骤2:取出20.00mL配制的溶液于锥形瓶中,加入略过量的1.000mol/LKI溶液,塞上瓶
塞。充分反应后,向锥形瓶中滴加两滴淀粉溶液,用2.000mol/LNa SO 溶液滴定至终点。
2 2 3
步骤3:重复以上操作2~3次,测得滴定NaSO 溶液的平均体积为22.00mL。
2 2 3
已知: +4I-+4H+=Cl-+2I +2H O,I+2 =2I-+
2 2 2
试计算该NaClO·3H O样品的纯度___________(写出计算过程)。
2 2
3.乳酸亚铁晶体{[CH CH(OH)COO] Fe•3H O}几乎不溶于乙醇,易被氧化。以赤铁矿渣
3 2 2
(主要成分是Fe O,含少量Al O、SiO 杂质)和乳酸[CHCH(OH)COOH]为原料制取乳酸
2 3 2 3 2 3
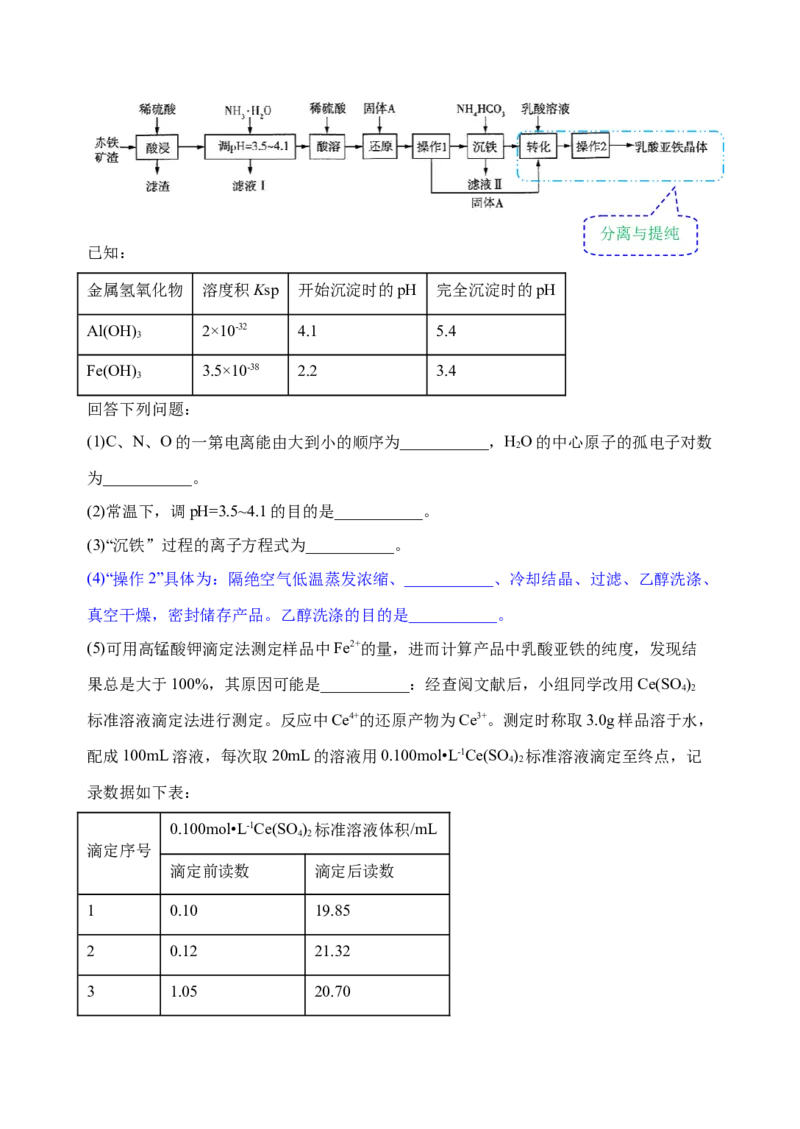
亚铁晶体的工艺如图所示:分离与提纯
已知:
金属氢氧化物 溶度积Ksp 开始沉淀时的pH 完全沉淀时的pH
Al(OH) 2×10-32 4.1 5.4
3
Fe(OH) 3.5×10-38 2.2 3.4
3
回答下列问题:
(1)C、N、O的一第电离能由大到小的顺序为___________,HO的中心原子的孤电子对数
2
为___________。
(2)常温下,调pH=3.5~4.1的目的是___________。
(3)“沉铁”过程的离子方程式为___________。
(4)“操作2”具体为:隔绝空气低温蒸发浓缩、___________、冷却结晶、过滤、乙醇洗涤、
真空干燥,密封储存产品。乙醇洗涤的目的是___________。
(5)可用高锰酸钾滴定法测定样品中Fe2+的量,进而计算产品中乳酸亚铁的纯度,发现结
果总是大于100%,其原因可能是___________:经查阅文献后,小组同学改用Ce(SO)
4 2
标准溶液滴定法进行测定。反应中Ce4+的还原产物为Ce3+。测定时称取3.0g样品溶于水,
配成100mL溶液,每次取20mL的溶液用0.100mol•L-1Ce(SO) 标准溶液滴定至终点,记
4 2
录数据如下表:
0.100mol•L-1Ce(SO) 标准溶液体积/mL
4 2
滴定序号
滴定前读数 滴定后读数
1 0.10 19.85
2 0.12 21.32
3 1.05 20.70则产品中乳酸亚铁晶体的纯度为___________。
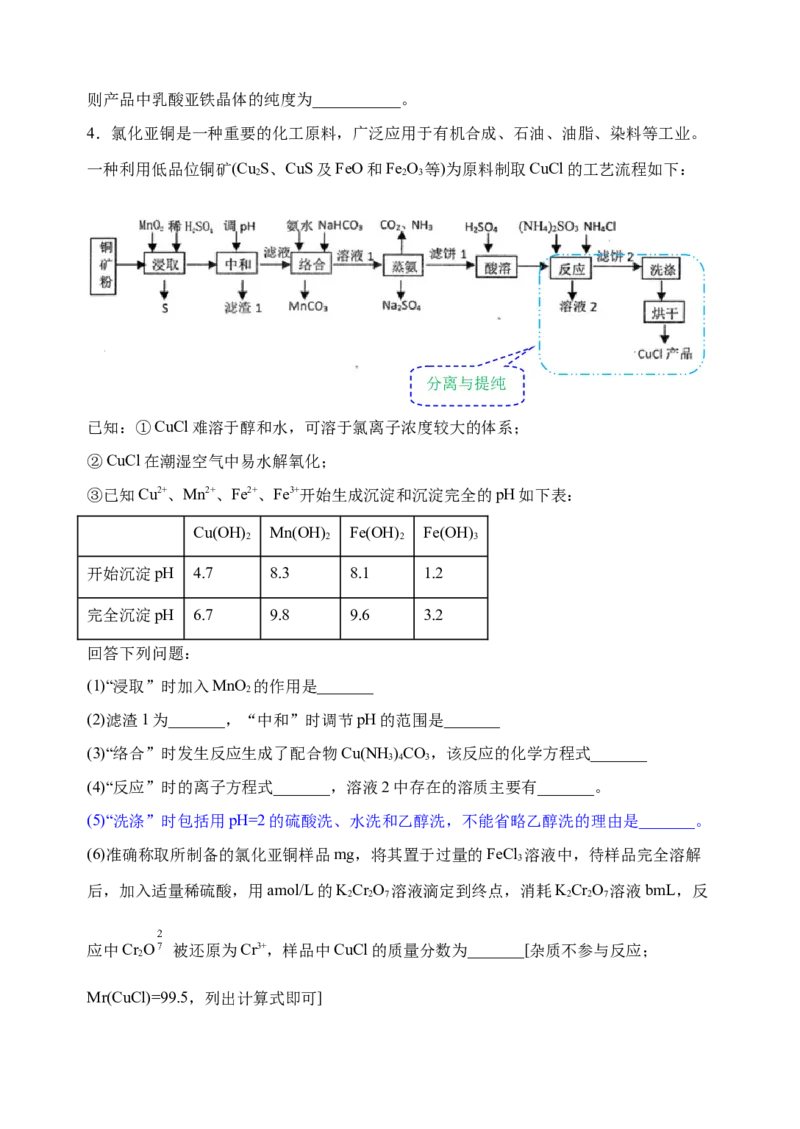
4.氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、油脂、染料等工业。
一种利用低品位铜矿(Cu S、CuS及FeO和Fe O 等)为原料制取CuCl的工艺流程如下:
2 2 3
分离与提纯
已知:①CuCl难溶于醇和水,可溶于氯离子浓度较大的体系;
②CuCl在潮湿空气中易水解氧化;
③已知Cu2+、Mn2+、Fe2+、Fe3+开始生成沉淀和沉淀完全的pH如下表:
Cu(OH) Mn(OH) Fe(OH) Fe(OH)
2 2 2 3
开始沉淀pH 4.7 8.3 8.1 1.2
完全沉淀pH 6.7 9.8 9.6 3.2
回答下列问题:
(1)“浸取”时加入MnO 的作用是_______
2
(2)滤渣1为_______,“中和”时调节pH的范围是_______
(3)“络合”时发生反应生成了配合物Cu(NH )CO,该反应的化学方程式_______
3 4 3
(4)“反应”时的离子方程式_______,溶液2中存在的溶质主要有_______。
(5)“洗涤”时包括用pH=2的硫酸洗、水洗和乙醇洗,不能省略乙醇洗的理由是_______。
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl 溶液中,待样品完全溶解
3
后,加入适量稀硫酸,用amol/L的KCr O 溶液滴定到终点,消耗KCr O 溶液bmL,反
2 2 7 2 2 7
应中Cr O 被还原为Cr3+,样品中CuCl的质量分数为_______[杂质不参与反应;
2
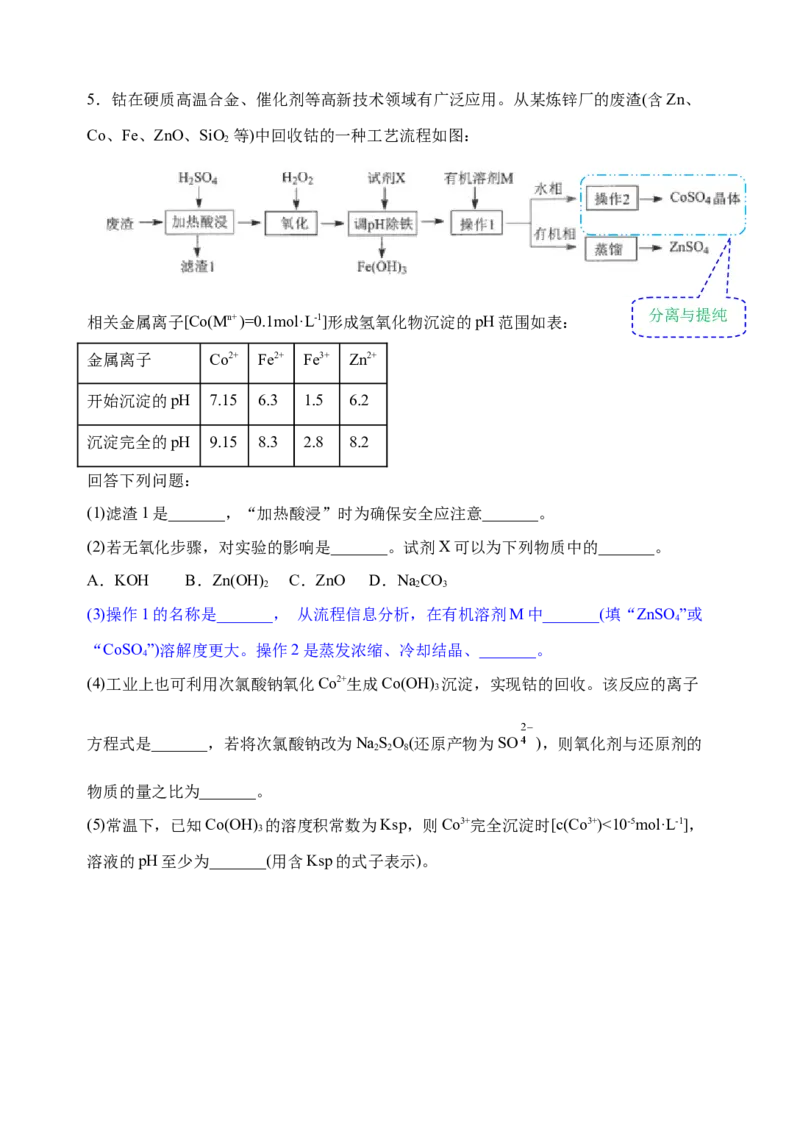
Mr(CuCl)=99.5,列出计算式即可]5.钴在硬质高温合金、催化剂等高新技术领域有广泛应用。从某炼锌厂的废渣(含Zn、
Co、Fe、ZnO、SiO 等)中回收钴的一种工艺流程如图:
2
分离与提纯
相关金属离子[Co(Mn+ )=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:
金属离子 Co2+ Fe2+ Fe3+ Zn2+
开始沉淀的pH 7.15 6.3 1.5 6.2
沉淀完全的pH 9.15 8.3 2.8 8.2
回答下列问题:
(1)滤渣1是_______,“加热酸浸”时为确保安全应注意_______。
(2)若无氧化步骤,对实验的影响是_______。试剂X可以为下列物质中的_______。
A.KOH B.Zn(OH) C.ZnO D.NaCO
2 2 3
(3)操作1的名称是_______, 从流程信息分析,在有机溶剂M中_______(填“ZnSO”或
4
“CoSO ”)溶解度更大。操作2是蒸发浓缩、冷却结晶、_______。
4
(4)工业上也可利用次氯酸钠氧化Co2+生成Co(OH) 沉淀,实现钴的回收。该反应的离子
3
方程式是_______,若将次氯酸钠改为NaSO(还原产物为SO ),则氧化剂与还原剂的
2 2 8
物质的量之比为_______。
(5)常温下,已知Co(OH) 的溶度积常数为Ksp,则Co3+完全沉淀时[c(Co3+)<10-5mol·L-1],
3
溶液的pH至少为_______(用含Ksp的式子表示)。