文档内容
第十单元 酸和碱
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13
1.2008年诺贝尔化学奖授予发明和研究绿色荧光蛋白的三位科学家。绿色荧光蛋白分子中含
有氨基(—NH ,具有碱的性质)和羧基(—COOH,具有酸的性质)。则绿色荧光蛋白具有的性
2
质是
A.既能与盐酸反应,又能与氢氧化钠反应
B.只能与氢氧化钠反应,不能与盐酸反应
C.只能与盐酸反应,不能与氢氧化钠反应
D.既不能与盐酸反应,又不能与氢氧化钠反应
2.下列质量增加的变化有一种与其他三种存在着本质的区别,这种变化是
A.长期放置在空气中的氢氧化钠质量增加B.久置在潮湿空气中的铁钉质量增加
C.久置在空气中的生石灰质量增加D.长期敞口放置的浓硫酸质量增加
3.推理是一种重要的研究和学习方法。下列推理正确的是
A.碱中都含有氢氧根,所以碱中一定含有氢元素
B.分子是构成物质的微粒,因此物质都是由分子构成的
C.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
D.铁丝能在氧气中燃烧,空气中有氧气,所以铁丝也能在空气中燃烧
4.以下是一些食物的近似pH,对于胃酸过多的人比较适宜的食物是:
物质 橘子 泡菜 葡萄 玉米粥
pH 2.9~3.5 3.0~4.0 3.5~4.5 6.8-8.0
选项 A B C D
5.稀盐酸和稀硫酸具有许多相似化学性质的原因是
A.它们都是溶液 B.它们都含有酸根离子
C.它们都含有氢元素 D.它们都电离出了氢离子
6.胃酸能帮助消化,但过多的胃酸会危害健康。可用于治疗胃酸过多的物质是
A.NaCl B.Al(OH) C.CaO D.NaOH
3
7. 有一食品包装说明书中注明防腐剂是苯甲酸(C HCOOH),张华同学查资料得知苯甲酸的
6 5
酸性比醋酸强,可用做食品防腐剂。下列对苯甲酸性质的推测中不合理的是
A. 苯甲酸溶液的pH小于7 B. 相同浓度的苯甲酸溶液的pH比醋酸的pH大
C. 苯甲酸溶液能使紫色石蕊试液变红 D. 苯甲酸溶液不能使无色酚酞试液变色
8.张伟同学学习了溶液酸碱度的表示方法—pH值之后,对家中的一些食品及生活用品,进行
了pH值测定,结果如下:参照上图,下列说法正确的是
A.煮骨头汤时加点醋,有利于增加汤中钙的含量 B.牙膏是中性物质
C.酱油显碱性,可使酚酞变红色 D.胃酸过多的人宜多吃葡
9.某学校化学课外活动小组的同学,取刚降到地面的雨水的水样,用PH计(测PH的仪器)
每隔10分钟测一次PH,其数据如下表所示,其中雨水酸性最强的时刻 是:
测定时间 9:00 9:10 9:20 9:30
[来源:学科网]
PH 4.95 4.94 4.86 4.85
A.9:00 B.9:10 C.9:20 D.9:30
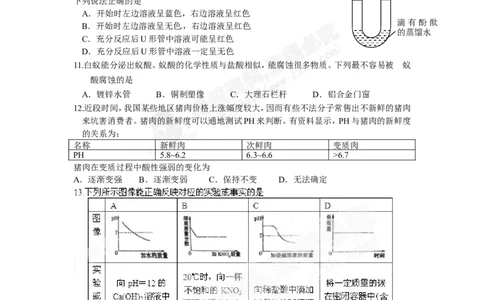
10.U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别
氢氧化钠 稀盐酸
同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。稀溶液
下列说法正确的是
A.开始时左边溶液呈蓝色,右边溶液呈红色
滴有酚酞
B.开始时左边溶液呈无色,右边溶液呈红色
的蒸馏水
C.充分反应后U形管中溶液可能呈红色
D.充分反应后U形管中溶液一定呈无色
11.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易被 蚁
酸腐蚀的是
A.镀锌水管 B.铜制塑像 C.大理石栏杆 D.铝合金门窗
12.近段时间,我国某些地区猪肉价格上涨幅度较大,因而有些不法分子常售出不新鲜的猪肉
来坑害消费者。猪肉的新鲜度可以通地测试PH来判断。有资料显示,PH与猪肉的新鲜度
的关系为:
名称 新鲜肉 次鲜肉 变质肉
PH 5.8~6.2 6.3~6.6 >6.7
猪肉在变质过程中酸性强弱的变化为
A.逐渐变强 B.逐渐变弱 C.保持不变 D.无法确定
二、填空题
14.(1)硫化氢(HS)是一种易溶于水的气体,测定它水溶液的酸碱度,可选用 。
2
(2)硫化氢与浓硫酸反应生成硫、二氧化硫和水。在这个反应中,所有含硫物质硫元素的化
合价共有 种。硫化氢在空气中点燃可完全燃烧,生成二氧化硫和水。这一反应的化学
方程式是 。
15.小政同学在复习Ca(OH) 化学性质时,归纳出了Ca(OH) 与其它物质
2 2
间相互反应的关系如图4(图中“——”表示相连的两种物质能发生反应)。
(1)若X是与其它三种不同类别的化合物,则X可以是 。
(2)根据图4所示的物质间关系,写出其中两个化学方程式:
① ;② 。
16.食品吸潮和吸氧后容易变质,为了延长食品保质期.通常在包装袋中加入1小包干燥剂。
某化学兴趣小组经过查阅资料,发现常见的食品干燥剂主要有’两种:一种 是以生石灰
为主要成份的千燥剂(简称A类,下同);另一种是以硅胶为主要成份的干燥剂(简称B类,下
同)。请问答下列问题:
(1)将装有A类干燥剂的小纸袋打开露置于潮湿的空气中,发现纸袋发热,与出其发生
反应的化学方程式________________________________________。
(2)B类干燥剂中硅胶的主要成分为SiO·nH O。SiO 是__________ (填“酸”、“碱”、
2 2 2
“盐”、“氧化物”),其中Si的化合价为____________________。
(3)小组在杳阅资料中,还发现了—种新型的食品干燥剂:泡沫铁粉(铁粉包裹在泡沫塑
料中)。当它露置于潮湿的空气中,很快变成铁锈(主要成分为Fe O·nH O),并有发热现象,说
2 3 2
明化学反应除了生成新物质外,还伴随着__________变化。与A类干燥 剂比较,泡沫铁
粉除了做干燥剂外,还可做__________剂。
17.小勇在化学晚会上观看了“瓶吞鸡蛋”的魔术(如下图1),看到鸡蛋被吞进瓶内。该反
应的化学方程式是 。
小勇思考:瓶能吞蛋,能不能吐蛋呢?他进行了如上图2的实验,结果鸡蛋吐了出来。他
加入的试剂P是 (写溶液名称),吐蛋的原理是
。
18.酸与碱作用生成盐和水的反应,叫中和反应。在用盐酸和氢氧化
钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如
图所示:
(1)要得到此变化曲线,所进行的操作是 (填序号)。
①将稀盐酸滴加到氢氧化钠溶液中
②将氢氧化钠溶液滴加到稀盐酸中
(2)该反应的化学方程式 。
19.甲酸(HCOOH)是一种有机酸,它的酸性比碳酸强,比盐酸弱,有刺激性气味和较强的腐
蚀性。蚂蚁、蚊虫叮咬时会分泌出甲酸,所以甲酸又俗称蚁酸。
(1)人被蚊虫叮咬后会痒痛,可以涂抹下列物质中的(填序号) 消除。
①稀盐酸 ②食醋 ③肥皂水 ④食盐水
(2)白蚂蚁除了会蛀蚀木头以外,它分泌的蚁酸还会腐蚀很多建筑材料,下列建筑材料不容
易被蚁酸腐蚀的是(填字母) 。
A.铜栏杆 B.钢筋 C.大理石 D.玻璃
(3)使用浓硫酸作催化剂,在加热的条件下,甲酸分解得到一种常见的有毒气体和另一种氧化
物,其化学方程式为 。
三、实验探究题20.某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥
剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH) 的混合物;
2
猜想三:全部是Ca(OH) ; 猜想四:是Ca(OH) 和CaCO 的混合物。
2 2 3
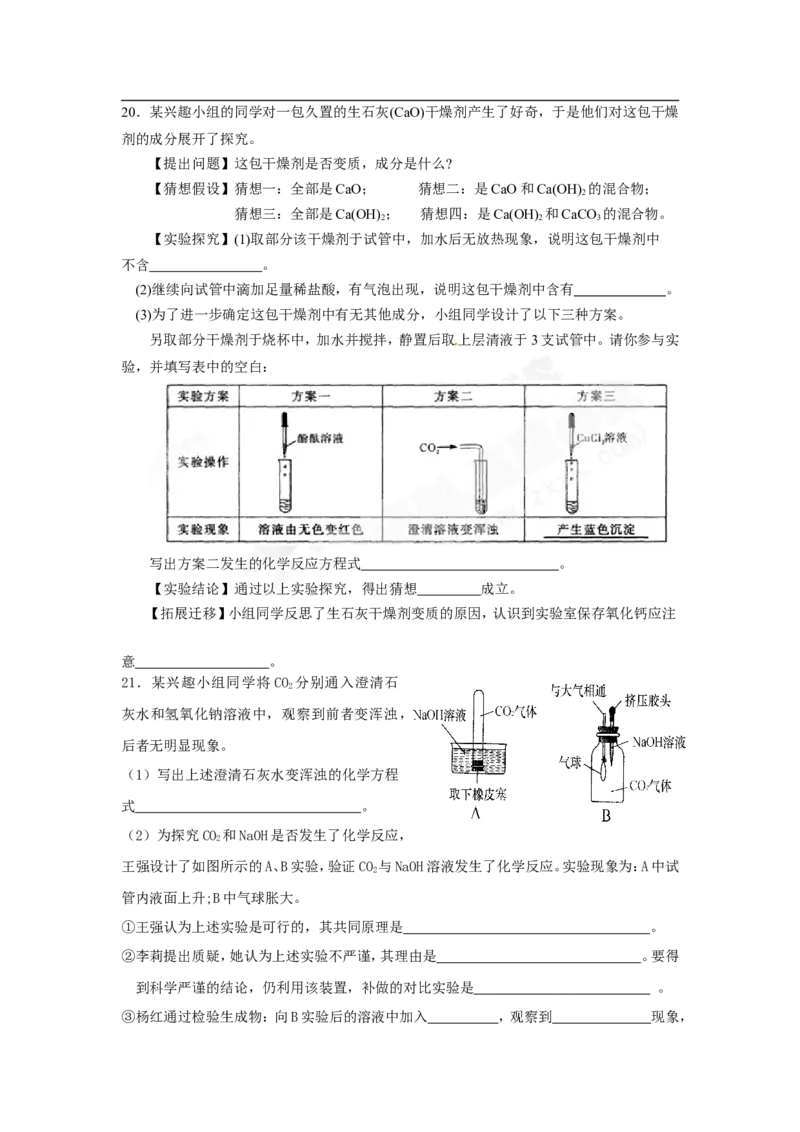
【实验探究】(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中
不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
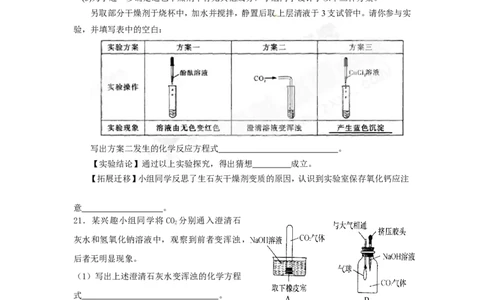
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案。
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中。请你参与实
验,并填写表中的空白:
写出方案二发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注
[来
源:Zxxk.Com]
意 。
21.某兴趣小组同学将CO 分别通入澄清石
2
灰水和氢氧化钠溶液中,观察到前者变浑浊,
后者无明显现象。
(1)写出上述澄清石灰水变浑浊的化学方程
式 。
(2)为探究CO 和NaOH是否发生了化学反应,
2
王强设计了如图所示的A、B实验,验证CO 与NaOH溶液发生了化学反应。实验现象为:A中试
2
管内液面上升;B中气球胀大。
①王强认为上述实验是可行的,其共同原理是 。
②李莉提出质疑,她认为上述实验不严谨,其理由是 。要得
到科学严谨的结论,仍利用该装置,补做的对比实验是 。
③杨红通过检验生成物:向B实验后的溶液中加入 ,观察到 现象,从而也证明CO 与NaOH发生了反应。
2
④你认为两实验中存在安全隐患的是 (填代号),理由是 。
22.氯气(Cl)是黄绿色气体,水溶液叫氯水。把品红试纸(染有品红的纸)伸入氯水中,品红
2
褪色。
【发现问题】 氯水中的哪些成分能使品红褪色呢?
【查阅资料】 氯气溶于水,部分与水反应,方程式为Cl + H O = HCl + HClO。其中,HClO的
2 2
名称叫次氯酸,是一种弱酸,具有强氧化性。
【猜 想】猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的_________(填化学式)使品红褪色的;
猜想3:是氯水中的盐酸使品红褪色的;
猜想1:是氯水中的次氯酸使品红褪色的。
【实验探究】
实验操作 实验现象 过程分析
①把品红试纸伸入水中 没有褪色 猜想1不成立
②把品红试纸伸入干燥的氯气中 没有褪色 猜想2不成立
③ 没有褪色 猜想3不成立
【结 论】综合分析:氯水中的 (填化学式)使品红褪色,具有漂白作用
(能使品红等有色物质褪色)。
【反 思】(1)HClO中氯元素的化合价为 价。
(2) 氯 水 中 加 入 AgNO 溶 液 有 白 色 沉 淀 生 成 , 化 学 方 程 式 为
3
___________________________________________________________________________。
(3) 向氯水中滴加紫色石蕊试液,观察到的现象是___________________________________。
23.小林在凉拌紫卷心菜时,加入一些食醋,发现紫卷心菜变红了,激发了他的探究欲望,特
邀你协助完成下列活动与探究。
[提出问题] 紫卷心菜等植物的汁液能作酸碱指示剂吗?
[实验探究] 取紫卷心菜、牵牛花的花瓣、胡萝卜,分别在研钵中捣烂,加入酒精(乙醇与
水的体积比为1:1)浸泡,用纱布将浸泡出的汁液挤出,分别加入到蒸馏水、稀
酸溶液和稀碱溶液中,有关颜色变化情况如下:
汁液 在不同液体中的颜色变化
[来源:Z+xx+k.Com] [来源:学+科+网Z+X+X+K]
蒸馏水 稀酸溶液 稀碱溶液
紫卷心菜 蓝紫色 红色 绿色
牵牛花 紫色 红色 蓝色
胡萝卜 橙色 橙色 橙色
[得出结论] 、 的汁液能做酸碱指示剂, 的汁液不能
做酸碱指示剂。
[拓展应用] 小林用上述的牵牛花汁液来测定某雨水样品的酸碱性,发现牵牛花汁液呈红色。
则该雨水呈 性(选填“酸”或“碱”或“中”)。
[反思与评价] 小林发现,上述汁液无法测出溶液的酸碱度,请你告诉他,在实验室测定溶
液的酸碱度常用 。四、计算题
24.小青同学为了制作叶脉书签,打算配制125g10%的NaOH溶液。
(l)计算小青需要称取NaOH的质量。
(2)小青将洗净的树叶放在配制好的溶液中煮沸后取出,溶液的质量减少了5g,溶质质量分
数也有所减小。为了侧定剩下溶液中NaOH的质量分数,小青向溶液中逐渐加入7.3%的稀盐
酸,当溶液PH=7时,消耗盐酸50g。计算:
①生成NaCl的质量。
②剩下溶液中NaOH的质量分数。
25.把标准状况下1120mL二氧化碳气体(密度为1.977g/L)通入溶质质量分数为10%的氢氧
化钠溶液中恰好完全反应,反应方程式:CO+2NaOH=NaCO+HO,
2 2 3 2
求(计算结果精确到0.1%):
⑴ 反应前溶质质量分数为10%的氢氧化钠溶液的质量;
⑵ 反应后所得溶液中溶质NaCO 的质量分数。
2 3第十单元 酸和碱
一、选择题
1 2 3 4 5 6 7 8 9 10 11 12 13
A D A D D B B A D C B B D
二、填空题
14.(1)pH试纸 ;(2)4 ;2HS+3O 2SO+2HO ;
2 2 2 2
15.(1)CO(合理答案均可得分)
2
(2)Ca(OH) +2HCl=CaCl +2H O
2 2 2
NaCO+Ca(OH) =CaCO↓+2NaOH(合理答案均可得分)
2 3 2 3
16.(1)CaO+H O==Ca(OH) (2)+4 (3)热量 脱氧剂
2 2
17.2NaOH+ CO=NaCO +HO 稀盐酸(或稀硫酸、稀硝酸等) 碳酸钠与稀盐酸反应产生大
2 2 3 2
量的气体,使瓶内压强增大
提示:吞蛋利用的是瓶外压强大于瓶内压强的原理,而吐蛋相反,即瓶内压强大于瓶外压强。
18.(1)② (2)NaOH+HCl=NaCl+H O
2
19. (1)③(2)D(3)HCOOH 浓硫酸 CO+HO
2
三、实验探究题
20. 【实验探究】(1) CaO或氧化钙(2)CaCO 或碳酸钙(3) Ca(OH) +CO==CaCO↓+H O
3 2 2 3 2
【实验结论】四【拓展迁移】密封保存
四、计算题
24.解:(1)m(NaOH)=125g×10%=12.5g
(2)NaOH + HCl = NaCl + HO
2
40 36.5 58.5
m(NaOH) 50g×7.3% m(NaCl)
m(NaOH)=4g m(NaCl)=5.85g
ω(NaOH)=×100%=3.3%
答:略
25.解:设反应前溶质质量分数为10%的氢氧化钠溶液的质量为x, 反应后所得溶液中
溶质NaCO 的质量分数y
2 3
CO + 2NaOH === NaCO+HO
2 2 3 2
44 80 106
1.12L×1.977g/L 10% x (1.12L×1.977g/L +x)y44 80
=
1.12L×1.977g/L 10% x
x=40g
44 106
=
1.12L×1.977g/L (1.12L×1.977g/L +x)y
y=12.6%
答:⑴反应前溶质质量分数为10%的氢氧化钠溶液的质量是40g;
⑵ 反应后所得溶液中溶质NaCO 的质量分数是12.6%。
2 3