文档内容
元素周期律
【学习目标】
1、掌握原子结构的周期性的变化,能够以短周期元素为例,说明同周期元素性质的递变情况
2、掌握元素周期律的具体内容,熟悉原子半径、金属性和非金属性的变化规律
【主干知识梳理】
一、元素的原子核外电子排布、原子半径、元素化合价的变化规律
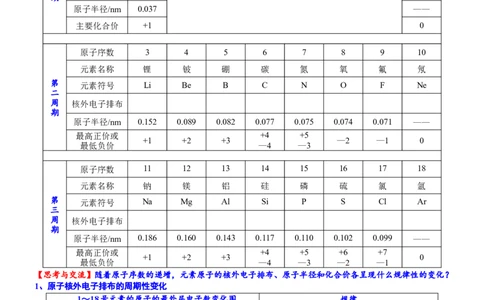
1~18号元素的原子核外电子排布、原子半径和主要化合价
原子序数 1 2
元素名称 氢 氦
第
元素符号 H He
一
周
核外电子排布
期
原子半径/nm 0.037 ——
主要化合价 +1 0
原子序数 3 4 5 6 7 8 9 10
元素名称 锂 铍 硼 碳 氮 氧 氟 氖
第
元素符号 Li Be B C N O F Ne
二
周 核外电子排布
期
原子半径/nm 0.152 0.089 0.082 0.077 0.075 0.074 0.071 ——
最高正价或 +4 +5
+1 +2 +3 —2 —1 0
最低负价 —4 —3
原子序数 11 12 13 14 15 16 17 18
元素名称 钠 镁 铝 硅 磷 硫 氯 氩
第 元素符号 Na Mg Al Si P S Cl Ar
三
周 核外电子排布
期
原子半径/nm 0.186 0.160 0.143 0.117 0.110 0.102 0.099 ——
最高正价或 +4 +5 +6 +7
+1 +2 +3 0
最低负价 —4 —3 —2 —1
【思考与交流】随着原子序数的递增,元素原子的核外电子排布、原子半径和化合价各呈现什么规律性的变化?
1、原子核外电子排布的周期性变化
1~18号元素的原子的最外层电子数变化图 规律
随着原子序数的递增,元素原子的最外层电
子排布呈现 1 ~ 8 的周期性变化(第一周期除
外)
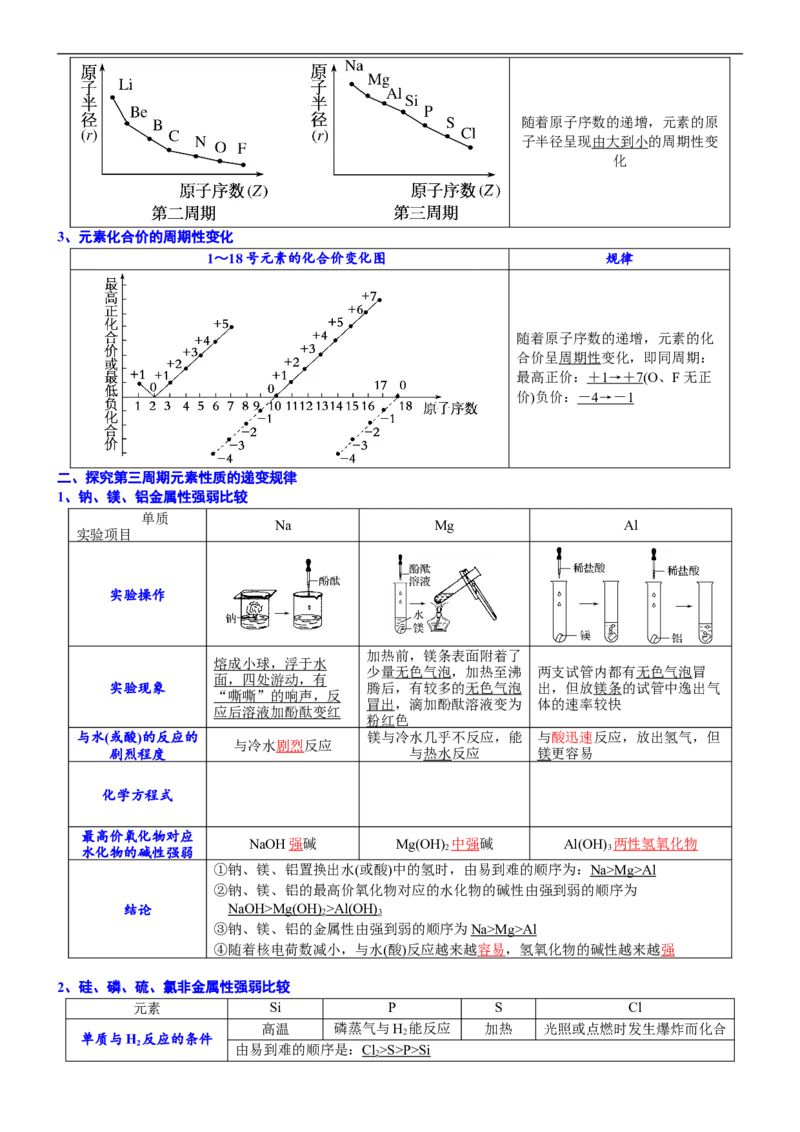
2、原子半径的周期性变化
1~18号元素的原子的原子半径变化图 规律随着原子序数的递增,元素的原
子半径呈现由大到小的周期性变
化
3、元素化合价的周期性变化
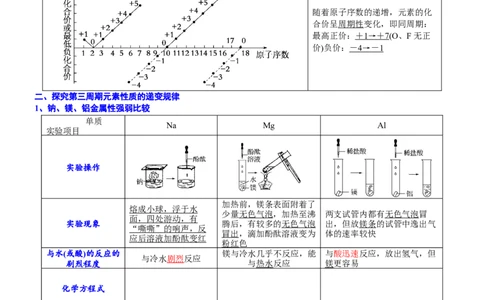
1~18号元素的化合价变化图 规律
随着原子序数的递增,元素的化
合价呈周期性变化,即同周期:
最高正价: + 1 → + 7(O、F无正
价)负价: - 4 → - 1
二、探究第三周期元素性质的递变规律
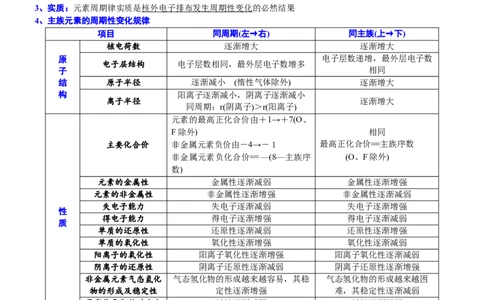
1、钠、镁、铝金属性强弱比较
单质
Na Mg Al
实验项目
实验操作
加热前,镁条表面附着了
熔成小球,浮于水
少量无色气泡,加热至沸 两支试管内都有无色气泡冒
面,四处游动,有
实验现象 腾后,有较多的无色气泡 出,但放镁条的试管中逸出气
“ 嘶嘶 ” 的响声,反
冒出,滴加酚酞溶液变为 体的速率较快
应后溶液加酚酞变红
粉红色
与水(或酸)的反应的 镁与冷水几乎不反应,能 与酸迅速反应,放出氢气,但
与冷水剧烈反应
剧烈程度 与热水反应 镁更容易
化学方程式
最高价氧化物对应
NaOH强碱 Mg(OH) 中强碱 Al(OH) 两性氢氧化物
水化物的碱性强弱 2 3
①钠、镁、铝置换出水(或酸)中的氢时,由易到难的顺序为:Na>Mg>Al
②钠、镁、铝的最高价氧化物对应的水化物的碱性由强到弱的顺序为
结论 NaOH>Mg(OH) >Al(OH)
2 3
③钠、镁、铝的金属性由强到弱的顺序为Na>Mg>Al
④随着核电荷数减小,与水(酸)反应越来越容易,氢氧化物的碱性越来越强
2、硅、磷、硫、氯非金属性强弱比较
元素 Si P S Cl
高温 磷蒸气与H 能反应 加热 光照或点燃时发生爆炸而化合
单质与H 反应的条件 2
2 由易到难的顺序是:Cl>S>P>Si
2最高价氧化物的化学式 SiO PO SO ClO
2 2 5 3 2 7
HSiO HPO HSO 强
最高价氧化物对应水化 2 3 3 4 2 4 HClO 酸性比HSO 强
弱酸 中强酸 酸 4 2 4
物的化学式及酸性
酸性:HClO>H SO >H PO >H SiO
4 2 4 3 4 2 3
氢化物的稳定性 不稳定 受热分解 受热分解 稳定
①硅、磷、硫、氯单质与氢气化合时条件由易到难的顺序为:Cl>S>P>Si
②硅、磷、硫、氯最高价氧化物对应水化物的酸性由强到弱的顺序为:
结论
HClO>H SO >H PO >H SiO
4 2 4 3 4 2 3
③硅、磷、硫、氯元素非金属性由强到弱的顺序为:Cl>S>P>Si
3、同周期元素性质递变规律:同一周期从左往右,金属性逐渐减弱,非金属性逐渐增强
三、元素周期律
1、内容:元素周期律是指元素的性质随着原子序数的递增而呈现周期性的变化
2、元素的性质包括:原子半径、主要化合价、金属性、非金属性等
3、实质:元素周期律实质是核外电子排布发生周期性变化的必然结果
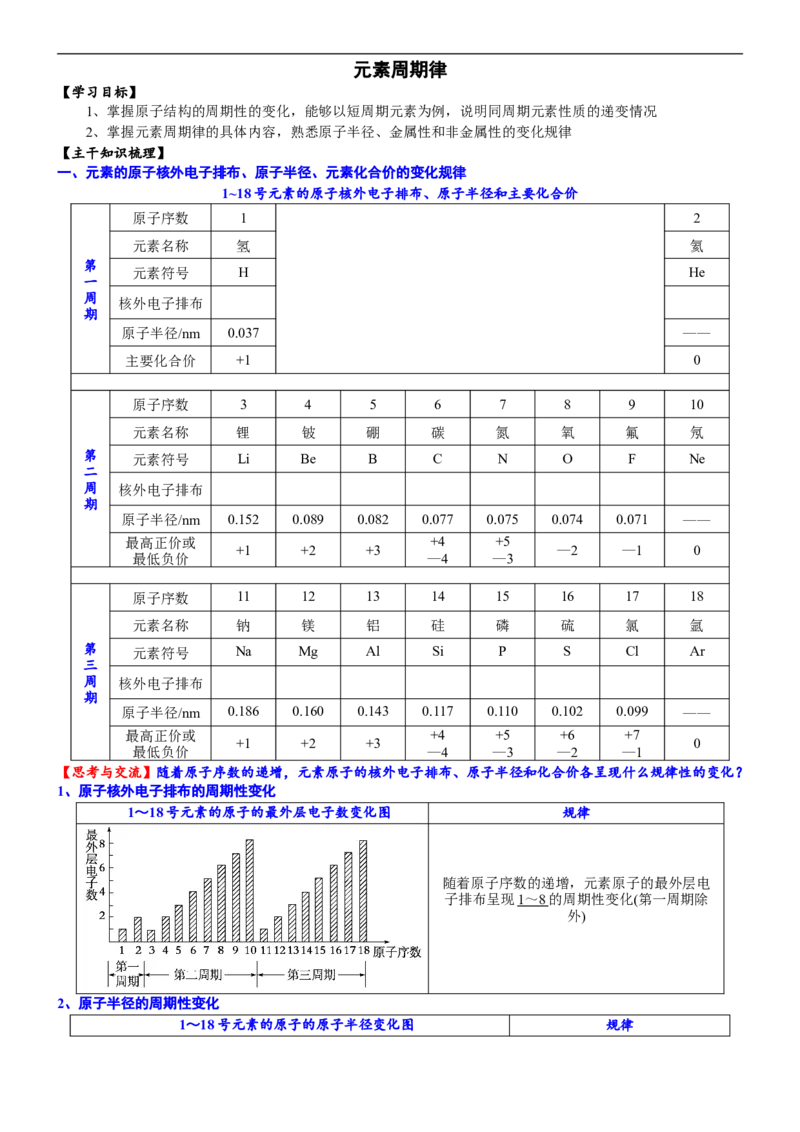
4、主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
原 电子层数递增,最外层电子数
电子层结构 电子层数相同,最外层电子数增多
子 相同
结 原子半径 逐渐减小 (惰性气体除外) 逐渐增大
构 阳离子逐渐减小,阴离子逐渐减小
离子半径 逐渐增大
同周期:r(阴离子)>r(阳离子)
元素的最高正化合价由+1→+7(O、
F除外) 相同
主要化合价 非金属元素负价由-4→-1 最高正化合价==主族序数
非金属元素负化合价== —(8—主族序 (O、F除外)
数)
元素的金属性 金属性逐渐减弱 金属性逐渐增强
元素的非金属性 非金属性逐渐增强 非金属性逐渐减弱
失电子能力 失电子逐渐减弱 失电子逐渐增强
性
得电子能力 得电子逐渐增强 得电子逐渐减弱
质
单质的还原性 还原性逐渐减弱 还原性逐渐增强
单质的氧化性 氧化性逐渐增强 氧化性逐渐减弱
阳离子的氧化性 阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
阴离子的还原性 阴离子还原性逐渐减弱 阴离子还原性逐渐增强
非金属元素气态氢化 气态氢化物的形成越来越容易,其稳 气态氢化物的形成越来越困
物的形成及稳定性 定性逐渐增强 难,其稳定性逐渐减弱
最高价氧化物对应水 碱性逐渐减弱 碱性逐渐增强
化物的酸碱性 酸性逐渐增强 酸性逐渐减弱
【即学即练1】
1、下列有关原子结构和元素周期律的表述正确的是( )
A.同周期非金属元素的氧化物对应的水化物的酸性从左到右依次增强
B.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
C.ⅦA族元素是同周期中非金属性最强的元素
D.原子序数为15的元素的最高化合价为+3
2、不能用元素周期律解释的是( )
A.酸性HCl>H S>PH B.原子半径P>S>Cl
2 3C.最高正价Cl>S>P D.酸性HClO>H SO >H PO
4 2 4 3 4
3、已知X、Y、Z是三种原子序数相连的元素,其最高价氧化物对应水化物酸性相对强弱的顺序是
HXO>H YO >H ZO,则下列判断正确的是( )
4 2 4 3 4
A.气态氢化物的稳定性:HX>H Y>ZH B.非金属活泼性:YY>Z D.原子最外层电子数:Xr(Mg)>r(Al)>r(Si)>r(P)r(Cl)
同主族原子半径随原子序数递增逐渐增大
(2)
如:r(Li)r(Na+)
(2)阴离子半径总比相应原子半径大,如:r(Cl)r(Mg2+)>r(Al3+)
(6)同周期阴离子半径随原子序数递增逐渐减小,如:r(N3— )>r(O2—)>r(F—)
【微点拨】同周期:r(阴离子)>r(阳离子),阴离子比阳离子电子层多一层,如:r(S2-)>r(Na+)
(7)电子层结构相同的离子半径随核电荷数的增大而减小,如:r(S2-)>r(Cl-)>r(K+)>r(Ca2+)
(8)同一元素不同价态的离子半径,价态越高则离子半径越小,如:r(Fe)>r(Fe2+)>r(Fe3+)
【微点拨】
①稀有气体元素的原子半径比与它相邻的卤素原子的原子半径大,如:r(Ar)>r(Cl)
②不同周期、不同主族元素原子半径大小的比较。先找参照元素,使其建立起同周期、同主族的关系,然后
进行比较。比较S与F的原子半径大小,先找O做参照,因为O与F同周期,r(F)Cl->Na+>Al3+
C.NaA>B
B.原子半径由大到小的顺序是r(B)>r(A)>r(C)
C.离子半径由大到小的顺序是r(C-)>r(B2+)>r(A2-)D.原子最外层电子数由多到少的顺序是B>A>C
3、已知下列原子的半径,根据以上数据,P原子的半径可能是( )
原子 N S O Si
半径r/10-10 m 0.75 1.02 0.74 1.17
A.1.10×10-10 m B.0.80×10-10 m C.1.20×10-10 m D.0.70×10-10 m
五、元素的金属性和非金属性强弱的判断方法
1、元素金属性强弱的判断方法
(1)金属性:指金属元素的原子失去电子能力
【微点拨】比较金属性的强弱,其实质是看元素原子失去电子的难易程度,越易失电子,金属性越强
(2)结构比较法:最外层电子数越少,电子层数越多,元素金属性越强
(3)位置比较法:同周期元素,从左到右,随原子序数增加,金属性减弱;
同主族元素,从上到下,随原子序数增加,金属性增强。金属性最强的元素为铯
(4)根据元素单质及其化合物的相关性质判断
①依据最高价氧化物对应水化的碱性强弱来比较:碱性越强则对应元素的金属性越强
如:碱性:NaOH > Mg(OH) > Al(OH) ,则金属性:Na>Mg>Al
2 3
②依据单质与水或非氧化性酸反应置换出氢气的难易程度或剧烈程度来比较:越容易反应或反应越剧烈,则
对应元素的金属性越强
如:Zn与盐酸反应比Fe与盐酸反应更容易,则金属性:Zn>Fe
③依据金属单质之间的置换反应来比较:若xn++y===x+ym+ ,则y比x金属性强
如:Zn+Cu2+===Zn2++Cu,则金属性:Zn>Cu
④依据单质的还原性或离子氧的化性强弱来比较:单质的还原性越强(或离子的氧化性越弱),则对应元素的
金属性越强
如:氧化性:Mg2+>Na+,则金属性:Mg<Na
⑤依据金属活动性顺序来比较:一般来说,排在前面的金属元素其金属性比排在后面的强
如:Fe排在Cu的前面,则金属性:Fe>Cu。
2、元素非金属性强弱的判断方法
(1)非金属性:元素的原子得到电子能力
【微点拨】比较元素非金属性的强弱,其实质是看元素原子得到电子的难易程度,越易得电子,非金属性越强
(2)结构比较法:最外层电子数越多,电子层数越少,非金属性越强
(3)位置比较法:同周期元素,从左到右,随原子序数增加,非金属性增强
同主族元素,从上到下,随原子序数增加,非金属性减弱。非金属性最强的元素为氟
(4)根据元素单质及其化合物的相关性质判断
①依据最高价氧化物的水化物酸性强弱来比较:酸性越强则对应元素的非金属性越强
如:酸性:HClO (最强酸)>H SO (强酸)>H PO (中强酸)>H SiO(弱酸),则非金属性:Cl > S > P > Si
4 2 4 3 4 2 3
②依据非金属元素单质与H 化合的难易程度来比较:化合越容易,非金属性越强
2
如:F 与H 在黑暗中就可反应,Br 与H 在加热条件下才能反应,则非金属性:F>Br
2 2 2 2
③依据形成气态氢化物的稳定性来比较:气态氢化物越稳定,元素的非金属性越强
如:如稳定性:HF>HCl,则非金属性:F>Cl
④依据单质的氧化性或阴离子的还原性越弱来比较:单质的氧化性越强(或离子的还原性越弱),则对应元素
的非金属性越强
如:还原性:S2->Cl-,则非金属性:Cl>S
⑤依据与盐溶液或气体、无氧酸溶液间的置换反应来比较:若An-+B===Bm-+A ,则B比A非金属性强
如:Cl+2KI===2KCl+I,则非金属性:Cl>I
2 2
⑥依据与同一种金属反应,生成化合物中金属元素的化合价的高低进来比较:化合价越高,则非金属性越强
如:Cu+Cl=====CuCl ,2Cu+S=====Cu S,即得非金属性:Cl>S。
2 2 2
【微点拨】
①一般来说,在氧化还原反应中,单质的氧化性越强(或离子的还原性越弱),则元素的非金属性就越强;单
质的还原性越强(或离子的氧化性越弱),则元素的金属性就越强。故一般来说,元素的金属性和非金属性
的强弱判断方法与单质的氧化性和还原性的强弱判断方法是相一致的
②金属性强弱的比较,关键是比较原子失去电子的难易,而不是失去电子数的多少如:Na失去一个电子,而Mg失去两个电子,但Na的金属性比Mg强
③原子半径与元素的金属性、非金属性之间的关系:原子半径越大,最外层电子数越少,越容易失去电子,
金属性越强;原子半径越小,最外层电子数越多,越容易得到电子,非金属性越强。因此:同周期中,从
左到右,原子半径减小,最外层电子数增加,失去电子能力减弱,得到电子能力增强,金属性减弱,非金
属性增强;同主族中,由上往下,原子半径增大,最外层电子数相同,失去电子能力增强,得到电子能力
减弱,金属性增强,非金属性减弱
【即学即练3】
1、X、Y两元素是同周期的非金属主族元素,如果X原子半径比Y的大,下面说法正确的是( )
A.最高价氧化物对应水化物的酸性,X的比Y的强 B.X的非金属性比Y的强
C.X的阴离子比Y的阴离子还原性强 D.X的气态氢化物比Y的稳定
2、下列事实与推论相符的是( )
选项 实验事实 推论
A HO的沸点比HS的沸点高 非金属性:O>S
2 2
B 盐酸的酸性比HSO 的酸性强 非金属性:Cl>S
2 3
C 钾与水的反应比钠与水的反应更剧烈 金属性:Na>K
D HF的热稳定性比HCl的强 非金属性:F>Cl
3、X、Y是元素周期表中ⅦA族的两种元素。下列叙述能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.X的氢化物的沸点比Y的氢化物的沸点低
C.Y的单质能将X从NaX的溶液中置换出来
D.X的气态氢化物比Y的气态氢化物稳定
4、甲、乙两种非金属元素:①甲比乙容易与H 化合;②甲原子能与乙的阴离子发生置换反应;③甲的最高价
2
氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目
比乙的多;⑤甲的单质熔、沸点比乙的低。能说明甲的非金属性比乙强的是( )
A.只有④ B.只有⑤ C.①②③ D.①②③④⑤
5、下列事实能说明氯元素原子得电子能力比硫元素原子强的是________
①HCl的溶解度比HS大 ②HCl的酸性比HS强 ③HCl的稳定性比HS大 ④HCl的还原性比HS弱
2 2 2 2
⑤HClO 的酸性比HSO 强 ⑥Cl 与铁反应生成FeCl ,而S与铁反应生成FeS ⑦Cl 能与HS反应生成S
4 2 4 2 3 2 2
⑧在周期表中Cl处于S同周期的右侧 ⑨还原性:Cl-<S2-
【课后作业 】
1、对于随原子序数依次增大的11~17号元素,下列说法中不正确的是( )
A.原子半径逐渐减小 B.电子层数逐渐增多
C.最高正化合价逐渐增大 D.元素的非金属性逐渐增强
2、下列关于元素周期表和元素周期律的说法错误的是( )
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Mg比Na会多失去1个电子,所以Mg比Na的金属性强
D.O与S为同主族元素,且O比S的非金属性强
3、应用元素周期律分析下列推断,其中正确的组合是( )
①碱金属单质的熔点随原子序数的增大而降低
②Cs是第ⅠA族元素,Cs失电子能力比Na的强
③砹(At)是第ⅦA族,其氢化物的稳定性大于HCl
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A.①③⑤ B.①②⑤ C.②③⑤ D.①②④4、下列各组元素性质或原子结构递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多 B.P、S、Cl元素最高正化合价依次升高
C.N、O、F原子半径依次增大 D.Na、K、Rb的电子层数依次增多
5、A、B、C为三种短周期元素,A、B在同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的
电子层结构。下列说法正确的是( )
A.原子序数:A>B>C B.原子半径:A>B>C
C.离子半径:A2->B2+>C- D.原子最外层电子数:A>C>B
6、下列化合物中,阴离子和阳离子的半径之比最大的是( )
A.CsI B.NaF C.KCl D.LiI
7、下列各组元素中按微粒半径递增顺序排列的是( )
A.K Na Li B.N O F C.Ca2+ K+ Cl- D.Ba2+ Ca2+ Mg2+
8、A、B两元素原子电子层数相同,如果A原子半径比B的大,则下列判断正确的是( )
A.两元素形成的最高价氧化物对应的水化物的酸性应是A强于B
B.A的气态氢化物比B的气态氢化物稳定
C.A的金属性比B的金属性强
D.A的阴离子比B的阴离子还原性弱
9、X、Y为同周期元素,如果X的原子半径大于Y,则下列判断不正确的是( )
A.若X、Y均为金属元素,则X的金属性强于Y
B.若X、Y均为金属元素,则X的阳离子氧化性比Y的阳离子强
C.若X、Y均为非金属元素,则Y的非金属性比X强
D.若X、Y均为非金属元素,则最高价含氧酸的酸性Y强于X
10、短周期金属元素甲~戊在元素周期表中的相对位置如下表所示,下列判断正确的是( )
甲 乙
丙 丁 戊
A.原子半径:丙<丁<戊 B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊 D.最外层电子数:甲>乙
11、下列递变规律不正确的是 ( )
A.HClO、HSO 、HPO 的酸性依次增强 B.钠、镁、铝的还原性依次减弱
4 2 4 3 4
C.HCl、HS、PH 的稳定性依次减弱 D.P、S、Cl三种元素的最高正化合价依次升高
2 3
12、下列结论正确的是( )
①粒子半径:K+>Al3+>S2->Cl- ②氢化物的稳定性:HF>HCl>H S>PH>SiH
2 3 4
③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl>S>Se>Te
2
⑤酸性:HSO >H PO >H CO>HClO ⑥非金属性:O>N>P>Si ⑦金属性:BeO2->Na+ B.气态氢化物稳定性:HBrNaOH>LiOH D.还原性强弱:F->Cl->Br->I-
14、短周期元素X、Y、Z、W的原子序数依次增大。X的原子半径比Y的小,且X与Y的最外层电子数之和
等于Z的最外层电子数。X与W同主族,Z是地壳中含量最高的元素。下列说法不正确的是( )
A.原子半径的大小顺序:r(W)>r(Y)>r(Z)>r(X)
B.元素Z、W的简单离子的电子层结构相同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.X、Y两种元素可形成分别含有10e-和18e-的化合物
15、根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
元素代号 L M Q R T
原子半径/nm 0.160 0.143 0.089 0.102 0.074
主要化合价 +2 +3 +2 +6、-2 -2A.氢化物的沸点为HTA,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则原子序数由小到大的
顺序( )
A.A、B、C、D、E B.E、C、D、B、A C.B、A、D、C、E D.C、D、A、B、E
17、某同学设计实验以探究元素性质的递变规律,实验装置如图所示。
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。已知A装置的烧瓶里装有大理石,分
液漏斗里装有稀HNO,B装置中装有饱和碳酸氢钠溶液,装置C中装有NaSiO 溶液,试回答:
3 2 3
(1)A中反应的离子方程式为______________,C中可观察到的现象是________
(2)B装置的作用是_____________________________________
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是______________,由此得出碳、硅、氮三种元素非
金属性的强弱顺序是______________
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱。
(4)写出B装置中发生反应的离子方程式:___________________
(5)C装置的作用是_____________________________________
(6)实验结论:氧化性____________________,非金属性:_________________
【元素周期律】答案
【即学即练1】
1、C。解析:在同周期中,非金属元素的最高价氧化物对应水化物的酸性从左到右依次增强,A项错误;同周
期的第ⅠA族和第ⅡA族的金属元素比较,第ⅠA族的元素比第ⅡA族的元素的金属性强,但不同周期的是无
法比较的,如Ca的金属性比Na的金属性强,B项错误;ⅦA族元素是同周期中非金属性最强的元素,C项正
确;原子序数为15的元素是P,最外层电子数为5,则最高化合价为+5价,D项错误;答案选C。
2、A。解析:氢化物的酸性与元素在同一周期、同一主族没有递变性和规律性,不能用周期律解释,元素的非
金属性与最高价氧化物对应的水化物的酸性有关,故A符合题意;同周期元素从左到右原子半径减小,则原子
半径P>S>Cl,可解释,故B不符合题意;Cl、S、P的最外层电子数分别为7、6、5,最高正价为+7、+6、+
5,最高正价为Cl>S>P,故C不符合题意;非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水
化物的酸性越强,酸性强弱顺序是HClO>H SO >H PO ,故D不符合题意。
4 2 4 3 4
3、A。解析:本题的关键是“最高价氧化物对应水化物的酸性相对强弱”这一信息,由此可推知X、Y、Z为
非金属元素,原子序数相连意味着它们属同周期元素,故活泼性:X>Y>Z,原子半径:XY>Z,气态氢化物的稳定性顺序为HX>H Y>ZH 。
2 3
【即学即练2】
1、B。解析:A项,4种离子电子层结构相同,随着核电荷数增多,离子半径依次减小,“序小径大”,即 Al3
+r(Rb)>r(K)>r(Na),D错误;S2-和Cl-核外电子数相同,但核电荷数Cl>S,故离子
半径r(S2-)>r(Cl-);Na+和Al3+核外电子数相同,且核电荷数Al>Na,则离子半径,r(Na+)>r(Al3+),B项正确。
2、B。解析:三种元素在周期表中的位置为,可知A、B、C分别为S、Mg、F。A项,原子序数由大到小的顺序应为A>B>C;C项,离子半径应为r(A2-)>r(C-)>r(B2+);D项,最外层电子数应为C>A>B。
3、A:解析:N、S、O、Si、P在元素周期表中的位置如下图所示。原子半径,r(Si)>r(P)>r(S),故磷原子的半
径可能是1.10×10-10 m。
【即学即练3】
1、C。解析:X原子半径比Y的大,说明X在Y的左边,原子序数X比Y小,X的非金属性比Y的弱,因此
最高价氧化物对应水化物的酸性X比Y的弱,X的阴离子比Y的阴离子还原性强,X的气态氢化物不如Y的稳
定。
2、D。解析:A项,HO常温下是液体,HS常温下是气体,沸点HO>HS,但沸点高低是物理性质,与元素
2 2 2 2
的非金属性强弱无关,错误;B项,盐酸是无氧酸,HSO 不是最高价含氧酸,即两者都不属于最高价氧化物的
2 3
水化物,虽然盐酸比HSO 酸性强,也不能证明非金属性:Cl>S;C项,元素的金属性越强,其单质与水或酸
2 3
发生反应产生氢气就越容易,则钾与水的反应比钠与水的反应更剧烈,则金属性 K>Na错误;D项,元素的非
金属性越强,其相应氢化物的稳定性越强,热稳定性:HF>HCl,则非金属性:F>Cl,正确。
3、D。解析:非金属性越强,其单质与H 化合的能力越强,气态氢化物的稳定性越强,最高价氧化物的水化物
2
的酸性越强,能将非金属性较弱的元素的单质从它们的化合物中置换出来。
4、C。解析:由①可知甲的非金属性比乙强,由②可得甲能置换出乙,所以甲比乙的非金属性强,非金属性越
强,最高价氧化物对应水化物的酸性越强,非金属性强弱与非金属反应时得电子多少无关,与单质熔、沸点高
低无关。
5、(1)③④⑤⑥⑦⑧⑨
【课后作业】
1、B。解析:在元素周期表中同一周期的元素从左到右原子半径依次减小,故A不符合题意;在元素周期表中
同一周期的元素电子层数相同,故B符合题意;在元素周期表第三周期,元素的最高正价等于其最外层电子数,
最外层电子数依次增多,故最高正化合价逐渐增大,故C不符合题意。在元素周期表中,同一周期的元素从左
到右,元素的非金属性逐渐增强,故D不符合题意。
2、C。解析:同主族元素从上到下,原子核外电子层数随着核电荷数的增加而增多,A项正确;同周期元素从
左到右,非金属性逐渐增强,B项正确;同周期元素从左到右,金属性逐渐减弱,所以 Mg比Na的金属性弱,
C项错误;同主族元素从上到下,非金属性逐渐减弱,O比S的非金属性强,D项正确。
3、B。解析:①从Li到Cs碱金属的熔点逐渐降低,正确;②同主族元素从上到下金属性逐渐增强,故Cs的金
属性强于Na,Cs失电子能力比Na强,正确;③At的非金属性弱于Cl,非金属性越弱,对应气态氢化物的稳
定性越弱,错误;④N元素气态氢化物为NH ,溶于水后显碱性,错误;⑤碱性:NaOH>Mg(OH) >Al(OH) ,
3 2 3
正确。
4、C。解析:N、O、F同为第二周期元素,随着原子序数的增加,原子半径依次减小。
5、A。解析:由题意可知A、B、C三种元素的位置关系可以表示为
,由此可知原子序数:A>B>C,A正确;原子半径:B>A>C,B错误;
离子半径:A2->C->B2+,C错误;原子最外层电子数:C>A>B,D错误。
6、D。解析:阳离子都为碱金属元素的阳离子,元素的核电荷核数越大,离子半径越大,阴离子都为卤素阴离
子,元素的核电核数越大,离子半径越大,则金属离子半径最小的是 Li+,阴离子半径最大的是I-,所以阴离
子半径和阳离子半径之比最大的是LiI。
7、C。解析:同主族自上而下原子半径逐渐增大,则原子半径大小为 LiO>F,B错误;离子电子层结构相同,核电荷数越大离子半径越小,
则离子半径大小为Ca2+Ca2+>Mg2+,D错误。
8、C。解析:A、B两元素位于同周期,A的原子半径比B的大,则A位于B的左边,A元素的金属性比B的
强。
9、B。解析:X、Y为同周期元素,由原子半径:X>Y可知原子序数:X<Y,若二者均为金属元素,则有金
属性:X>Y,阳离子的氧化性:X<Y;若二者均为非金属元素,则有非金属性:Y>X,最高价含氧酸的酸性:
Y>X。
10、C。解析:根据元素周期律可知,同周期元素自左向右,原子半径逐渐减小,最外层电子数逐渐增多,故
A、D两项错误;同周期金属元素从左到右,最高价氧化物对应的水化物碱性逐渐减弱,故C项正确;同主族
元素自上而下,金属性逐渐增强,故B项错误。
11、A。解析:非金属性:Cl>S>P,元素的非金属性越强,最高价氧化物对应的水化物的酸性越强,则
HClO 、HSO 、HPO 的酸性依次减弱,故A项错误;金属性:Na>Mg>Al,元素的金属性越强,对应的单质
4 2 4 3 4
的还原性越强,则钠、镁、铝的还原性依次减弱,故B项正确;非金属性:Cl>S>P,元素的非金属性越强,对
应的氢化物越稳定,故C项正确;P、S、Cl三种元素原子的最外层电子数分别为5、6、7,最高正化合价分别
为+5、+6、+7,故D项正确。
12、C
13、D。解析:核外电子排布相同的离子,核电荷数越大,离子半径越小,所以 O2->Na+,电子层数多的离子,
半径越大,因此离子半径大小为 S2->O2->Na+,A 正确;非金属性:F>Cl>Br,气态氢化物的稳定性为
HBrNa>Li,对应最高价氧化物的水化物的碱性为 KOH>NaOH>LiOH,C正确;
非金属性:F>Cl>Br>I,对应离子的还原性为F-r(N)>r(O)>r(H),正确;B项,O2-、Na+的核外电子数相等,均为10,即电子层结构相同,正确;
C项,稳定性:HO>NH ,错误;D项,NH 为10e-微粒,而NH 为18e-微粒,正确。
2 3 3 2 4
15、C。解析:由信息表中的原子半径和主要化合价可以判断出 T为O,R为S,Q为Be,M为Al,L为Mg。
HO的沸点高于HS,A错误;Mg的金属性强于Be,与HCl反应的速率Mg>Be,错误;Al3+、O2-相同的电子
2 2
层数,核电荷数越大,半径越小,即r(Al3+)A,故B和A在左端,且原子序数
BD,则C和D为非金属,靠近右端,原子序数DH CO >H SiO N>C>Si
3 2 3 2 3
(4)Cl+2Br-===Br +2Cl-
2 2
(5)吸收尾气,防止氯气污染环境
(6)Cl>Br Cl>Br
2 2
解析:(1)A中硝酸与碳酸钙反应产生二氧化碳:CaCO +2HNO===Ca(NO) +CO↑+HO,证明碳酸的酸性比
3 3 3 2 2 2
硅酸强,C 中发生反应:NaSiO +CO +HO===H SiO↓+NaCO 或 NaSiO +2CO +2HO===2NaHCO +
2 3 2 2 2 3 2 3 2 3 2 2 3
HSiO↓,因此C中产生白色沉淀或溶液变浑浊。
2 3
(2)由于硝酸具有挥发性,为避免硝酸与硅酸钠反应而干扰二氧化碳与硅酸钠溶液反应,必须净化二氧化
碳,利用饱和碳酸氢钠溶液吸收硝酸蒸气。
(3)由实验现象可知三种酸中,硝酸酸性最强,硅酸酸性最弱;由此推知,氮的非金属性最强,硅的非金
属性最弱。在元素周期表中,氮和碳位于同一周期,碳与硅位于同一主族,由此可以推出同主族、同周期非金
属元素性质的递变规律。
(4)题目已限制探究氯与溴的非金属性强弱,所以B中应装溴化钾或溴化钠溶液。
(5)由于尾气中含有氯气,故要用碱溶液吸收,以避免污染环境。
(6)根据置换反应可得出单质的氧化性强弱。