文档内容
第四章 物质结构 元素周期律
第一节 原子结构与元素周期表
本章内容是继氧化还原反应和离子反应之后又一个化学的理论知识点,通过本章的学习
可以体会化学也是有规律可循的,本节内容是本章的基础,也是整个周期表周期律的基
础,这一节学不好,就很难体会化学上结构决定性质的奥秘,也就很难体会化学的规律
性,本节内容共有13个重点内容,静下心来慢慢体会吧!
一、核外电子排布的表示方法
(1)原子结构示意图
①小圆圈和圆圈内的符号及数字表示原子核及核内质子数。
②弧线表示电子层。
③弧线内数字表示该层中的电子数。
(2)离子结构示意图
①当主族中的金属元素原子失去最外层所有电子变为离子时,电子层数减少一层,形成与少一个电子层的稀有气
体元素原子相同的电子层结构。
②非金属元素的原子得电子形成简单离子时,形成与电子层数相同的稀有气体元素原子相同的电子层结构。
对点练习1(2020·上海市奉贤区奉城高级中学高一期末)有四种微粒的结构示意图,下列叙述中错误的是( )
它们属于不同种元素
它们的核外电子排布相同
它们都是离子
它们都具有稀有气体原子的稳定结构
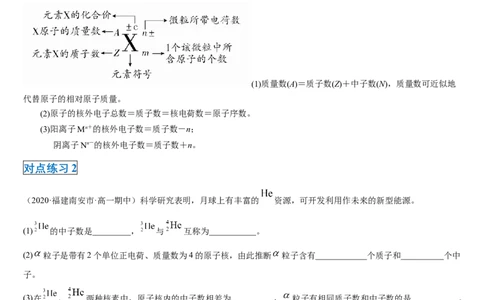
二、 明确符号X中各个字母的含义并了解它们之间的关系
(1)质量数(A)=质子数(Z)+中子数(N),质量数可近似地
代替原子的相对原子质量。
(2)原子的核外电子总数=质子数=核电荷数=原子序数。
(3)阳离子Mn+的核外电子数=质子数-n;
阴离子Nn-的核外电子数=质子数+n。
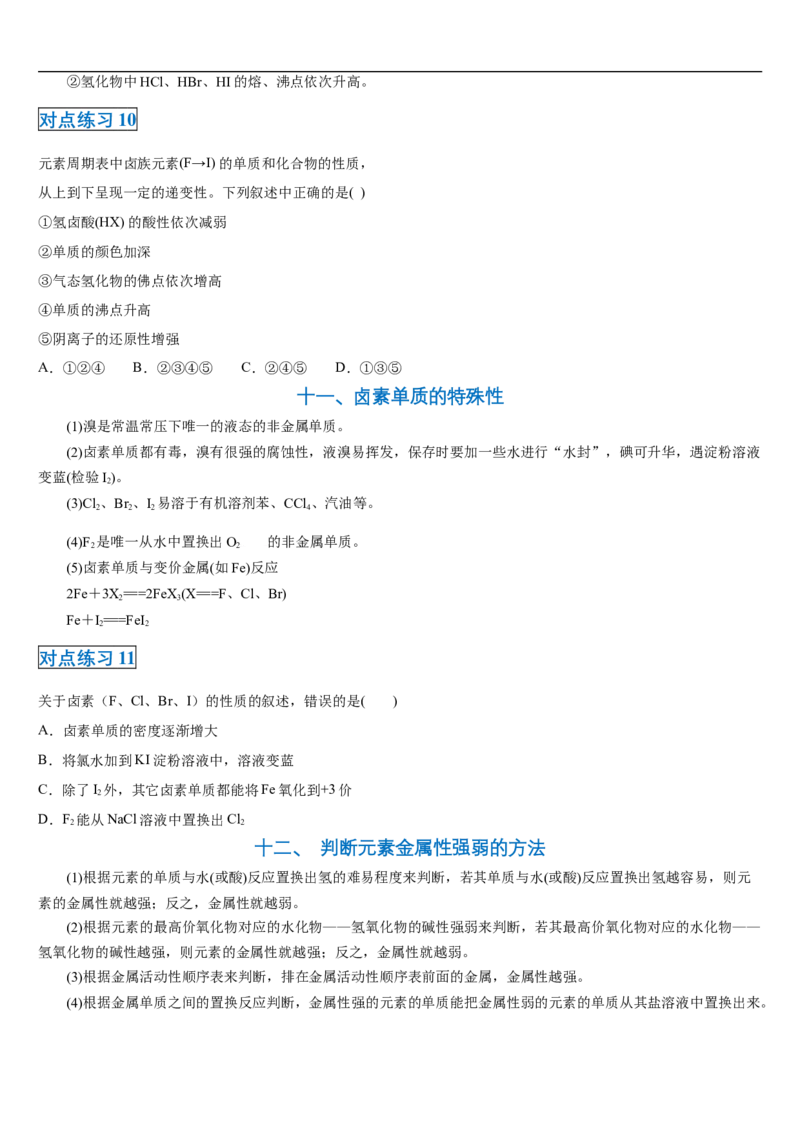
对点练习2
(2020·福建南安市·高一期中)科学研究表明,月球上有丰富的 资源,可开发利用作未来的新型能源。
(1) 的中子数是_________, 与 互称为___________。
(2) 粒子是带有2个单位正电荷、质量数为4的原子核,由此推断 粒子含有____________个质子和__________个中
子。
(3)在 、 两种核素中,原子核内的中子数相差为__________, 粒子有相同质子数和中子数的是___________。
三、同位素、同素异形体的判断和理解
(1)同种元素可以有多种不同的核素,即可存在不同的原子,所以元素的种类数远小于原子的种类数。
(2)判断某组微粒是同位素还是同素异形体,关键是要确定微粒的类别。只有原子才可能是同位素,单质才可能是
同素异形体。
对点练习1
下列说法正确的是 ( )
A.红磷、白磷属于同位素 B.H、D 属于同素异形体
2 2C.40 K、40 Ca互为同位素 D.H、D、T互为同位素
19 20
四、 构成原子的粒子数目与元素种类、原子种类的关系
对点练习4
有①质子数②中子数③核外电子数④价电子数
⑤最外层电子数⑥电子层数。请用上述序号回答:
(1)原子种类由 决定,元素种类由 决定。
(2)原子的质量数由 决定,元素在周期表中的位置由 决定。
五、主族元素原子结构与其在周期表中的位置关系
(1)核外电子层数=周期数。
(2)主族序数=最外层电子数=最高正价(O,F除外)=8-|最低负价|。
(3)元素原子的K、L、M层电子数为偶数时,K、L、M不一定是最外层,即使是最外层也不一定是主族元素,
如零族。
对点练习5
根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
A.K层电子数为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子数为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子数为偶数的所有主族元素所在族的序数与该元素原子L层电子数相等
D.M层电子数为奇数的所有主族元素所在族的序数与该元素原子M层电子数相等
六、根据稀有气体元素的原子序数确定
主族元素在周期表中的位置的方法
(1)记住稀有气体元素的原子序数(He、 Ne、 Ar、 Kr、 Xe、 Rn、 Uuo),便可确定主族元素的位置。
2 10 18 36 54 86 118
(2)原子序数-最邻近的稀有气体元素的原子序数=ΔZ
①若ΔZ>0,则位于稀有气体元素下一周期,族序数为ΔZ;
②若ΔZ<0,则与稀有气体元素同周期,族序数为8-|ΔZ|。
对点练习6
115号元素在元素周期表中的位置是
A.第七周期第VIIA族 B.第七周期第VA族C.第七周期第VIIB族 D.第七周期第VB族
七、“相邻”两元素的原子序数差
(1)同周期相邻主族元素原子序数差。
①第二周期到第七周期非第ⅡA族和第ⅢA族
同周期相邻元素原子序数差为1。
②同周期第ⅢA族与第ⅡA族元素原子序数差从
第二周期到第七周期分别依次为1,1,11,11,25,25。
(2)同主族及0族上下相邻元素原子序数差。
①若为第ⅠA、ⅡA族元素:相差上一周期全部元素种数。
②若为第ⅢA~ⅦA族、0族元素:相差下一周期全部元素种数。
对点练习7
下列说法正确的是
A.同一周期中的第ⅡA族和第ⅢA族元素的原子序数差一定为1
B.L层上的电子数为奇数的元素一定是主族元素
C.同一主族相邻两个周期的元素的原子序数差为上一周期所含元素种类
D.族序数等于周期序数的元素一定是金属元素
八、特殊的原子结构与其在周期表中的位置
(1)族序数等于周期数的元素是:H元素、Be元素、Al元素;族序数等于周期数2倍的元素是:C元素、S元素;
族序数等于周期数3倍的元素是:O元素;
(2)周期数是族序数2倍的元素是:Li元素;周期数是族序数3倍的元素是:Na元素;
对点练习8
(2020·全国高一课时练习)周期表中特殊位置的短周期元素
①族序数等于周期数的元素:___;
②族序数等于周期数2倍的元素:___;
③族序数等于周期数3倍的元素:___;
④周期数是族序数2倍的元素:___;
⑤周期数是族序数3倍的元素是:___;
⑥最高正价不等于族序数的元素是:___。
九、 碱金属的相似性和递变性(用R表示碱金属元素)
(相似性)(递变性)
(1)与O 反应
2
从Li→Cs,与O 反应越来越剧烈,产物越来越复杂,如Li与O 反应只能生成LiO,Na与O 反应还可以生成
2 2 2 2
NaO,而K与O 反应能够生成KO 等。
2 2 2 2
(2)与HO(或酸)的反应
2
从Li→Cs,与HO(或酸)反应越来越剧烈,如K与HO反应可能会发生轻微爆炸,Rb和Cs遇水发生剧烈爆炸。
2 2
(3)最高价氧化物对应水化物的碱性
碱性:LiOH”、“<”或“=”)。
3 4 2 4 3 4 2 4
③简单氢化物的熔沸点:HO___________H S(填“>”、“<”或“=”)。
2 2
(4)①Se Cl 常用作分析试剂,其电子式为___________。
2 2
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是___________(填字母)。
A.原子半径:In>Se
B.In 的金属性比 Se 强
C.In 的金属性比 Al 弱
D.硒化铟的化学式为 InSe
2
(5)请设计实验比较 C、Si 的非金属性强弱顺序(可供选择的药品有:CaCO 固体、稀硫酸、盐酸、饱和NaHCO 溶液、
3 3
饱和 NaCO 溶液、硅酸钠溶液,化学仪器根据需要选择)。
2 3
实验步骤 实验现象与结论
在试管中加入_______,再加入_______,将生成气体通过 _____洗气后,通入 现象: ___结论:非金属性
_____。 C>Si
20.(2020·全国高一课时练习)某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
Ⅰ.探究同周期元素性质的递变规律
(1)相同条件下,将钠、镁、铝各1 mol分别投入到足量的同浓度的稀盐酸中,试预测实验结果:___________与稀盐
酸反应最剧烈;___________与稀盐酸反应产生的气体最多。
(2)向NaSiO 溶液中加入稀HSO 出现白色沉淀,可证明S的非金属性比Si强,反应的离子方程式为___________。
2 3 2 4
Ⅱ.探究同主族元素非金属性的递变规律
某研究性学习小组设计了一组实验来探究ⅦA族元素原子的得电子能力强弱规律。图中A、B、C是三个可供选择制
取氯气的装置,装置D的玻璃管中①、②处依次放置蘸有NaBr溶液、NaOH浓溶液的棉球。
(3)写出装置B中仪器a的名称___________。(4)实验室制取氯气还可采用如下原理:2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O,依据该反应原理选择
4 2 2 2
___________(填“A”或“B”或“C”)装置制取氯气。
(5)反应装置的导气管连接装置D的X导管,①处发生反应的离子方程式为:___________。②处发生反应的离子方程
式为:___________。