文档内容
第四章 物质结构 元素周期律
第二节 元素周期律
第2课时 元素周期表和周期律的应用
(1)基于元素“位置-结构-性质”认识元素性质,基于物质“结构-性质-用途”认识物质性质,基于元素性
质递变的本质原因认识物质世界。
(2)加深对分类法、归纳法等科学方法的认识,提高逻辑推理能力、论证能力,从而发展证据推理与模型认
知的化学学科核心素养。
【内容分析】
对于中学阶段重要的理论知识,教材编写体现学科知识的逻辑性,重视推理,借助实验和事实进行分析;应
用演绎、归纳的方法,培养学生的逻辑思维能力。本节内容在讨论了碱金属元素的金属性、卤族元素的非
金属性变化规律,第三周期元素性质的递变规律之后展开,使学生进一步认识“构” “位”“性”的关
系。通过学习族和周期元素性质的变化,可以使学生综合认识元素性质的周期性递变规律,从而归纳出元素
周期律,了解元素周期表和周期律的应用,对“构”“位”“性”的关系有进一步的认识。
【教学重点和难点】
重点:元素性质与原子结构的关系
难点:元素性质与原子结构的关系
【教学流程】
【思考与讨论】
门捷列夫在他的第一张周期表 上留下的空位中的元素“类铝”于 1875年由法国化学家布瓦博德朗发现,
并命名为镓,而布瓦博德朗当时并未受到门捷列夫预言的启发。门捷列夫在得知这一发现后指出:他相信镓
和“类铝”是同一种物质,并认为镓的密度应该是5.9~ 6.0 g/cm3,而不是布瓦博德朗发表的4.7 g/cm3。当时布瓦博德朗认为只有他本人才拥有镓,门捷列夫怎么会知道这种金属的密度呢?他没有固执已见,重新
提纯了镓,最后测得的密度果然是5.94 g/cm'。这一发现使他大为惊讶,他在一篇论文中写道:“我以为没有
必要再来说明]捷列夫这一-理论的巨 大意义了。”
(1)阅读上述资料,你得到什么启示?写一篇小论文与同学交流。
①理论指导实践,实践检验理论;
②勇于创新,敢于质疑的科学精神对推动科学进步的作用;
③严谨求实的科学态度在科学实验中的意义
(2)请你查阅资料,了解门捷列夫还预言了哪些新元素,以及当时这些新元素是如何被确认的,撰写研究报告,
并与同学交流。
【设计意图】通过化学史,感受元素周期表的魅力,提升学生的学习积极性,落实科学态度和社会责任素
养。
【学习任务一】认识元素位、构、性的关系
元素周期律的发现,对化学的发展有很大的影响。作为元素周期律表现形式的元素周期表,反映了元素之
间的内在联系,是学习、研究和应用化学的一种重要工具。
一、原子半径的变化规律
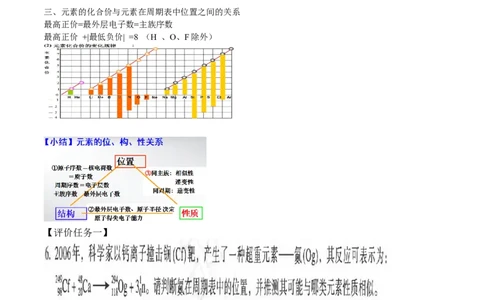
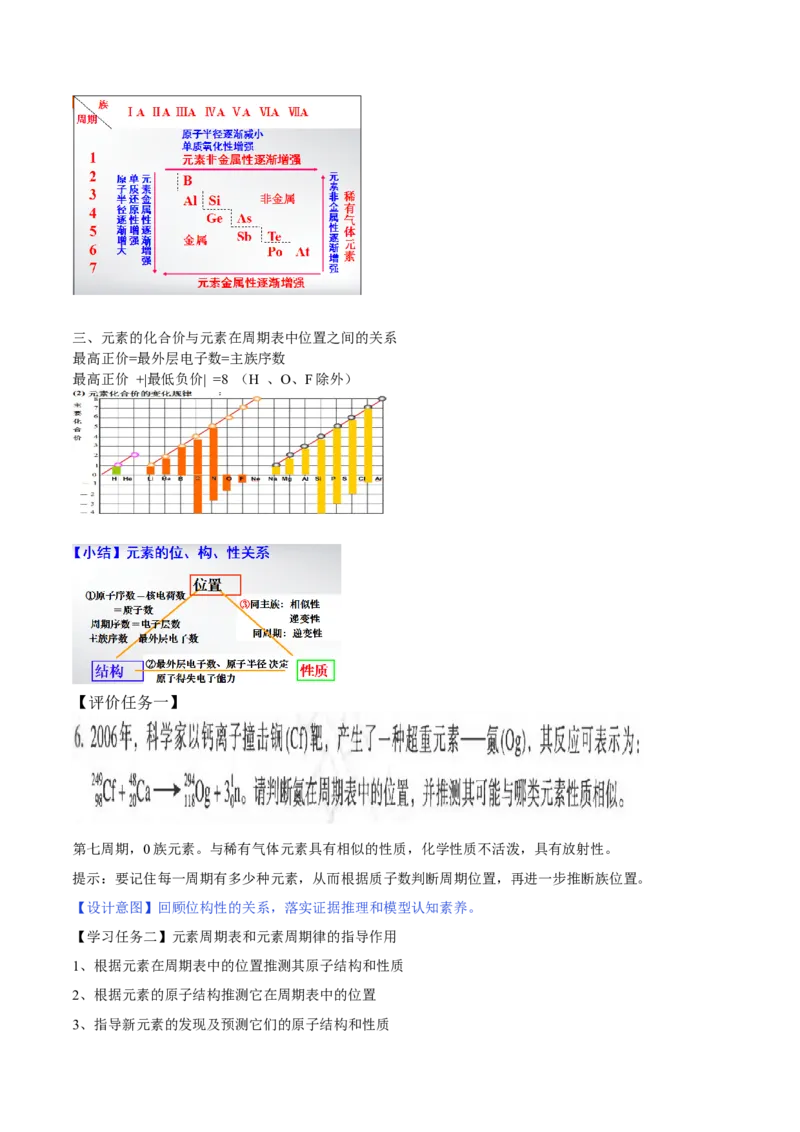
二、原子半径与性质的关系三、元素的化合价与元素在周期表中位置之间的关系
最高正价=最外层电子数=主族序数
最高正价 +|最低负价| =8 (H 、O、F除外)
【评价任务一】
第七周期,0族元素。与稀有气体元素具有相似的性质,化学性质不活泼,具有放射性。
提示:要记住每一周期有多少种元素,从而根据质子数判断周期位置,再进一步推断族位置。
【设计意图】回顾位构性的关系,落实证据推理和模型认知素养。
【学习任务二】元素周期表和元素周期律的指导作用
1、根据元素在周期表中的位置推测其原子结构和性质
2、根据元素的原子结构推测它在周期表中的位置
3、指导新元素的发现及预测它们的原子结构和性质4、指导其他与化学相关的科学技术。
在周期表中一定的区域内寻找有特定性质的物质
(1)寻找半导体材料
(2)寻找制取农药的元素
(3)寻找催化剂、耐高温、耐腐蚀的合金材料
【评价任务二】
镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。下列有关镓和镓的化合物的
说法正确的是 ___(填字母序号)。
A.一定条件下,Ga可溶于盐酸和氢氧化钠
B.常温下,Ga可与水剧烈反应放出氢气
C.一定条件下,Ga(OH)3可与NaOH反应生成盐
【答案】AC
【评价任务三】
1782年,奥地利首都维也纳一家矿场监督牟勒是第一个提取出碲的人,他在罗马尼亚的一个矿坑中在当
地人称为“奇异金”的矿石中提取出碲。碲(Te)是与O、S同主族的元素,位于第五周期。据此,推断碲的相
关性质错误的是 ( )
A.碲的单质在常温下是固态
B.碲的常见化合价是-2、+4、+6
C.碲可能作半导体材料
D.碲的氢化物H2Te很稳定
【答案】D
【评价任务四】比较以下微粒半径大小
1、F、Cl、Br
2、Na、Mg、Al
3、 N、P、Si4、 Na 、 Na+
5、 Na+、O2—
【设计意图】通过元素周期表和周期律的应用,掌握化学学习的方法,感受化学魅力。
【思考】与Ne原子电子层结构相同的粒子有?与Ar原子电子层结构相同的粒子有?
【评价任务五】
【答案】B
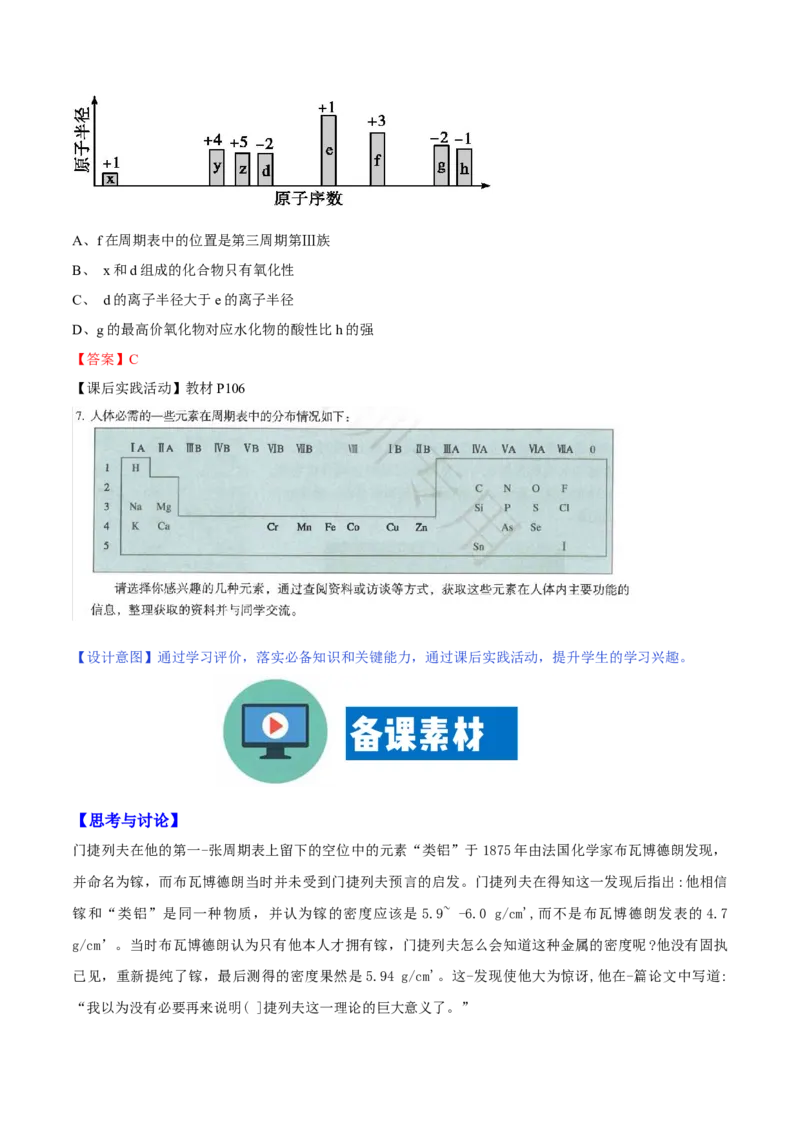
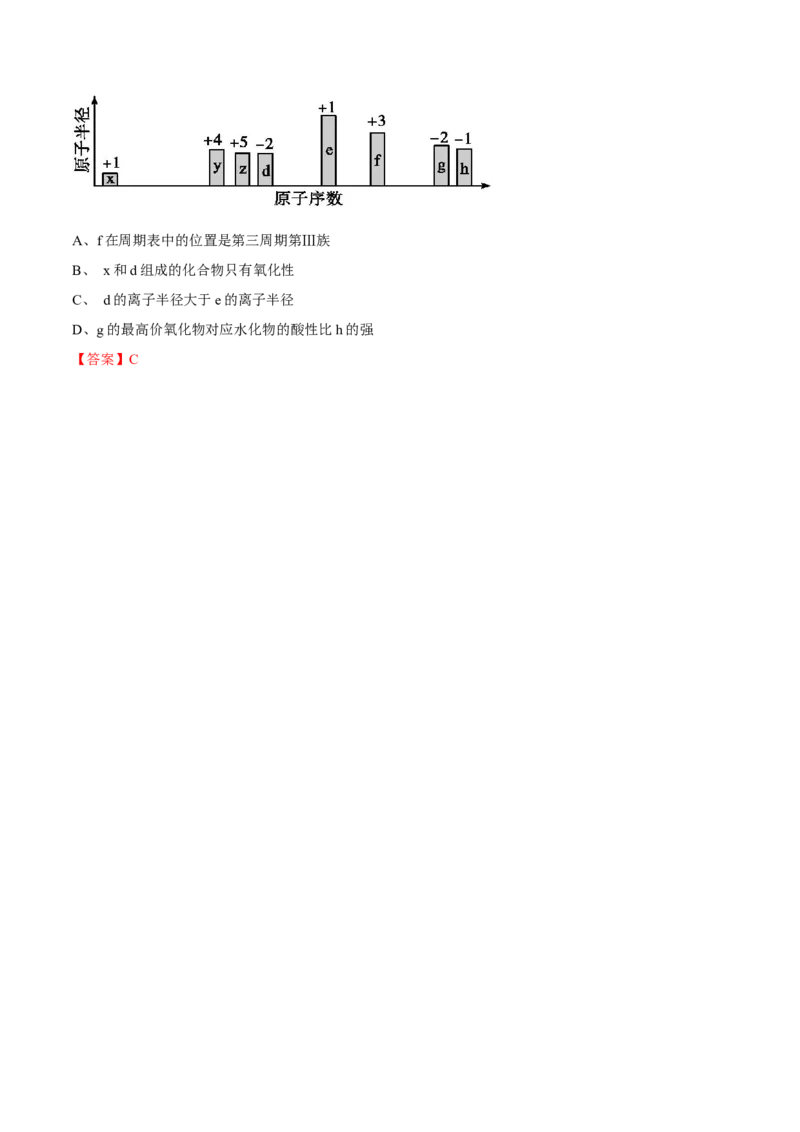
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图
所示。下列说法正确的是( )A、f在周期表中的位置是第三周期第Ⅲ族
B、 x和d组成的化合物只有氧化性
C、 d的离子半径大于e的离子半径
D、g的最高价氧化物对应水化物的酸性比h的强
【答案】C
【课后实践活动】教材P106
【设计意图】通过学习评价,落实必备知识和关键能力,通过课后实践活动,提升学生的学习兴趣。
【思考与讨论】
门捷列夫在他的第一-张周期表上留下的空位中的元素“类铝”于1875年由法国化学家布瓦博德朗发现,
并命名为镓,而布瓦博德朗当时并未受到门捷列夫预言的启发。门捷列夫在得知这一发现后指出:他相信
镓和“类铝”是同一种物质,并认为镓的密度应该是 5.9~ -6.0 g/cm',而不是布瓦博德朗发表的 4.7
g/cm’。当时布瓦博德朗认为只有他本人才拥有镓,门捷列夫怎么会知道这种金属的密度呢?他没有固执
已见,重新提纯了镓,最后测得的密度果然是5.94 g/cm'。这-发现使他大为惊讶,他在-篇论文中写道:
“我以为没有必要再来说明( ]捷列夫这一理论的巨大意义了。”(1) 阅读上述资料,你得到什么启示?写- -篇小论文与同学交流。
提示:立意角度可选择①理论指导实践,实践检验理论;②勇于创新,敢于质疑的科学精神对推动科学进步
的作用;③严谨求实的科学态度在科学实验中的意义;等等。
(2)请你查阅资料,了解门捷列夫还预言了哪些新元素,以及当时这些新元素是如何被确认的,撰写
研究报告,并与同学交流。
提示:门捷列夫还预言了“类硼”(钪)、“类硅”(锗)。
【科学史话】
门捷列夫的预言
【练习与应用】教材P106
3.元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )。
A.左下方区域的金属元素
B.金属元素和非金属元素分界线附近的元素
C.右上方区域的非金属元素
D.稀有气体元素
4.比较下列各组元素中金属性或非金属性的强弱。
(1)Na、K
(2)P、CI
(3)S、Cl
(4)0、S
5.根据元素在周期表中的位置,判断下列各组化合物的酸、碱性强弱。
(1 )H PO 和HNO ( 2)KOH和Mg(OH) (3 )AI(OH) 和Mg(OH)
3 4 3 2 3 2
6. 2006年,科学家以钙离子撞击锎(Cf)靶,产生了一种超重元素一氟(Og), 其反应可表示为:
。请判断氮在周期表中的位置,并推测其可能与哪类元素性质相似。
【答案】
3. B
4. (1)金属性: Na< K(2)非金属性: PS
5. (1)酸性: HPO < HNO
3 4 3
(2)碱性: KOH > Mg(OH)
2
(3)碱性: Al(OH) < Mg(OH)
3 2
6.第七周期,0族元素。与稀有气体元素具有相似的性质,化学性质不活泼,具有放射性。
【补充练习】
镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似。下列有关镓和镓的化合物的
说法正确的是 ___(填字母序号)。
A.一定条件下,Ga可溶于盐酸和氢氧化钠
B.常温下,Ga可与水剧烈反应放出氢气
C.一定条件下,Ga(OH)3可与NaOH反应生成盐
【答案】AC
1782年,奥地利首都维也纳一家矿场监督牟勒是第一个提取出碲的人,他在罗马尼亚的一个矿坑中在当地人
称为“奇异金”的矿石中提取出碲。碲(Te)是与O、S同主族的元素,位于第五周期。据此,推断碲的相关性
质错误的是 ( )
A.碲的单质在常温下是固态
B.碲的常见化合价是-2、+4、+6
C.碲可能作半导体材料
D.碲的氢化物H2Te很稳定
【答案】D
【答案】B
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图
所示。下列说法正确的是( )A、f在周期表中的位置是第三周期第Ⅲ族
B、 x和d组成的化合物只有氧化性
C、 d的离子半径大于e的离子半径
D、g的最高价氧化物对应水化物的酸性比h的强
【答案】C