文档内容
第三章 铁 金属材料
第二节 金属材料
第2课时 物质的量在化学方程式计算中的应用
(1)能基于物质的量认识化学变化;
(2)运用物质的量及相关物理量根据化学方程式进行简单计算,感受定量研究对化学科学的重要作用。
【内容分析】
本节内容包括"金属材料"和"物质的量在化学方程式计算中的应用"两部分内容。教材按照"铁合金→铝
和铝合金→新型合金"的顺序介绍了金属材料。在第二章的第三节"物质的量"里,教材介绍了摩尔、摩尔质
量、气体摩尔体积、物质的量浓度等基本概念,为了分散学习难点,把"物质的量在化学方程式计算中的应
用"安排在本节里。
教材在这一节的最后安排了物质的量在化学方程式中的应用,利用方程式中各物质的化学计量数之
比等于各物质的物质的量之比,通过一个例题把在第二章里学习的物质的量、摩尔质量、气体摩尔体积、
物质的量浓度等知识应用化学方程式的计算中,分散了第二章集中学习物质的量及相关概念的难点。
【教学重点和难点】
重点∶物质的量在化学方程式计算中的应用。
难点∶物质的量在化学方程式计算中的应用。
【教学流程】
【引入】物质是由原子、分子、离子等粒子构成的,物质之间的化学反应也是这些粒子按一定的数目关系
进行的。化学方程式中的化学计量数可以明确地表示出化学反应中粒子之间的数目关系。
【学习任务一】以H 和O 反应为例,从物质的量角度认识化学方程式的意义。
2 2
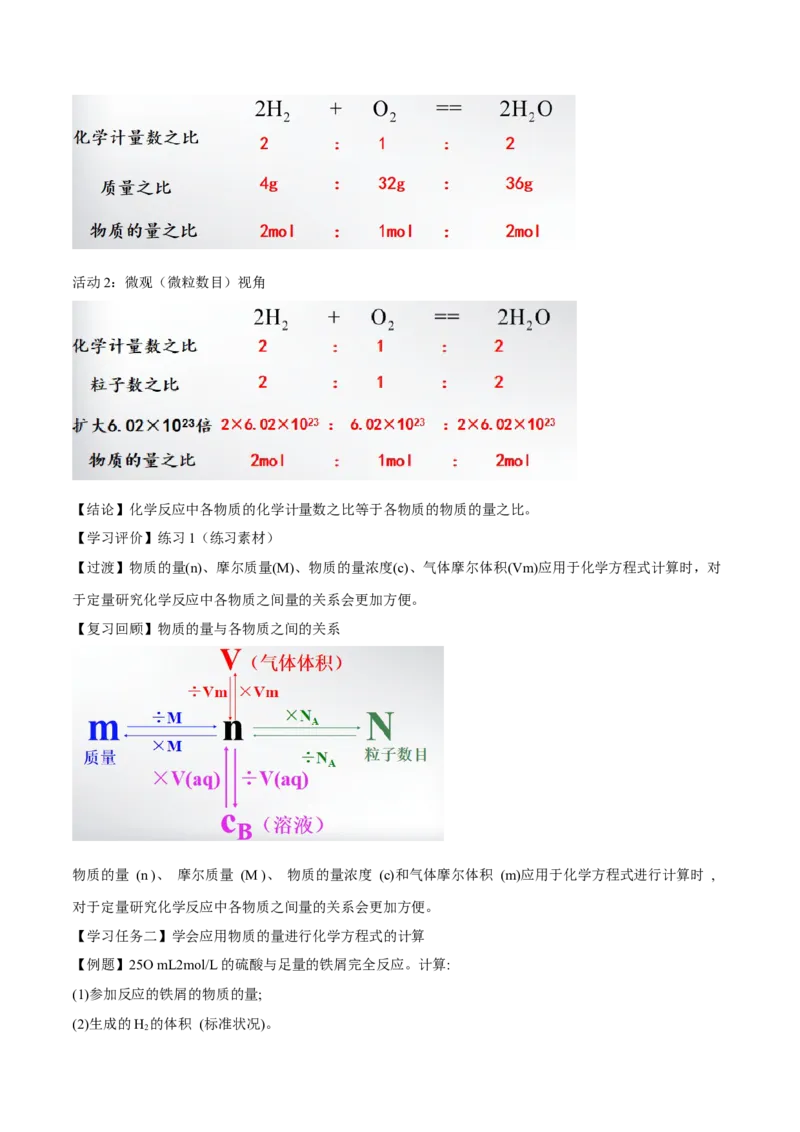
活动1:宏观(质量关系)视角活动2:微观(微粒数目)视角
【结论】化学反应中各物质的化学计量数之比等于各物质的物质的量之比。
【学习评价】练习1(练习素材)
【过渡】物质的量(n)、摩尔质量(M)、物质的量浓度(c)、气体摩尔体积(Vm)应用于化学方程式计算时,对
于定量研究化学反应中各物质之间量的关系会更加方便。
【复习回顾】物质的量与各物质之间的关系
物质的量 (n )、 摩尔质量 (M )、 物质的量浓度 (c)和气体摩尔体积 (m)应用于化学方程式进行计算时 ,
对于定量研究化学反应中各物质之间量的关系会更加方便。
【学习任务二】学会应用物质的量进行化学方程式的计算
【例题】25O mL2mol/L的硫酸与足量的铁屑完全反应。计算:
(1)参加反应的铁屑的物质的量;
(2)生成的H 的体积 (标准状况)。
2【分析 】根据硫酸的体积和HSO 的物质的量浓度求算可计算出参加反应的HSO 的物质的量。然后根据
2 4 2 4
化学反应中各物质之间的化学计量数之比,计算出参加反应的铁屑的物质的量和生成的H 的体积。
2
解:n(H SO )=cV=0.25L×2mol/L=0.5mol
2 4
(1)Fe + H SO === FeSO + H
2 4 4 2
1 1
n(Fe) 0.5mol
1/1=n(Fe)/0.5mol; n(Fe)=0.5mol
(2)Fe + H SO === FeSO + H
2 4 4 2
解法一: 1 1
0.5mol n(H )
2
1/1=n(H )/0.5mol; n(H )=0.5mol ;
2 2
标况下,V(H )=n(H)×22.4L/mol=0.5mol×22.4L/mol=11.2L
2 2
(2)Fe + H SO === FeSO + H
2 4 4 2
解法二: 1 mol 22.4L
0.5mol V(H )
2
1mol/0.5mol=22.4L/V(H ); V(H )=11.2L ;
2 2
答:(1)参加反应的铁屑物质的量为0.5mol;
(2)标准状况下,生成H 体积为11.2L。
2
【变式】【例题】25O mL2mol/L的硫酸与足量的铁屑完全反应。
若求算生成的H 的质量,还可以怎样列关系式?
2
Fe + H SO === FeSO + H
2 4 4 2
1 mol 2g
0.5mol m(H )
2
1mol/0.5mol=2g/m(H ); m(H )=1g ;
2 2
【设计意图】通过例题的讲解,重点让学生掌握怎么通过化学方程式求算有关物理量,解题的关键——反
应中各物质的化学计量数之比等于各物质的物质的量之比,利用其它物理量列比例关系时必须注意:①左
右物理量关系要成比例;②上下单位(物理量)要相一致。
【总结】
利用化学方程式进行计算的步骤:
(1)审题并设有关物理量(n、m、V)
(2)写出正确的化学方程式
(3)在方程式有关物质的化学式下方标出相关物理量注意:注意左右比例相当,上下单位一致
(4)列出正确比例式求解
【学习评价】练习2
【学习任务三】化学计算中常用的方法
1、关系式法
化学计算的依据是物质之间量的比例关系,这种比例关系通常可从化学方程式或化学式中得到。
例如:2Al+2NaOH+2H O===2NaAlO +3H ;有关Al和NaOH、H 的反应比例关系为:
2 2 2 2
2Al------2NaOH----------3H
2
【过渡】有些反应很复杂,或者如已知和待求物之间是靠很多个反应来联系的,这时直接确定已知量和未
知量之间的比例关系求解。如何快速确定已知量和未知量之间的关系式呢?
已知量与未知量之间关系式的确定常用方法
2、守恒法的应用
(1)质量守恒:反应前后元素的原子个数守恒;
例如:2.3g金属钠通过多步反应完全转化为_______molNa CO。
2 3
列关系式: 2Na-----Na CO
2 3
(2)得失电子守恒:氧化剂得电子数目等于还原剂失电子数目。
例如:由金属铝或碱反应制备H,根据得失电子守恒确定关系式:2Al---3H
2 2
(3) 电荷守恒:
电解质溶液中,阴离子所带负电荷总数等于阳离子所带正电荷总数;
离子方程式中,反应物所带电荷总数等于生成物所带电荷总数且电性相同。
【学习评价】练习3、4
【练习素材】1、2.3g的金属钠放入足量水中,若所得溶液体积为VL,则溶液中含溶质的浓度为___________;含Na+数目
为____________。
【答案】
2、标准状况下,2.7g铝与足量的盐酸反应生成aL的氢气,化学方程式比例关系正确的是( )
【答案】C
3、(P80教材习题6)相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压
下体积之比为( )。
A.1:1 B.1:6
C.2:3 D.3:2
【答案】A
4、(教材P80练习与应用10)把5.4gAl放入足量氢氧化钠溶液中完全反应,计算生成氢气的体积(标准状
况下)。