文档内容
第一章 物质及其变化
专题2 化学键 分子间作用力和氢键
课时作业
基础达标
1.下列关于化学键的说法中,不正确的是
A.化学反应过程包含反应物中化学键断裂和生成物中化学键形成
B.氯化氢气体溶解于水产生氢离子和氯离子的过程中有离子键被破坏
C.化学键是相邻原子或离子间的强烈的相互作用
D.非极性键属于一种化学键
2.下列叙述正确的是( )
A.离子键、共价键、分子间作用力均属于化学键
B.氯气中含离子键
C.共价化合物中一定含有共价键
D.所有物质一定含有化学键
3.下列每组中各物质内既有离子键又有共价键的一组是( )
A.NaOH、HSO 、(NH )SO B.MgO、NaSO 、NH HCO
2 4 4 2 4 2 4 4 3
C.NaO、KOH、NaSO D.HCl、Al O、MgCl
2 2 2 4 2 3 2
4.下列说法错误的是( )
A.稀有气体分子中不存在化学键
B.离子化合物中不一定含有金属元素
C.含有非极性键的化合物,不一定是共价化合物
D.阴、阳离子通过静电引力所形成的化学键叫离子键
5.实验室利用反应2NH Cl+Ca(OH) =====CaCl2+2HO制取氨气。在Pt催化条件下,
4 2 2
NH 可发生催化氧化反应:4NH +5O =====4NO+6H O。下列关于NH Cl说法正确的是
3 3 2 2 4
A.只含离子键 B.只含共价键
C.既含离子键也含共价键 D.既不含离子键也不含共价键
6.下列说法正确的是( )
A.分子间作用力与化学键的大小相当
B.分子间作用力的大小远大于化学键,是一种很强的作用力C.分子间作用力主要影响物质的化学性质
D.分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间也存在相互作
用,称为分子间作用力
7.下列说法正确的是 ( )
A.HO分子间存在氢键,所以HO比HS稳定
2 2 2
B.He、CO 和CH 都是由分子构成,它们中都存在共价键
2 4
C.PCl 中各微粒最外层均达到8电子稳定结构
5
D.NaHCO 受热分解生成NaCO、CO 和HO,既破坏了离子键,也破坏了共价键
3 2 3 2 2
8.下列说法正确的是( )
A.碘晶体受热转变为碘蒸气,吸收的热量用于克服碘原子间的作用力
B.硫酸钾和硫酸溶于水都电离出硫酸根离子,所以它们在熔融状态下都能导电
C.在N、CO 和SiO 物质中,都存在共价键,它们都是由分子构成
2 2 2
D.H 和Cl 在光照条件反应生成HCl,一定有共价键的断裂和形成
2 2
9.短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期
且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的
是( )
A.原子半径:
B.X、Y、Z三种元素可以组成共价化合物或离子化合物
C.Y的单质的氧化性比Z的强
D.Y的气态氢化物稳定性强于Z气态氢化物
10.如图是卤素单质(F 、Cl、Br 、I)的沸点与相对分子质量的关系图,下列说法不
2 2 2 2
正确的是( )
A.单质①是最活泼的非金属单质
B.单质④的氢化物在卤素氢化物中热稳定性最
强
C.保存少量的单质③时加少量水进行水封
D.单质②能使品红溶液褪色
能力提升
11.X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次增大的同周期元素,X与Z可形成常见的XZ或XZ 型分子,Y与M形成的气态化合物质量是相同条件下
2
同体积氢气的8.5倍,W是原子半径最大的短周期元素。下列判断正确的是( )
A.最高价含氧酸酸性:X>Y B.M、Y、Z可形成离子化合物
C.W可形成双原子分子 D.M与W形成的化合物含极性共价键
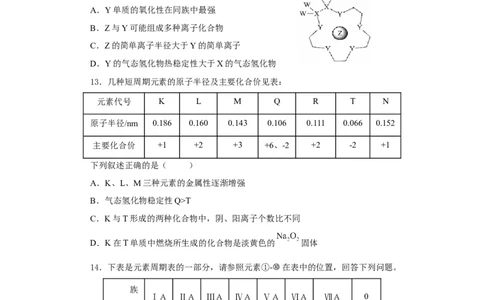
12.科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超
分子,具有高效的催化性能,其结构示意图如图(实线代表共价键,其他重复单元的W、
X未标注),W、X、Z分别位于不同周期,Z的原子半径在同周期中最大。下列说法错误
的是( )
A.Y单质的氧化性在同族中最强
B.Z与Y可能组成多种离子化合物
C.Z的简单离子半径大于Y的简单离子
D.Y的气态氢化物热稳定性大于X的气态氢化物
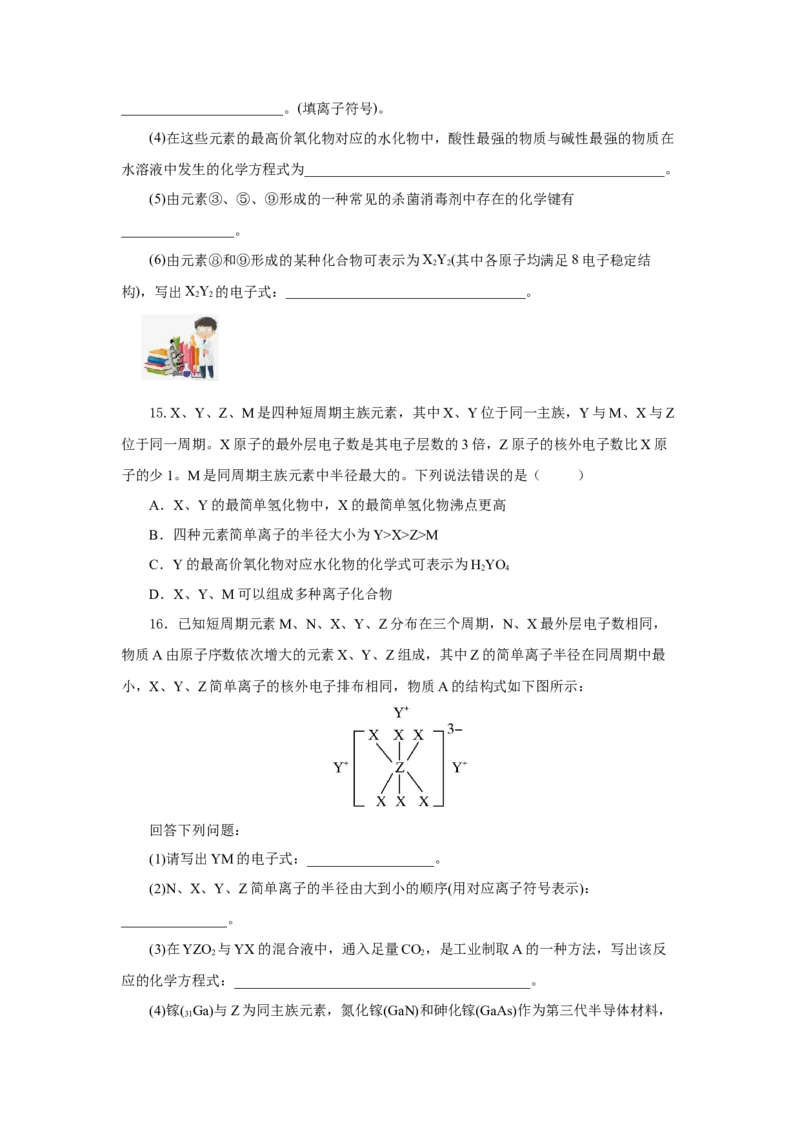
13.几种短周期元素的原子半径及主要化合价见表:
元素代号 K L M Q R T N
原子半径/nm 0.186 0.160 0.143 0.106 0.111 0.066 0.152
主要化合价 +1 +2 +3 +6、-2 +2 -2 +1
下列叙述正确的是( )
A.K、L、M三种元素的金属性逐渐增强
B.气态氢化物稳定性Q>T
C.K与T形成的两种化合物中,阴、阳离子个数比不同
D.K在T单质中燃烧所生成的化合物是淡黄色的 固体
14.下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
族
IA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
2 ① ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)②的原子结构示意图是____。
(2)化学性质最不活泼的元素是_____(填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是_______________________。(填离子符号)。
(4)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在
水溶液中发生的化学方程式为___________________________________________________。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
________________。
(6)由元素⑧和⑨形成的某种化合物可表示为XY(其中各原子均满足8电子稳定结
2 2
构),写出XY 的电子式:__________________________________。
2 2
直击高考
15.X、Y、Z、M是四种短周期主族元素,其中X、Y位于同一主族,Y与M、X与Z
位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比X原
子的少1。M是同周期主族元素中半径最大的。下列说法错误的是( )
A.X、Y的最简单氢化物中,X的最简单氢化物沸点更高
B.四种元素简单离子的半径大小为Y>X>Z>M
C.Y的最高价氧化物对应水化物的化学式可表示为HYO
2 4
D.X、Y、M可以组成多种离子化合物
16.已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,
物质A由原子序数依次增大的元素X、Y、Z组成,其中Z的简单离子半径在同周期中最
小,X、Y、Z简单离子的核外电子排布相同,物质A的结构式如下图所示:
回答下列问题:
(1)请写出YM的电子式:__________________。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):
_______________。
(3)在YZO 与YX的混合液中,通入足量CO,是工业制取A的一种方法,写出该反
2 2
应的化学方程式:__________________________________________。
(4)镓( Ga)与Z为同主族元素,氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,
31具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
下列有关说法正确的是__________________。
a. Ga位于元素周期表第四周期IVA族
b. GaN为新型无机非金属材料
c. Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d. 酸性:HAsO >H PO >HNO
3 4 3 4 3
(5)YZM 是有机合成的重要还原剂,其合成路线如图所示
4
利用YZM 遇水反应生成的氢气的体积测定YZM 样品纯度。
4 4
①其反应的化学方程式为___________________________________________________。
②现设计如图四种装置测定YZM 样品的纯度(假设杂质不参与反应)。
4
从简约性、准确性考虑,最适宜的方案是_______(填编号)。
③取样品ag,若实验测得氢气的体积为V L(标准状态),则YZM 样品纯度为
4
_______(用代数式表示)。