文档内容
第三章 铁 金属材料
第一节 铁及其化合物
专题1(实验活动) 铁及其重要化合物
【学习目标】1.进一步认识铁及其化合物的化学性质和Fe3+的检验方法,能由氢氧化亚铁性质实验分
析并设计出制备氢氧化亚铁的实验,构建“铁三角”转化关系模型。
2.以铁及其化合物的性质为例,能从物质类别和元素价态的视角建立含变价元素物质的转化关系,丰
富研究物质的思路和方法。
3.通过阅读硫酸亚铁药片说明书,培养获取信息和初步加工信息的能力,学会设计简单实验的方法。
并从实际条件出发,解决生产、生活中的简单问题,进一步感受化学与生活的紧密联系和对人类所作的贡
献。
【学习重点】Fe2+的还原性、Fe3+的氧化性及检验
【学习难点】铁及其化合物的学习方法的建构、实验方案的设计
【课前预习】
旧知回顾:1.铁在潮湿的空气中生成铁锈的主要成分是 ,而铁在纯氧中燃烧的产物是
。
Fe与Cl 反应特点是 ,而Fe与盐酸反应生成 。
2
2.从价态的角度看铁单质具有 性,铁盐具有 性,亚铁盐具有
。
新知预习:1.Fe与Br 反应生成 ,与I 反应时生成 ,通过这一事实可以说明Br 的氧
2 2 2
化性比I 。
2
2.FeO和Fe O 与HNO 反应时,除考虑与 的反应外,还考虑 。
3 4 3
Fe O、Fe O、Fe(OH) 与HI反应时,除考虑与 的反应外,还考虑 。
2 3 3 4 3
【课中探究】
情景导入:已知铁直接与35%硝酸反应是很快的,但将一小块纯铁放入盛70%浓硝酸的小烧杯中(室
温),铁在浓硝酸不溶解。再用滴管缓慢地向烧杯中加蒸馏水,直加到溶液体积是
原酸液的2倍,浓度约为35%,铁在这稀释后的硝酸还是不溶解。那么为什么浓度
从70%慢慢降为35%就不反应了呢?困惑的法拉第拿起玻璃棒,想去翻动一下铁
块,看看它是否出了什么问题。当它刚用玻璃棒的尖端触到铁块时,烧杯里发生了
异常现象—铁块迅速地反应起来,就这样这种奇异的钝化现象被法拉第发现了,人
们称这个实验为法拉第钝化实验。
一、铁单质的还原性和Fe3+的氧化性
活动一、探究铁单质的还原性
任务一、实验探究:铁与硝酸溶液、硫酸铜溶液反应的现象,并分析其原理是什么?完成下表内容。
实验步骤 实验现象 实验原理 实验结论
步骤 1:在一支试管中加入2mLCuSO 溶液,再将一段铁丝
4
放入硫酸铜溶液中,过一会儿,
取出铁丝,观察现象并加以解
释。
步骤2:在一支试管中加入2mL
稀硝酸溶液,再将一段铁丝放入
溶液中,观察现象并加以解释。
步骤 3:在一支试管中加入
2mL70%的浓硝酸溶液,将一段
铁丝放入溶液中,观察现象,再
将溶液加热,观察现象,并加以
解释。
步骤 4:在一支试管中加入
2mL98%的浓硫酸,将一段铁丝
放入溶液中,观察现象,再将溶
液加热,观察现象,并加以解
释。
任务二、问题探究:将铁丝插入稀硫酸和稀硝酸的混合溶液中,可能发生哪些化学反应,其先后顺序
时什么?
【对应训练】1.下列有关铁的说法正确的是( )
A.Fe在稀硝酸中发生钝化
B.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
C.向FeCl 溶液中滴加NH SCN溶液,溶液显红色
2 4
D.镀锌铁不如镀锡铁耐腐蚀
2.将0.02mol铁分别投入足量的下列物质中,在一定条件下充分反应,产生氢气最多的是( )
A.2mol/L稀硫酸 B.18.4mol/L硫酸
C.5mol/L硝酸 D.灼热的水蒸气
活动二、探究Fe3+的氧化性任务一、实验探究:根据表格内容,完成相关实验,观察实验现象,并分析实验原理。
序号 实验操作 实验现象 实验原理 实验结论
1 取3mLFeCl 溶液加入试管中,加
3
入几小块铜片,振荡,观察现
象。
在一支盛有3mL蒸馏水的试管中
2 加几滴 FeCl 溶液,再滴加 3 滴
3
KI溶液,观察现象。然后向溶液
中滴加 2 滴淀粉溶液,观察现
象。
任务二、问题探究:Fe3+具有氧化性,有何特点和规律?有何应用?
【对应训练】1.取某含铁元素的固体A进行如下实验:
根据下列转化关系,下列叙述不正确的是( )
A.试剂1是KSCN溶液
B.试剂2可以是新制氯水
C.溶液B中只有Fe3+无Fe2+
D.溶液C到溶液F红色加深的原因是溶液中的Fe2+被氧化剂氧化成Fe3+,使Fe3+浓度增大
2.将金属铁、铜投入FeCl 溶液中充分反应,下列对反应情况设想的评价正确的是( )
3
选项 反应情况设想 评价
当铁、铜均无剩余时,溶液中一定有
A 正确,Fe3+和铁、铜均可反应
Fe2+、Cu2+,一定无Fe3+
当铁、铜均有剩余时,溶液中一定有
B 正确,铁和铜都与Fe3+反应,故无Fe3+
Fe2+、Cu2+,无Fe3+
当铜有剩余,铁无剩余时,溶液中一定
C 正确,铜有剩余,故无Cu2+
只有Fe2+,无Cu2+
D
当铁有剩余,铜无剩余时,溶液中一定 不正确,不可能出现铁有剩余而铜无剩余的情况,因为铁的还原性比铜的强,铁先与Fe3
有Fe2+、Cu2+
+反应
二、亚铁盐的氧化性和还原性
活动一、探究亚铁盐的氧化性和还原性
任务一、实验探究:根据表格内容,完成相关实验,观察实验现象,分析实验原理。
序号 实验操作 实验现象 实验原理 实验结论
1 取3mLFeCl 溶液加入试管中,
2
加入几小块锌片,振荡,观察现
象。
2 取3mLFeCl 溶液入试管中,加
3
入足量铁粉,振荡,观察现象。
3 取3mLFeCl 溶液加入试管中,
2
滴加几滴氯水,振荡,观察现
象。
取少量酸性KMnO 溶液于试管
4
中,逐滴加入FeSO 溶液,当溶
4
液紫色褪去时,再滴加2滴
4 KSCN溶液,观察现象
任务二、问题探究:某溶液中加KSCN溶液,颜色无变化,再加氯水溶液变红,说明什么?发生的反
应是什么?若溶液变红,然后加足量Fe粉,红色又褪去,说明什么?写出反应的离子方程式。
【对应训练】1.把表面有少量氧化物的铜片和铁片一起放入盐酸中,充分反应后,所得溶液中的金
属离子为( )
A.Fe3+和Cu2+ B.Fe2+和Cu2+
C.Fe2+和Fe3+ D.Fe2+
2.已知氯气有强氧化性,能氧化Fe2+、Br-、I-等。又已知还原性I->Fe2+>Br-。向含有Fe2+、I-、Br-的溶
液中通入一定量氯气后,对所得溶液中离子的成分分析正确的是( )
A.I-、Fe3+、Cl- B.Fe2+、Cl-、Br-
C.Fe2+、Fe3+、Cl- D.Fe2+、I-、Cl-
活动二、Fe(OH) 的制备
2任务一、问题探究:为了提高皮革的耐曲折强度以及耐化学药剂和微生物的作用,常常使用绿矾作为
鞣革剂。绿矾晶体(FeSO ·7H O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质。为探究绿矾
4 2
样品的变质情况,化学兴趣小组的同学设计了下列实验方案。
可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液、铁粉,请
参与完成方案设计。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
①如何证明绿矾已被氧化?
②如何证明绿矾已完全被氧化
③为了防止绿矾溶液被氧化,如何操作?
任务二、结合Fe(OH) 容易被空气中的氧气氧化成Fe(OH) 的性质,思考制备Fe(OH) 有哪些方法?
2 3 2
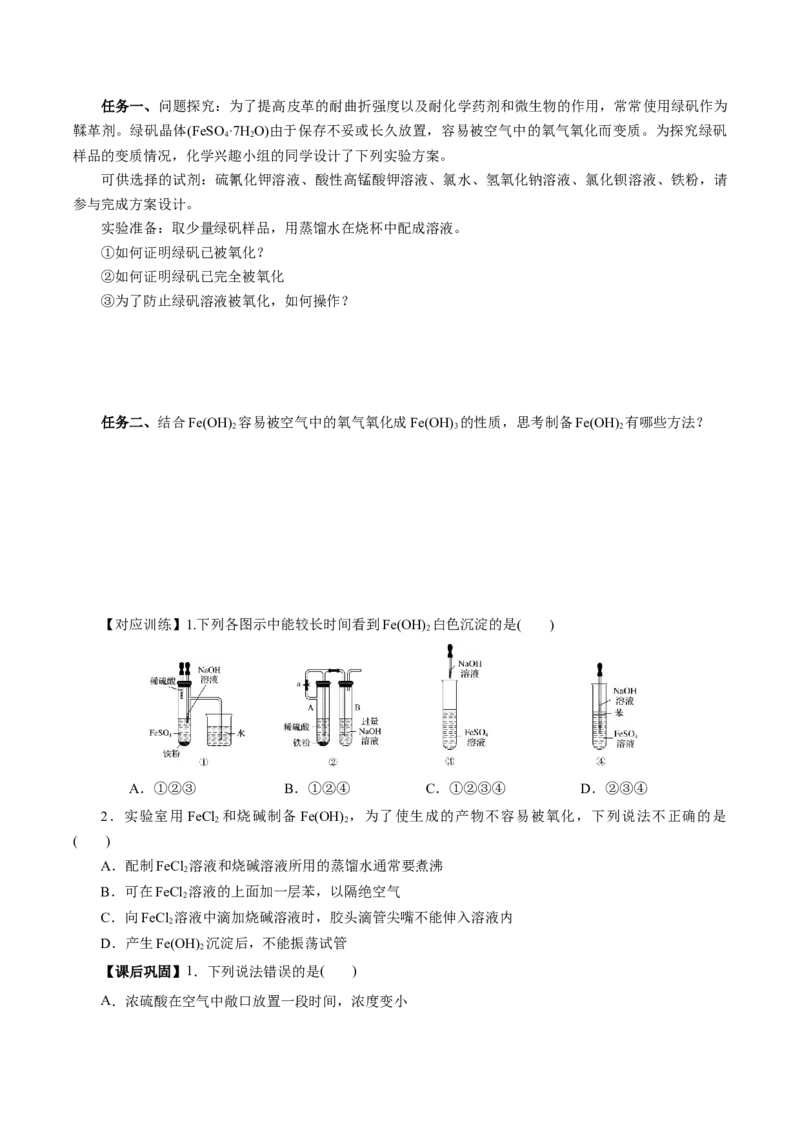
【对应训练】1.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2
A.①②③ B.①②④ C.①②③④ D.②③④
2.实验室用 FeCl 和烧碱制备 Fe(OH) ,为了使生成的产物不容易被氧化,下列说法不正确的是
2 2
( )
A.配制FeCl 溶液和烧碱溶液所用的蒸馏水通常要煮沸
2
B.可在FeCl 溶液的上面加一层苯,以隔绝空气
2
C.向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入溶液内
2
D.产生Fe(OH) 沉淀后,不能振荡试管
2
【课后巩固】1.下列说法错误的是( )
A.浓硫酸在空气中敞口放置一段时间,浓度变小B.铁片投入冷的浓硝酸中,铁片不溶解
C.钢片投入浓硝酸中,产生红棕色气体
D.石蕊溶液滴入稀硫酸中,溶液变蓝
2.向FeCl 溶液中同时加入铁粉和铜粉,充分反应后不会出现的结果是( )
3
A.铁、铜均有 B.铁、铜均无
C.有铜无铁 D.有铁无铜
3.在硫酸铁溶液中,加入a g铜完全溶解后再加入b g铁,充分反应后得到c g残余固体,且a>c,
则下列说法中正确的是( )
A.残余固体可能为铁和铜的混合物 B.最后得到的溶液可能含有Fe3+
C.残余固体是铁,溶液中一定不含Cu2+ D.残余固体全部是铜
4.将过氧化钠投入FeCl 溶液中,可观察到的实验现象是( )
2
A.有无色气体和白色沉淀生成 B.有无色气体和红褐色沉淀生成
C.无气体产生,有沉淀生成 D.有气体产生,无沉淀生成
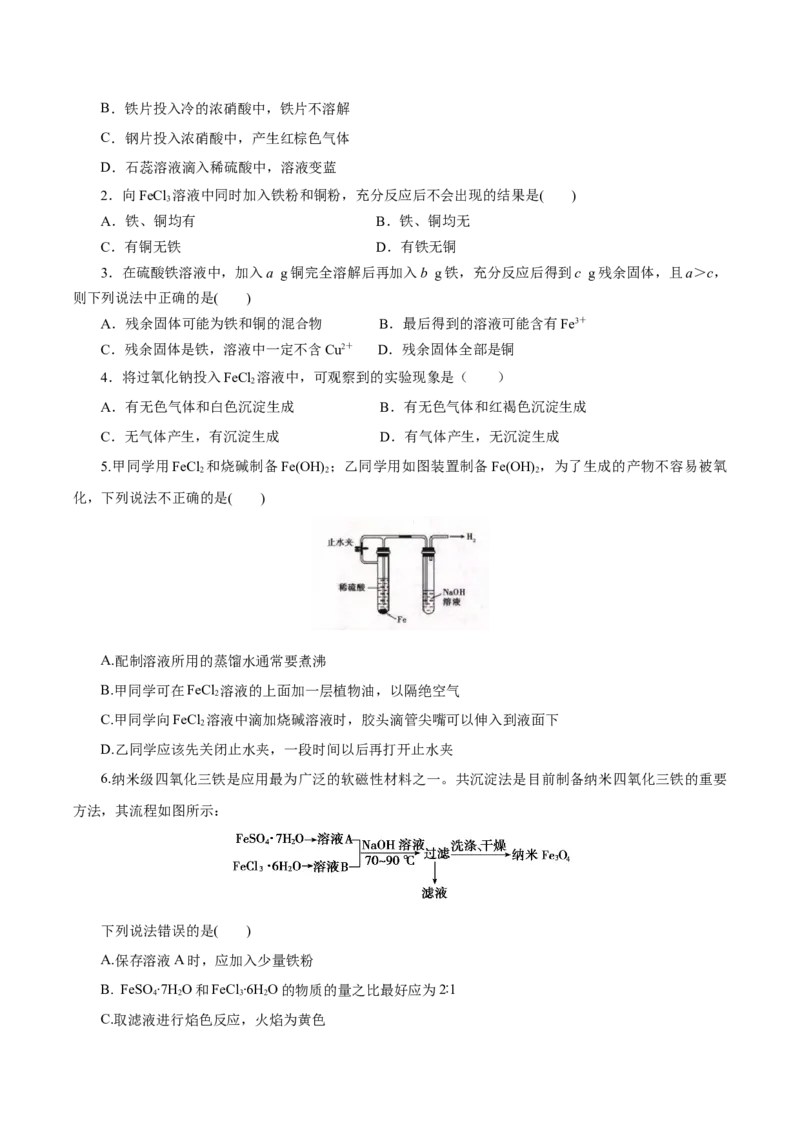
5.甲同学用FeCl 和烧碱制备Fe(OH) ;乙同学用如图装置制备Fe(OH) ,为了生成的产物不容易被氧
2 2 2
化,下列说法不正确的是( )
A.配制溶液所用的蒸馏水通常要煮沸
B.甲同学可在FeCl 溶液的上面加一层植物油,以隔绝空气
2
C.甲同学向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴可以伸入到液面下
2
D.乙同学应该先关闭止水夹,一段时间以后再打开止水夹
6.纳米级四氧化三铁是应用最为广泛的软磁性材料之一。共沉淀法是目前制备纳米四氧化三铁的重要
方法,其流程如图所示:
下列说法错误的是( )
A.保存溶液A时,应加入少量铁粉
B. FeSO ‧7H O和FeCl ‧6H O的物质的量之比最好应为2∶1
4 2 3 2
C.取滤液进行焰色反应,火焰为黄色D.其制备反应类型不属于氧化还原反应
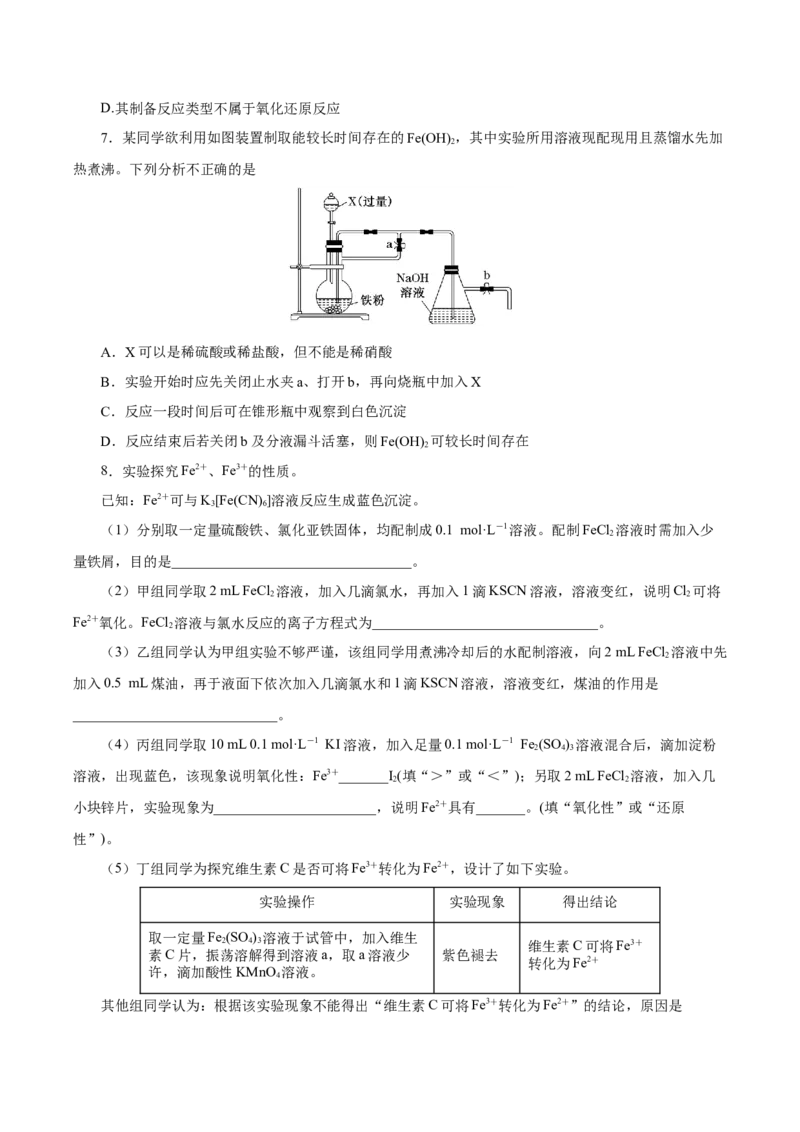
7.某同学欲利用如图装置制取能较长时间存在的Fe(OH) ,其中实验所用溶液现配现用且蒸馏水先加
2
热煮沸。下列分析不正确的是
A.X可以是稀硫酸或稀盐酸,但不能是稀硝酸
B.实验开始时应先关闭止水夹a、打开b,再向烧瓶中加入X
C.反应一段时间后可在锥形瓶中观察到白色沉淀
D.反应结束后若关闭b及分液漏斗活塞,则Fe(OH) 可较长时间存在
2
8.实验探究Fe2+、Fe3+的性质。
已知:Fe2+可与K[Fe(CN) ]溶液反应生成蓝色沉淀。
3 6
(1)分别取一定量硫酸铁、氯化亚铁固体,均配制成0.1 mol·L-1溶液。配制FeCl 溶液时需加入少
2
量铁屑,目的是__________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将
2 2
Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为________________________________。
2
(3)乙组同学认为甲组实验不够严谨,该组同学用煮沸冷却后的水配制溶液,向2 mL FeCl 溶液中先
2
加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
_____________________________。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入足量0.1 mol·L-1 Fe (SO ) 溶液混合后,滴加淀粉
2 4 3
溶液,出现蓝色,该现象说明氧化性:Fe3+_______I(填“>”或“<”);另取2 mL FeCl 溶液,加入几
2 2
小块锌片,实验现象为_______________________,说明Fe2+具有_______。(填“氧化性”或“还原
性”)。
(5)丁组同学为探究维生素C是否可将Fe3+转化为Fe2+,设计了如下实验。
实验操作 实验现象 得出结论
取一定量Fe (SO ) 溶液于试管中,加入维生
2 4 3 维生素C可将Fe3+
素C片,振荡溶解得到溶液a,取a溶液少 紫色褪去
转化为Fe2+
许,滴加酸性KMnO 溶液。
4
其他组同学认为:根据该实验现象不能得出“维生素C可将Fe3+转化为Fe2+”的结论,原因是_______________________________________________________________;认为可另外设计实验验证结论
是否正确:取a溶液少许,滴加______________,若出现_________________________________________,
则结论正确。