文档内容
第三章 铁 金属材料
第一节 铁及其化合物 课时作业
专题1 铁及其重要化合物
基础达标
1.下列有关物质的颜色正确的是( )
①FeSO ‧7H O:棕黄色 ②Fe O:红棕色 ③Fe(OH) :白色 ④Fe O:黑色
4 2 2 3 2 3 4
⑤CuSO ‧5H O:白色
4 2
A.①③④ B.②③④ C.②③⑤ D.①②④
2.下列说法正确的是( )
A.赤铁矿的主要成分是Fe O
3 4
B.Fe O 为碱性氧化物,可与水反应生成Fe(OH)
2 3 3
C.铁锈的主要成分是Fe O
2 3
D.Fe O 中铁元素有+2价和+3价,Fe O 是混合物
3 4 3 4
3.以下有关铁的氧化物的叙述中正确的是( )
A.Fe O、Fe O 都是炼铁的原料
2 3 3 4
B.FeO、Fe O、Fe O 都只有氧化性
2 3 3 4
C.FeO、Fe O、Fe O 都是不溶于水的黑色固体
2 3 3 4
D.FeO、Fe O、Fe O 都能与酸反应生成盐和水,都属于碱性氧化物
2 3 3 4
4.下列有关铁及其化合物的说法中正确的是( )
A.Fe O 的颜色为红棕色
3 4
B.铁丝可在空气中燃烧生成Fe O
3 4
C.FeCl 可通过置换反应或复分解反应制得
2
D.铁的氧化物均为黑色,不溶于水
5. 如图两圆相交部分A、B、C、D分别表示两物质间的反应。下列各对应反应的离
子方程式书写不正确的是( )
A.Fe+4H++NO===Fe3++NO↑+2HO
2
B.Fe O+8H+===Fe2++2Fe3++4HO
3 4 2
C.Fe(OH) +3H+===Fe3++3HO
3 2
D.3Fe(OH) +10H++NO===3Fe3++NO↑+8HO
2 2
6. 已知下列三个实验均能发生化学反应:① ② ③
将铁钉放入硫酸铜 向硫酸亚铁溶液中滴入几
将铜丝放入氯化铁溶液中
溶液中 滴氯水
下列判断正确的是( )
A.实验①中铁钉只做还原剂
B.实验②中Fe2+既显氧化性又显还原性
C.实验③中发生的是置换反应
D.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
7.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在
空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是(
)
A.Fe(OH) Fe O B.Fe(OH) Fe O
3 2 3 2 2 3
C.Fe(OH) Fe(OH) D.Fe(OH) FeO
2 3 2
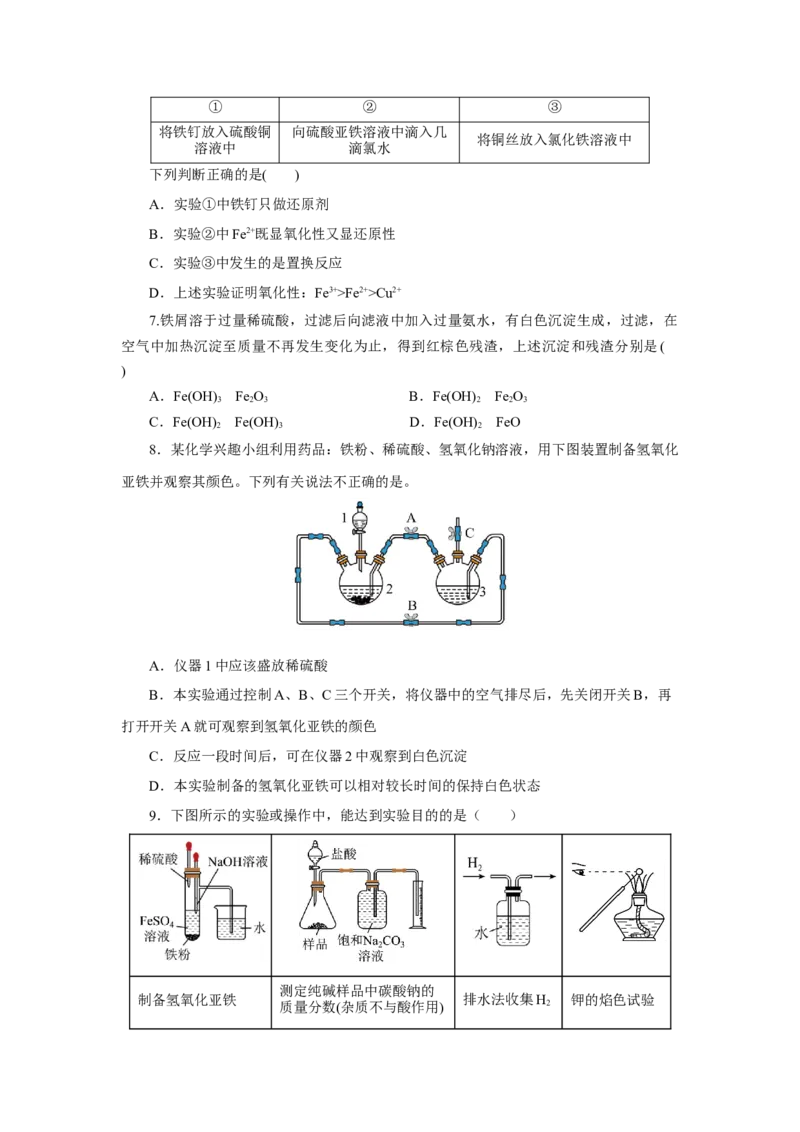
8.某化学兴趣小组利用药品:铁粉、稀硫酸、氢氧化钠溶液,用下图装置制备氢氧化
亚铁并观察其颜色。下列有关说法不正确的是。
A.仪器1中应该盛放稀硫酸
B.本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,先关闭开关B,再
打开开关A就可观察到氢氧化亚铁的颜色
C.反应一段时间后,可在仪器2中观察到白色沉淀
D.本实验制备的氢氧化亚铁可以相对较长时间的保持白色状态
9.下图所示的实验或操作中,能达到实验目的的是( )
测定纯碱样品中碳酸钠的
制备氢氧化亚铁 排水法收集H 钾的焰色试验
质量分数(杂质不与酸作用) 2A B C D
A.A B.B C.C D.D
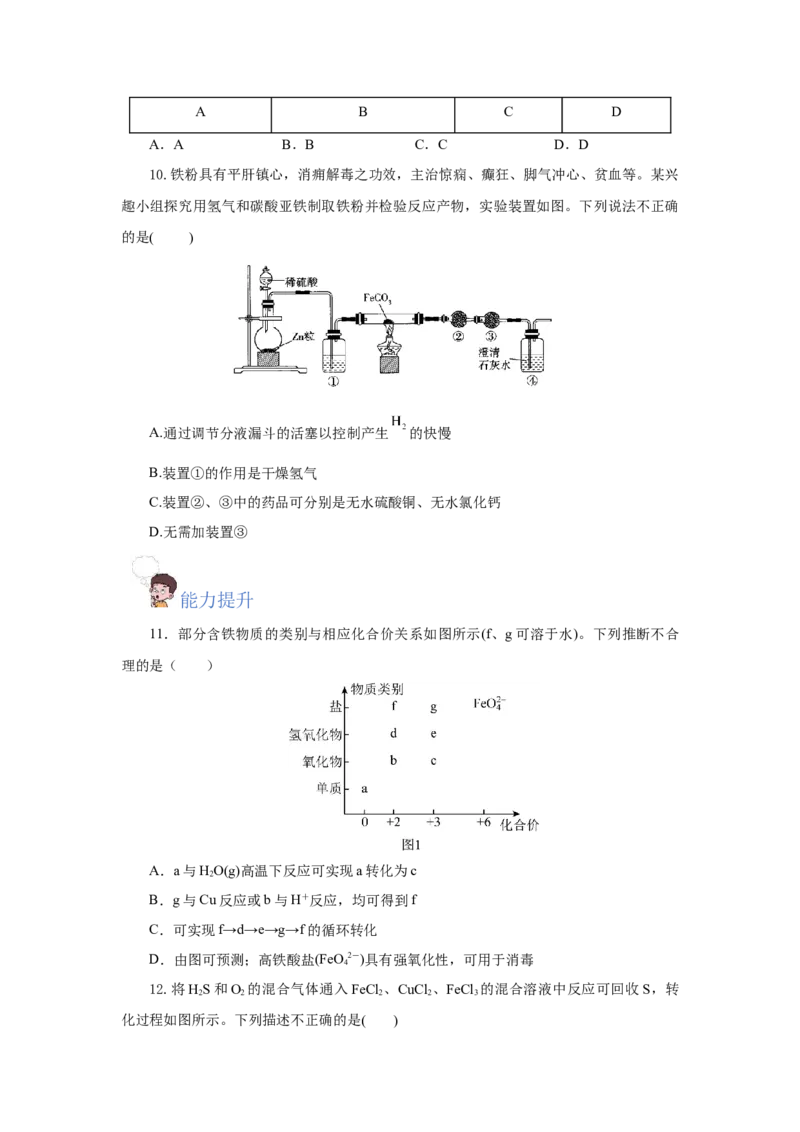
10.铁粉具有平肝镇心,消痈解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴
趣小组探究用氢气和碳酸亚铁制取铁粉并检验反应产物,实验装置如图。下列说法不正确
的是( )
A.通过调节分液漏斗的活塞以控制产生 的快慢
B.装置①的作用是干燥氢气
C.装置②、③中的药品可分别是无水硫酸铜、无水氯化钙
D.无需加装置③
能力提升
11.部分含铁物质的类别与相应化合价关系如图所示(f、g可溶于水)。下列推断不合
理的是( )
A.a与HO(g)高温下反应可实现a转化为c
2
B.g与Cu反应或b与H+反应,均可得到f
C.可实现f→d→e→g→f的循环转化
D.由图可预测;高铁酸盐(FeO 2-)具有强氧化性,可用于消毒
4
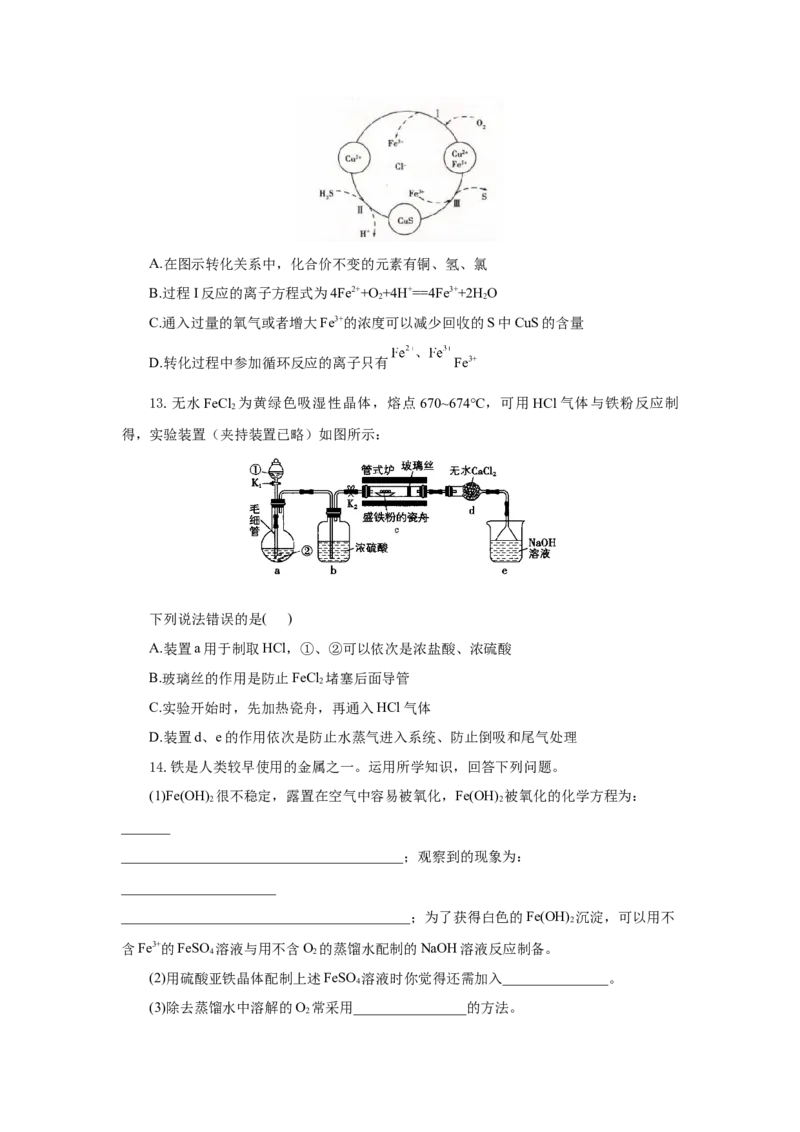
12.将HS和O 的混合气体通入FeCl 、CuCl 、FeCl 的混合溶液中反应可回收S,转
2 2 2 2 3
化过程如图所示。下列描述不正确的是( )A.在图示转化关系中,化合价不变的元素有铜、氢、氯
B.过程I反应的离子方程式为4Fe2++O +4H+==4Fe3++2H O
2 2
C.通入过量的氧气或者增大Fe3+的浓度可以减少回收的S中CuS的含量
D.转化过程中参加循环反应的离子只有 Fe3+
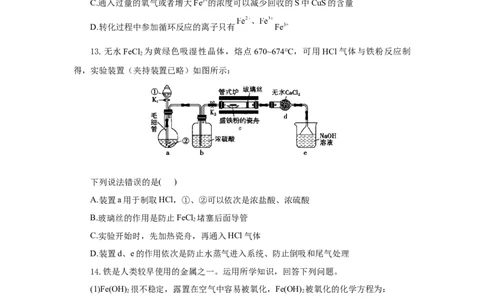
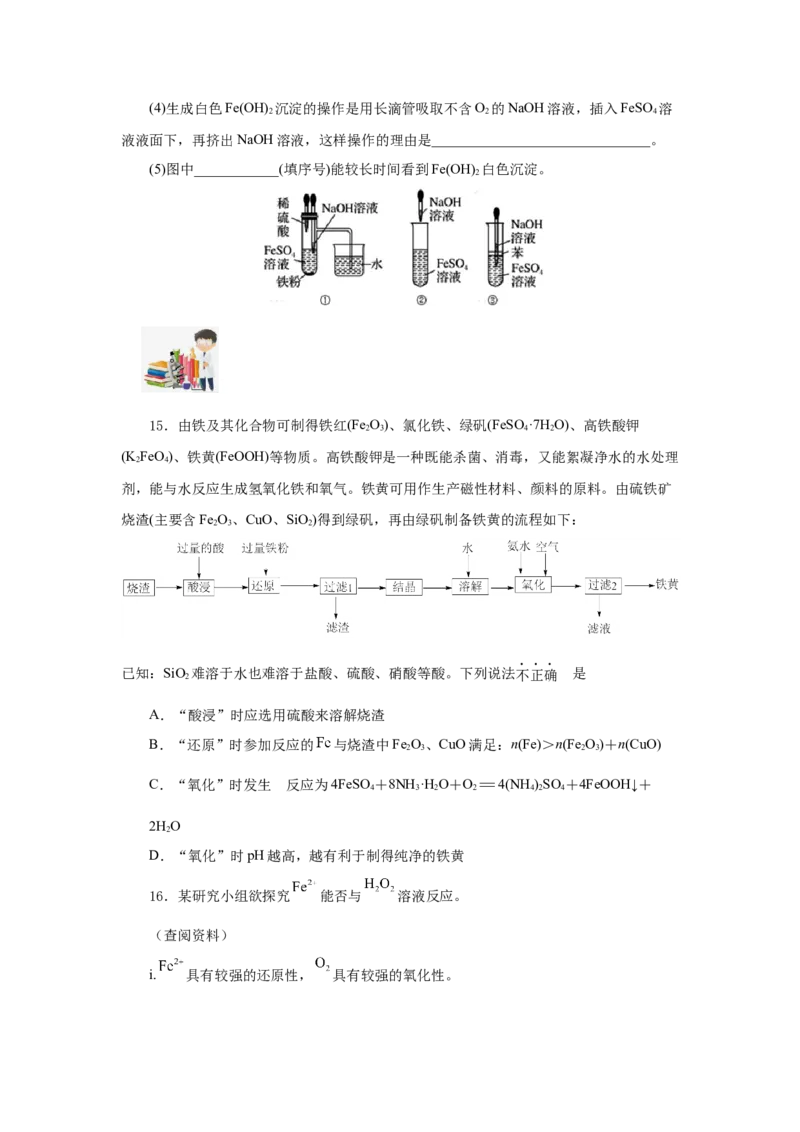
13.无水FeCl 为黄绿色吸湿性晶体,熔点 670~674℃,可用HCl气体与铁粉反应制
2
得,实验装置(夹持装置已略)如图所示:
下列说法错误的是( )
A.装置a用于制取HCl,①、②可以依次是浓盐酸、浓硫酸
B.玻璃丝的作用是防止FeCl 堵塞后面导管
2
C.实验开始时,先加热瓷舟,再通入HCl气体
D.装置d、e的作用依次是防止水蒸气进入系统、防止倒吸和尾气处理
14.铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)Fe(OH) 很不稳定,露置在空气中容易被氧化,Fe(OH) 被氧化的化学方程为:
2 2
_______
________________________________________;观察到的现象为:
______________________
_________________________________________;为了获得白色的Fe(OH) 沉淀,可以用不
2
含Fe3+的FeSO 溶液与用不含O 的蒸馏水配制的NaOH溶液反应制备。
4 2
(2)用硫酸亚铁晶体配制上述FeSO 溶液时你觉得还需加入_______________。
4
(3)除去蒸馏水中溶解的O 常采用________________的方法。
2(4)生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶
2 2 4
液液面下,再挤出NaOH溶液,这样操作的理由是_______________________________。
(5)图中____________(填序号)能较长时间看到Fe(OH) 白色沉淀。
2
直击高考
15.由铁及其化合物可制得铁红(Fe O)、氯化铁、绿矾(FeSO ·7H O)、高铁酸钾
2 3 4 2
(K FeO)、铁黄(FeOOH)等物质。高铁酸钾是一种既能杀菌、消毒,又能絮凝净水的水处理
2 4
剂,能与水反应生成氢氧化铁和氧气。铁黄可用作生产磁性材料、颜料的原料。由硫铁矿
烧渣(主要含Fe O、CuO、SiO)得到绿矾,再由绿矾制备铁黄的流程如下:
2 3 2
已知:SiO 难溶于水也难溶于盐酸、硫酸、硝酸等酸。下列说法不正确 是的
2
A.“酸浸”时应选用硫酸来溶解烧渣
B.“还原”时参加反应的 与烧渣中Fe O、CuO满足:n(Fe)>n(Fe O)+n(CuO)
2 3 2 3
的
C.“氧化”时发生 反应为4FeSO +8NH ·HO+O=4(NH )SO +4FeOOH↓+
4 3 2 2 4 2 4
2HO
2
D.“氧化”时pH越高,越有利于制得纯净的铁黄
16.某研究小组欲探究 能否与 溶液反应。
(查阅资料)
i. 具有较强的还原性, 具有较强的氧化性。ii. 遇 可生成 , 溶液呈血红色,可用于 的检验。
(提出猜想)杨sir化学,侵权必究
(1)小组同学经过讨论后,认为 溶液可以与 溶液反应,请从化合价的角
度加以解释:
____________________________________________________________________。
(设计实验)
(2)实验I:在试管中加入 溶液和 溶液,再加入 溶液,发现溶液
_____
___________________________________________________,小组同学认为 和 溶
液反应生成了 。
(3)甲同学注意到盛放 溶液的试剂瓶中有空气,因此不同意该结论,他的理由
是_________________________________________________________________。
重新设计实验:
实验II:在试管中加入 溶液,然后加入 溶液,发现溶液无明显变化,再
加入 溶液,发现溶液变红。
(获得结论)
(4)过氧化氢___________(填“能”或者“不能”)氧化 。
(发现异常)
乙同学继续向实验II所得溶液中滴加溶液,发现溶液褪色。
小组同学经过重新查阅资料后,发现可以将 氧化为 。乙同学设计实验III并
证实了该资料中的说法。
(5)补全实验III的方案:在试管中加入 溶液,加入 溶液,再加入
__________,产生________________________________。(总结反思)杨sir化学,侵权必究
(6)小组同学经过讨论后,提出了 的检验方法:取待测液于试管中,
____________
___________________________________________________________,证明待测液含有
。
(7)从上述实验中可以得出结论,在物 质性质的检验中,应注意
_________________(至少写出两条)对实验结果的影响。