文档内容
第三章 铁 金属材料
第一节 铁及其化合物
专题1(实验活动) 铁及其重要化合物
【学习目标】1.进一步认识铁及其化合物的化学性质和Fe3+的检验方法,能由氢氧化亚铁性质实验分
析并设计出制备氢氧化亚铁的实验,构建“铁三角”转化关系模型。
2.以铁及其化合物的性质为例,能从物质类别和元素价态的视角建立含变价元素物质的转化关系,丰
富研究物质的思路和方法。
3.通过阅读硫酸亚铁药片说明书,培养获取信息和初步加工信息的能力,学会设计简单实验的方法。
并从实际条件出发,解决生产、生活中的简单问题,进一步感受化学与生活的紧密联系和对人类所作的贡
献。
【学习重点】Fe2+的还原性、Fe3+的氧化性及检验
【学习难点】铁及其化合物的学习方法的建构、实验方案的设计
【课前预习】
旧知回顾:1.铁在潮湿的空气中生成铁锈的主要成分是 F e O ,而铁在纯氧中燃烧的产物是 F e O 。
2 3 3 4
Fe与Cl 反应特点是 不论用量多少都生成 FeC l ,而Fe与盐酸反应生成 FeC l 。
2 3 2
2.从价态的角度看铁单质具有 还原 性,铁盐具有 氧化 性,亚铁盐具有 氧化性和还原性 。
新知预习:1.Fe与Br 反应生成 FeB r ,与I 反应时生成 Fe I ,通过这一事实可以说明Br 的氧化性
2 3 2 2 2
比I 强 。
2
2.FeO和Fe O 与HNO 反应时,除考虑与 H + 的反应外,还考虑 F e 2 + 被 HNO 氧化成 F e 3 + 。Fe O 、
3 4 3 3 2 3
Fe O、Fe(OH) 与HI反应时,除考虑与 H + 的反应外,还考虑 F e 3 + 被 I - 还原为 F e 2 + 。
3 4 3
【课中探究】
情景导入:已知铁直接与35%硝酸反应是很快的,但将一小块纯铁放入盛70%浓硝酸的小烧杯中(室
温),铁在浓硝酸不溶解。再用滴管缓慢地向烧杯中加蒸馏水,直加到溶液体积是
原酸液的2倍,浓度约为35%,铁在这稀释后的硝酸还是不溶解。那么为什么浓度
从70%慢慢降为35%就不反应了呢?困惑的法拉第拿起玻璃棒,想去翻动一下铁
块,看看它是否出了什么问题。当它刚用玻璃棒的尖端触到铁块时,烧杯里发生了
异常现象—铁块迅速地反应起来,就这样这种奇异的钝化现象被法拉第发现了,人
们称这个实验为法拉第钝化实验。
一、铁单质的还原性和Fe3+的氧化性
活动一、探究铁单质的还原性
任务一、实验探究:铁与硝酸溶液、硫酸铜溶液反应的现象,并分析其原理是什么?完成下表内容。
【答案要点】
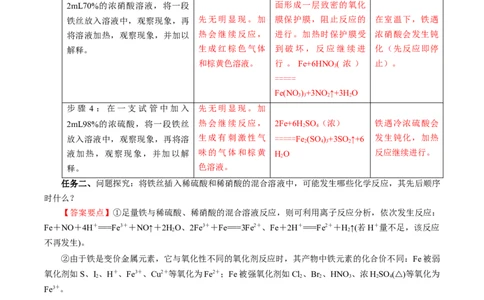
实验步骤 实验现象 实验原理 实验结论
步骤 1:在一支试管中加入 金属铁可以从盐
2mLCuSO 溶液,再将一段铁丝 铁丝表面有红色 溶液中置换出比
4放入硫酸铜溶液中,过一会儿, 物质生成。 Fe+CuSO=Cu+FeSO 它更不活泼的金
4 4
取出铁丝,观察现象并加以解 属。
释。
步骤2:在一支试管中加入2mL 铁丝不断溶解,
稀硝酸溶液,再将一段铁丝放入 产生大量气泡, Fe+4HNO (稀) 铁单质可以被稀
3
溶液中,观察现象并加以解释。 在试管口变为红 =Fe(NO)+NO↑+2HO 硝 酸 氧 化 成
3 3 2
棕色,溶液变为 2NO+O =2NO Fe3+盐
2 2
棕黄色。
步骤 3:在一支试管中加入 室温,铁遇浓硝酸,表
2mL70%的浓硝酸溶液,将一段 面形成一层致密的氧化
铁丝放入溶液中,观察现象,再 先无明显现。加 膜保护膜,阻止反应的 在室温下,铁遇
将溶液加热,观察现象,并加以 热会继续反应, 进行。加热时保护膜受 浓硝酸会发生钝
解释。 生成红棕色气体 到破坏,反应继续进 化(先反应即停
和棕黄色溶液。 行 。 Fe+6HNO ( 浓 ) 止)。
3
=====
Fe(NO )+3NO↑+3H O
3 3 2 2
步骤 4:在一支试管中加入 先无明显现。加
2mL98%的浓硫酸,将一段铁丝 热会继续反应, 2Fe+6H SO (浓) 铁遇冷浓硫酸会
2 4
放入溶液中,观察现象,再将溶 生成有刺激性气 =====Fe (SO )+3SO↑+6 发生钝化,加热
2 4 3 2
液加热,观察现象,并加以解 味的气体和棕黄 HO 反应继续进行。
2
释。 色溶液。
任务二、问题探究:将铁丝插入稀硫酸和稀硝酸的混合溶液中,可能发生哪些化学反应,其先后顺序
时什么?
【答案要点】①足量铁与稀硫酸、稀硝酸的混合溶液反应,则可利用离子反应分析,依次发生反应:
Fe+NO+4H+===Fe3++NO↑+2HO、2Fe3++Fe===3Fe2+、Fe+2H+===Fe2++H↑(若H+量不足,该反应
2 2
不再发生)。
②由于铁是变价金属元素,它与氧化性不同的氧化剂反应时,其产物中铁元素的化合价不同:Fe被弱
氧化剂如S、I、H+、Fe3+、Cu2+等氧化为Fe2+;Fe被强氧化剂如Cl、Br 、HNO、浓HSO (△)等氧化为
2 2 2 3 2 4
Fe3+。
【对应训练】1.下列有关铁的说法正确的是( )
A.Fe在稀硝酸中发生钝化
B.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
C.向FeCl 溶液中滴加NH SCN溶液,溶液显红色
2 4
D.镀锌铁不如镀锡铁耐腐蚀
【答案】B
【解析】常温下,Fe在浓硝酸中发生钝化反应,A项错误;铁和亚铁离子能将氯气还原为氯离子,从
而除去工业废气中的氯气,B项正确;FeCl 溶液中含Fe2+,NH SCN可用于检验Fe3+,向FeCl 溶液中滴
2 4 2加NH SCN溶液,溶液不会显红色,C项错误;镀锌铁因Zn比Fe活泼,镀层破损时Zn被腐蚀,镀锡铁因
4
Fe比Sn活泼,因而镀层破损时是铁被腐蚀,所以镀锌铁比镀锡铁更耐腐蚀,D项错误。
2.将0.02mol铁分别投入足量的下列物质中,在一定条件下充分反应,产生氢气最多的是( )
A.2mol/L稀硫酸 B.18.4mol/L硫酸
C.5mol/L硝酸 D.灼热的水蒸气
【答案】D
【解析】A.铁与稀硫酸反应的化学方程式为:Fe+H SO =FeSO+H ↑,0.02molFe与足量稀硫酸反应
2 4 4 2
生成0.02molH;B.铁与浓硫酸反应不产生氢气;C.铁与硝酸反应不生成氢气;D.铁与灼热的水蒸气
2
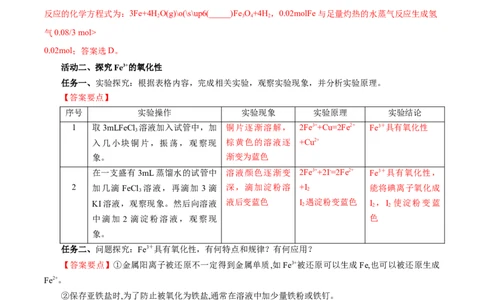
反应的化学方程式为:3Fe+4H O(g)\o(\s\up6(_____)Fe O+4H ,0.02molFe与足量灼热的水蒸气反应生成氢
2 3 4 2
气0.08/3mol>
0.02mol;答案选D。
活动二、探究Fe3+的氧化性
任务一、实验探究:根据表格内容,完成相关实验,观察实验现象,并分析实验原理。
【答案要点】
序号 实验操作 实验现象 实验原理 实验结论
1 取3mLFeCl 溶液加入试管中,加 铜片逐渐溶解, 2Fe3++Cu=2Fe2+ Fe3+具有氧化性
3
入几小块铜片,振荡,观察现 棕黄色的溶液逐 +Cu2+
象。 渐变为蓝色
在一支盛有3mL蒸馏水的试管中 溶液颜色逐渐变 2Fe3++2I-=2Fe2+ Fe3+具有氧化性,
2 加几滴 FeCl 3 溶液,再滴加 3 滴 深,滴加淀粉溶 +I 2 能将碘离子氧化成
KI溶液,观察现象。然后向溶液 液后变蓝色 I
2
遇淀粉变蓝色 I
2
,I
2
使淀粉变蓝
中滴加 2 滴淀粉溶液,观察现 色
象。
任务二、问题探究:Fe3+具有氧化性,有何特点和规律?有何应用?
【答案要点】①金属阳离子被还原不一定得到金属单质,如Fe3+被还原可以生成Fe,也可以被还原生成
Fe2+。
②保存亚铁盐时,为了防止被氧化为铁盐,通常在溶液中加少量铁粉或铁钉。
③Fe3+虽具有氧化性,但遇强氧化剂仍可将其氧化成更高价态的铁。如用过氧化钠与熔融的赤铁矿
(Fe O)在高温下反应可制得高铁酸钠(NaFeO)。3NaO+Fe O=====2NaFeO+NaO。
2 3 2 4 2 2 2 3 2 4 2
④Na FeO 具有很强的氧化性,非常有效地杀灭水中的病菌和病毒。与此同时,自身被还原生成
2 4
Fe(OH) 胶体能高效地除去水中的微细悬浮物。因此NaFeO 既是自来水的净水剂,又是消毒剂。
3 2 4
【对应训练】1.取某含铁元素的固体A进行如下实验:
根据下列转化关系,下列叙述不正确的是( )A.试剂1是KSCN溶液
B.试剂2可以是新制氯水
C.溶液B中只有Fe3+无Fe2+
D.溶液C到溶液F红色加深的原因是溶液中的Fe2+被氧化剂氧化成Fe3+,使Fe3+浓度增大
【答案】C
【解析】从框图可知,A和稀盐酸反应生成棕黄色溶液,加入试剂1变成淡红色溶液C,可以推断溶
液B中含有Fe3+,加入KSCN溶液生成Fe(SCN) ;加入试剂2得到深红色溶液F,可知试剂2为强氧化
3
剂,溶液B中含有Fe2+,加入试剂2(强氧化剂),Fe2+ 被氧化为Fe3+,并进一步转化为Fe(SCN) ,所以溶
3
液红色加深,故C错误。
2.将金属铁、铜投入FeCl 溶液中充分反应,下列对反应情况设想的评价正确的是( )
3
选项 反应情况设想 评价
当铁、铜均无剩余时,溶液中一定有
A 正确,Fe3+和铁、铜均可反应
Fe2+、Cu2+,一定无Fe3+
当铁、铜均有剩余时,溶液中一定有
B 正确,铁和铜都与Fe3+反应,故无Fe3+
Fe2+、Cu2+,无Fe3+
当铜有剩余,铁无剩余时,溶液中一定
C 正确,铜有剩余,故无Cu2+
只有Fe2+,无Cu2+
不正确,不可能出现铁有剩余而铜无剩余的
当铁有剩余,铜无剩余时,溶液中一定
D 情况,因为铁的还原性比铜的强,铁先与Fe3
有Fe2+、Cu2+
+反应
【答案】D
【解析】 对各选项的分析如下:
铁、铜均无剩余时,说明反应①②均发生,可能铁、铜恰好把Fe3+反应完,也
A 错误
可能铁、铜的量不足,Fe3+有剩余
铁、铜均有剩余时,说明只发生反应①,且Fe3+反应完了,反应②没发生,故
B 错误
溶液中无Cu2+
当铜有剩余,铁无剩余时,说明反应①发生,反应②可能发生也可能没发生,
C 错误
因此溶液中一定有Fe2+,可能有Cu2+
反应①先发生,把铁消耗完了,铜才参与反应,不可能存在铁有剩余而铜无剩
D 正确
余的情况
二、亚铁盐的氧化性和还原性
活动一、探究亚铁盐的氧化性和还原性
任务一、实验探究:根据表格内容,完成相关实验,观察实验现象,分析实验原理。
【答案要点】序号 实验操作 实验现象 实验原理 实验结论
1 取3mLFeCl 溶液加入试管中, 浅绿色溶液逐渐变为 Fe2++Zn==Fe+ Fe2+具有氧化性
2
加入几小块锌片,振荡,观察现 无色,同时有黑色固 Zn2+
象。 体生成
2 取3mLFeCl 溶液入试管中,加 铁粉逐渐溶解,溶液 2Fe3++Fe== Fe3+具有氧化性
3
入足量铁粉,振荡,观察现象。 由棕黄色变为浅绿色
3Fe2+
3 取3mLFeCl 溶液加入试管中, 溶液由浅绿色变为棕 Fe2++ Fe2+具有还原性
2
滴加几滴氯水,振荡,观察现 黄色 Cl==Fe3++2Cl-
2
象。
取少量酸性KMnO 溶液于试管 溶液的紫色逐渐褪 5Fe2++MnO- Fe2+具有还原
4 4
中,逐滴加入FeSO 溶液,当溶 去,后溶液呈现血红 +8H+= 5Fe3+ 性;Fe3+与
4
液紫色褪去时,再滴加2滴 色 +Mn2++4H 2 O KSCN溶液反应
4 KSCN溶液,观察现象
Fe3+ + 3SCN- =
成血红色溶液
Fe(SCN)
3
任务二、问题探究:某溶液中加KSCN溶液,颜色无变化,再加氯水溶液变红,说明什么?发生的反
应是什么?若溶液变红,然后加足量Fe粉,红色又褪去,说明什么?写出反应的离子方程式。
【答案要点】①颜色无变化,再加氯水溶液变红,说明原溶液中无Fe3+,有Fe2+,2Fe2++Cl===2Fe3
2
++2Cl-。
②若溶液变红,然后加足量Fe粉,红色又褪去,说明原溶液中有Fe3+,2Fe3++Fe===3Fe2+。
【对应训练】1.把表面有少量氧化物的铜片和铁片一起放入盐酸中,充分反应后,所得溶液中的金
属离子为( )
A.Fe3+和Cu2+ B.Fe2+和Cu2+
C.Fe2+和Fe3+ D.Fe2+
【答案】D
【解析】本题涉及的物质的性质有:CuO与盐酸的反应,Fe、Fe O 与盐酸的反应,Fe3+与Fe、Cu的
2 3
反应,Fe与Cu2+的反应等。表面氧化物较少,溶于盐酸后,生成的Fe3+和Cu2+较少,分别被Fe还原为
Fe2+和Cu,Cu与盐酸不反应,Fe与盐酸反应生成Fe2+。
2.已知氯气有强氧化性,能氧化Fe2+、Br-、I-等。又已知还原性I->Fe2+>Br-。向含有Fe2+、I-、Br-的溶
液中通入一定量氯气后,对所得溶液中离子的成分分析正确的是( )
A.I-、Fe3+、Cl- B.Fe2+、Cl-、Br-
C.Fe2+、Fe3+、Cl- D.Fe2+、I-、Cl-
【答案】B
【解析】在氧化还原反应中,氧化剂先氧化还原性强的离子,再氧化还原性弱的离子,只含有I-、
Fe2+、Br-溶液中通入氯气后,碘离子先被氧化,其次是亚铁离子,最后是溴离子。A.当溶液中含有碘离
子,就不会出现铁离子, I-、Fe3+、Cl-不能共存,故A错误;B. 通入氯气后,碘离子先被氧化,其次是
亚铁离子,当亚铁离子存在,则溴离子一定不会参与反应,氯气做氧化剂,对应产物是氯离子,故B正
确;C.当溶液中存在亚铁离子时,则一定会存在溴离子,故C错误;D.当溶液中存在亚铁离子时,则一定会存在溴离子,故D错误;故选B。
活动二、Fe(OH) 的制备
2
任务一、问题探究:为了提高皮革的耐曲折强度以及耐化学药剂和微生物的作用,常常使用绿矾作为
鞣革剂。绿矾晶体(FeSO ·7H O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质。为探究绿矾
4 2
样品的变质情况,化学兴趣小组的同学设计了下列实验方案。
可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液、铁粉,请
参与完成方案设计。
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。
①如何证明绿矾已被氧化?
②如何证明绿矾已完全被氧化
③为了防止绿矾溶液被氧化,如何操作?
【答案要点】①取少量溶液于试管中,加入几滴硫氰化钾溶液,若观察到溶液变红色,则证明绿矾样
品已被氧化。
②取少量溶液于试管中,加入几滴酸性高锰酸钾溶液,若观察到溶液不褪色,则证明绿矾样品完全被
氧化。
③取少量溶液于试管中,向溶液中加入适量铁粉防止绿矾溶液中的Fe2+被氧化:2Fe3++Fe==3Fe2+。
任务二、结合Fe(OH) 容易被空气中的氧气氧化成Fe(OH) 的性质,思考制备Fe(OH) 有哪些方法?
2 3 2
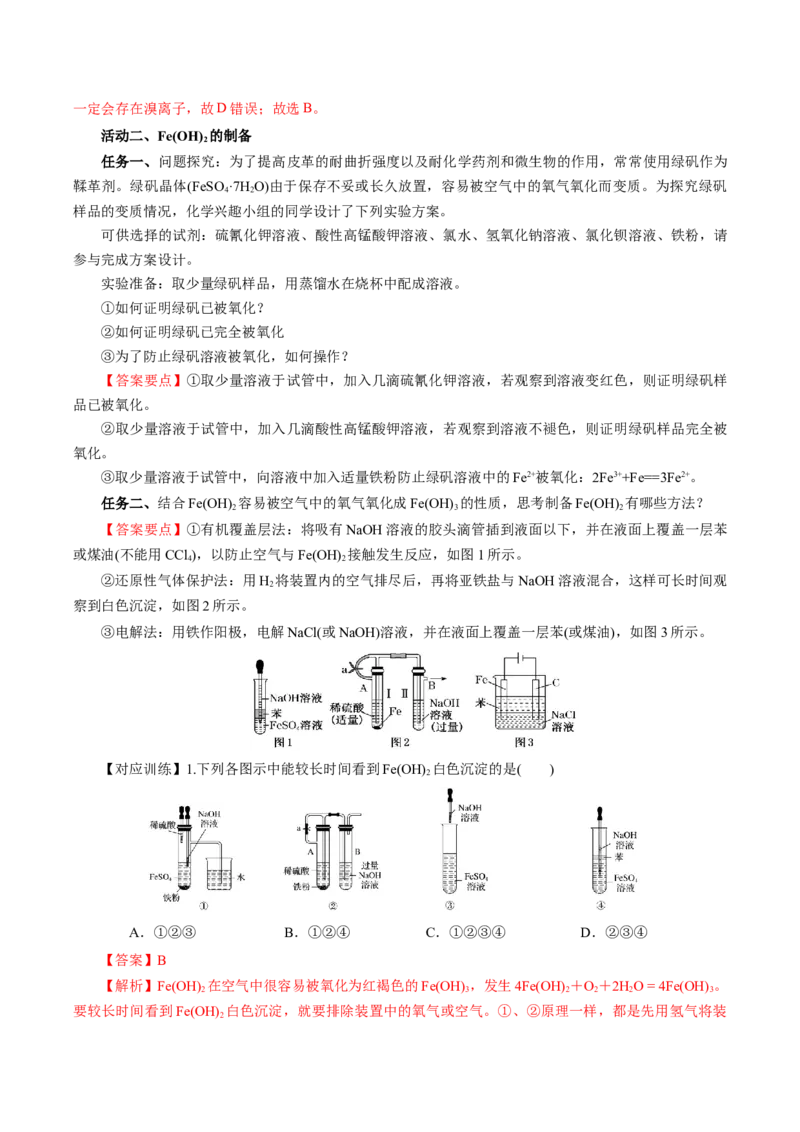
【答案要点】①有机覆盖层法:将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯
或煤油(不能用CCl ),以防止空气与Fe(OH) 接触发生反应,如图1所示。
4 2
②还原性气体保护法:用H 将装置内的空气排尽后,再将亚铁盐与NaOH溶液混合,这样可长时间观
2
察到白色沉淀,如图2所示。
③电解法:用铁作阳极,电解NaCl(或NaOH)溶液,并在液面上覆盖一层苯(或煤油),如图3所示。
【对应训练】1.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2
A.①②③ B.①②④ C.①②③④ D.②③④
【答案】B
【解析】Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,发生4Fe(OH) +O+2HO = 4Fe(OH) 。
2 3 2 2 2 3
要较长时间看到Fe(OH) 白色沉淀,就要排除装置中的氧气或空气。①、②原理一样,都是先用氢气将装
2置中的空气排尽,并使生成的Fe(OH) 处在氢气的保护中;③无法避免氧气与氢氧化亚铁的反应;④中液
2
面加苯阻止了空气进入,能较长时间看到白色沉淀,选B。
2.实验室用 FeCl 和烧碱制备 Fe(OH) ,为了使生成的产物不容易被氧化,下列说法不正确的是
2 2
( )
A.配制FeCl 溶液和烧碱溶液所用的蒸馏水通常要煮沸
2
B.可在FeCl 溶液的上面加一层苯,以隔绝空气
2
C.向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入溶液内
2
D.产生Fe(OH) 沉淀后,不能振荡试管
2
【答案】C
【解析】 A对,FeCl 溶液和烧碱溶液要现用现配,且配制溶液的蒸馏水要煮沸以除去氧气,确保
2
Fe(OH) 在无氧环境中生成。B对,在FeCl 溶液的上面加一层苯或一层油,以隔绝空气。C错,向FeCl 溶
2 2 2
液中滴加烧碱溶液时,要将胶头滴管的尖嘴伸入FeCl 溶液中,防止氢氧化钠溶液在滴入时接触空气而溶
2
有氧气。D对,产生Fe(OH) 沉淀后,若振荡试管,会增大沉淀与空气接触的机会,使沉淀更易被氧化。
2
【课后巩固】1.下列说法错误的是( )
A.浓硫酸在空气中敞口放置一段时间,浓度变小
B.铁片投入冷的浓硝酸中,铁片不溶解
C.钢片投入浓硝酸中,产生红棕色气体
D.石蕊溶液滴入稀硫酸中,溶液变蓝
【答案】D
【解析】A.浓硫酸具有吸水性,在空气中敞口放置一段时间,吸收空气中的水蒸气,浓度变小,故
A正确;B.铁片投入冷的浓硝酸中,铁片钝化,铁片不溶解,故B正确;C.钢片投入浓硝酸中发生反
应,硝酸被还原为红棕色二氧化氮气体,故C正确;D.石蕊遇酸变红,石蕊溶液滴入稀硫酸中,溶液变
红,故D错误;选D。
2.向FeCl 溶液中同时加入铁粉和铜粉,充分反应后不会出现的结果是( )
3
A.铁、铜均有 B.铁、铜均无
C.有铜无铁 D.有铁无铜
【答案】D
【解析】Fe3+先与Fe反应,Fe完全反应后,Fe3+再与Cu反应,故充分反应后不可能有铁无铜,D符
合题意。
3.在硫酸铁溶液中,加入a g铜完全溶解后再加入b g铁,充分反应后得到c g残余固体,且a>c,
则下列说法中正确的是( )
A.残余固体可能为铁和铜的混合物 B.最后得到的溶液可能含有Fe3+
C.残余固体是铁,溶液中一定不含Cu2+ D.残余固体全部是铜
【答案】D【解析】加入的a g铜由于发生反应:2Fe3++Cu===2Fe2++Cu2+而全部溶解,如果这部分铜在加入b
g铁后恰好被全部还原出来,则c应与a相等,现题给条件中知a>c,说明加入的a g铜没有全部被还
原,溶液中还有Cu2+,同时也说明加入的铁不足(否则a g铜将会被全部还原出来),加入的铁被氧化成Fe2
+;而Fe3+由于不能与单质铜共存,在溶液中已经不再存在;综上所述,c g残余固体是铜,溶液中还存在
Cu2+、Fe2+这2种金属阳离子,D项正确。
4.将过氧化钠投入FeCl 溶液中,可观察到的实验现象是( )
2
A.有无色气体和白色沉淀生成 B.有无色气体和红褐色沉淀生成
C.无气体产生,有沉淀生成 D.有气体产生,无沉淀生成
【答案】B
【解析】将过氧化钠投入FeCl 溶液中,过氧化钠会和水反应生成无色气体氧气和氢氧化钠,同时氧
2
化亚铁离子生成铁离子,再结合氢氧根离子生成红褐色的Fe(OH) 沉淀,所以可以看到的现象是:有无色
3
气体和红褐色沉淀生成,B正确。合理选项是B。
5.甲同学用FeCl 和烧碱制备Fe(OH) ;乙同学用如图装置制备Fe(OH) ,为了生成的产物不容易被氧
2 2 2
化,下列说法不正确的是( )
A.配制溶液所用的蒸馏水通常要煮沸
B.甲同学可在FeCl 溶液的上面加一层植物油,以隔绝空气
2
C.甲同学向FeCl 溶液中滴加烧碱溶液时,胶头滴管尖嘴可以伸入到液面下
2
D.乙同学应该先关闭止水夹,一段时间以后再打开止水夹
【答案】D
【解析】配制溶液时为防止水中溶解的氧气氧化亚铁离子,应先加热煮沸蒸馏水除去溶解氧,故 A正
确;植物油的密度比水小,浮在水面上,可以起到隔绝空气的作用,防止亚铁离子被氧化,故 B正确;向
FeCl 溶液中滴加烧碱溶液,为防止空气中的氧气被带入溶液中,将胶头滴管尖嘴直接伸入液面下再挤出烧
2
碱溶液,故C正确;实验过程中应先打开止水夹,让产生的氢气排尽装置内的空气,以防亚铁离子被氧
化,故D错误;故选D。
6.纳米级四氧化三铁是应用最为广泛的软磁性材料之一。共沉淀法是目前制备纳米四氧化三铁的重要
方法,其流程如图所示:下列说法错误的是( )
A.保存溶液A时,应加入少量铁粉
B. FeSO ‧7H O和FeCl ‧6H O的物质的量之比最好应为2∶1
4 2 3 2
C.取滤液进行焰色反应,火焰为黄色
D.其制备反应类型不属于氧化还原反应
【答案】B
【解析】保存溶液A时,应加入少量铁粉,防氧化;依据反应原理可知:FeSO ‧7H O和FeCl ‧6H O
4 2 3 2
的物质的量之比最好应为1∶2;取滤液(NaSO )进行焰色反应,火焰为黄色;其制备反应有化合价的变
2 4
化,属于氧化还原反应。
7.某同学欲利用如图装置制取能较长时间存在的Fe(OH) ,其中实验所用溶液现配现用且蒸馏水先加
2
热煮沸。下列分析不正确的是
A.X可以是稀硫酸或稀盐酸,但不能是稀硝酸
B.实验开始时应先关闭止水夹a、打开b,再向烧瓶中加入X
C.反应一段时间后可在锥形瓶中观察到白色沉淀
D.反应结束后若关闭b及分液漏斗活塞,则Fe(OH) 可较长时间存在
2
【答案】B
【解析】A.稀硝酸会将铁氧化为+3价的铁离子,故A正确;B.实验开始时,应先打开a、b,利用
生成的氢气将装置中的空气排出,然后关闭a,利用压强差将烧瓶中生成的亚铁离子排入锥形瓶中反应生
成Fe(OH) ,故B错误;C.反应一段时间后可在锥形瓶中观察到白色沉淀,故C正确;D.由于装置中的
2
空气及溶液中的氧气已经被除去,故Fe(OH) 可较长时间存在,故D正确。故选B。
2
8.实验探究Fe2+、Fe3+的性质。
已知:Fe2+可与K[Fe(CN) ]溶液反应生成蓝色沉淀。
3 6
(1)分别取一定量硫酸铁、氯化亚铁固体,均配制成0.1 mol·L-1溶液。配制FeCl 溶液时需加入少
2量铁屑,目的是__________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将
2 2
Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为________________________________。
2
(3)乙组同学认为甲组实验不够严谨,该组同学用煮沸冷却后的水配制溶液,向2 mL FeCl 溶液中先
2
加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
_____________________________。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入足量0.1 mol·L-1 Fe (SO ) 溶液混合后,滴加淀粉
2 4 3
溶液,出现蓝色,该现象说明氧化性:Fe3+_______I(填“>”或“<”);另取2 mL FeCl 溶液,加入几
2 2
小块锌片,实验现象为_______________________,说明Fe2+具有_______。(填“氧化性”或“还原
性”)。
(5)丁组同学为探究维生素C是否可将Fe3+转化为Fe2+,设计了如下实验。
实验操作 实验现象 得出结论
取一定量Fe (SO ) 溶液于试管中,加入维生
2 4 3 维生素C可将Fe3+
素C片,振荡溶解得到溶液a,取a溶液少 紫色褪去
转化为Fe2+
许,滴加酸性KMnO 溶液。
4
其他组同学认为:根据该实验现象不能得出“维生素C可将Fe3+转化为Fe2+”的结论,原因是
_______________________________________________________________;认为可另外设计实验验证结论
是否正确:取a溶液少许,滴加______________,若出现_________________________________________,
则结论正确。
【答案】(1)防止氯化亚铁被氧化 (2)2Fe2++Cl =2Fe3++2Cl- (3)隔绝空气,防止氯化亚
2
铁被氧化 (4)> 溶液由浅绿色变为无色 氧化性 (5)维生素C可能过量,也可使高锰酸钾溶液褪
色 氢氧化钠溶液 白色沉淀变为灰绿色最终变为红褐色