文档内容
第二章 海水中的重要元素—钠和氯
第一节 钠及其化合物 课时作业
专题 两种重要的钠盐
基础达标
1.下列有关各种物质的物理性质的叙述中不正确的是( )
A.金属钠的氧化物都是淡黄色的固体 B.金属钠的密度比水小
C.纯碱和小苏打都能溶于水 D.鉴别碳酸钠和碳酸钾可以使用焰
色反应
【答案】A
【解析】A项,NaO是白色固体,NaO 是淡黄色的固体,错误;B项,金属钠能浮
2 2 2
在水面上,金属钠的密度比水小,正确;C项,碳酸钠和碳酸氢钠都能溶于水,正确;D
项,钠元素的焰色为黄色、钾元素的焰色为紫色,鉴别碳酸钠和碳酸钾可以使用焰色反
应,正确。
2.下列说法错误的是( )
A.向碳酸钠中加入少量水后,插入温度计,显示温度上升
B.焰色反应的铂丝可用稀盐酸洗
C.可用澄清的石灰水鉴别NaCO 和NaHCO 两种溶液
2 3 3
D.NaCl可用作食品调味剂
【答案】C
【解析】碳酸钠溶于水放热,故A正确;盐酸可以溶解氧化物等杂质,且易挥发,不
会残留痕迹,故B正确;加入澄清的石灰水,NaCO 溶液和NaHCO 溶液都能生成CaCO
2 3 3 3
沉淀,不能区别两种溶液,故C错误。
3.下列关于碳酸钠和碳酸氢钠的叙述,正确的是( )
A.常温时,在水中的溶解度:碳酸钠>碳酸氢钠
B.热稳定性:碳酸钠<碳酸氢钠
C.质量相同时,分别与同体积、同浓度盐酸反应,产生气泡快慢:碳酸钠>碳酸氢
钠
D.质量相同时,分别与足量的盐酸反应,生成 的质量:碳酸钠=碳酸氢钠
【答案】A【解析】A.常温时,在水中的溶解度:碳酸钠>碳酸氢钠,故A正确;B.碳酸氢钠受
热易分解,生成碳酸钠、水和二氧化碳,碳酸钠不分解,热稳定性:碳酸钠>碳酸氢钠,
故B项错误;C.碳酸钠与盐酸反应首先转化为碳酸氢钠,然后碳酸氢钠与盐酸反应放出二
氧化碳,因此质量相同时,分别与同体积、同浓度盐酸反应,产生气泡快慢:碳酸钠<碳
酸氢钠,C项错误;D.质量相同时,分别与足量的盐酸反应,根据化学方程式计算得,生
成CO 的质量:碳酸钠<碳酸氢钠,D项错误。故选A。
2
4.为了检验NaHCO 固体中是否含有NaCO,下列实验及判断中,正确的是( )
3 2 3
A.加热,观察是否有气体放出
B.溶于水后加BaCl 溶液,看有无沉淀
2
C.溶于水后加澄清石灰水,看有无沉淀
D.取固体试样加盐酸,看是否有气泡产生
【答案】B
【解析】对题述物质加热,只能证明有 NaHCO ,而不能证明含有NaCO ;NaHCO
3 2 3 3
与NaCO 都能与澄清石灰水反应产生沉淀,都能与盐酸反应产生气泡,无法证明含有
2 3
NaCO。
2 3
5.钠元素广泛存在于自然界,中国科学技术大学的钱逸泰教授等以CCl 和金属钠为
4
原料,在700 ℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,
立刻被科学家们高度评价为“稻草变黄金”。下列关于含钠元素的物质的说法错误的是(
)
A.“稻草变黄金”的过程中元素种类没有改变
B.NaCl与NaCO 灼烧时火焰颜色相同
2 3
C.治疗胃酸过多可以用NaHCO ,糕点制作也可以用NaHCO
3 3
D.金属钠放置空气中,最终会变成NaO
2 2
【答案】D
【解析】化学变化过程中元素守恒,所以此过程中元素种类没有改变,故A正确;焰
色反应是元素的性质,钠元素的焰色为黄色,则NaCl与NaCO 灼烧时火焰颜色均为黄
2 3
色,故B正确;NaHCO 与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,所以可以
3
用NaHCO 治疗胃酸过多;NaHCO 受热分解也生成二氧化碳气体,遇热膨胀而形成小孔,
3 3
使得糕点松软多孔,故糕点生产也可以用NaHCO ,故C正确。
3
6.下列除去物质中少量杂质的方法正确的是( )
选项 物质 杂质 除去杂质的方法
A NaHCO 固体 NaCO 固体 将固体混合物加热至恒重
3 2 3
B NaO 粉末 NaO 将混合物在氧气中充分加热
2 2 2
C NaC1溶液 NaHCO 加入盐酸,加热
3D CO HCl 通过盛有氢氧化钠溶液的洗气瓶
2
A.A B.B C.C D.D
【答案】BC
【解析】A.将固体加热,固体NaHCO 受热分解变为Na2CO3固体,导致物质完全变
3
质,不能达到实验目的,A不符合题意;B.将混合物在氧气中充分加热,Na2O与空气中
的O 反应变为Na2O2,能够达到实验目的,B符合题意;C.向含有NaHCO3的NaCl溶
2
液中加入稀盐酸,盐酸与NaHCO3反应变为NaCl,最后加热,反应产生CO2气体及过量
HCl挥发逸出,能够达到除杂、净化的目的,C符合题意;D.CO2及杂质HCl都可以与
除杂试剂NaOH溶液反应,不能达到除杂、净化的目的,D不符合题意;故合理选项是
BC。
7.下列化学方程式中,不能正确表达反应颜色变化的是( )
A.向CuSO 溶液中加入足量Zn粉,溶液蓝色消失:Zn+CuSO =Cu+ZnSO
4 4 4
B.澄清的石灰水久置后出现白色固体:Ca(OH) +CO =CaCO ↓+H O
2 2 3 2
C.NaO 在空气中放置后由淡黄色变为白色:2NaO=2Na O+O↑
2 2 2 2 2 2
D.向Mg(OH) 悬浊液中滴加足量FeCl 溶液出现红褐色沉淀:
2 3
3Mg(OH) +2FeCl =2Fe(OH) +3MgCl
2 3 3 2
【答案】 C
【解析】C.过氧化钠在空气中放置后由淡黄色变为白色,发生反应的化学方程式:
2NaO+2CO =2Na CO+O 。所以C选项错误,故答案为:C
2 2 2 2 3 2
8.下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是(
)
选项 陈述Ⅰ 陈述Ⅱ 判断
Ⅰ对,Ⅱ
A 纯碱可用于治疗胃溃疡 纯碱可与盐酸反应
对,有
CO 中的少量HCl杂质可将气 NaCO 可与HCl反 Ⅰ对,Ⅱ
B 2 2 3
体通入饱和NaCO 溶液除去 应 错,无
2 3
NaCO 溶液中混有少量
2 3 NaHCO 可与NaOH Ⅰ对,Ⅱ
C NaHCO 杂质,可加入适量 3
3 反应生成NaCO 对,有
NaOH除去 2 3
向饱和NaCO 溶液中通入 Ⅰ对,Ⅱ
D 2 3 NaHCO 难溶于水
CO 气体,有白色晶体析出 3 对,有
2
【答案】C
【解析】A项,碳酸钠能够与盐酸反应,但是碳酸钠碱性较强,具有腐蚀性,不能用
于治疗胃酸过多,所以陈述Ⅰ错误,故A错误;B项,NaCO 可与HCl反应,但CO 也可
2 3 2以和NaCO 反应,所以不能用饱和NaCO 溶液除去CO 中少量的HCl杂质,故陈述Ⅰ错
2 3 2 3 2
误,故B错误;C项,NaHCO 可与NaOH反应生成NaCO 和HO,可用适量的NaOH溶
3 2 3 2
液除去NaCO 溶液中混有少量有NaHCO 杂质,陈述Ⅰ和陈述Ⅱ都对,故C正确;D项,
2 3 3
向饱和NaCO 溶液中通入CO2气体,可发生反应:NaCO+ CO+H O=2 NaHCO,由于相
2 3 2 3 2 2 3
同温度下,NaHCO 的溶解度小于NaCO 的溶解度,所以有NaHCO 晶体析出,陈述Ⅰ
3 2 3 3
对,陈述Ⅱ错误,故D错误;故选 C 。
9.用如图所示的实验装置模拟侯氏制碱法的主要反应原理。下列说法正确的是( )
A.侯氏制碱法中可循环利用的气体为NH
3
B.先从a管通入NH ,再从b管通入CO
3 2
C.为吸收剩余的NH ,c中应装入碱石灰
3
D.反应后冷却,瓶中析出的晶体主要是纯碱
【答案】B
【解析】侯氏制碱法中可循环利用的气体是CO ,A项错误;NH 在水中的溶解度极
2 3
大,为了防止倒吸,应先从a管通入NH ,再从b管通入CO ,B项正确;碱石灰(主要成
3 2
分是 NaOH 和 CaO)不能吸收 NH ,C 项错误;反应后冷却,瓶中析出的晶体主要是
3
NaHCO ,将其加热得到纯碱(Na CO),D项错误。
3 2 3
10.侯德榜是我国近代化学工业的奠基人之一,他将氨碱法和合成氨工艺联合起来,
发明了“联合制碱法”。氨碱法中涉及的反应有:
反应Ⅰ:NaCl+CO+NH +HO=NaHCO ↓+NH Cl;
2 3 2 3 4
反应Ⅱ:2NaHCO ====NaCO+CO↑+HO。
3 2 3 2 2
下列装置不能达到相应实验目的的是( )
A B C D
除去CO 中 的HCl 制取NaHCO 分离出NaHCO 制取NaCO
2 3 3 2 3【答案】A
【解析】A项,除去CO 中HCl,可以把混合气体通入饱和碳酸氢钠溶液,碳酸钠溶
2
液也能与CO 反应,不符合除杂原则,错误;B项,溶有氨气的饱和食盐水溶液呈碱性,
2
有利于增大二氧化碳的溶解,反应生成碳酸氢钠晶体和氯化铵,可制取NaHCO ,正确;C
3
项,NaHCO 在该反应中以固体析出,因此可用过滤操作分离,正确;D项,碳酸氢钠固
3
体受热分解过程中生成碳酸钠、二氧化碳和水,试管口略向下倾斜,可制取NaCO,正
2 3
确。
能力提升
11.以不同类别物质间的转化为线索,认识钠及其化合物。下列分析不正确的是(
)
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的稳定性强于NaCO
3 2 3
C.反应⑤⑥说明NaO 可用于潜水艇中氧气的供给
2 2
D.上述转化中发生的反应有分解反应、化合反应、置换反应等
【答案】B
【解析】与碱反应生成盐与水的氧化物为酸性氧化物,二氧化碳与氢氧化钠反应生成
碳酸钠和水,则反应③表明CO 具有酸性氧化物的性质,故A正确;碳酸氢钠受热分解生
2
成碳酸钠,则反应④说明NaCO 的稳定性强于NaHCO ,故B错误;过氧化钠与水、二
2 3 3
氧化碳反应生成氧气,反应⑤⑥说明NaO 可用于潜水艇中氧气的供给,故C正确;④是
2 2
分解反应,①是化合反应,②是置换反应,故D正确。
12.过碳酸钠(2Na CO·3H O),有NaCO 和HO 的双重性质,可用作漂白剂和氧化
2 3 2 2 2 3 2 2
剂,能有效杀灭禽流感病毒。合理组合下列装置能用于测定过碳酸钠中碳酸钠的含量,下
列说法不正确的是( )
A.连接顺序为装置Ⅲ→Ⅰ→Ⅱ
B.装置b和e中盛放的试剂相同C.装置d的作用是防止空气中的HO和CO 进入c中
2 2
D.若b中盛放的是澄清石灰水,只用装置Ⅰ即可验证过碳酸钠与硫酸反应是否生成
CO(不考虑空气中CO 的影响)
2 2
【答案】B
【解析】稀硫酸与过碳酸钠反应生成CO ,由于空气中含有CO ,所以需要除去空气
2 2
中的CO ,又因为还需要防止空气中的水蒸气进入c,所以连接顺序是装置Ⅲ→Ⅰ→Ⅱ,A
2
项正确;装置b和e中盛放的试剂分别是浓硫酸和氢氧化钠溶液,B项错误;氢氧化钙与
CO 反应生成碳酸钙沉淀,因此若b中盛放的是澄清石灰水,只用装置Ⅰ即可验证过碳酸
2
钠与硫酸反应是否生成CO,D项正确。
2
13.某班级化学兴趣小组做如下实验,请回答相关问题:
(1)甲组做金属钠在空气中燃烧的实验。实验室取用金属钠的方法是________________
_______________________________________________________。
(2)金属钠燃烧时会生成黑色固体,黑色固体的可能来源是________、________。
(3)某同学想用金属钠和空气制备纯度较高的NaO(不考虑空气中的N),可利用的装
2 2 2
置如下。
回答下列问题:
①装置Ⅳ中盛放的药品是________,若没有该装置可能导致生成的 NaO 中含有
2 2
________ , 其 反 应 的 化 学 方 程 式 为
__________________________________________________。
②若规定气流的方向为从左到右,各仪器连接的顺序是:空气进入________,
________接__________,________接______,______接________(填字母)。
③ 装 置 Ⅱ 的 作 用 是
___________________________________________________________。
【答案】(1)打开盛放金属钠的试剂瓶,用镊子取出一小块钠,放在滤纸上吸干表面的
煤油,再用小刀切下所需大小的钠块,余下的放回原试剂瓶,盖好瓶塞
(2)表面的煤油 空气中的二氧化碳(或酒精灯挥发的酒精;金属钠存在杂质铁元素,燃
烧时生成铁的氧化物;答任意两点即可)
(3)①氢氧化钠溶液 NaCO 2NaO+2CO===2Na CO+O
2 3 2 2 2 2 3 2
②h g f e a b c
③防止空气中的水和二氧化碳进入装置Ⅰ【解析】(3)要制备高纯度的NaO ,需要除去空气中的CO 和水蒸气。装置Ⅲ的作用
2 2 2
是除去水蒸气,装置Ⅳ的作用是用 NaOH溶液除去CO ,如果不除去CO ,则CO 会与
2 2 2
NaO 反应生成NaCO ;装置Ⅱ连接在硬质玻璃管末端,作用是防止空气中的水蒸气和
2 2 2 3
CO 进入装置Ⅰ。
2
直击高考
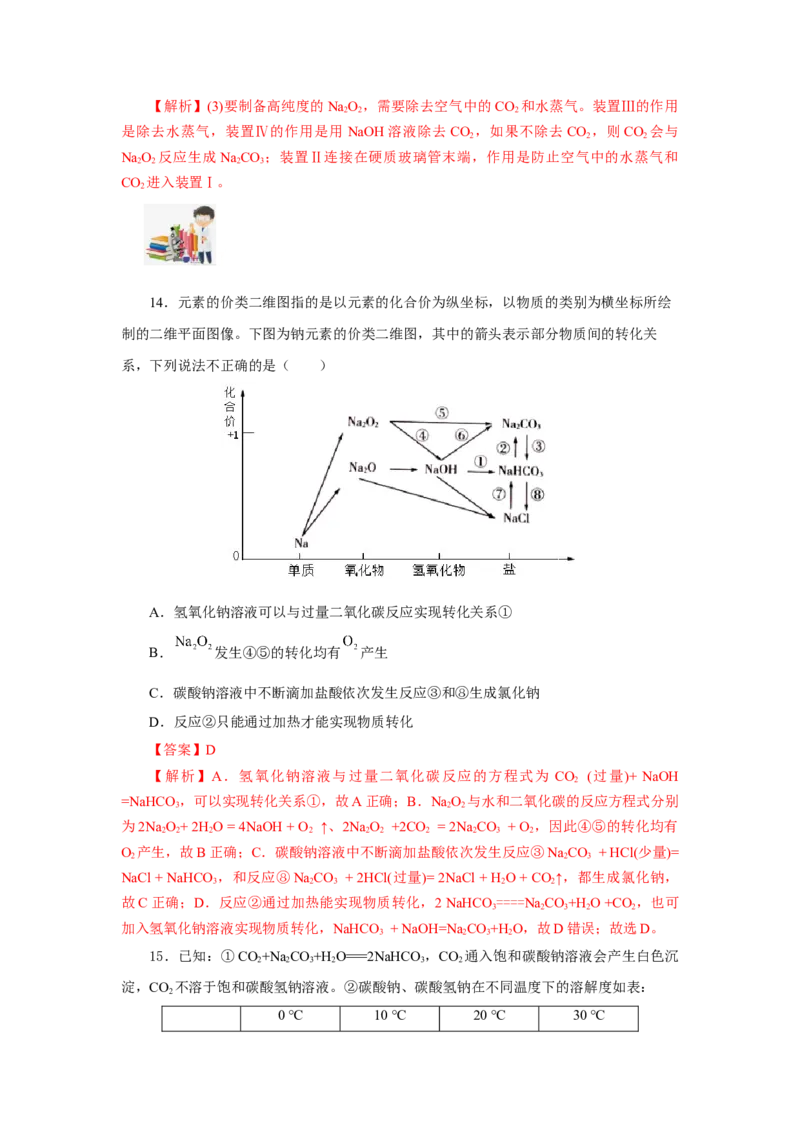
14.元素的价类二维图指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘
制的二维平面图像。下图为钠元素的价类二维图,其中的箭头表示部分物质间的转化关
系,下列说法不正确的是( )
A.氢氧化钠溶液可以与过量二氧化碳反应实现转化关系①
B. 发生④⑤的转化均有 产生
C.碳酸钠溶液中不断滴加盐酸依次发生反应③和⑧生成氯化钠
D.反应②只能通过加热才能实现物质转化
【答案】D
【解析】A.氢氧化钠溶液与过量二氧化碳反应的方程式为 CO (过量)+ NaOH
2
=NaHCO,可以实现转化关系①,故A正确;B.NaO 与水和二氧化碳的反应方程式分别
3 2 2
为2NaO+ 2H O = 4NaOH + O ↑、2NaO +2CO = 2Na CO + O ,因此④⑤的转化均有
2 2 2 2 2 2 2 2 3 2
O 产生,故B正确;C.碳酸钠溶液中不断滴加盐酸依次发生反应③NaCO + HCl(少量)=
2 2 3
NaCl + NaHCO ,和反应⑧NaCO + 2HCl(过量)= 2NaCl + H O + CO ↑,都生成氯化钠,
3 2 3 2 2
故C正确;D.反应②通过加热能实现物质转化,2 NaHCO ====NaCO+H O +CO ,也可
3 2 3 2 2
加入氢氧化钠溶液实现物质转化,NaHCO + NaOH=Na CO+H O,故D错误;故选D。
3 2 3 2
15.已知:①CO+Na CO+H O===2NaHCO ,CO 通入饱和碳酸钠溶液会产生白色沉
2 2 3 2 3 2
淀,CO 不溶于饱和碳酸氢钠溶液。②碳酸钠、碳酸氢钠在不同温度下的溶解度如表:
2
0 ℃ 10 ℃ 20 ℃ 30 ℃NaCO 7.1 12.2 21.8 39.7
2 3
NaHCO 6.9 8.1 9.6 11.1
3
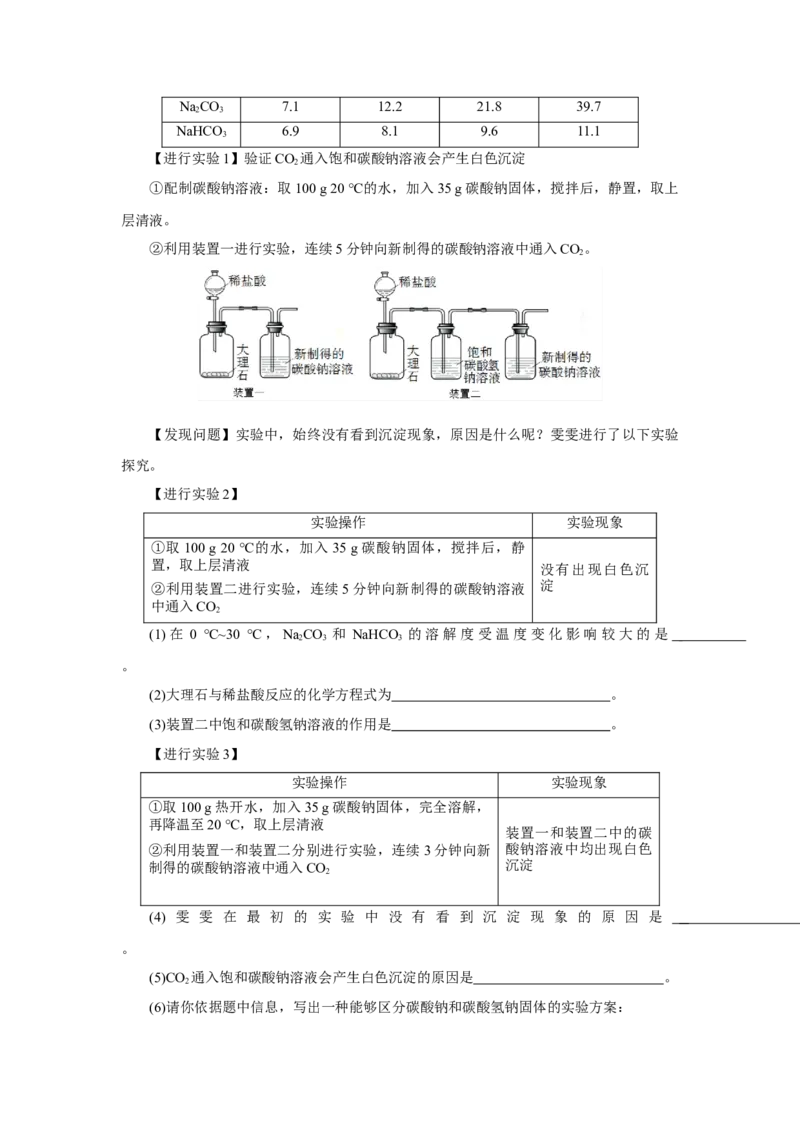
【进行实验1】验证CO 通入饱和碳酸钠溶液会产生白色沉淀
2
①配制碳酸钠溶液:取100 g 20 ℃的水,加入35 g碳酸钠固体,搅拌后,静置,取上
层清液。
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO。
2
【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验
探究。
【进行实验2】
实验操作 实验现象
①取100 g 20 ℃的水,加入35 g碳酸钠固体,搅拌后,静
置,取上层清液
没有出现白色沉
②利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液 淀
中通入CO
2
(1)在 0 ℃~30 ℃,NaCO 和 NaHCO 的溶解度受温度变化影响较大的是
2 3 3
。
(2)大理石与稀盐酸反应的化学方程式为 。
(3)装置二中饱和碳酸氢钠溶液的作用是 。
【进行实验3】
实验操作 实验现象
①取100 g热开水,加入35 g碳酸钠固体,完全溶解,
再降温至20 ℃,取上层清液
装置一和装置二中的碳
②利用装置一和装置二分别进行实验,连续3分钟向新 酸钠溶液中均出现白色
制得的碳酸钠溶液中通入CO 沉淀
2
(4) 雯 雯 在 最 初 的 实 验 中 没 有 看 到 沉 淀 现 象 的 原 因 是
。
(5)CO 通入饱和碳酸钠溶液会产生白色沉淀的原因是 。
2
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案:。
【答案】(1) Na CO (2)CaCO +2HCl===CaCl +H O+CO↑
2 3 3 2 2 2
(3)排除HCl的干扰 (4)配制的碳酸钠溶液没有达到饱和
(5)碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠
(6)方法一:取其中一种固体12 g,加入100 g热开水,充分溶解后,降温至20 ℃。若
有固体析出,为碳酸氢钠;否则为碳酸钠
方法二:取其中一种固体12 g,加入100 g 20 ℃的水,充分溶解后,若有白色固体剩
余,为碳酸氢钠;否则为碳酸钠