文档内容
第二章 海水中的重要元素----钠和氯
第二节 氯及其化合物
第3课时 氯气的制备
( 1)能通过氯气的制备,体会实验对认识和研究物质性质的重要作用,培养证据推理意识。
(2)通过氯气的制备,继续完善含氯元素的物质间的转化关系,进一步了解研究物质的思路和方法。
(3)通过氯气的制备,体会环境保护的重要意义,增强社会责任感。
(4)通过价类二维图的构建,掌握物质研究的基本思路和方法。
【内容分析】
本节内容以氯气的制备为主线,对气体的制备模型进行了初步构建。该模型包括发生装置、除杂装置、
收集装置和尾气处理装置。通过研究该模型的选择依据,深化氯气的性质,让学生对于氯及其化合物的相
互转化理解得更透彻。
在完成气体制备模型的构建后,本节还从氧化还原的角度深入探讨了氯气制备的原理,更好地落实了
宏观辨识和微观辨析、模型构建和证据推理素养。
在内容的选取上,借助了初中氧气和二氧化碳制备的知识作为对比,让学生的学习进一步体会对比法、
归纳法等对于化学学习的重要性。此外,在完成氯气制备的探讨后,还增加了氯的价类二维图的构建。通
过该活动,让学生进一步构建非金属及其化合物的研究模型,为学生后续学习其他的非金属元素及其相应
的化合物等奠定了基础。
【教学重点和难点】
重点:氯气的制备;气体制备的研究思路和方法的建构。
难点:装置的选择依据。
【教学流程】【学习任务一】温故知新,追求新知
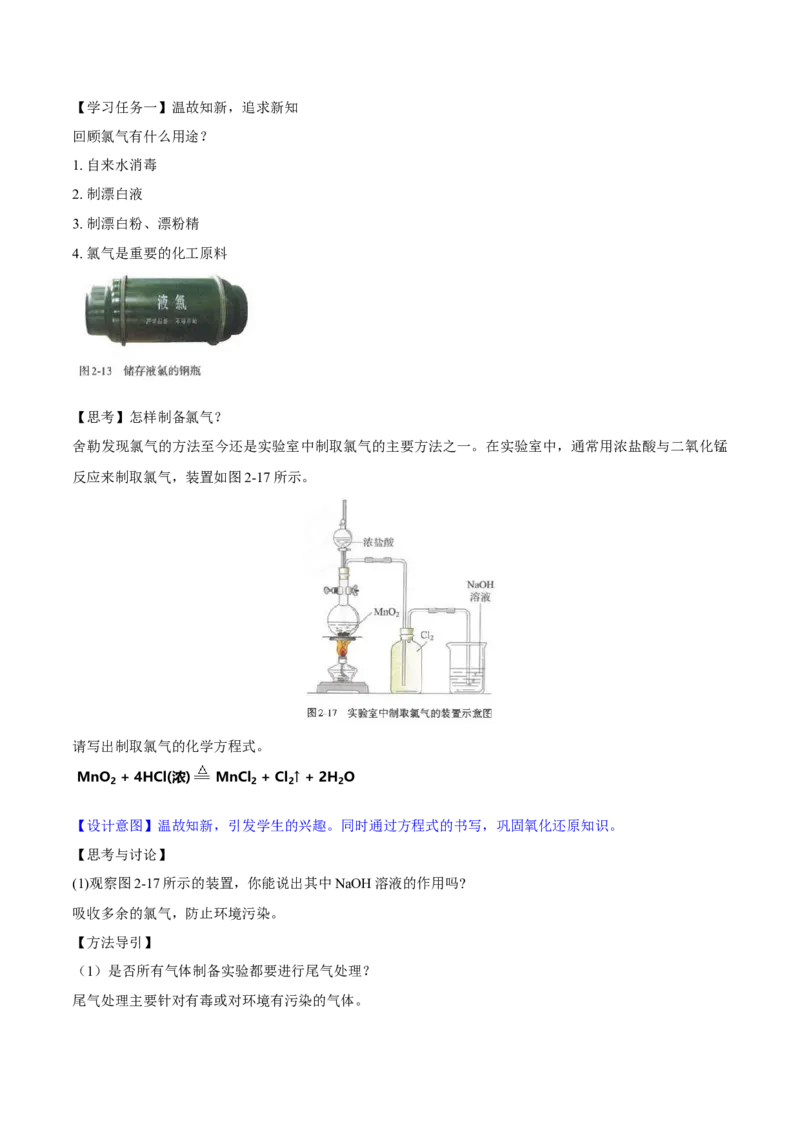
回顾氯气有什么用途?
1. 自来水消毒
2. 制漂白液
3. 制漂白粉、漂粉精
4. 氯气是重要的化工原料
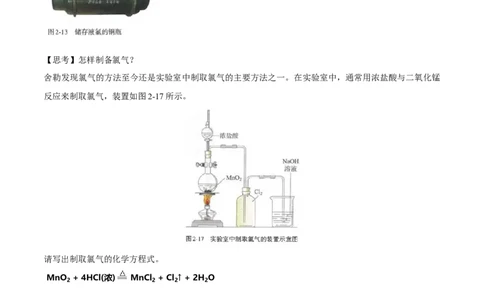
【思考】怎样制备氯气?
舍勒发现氯气的方法至今还是实验室中制取氯气的主要方法之一。在实验室中,通常用浓盐酸与二氧化锰
反应来制取氯气,装置如图2-17所示。
请写出制取氯气的化学方程式。
MnO + 4HCl(浓) MnCl + Cl ↑ + 2H O
2 2 2 2
【设计意图】温故知新,引发学生的兴趣。同时通过方程式的书写,巩固氧化还原知识。
【思考与讨论】
(1)观察图2-17所示的装置,你能说出其中NaOH溶液的作用吗?
吸收多余的氯气,防止环境污染。
【方法导引】
(1)是否所有气体制备实验都要进行尾气处理?
尾气处理主要针对有毒或对环境有污染的气体。(2)尾气处理的依据是什么?
依据是气体本身的性质。
【学习任务二】对比归纳,构建气体制备模型
【思考与讨论】
(2)回顾初中所学的氧气、二氧化碳等气体的实验室制取方法,将相关内容填入下表。讨论氯气的制备装置
和它们一样吗?如果一样,属于哪一种?如果不一样,请类比归纳氯气的制备装置。
氯气的实验室制取是固体+液体加热制取气体,不属于初中学习的任何一种实验室制取模型,一般会选取
分液漏斗、圆底烧瓶和酒精灯组装气体发生装置。
【方法导引】
如何选择气体的发生装置?
依据反应物的状态和条件。
【思考与讨论】
(3)根据上述装置图归纳氧气、二氧化碳和氯气是怎样收集的?依据是什么?
氧气用了排水法收集,二氧化碳和氯气都用了向上排空气法收集。
【方法导引】
依据气体的密度、气体在水中的溶解性,以及是否与水反应,选择收集装置。
【思考与讨论】
(4)应用上述装置能否收集到纯净干燥的氯气?如果不能,杂质是什么。
不能。浓盐酸会挥发,而且含有水蒸气。
【思考与讨论】
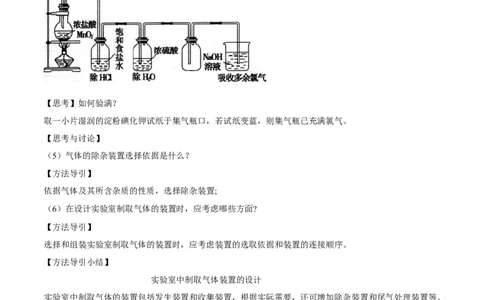
请根据以下信息,设计实验方案,制备并收集一瓶纯净干燥的氯气。
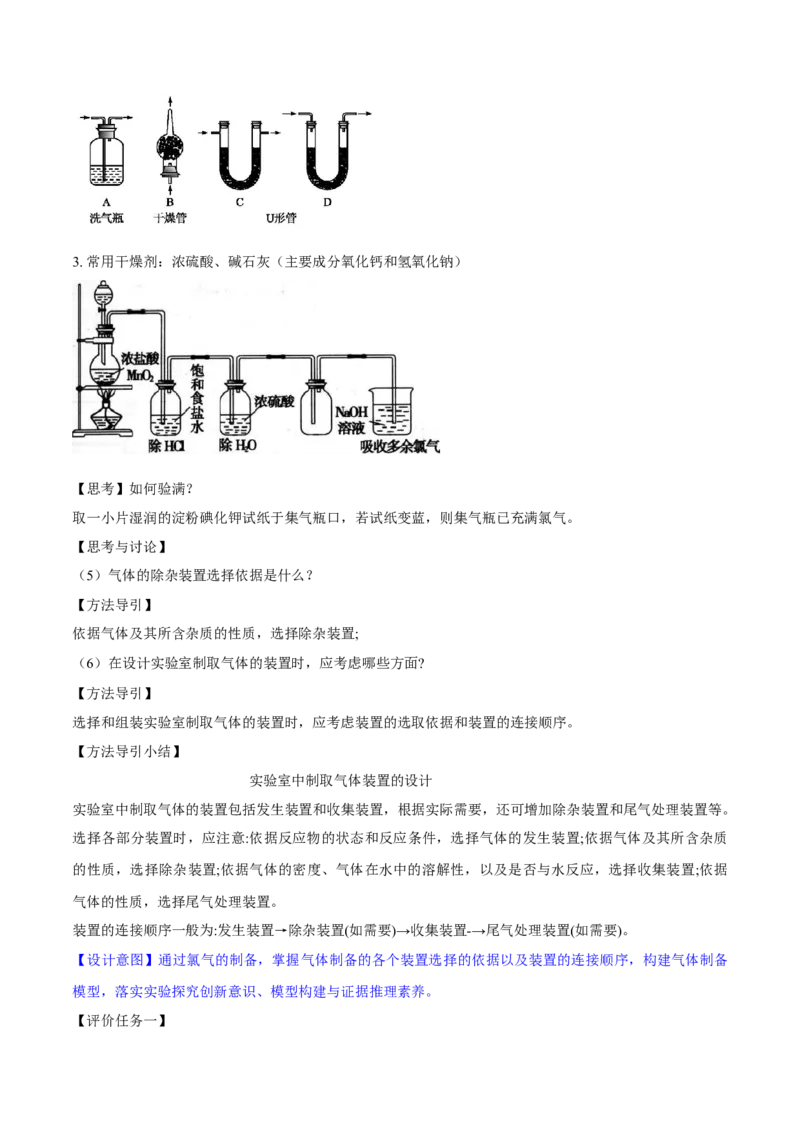
1. 常温常压下,HCl的溶解度为1:500
2. 常见除杂装置3. 常用干燥剂:浓硫酸、碱石灰(主要成分氧化钙和氢氧化钠)
【思考】如何验满?
取一小片湿润的淀粉碘化钾试纸于集气瓶口,若试纸变蓝,则集气瓶已充满氯气。
【思考与讨论】
(5)气体的除杂装置选择依据是什么?
【方法导引】
依据气体及其所含杂质的性质,选择除杂装置;
(6)在设计实验室制取气体的装置时,应考虑哪些方面?
【方法导引】
选择和组装实验室制取气体的装置时,应考虑装置的选取依据和装置的连接顺序。
【方法导引小结】
实验室中制取气体装置的设计
实验室中制取气体的装置包括发生装置和收集装置,根据实际需要,还可增加除杂装置和尾气处理装置等。
选择各部分装置时,应注意:依据反应物的状态和反应条件,选择气体的发生装置;依据气体及其所含杂质
的性质,选择除杂装置;依据气体的密度、气体在水中的溶解性,以及是否与水反应,选择收集装置;依据
气体的性质,选择尾气处理装置。
装置的连接顺序一般为:发生装置→除杂装置(如需要)→收集装置-→尾气处理装置(如需要)。
【设计意图】通过氯气的制备,掌握气体制备的各个装置选择的依据以及装置的连接顺序,构建气体制备
模型,落实实验探究创新意识、模型构建与证据推理素养。
【评价任务一】据台湾媒体报道,北县中和市锦和中学的部分学生,在清扫厕所时误以为浴厕清洁剂(主要成分是盐酸)
与漂白液混合,清洁效果会更强,结果混合后产生氯气,并冒出大量浓烟,九名学生疑似氯气吸入过多,
身体不适被送往双和医院,诊治后幸无大碍。 请尝试写出产生氯气的化学方程式。
2HCl+ NaClO = NaCl+HO+ Cl↑
2 2
【思考与讨论】
对比上述方程式与实验室制备氯气的方程式,你能总结出制备氯气的原理吗?
两个反应中盐酸都是做还原剂,要制备氯气可在浓盐酸中加入氧化剂。
【思考与讨论】
模仿上述方程式,试着用你熟悉的试剂写出其他制备氯气的方法。
【设计意图】结合氧化还原反应,拓展氯气的制备知识,巩固氧化还原知识。
【评价任务二】
1.分析下列反应,回答问题。
1. _________是氧化产物,_________是还原产物
2.浓盐酸表现出________性和________性
3.氧化剂与还原剂的质量之比为________
【答案】Cl Cl 还原 酸 73:49
2 22.实验室中为进行有关氯气的性质实验,需要 4瓶体积为100mL的氯气。(常温下,氯气的密度为2.91
g/L。)
(1)制取4瓶氯气,理论上需要MnO 的质量是多少?
2
(2)实际称取的MnO 固体的质量必须适当多于理论量,主要原因是什么?
2
【答案】1.426g 实际称取的MnO 固体的质量必须适当多于理论量
2
【解析】需制备氯气0.1*2.91*4=1.164g,MnO
2
+ 4HCl(浓) MnCl
2
+ Cl
2
↑ + 2H
2
O
根据反应方程式可计算需要MnO 的质量是1.426g。实际实验中不能实现全部转化,要考虑损耗,所以实
2
际称取的MnO 固体的质量必须适当多于理论量。
2
【设计意图】通过氧化还原的知识应用,回顾初中质量的计算知识,为后面学习物质的量打下基础。
【评价任务三】
1.在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。
2 2
下列收集Cl 的正确装置是___________。
2
【答案】C
2.对比上述C装置与教材中氯气收集的装置,有什么区别,哪个更合理。
【答案】C装置更合理。因为氯气和氢氧化钠反应后,会导致导管口压强减小,容易产生倒吸。
【评价任务四】【答案】A
【解析】
A. 二氧化碳中含有氯化氢,需用饱和碳酸氢钠溶液除去氯化氢,不能用饱和碳酸钠,因为碳酸钠和二氧化
碳也反应,故A不能达到目的;
B.氯气中混有少量的氯化氢气体,可以用饱和食盐水除去;饱和食盐水在吸收氯化氢气体的同时,也会
抑制氯气在水中的溶解,故B项能实现除杂目的;
C.氮气中混有少量氧气,在通过灼热的铜丝网时,氧气可以与之发生反应: ,而铜与氮气无法反应,因
此可以采取这种方式除去杂质氧气,故C项能实现除杂目的;
D. 一氧化碳中含有二氧化碳,可用氢氧化钠除去二氧化碳,D达到目的。
【设计意图】通过高考题的改编,结合初中知识以及气体制备的除杂与尾气处理知识,检测学生的学习成
果,落实证据推理与模型构建、宏观辨识与微观辨析素养。
【学习任务五】模型构建,形成知识体系
请把氯及其常见化合物填入下图。画出它们之间的转化关系,并写出相关的化学方程式或离子方程式。
(课后完成)
KClO
3
Ca(ClO)
2
单质
【设计意图】元素化合物的知识比较零散,通过价类二维图进行归纳总结能有效提高学习效率,在整个元
素及其化合物的学习过程中必须不断强化。一、思考与讨论
(1)观察图2-17所示的装置,你能说出其中NaOH溶液的作用吗?
(2)结合初中所学的氧气、二氧化碳等气体的实验室制取方法讨论:在设计实验室制取气体的装置时,应考虑
哪些方面?
【答案】
(1) NaOH溶液的作用是吸收多余的氯气,防止环境污染。
(2)选择和组装实验室制取气体的装置时,应考虑装置的选取依据和装置的连接顺序。
【建议】在实验室制法的学习中,可结合初中所学习的氧气、二氧化碳气体的制备,帮助学生梳理出从实
验原理的分析到实验装置的选择,再到实验仪器的连接的基本思路,构建制取气体的方法模型。
二、方法导引
实验室中制取气体装置的设计
实验室中制取气体的装置包括发生装置和收集装置,根据实际需要,还可增加除杂装置和尾气处理装置等。
选择各部分装置时,应注意:依据反应物的状态和反应条件,选择气体的发生装置;依据气体及其所含杂质
的性质,选择除杂装置;依据气体的密度、气体在水中的溶解性,以及是否与水反应,选择收集装置;依据
气体的性质,选择尾气处理装置。
装置的连接顺序一般为:发生装置→除杂装置(如需要)→收集装置-→尾气处理装置(如需要)。
三、日常生活情境的应用
84消毒液与洁厕灵( 酸)能否混合使用?
【建议】一、可通过具体生活案例引入。如“据台湾媒体报道,北县中和市锦和中学的部分学生,在清扫
厕所时误以为浴厕清洁剂(主要成分是盐酸)与漂白液混合,清洁效果会更强,结果混合后产生氯气,并
冒出大量浓烟,九名学生疑似氯气吸入过多,身体不适被送往双和医院,诊治后幸无大碍。 请尝试写出
产生氯气的化学方程式。”
二、可通过实验探究引入:探究84消毒液与酸反应得到的气体产物的性质,包括实验中观察到的物理性质,
分别遇干、湿红色石蕊试纸的现象等,获取证据进行推理,培养证据意识。实验结论:得出84消毒液与洁
厕灵不能混合使用的结论,发展学生的社会参与意识。
这样的教学设计,问题来自于实际生活,探究中突出了对证据意识的培养,也突出了化学学习的社会价值。
四、课后练习(教材P48)6.实验室中为进行有关氯气的性质实验,需要 4瓶体积为100mL的氯气。(常温下,氯气的密度为2.91
g/L。)
(1)制取4瓶氯气,理论上需要MnO 的质量是多少?
2
(2)实际称取的MnO 固体的质量必须适当多于理论量,主要原因是什么?
2
【答案】1.426g 实际称取的MnO 固体的质量必须适当多于理论量
2
【解析】需制备氯气0.1*2.91*4=1.164g,MnO
2
+ 4HCl(浓) MnCl
2
+ Cl
2
↑ + 2H
2
O
根据反应方程式可计算需要MnO 的质量是1.426g。实际实验中不能实现全部转化,要考虑损耗,所以实
2
际称取的MnO 固体的质量必须适当多于理论量。
2