文档内容
第二章 海水中的重要元素—钠和氯
第一节 钠及其化合物
专题 两种重要的钠盐
【学习目标】1.通过从微观组成角度再认识碳酸钠和碳酸氢钠的相同的和不同点,掌握碳酸钠和碳酸
氢钠的鉴别、提纯基本方法,加深对“由表及里,透过现象看本质”的认识。
2.通过对碳酸钠和碳酸氢钠性质的深入探究,能以碳酸钠和碳酸氢钠知识的学习为线索,运用控制变
量法、定性与定量相结合设计简单的实验方案,认识碳酸盐和碳酸氢盐的性质,初步形成物质转化可通过
条件控制实现的化学观念。
3.通过纯碱有关的化学史学习,以及对综合性任务的完成过程体验,感受化学工业发展中技术进步的
重要性,体会建设生态文明的意义,培养培养爱国情怀及科学态度与社会责任的化学核心素养。
【学习重点】碳酸钠和碳酸氢钠的化学性质及比较
【学习难点】碳酸钠和碳酸氢钠的相互转化与鉴别方法。
【课前预习】
旧知回顾:关于NaCO 和NaHCO 性质比较中,热稳定性:NaCO > NaHCO ;常温下在水溶液中
2 3 3 2 3 3
的溶解度:NaCO > NaHCO ;等质量的固体分别与足量盐酸反应产生CO 的质量:NaCO <
2 3 3 2 2 3
NaHCO ;
3
等浓度溶液的碱性:NaCO > NaHCO
2 3 3
新知预习:NaCO 和NaHCO 与盐和碱发生反应,可以产生不同的现象,请填写表格内容。
2 3 3
物质 盐 碱
操作
现象 产生白色沉淀 产生白色沉淀,有气体生成 产生白色沉淀 产生白色沉淀
【课中探究】
情景导入:馒头是中华传统美食,碳酸氢钠(又名小苏打)是蒸馒头时用到的发酵粉的主要成分之
一,你知道这是什么原因吗?让我们一起观看视频,看看馒头是如何制作的?
一、碳酸钠和碳酸氢钠的重要化学性质
活动一、探究碳酸钠和碳酸氢钠的热稳定性
任务一、联系教材P39页【实验2-5】碳酸钠、碳酸氢钠热稳定性比较,完成下表内容:
【答案要点】实验 碳酸钠 碳酸氢钠
装置
如图所示实验为“套管实验”,小试管内塞有沾有白色无水硫酸铜粉末的棉花
操作
球。点燃酒精灯加热,能观察到的实验现象
现象 小试管中棉花球变蓝色,B烧杯中澄清石灰水变浑浊,A烧杯中有少量气泡冒出。
方程式 2NaHCO ====NaCO+HO+CO↑
3 2 3 2 2
NaCO 受热不分解;NaHCO 受热易分解,生成物中含有CO 和HO。由此可知,
2 3 3 2 2
结论
NaCO 的热稳定性比NaHCO 强。
2 3 3
任务二、问题探究:依据碳酸氢钠的性质,思考馒头制作过程中加入碳酸氢钠作膨松剂原理是什么?
油炸面拖黄鱼、鲜虾、鸡排或排骨时,在面粉糊里和上一点小苏打,吃起来又松又脆。你知道其中的道理吗?
【答案要点】①利用NaHCO 受热分解产生CO 使馒头松软,但NaHCO 受热分解生成的NaCO 或
3 2 3 2 3
可能剩余的NaHCO 使馒头发黄,并略带碱味。
3
②酵头发酵后生成少量CO 和酸性物质,利用NaHCO 与酸的反应,可调节面团酸度。
2 3
③同理,油炸面拖黄鱼、鲜虾、鸡排或排骨时,在面粉糊里和上一点小苏打,是因为小苏打受热后分解,
会产生大量的二氧化碳气体,使油炸面糊里留下许多气孔,吃起来又松又脆。
【对应训练】1.下列有关物质的性质与用途有对应性且说法均正确的是( )
A.苏打易溶于水,可用于去除物品表面的油污
B.小苏打受热易分解,可用于制胃酸中和剂
C.小苏打受热分解时生成二氧化碳气体,可用于制作膨松剂
D.盐碱地(含较多NaCO 等)不利于作物生长,可施加熟石灰进行改良
2 3
【答案】C
【解析】A.碳酸钠俗称苏打,水溶液呈碱性,可用于去除物品表面的油污,与其易溶于水无关,A
错误;B.碳酸氢钠俗称小苏打,受热易分解,但可用于制胃酸中和剂,利用的是碳酸氢钠能与盐酸反
应,B错误;C.碳酸氢钠俗称小苏打,受热易分解生成碳酸钠、水和二氧化碳,可用于制作膨松剂,C正
确;D.NaCO 与氢氧化钙反应生成碳酸钙和氢氧化钠,会加重土壤碱性,D错误;答案选C。
2 3
2.现将NaO 与过量NaHCO 混合固体在密闭容器中充分加热反应(已知:2NaHCO ====NaCO+
2 2 3 3 2 3
CO↑+H O),排出气体后最终剩余固体是( )
2 2
A.NaOH和NaO B.NaOH和NaCO
2 2 2 3
C.NaCO D.NaO
2 3 2 2
【答案】C【解析】加热时,2NaHCO ====NaCO+CO ↑+H O,生成的CO、HO都能与NaO 发生反应,
3 2 3 2 2 2 2 2 2
2NaO+2H O==4NaOH+O↑、2NaO+2CO ==2Na CO+O ,但由于2NaOH+CO =Na CO+H O,所以当
2 2 2 2 2 2 2 2 3 2 2 2 3 2
NaO 不足量时,我们只考虑CO 与NaO 的反应,因此,最终所得的固体产物为NaCO。故选C。
2 2 2 2 2 2 3
活动二、碳酸钠和碳酸氢钠与酸的反应
任务一、观看视频:碳酸钠和碳酸氢钠与酸的反应。观察实验现象,分析实验原理,完成表格内容。
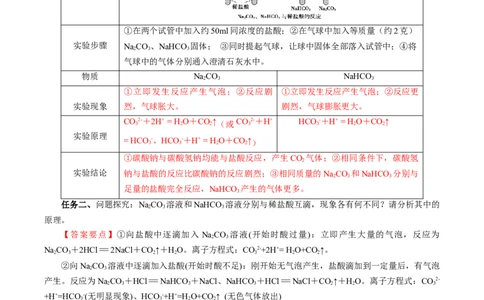
【答案要点】
实验装置
①在两个试管中加入约50ml同浓度的盐酸;②在气球中加入等质量(约2克)
实验步骤 NaCO、NaHCO 固体; ③同时提起气球,让球中固体全部落入试管中;④将
2 3 3
气球中的气体分别通入澄清石灰水中。
物质 NaCO NaHCO
2 3 3
①立即发生反应产生气泡;②反应剧 ①立即发生反应产生气泡;②反应更
实验现象 烈,气球胀大。 剧烈,气球膨胀更大。
CO
3
2-+2H+ = H
2
O+CO
2
↑(或CO
3
2-+H+ HCO
3
-+H+ = H
2
O+CO
2
↑
实验原理
= HCO
3
-、HCO
3
-+H+ = H
2
O+CO
2
↑)
①碳酸钠与碳酸氢钠均能与盐酸反应,产生CO 气体;②相同条件下,碳酸氢
2
实验结论 钠与盐酸的反应比碳酸钠的反应剧烈;③相同质量的NaCO 和NaHCO 分别与
2 3 3
足量的盐酸完全反应,NaHCO 产生的气体更多。
3
任务二、问题探究:NaCO 溶液和NaHCO 溶液分别与稀盐酸互滴,现象各有何不同?请分析其中的
2 3 3
原理。
【答案要点】①向盐酸中逐滴加入 NaCO 溶液(开始时酸过量):立即产生大量的气泡,反应为
2 3
NaCO+2HCl=2NaCl+CO↑+HO。离子方程式:CO2-+2H+= H O+CO↑。
2 3 2 2 3 2 2
②向NaCO 溶液中逐滴加入盐酸(开始时酸不足):刚开始无气泡产生,盐酸滴加到一定量后,有气泡
2 3
产生。反应为NaCO +HCl=NaHCO +NaCl、NaHCO +HCl=NaCl+CO↑+HO。离子方程式:CO2-
2 3 3 3 2 2 3
+H+=HCO-(无明显现象)、HCO -+H+=H O+CO↑ (无色气体放出)
3 3 2 2
③盐酸逐滴加入到NaHCO 溶液和NaHCO 溶液逐滴加入到稀盐酸中,现象相同,均会立即有无色气
3 3
体放出。离子方程式:HCO -+H+=H O+CO↑。
3 2 2
④可以用互滴法鉴别盐酸和碳酸钠溶液。
【对应训练】1.有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06 g Na CO 和0.84
2 3
g NaHCO ,A、B中分别有10 mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙
3
述正确的是 ( )
A.B装置的气球膨胀的体积大
B.最终两试管中NaCl的质量一定相同C.若最终两气球体积不同,则加入NaCO 的试管中盐酸已经消耗完
2 3
D.若最终两气球体积相同,则可能加入两只试管中盐酸都已经消耗完
【答案】D
【解析】A,不一定,两个气球可能一样大B、这个得看反应程度,有可能出现其中一种物质反应
完,另一种没反应完的情况 C、体积不同肯定是NaHCO 先消耗完,而且碳酸氢钠产生的气体更多。D、
3
这个有可能确实是的。
2.下列两种物质相互作用,反应条件或者反应物用量改变,不会引起产物种类改变的是 ( )
A.Na和O B.NaOH和CO
2 2
C.Fe和Cl D.HCl和NaCO
2 2 3
【答案】C
【解析】A.常温下生成氧化钠,点燃或加热生成过氧化钠,4Na+O=2Na O、2Na+O==== Na O ,
2 2 2 2 2
反应温度不同其产物不同,故 A不符合题意; B.氢氧化钠与二氧化碳反应,二氧化碳不足时生成碳酸
钠,CO+2NaOH═Na CO+H O,二氧化碳过量时生成碳酸氢钠,NaCO+H O+CO═2NaHCO , 反应物
2 2 3 2 2 3 2 2 3
用量比改变,会引起产物的种类改变,故B不符合题意;C.氯气具有较强的氧化性,铁和氯气反应只生成
氯化铁,与量以及温度无关,故C符合题意;D.在NaCO 溶液中滴加稀盐酸,若盐酸少量产物为NaHCO
2 3 3
和NaCl,盐酸过量产物为NaCl、HO和CO , 故D不符合题意;故答案为C。
2 2
活动三、碳酸盐和碳酸氢盐与碱的反应
任务一、讨论交流:将NaOH溶液分别滴加到NaCO 和NaHCO 溶液中有何现象?能反应吗?若将
2 3 3
NaOH溶液滴加到Ca(HCO ) 溶液呢?
3 2
【答案要点】①NaOH溶液分别滴加到NaCO 和NaHCO 溶液中均没有明显现象。
2 3 3
②NaOH 溶液与 NaCO 溶液不反应,NaOH 溶液与 NaHCO 溶液反应。化学方程式:NaHCO +
2 3 3 3
NaOH===Na CO+HO,离子方程式:OH-+HCO==CO+H O。
2 3 2 2
③NaOH溶液滴加到Ca(HCO ) 溶液,有白色沉淀生成。化学方程式:Ca(HCO ) +2NaOH===CaCO↓
3 2 3 2 3
+NaCO+HO,离子方程式:Ca2+ + OH-+HCO- = CaCO ↓+H O(碱过量)或 Ca2++ 2OH- + 2HCO -
2 3 2 3 3 2 3
= CaCO ↓+CO 2-+2H O(碱不足)。
3 3 2
④碳酸氢盐与碱溶液反应的实质是HCO与OH-反应生成CO,CO有可能发生后续反应,如NaHCO
3
与Ca(OH) 溶液反应可以生成白色沉淀 CaCO 。
2 3
任务二、归纳总结:碳酸钠与碳酸氢钠的化学性质,请举例完成下表内容。
物质 NaCO(纯碱或苏打) NaHCO (小苏打)
2 3 3
NaCO+CaCl =CaCO ↓+ 2NaHCO 3 +CaCl 2 =
与盐反应 2 3 2 3
2NaCl CaCO ↓+CO↑+2NaCl+HO
3 2 2
NaOH 不反应 NaHCO +NaOH=NaCO+HO
3 2 3 2
Ca(OH) 少量:
与 2
碱 2NaHCO + Ca(OH) = CaCO ↓ + NaCO +
3 2 3 2 3
反 应 Ca(OH) 2 Na 2 CO 3 +Ca 2 (O N H aO ) 2 H =CaCO 3 ↓+ 2H 2 O
Ca(OH) 过量:
2
NaHCO +Ca(OH) =CaCO ↓+NaOH+HO
3 2 3 2盐酸过量:NaCO +2HCl=
2 3
2NaCl+CO↑+HO
2 2
与酸反应 NaHCO +HCl=NaCl+ CO↑+HO
盐酸少量: 3 2 2
NaCO+HCl=NaHCO +NaCl
2 3 3
与CO 反应 NaCO+CO+HO=2NaHCO 不反应
2 2 3 2 2 3
热稳定性 稳定 2NaHCO ====NaCO+CO↑+HO
3 2 3 2 2
相互转化
用途 制玻璃、造纸、洗涤剂 发酵粉、灭火剂、治胃酸过多
【对应练习】1.下列离子方程式正确的是( )
A.过量石灰水与少量碳酸氢钠溶液反应:HCO+Ca2++OH-=CaCO ↓+HO
3 2
B.向沸水中滴加饱和的FeCl 溶液制备Fe(OH) 胶体:Fe3++3HO(沸水)====Fe(OH) (胶体)+3H+
3 3 2 3
C.氢氧化铜与稀硫酸反应:H++OH-=H O
2
D.碳酸氢钠溶液中加入盐酸:CO+2H+=CO ↑+HO
2 2
【答案】AB
【解析】A. 过量石灰水与少量碳酸氢钠溶液反应,假设碳酸氢钠为 1个,则1个HCO 消耗1个
OH-,生成1个 CO和1个水,1个CO再结合1个 Ca2+生成1个CaCO ,离子方程式正确,故A正确;B.
3
向沸水中滴加饱和的FeCl 溶液制备Fe(OH) 胶体,Fe(OH) 不能拆,离子方程式正确,故B正确;C. 氢氧
3 3 3
化铜难溶,应该用化学式表示,故C错误;D. 弱酸的酸式酸根不能拆开,碳酸氢钠溶液中加入盐酸生成
氯化钠、水和CO,正确的离子方程式为HCO+H+=CO ↑+HO,故D错误,答案选AB。
2 2 2
2.以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是( )
A.反应①、②均属于氧化还原反应 B.反应③表明CO 具有酸性氧化物的性质
2
C.反应④说明NaHCO 的稳定性强于NaCO D.反应⑤、⑥可用于潜水艇中氧气的供给
3 2 3
【答案】C
【解析】A项,反应①、②中Na转化为Na的化合物,Na元素化合价由0价升高到+1价,故属于氧
化还原反应,正确;B项,反应③对应反应为:CO+2NaOH=NaCO+HO,符合酸性氧化物定义,故
2 2 3 2
CO 为酸性氧化物,正确;C项,反应④为NaHCO 受热分解生成NaCO,说明NaCO 稳定性强于
2 3 2 3 2 3
NaHCO ,错误;D项,反应⑤、⑥均有O 产生,可用于潜水艇中氧气的供给,正确。
3 2
二、碳酸钠和碳酸氢钠的鉴别及制备活动一、碳酸钠和碳酸氢钠的鉴别方法及原理
任务一、结合碳酸钠与碳酸氢钠的性质,思考鉴别碳酸钠与碳酸氢钠有哪些方法,完成小表内容。
【答案要点】
方法依据 原理 结论
2NaHCO ====NaCO+CO↑+HO; 加热有气体产生的是NaHCO ,无变化的
3 2 3 2 2 3
热稳定性
NaCO 受热不易分解 是NaCO
2 3 2 3
CO+Ca2+===CaCO ↓,
3
与CaCl 、 有沉淀生成的是 NaCO ,无变化的是
2 2 3
CO+Ba2+===BaCO ↓;
3
BaCl 的反应 NaHCO
2 3
HCO与Ca2+、Ba2+不反应
NaCO + 2HCl===2NaCl + HO +
2 3 2
与盐酸反应的 生成气体剧烈的是NaHCO ,相对不剧烈
3
CO↑;
2
剧烈程度 的是NaCO
2 3
NaHCO +HCl===NaCl+HO+CO↑
3 2 2
逐 滴 加 入 盐 酸 立 即 产 生 气 体 的 是
盐酸逐滴加入 CO+H+===HCO;
NaHCO ,开始不产生气体,滴加一会才
3
时的现象 HCO+H+===CO ↑+HO
2 2
产生气体的是NaCO
2 3
任务二、结合任务一归纳总结鉴别碳酸钠和碳酸氢钠又哪些方法?思考如何除去碳酸钠中碳酸氢钠和
碳酸氢钠中的碳酸钠?
【答案要点】①碳酸钠和碳酸氢钠的鉴别方法:a.将固体溶于水,测温度的变化,升高的是碳酸钠、
降低的是碳酸氢钠;
b.将等质量的固体溶于等体积的水中,溶解度大的是碳酸钠、小的是碳酸氢钠;
c.将固体分别置于试管加热,如有水珠生成的是碳酸氢钠或加热后固体质量未变的是碳酸钠、质量减
小的是碳酸氢钠。
②碳酸钠和碳酸氢钠的常见三种除杂方法:
混合物 除杂方法
NaCO 固体(NaHCO ) 加热
2 3 3
NaHCO 溶液(Na CO) 通入足量CO 气体
3 2 3 2
NaCO 溶液(NaHCO ) 加入适量NaOH溶液
2 3 3
【对应练习】1.在课堂上老师出示了两瓶失去标签的NaCO 和NaHCO 无色饱和溶液,希望班里同学
2 3 3
提出简便的鉴别方法。该班同学踊跃提出方法,其中不合理的是 ( )
①取等量的溶液于两支试管中,加热,有气泡产生的是NaHCO 饱和溶液
3
②取等量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO 饱和溶液
3
③取等量的溶液于两支试管中,滴加BaCl 溶液,生成白色沉淀的是NaCO 饱和溶液
2 2 3
④取等量的溶液于两支试管中,滴加Ba(OH) 溶液,生成白色沉淀的是NaCO 饱和溶液
2 2 3
A.①② B.①④ C.③④ D.②③
【答案】B
【解析】NaHCO 在溶液中时受热不分解,只有NaHCO 固体受热才分解,①不合理;分别向两支试管中
3 3
滴 加 Ba(OH) 溶 液 , 都 能 出 现 白 色 沉 淀 , 化 学 方 程 式 为 NaCO+Ba(OH) =2NaOH+BaCO ↓ 、
2 2 3 2 32NaHCO +Ba(OH) =Na CO+BaCO ↓+2H O,④不合理。
3 2 2 3 3 2
2.为除去括号内的杂质,所选用的试剂或方法错误的是( )
A.CO 气体(HCl):饱和NaHCO 溶液 B.NaCO 固体(NaHCO ):加热至不再产生气体
2 3 2 3 3
C.NaHCO 溶液(Na CO):通过量CO D.NaCO 溶液(Na SO ):加入适量Ba(OH) 溶液,过滤
3 2 3 2 2 3 2 4 2
【答案】D
【解析】A项,二氧化碳与碳酸氢钠不反应,氯化氢能与碳酸氢钠反应生成二氧化碳,故A正确;B
项,碳酸氢钠加热分解生成碳酸钠,碳酸钠受热不分解,则加热法可除杂,故B正确;C项,碳酸钠溶液
吸收二氧化碳转化为碳酸氢钠,则用二氧化碳能除去碳酸氢钠溶液中的碳酸钠,故C正确;D项,二者都
与氢氧化钡反应生成沉淀,主要物质也被除去了,故D错误;故选D。
活动二、Na CO 的制备—侯氏制碱法
2 3
任务一、阅读教材P40页“科学史话”,查阅资料,从原料、原理、流程等方面,回答什么是侯氏制
碱法?
【答案要点】侯氏制碱法,又称联合制碱法:
①原料:食盐、氨气、二氧化碳——合成氨厂用水煤气制取氢气时的废气
其反应为C+HO(g)=====CO+H,CO+HO(g)=====CO+H。
2 2 2 2 2
②反应原理:往饱和食盐水中依次通入足量的 NH 、CO(氨碱法),利用 NaHCO 的溶解性小于
3 2 3
NH HCO 的溶解性原理,使NaHCO 从溶液中析出。过滤,碳酸氢钠不稳定受热易分解。
4 3 3
NH +CO+HO=NH HCO 、NH HCO +NaCl(饱和)=NaHCO ↓+NH Cl
3 2 2 4 3 4 3 3 4
总反应为:NH +CO+HO+NaCl(饱和)=NaHCO ↓+NH Cl
3 2 2 3 4
2NaHCO ====NaCO+HO+CO↑
3 2 3 2 2
③工艺流程
④循环使用的物质:CO、饱和食盐水。
2
任务二、讨论交流:侯氏制碱法中,能否先通CO 后通NH ?.侯氏制碱法作为我国化学家对化学工业
2 3
的巨大成就,具有哪些现实意义?
【答案要点】①不能。从气体的溶解度考虑,CO 可溶于水而NH 极易溶于水。如先通过CO 则产生
2 3 2
的NaHCO 的量极少。
3
②符合现在提倡的“绿色化学的要求,不产生无用的CaCl ,减少了对环境的污染。
2
③提高了原料(NaCl)的利用率,缩短了生产流程,降低了成本,提高了综合经济效益。④将制碱技术发展到一个新的水平,贏得了国际化工界的高度评价。热爱祖国、自强不息和艰苦创业
的精神,始终是后人学习的典范。
【对应练习】1.“侯氏制碱法”是将 CO 通入含NH 的饱和NaCl溶液中,结晶,过滤,加热分解
2 3
NaHCO 制得NaCO。实验室模拟制取NaCO,使用的装置能达到实验目的的是( )
3 2 3 2 3
A.用图1所示装置制取CO 气体 B.用图2所示装置除去CO 气体中的HCl杂质
2 2
C.用图3所示装置从溶液中分离出NaHCO 固体 D.用图4所示装置加热分解制取NaCO
3 2 3
【答案】C
【解析】A项,稀盐酸与CaCO 反应产生的CO 气体会通过长颈漏斗逸出,不能收集到CO 气体,不
3 2 2
符合题意;B项,用NaHCO 饱和溶液除去杂质HCl时,导气管应该长进短出,不符合题意;C项,可以
3
采用如图所示的过滤装置分离NaHCO 固体与溶液,符合题意;D项,加热分解NaHCO 制取NaCO 应该
3 3 2 3
在坩埚中进行,不能采用蒸发方法,不符合题意。
2.1943年侯德榜发明联合制碱法,其生产流程可简要表示为
已知:NH 极易溶于水生成NH ·H O,NH ·H O可电离产生NH +和OH-。 下列说法错误的是( )
3 3 2 3 2 4
A.纯碱分类属于盐不属于碱
B.流程中先通入CO 再通入NH 可达同样效果
2 3
C.若实验室进行第③步操作需要用到的玻璃仪器有烧杯、漏斗和玻璃棒
D.侯氏制碱法制备NaHCO 利用了物质溶解度差异
3
【答案】B
【解析】纯碱是NaCO ,属于盐类,A正确;CO 溶解度较小,通入水中生成的HCO 较少,且再通
2 3 2 2 3
入NH 不易控制生成NH HCO ,而NH3极易溶于水,通入水中生成NH ·H O,再通入过量CO ,可以生
3 4 3 3 2 2
成NH HCO ,有利于NaHCO 的析出,因此效果不同,B错误;第③步操作是过滤,需要用到的玻璃仪器
4 3 3
有烧杯、漏斗和玻璃棒,C正确;D项, NaHCO3的溶解度较小,铵盐的溶解度较大,当溶液中Na+和
HCO -浓度较大时,可以析出NaHCO 固体,因此利用了物质溶解度差异,D正确;故选B。
3 3【课后巩固】1.(易)教材作业:P43页练习6
2.(易)把X溶液逐滴滴入Y溶液中,与把Y溶液逐滴滴入X溶液中,反应现象不同的是( )
A B C D
X NaHCO NaCO NaHCO MgCl
3 2 3 3 2
Y Ca(OH) HCl HCl NaOH
2
【答案】 B
【解析】Ca(OH) 过量:Ca(OH) +NaHCO=CaCO ↓+NaOH+HO,NaHCO 过量:Ca(OH) +2NaHCO
2 2 3 3 2 3 2 3
=CaCO ↓+Na CO+2H O,均有白色沉淀,故A不符合题意; HCl滴入NaCO 中,开始生成NaHCO 无明
3 2 3 2 2 3 3
显现象,后生成CO,有气泡产生,NaCO 滴入HCl中,开始盐酸过量有气泡产生,故B符合题意;
2 2 3
NaHCO 与HCl均产生气泡,故C不符合题意;均产生白色沉淀,故D不符合题意。故答案为:B。
3
3.(易)不能用来鉴别NaCO 和NaHCO 两种固体的操作是( )
2 3 3
A.分别加热这两种固体物质,并将生成的气体通入澄清的石灰水中
B.分别测量两种固体溶于水时,溶液的温度变化
C.分别在这两种固体中,逐滴加入同浓度的稀盐酸
D.分别在这两种物质的溶液中,加入少量澄清的石灰水
【答案】D
【解析】A.碳酸钠受热不分解,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳气体,二氧化碳能使
澄清石灰水变浑浊,可以鉴别,A不符合题意;B.碳酸钠溶于水,溶液温度升高,碳酸氢钠溶于水,溶
液温度降低,可以鉴别,B不符合题意;C.向碳酸钠溶液中逐滴加入稀盐酸,先无气体产生,当盐酸量
较多时,产生气体,向碳酸氢钠溶液中逐滴加入稀盐酸,立即产生气体,现象不同,可以鉴别,C不符合
题意;D.碳酸钠和碳酸氢钠均能与澄清石灰水反应生成沉淀,无法鉴别,D符合题意;答案选D。
4.(易)有两支试管分别装有NaCO 和NaHCO 溶液,下列鉴别二者的操作和判断均正确的是(
2 3 3
)
选项 操作 判断
A 分别加入澄清石灰水 产生沉淀者为NaCO
2 3
B 分别加入等浓度的稀盐酸 反应较剧烈者为NaCO
2 3
C 分别加入CaCl 溶液 产生沉淀者为NaCO
2 2 3
D 逐滴加入等浓度的盐酸 立即产生气泡者为NaCO
2 3
【答案】C
【 解 析 】 A 项 , 发 生 的 反 应 分 别 为 NaCO + Ca(OH) ===CaCO ↓ + 2NaOH , 2NaHCO +
2 3 2 3 3
Ca(OH) ===CaCO ↓+NaCO +2HO,两者现象相同(产生白色沉淀);B项,滴加等浓度的稀盐酸时,
2 3 2 3 2
NaHCO 溶液反应更剧烈;C项,NaCO 与CaCl 发生反应NaCO +CaCl ===CaCO ↓+2NaCl,产生白色
3 2 3 2 2 3 2 3
沉淀,NaHCO 与CaCl 不反应;D项,逐滴加入等浓度的盐酸时,NaHCO 立即产生气泡,NaCO 开始无
3 2 3 2 3
气泡产生,过一会儿才产生气泡。5.(中)将NaHCO 和NaO 的固体混合物置于密闭容器中,加热至270℃,使其充分反应,最后测得
3 2 2
生成的气体和剩余固体均由两种物质组成,则其组成应是( )
生成气体 剩余固体
A. CO、HO(g) NaCO、NaO
2 2 2 3 2 2
B. HO(g)、O NaCO、NaHCO
2 2 2 3 3
C. HO(g)、O NaCO、NaOH
2 2 2 3
D. HO(g)、O NaOH、NaO
2 2 2 2
【答案】C
【解析】将NaHCO 和NaO 的固体混合物置于密闭容器中,加热至270℃,首先NaHCO 分解生成
3 2 2 3
NaCO 、CO 和HO;之后是NaO 分别与CO 、HO反应。注意CO 、HO同时通过足量的NaO 时可认
2 3 2 2 2 2 2 2 2 2 2 2
为是CO 先与NaO 反应,后是HO与NaO 反应。A项,NaO 剩余,则不可能存在CO、HO,错误;B
2 2 2 2 2 2 2 2 2 2
项,根据题意加热条件下,NaHCO 已完全分解,错误;C项,如NaHCO 适量,则其分解生成的CO 先与
3 3 2
NaO 完全反应生成O ,部分的水与NaO 反应生成NaOH,固体为NaCO 和NaOH,气体有生成的O 与
2 2 2 2 2 2 3 2
剩余的水,正确;D项,NaO 剩余,则不可能有HO剩余,错误。
2 2 2
6.(中)加热10.0g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45g求混合物
中碳酸钠的质量分数( )
A.58% B.42% C.36% D.64%
【答案】A
【解析】加热碳酸钠和碳酸氢钠的混合物时,碳酸钠不分解,碳酸氢钠不稳定,加热时分解生成碳酸
钠、二氧化碳和水,发生反应为2NaHCO ====NaCO+CO ↑+H O,则固体质量减少的原因是由于碳酸氢
3 2 3 2 2
钠分解的缘故,设混合物中碳酸氢钠的质量为m,利用差量法计算,则
2NaHCO ====NaCO+CO ↑+H O △m
3 2 3 2 2
2×84 106 62
m 10.0g-8.45g=1.55g
m=4.2g
所以混合物中碳酸钠的质量为10.0g-4.2g=5.8g ,
混合物中碳酸钠的质量分数为 。故选A。
7.(中)侯德榜是我国杰出的化学家,“侯氏制碱法”的创始人。NaCl+CO +NH +HO===
2 3 2
NaHCO ↓+NH Cl是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见
3 4
解,其中不正确的是( )
A.甲同学说:该条件下NaHCO 的溶解度较小
3
B.乙同学说:NaHCO 不是纯碱
3C.丙同学说:析出NaHCO 固体后的溶液中只含氯化铵
3
D.丁同学说:该反应是在饱和食盐水中先通入氨气,再通入二氧化碳
【答案】C
【解析】碳酸氢钠是小苏打,纯碱是碳酸钠,B项正确;析出碳酸氢钠,说明剩余的溶液为碳酸氢钠
的饱和溶液,C项错误;先通入氨气至饱和,再通入过量二氧化碳,这样可以保证在碱性条件下生成更多
的HCO,D项正确。
8.(难)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中
NaCO 的含量。
2 3
(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的
水,使漏斗内的水面高于瓶内的水面,停止加水后,若___________________________,说明装置不漏
气。
(2)实验结束后通入空气的目的为______________________________________________。
(3)装置A的试剂为____________,装置C中的试剂为_____________________________。
(4)装置E作用为_______________________________________________。
(5)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中NaCO 的质量分数为
2 3
____________。
(6)有同学认为该实验设计有较大缺陷,你认为要如何改进____________________________________。
【答案】(1)漏斗中与广口瓶中的液面差保持不变或漏斗中的液面不再下降
(2)把生成的二氧化碳气体全部排入装置D中
(3)氢氧化钠溶液 浓硫酸
(4)吸收空气中的二氧化碳和水蒸气,防止影响测量结果
(5)73.6% (6)用稀硫酸代替稀盐酸
【解析】(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入
一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,利用压强变化和液面变化分析判断,若漏斗
中与广口瓶中的液面差保持不变,证明装置气密性完好;故故选:漏斗中与广口瓶中的液面差保持不变;
(2)由于生成的二氧化碳会残留在装置中,所以实验结束后通入空气的目的为了把生成的二氧化碳气体全部
排入装置D中;故故选:把生成的二氧化碳气体全部排入装置D中;(3)装置A是为了吸收空气中二氧化碳,避免影响碳酸钠含量的测定,其中试剂是氢氧化钠溶液;装置C中试剂是浓硫酸,目的是干燥生成的
二氧化碳气体,以便D装置中实验前后增加的质量为二氧化碳的质量;(4)U形管是吸收二氧化碳气体称重
来测定碳酸钠含量的方法,若与空气直接接通,会吸收空气中二氧化碳和水蒸气,测定结果偏高,影响测
定结果的准确性,因此装置E的作用是吸收空气中的二氧化碳和水蒸气,防止影响测量结果;(5)实验前称
取28.80g样品,实验后测得D装置增重8.80g,为二氧化碳质量,结合碳元素守恒计算,样品中NaCO 的
2 3
质量分数= ×100%≈73.6%;(6)由于盐酸易挥发,生成的二氧化碳中含有氯化氢会干扰
二氧化碳的吸收,改进的方法代替是用稀硫酸代替稀盐酸。